La epilepsia es un grupo de trastornos neurológicos no transmisibles caracterizados por convulsiones epilépticas recurrentes . [10] Una convulsión epiléptica es la manifestación clínica de una descarga eléctrica anormal, excesiva y sincronizada en las neuronas . [1] La aparición de dos o más convulsiones no provocadas define la epilepsia. [11] La aparición de una sola convulsión puede justificar la definición (establecida por la Liga Internacional Contra la Epilepsia ) en un uso más clínico donde la recurrencia puede ser capaz de prejuzgarse. [10] Las convulsiones epilépticas pueden variar desde períodos breves y casi indetectables hasta largos períodos de temblores vigorosos debido a la actividad eléctrica anormal en el cerebro. [1] Estos episodios pueden resultar en lesiones físicas, ya sea directamente, como huesos rotos, o al provocar accidentes. [1] En la epilepsia, las convulsiones tienden a repetirse y pueden no tener una causa subyacente detectable. [11] Las convulsiones aisladas que son provocadas por una causa específica, como el envenenamiento, no se consideran representativas de epilepsia. [12] Las personas con epilepsia pueden recibir un trato diferente en distintas zonas del mundo y experimentar distintos grados de estigma social debido a la naturaleza alarmante de sus síntomas. [11]
El mecanismo subyacente de una convulsión epiléptica es una actividad neuronal excesiva y anormal en la corteza del cerebro , [12] que se puede observar en el electroencefalograma (EEG) de un individuo. La razón por la que esto ocurre en la mayoría de los casos de epilepsia es desconocida ( criptogénica ); [1] algunos casos ocurren como resultado de una lesión cerebral , accidente cerebrovascular, tumores cerebrales , infecciones del cerebro o defectos de nacimiento a través de un proceso conocido como epileptogénesis . [1] [2] [3] Las mutaciones genéticas conocidas están directamente relacionadas con una pequeña proporción de casos. [4] [13] El diagnóstico implica descartar otras afecciones que podrían causar síntomas similares , como desmayos , y determinar si existe otra causa de convulsiones, como abstinencia de alcohol o problemas de electrolitos . [4] Esto puede hacerse en parte mediante imágenes del cerebro y realizando análisis de sangre . [4] La epilepsia a menudo se puede confirmar con un EEG, pero una lectura normal no descarta la afección. [4]
La epilepsia que se produce como resultado de otros problemas puede prevenirse. [1] Las convulsiones se pueden controlar con medicamentos en aproximadamente el 69% de los casos; [7] a menudo se encuentran disponibles medicamentos anticonvulsivos económicos. [1] En aquellos cuyas convulsiones no responden a la medicación, se puede considerar la cirugía , la neuroestimulación o los cambios en la dieta . [5] [6] No todos los casos de epilepsia duran toda la vida, y muchas personas mejoran hasta el punto de que ya no necesitan tratamiento. [1]
A partir de 2021 [actualizar], alrededor de 51 millones de personas padecen epilepsia. Casi el 80% de los casos ocurren en el mundo en desarrollo . [1] [8] En 2021, resultó en 140.000 muertes, un aumento de 125.000 en 1990. [9] [14] [15] La epilepsia es más común en niños y personas mayores. [16] [17] En el mundo desarrollado , la aparición de nuevos casos ocurre con mayor frecuencia en bebés y ancianos. [18] En el mundo en desarrollo, la aparición es más común en los extremos de la edad, en niños más pequeños y en niños mayores y adultos jóvenes debido a las diferencias en la frecuencia de las causas subyacentes. [19] Aproximadamente entre el 5 y el 10% de las personas tendrán una convulsión no provocada a la edad de 80 años. [20] La probabilidad de experimentar una segunda convulsión dentro de los dos años posteriores a la primera es de alrededor del 40%. [21] [22] En muchas áreas del mundo, a las personas con epilepsia se les imponen restricciones en su capacidad para conducir o no se les permite conducir hasta que estén libres de convulsiones durante un período de tiempo específico. [23] La palabra epilepsia proviene del griego antiguo ἐπιλαμβάνειν , 'apoderarse, poseer o afligir'. [24]

La epilepsia se caracteriza por un riesgo a largo plazo de convulsiones epilépticas recurrentes . [25] Estas convulsiones pueden presentarse de varias maneras dependiendo de las partes del cerebro involucradas y la edad de la persona. [25] [26]
El tipo más común (60%) de convulsiones son las convulsivas , que implican contracciones musculares involuntarias. [26] De estas, un tercio comienza como convulsiones generalizadas desde el principio, afectando a ambos hemisferios del cerebro y deteriorando la conciencia . [26] Dos tercios comienzan como convulsiones focales (que afectan a un hemisferio del cerebro) que pueden progresar a convulsiones generalizadas. [26] El 40% restante de las convulsiones no son convulsivas. Un ejemplo de este tipo es la crisis de ausencia , que se presenta como una disminución del nivel de conciencia y suele durar unos 10 segundos. [2] [27]
Ciertas experiencias, conocidas como auras , a menudo preceden a las convulsiones focales. [28] Las convulsiones pueden incluir fenómenos sensoriales (visuales, auditivos u olfativos), psíquicos, autónomos y motores según qué parte del cerebro esté involucrada. [2] Las sacudidas musculares pueden comenzar en un grupo muscular específico y extenderse a los grupos musculares circundantes, en cuyo caso se conoce como marcha jacksoniana . [29] Pueden ocurrir automatismos , que son actividades generadas de forma no consciente y, en su mayoría, movimientos repetitivos simples como chasquear los labios o actividades más complejas como intentar recoger algo. [29]
Hay seis tipos principales de convulsiones generalizadas:
Todos ellos implican pérdida de conciencia y generalmente ocurren sin previo aviso.
Las convulsiones tónico-clónicas se producen con una contracción de las extremidades seguida de su extensión y arqueamiento de la espalda que dura 10-30 segundos (la fase tónica). Se puede escuchar un grito debido a la contracción de los músculos del pecho , seguido de un temblor de las extremidades al unísono (fase clónica). Las convulsiones tónicas producen contracciones constantes de los músculos. Una persona a menudo se pone azul al detener la respiración. En las convulsiones clónicas hay temblores de las extremidades al unísono. Una vez que el temblor ha cesado, la persona puede tardar entre 10 y 30 minutos en volver a la normalidad; este período se llama " estado postictal " o "fase postictal". La pérdida del control de los intestinos o la vejiga puede ocurrir durante una convulsión. [31] Las personas que experimentan una convulsión pueden morderse la lengua, ya sea la punta o los lados; [32] en la convulsión tónico-clónica , las mordeduras en los lados son más comunes. [32] Las mordeduras de lengua también son relativamente comunes en las convulsiones psicógenas no epilépticas . [32] Las convulsiones psicógenas no epilépticas son un comportamiento similar a una convulsión sin una descarga eléctrica sincronizada asociada en el EEG y se consideran un trastorno disociativo. [32]
Las convulsiones mioclónicas implican espasmos musculares muy breves en algunas áreas o en todo el cuerpo. [33] [34] A veces, estas hacen que la persona se caiga, lo que puede causar lesiones. [33] Las convulsiones de ausencia pueden ser sutiles con solo un ligero giro de la cabeza o parpadeo de los ojos con alteración de la conciencia; [2] por lo general, la persona no se cae y vuelve a la normalidad inmediatamente después de que termina. [2] Las convulsiones atónicas implican la pérdida de actividad muscular durante más de un segundo, [29] que generalmente ocurren en ambos lados del cuerpo. [29] Los tipos de convulsiones más raros pueden causar risa antinatural involuntaria (gelástica), llanto (discrástica) o experiencias más complejas como déjà vu . [34]
Alrededor del 6% de las personas con epilepsia tienen convulsiones que a menudo son desencadenadas por eventos específicos y se conocen como convulsiones reflejas . [35] Las personas con epilepsia refleja tienen convulsiones que solo se desencadenan por estímulos específicos. [36] Los desencadenantes comunes incluyen luces intermitentes y ruidos repentinos. [35] En ciertos tipos de epilepsia, las convulsiones ocurren con más frecuencia durante el sueño , [37] y en otros tipos ocurren casi solo durante el sueño. [38] En 2017, la Liga Internacional Contra la Epilepsia publicó nuevas pautas uniformes para la clasificación de las convulsiones, así como de las epilepsias junto con su causa y comorbilidades. [39]
Los pacientes con epilepsia pueden experimentar ataques de racimos que pueden definirse ampliamente como un deterioro agudo en el control de las convulsiones. [40] La prevalencia de ataques de racimos es incierta dado que los estudios han utilizado diferentes definiciones para definirlos. [41] Sin embargo, las estimaciones sugieren que la prevalencia puede variar del 5% al 50% de los pacientes con epilepsia. [42] Los pacientes con epilepsia refractaria que tienen una alta frecuencia de convulsiones tienen el mayor riesgo de tener ataques de racimos. [43] [44] [45] Los ataques de racimos se asocian con un mayor uso de la atención médica, peor calidad de vida, deterioro del funcionamiento psicosocial y posiblemente mayor mortalidad. [41] [46] Las benzodiazepinas se utilizan como tratamiento agudo para los ataques de racimos. [47]
Después de la parte activa de una convulsión (el estado ictal ), suele haber un período de recuperación durante el cual hay confusión, conocido como período postictal , antes de que se recupere un nivel normal de conciencia . [28] Suele durar de 3 a 15 minutos [48], pero puede durar horas. [49] Otros síntomas comunes incluyen sensación de cansancio, dolor de cabeza , dificultad para hablar y comportamiento anormal. [49] La psicosis después de una convulsión es relativamente común y se presenta en el 6-10% de las personas. [50] A menudo, las personas no recuerdan lo que sucedió durante este tiempo. [49] La debilidad localizada, conocida como parálisis de Todd , también puede ocurrir después de una convulsión focal. Normalmente dura unos segundos o minutos, pero rara vez puede durar un día o dos. [51]
La epilepsia puede tener efectos adversos en el bienestar social y psicológico. [26] Estos efectos pueden incluir aislamiento social, estigmatización o discapacidad. [26] Pueden resultar en un menor rendimiento educativo y peores resultados laborales. [26] Las discapacidades de aprendizaje son comunes en las personas con la afección, y especialmente entre los niños con epilepsia . [26] El estigma de la epilepsia también puede afectar a las familias de las personas con el trastorno. [31]
Ciertos trastornos se presentan con mayor frecuencia en personas con epilepsia, dependiendo en parte del síndrome epiléptico presente. Estos incluyen depresión , ansiedad , trastorno obsesivo-compulsivo (TOC), [52] y migraña . [53] El trastorno por déficit de atención con hiperactividad (TDAH) afecta de tres a cinco veces más niños con epilepsia que niños sin la afección. [54] El TDAH y la epilepsia tienen consecuencias significativas en el desarrollo conductual, de aprendizaje y social de un niño. [55] La epilepsia también es más común en niños con autismo . [56]
Aproximadamente una de cada tres personas con epilepsia tiene antecedentes de algún trastorno psiquiátrico en su vida. [57] Se cree que existen múltiples causas para esto, incluidos cambios fisiopatológicos relacionados con la epilepsia en sí, así como experiencias adversas relacionadas con vivir con epilepsia (p. ej., estigma, discriminación). [58] Además, se cree que la relación entre la epilepsia y los trastornos psiquiátricos no es unilateral sino más bien bidireccional. Por ejemplo, los pacientes con depresión tienen un mayor riesgo de desarrollar epilepsia de nueva aparición. [59]
La presencia de depresión o ansiedad comórbida en pacientes con epilepsia se asocia con una peor calidad de vida, mayor mortalidad, mayor uso de atención médica y una peor respuesta al tratamiento (incluido el quirúrgico). [60] [61] [62] [63] Los trastornos de ansiedad y la depresión pueden explicar más variabilidad en la calidad de vida que el tipo o la frecuencia de las convulsiones. [64] Hay evidencia de que tanto la depresión como los trastornos de ansiedad están subdiagnosticados y subtratados en pacientes con epilepsia. [65]
La epilepsia puede tener causas tanto genéticas como adquiridas, con la interacción de estos factores en muchos casos. [66] [67] Las causas adquiridas establecidas incluyen traumatismo cerebral grave, accidente cerebrovascular, tumores y problemas cerebrales resultantes de una infección previa. [66] En aproximadamente el 60% de los casos, la causa es desconocida. [26] [31] Las epilepsias causadas por condiciones genéticas , congénitas o del desarrollo son más comunes entre las personas más jóvenes, mientras que los tumores cerebrales y los accidentes cerebrovasculares son más probables en las personas mayores. [26]
Las convulsiones también pueden ocurrir como consecuencia de otros problemas de salud; [30] si ocurren justo en torno a una causa específica, como un derrame cerebral, una lesión en la cabeza, una ingestión tóxica o un problema metabólico, se conocen como convulsiones sintomáticas agudas y se encuentran en la clasificación más amplia de trastornos relacionados con convulsiones en lugar de la epilepsia en sí. [68] [69]
Se cree que la genética está involucrada en la mayoría de los casos, ya sea directa o indirectamente. [13] [70] Algunas epilepsias se deben a un solo defecto genético (1-2%); la mayoría se deben a la interacción de múltiples genes y factores ambientales. [13] Cada uno de los defectos de un solo gen es raro, con más de 200 en total descritos. [71] La mayoría de los genes involucrados afectan los canales iónicos , ya sea directa o indirectamente. [66] Estos incluyen genes para canales iónicos, enzimas , GABA y receptores acoplados a proteína G. [33]
En gemelos idénticos , si uno está afectado, hay una probabilidad del 50-60% de que el otro también lo esté. [13] En gemelos no idénticos, el riesgo es del 15%. [13] Estos riesgos son mayores en aquellos con convulsiones generalizadas en lugar de focales. [13] Si ambos gemelos están afectados, la mayoría de las veces tienen el mismo síndrome epiléptico (70-90%). [13] Otros parientes cercanos de una persona con epilepsia tienen un riesgo cinco veces mayor que la población general. [72] Entre el 1 y el 10% de los que tienen síndrome de Down y el 90% de los que tienen síndrome de Angelman tienen epilepsia. [72]
Las facomatosis , también conocidas como trastornos neurocutáneos, son un grupo de enfermedades multisistémicas que afectan principalmente a la piel y al sistema nervioso central. Son causadas por un desarrollo defectuoso del tejido ectodérmico embrionario que, con mayor frecuencia, se debe a una única mutación genética. El cerebro, así como otros tejidos neuronales y la piel, derivan del ectodermo y, por lo tanto, un desarrollo defectuoso puede provocar epilepsia y otras manifestaciones como el autismo y la discapacidad intelectual. Algunos tipos de facomatosis, como el complejo de esclerosis tuberosa y el síndrome de Sturge-Weber, tienen una prevalencia de epilepsia más alta en relación con otros, como la neurofibromatosis tipo 1. [73]
El complejo de esclerosis tuberosa es un trastorno autosómico dominante causado por mutaciones en el gen TSC1 o TSC2 y afecta aproximadamente a 1 de cada 6000 a 10 000 nacidos vivos. [74] [75] Estas mutaciones dan como resultado la regulación positiva de la vía del objetivo mecanicista de la rapamicina (mTOR) , que conduce al crecimiento de tumores en muchos órganos, incluidos el cerebro, la piel, el corazón, los ojos y los riñones. [75] Además, se cree que la actividad anormal de mTOR altera la excitabilidad neuronal. [76] Se estima que la prevalencia de la epilepsia es del 80 al 90 %. [73] [76] La mayoría de los casos de epilepsia se presentan dentro de los primeros 3 años de vida y son refractarios a los tratamientos médicos. [77] Los desarrollos relativamente recientes para el tratamiento de la epilepsia en pacientes con esclerosis tuberosa incluyen inhibidores de mTOR , cannabidiol y vigabatrina. A menudo se recurre a la cirugía de la epilepsia.
El síndrome de Sturge-Weber es causado por una mutación somática activadora en el gen GNAQ y afecta aproximadamente a 1 de cada 20.000 a 50.000 nacidos vivos. [78] La mutación produce malformaciones vasculares que afectan al cerebro, la piel y los ojos. La presentación típica incluye una marca de nacimiento en vino de Oporto en la cara, angiomas oculares y malformaciones vasculares cerebrales que suelen ser unilaterales, pero son bilaterales en el 15% de los casos. [79] La prevalencia de la epilepsia es del 75-100% y es mayor en aquellos con afectación bilateral. [79] Las convulsiones suelen ocurrir dentro de los primeros dos años de vida y son refractarias en casi la mitad de los casos. [80] Sin embargo, se han informado altas tasas de libertad de convulsiones con cirugía en hasta el 83%. [81]
La neurofibromatosis tipo 1 es la facomatosis más común y se presenta en aproximadamente 1 de cada 3000 nacidos vivos. [82] Es causada por mutaciones autosómicas dominantes en el gen de la neurofibromina 1. Las manifestaciones clínicas son variables, pero pueden incluir marcas cutáneas hiperpigmentadas, hamartomas del iris llamados nódulos de Lisch , neurofibromas , gliomas de la vía óptica y deterioro cognitivo. Se estima que la prevalencia de la epilepsia es del 4 al 7 %. [83] Las convulsiones suelen ser más fáciles de controlar con medicamentos anticonvulsivos en comparación con otras facomatosis, pero en algunos casos refractarios puede ser necesario recurrir a la cirugía. [84]
La epilepsia puede ocurrir como resultado de varias otras condiciones, incluyendo tumores, accidentes cerebrovasculares, traumatismo craneal, infecciones previas del sistema nervioso central , anomalías genéticas y como resultado de daño cerebral alrededor del momento del nacimiento. [30] [31] De aquellos con tumores cerebrales, casi el 30% tiene epilepsia, lo que los convierte en la causa de aproximadamente el 4% de los casos. [72] El riesgo es mayor para los tumores en el lóbulo temporal y los que crecen lentamente. [72] Otras lesiones de masa como las malformaciones cavernosas cerebrales y las malformaciones arteriovenosas tienen riesgos tan altos como 40-60%. [72] De aquellos que han tenido un accidente cerebrovascular, 6-10% desarrollan epilepsia. [85] [86] Los factores de riesgo para la epilepsia posterior al accidente cerebrovascular incluyen la gravedad del accidente cerebrovascular, la afectación cortical, la hemorragia y las convulsiones tempranas. [87] [88] Se cree que entre el 6 y el 20% de la epilepsia se debe a un traumatismo craneal. [72] Una lesión cerebral leve aumenta el riesgo aproximadamente dos veces, mientras que una lesión cerebral grave lo aumenta siete veces. [72] En aquellos que han sufrido una herida de bala de alta potencia en la cabeza, el riesgo es de aproximadamente el 50%. [72]
Algunas evidencias vinculan la epilepsia con la enfermedad celíaca y la sensibilidad al gluten no celíaca , mientras que otras evidencias no lo hacen. Parece haber un síndrome específico que incluye la enfermedad celíaca, la epilepsia y las calcificaciones en el cerebro. [89] [90] Una revisión de 2012 estima que entre el 1% y el 6% de las personas con epilepsia tienen enfermedad celíaca, mientras que el 1% de la población general tiene la afección. [90]
El riesgo de epilepsia después de la meningitis es inferior al 10%; más comúnmente causa convulsiones durante la infección misma. [72] En la encefalitis por herpes simple, el riesgo de una convulsión es de alrededor del 50% [72] con un alto riesgo de epilepsia posterior (hasta un 25%). [91] [92] Una forma de infección con la tenia del cerdo ( cisticercosis ), en el cerebro, se conoce como neurocisticercosis , y es la causa de hasta la mitad de los casos de epilepsia en áreas del mundo donde el parásito es común. [72] La epilepsia también puede ocurrir después de otras infecciones cerebrales como la malaria cerebral , la toxoplasmosis y la toxocariasis . [72] El consumo crónico de alcohol aumenta el riesgo de epilepsia: quienes beben seis unidades de alcohol por día tienen un riesgo 2,5 veces mayor. [72] Otros riesgos incluyen la enfermedad de Alzheimer , la esclerosis múltiple y la encefalitis autoinmune . [72] Vacunarse no aumenta el riesgo de epilepsia. [72] La desnutrición es un factor de riesgo que se observa principalmente en el mundo en desarrollo, aunque no está claro si es una causa directa o una asociación. [19] Las personas con parálisis cerebral tienen un mayor riesgo de epilepsia, y la mitad de las personas con cuadriplejia espástica y hemiplejia espástica tienen esta afección. [93]
Normalmente, la actividad eléctrica cerebral no es sincrónica, ya que un gran número de neuronas normalmente no se activan al mismo tiempo, sino que lo hacen en orden a medida que las señales viajan por todo el cerebro. [2] La actividad neuronal está regulada por varios factores tanto dentro de la célula como del entorno celular. Los factores dentro de la neurona incluyen el tipo, número y distribución de canales iónicos, cambios en los receptores y cambios en la expresión genética . [94] Los factores alrededor de la neurona incluyen concentraciones de iones , plasticidad sináptica y regulación de la degradación del transmisor por las células gliales . [94] [95]
Se desconoce el mecanismo exacto de la epilepsia, [96] pero se sabe poco sobre sus mecanismos celulares y de red. Sin embargo, se desconoce en qué circunstancias el cerebro cambia a la actividad de una convulsión con su sincronización excesiva . [97] [98] [99] [100]
En la epilepsia, la resistencia de las neuronas excitadoras a activarse durante este período disminuye. [2] Esto puede ocurrir debido a cambios en los canales iónicos o neuronas inhibidoras que no funcionan correctamente. [2] Esto da como resultado un área específica desde la cual pueden desarrollarse convulsiones, conocida como "foco convulsivo". [2] Otro mecanismo de la epilepsia puede ser la regulación positiva de los circuitos excitadores o la regulación negativa de los circuitos inhibidores después de una lesión en el cerebro. [2] [3] Estas epilepsias secundarias ocurren a través de procesos conocidos como epileptogénesis . [2] [3] La falla de la barrera hematoencefálica también puede ser un mecanismo causal, ya que permitiría que las sustancias en la sangre ingresen al cerebro. [101]
Existen evidencias de que las convulsiones epilépticas no suelen ser un evento aleatorio. Las convulsiones suelen ser provocadas por factores (también conocidos como desencadenantes) como el estrés, el consumo excesivo de alcohol , la luz parpadeante o la falta de sueño, entre otros. El término umbral convulsivo se utiliza para indicar la cantidad de estímulo necesario para provocar una convulsión; este umbral es más bajo en la epilepsia. [97]
En las convulsiones epilépticas, un grupo de neuronas comienza a dispararse de manera anormal, excesiva [26] y sincronizada. [2] Esto da como resultado una onda de despolarización conocida como cambio despolarizante paroxístico . [102] Normalmente, después de que una neurona excitadora se dispara, se vuelve más resistente a dispararse durante un período de tiempo. [2] Esto se debe en parte al efecto de las neuronas inhibidoras, los cambios eléctricos dentro de la neurona excitadora y los efectos negativos de la adenosina . [2]
Las convulsiones focales comienzan en un área del cerebro mientras que las convulsiones generalizadas comienzan en ambos hemisferios . [30] Algunos tipos de convulsiones pueden cambiar la estructura cerebral, mientras que otras parecen tener poco efecto. [103] La gliosis , la pérdida neuronal y la atrofia de áreas específicas del cerebro están relacionadas con la epilepsia, pero no está claro si la epilepsia causa estos cambios o si estos cambios resultan en epilepsia. [103]
Las convulsiones se pueden describir en diferentes escalas, desde el nivel celular [104] hasta el cerebro entero. [105] Se trata de varios factores concomitantes que, en diferentes escalas, pueden "llevar" al cerebro a estados patológicos y desencadenar una convulsión.

El diagnóstico de epilepsia se realiza generalmente en base a la observación del inicio de la convulsión y la causa subyacente. [26] Un electroencefalograma (EEG) para buscar patrones anormales de ondas cerebrales y neuroimagen ( tomografía computarizada o resonancia magnética ) para observar la estructura del cerebro también suelen ser parte de las investigaciones iniciales. [26] Si bien a menudo se intenta determinar un síndrome epiléptico específico, no siempre es posible. [26] La monitorización por video y EEG puede ser útil en casos difíciles. [106]
La epilepsia es un trastorno del cerebro definido por cualquiera de las siguientes condiciones: [10]
Además, se considera que la epilepsia está resuelta en personas que tenían un síndrome de epilepsia dependiente de la edad pero que ya han pasado esa edad o que han permanecido libres de convulsiones durante los últimos 10 años y sin tomar medicamentos anticonvulsivos durante los últimos 5 años. [10]
Esta definición de 2014 de la Liga Internacional Contra la Epilepsia [10] (ILAE) es una aclaración de la definición conceptual de la ILAE de 2005, según la cual la epilepsia es "un trastorno del cerebro caracterizado por una predisposición duradera a generar convulsiones epilépticas y por las consecuencias neurobiológicas, cognitivas, psicológicas y sociales de esta condición. La definición de epilepsia requiere la ocurrencia de al menos una convulsión epiléptica". [107] [108]
Por lo tanto, es posible superar la epilepsia o someterse a un tratamiento que haga que se resuelva, pero sin garantía de que no vuelva. En la definición, la epilepsia ahora se llama enfermedad, en lugar de trastorno. Esta fue una decisión del comité ejecutivo de la ILAE, tomada porque la palabra trastorno , si bien tal vez tenga menos estigma que enfermedad , tampoco expresa el grado de gravedad que merece la epilepsia. [10]
La definición es de naturaleza práctica y está diseñada para uso clínico. En particular, tiene como objetivo aclarar cuándo está presente una "predisposición duradera" según la definición conceptual de 2005. Los investigadores, los epidemiólogos con mentalidad estadística y otros grupos especializados pueden optar por utilizar la definición anterior o una definición de su propia invención. La ILAE considera que hacerlo es perfectamente admisible, siempre que esté claro qué definición se está utilizando. [10]
La definición de la ILAE para una convulsión requiere la comprensión de la proyección de una predisposición duradera a la generación de convulsiones epilépticas. [10] La OMS, por ejemplo, opta por utilizar simplemente la definición tradicional de dos convulsiones no provocadas. [11]
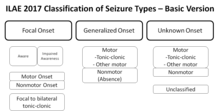
A diferencia de la clasificación de las convulsiones , que se centra en lo que sucede durante una convulsión, la clasificación de las epilepsias se centra en las causas subyacentes. Cuando una persona ingresa en el hospital después de una convulsión epiléptica, el diagnóstico da como resultado, preferentemente, la clasificación de la convulsión en sí (p. ej., tónico-clónica) y la identificación de la enfermedad subyacente (p. ej., esclerosis hipocampal ). [106] El nombre del diagnóstico que finalmente se realiza depende de los resultados diagnósticos disponibles y de las definiciones y clasificaciones aplicadas (de convulsiones y epilepsias) y su respectiva terminología.
La Liga Internacional Contra la Epilepsia (ILAE) proporcionó una clasificación de las epilepsias y síndromes epilépticos en 1989 de la siguiente manera: [109]
Esta clasificación fue ampliamente aceptada pero también ha sido criticada principalmente porque las causas subyacentes de la epilepsia (que son un determinante principal del curso clínico y el pronóstico) no fueron cubiertas en detalle. [110] En 2010 la Comisión de Clasificación de las Epilepsias de la ILAE abordó este tema y dividió las epilepsias en tres categorías (genética, estructural/metabólica, causa desconocida) [111] que fueron refinadas en su recomendación de 2011 en cuatro categorías y una serie de subcategorías que reflejan avances tecnológicos y científicos recientes. [112]
Los casos de epilepsia pueden clasificarse en síndromes epilépticos según las características específicas que presentan. Estas características incluyen la edad en la que comienzan las convulsiones, los tipos de convulsiones, los hallazgos del EEG , entre otros. Identificar un síndrome epiléptico es útil ya que ayuda a determinar las causas subyacentes, así como también qué medicamento anticonvulsivo se debe probar. [30] [115]
La capacidad de categorizar un caso de epilepsia en un síndrome específico ocurre con mayor frecuencia en niños, ya que el inicio de las convulsiones suele ser temprano. [69] Ejemplos menos graves son la epilepsia rolándica benigna (2,8 por 100 000), la epilepsia de ausencia infantil (0,8 por 100 000) y la epilepsia mioclónica juvenil (0,7 por 100 000). [69] Los síndromes graves con disfunción cerebral difusa causada, al menos en parte, por algún aspecto de la epilepsia, también se denominan encefalopatías del desarrollo y epilépticas. Estas se asocian con convulsiones frecuentes que son resistentes al tratamiento y disfunción cognitiva, por ejemplo, el síndrome de Lennox-Gastaut (1-2 % de todas las personas con epilepsia), [116] el síndrome de Dravet (1: 15 000-40 000 en todo el mundo [117] ) y el síndrome de West (1-9: 100 000 [118] ). [119] Se cree que la genética desempeña un papel importante en las epilepsias mediante una serie de mecanismos. Se han identificado modos de herencia simples y complejos para algunas de ellas. Sin embargo, una detección exhaustiva no ha logrado identificar muchas variantes de un solo gen de gran efecto. [120] Estudios más recientes de secuenciación del exoma y el genoma han comenzado a revelar una serie de mutaciones genéticas de novo que son responsables de algunas encefalopatías epilépticas, incluidas CHD2 y SYNGAP1 [121] [122] [123] y DNM1 , GABBR2 , FASN y RYR3 . [124]
Los síndromes en los que no se identifican claramente las causas son difíciles de hacer coincidir con las categorías de la clasificación actual de la epilepsia. La categorización de estos casos se realizó de forma algo arbitraria. [112] La categoría idiopática (causa desconocida) de la clasificación de 2011 incluye síndromes en los que las características clínicas generales y/o la especificidad de la edad apuntan firmemente a una presunta causa genética. [112] Algunos síndromes de epilepsia infantil se incluyen en la categoría de causa desconocida en la que la causa se presume genética, por ejemplo, la epilepsia rolándica benigna. [112] Los síndromes clínicos en los que la epilepsia no es la característica principal (por ejemplo, el síndrome de Angelman) se categorizaron como sintomáticos , pero se argumentó que se incluirían dentro de la categoría idiopática . [112] La clasificación de las epilepsias y, en particular, de los síndromes de epilepsia cambiará con los avances en la investigación. [112]
Un electroencefalograma (EEG) puede ayudar a mostrar la actividad cerebral sugestiva de un mayor riesgo de convulsiones. Solo se recomienda para aquellos que probablemente hayan tenido una convulsión epiléptica en función de los síntomas. En el diagnóstico de la epilepsia, el electroencefalograma puede ayudar a distinguir el tipo de convulsión o síndrome presente. [125] En los niños, por lo general, solo se necesita después de una segunda convulsión, a menos que lo especifique un especialista. No se puede utilizar para descartar el diagnóstico y puede ser falso positivo en aquellos que no tienen la afección. [125] En ciertas situaciones, puede ser útil realizar el EEG mientras el individuo afectado está durmiendo o privado de sueño. [106]
Se recomiendan las imágenes diagnósticas mediante tomografía computarizada y resonancia magnética después de una primera convulsión no febril para detectar problemas estructurales en el cerebro y sus alrededores. [106] La resonancia magnética es generalmente una mejor prueba de diagnóstico por imágenes, excepto cuando se sospecha sangrado, para lo cual la tomografía computarizada es más sensible y está más disponible. [20] Si alguien acude a la sala de emergencias con una convulsión pero vuelve a la normalidad rápidamente, las pruebas de diagnóstico por imágenes pueden realizarse en un momento posterior. [20] Si una persona tiene un diagnóstico previo de epilepsia con imágenes previas, generalmente no es necesario repetir las imágenes incluso si hay convulsiones posteriores. [106] [126]
En los adultos, es importante realizar pruebas de electrolitos, glucosa en sangre y niveles de calcio para descartar problemas con estas como causas. [106] Un electrocardiograma puede descartar problemas con el ritmo del corazón. [106] Una punción lumbar puede ser útil para diagnosticar una infección del sistema nervioso central, pero no es necesaria de manera rutinaria. [20] En los niños, pueden requerirse pruebas adicionales, como bioquímica de orina y análisis de sangre en busca de trastornos metabólicos . [106] [127] Junto con el EEG y la neuroimagen, las pruebas genéticas se están convirtiendo en una de las técnicas de diagnóstico más importantes para la epilepsia, ya que se puede lograr un diagnóstico en una proporción relevante de casos con epilepsias graves, tanto en niños como en adultos. [128] Para aquellos con pruebas genéticas negativas, en algunos puede ser importante repetir o volver a analizar los estudios genéticos previos después de 2 a 3 años. [129]
Un nivel alto de prolactina en sangre dentro de los primeros 20 minutos posteriores a una convulsión puede ser útil para ayudar a confirmar una convulsión epiléptica en lugar de una convulsión psicógena no epiléptica . [130] [131] El nivel de prolactina sérica es menos útil para detectar convulsiones focales. [132] Si es normal, todavía es posible una convulsión epiléptica [131] y una prolactina sérica no separa las convulsiones epilépticas del síncope. [133] No se recomienda como parte rutinaria del diagnóstico de la epilepsia. [106]
El diagnóstico de la epilepsia puede ser difícil. Una serie de otras afecciones pueden presentar signos y síntomas muy similares a las convulsiones, incluyendo síncope , hiperventilación , migrañas, narcolepsia , ataques de pánico y convulsiones psicógenas no epilépticas (CNEP). [134] [135] En particular, el síncope puede ir acompañado de un breve episodio de convulsiones. [136] La epilepsia del lóbulo frontal nocturna , a menudo mal diagnosticada como pesadillas, se consideraba una parasomnia , pero más tarde se identificó como un síndrome epiléptico. [137] Los ataques del trastorno del movimiento discinesia paroxística pueden confundirse con convulsiones epilépticas. [138] La causa de un ataque de caída puede ser, entre muchas otras, una convulsión atónica. [135]
Los niños pueden tener conductas que se confunden fácilmente con ataques epilépticos, pero que no lo son. Estas incluyen espasmos del sollozo , enuresis , terrores nocturnos , tics y ataques de escalofríos . [135] El reflujo gastroesofágico puede causar arqueamiento de la espalda y torsión de la cabeza hacia un lado en los bebés, lo que puede confundirse con ataques tónico-clónicos. [135]
El diagnóstico erróneo es frecuente (ocurre en alrededor del 5 al 30% de los casos). [26] Diferentes estudios han demostrado que en muchos casos los ataques similares a convulsiones en la epilepsia aparentemente resistente al tratamiento tienen una causa cardiovascular. [136] [139] Aproximadamente el 20% de las personas atendidas en clínicas de epilepsia tienen CPNE [20] y de las que tienen CPNE, aproximadamente el 10% también tiene epilepsia; [140] separar los dos basándose solo en el episodio de convulsión sin más pruebas es a menudo difícil. [140]
Si bien muchos casos no se pueden prevenir, los esfuerzos para reducir las lesiones en la cabeza, [7] brindar una buena atención en el momento del nacimiento y reducir los parásitos ambientales como la tenia del cerdo pueden ser eficaces. [31] Los esfuerzos en una parte de América Central para reducir las tasas de tenia del cerdo resultaron en una disminución del 50% en nuevos casos de epilepsia. [19] El Nadi Shodhana Pranayama basado en yoga, también conocido como respiración nasal alternada, puede tener un impacto positivo en el sistema nervioso y ayudar a controlar los trastornos convulsivos. El ejercicio regular ayuda a equilibrar la función cerebral al proporcionarle oxígeno al cuerpo y eliminar el dióxido de carbono y las toxinas de la sangre. [141]
La epilepsia puede ser peligrosa cuando las convulsiones se producen en determinados momentos. El riesgo de ahogarse o de sufrir una colisión con un vehículo de motor es mayor. También se ha descubierto que las personas con epilepsia tienen más probabilidades de tener problemas psicológicos. [142] Otras complicaciones incluyen neumonía por aspiración y dificultad para aprender. [143]

La epilepsia generalmente se trata con medicación diaria una vez que se ha producido una segunda convulsión, [26] [106] mientras que la medicación puede iniciarse después de la primera convulsión en aquellos con alto riesgo de convulsiones posteriores. [106] Puede ser útil apoyar la autogestión de la enfermedad por parte de las personas . [144] En los casos resistentes a los fármacos se pueden considerar diferentes opciones de tratamiento , incluidas dietas especiales, la implantación de un neuroestimulador o neurocirugía .
Poner a las personas con una convulsión tónico-clónica activa de lado y en posición de recuperación ayuda a evitar que los líquidos entren en los pulmones. [145] No se recomienda introducir los dedos, un bloque de mordida o un depresor de lengua en la boca, ya que podría provocar vómitos en la persona o provocar que el rescatador sea mordido. [28] [145] Se deben tomar medidas para evitar más autolesiones. [28] Por lo general, no se necesitan precauciones para la columna vertebral . [145]
Si una convulsión dura más de 5 minutos o si hay más de dos convulsiones en 5 minutos sin un retorno a un nivel normal de conciencia entre ellas, se considera una emergencia médica conocida como estado epiléptico . [106] [146] Esto puede requerir ayuda médica para mantener la vía aérea abierta y protegida ; [106] una vía aérea nasofaríngea puede ser útil para esto. [145] En casa, la medicación inicial recomendada para la convulsión de larga duración es midazolam colocado en la nariz o la boca. [147] El diazepam también se puede usar por vía rectal . [147] En el hospital, se prefiere el lorazepam intravenoso. [106]
Si dos dosis de benzodiazepinas no son efectivas, se recomiendan otros medicamentos como la fenitoína . [106] El estado epiléptico convulsivo que no responde al tratamiento inicial generalmente requiere ingreso en la unidad de cuidados intensivos y tratamiento con agentes más fuertes como infusión de midazolam, ketamina, tiopentona o propofol. [106] La mayoría de las instituciones tienen una vía o protocolo preferido para ser utilizado en una emergencia convulsiva como el estado epiléptico. [106] Se ha descubierto que estos protocolos son efectivos para reducir el tiempo de administración del tratamiento. [106]

El tratamiento principal de la epilepsia son los anticonvulsivos, posiblemente durante toda la vida de la persona. [26] La elección del anticonvulsivo se basa en el tipo de convulsión, el síndrome epiléptico, otros medicamentos utilizados, otros problemas de salud y la edad y el estilo de vida de la persona. [147] Se recomienda un solo medicamento inicialmente; [148] si este no es eficaz, se recomienda cambiar a otro solo medicamento. [106] Se recomiendan dos medicamentos a la vez solo si un solo medicamento no funciona. [106] En aproximadamente la mitad, el primer agente es eficaz; un segundo agente único ayuda en aproximadamente el 13% y un tercero o dos agentes al mismo tiempo pueden ayudar a un 4% adicional. [149] Aproximadamente el 30% de las personas continúan teniendo convulsiones a pesar del tratamiento anticonvulsivo. [7]
Hay una serie de medicamentos disponibles, incluidos la fenitoína, la carbamazepina y el valproato . La evidencia sugiere que la fenitoína, la carbamazepina y el valproato pueden ser igualmente eficaces tanto en las convulsiones focales como en las generalizadas. [150] [151] La carbamazepina de liberación controlada parece funcionar tan bien como la carbamazepina de liberación inmediata y puede tener menos efectos secundarios . [152] [153] En el Reino Unido, la carbamazepina o la lamotrigina se recomiendan como tratamiento de primera línea para las convulsiones focales, y el levetiracetam y el valproato como segunda línea debido a problemas de costo y efectos secundarios. [106] [154] El valproato se recomienda como tratamiento de primera línea para las convulsiones generalizadas y la lamotrigina como segunda línea. [106] En aquellos con convulsiones de ausencia, se recomiendan etosuximida o valproato; el valproato es particularmente eficaz en las convulsiones mioclónicas y las convulsiones tónicas o atónicas. [106] Si las convulsiones están bien controladas con un tratamiento particular, generalmente no es necesario controlar rutinariamente los niveles de medicamento en la sangre. [106]
El anticonvulsivo menos costoso es el fenobarbital , cuyo precio ronda los 5 dólares al año. [19] La Organización Mundial de la Salud lo recomienda como medicamento de primera línea en el mundo en desarrollo y allí se utiliza habitualmente. [155] [156] Sin embargo, el acceso puede ser difícil, ya que algunos países lo etiquetan como un fármaco controlado . [19]
Los efectos adversos de los medicamentos se informan en el 10% al 90% de las personas, dependiendo de cómo y de quién se recopilan los datos. [157] La mayoría de los efectos adversos están relacionados con la dosis y son leves. [157] Algunos ejemplos incluyen cambios de humor, somnolencia o inestabilidad en la marcha. [157] Ciertos medicamentos tienen efectos secundarios que no están relacionados con la dosis, como erupciones cutáneas, toxicidad hepática o supresión de la médula ósea . [157] Hasta una cuarta parte de las personas interrumpen el tratamiento debido a efectos adversos. [157] Algunos medicamentos se asocian con defectos de nacimiento cuando se usan durante el embarazo. [106] Se ha informado que muchos de los medicamentos de uso común, como valproato, fenitoína, carbamazepina, fenobarbital y gabapentina, causan un mayor riesgo de defectos de nacimiento, [158] especialmente cuando se usan durante el primer trimestre . [159] A pesar de esto, el tratamiento a menudo se continúa una vez que es eficaz, porque se cree que el riesgo de epilepsia no tratada es mayor que el riesgo de los medicamentos. [159] Entre los medicamentos antiepilépticos, el levetiracetam y la lamotrigina parecen tener el menor riesgo de causar defectos de nacimiento. [158]
En algunas personas que no han tenido convulsiones durante dos a cuatro años, puede ser razonable suspender la medicación de forma gradual; sin embargo, alrededor de un tercio de las personas sufren una recurrencia, con mayor frecuencia durante los primeros seis meses. [106] [160] La suspensión es posible en aproximadamente el 70% de los niños y el 60% de los adultos. [31] Por lo general, no es necesario medir los niveles de medicación en aquellas personas cuyas convulsiones están bien controladas. [126]
La cirugía de la epilepsia debe considerarse para cualquier persona con epilepsia que sea refractaria al tratamiento médico. [16] Los pacientes son evaluados caso por caso en centros que están familiarizados y tienen experiencia en la cirugía de la epilepsia. [16] Los resultados de una revisión sistemática de 2023 encontraron que las intervenciones quirúrgicas para niños de 1 a 36 meses con epilepsia resistente a los medicamentos pueden conducir a una reducción significativa de las convulsiones o a la liberación de las mismas, especialmente cuando otros tratamientos han fallado. [161] La cirugía de la epilepsia puede ser una opción para las personas con convulsiones focales que siguen siendo un problema a pesar de otros tratamientos. [162] [163] Estos otros tratamientos incluyen al menos una prueba de dos o tres medicamentos. [164] El objetivo de la cirugía ha sido el control total de las convulsiones. [165] Sin embargo, la mayoría de los médicos creen que incluso la cirugía paliativa, en la que se reduce significativamente la carga de las convulsiones, puede ayudar a lograr un progreso en el desarrollo o la reversión del estancamiento del desarrollo en niños con epilepsia resistente a los medicamentos y esto puede lograrse en el 60-70% de los casos. [164] Los procedimientos comunes incluyen la extirpación del hipocampo a través de una resección del lóbulo temporal anterior, la extirpación de tumores y la extirpación de partes del neocórtex . [164] Algunos procedimientos como la callosotomía se intentan en un esfuerzo por disminuir la cantidad de convulsiones en lugar de curar la afección. [164] Después de la cirugía, los medicamentos pueden retirarse lentamente en muchos casos. [164] [162]
La neuroestimulación mediante la implantación de prótesis neurocibernéticas puede ser otra opción en aquellos que no son candidatos a la cirugía, proporcionando estimulación eléctrica pulsátil crónica de regiones nerviosas o cerebrales específicas, junto con la atención estándar. [106] Se han utilizado tres tipos en aquellos que no responden a los medicamentos: estimulación del nervio vago (VNS) , estimulación talámica anterior y estimulación reactiva de circuito cerrado (RNS). [5] [166] [167]
La modulación no farmacológica de los neurotransmisores a través de la estimulación sexual de alto nivel (h-VNS) puede reducir la frecuencia de las convulsiones en niños y adultos que no responden a la terapia médica y/o quirúrgica, en comparación con la estimulación sexual de bajo nivel (l-VNS). [167] En una revisión Cochrane de 2022 de cuatro ensayos controlados aleatorizados , con una certeza moderada de la evidencia, las personas que recibieron tratamiento con h-VNS tenían un 73 % más de probabilidades (13 % más de probabilidades a 164 % más de probabilidades) de experimentar una reducción en la frecuencia de las convulsiones de al menos el 50 % (el umbral mínimo definido para la respuesta clínica individual). [167] Potencialmente, 249 (163 a 380) por cada 1000 personas con epilepsia resistente a los medicamentos pueden lograr una reducción del 50 % en las convulsiones después de la h-VNS, lo que beneficia a 105 por cada 1000 personas adicionales en comparación con la l-VNS. [167]
Este resultado estuvo limitado por la cantidad de estudios disponibles y la calidad de un ensayo en particular, en el que tres personas recibieron l-VNS por error. Un análisis de sensibilidad sugirió que, en el mejor de los casos, la probabilidad de respuesta clínica a h-VNS podría ser un 91 % (27 % a 189 %) mayor que en aquellos que recibieron l-VNS. En el peor de los casos, la probabilidad de respuesta clínica a h-VNS todavía era un 61 % mayor (7 % mayor a 143 % mayor) que en aquellos que recibieron l-VNS. [167]
A pesar del beneficio potencial del tratamiento con h-VNS, la revisión Cochrane también encontró que el riesgo de varios efectos adversos era mayor que en quienes recibían l-VNS. Hubo certeza moderada de evidencia de que el riesgo de alteración de la voz o ronquera puede ser 2,17 (1,49 a 3,17) veces mayor que en las personas que recibían l-VNS. El riesgo de disnea también fue 2,45 (1,07 a 5,60) veces mayor que en los receptores de l-VNS, aunque el bajo número de eventos y estudios significó que la certeza de la evidencia fue baja. El riesgo de síntomas de rebote-abstinencia, tos, dolor y parestesia no fue claro. [167]
Hay evidencia prometedora de que una dieta cetogénica (alta en grasas, baja en carbohidratos , adecuada en proteínas ) disminuye la cantidad de convulsiones y elimina las convulsiones en algunos; sin embargo, es necesaria más investigación. [6] Una revisión sistemática de la literatura de 2022 ha encontrado alguna evidencia que respalda que una dieta cetogénica o una dieta Atkins modificada puede ser útil en el tratamiento de la epilepsia en algunos bebés. [168] Este tipo de dietas pueden ser beneficiosas para los niños con epilepsia resistente a los medicamentos; el uso para adultos sigue siendo incierto. [6] Los efectos adversos notificados con mayor frecuencia fueron vómitos, estreñimiento y diarrea. [6] No está claro por qué funciona esta dieta. [169] En personas con enfermedad celíaca o sensibilidad al gluten no celíaca y calcificaciones occipitales, una dieta sin gluten puede disminuir la frecuencia de las convulsiones. [90]
La terapia de evitación consiste en minimizar o eliminar los desencadenantes. Por ejemplo, las personas sensibles a la luz pueden tener éxito utilizando un televisor pequeño, evitando los videojuegos o usando gafas oscuras. [170] La biorretroalimentación operante basada en las ondas del EEG tiene cierto apoyo en aquellas personas que no responden a los medicamentos. [171] Sin embargo, los métodos psicológicos no deben utilizarse para reemplazar los medicamentos. [106]
Se ha propuesto que el ejercicio podría ser útil para prevenir las convulsiones, [172] con algunos datos que respaldan esta afirmación. [173] Algunos perros, comúnmente conocidos como perros de convulsiones , pueden ayudar durante o después de una convulsión. [174] [175] No está claro si los perros tienen la capacidad de predecir las convulsiones antes de que ocurran. [176]
Hay evidencia de calidad moderada que apoya el uso de intervenciones psicológicas junto con otros tratamientos para la epilepsia. [177] Esto puede mejorar la calidad de vida, mejorar el bienestar emocional y reducir la fatiga en adultos y adolescentes. [177] Las intervenciones psicológicas también pueden mejorar el control de las convulsiones en algunas personas al promover la autogestión y la adherencia. [177]
Como terapia complementaria en aquellos que no están bien controlados con otros medicamentos, el cannabidiol parece ser útil en algunos niños. [178] [179] En 2018, la FDA aprobó este producto para el síndrome de Lennox-Gastaut y el síndrome de Dravet. [180]
Hay algunos estudios sobre el uso de dexametasona para el tratamiento exitoso de convulsiones resistentes a medicamentos tanto en adultos como en niños. [181]
La medicina alternativa, incluida la acupuntura , [182] las vitaminas de rutina , [183] y el yoga , [184] no tienen evidencia confiable que respalde su uso en la epilepsia. La melatonina , a partir de 2016 [actualizar], no está respaldada por evidencia suficiente. [185] Los ensayos fueron de mala calidad metodológica y no fue posible extraer conclusiones definitivas. [185]
Se ha informado que varios suplementos (con evidencias de distinta fiabilidad) son útiles para la epilepsia resistente a los fármacos. Entre ellos se incluyen dosis altas de Omega-3, berberina, miel de Manuka, hongos reishi y melena de león, curcumina [186] , vitamina E, coenzima Q-10 y resveratrol. La razón por la que estos pueden funcionar (en teoría) es que reducen la inflamación o el estrés oxidativo, dos de los principales mecanismos que contribuyen a la epilepsia [187] .
Las mujeres en edad fértil, incluidas aquellas con epilepsia, corren el riesgo de embarazos no deseados si no utilizan un método anticonceptivo eficaz . [188] Las mujeres con epilepsia pueden experimentar un aumento temporal en la frecuencia de las convulsiones cuando comienzan a usar anticoncepción hormonal . [188]
Algunos medicamentos anticonvulsivos interactúan con las enzimas del hígado y hacen que los fármacos de la anticoncepción hormonal se descompongan más rápidamente. Estos fármacos inductores de enzimas hacen que la anticoncepción hormonal sea menos efectiva, y esto es particularmente peligroso si el medicamento anticonvulsivo está asociado con defectos de nacimiento. [189] Los medicamentos anticonvulsivos inductores de enzimas potentes incluyen carbamazepina , acetato de eslicarbazepina , oxcarbazepina , fenobarbital , fenitoína , primidona y rufinamida . Los medicamentos perampanel y topiramato pueden ser inductores de enzimas en dosis más altas. [190] Por el contrario, la anticoncepción hormonal puede reducir la cantidad del medicamento anticonvulsivo lamotrigina que circula en el cuerpo, haciéndolo menos efectivo. [188] La tasa de fracaso de los anticonceptivos orales, cuando se usan correctamente, es del 1%, pero aumenta a entre el 3 y el 6% en mujeres con epilepsia. [189] En general, los dispositivos intrauterinos (DIU) son los preferidos para las mujeres con epilepsia que no tienen intención de quedar embarazadas. [188]
Las mujeres con epilepsia, especialmente si tienen otras afecciones médicas, pueden tener una probabilidad ligeramente menor, pero aún alta, de quedar embarazadas. [188] Las mujeres con infertilidad tienen aproximadamente la misma probabilidad de éxito con la fertilización in vitro u otras formas de tecnología de reproducción asistida que las mujeres sin epilepsia. [188] Puede haber un mayor riesgo de pérdida del embarazo . [188]
Una vez que se queda embarazada, existen dos preocupaciones principales relacionadas con el embarazo . La primera preocupación es el riesgo de convulsiones durante el embarazo, y la segunda preocupación es que los medicamentos anticonvulsivos pueden provocar defectos de nacimiento . [158] La mayoría de las mujeres con epilepsia deben continuar el tratamiento con medicamentos anticonvulsivos, y el objetivo del tratamiento es equilibrar la necesidad de prevenir las convulsiones con la necesidad de prevenir los defectos de nacimiento inducidos por los medicamentos. [188] [191]
El embarazo no parece cambiar mucho la frecuencia de las convulsiones. [188] Sin embargo, cuando ocurren convulsiones, pueden causar algunas complicaciones durante el embarazo, como partos prematuros o bebés que nacen más pequeños de lo normal . [188]
Todos los embarazos tienen un riesgo de defectos congénitos, por ejemplo, debido al tabaquismo durante el embarazo . [188] Además de este nivel típico de riesgo, algunos medicamentos anticonvulsivos aumentan significativamente el riesgo de defectos congénitos y restricción del crecimiento intrauterino , así como trastornos del desarrollo , neurocognitivos y del comportamiento . [191] La mayoría de las mujeres con epilepsia reciben un tratamiento seguro y eficaz y tienen hijos típicos y sanos. [191] Los riesgos más altos están asociados con medicamentos anticonvulsivos específicos, como el ácido valproico y la carbamazepina, y con dosis más altas. [158] [188] La suplementación con ácido fólico , como a través de vitaminas prenatales , redujo el riesgo. [188] Planificar los embarazos con anticipación brinda a las mujeres con epilepsia la oportunidad de cambiar a un programa de tratamiento de menor riesgo y dosis reducidas del medicamento. [188]
Aunque los medicamentos anticonvulsivos se pueden encontrar en la leche materna , las mujeres con epilepsia pueden amamantar a sus bebés y los beneficios generalmente superan los riesgos. [188]

La epilepsia no suele curarse, pero la medicación puede controlar las convulsiones de forma eficaz en aproximadamente el 70% de los casos. [7] De las personas con convulsiones generalizadas, más del 80% se pueden controlar bien con medicamentos, mientras que esto es cierto solo en el 50% de las personas con convulsiones focales. [5] Un predictor del resultado a largo plazo es el número de convulsiones que ocurren en los primeros seis meses. [26] Otros factores que aumentan el riesgo de un mal resultado incluyen poca respuesta al tratamiento inicial, convulsiones generalizadas, antecedentes familiares de epilepsia, problemas psiquiátricos y ondas en el EEG que representan actividad epileptiforme generalizada. [192] Según la ILAE, la epilepsia se considera resuelta si un individuo con epilepsia no tiene convulsiones durante 10 años y no toma anticonvulsivos durante 5 años. [193]
En el mundo en desarrollo, el 75% de las personas no reciben tratamiento o no reciben el tratamiento adecuado. [31] En África, el 90% no recibe tratamiento. [31] Esto se debe en parte a que no se dispone de medicamentos adecuados o estos son demasiado caros. [31]
Las personas con epilepsia pueden tener un mayor riesgo de muerte prematura en comparación con aquellas que no padecen esta afección. [194] Se estima que este riesgo es entre 1,6 y 4,1 veces mayor que el de la población general. [195] El mayor aumento de mortalidad por epilepsia se da entre los ancianos. [195] Las personas con epilepsia debido a una causa desconocida tienen un aumento relativamente bajo del riesgo. [195]
La mortalidad a menudo está relacionada con la causa subyacente de las convulsiones, el estado epiléptico, el suicidio, el trauma y la muerte súbita inesperada en la epilepsia (SUDEP). [194] La muerte por estado epiléptico se debe principalmente a un problema subyacente en lugar de a la omisión de dosis de medicamentos. [194] El riesgo de suicidio es entre dos y seis veces mayor en las personas con epilepsia; [196] [197] la causa de esto no está clara. [196] La SUDEP parece estar parcialmente relacionada con la frecuencia de las convulsiones tónico-clónicas generalizadas [198] y representa aproximadamente el 15% de las muertes relacionadas con la epilepsia; [192] no está claro cómo disminuir su riesgo. [198] Los factores de riesgo de SUDEP incluyen convulsiones tónico-clónicas generalizadas nocturnas, convulsiones, dormir solo y epilepsia médicamente intratable. [199]
En el Reino Unido, se estima que entre el 40% y el 60% de las muertes son posiblemente prevenibles. [26] En el mundo en desarrollo, muchas muertes se deben a una epilepsia no tratada que provoca caídas o estado epiléptico. [19]
La epilepsia es uno de los trastornos neurológicos graves más comunes [200] que afecta a unos 50 millones de personas en 2021. [actualizar][ 8] [201] Afecta al 1% de la población a los 20 años y al 3% a los 75 años. [17] Es más común en hombres que en mujeres y la diferencia general es pequeña. [19] [69] La mayoría de las personas con el trastorno (80%) pertenecen a poblaciones de bajos ingresos [202] o al mundo en desarrollo . [31]
La prevalencia estimada de epilepsia activa (a partir de 2012 [actualizar]) está en el rango de 3 a 10 por 1000, y se define como epilepsia activa a alguien con epilepsia que ha tenido al menos una convulsión no provocada en los últimos cinco años. [69] [203] La epilepsia comienza cada año en 40 a 70 por 100 000 en los países desarrollados y en 80 a 140 por 100 000 en los países en desarrollo. [31] La pobreza es un riesgo e incluye tanto ser de un país pobre como ser pobre en relación con otros dentro del propio país. [19] En el mundo desarrollado, la epilepsia comienza más comúnmente en los jóvenes o en los ancianos. [19] En el mundo en desarrollo, su aparición es más común en niños mayores y adultos jóvenes debido a las mayores tasas de trauma y enfermedades infecciosas. [19] En los países desarrollados, el número de casos al año ha disminuido en niños y ha aumentado entre los ancianos entre los años 1970 y 2003. [203] Esto se ha atribuido en parte a una mejor supervivencia después de los accidentes cerebrovasculares en los ancianos. [69]

Los registros médicos más antiguos muestran que la epilepsia ha estado afectando a las personas al menos desde el comienzo de la historia registrada. [204] A lo largo de la historia antigua , se pensó que la condición era de causa espiritual. [204] La descripción más antigua del mundo de una convulsión epiléptica proviene de un texto en acadio (un idioma usado en la antigua Mesopotamia ) y fue escrito alrededor del 2000 a. C. [24] La persona descrita en el texto fue diagnosticada como bajo la influencia de un dios de la luna y se sometió a un exorcismo . [24] Las convulsiones epilépticas se enumeran en el Código de Hammurabi ( c. 1790 a. C. ) como motivo por el cual un esclavo comprado puede ser devuelto para un reembolso, [24] y el Papiro de Edwin Smith ( c. 1700 a. C. ) describe casos de individuos con convulsiones epilépticas. [24]
El registro detallado más antiguo conocido de la condición en sí se encuentra en el Sakikku , un texto médico cuneiforme babilónico de 1067-1046 a. C. [204] Este texto proporciona signos y síntomas, detalla el tratamiento y los resultados probables, [24] y describe muchas características de los diferentes tipos de convulsiones. [204] Como los babilonios no tenían un conocimiento biomédico de la naturaleza de la epilepsia, atribuyeron las convulsiones a la posesión de espíritus malignos y pidieron que se tratara la condición a través de medios espirituales. [204] Alrededor del 900 a. C., Punarvasu Atreya describió la epilepsia como pérdida de conciencia; [205] esta definición se trasladó al texto ayurvédico de Charaka Samhita ( c. 400 a. C. ). [206]
Los antiguos griegos tenían puntos de vista contradictorios sobre la condición. Pensaban en la epilepsia como una forma de posesión espiritual, pero también asociaban la condición con el genio y lo divino. Uno de los nombres que le dieron fue la enfermedad sagrada ( griego antiguo : ἠ ἱερὰ νόσος ). [24] [207] La epilepsia aparece dentro de la mitología griega: está asociada con las diosas lunares Selene y Artemisa , que afligían a quienes las molestaban. Los griegos pensaban que figuras importantes como Julio César y Hércules tenían la condición. [24] La notable excepción a esta visión divina y espiritual fue la de la escuela de Hipócrates . En el siglo V a. C., Hipócrates rechazó la idea de que la condición fuera causada por espíritus. En su obra histórica Sobre la enfermedad sagrada , propuso que la epilepsia no era de origen divino y, en cambio, era un problema médicamente tratable que se originaba en el cerebro. [24] [204] Acusó a los de atribuir una causa sagrada a la condición de difundir la ignorancia a través de una creencia en la magia supersticiosa. [24] Hipócrates propuso que la herencia era importante como causa, describió peores resultados si la condición se presenta a una edad temprana e hizo notar las características físicas, así como la vergüenza social asociada con ella. [24] En lugar de referirse a ella como la enfermedad sagrada , utilizó el término gran enfermedad , dando lugar al término moderno grand mal , utilizado para las convulsiones tónico-clónicas. [24] A pesar de su trabajo que detalla los orígenes físicos de la condición, su punto de vista no fue aceptado en ese momento. [204] Los espíritus malignos continuaron siendo culpados hasta al menos el siglo XVII. [204]
En la antigua Roma, la gente no comía ni bebía con la misma cerámica que usaba alguien afectado. [208] La gente de la época escupía en su pecho creyendo que esto evitaría que el problema los afectara. [208] Según Apuleyo y otros médicos antiguos, para detectar la epilepsia, era común encender un trozo de gagates , cuyo humo desencadenaría la convulsión. [209] Ocasionalmente se usaba un torno de alfarero giratorio, tal vez una referencia a la epilepsia fotosensible . [210]
En la mayoría de las culturas, las personas con epilepsia han sido estigmatizadas, rechazadas o incluso encarceladas. Incluso en la segunda mitad del siglo XX, en Tanzania y otras partes de África, la epilepsia se asociaba con la posesión por espíritus malignos, la brujería o el envenenamiento y muchos creían que era contagiosa. [211] En la Salpêtrière , la cuna de la neurología moderna, Jean-Martin Charcot encontró a personas con epilepsia junto a enfermos mentales, personas con sífilis crónica y criminales locos. [212] En la antigua Roma, la epilepsia se conocía como morbus comitialis o "enfermedad del salón de actos" y se consideraba una maldición de los dioses. En el norte de Italia, la epilepsia se conocía tradicionalmente como la enfermedad de San Valentín. [213] Al menos en la década de 1840 en los Estados Unidos de América, la epilepsia era conocida como la enfermedad de las caídas o los ataques de caída , y era considerada una forma de locura médica . [214] Alrededor del mismo período de tiempo, la epilepsia era conocida en Francia como haut-mal (lit. " gran mal ") , mal-de terre (lit. " enfermedad de la tierra ") , mal de Saint Jean (lit. " enfermedad de San Juan" ) , mal des enfans (lit. " enfermedad de los niños ") y mal-caduc (lit. " enfermedad de las caídas ") . [214] Los pacientes de epilepsia en Francia también eran conocidos como tombeurs (lit. " personas que se caen ") , debido a las convulsiones y la pérdida de conciencia en un episodio epiléptico. [214]
A mediados del siglo XIX se introdujo el primer medicamento anticonvulsivo eficaz, el bromuro . [157] El primer tratamiento moderno, el fenobarbital, se desarrolló en 1912, y la fenitoína empezó a utilizarse en 1938. [215]
El estigma social es una experiencia común, en todo el mundo, para aquellos con epilepsia. [11] [216] Puede afectar a las personas económica, social y culturalmente. [216] En India y China, la epilepsia puede usarse como justificación para negar el matrimonio. [31] La gente en algunas áreas todavía cree que aquellos con epilepsia están malditos . [19] En partes de África, como Tanzania y Uganda , se afirma que la epilepsia está asociada con la posesión por espíritus malignos, la brujería o el envenenamiento y muchos creen incorrectamente que es contagiosa . [211] [19] Antes de 1971 en el Reino Unido, la epilepsia se consideraba motivo de anulación del matrimonio. [31] El estigma puede dar lugar a que algunas personas con epilepsia nieguen haber tenido alguna vez convulsiones. [69]
Las convulsiones tienen un coste económico directo de unos mil millones de dólares en Estados Unidos. [20] La epilepsia tuvo un coste económico en Europa de unos 15.500 millones de euros en 2004. [26] En la India, se calcula que la epilepsia tiene un coste de 1.700 millones de dólares estadounidenses o el 0,5% del PIB. [31] Es la causa de aproximadamente el 1% de las visitas a urgencias (el 2% en el caso de los servicios de urgencias pediátricas) en Estados Unidos. [217]
Las personas con epilepsia tienen aproximadamente el doble de riesgo de verse involucradas en una colisión de vehículos de motor y, por lo tanto, en muchas áreas del mundo no se les permite conducir o solo pueden conducir si se cumplen ciertas condiciones. [23] Se ha sugerido que el retraso en el diagnóstico es una causa de algunas colisiones de vehículos de motor potencialmente evitables, ya que al menos un estudio mostró que la mayoría de los accidentes de vehículos de motor ocurrieron en personas con convulsiones no motoras no diagnosticadas en comparación con aquellos con convulsiones motoras al inicio de la epilepsia. [218] En algunos lugares, los médicos están obligados por ley a informar si una persona ha tenido una convulsión al organismo de licencias, mientras que en otros el requisito es solo que alienten a la persona en cuestión a informarlo él mismo. [23] Los países que requieren informes médicos incluyen Suecia, Austria, Dinamarca y España. [23] Los países que requieren que la persona informe incluyen el Reino Unido y Nueva Zelanda, y los médicos pueden informar si creen que la persona aún no lo ha hecho. [23] En Canadá, Estados Unidos y Australia, los requisitos sobre informes varían según la provincia o el estado. [23] Si las convulsiones están bien controladas, la mayoría cree que es razonable permitir conducir. [219] El tiempo que una persona debe estar libre de convulsiones antes de poder conducir varía según el país. [219] Muchos países exigen que pase de uno a tres años sin convulsiones. [219] En los Estados Unidos, el tiempo necesario sin convulsiones lo determina cada estado y es de entre tres meses y un año. [219]
A las personas que padecen epilepsia o convulsiones generalmente se les niega la licencia de piloto. [220]
Existen organizaciones que brindan apoyo a las personas y familias afectadas por la epilepsia. La campaña Out of the Shadows , un esfuerzo conjunto de la Organización Mundial de la Salud, la ILAE y la Oficina Internacional para la Epilepsia , brinda ayuda a nivel internacional. [31] En los Estados Unidos, la Fundación para la Epilepsia es una organización nacional que trabaja para aumentar la aceptación de las personas con el trastorno, su capacidad para funcionar en la sociedad y promover la investigación para una cura. [226] La Fundación para la Epilepsia, algunos hospitales y algunas personas también dirigen grupos de apoyo en los Estados Unidos. [227] En Australia, la Fundación para la Epilepsia brinda apoyo, brinda educación y capacitación y financia la investigación para personas que viven con epilepsia.
El Día Internacional de la Epilepsia (Día Mundial de la Epilepsia) comenzó en 2015 y se celebra el segundo lunes de febrero. [228] [229]
El Día Púrpura , un día mundial diferente de concientización sobre la epilepsia, fue iniciado por una niña canadiense de nueve años llamada Cassidy Megan en 2008, y se celebra cada año el 26 de marzo. [230]
La predicción de convulsiones se refiere a los intentos de pronosticar convulsiones epilépticas basándose en el EEG antes de que ocurran. [231] Hasta 2011 [actualizar], no se ha desarrollado ningún mecanismo eficaz para predecir las convulsiones. [231] Aunque no hay ningún dispositivo eficaz que pueda predecir las convulsiones, la ciencia detrás de la predicción de convulsiones y la capacidad de proporcionar dicha herramienta ha avanzado.
El kindling , donde las exposiciones repetidas a eventos que podrían causar convulsiones eventualmente causan convulsiones más fácilmente, se ha utilizado para crear modelos animales de epilepsia. [232] Se han caracterizado diferentes modelos animales de epilepsia en roedores que recapitulan el EEG y los concomitantes conductuales de diferentes formas de epilepsia, en particular la aparición de convulsiones espontáneas recurrentes. [233] Debido a que las convulsiones epilépticas de diferentes tipos se observan naturalmente en algunos de estos animales, se han seleccionado cepas de ratones y ratas para ser utilizadas como modelos genéticos de epilepsia. En particular, varias líneas de ratones y ratas muestran descargas de punta y onda cuando se registra el EEG y se han estudiado para comprender la epilepsia de ausencia. [234] Entre estos modelos, la cepa de GAERS (Ratas de Epilepsia de Ausencia Genética de Estrasburgo) se caracterizó en la década de 1980 y ha ayudado a comprender los mecanismos subyacentes a la epilepsia de ausencia infantil. [235]
Los cortes de cerebro de rata sirven como un modelo valioso para evaluar el potencial de los compuestos para reducir la actividad epileptiforme. Al evaluar la frecuencia de la explosión epileptiforme en las redes del hipocampo, los investigadores pueden identificar candidatos prometedores para nuevos fármacos anticonvulsivos. [236]
Una de las hipótesis presentes en la literatura se basa en las vías inflamatorias. Estudios que apoyan este mecanismo revelaron que los factores inflamatorios, glucolipídicos y oxidativos están más elevados en pacientes con epilepsia, especialmente en aquellos con epilepsia generalizada. [237]
La terapia génica se está estudiando en algunos tipos de epilepsia. [238] Los medicamentos que alteran la función inmunológica, como las inmunoglobulinas intravenosas , pueden reducir la frecuencia de las convulsiones cuando se incluyen en la atención normal como terapia complementaria; sin embargo, se requiere más investigación para determinar si estos medicamentos son muy bien tolerados en niños y adultos con epilepsia. [239] La radiocirugía estereotáctica no invasiva se [actualizar]está comparando , a partir de 2012 , con la cirugía estándar para ciertos tipos de epilepsia. [240]
La epilepsia se presenta en otros animales, incluidos perros y gatos; de hecho, es el trastorno cerebral más común en perros. [241] Por lo general, se trata con anticonvulsivos como levetiracetam, fenobarbital o bromuro en perros y fenobarbital en gatos. [241] La imepitoína también se utiliza en perros. [242] Si bien las convulsiones generalizadas en caballos son bastante fáciles de diagnosticar, puede ser más difícil en convulsiones no generalizadas y los EEG pueden ser útiles. [243]
A San Valentín se lo invoca para la curación y el amor. Protege contra los desmayos y se le pide que cure la epilepsia y otros trastornos convulsivos. En el norte de Italia, la epilepsia se conocía tradicionalmente como la enfermedad de San Valentín.