La toxoplasmosis es una enfermedad parasitaria causada por Toxoplasma gondii , un apicomplejo . [3] Las infecciones por toxoplasmosis están asociadas con una variedad de afecciones neuropsiquiátricas y conductuales. [8] Ocasionalmente, las personas pueden tener algunas semanas o meses de una enfermedad leve similar a la gripe , como dolores musculares y sensibilidad en los ganglios linfáticos . [1] En un pequeño número de personas, se pueden desarrollar problemas oculares. [1] En personas con un sistema inmunológico débil , pueden ocurrir síntomas graves como convulsiones y mala coordinación. [1] Si una mujer se infecta durante el embarazo , una condición conocida como toxoplasmosis congénita puede afectar al niño. [1]
La toxoplasmosis generalmente se transmite al comer alimentos mal cocinados que contienen quistes , la exposición a heces de gatos infectados y de una mujer infectada a su bebé durante el embarazo. [3] En raras ocasiones, la enfermedad se puede transmitir mediante transfusión de sangre . [3] De lo contrario, no se transmite entre personas. [3] Se sabe que el parásito se reproduce sexualmente sólo en la familia de los gatos . [9] Sin embargo, puede infectar a la mayoría de los tipos de animales de sangre caliente , incluidos los humanos. [9] El diagnóstico generalmente se realiza mediante análisis de sangre en busca de anticuerpos o mediante análisis del líquido amniótico en una paciente embarazada para detectar el ADN del parásito . [4]
La prevención consiste en preparar y cocinar adecuadamente los alimentos. [10] También se recomienda a las mujeres embarazadas que no limpien las cajas de arena para gatos o, si es necesario, que usen guantes y se laven las manos después. [10] Por lo general, no es necesario tratar a personas que por lo demás están sanas. [5] Durante el embarazo, se puede utilizar espiramicina o pirimetamina / sulfadiazina y ácido folínico como tratamiento. [5]
Hasta la mitad de la población mundial está infectada por T. gondii , pero no presenta síntomas. [7] En los Estados Unidos, aproximadamente el 11% de las personas han sido infectadas, mientras que en algunas áreas del mundo esto es más del 60%. [3] Aproximadamente 200.000 casos de toxoplasmosis congénita ocurren al año. [6] Charles Nicolle y Louis Manceaux describieron por primera vez el organismo en 1908. [11] En 1941, se confirmó la transmisión durante el embarazo de una mujer embarazada a su bebé. [11] Hay pruebas provisionales de que la infección puede afectar el comportamiento de las personas. [12]
La infección tiene tres etapas:
La toxoplasmosis aguda suele ser asintomática en adultos sanos. [13] [14] Sin embargo, los síntomas pueden manifestarse y, a menudo, son similares a los de la gripe : ganglios linfáticos inflamados , dolores de cabeza, fiebre y fatiga, [15] o dolores musculares que duran un mes o más. Es raro que un ser humano con un sistema inmunológico en pleno funcionamiento desarrolle síntomas graves después de una infección. Es probable que las personas con sistemas inmunitarios debilitados experimenten dolor de cabeza, confusión, mala coordinación, convulsiones, problemas pulmonares que pueden parecerse a la tuberculosis o la neumonía por Pneumocystis jirovecii (una infección oportunista común que ocurre en personas con SIDA) o coriorretinitis causada por una inflamación grave de la retina. (toxoplasmosis ocular). [15] Los niños pequeños y las personas inmunocomprometidas , como aquellos con VIH/SIDA, aquellos que reciben ciertos tipos de quimioterapia o aquellos que han recibido recientemente un trasplante de órgano , pueden desarrollar toxoplasmosis grave. Esto puede causar daño al cerebro ( encefalitis ) o a los ojos ( retinocoroiditis necrotizante ). [16] Los bebés infectados por transmisión placentaria pueden nacer con cualquiera de estos problemas o con malformaciones nasales, aunque estas complicaciones son poco comunes en los recién nacidos. Los trofozoítos toxoplásmicos que causan la toxoplasmosis aguda se denominan taquizoítos y normalmente se encuentran en diversos tejidos y fluidos corporales, pero rara vez en la sangre o el líquido cefalorraquídeo. [17]
Los ganglios linfáticos inflamados se encuentran comúnmente en el cuello o debajo del mentón, seguidos de las axilas y la ingle. La hinchazón puede ocurrir en diferentes momentos después de la infección inicial, persistir y reaparecer durante varios momentos independientemente del tratamiento antiparasitario. [18] Por lo general, se encuentra en sitios únicos en adultos, pero en niños, puede ser más común que existan sitios múltiples. Los ganglios linfáticos agrandados se resolverán en 1 a 2 meses en el 60% de los casos. Sin embargo, una cuarta parte de los afectados tarda entre 2 y 4 meses en volver a la normalidad, y el 8% tarda entre 4 y 6 meses. Un número considerable (6%) no vuelve a la normalidad hasta mucho más tarde. [19]
Debido a la ausencia de síntomas obvios, [13] [14] los huéspedes se infectan fácilmente con T. gondii y desarrollan toxoplasmosis sin saberlo. Aunque ocasionalmente se presentan síntomas leves parecidos a los de la gripe durante las primeras semanas después de la exposición, la infección por T. gondii no produce síntomas fácilmente observables en adultos humanos sanos. [7] [20] En la mayoría de las personas inmunocompetentes , la infección entra en una fase latente, durante la cual sólo están presentes bradizoítos ( en quistes tisulares ); [21] Estos quistes tisulares e incluso lesiones pueden ocurrir en las retinas , el revestimiento alveolar de los pulmones (donde una infección aguda puede imitar una infección por Pneumocystis jirovecii ), el corazón, el músculo esquelético y el sistema nervioso central (SNC), incluido el cerebro. . [22] Los quistes se forman en el SNC ( tejido cerebral ) tras la infección con T. gondii y persisten durante toda la vida del huésped. [23] La mayoría de los bebés que se infectan mientras están en el útero no presentan síntomas al nacer, pero pueden desarrollar síntomas más adelante en la vida. [24]
Las revisiones de estudios serológicos han estimado que entre el 30% y el 50% de la población mundial ha estado expuesta y puede estar infectada crónicamente con toxoplasmosis latente, aunque las tasas de infección difieren significativamente de un país a otro. [7] [25] [26] Este estado latente de infección se ha asociado recientemente con numerosas cargas de enfermedad , [7] alteraciones neuronales, [23] [25] y cambios sutiles de comportamiento dependientes del género en humanos inmunocompetentes, [27] [ 28] así como un mayor riesgo de colisiones de vehículos de motor. [29]
Aunque son raras, pueden ocurrir lesiones cutáneas en la forma adquirida de la enfermedad, incluidas erupciones similares a roséola y eritema multiforme, nódulos similares a prurigo , urticaria y lesiones maculopapulares . Los recién nacidos pueden tener máculas puntiformes, equimosis o lesiones en forma de "muffin de arándanos". El diagnóstico de toxoplasmosis cutánea se basa en la forma taquizoítica de T. gondii que se encuentra en la epidermis . [30] Se encuentra en todos los niveles de la epidermis, mide aproximadamente 6 por 2 μm y tiene forma de arco, y el núcleo mide un tercio de su tamaño. Se puede identificar mediante microscopía electrónica o mediante tinción de tejido con Giemsa, donde el citoplasma se muestra azul y el núcleo rojo. [31]
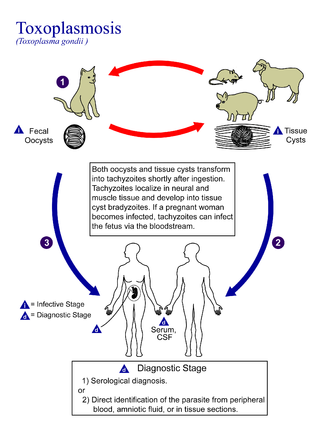
En su ciclo de vida, T. gondii adopta varias formas. [32] Los taquizoitos son responsables de la infección aguda; se dividen rápidamente y se diseminan a través de los tejidos del cuerpo. Los taquizoitos también se conocen como "merozoitos taquizoicos", término descriptivo que transmite con mayor precisión la naturaleza parasitológica de esta etapa. [33] Después de proliferar, los taquizoítos se convierten en bradizoítos , que se encuentran dentro de quistes de tejido intracelular latentes que se forman principalmente en los músculos y el cerebro. La formación de quistes es provocada en parte por la presión del sistema inmunológico del huésped. [34] Los bradizoitos (también llamados "merozoitos bradizoicos") no responden a los antibióticos. Los bradizoitos, una vez formados, pueden permanecer en los tejidos durante toda la vida del huésped. En un huésped sano, si algunos bradizoítos se convierten nuevamente en taquizoítos activos, el sistema inmunológico los destruirá rápidamente. Sin embargo, en personas inmunocomprometidas o en fetos que carecen de un sistema inmunológico desarrollado, los taquizoítos pueden proliferar y causar daños neurológicos importantes. [32]
La supervivencia del parásito depende de un equilibrio entre la supervivencia del huésped y la proliferación del parásito. [34] T. gondii logra este equilibrio manipulando la respuesta inmune del huésped, reduciendo la respuesta inmune del huésped y mejorando la ventaja reproductiva del parásito. [34] Una vez que infecta una célula huésped normal, resiste el daño causado por el sistema inmunológico del huésped y cambia los procesos inmunológicos del huésped. [35] A medida que se abre paso hacia la célula huésped, el parásito forma una membrana de vacuola parasitófora (PV) a partir de la membrana de la célula huésped. [2] [36] El PV encapsula al parásito y es resistente a la actividad del sistema endolisosomal y puede tomar el control de las mitocondrias y el retículo endoplásmico del huésped . [2] [36]
Cuando invade la célula por primera vez, el parásito libera proteínas ROP del bulbo del orgánulo róptrio . [2] Estas proteínas se trasladan al núcleo y a la superficie de la membrana PV donde pueden activar vías STAT para modular la expresión de citocinas a nivel transcripcional, unirse e inactivar la membrana PV destruyendo las proteínas IRG , entre otros posibles efectos. [2] [36] [37] Además, ciertas cepas de T. gondii pueden secretar una proteína conocida como GRA15, que activa la vía NF-κB , que regula positivamente la citoquina proinflamatoria IL-12 en la respuesta inmune temprana, lo que posiblemente lleve a a la fase latente del parásito. [2] La capacidad del parásito para secretar estas proteínas depende de su genotipo y afecta su virulencia. [2] [37]
El parásito también influye en un mecanismo antiapoptótico, lo que permite que las células huésped infectadas persistan y se repliquen. Un método de resistencia a la apoptosis es alterar las proteínas efectoras de proapoptosis, como BAX y BAK . [38] Para alterar estas proteínas, T. gondii provoca cambios conformacionales en las proteínas, que impiden que las proteínas sean transportadas a varios compartimentos celulares donde inician eventos de apoptosis. Sin embargo, T. gondii no provoca una regulación negativa de las proteínas efectoras de proapoptosis. [38]
T. gondii también tiene la capacidad de iniciar la autofagia de las células del huésped. [39] Esto conduce a una disminución de las células sanas y no infectadas y, en consecuencia, a un menor número de células huésped para atacar a las células infectadas. La investigación de Wang et al encuentra que las células infectadas conducen a niveles más altos de autofagosomas en las células normales e infectadas. [39] Su investigación revela que T. gondii provoca la autofagia de la célula huésped utilizando una vía dependiente del calcio. [39] Otro estudio sugiere que el parásito puede afectar directamente el calcio que se libera de las reservas de calcio, que son importantes para los procesos de señalización de las células. [38]
Los mecanismos anteriores permiten que T. gondii persista en un huésped. Uno de los factores limitantes del toxoplasma es que su influencia sobre las células huésped es más fuerte en un sistema inmunológico débil y depende de la cantidad, por lo que una gran cantidad de T. gondii por célula huésped causa un efecto más severo. [40] El efecto sobre el huésped también depende de la fortaleza del sistema inmunológico del huésped. Las personas inmunocompetentes normalmente no muestran síntomas graves o ninguno, mientras que las personas inmunodeprimidas pueden sufrir muerte o complicaciones graves. [40]
Se ha demostrado que T. gondii produce una proteína llamada GRA28, liberada por la vía secretora MYR1, que interfiere con la expresión genética en las células infectadas y da como resultado células que se comportan como células dendríticas y se vuelven muy móviles en el cuerpo. [41]
Dado que el parásito puede cambiar la respuesta inmune del huésped, también puede tener un efecto, positivo o negativo, en la respuesta inmune a otras amenazas patógenas. [34] Esto incluye, entre otras, las respuestas a las infecciones por Helicobacter felis , Leishmania major u otros parásitos, como Nippostrongylus brasiliensis . [34]
La toxoplasmosis generalmente se transmite a través de la boca cuando se ingieren accidentalmente ooquistes o quistes de tejido de Toxoplasma gondii . [42] También puede ocurrir transmisión congénita de la madre al feto. [43] La transmisión también puede ocurrir durante el proceso de trasplante de órganos sólidos [44] o trasplantes de células madre hematógenas. [45]
La transmisión oral puede ocurrir a través de:
Los gatos excretan el patógeno en sus heces durante varias semanas después de contraer la enfermedad, generalmente al comer un huésped intermedio infectado que podría incluir mamíferos (como roedores) o aves. La eliminación de ooquistes suele comenzar a partir del tercer día después de la ingestión de huéspedes intermediarios infectados y puede continuar durante semanas. Los ooquistes no son infecciosos cuando se excretan. Después de aproximadamente un día, el ooquiste sufre un proceso llamado esporulación y se vuelve potencialmente patógeno. [52] Además de los gatos, las aves y los mamíferos, incluido el ser humano, también son huéspedes intermediarios del parásito y participan en el proceso de transmisión. Sin embargo, la patogenicidad varía según la edad y la especie involucrada en la infección y el modo de transmisión de T. gondii . [53]
La toxoplasmosis también puede transmitirse mediante trasplantes de órganos sólidos. Los receptores seronegativos para toxoplasma que reciben órganos de donantes seropositivos para toxoplasma recientemente infectados están en riesgo. Los receptores de órganos que tienen toxoplasmosis latente corren el riesgo de que la enfermedad se reactive en su sistema debido a la inmunosupresión que se produce durante el trasplante de órganos sólidos. [44] Los receptores de trasplantes de células madre hematógenas pueden experimentar un mayor riesgo de infección debido a períodos más prolongados de inmunosupresión. [45]
Los trasplantes de corazón y pulmón presentan el mayor riesgo de infección por toxoplasmosis debido al músculo estriado que forma el corazón, [44] que puede contener quistes, y los riesgos para otros órganos y tejidos varían ampliamente. [54] El riesgo de transmisión se puede reducir examinando a los donantes y receptores antes del procedimiento de trasplante y proporcionando tratamiento. [54]
La toxoplasmosis congénita es una forma específica de toxoplasmosis en la que el feto no nacido se infecta a través de la placenta . [55] La toxoplasmosis congénita se asocia con muerte fetal y aborto espontáneo, y en los bebés, se asocia con hidrocefalia, calcificaciones cerebrales y coriorretinitis , lo que provoca encefalopatía y posiblemente ceguera. [6] Si una mujer recibe su primera exposición a T. gondii durante el embarazo, el feto corre un riesgo particular. [6] Una simple extracción de sangre en la primera visita al médico prenatal puede determinar si una mujer ha tenido exposición previa y, por lo tanto, si está en riesgo o no. Un título de anticuerpos positivo indica exposición e inmunidad previas y garantiza en gran medida la seguridad del feto.
No existe mucha evidencia sobre el efecto de la educación antes del embarazo para prevenir la toxoplasmosis congénita. [56] Sin embargo, se ha sugerido que educar a los padres antes de que nazca el bebé sea eficaz porque puede mejorar la higiene alimentaria, personal y de las mascotas. [56] Se necesita más investigación para determinar si la educación prenatal puede reducir la toxoplasmosis congénita. [56]
Para las mujeres embarazadas con títulos de anticuerpos negativos, que indican que no han estado expuestas previamente a T. gondii , se recomienda realizar pruebas serológicas con una frecuencia mensual, ya que el tratamiento durante el embarazo para aquellas mujeres expuestas a T. gondii por primera vez disminuye drásticamente el riesgo de transmitir el parásito a el feto. Dado que el sistema inmunológico de un bebé no se desarrolla completamente durante el primer año de vida y los quistes resistentes que se forman en todo el cuerpo son muy difíciles de erradicar con antiprotozoos, una infección puede ser muy grave en los niños jóvenes. [ cita necesaria ]
A pesar de estos riesgos, en la mayoría de los países las mujeres embarazadas no se someten sistemáticamente a pruebas de detección de toxoplasmosis, por razones de rentabilidad y el elevado número de falsos positivos que se generan; Portugal , [57] Francia , [58] Austria , [58] Uruguay , [59] e Italia [60] son excepciones notables, y algunos programas regionales de detección funcionan en Alemania , Suiza y Bélgica . [60] Como las pruebas prenatales invasivas conllevan cierto riesgo para el feto (18,5 pérdidas de embarazos por caso de toxoplasmosis evitado), [58] se prefiere la detección postnatal o neonatal . Las excepciones son los casos en los que se observan anomalías fetales y, por lo tanto, se puede orientar la detección. [58]
Las mujeres embarazadas deben evitar manipular carne cruda , beber leche cruda (especialmente leche de cabra) y se les debe recomendar que no coman carne cruda o poco cocida, independientemente del tipo. [61] Debido a la relación obvia entre el Toxoplasma y los gatos, a menudo también se recomienda evitar la exposición a las heces de los gatos y abstenerse de trabajar en el jardín (las heces de los gatos son comunes en la tierra de los jardines) o al menos usar guantes cuando lo haga. [61] La mayoría de los gatos no eliminan ooquistes activamente , ya que se infectan en los primeros seis meses de su vida, cuando eliminan ooquistes durante un corto período de tiempo (1 a 2 semanas). [62] Sin embargo, estos ooquistes quedan enterrados en el suelo, esporulan y permanecen infecciosos durante períodos que van desde varios meses hasta más de un año. [61] Numerosos estudios han demostrado que vivir en una casa con un gato no es un factor de riesgo significativo para la infección por T. gondii , [61] [63] [64] aunque vivir con varios gatitos tiene cierta importancia. [sesenta y cinco]
En 2006, un equipo de investigación checo [66] descubrió que las mujeres con niveles elevados de anticuerpos contra la toxoplasmosis tenían significativamente más probabilidades de dar a luz a niños que a niñas. En la mayoría de las poblaciones, la tasa de natalidad es de alrededor del 51% de niños, pero las personas infectadas con T. gondii tenían hasta un 72% de posibilidades de tener un niño. [67]
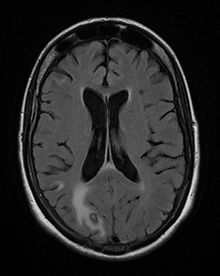
El diagnóstico de toxoplasmosis en humanos se realiza mediante métodos biológicos, serológicos, histológicos o moleculares, o mediante alguna combinación de los anteriores. [62] La toxoplasmosis puede ser difícil de distinguir del linfoma primario del sistema nervioso central . Imita muchas otras enfermedades infecciosas, por lo que los signos clínicos no son específicos y no son lo suficientemente característicos para un diagnóstico definitivo. Como resultado, la posibilidad de un diagnóstico alternativo está respaldada por un ensayo fallido de terapia antimicrobiana ( pirimetamina , sulfadiazina y ácido folínico ( USAN : leucovorina)), es decir, si los fármacos no producen ningún efecto clínico ni mejoría en las imágenes repetidas. [ cita necesaria ]
T. gondii también se puede detectar en la sangre , el líquido amniótico o el líquido cefalorraquídeo mediante la reacción en cadena de la polimerasa . [68] T. gondii puede existir en un huésped como un quiste inactivo que probablemente evadiría la detección. [ cita necesaria ]
Las pruebas serológicas pueden detectar anticuerpos contra T. gondii en el suero sanguíneo, utilizando métodos que incluyen la prueba de colorante de Sabin-Feldman (DT), el ensayo de hemaglutinación indirecta , el ensayo de anticuerpos fluorescentes indirectos (IFA) , la prueba de aglutinación directa , la prueba de aglutinación en látex (LAT). ), el ensayo inmunoabsorbente ligado a enzimas (ELISA) y la prueba de ensayo inmunoabsorbente de aglutinación (IAAT). [62]
Las pruebas más utilizadas para medir el anticuerpo IgG son el DT, el ELISA, el IFA y la prueba de aglutinación directa modificada. [69] Los anticuerpos IgG generalmente aparecen una o dos semanas después de la infección, alcanzan su punto máximo dentro de uno o dos meses y luego disminuyen a distintos ritmos. [69] Los anticuerpos IgG contra toxoplasma generalmente persisten durante toda la vida y, por lo tanto, pueden estar presentes en el torrente sanguíneo como resultado de una infección actual o previa. [70]
Hasta cierto punto, las infecciones agudas por toxoplasmosis se pueden diferenciar de las infecciones crónicas mediante una prueba de avidez de IgG , que es una variación del ELISA. En la primera respuesta a la infección, la IgG específica de toxoplasma tiene una baja afinidad por el antígeno de toxoplasma; en las semanas y meses siguientes, aumenta la afinidad de la IgG por el antígeno. Según la prueba de avidez de IgG, si la IgG del individuo infectado tiene una alta afinidad, significa que la infección comenzó de tres a cinco meses antes de la prueba. Esto es particularmente útil en infecciones congénitas, donde el estado del embarazo y la edad gestacional en el momento de la infección determinan el tratamiento. [71]
A diferencia de la IgG, los anticuerpos IgM se pueden utilizar para detectar una infección aguda, pero generalmente no una infección crónica. [70] Los anticuerpos IgM aparecen antes después de la infección que los anticuerpos IgG y desaparecen más rápido que los anticuerpos IgG después de la recuperación. [62] En la mayoría de los casos, los anticuerpos IgM específicos de T. gondii pueden detectarse por primera vez aproximadamente una semana después de adquirir la infección primaria y disminuir entre uno y seis meses; El 25% de los infectados dan negativo en IgM específica de T. gondii en siete meses. [70] Sin embargo, la IgM puede ser detectable meses o años después de la infección, durante la fase crónica, y es posible que se obtengan falsos positivos de infección aguda. [69] Las pruebas más comúnmente utilizadas para la medición de anticuerpos IgM son el IgM-ELISA de doble sándwich , la prueba IFA y el ensayo de aglutinación inmunoabsorbente (IgM-ISAGA). Los kits de prueba comerciales suelen tener una especificidad baja y los resultados informados con frecuencia se malinterpretan. [69]
En 2021, se evaluaron veinte ensayos comerciales de IgG anti- Toxoplasma en una revisión sistemática , en comparación con un método de referencia aceptado. [72] La mayoría de ellos eran inmunoensayos enzimáticos, seguidos de pruebas de aglutinación, pruebas inmunocromatográficas y un ensayo de transferencia Western . La sensibilidad media de los ensayos de IgG osciló entre el 89,7% y el 100% para títulos estándar y entre el 13,4% y el 99,2% para títulos bajos de IgG. Algunos estudios señalaron la capacidad de algunos métodos, especialmente el WB, para detectar IgG temprano después de la infección primaria. La especificidad de las pruebas de IgG fue generalmente alta, oscilando entre 91,3% y 100%; y superior al 99% para la mayoría de los ensayos EIA. El valor predictivo positivo (VPP) no fue un indicador discriminante entre los métodos, mientras que se informaron disparidades significativas (87,5-100%) entre los valores predictivos negativos (VPN), un parámetro clave que evalúa la capacidad de descartar definitivamente una infección por Toxoplasma en pacientes. en riesgo de contraer infecciones oportunistas. [72]

Las recomendaciones para el diagnóstico de toxoplasmosis congénita incluyen: diagnóstico prenatal basado en pruebas de líquido amniótico y exámenes de ultrasonido ; diagnóstico neonatal basado en pruebas moleculares de la placenta y la sangre del cordón umbilical y pruebas serológicas comparativas entre madre e hijo y un examen clínico al nacer; y diagnóstico en la primera infancia basado en exámenes neurológicos y oftalmológicos y una encuesta serológica durante el primer año de vida. [55] Durante el embarazo, se recomiendan pruebas serológicas a intervalos de tres semanas. [73]
Aunque el diagnóstico de toxoplasmosis depende en gran medida de la detección serológica de inmunoglobulina anti- Toxoplasma específica , las pruebas serológicas tienen limitaciones. Por ejemplo, es posible que no detecte la fase activa de la infección por T. gondii porque es posible que las IgG o IgM anti- Toxoplasma específicas no se produzcan hasta después de varias semanas de infección. Como resultado, una mujer embarazada podría dar negativo durante la fase activa de la infección por T. gondii, lo que provocaría una toxoplasmosis congénita no detectada y, por tanto, no tratada. [74] Además, es posible que la prueba no detecte infecciones por T. gondii en pacientes inmunocomprometidos porque los títulos de IgG o IgM anti- Toxoplasma específicos pueden no aumentar en este tipo de pacientes. [ cita necesaria ]
Se han desarrollado muchas técnicas basadas en PCR para diagnosticar la toxoplasmosis utilizando muestras clínicas que incluyen líquido amniótico, sangre , líquido cefalorraquídeo y biopsia de tejido . La técnica basada en PCR más sensible es la PCR anidada , seguida de la hibridación de productos de PCR. [74] La principal desventaja de estas técnicas es que requieren mucho tiempo y no proporcionan datos cuantitativos. [74]
La PCR en tiempo real es útil en la detección de patógenos, la expresión y regulación de genes y la discriminación alélica. Esta técnica de PCR utiliza la actividad nucleasa 5' de la ADN polimerasa Taq para escindir una sonda de hibridación marcada con fluorescencia no extensible durante la fase de extensión de la PCR. [74] Un segundo tinte fluorescente, por ejemplo, 6-carboxitetrametil-rodamina, apaga la fluorescencia de la sonda intacta. [74] La escisión de la nucleasa de la sonda de hibridación durante la PCR libera el efecto de extinción, lo que da como resultado un aumento de la fluorescencia proporcional a la cantidad de producto de la PCR, que puede controlarse mediante un detector de secuencia. [74]
Los ganglios linfáticos afectados por Toxoplasma tienen cambios característicos, que incluyen centros germinales reactivos mal delimitados , grupos de células B monocitoides e histiocitos epitelioides dispersos . [ cita necesaria ]
La tríada clásica de toxoplasmosis congénita incluye: coriorretinitis , hidrocefalia y arteriosclerosis intracraneal . [75] Otras consecuencias incluyen sordera neurosensorial, convulsiones y discapacidad intelectual. [76]
La toxoplasmosis congénita también puede afectar la audición de un niño. Hasta el 30% de los recién nacidos presentan algún grado de pérdida auditiva neurosensorial. [77] Las habilidades de comunicación del niño también pueden verse afectadas. Un estudio publicado en 2010 examinó a 106 pacientes, todos los cuales recibieron tratamiento contra la toxoplasmosis antes de 2,5 meses. De este grupo, el 26,4% presentó trastornos del lenguaje. [78]
El tratamiento se recomienda para personas con problemas de salud graves, como personas con VIH cuyos recuentos de CD4 son inferiores a 200 células/mm 3 . Trimetoprima/sulfametoxazol es el fármaco de elección para prevenir la toxoplasmosis, pero no para tratar la enfermedad activa. Un estudio de 2012 muestra una nueva y prometedora forma de tratar la forma activa y latente de esta enfermedad utilizando dos quinolonas similares a las endoquinas . [79]
Los medicamentos recetados para la toxoplasmosis aguda son los siguientes: [ cita necesaria ]
(Otros antibióticos, como la minociclina , han tenido algún uso como terapia de rescate ).
Si se infecta durante el embarazo, se recomienda espiramicina en el primer y principios del segundo trimestre, mientras que pirimetamina/sulfadiazina y leucovorina se recomiendan al final del segundo y tercer trimestre. [81]
En personas con toxoplasmosis latente, los quistes son inmunes a estos tratamientos, ya que los antibióticos no llegan a los bradizoítos en concentración suficiente.
Los medicamentos recetados para la toxoplasmosis latente son:
Cuando a una mujer embarazada se le diagnostica toxoplasmosis aguda, se puede utilizar la amniocentesis para determinar si el feto ha sido infectado o no. Cuando una mujer embarazada desarrolla toxoplasmosis aguda, los taquizoitos tienen aproximadamente un 30% de posibilidades de ingresar al tejido placentario y desde allí ingresar e infectar al feto. A medida que aumenta la edad gestacional en el momento de la infección, también aumenta la posibilidad de infección fetal. [32]
Si el parásito aún no ha llegado al feto, la espiramicina puede ayudar a prevenir la transmisión placentaria. Si el feto ha sido infectado, la gestante puede ser tratada con pirimetamina y sulfadiazina , con ácido folínico , después del primer trimestre. Se tratan después del primer trimestre porque la pirimetamina tiene un efecto antifolato y la falta de ácido fólico puede interferir con la formación del cerebro fetal y causar trombocitopenia . [84] La infección en etapas gestacionales más tempranas se correlaciona con peores resultados fetales y neonatales, particularmente cuando la infección no se trata. [85]
Los recién nacidos que se someten a 12 meses de tratamiento posnatal contra la toxoplasmosis tienen pocas posibilidades de sufrir pérdida auditiva neurosensorial. [86] Para este grupo se ha creado información sobre los hitos del tratamiento para niños con toxoplasmosis congénita. [87]
Las infecciones por T. gondii ocurren en todo el mundo, aunque las tasas de infección difieren significativamente según el país. [26] Para las mujeres en edad fértil, una encuesta de 99 estudios realizados en 44 países encontró que las áreas de mayor prevalencia se encuentran en América Latina (alrededor del 50-80%), partes de Europa central y oriental (alrededor del 20-60%), Medio Oriente (alrededor del 30 al 50 %), partes del sudeste asiático (alrededor del 20 al 60 %) y partes de África (alrededor del 20 al 55 %). [26]
En los Estados Unidos, los datos de la Encuesta Nacional de Examen de Salud y Nutrición (NHANES) de 1999 a 2004 encontraron que el 9,0% de las personas nacidas en los EE.UU. entre 12 y 49 años eran seropositivas para anticuerpos IgG contra T. gondii , frente al 14,1% registrado medido en el NHANES 1988-1994. [88] En la encuesta de 1999-2004, el 7,7% de las mujeres nacidas en los EE. UU. y el 28,1% de las nacidas en el extranjero de entre 15 y 44 años eran seropositivas para T. gondii . [88] Numerosos estudios han observado una tendencia a la disminución de la seroprevalencia en los Estados Unidos y muchos países europeos. [26] Toxoplasma gondii se considera la segunda causa principal de muertes relacionadas con alimentos y la cuarta causa principal de hospitalizaciones relacionadas con alimentos en los Estados Unidos. [89]
El protista responsable de la toxoplasmosis es T. gondii . Hay tres tipos principales de T. gondii responsables de los patrones de toxoplasmosis en todo el mundo. Hay tipos I, II y III. Estos tres tipos de T. gondii tienen efectos diferentes en ciertos huéspedes, principalmente ratones y humanos, debido a su variación en los genotipos. [90]
Las técnicas actuales de serotipificación sólo pueden separar los parásitos de tipo I o III de los de tipo II. [91]
Debido a que el parásito representa una amenaza particular para los fetos cuando se contrae durante el embarazo, [92] gran parte de los datos epidemiológicos globales sobre T. gondii provienen de pruebas de seropositividad en mujeres en edad fértil. Las pruebas de seropositividad buscan la presencia de anticuerpos contra T. gondii en la sangre, por lo que, si bien la seropositividad garantiza que uno ha estado expuesto al parásito, no necesariamente garantiza que uno esté infectado crónicamente. [93]
Toxoplasma gondii fue descrito por primera vez en 1908 por Nicolle y Manceaux en Túnez, e independientemente por Splendore en Brasil. [11] Splendore informó del protozoo en un conejo, mientras que Nicolle y Manceaux lo identificaron en un roedor del norte de África, el gundi ( Ctenodactylus gundi ). [42] En 1909 Nicolle y Manceaux diferenciaron el protozoo de Leishmania . [11] Nicolle y Manceaux luego lo llamaron Toxoplasma gondii por la forma curva de su etapa infecciosa (raíz griega toxon = arco). [11]
El primer caso registrado de toxoplasmosis congénita fue en 1923, pero no se identificó como causada por T. gondii . [42] Janků (1923) describió en detalle los resultados de la autopsia de un niño de 11 meses que había acudido al hospital con hidrocefalia . El niño tenía las marcas clásicas de toxoplasmosis, incluida coriorretinitis (inflamación de la coroides y la retina del ojo). [42] La histología reveló una serie de "esporocitos", aunque Janků no los identificó como T. gondii . [42]
No fue hasta 1937 que se realizó el primer análisis científico detallado de T. gondii utilizando técnicas previamente desarrolladas para analizar virus. [11] En 1937, Sabin y Olitsky analizaron T. gondii en monos y ratones de laboratorio. Sabin y Olitsky demostraron que T. gondii era un parásito intracelular obligado y que los ratones alimentados con tejido contaminado con T. gondii también contraían la infección. [11] Así, Sabin y Olitsky demostraron que T. gondii es un patógeno transmisible entre animales. [ cita necesaria ]
T. gondii se describió por primera vez como patógeno humano en 1939 en el Babies Hospital de la ciudad de Nueva York . [11] [94] Wolf, Cowen y Paige identificaron la infección por T. gondii en una niña nacida a término mediante cesárea . [42] El bebé desarrolló convulsiones y tuvo coriorretinitis en ambos ojos a los tres días. Luego, el bebé desarrolló encefalomielitis y murió al mes de edad. Wolf, Cowen y Paige aislaron T. gondii de lesiones del tejido cerebral. La inyección intracraneal de muestras de cerebro y médula espinal en ratones, conejos y ratas produjo encefalitis en los animales. [11] Wolf, Cowen y Page revisaron casos adicionales y concluyeron que T. gondii producía síntomas reconocibles y podía transmitirse de madre a hijo. [42]
El primer caso de toxoplasmosis en adultos se informó en 1940 sin signos neurológicos. Pinkerton y Weinman informaron la presencia de Toxoplasma en un hombre de 22 años de Perú que murió a causa de una infección bacteriana y fiebre posteriores. [42]
En 1948, Sabin y Feldman crearon una prueba de colorante serológica basada en la capacidad de los anticuerpos del paciente para alterar la tinción de Toxoplasma . [11] [95] La prueba de colorante Sabin Feldman es ahora el estándar de oro para identificar la infección por Toxoplasma . [11]
Desmonts et al. demostraron la transmisión de Toxoplasma al comer carne cruda o poco cocida. en 1965 París. [11] Desmonts observó que el consumo terapéutico de carne cruda de res o de caballo en un hospital de tuberculosis se asoció con un aumento del 50% anual en los anticuerpos contra Toxoplasma . [11] Esto significa que se transmitía más T. gondii a través de la carne cruda.
En 1974, Desmonts y Couvreur demostraron que la infección durante los dos primeros trimestres produce el mayor daño al feto, que la transmisión dependía de cuándo las madres estaban infectadas durante el embarazo, que las madres con anticuerpos antes del embarazo no transmitían la infección al feto y que la espiramicina Disminuyó la transmisión al feto. [42]
El toxoplasma ganó más atención en la década de 1970 con el aumento del tratamiento inmunosupresor administrado después de trasplantes de órganos o de médula ósea y la epidemia de SIDA de la década de 1980. [11] Los pacientes con una función del sistema inmunológico debilitada son mucho más susceptibles a las enfermedades.
El "síndrome de la dama loca de los gatos" es un término acuñado por organizaciones de noticias para describir hallazgos científicos que vinculan el parásito Toxoplasma gondii con varios trastornos mentales y problemas de conducta. [96] [97] La sospecha de correlación entre tener un gato en la infancia y el desarrollo posterior de la esquizofrenia sugirió que se necesitaban más estudios para determinar un factor de riesgo para los niños; [98] sin embargo, estudios posteriores demostraron que T. gondii no era un factor causal en psicosis posteriores. [99] Los investigadores también descubrieron que tener un gato no aumenta considerablemente el riesgo de infección por T. gondii en mujeres embarazadas. [61] [100]
El término síndrome de la dama loca de los gatos se basa tanto en estereotipos como en referencias culturales populares. Se originó cuando se observaron casos de las aflicciones antes mencionadas entre la población. Una dama gato es un estereotipo cultural de una mujer que atesora y adora compulsivamente a los gatos. El biólogo Jaroslav Flegr defiende la teoría de que la toxoplasmosis afecta el comportamiento humano. [101] [102]


Aunque T. gondii tiene la capacidad de infectar prácticamente a todos los animales de sangre caliente, la susceptibilidad y las tasas de infección varían ampliamente entre los diferentes géneros y especies . [112] [113] Las tasas de infección en poblaciones de la misma especie también pueden variar ampliamente debido a diferencias en la ubicación, la dieta y otros factores. [ cita necesaria ]
Aunque se ha observado infección por T. gondii en varias especies de primates asiáticos, se encontró por primera vez seroprevalencia de anticuerpos contra T. gondii en macacos toque ( Macaca sinica ), endémicos de la isla de Sri Lanka. [114]
Los marsupiales australianos son particularmente susceptibles a la toxoplasmosis. [115] Wallabies , koalas , wombats , pademelones y pequeños dasyuridos pueden morir, y los bandicoots barrados orientales generalmente mueren dentro de aproximadamente 3 semanas después de la infección. [116]
Se estima que el 23% de los cerdos salvajes en todo el mundo son seropositivos para T. gondii . [117] La seroprevalencia varía en todo el mundo, con la seroprevalencia más alta en América del Norte (32%) y Europa (26%) y la más baja en Asia (13%) y América del Sur (5%). [117] Las regiones geográficas ubicadas en latitudes más altas y las regiones que experimentan climas más cálidos y húmedos se asocian con una mayor seroprevalencia de T. gondii entre los jabalíes. [117] Los jabalíes infectados con T. gondii representan un riesgo potencial para la salud de los humanos que consumen su carne. [117]
Entre el ganado , los cerdos, [118] [119] [120] las ovejas [121] y las cabras tienen las tasas más altas de infección crónica por T. gondii . [122] La prevalencia de T. gondii en animales productores de carne varía ampliamente tanto dentro como entre países, [122] y se ha demostrado que las tasas de infección están dramáticamente influenciadas por las diferentes prácticas agrícolas y de manejo. [14] Por ejemplo, los animales mantenidos al aire libre o en ambientes libres tienen mayor riesgo de infección que los animales criados en interiores o en operaciones de confinamiento comercial . [14] [47]
En todo el mundo, se ha medido que el porcentaje de cerdos que albergan parásitos viables es del 3% al 71,43% [120] y en los Estados Unidos (mediante bioensayos en ratones o gatos) llega al 92,7% y al 0%, dependiendo de la granja o el rebaño. [47] Las encuestas de seroprevalencia ( anticuerpos contra T. gondii en la sangre) son más comunes y dichas mediciones son indicativas de la alta seroprevalencia relativa en cerdos en todo el mundo. [123] Se ha descubierto que los lechones neonatales experimentan todo el rango de gravedad, incluida la progresión a la muerte fetal . [124] [118] : 95 Esto quedó especialmente demostrado en el estudio fundacional de Thiptara et al. 2006, informó el nacimiento de una camada de tres nacidos muertos y seis viven en Tailandia. Esta observación ha sido relevante no sólo para ese país sino también para el control de la toxoplasmosis en la porcicultura en todo el mundo. [125] [118] : 95 [120]
Junto con los cerdos, las ovejas y las cabras se encuentran entre el ganado infectado con mayor frecuencia y de importancia epidemiológica para la infección humana. [122] Se ha medido (mediante bioensayo) que la prevalencia de T. gondii viable en tejido de oveja llega al 78% en los Estados Unidos, [126] y una encuesta de 2011 de cabras destinadas al consumo en los Estados Unidos encontró una seroprevalencia del 53,4%. [127]
Debido a la falta de exposición al aire libre, los pollos criados en operaciones de confinamiento en interiores a gran escala no suelen infectarse con T. gondii . [14] Los pollos criados en libertad o criados en patios traseros se infectan con mucha más frecuencia. [14] Una encuesta de pollos criados en libertad en los Estados Unidos encontró que su prevalencia era del 17% al 100%, dependiendo de la granja. [128] Debido a que la carne de pollo generalmente se cocina bien antes de su consumo, las aves de corral generalmente no se consideran un factor de riesgo significativo para la infección humana por T. gondii . [129]
Aunque el ganado vacuno y los búfalos pueden infectarse con T. gondii , el parásito generalmente se elimina o se reduce a niveles indetectables unas pocas semanas después de la exposición. [14] Los quistes tisulares rara vez están presentes en la carne de búfalo o de res, y se considera que la carne de estos animales tiene bajo riesgo de albergar parásitos viables. [47] [122] [130]
Los caballos se consideran resistentes a la infección crónica por T. gondii . [14] Sin embargo, se han aislado células viables de caballos estadounidenses sacrificados para la exportación, y la toxoplasmosis humana grave en Francia se ha relacionado epidemiológicamente con el consumo de carne de caballo . [47] [131]
En 1942, se diagnosticó y notificó el primer caso de toxoplasmosis felina en un gato doméstico en Middletown, Nueva York. [132] Los investigadores aislaron ooquistes de heces felinas y descubrieron que podían ser infecciosos hasta por 12 meses en el medio ambiente. [133]
Se ha estimado que la seroprevalencia de T. gondii en gatos domésticos a nivel mundial es de alrededor del 30% al 40% [134] y presenta una variación geográfica significativa. En Estados Unidos no se ha hecho ninguna estimación nacional oficial, pero las encuestas locales han mostrado niveles que varían entre el 16% y el 80%. [134] Una encuesta de 2012 de 445 gatos domésticos de pura raza y 45 gatos de refugio en Finlandia encontró una seroprevalencia general del 48,4%, [135] mientras que una encuesta de 2010 de gatos salvajes de Giza, Egipto, encontró una tasa de seroprevalencia del 97,4%. [136] Otra encuesta realizada en Colombia registró una seroprevalencia del 89,3%, [137] mientras que un estudio chino ( Guangdong ) encontró sólo una prevalencia del 2,1%. [138]
Las tasas de infección por T. gondii en gatos domésticos varían ampliamente según la dieta y el estilo de vida de los gatos. [139] Los gatos salvajes que cazan para alimentarse tienen más probabilidades de infectarse que los gatos domésticos y, naturalmente, también depende de la prevalencia de presas infectadas con T. gondii , como aves y pequeños mamíferos . [140]
La mayoría de los gatos infectados expulsarán ooquistes sólo una vez en su vida, durante un período de aproximadamente una a dos semanas. [134] Este desprendimiento puede liberar millones de ooquistes, cada uno de ellos capaz de propagarse y sobrevivir durante meses. [134] Se estima que el 1% de los gatos en un momento dado están eliminando activamente ooquistes. [14]
Es difícil controlar la población de gatos con ooquistes infectados debido a la falta de una vacuna eficaz. Esto sigue siendo un desafío en la mayoría de los casos y la eficacia de los programas que están disponibles es cuestionable. [141]
Se ha demostrado que la infección con T. gondii altera el comportamiento de ratones y ratas de manera que se cree que aumenta las posibilidades de que los roedores sean presa de los gatos. [142] [143] [144] Los roedores infectados muestran una reducción en su aversión innata a los olores de los gatos; Si bien los ratones y ratas no infectados generalmente evitan las áreas marcadas con orina de gato o con olor corporal de gato, esta evitación se reduce o elimina en los animales infectados. [142] [144] [145] Además, algunas pruebas sugieren que esta pérdida de aversión puede ser específica de los olores felinos: cuando se les da a elegir entre dos olores de depredador (gato o visón ), los roedores infectados muestran una preferencia significativamente mayor por los olores de gato que hacer controles de no infectados . [146] [147]
En roedores, los cambios de comportamiento inducidos por T. gondii ocurren a través de la remodelación epigenética en las neuronas asociadas con los comportamientos observados; [148] [149] por ejemplo, modifica la metilación epigenética para inducir la hipometilación de genes relacionados con la arginina vasopresina en la amígdala medial para disminuir en gran medida la aversión a los depredadores. [148] [149] También se han observado cambios de comportamiento similares inducidos epigenéticamente en modelos de adicción en ratones, donde los cambios en la expresión de enzimas modificadoras de histonas mediante la desactivación de genes o la inhibición de enzimas en neuronas específicas produjeron alteraciones en los comportamientos relacionados con las drogas. [150] [151] [152] La acetilación generalizada de histonas-lisina en astrocitos corticales parece ser otro mecanismo epigenético empleado por T. gondii . [153] [154]
Los roedores infectados con T. gondii muestran una serie de cambios de comportamiento más allá de las respuestas alteradas a los olores de los gatos. Las ratas infectadas con el parásito muestran mayores niveles de actividad y una disminución del comportamiento neofóbico . [155] De manera similar, los ratones infectados muestran alteraciones en los patrones de locomoción y comportamiento exploratorio durante las pruebas experimentales. Estos patrones incluyen viajar distancias mayores, moverse a velocidades más altas, acelerar durante períodos de tiempo más largos y mostrar un tiempo de pausa reducido cuando se los coloca en nuevas arenas. [156] También se ha demostrado que los roedores infectados tienen menor ansiedad , utilizando modelos tradicionales como laberintos elevados , arenas de campo abierto y pruebas de interacción social. [156] [157]
Un estudio de la Universidad de California en Davis sobre nutrias marinas muertas recolectadas entre 1998 y 2004 encontró que la toxoplasmosis fue la causa de la muerte del 13% de los animales. [158] La proximidad a las salidas de agua dulce al océano fue un factor de riesgo importante. Se considera que la fuente final más probable es la ingestión de ooquistes de heces de gato. [159] La escorrentía superficial que contiene heces de gatos salvajes y arena de gatos domésticos arrojadas a los inodoros son posibles fuentes de ooquistes. [160] [161] Estas mismas fuentes también pueden haber introducido la infección por toxoplasmosis en la foca monje hawaiana en peligro de extinción . [162] La infección por el parásito ha contribuido a la muerte de al menos cuatro focas monje hawaianas. [162] La infección de una foca monje hawaiana con T. gondii se observó por primera vez en 2004. [163] La propagación del parásito amenaza la recuperación de este pinnípedo en grave peligro de extinción. Los parásitos se han encontrado en delfines y ballenas. [164] [165] Los investigadores Black y Massie creen que las anchoas, que viajan desde los estuarios hacia el océano abierto, pueden estar ayudando a propagar la enfermedad. [166]
Se ha informado que Toxoplasma gondii es la causa de la muerte de un panda gigante mantenido en un zoológico en China, que murió en 2014 de gastroenteritis aguda y una enfermedad respiratoria . [111] Aunque parezca anecdótico , este informe enfatiza que todas las especies de sangre caliente probablemente estén infectadas por T. gondii , incluidas las especies en peligro de extinción como el panda gigante. [ cita necesaria ]

La infección crónica por T. gondii se ha considerado tradicionalmente asintomática en personas con función inmune normal. [167] Alguna evidencia sugiere que la infección latente puede influir sutilmente en una variedad de comportamientos y tendencias humanas, y la infección puede alterar la susceptibilidad o la intensidad de una serie de trastornos psiquiátricos o neurológicos. [168] [167]
En la mayoría de los estudios actuales en los que se han encontrado correlaciones positivas entre los títulos de anticuerpos contra T. gondii y ciertos rasgos de comportamiento o trastornos neurológicos, las pruebas de seropositividad para T. gondii se realizan después de la aparición de la enfermedad o rasgo de comportamiento examinado; es decir, a menudo no está claro si la infección por el parásito aumenta las posibilidades de tener un determinado rasgo o trastorno, o si tener un determinado rasgo o trastorno aumenta las posibilidades de infectarse con el parásito. [169] Grupos de individuos con ciertos rasgos de comportamiento o trastornos neurológicos pueden compartir ciertas tendencias de comportamiento que aumentan la probabilidad de exposición e infección por T. gondii ; como resultado, es difícil confirmar relaciones causales entre las infecciones por T. gondii y los trastornos neurológicos o rasgos de comportamiento asociados. [169]
Alguna evidencia vincula a T. gondii con la esquizofrenia . [167] Dos metanálisis de 2012 encontraron que las tasas de anticuerpos contra T. gondii en personas con esquizofrenia eran 2,7 veces más altas que en los controles. [170] [171] Por lo tanto, la positividad de anticuerpos contra T. gondii se consideró un factor de riesgo intermedio en relación con otros factores de riesgo conocidos. [170] Las precauciones señaladas incluyen que las pruebas de anticuerpos no detectan la toxoplasmosis directamente, la mayoría de las personas con esquizofrenia no tienen anticuerpos contra la toxoplasmosis y podría existir un sesgo de publicación . [171] Si bien la mayoría de estos estudios evaluaron a personas ya diagnosticadas con esquizofrenia en busca de anticuerpos contra T. gondii , se han encontrado asociaciones entre T. gondii y la esquizofrenia antes de la aparición de los síntomas de la esquizofrenia. [142] Las diferencias de sexo en la edad de inicio de la esquizofrenia pueden explicarse en parte por un segundo pico de incidencia de infección por T. gondii entre los 25 y 30 años solo en mujeres. [172] Aunque no está claro el mecanismo que respalda la asociación entre la esquizofrenia y la infección por T. gondii , los estudios han investigado la base molecular de esta correlación. [172] Los fármacos antipsicóticos utilizados en la esquizofrenia parecen inhibir la replicación de los taquizoitos de T. gondii en cultivos celulares. [142] Suponiendo que existe un vínculo causal entre T. gondii y la esquizofrenia, los estudios aún tienen que determinar por qué sólo algunos individuos con toxoplasmosis latente desarrollan esquizofrenia; algunas explicaciones plausibles incluyen diferentes susceptibilidades genéticas, diferencias en las cepas del parásito y diferencias en la ruta de la infección adquirida por T. gondii . [173]
También se han encontrado correlaciones entre los títulos de anticuerpos contra T. gondii y el TOC , así como el suicidio entre personas con trastornos del estado de ánimo, incluido el trastorno bipolar . [168] [174] Los títulos positivos de anticuerpos contra T. gondii parecen no estar correlacionados con la depresión mayor o la distimia . [175] Aunque existe una correlación entre T. gondii y muchos trastornos psicológicos, el mecanismo subyacente no está claro. Un estudio de 2016 de 236 personas con niveles altos de anticuerpos contra la toxoplasmosis encontró que "había poca evidencia de que T. gondii estuviera relacionado con un mayor riesgo de trastorno psiquiátrico, control deficiente de los impulsos, aberraciones de la personalidad o deterioro neurocognitivo". [176]
La infección latente se ha relacionado con la enfermedad de Parkinson y la enfermedad de Alzheimer . [168]
Las personas con esclerosis múltiple muestran tasas de infección alrededor de un 15% más bajas que el público en general. [177]
La infección latente por T. gondii en humanos se ha asociado con un mayor riesgo de accidentes automovilísticos , [178] potencialmente debido a un deterioro del rendimiento psicomotor o a perfiles de personalidad más arriesgados. [168]
Se ha informado que el cambio climático afecta la aparición, supervivencia, distribución y transmisión de T. gondii . [179] T. gondii ha sido identificado en el ártico canadiense, un lugar que alguna vez fue demasiado frío para su supervivencia. [180] Las temperaturas más altas aumentan el tiempo de supervivencia de T. gondii . [179] Un mayor deshielo y precipitaciones pueden aumentar la cantidad de ooquistes de T. gondii que se transportan a través del flujo del río. [179] Los cambios en las poblaciones de aves, roedores e insectos y los patrones de migración pueden afectar la distribución de T. gondii debido a su papel como reservorio y vector. [179] También se sugiere que la urbanización y la degradación ambiental natural afectan la transmisión de T. gondii y aumentan el riesgo de infección. [179]
La toxoplasmosis se está convirtiendo en un peligro para la salud mundial, ya que infecta entre el 30% y el 50% de la población humana mundial.
La evidencia acumulada sugiere que la infección latente por Toxoplasma gondii está asociada con una variedad de afecciones neuropsiquiátricas y conductuales.
La seroprevalencia de T. gondii en humanos varía entre el 10 y el 70% en todo el mundo, según la región y aumenta significativamente con la edad. Tras la infección, los parásitos persisten como quistes intraneuronales en el sistema nervioso central (SNC) durante toda la vida del huésped (1, Figura 1). Hasta hace poco, la persistencia del parásito en individuos sanos se consideraba clínicamente asintomática. Sin embargo, en la última década, varios informes han indicado que la toxoplasmosis cerebral crónica puede afectar el comportamiento de su huésped (2).
El patógeno zoonótico
Toxoplasma gondii
infecta a más del 30% de la población humana. El parásito intracelular puede persistir durante toda la vida en el SNC dentro de las neuronas, modificando su función y estructura, lo que lleva a cambios de comportamiento específicos del huésped. ... Además, investigaciones en población humana han correlacionado la seropositividad
a Toxoplasma
con cambios en las funciones neurológicas; sin embargo, los complejos mecanismos subyacentes de la sutil alteración del comportamiento aún no se comprenden completamente. Los parásitos son capaces de inducir modificaciones directas en las células infectadas, por ejemplo alterando el metabolismo de la dopamina, silenciando funcionalmente las neuronas e impidiendo la apoptosis.
Nueve de once estudios que utilizaron el cuestionario de autoinforme del factor de personalidad 16 de Cattell encontraron resultados significativos y consistentes para ambos sexos. Los hombres seropositivos en general tenían menos respeto por las reglas y mayor vigilancia (sospechosos, celosos, rígidos/inflexibles) que los hombres seronegativos. Por el contrario, las mujeres seropositivas tenían mayor respeto por las reglas y mayor calidez que las mujeres seronegativas. Ambos sexos seropositivos estaban más ansiosos que los sujetos sanos de comparación. ... Se completaron observaciones de comportamiento y entrevistas para determinar si las diferencias de género encontradas en las medidas de autoinforme se replicaban mediante medidas objetivas. Los hombres seropositivos obtuvieron puntuaciones significativamente más bajas que los hombres seronegativos en autocontrol, orden de la ropa y relaciones. Las diferencias fueron menos impresionantes para las mujeres seropositivas, con solo tendencias hacia puntuaciones más altas en autocontrol y orden de la ropa en comparación con las mujeres seronegativas. Los autores ven los resultados del estudio como una confirmación objetiva de que la presencia
de T. gondii
puede cambiar el comportamiento de un huésped humano.
Las modificaciones epigenéticas causadas por drogas adictivas juegan un papel importante en la plasticidad neuronal y en las respuestas conductuales inducidas por drogas. Aunque pocos estudios han investigado los efectos de AMPH en la regulación genética (Tabla 1), los datos actuales sugieren que AMPH actúa en múltiples niveles para alterar la interacción histona/ADN y reclutar factores de transcripción que en última instancia causan la represión de algunos genes y la activación de otros genes. Es importante destacar que algunos estudios también han correlacionado la regulación epigenética inducida por AMPH con los resultados conductuales causados por este fármaco, lo que sugiere, por lo tanto, que la remodelación epigenética subyace a los cambios de comportamiento inducidos por AMPH. Si esto resulta ser cierto, el uso de medicamentos específicos que inhiban la acetilación, metilación o metilación del ADN de histonas podría ser una alternativa terapéutica importante para prevenir y/o revertir la adicción al AMPH y mitigar los efectos secundarios que genera el AMPH cuando se usa para tratar el TDAH.
Los aumentos a corto plazo en la acetilación de histonas generalmente promueven respuestas conductuales a las drogas, mientras que los aumentos sostenidos se oponen a los efectos de la cocaína, según las acciones de la administración sistémica o intra-NAc de inhibidores de HDAC. ... El bloqueo genético o farmacológico de G9a en la NAc potencia las respuestas conductuales a la cocaína y los opiáceos, mientras que el aumento de la función de G9a ejerce el efecto contrario (Maze et al., 2010; Sun et al., 2012a). Esta regulación negativa de G9a y H3K9me2 inducida por fármacos también sensibiliza a los animales a los efectos nocivos del estrés crónico posterior (Covington et al., 2011). La regulación negativa de G9a aumenta la arborización dendrítica de las neuronas NAc y se asocia con una mayor expresión de numerosas proteínas implicadas en la función sináptica, que conecta directamente G9a/H3K9me2 alterado en la plasticidad sináptica asociada con la adicción (Maze et al., 2010).
"G9a parece ser un punto de control crítico para la regulación epigenética en NAc, como sabemos, funciona en dos circuitos de retroalimentación negativa. Se opone a la inducción de ΔFosB, un factor de transcripción duradero importante para la adicción a las drogas (Robison y Nestler, 2011) , mientras que ΔFosB a su vez suprime la expresión de G9a (Maze et al., 2010; Sun et al., 2012a... Además, G9a se induce en NAc tras una inhibición prolongada de HDAC, lo que explica la atenuación paradójica de los efectos conductuales de la cocaína que se observan en). Estas condiciones, como se señaló anteriormente (Kennedy et al., 2013). Los genes de la subunidad del receptor GABAA se encuentran entre los que están controlados por este circuito de retroalimentación. Por lo tanto, la cocaína crónica o la inhibición prolongada de HDAC induce varias subunidades del receptor GABAA en NAc. asociado con una mayor frecuencia de corrientes postsinápticas inhibidoras (IPSC). En sorprendente contraste, la exposición combinada a la cocaína y la inhibición de HDAC, que desencadena la inducción de G9a y un aumento de los niveles globales de H3K9me2, conduce al bloqueo del receptor GABAA y la regulación de IPSC.