El benceno es un compuesto químico orgánico con la fórmula molecular C 6 H 6 . La molécula de benceno está compuesta por seis átomos de carbono unidos en un anillo hexagonal plano con un átomo de hidrógeno unido a cada uno. Debido a que sólo contiene átomos de carbono e hidrógeno, el benceno se clasifica como un hidrocarburo .
El benceno es un componente natural del petróleo y es uno de los petroquímicos elementales . Debido a los enlaces pi cíclicos continuos entre los átomos de carbono, el benceno se clasifica como un hidrocarburo aromático . El benceno es un líquido incoloro y altamente inflamable con un olor dulce, y es parcialmente responsable del aroma de la gasolina . Se utiliza principalmente como precursor para la fabricación de sustancias químicas con estructuras más complejas, como el etilbenceno y el cumeno , de los cuales se producen miles de millones de kilogramos anualmente. Aunque el benceno es una sustancia química industrial importante , tiene un uso limitado en artículos de consumo debido a su toxicidad. El benceno es un compuesto orgánico volátil . [15]
El benceno está clasificado como carcinógeno . Organizaciones de noticias como The New York Times han informado sobre sus efectos particulares en la salud humana , como los resultados a largo plazo de la exposición accidental . Por ejemplo, un artículo de 2022 afirmó que la contaminación por benceno en el área metropolitana de Boston causó condiciones peligrosas en varios lugares, y la publicación señaló que el compuesto podría eventualmente causar leucemia en algunas personas. [dieciséis]
La palabra " benceno " deriva de " goma de benjuí " ( resina de benjuí ), una resina aromática conocida desde la antigüedad en el sudeste asiático, y más tarde por los farmacéuticos y perfumistas europeos en el siglo XVI a través de las rutas comerciales. [17] Un material ácido se derivó del benjuí por sublimación y se denominó "flores de benjuí" o ácido benzoico. El hidrocarburo derivado del ácido benzoico adquirió así el nombre de bencina, benzol o benceno. [18] Michael Faraday aisló e identificó por primera vez el benceno en 1825 a partir del residuo oleoso derivado de la producción de gas de iluminación, dándole el nombre de bicarbureto de hidrógeno . [19] [20] En 1833, Eilhard Mitscherlich lo produjo destilando ácido benzoico (de la goma de benjuí ) y cal . Le dio al compuesto el nombre de bencina . [21] En 1836, el químico francés Auguste Laurent llamó a la sustancia "phène"; [22] esta palabra se ha convertido en la raíz de la palabra inglesa " fenol ", que es benceno hidroxilado , y " fenilo ", el radical formado por abstracción de un átomo de hidrógeno del benceno.
En 1845, Charles Blachford Mansfield , trabajando bajo la dirección de August Wilhelm von Hofmann , aisló benceno del alquitrán de hulla . [23] Cuatro años más tarde, Mansfield inició la primera producción de benceno a escala industrial, basada en el método del alquitrán de hulla. [24] [25] Poco a poco, se desarrolló entre los químicos la sensación de que varias sustancias estaban químicamente relacionadas con el benceno, lo que comprendía una familia química diversa. En 1855, Hofmann fue el primero en aplicar la palabra " aromática " para designar esta relación familiar, en honor a una propiedad característica de muchos de sus miembros. [26] En 1997, se detectó benceno en el espacio profundo . [27]
La fórmula empírica del benceno se conocía desde hacía mucho tiempo, pero determinar su estructura altamente poliinsaturada , con solo un átomo de hidrógeno por cada átomo de carbono , era un desafío. Archibald Scott Couper en 1858 y Johann Josef Loschmidt en 1861 [37] sugirieron posibles estructuras que contenían múltiples dobles enlaces o múltiples anillos, pero en aquellos años se sabía muy poco sobre la química aromática, por lo que los químicos no pudieron aducir evidencia apropiada para favorecer cualquier fórmula determinada.
Pero muchos químicos habían comenzado a trabajar con sustancias aromáticas, especialmente en Alemania, y los datos relevantes llegaban rápidamente. En 1865, el químico alemán Friedrich August Kekulé publicó un artículo en francés (porque entonces enseñaba en la Bélgica francófona) sugiriendo que la estructura contenía un anillo de seis átomos de carbono con enlaces simples y dobles alternos. Al año siguiente publicó un artículo mucho más extenso en alemán sobre el mismo tema. [31] [38] Kekulé utilizó evidencia que se había acumulado en los años intermedios, es decir, que siempre parecía haber un solo isómero de cualquier monoderivado de benceno, y que siempre parecía haber exactamente tres isómeros de cada derivado disustituido; ahora entendido que corresponde a los patrones orto, meta y para de sustitución de arenos , para argumentar en apoyo de su estructura propuesta. [39] El anillo simétrico de Kekulé podría explicar estos hechos curiosos, así como la relación carbono-hidrógeno 1:1 del benceno.
La nueva comprensión del benceno, y por tanto de todos los compuestos aromáticos, resultó ser tan importante tanto para la química pura como para la química aplicada que en 1890 la Sociedad Química Alemana organizó una elaborada apreciación en honor de Kekulé, celebrando el vigésimo quinto aniversario de su primer artículo sobre benceno. . Aquí Kekulé habló de la creación de la teoría. Dijo que había descubierto la forma de anillo de la molécula de benceno después de soñar despierto con una serpiente que se mordía la cola (un símbolo en las culturas antiguas conocido como ouroboros ). [40] Esta visión, dijo, le llegó después de años de estudiar la naturaleza de los enlaces carbono-carbono. Esto fue siete años después de haber resuelto el problema de cómo los átomos de carbono podían unirse hasta con otros cuatro átomos al mismo tiempo. Curiosamente, una representación humorística similar del benceno había aparecido en 1886 en un panfleto titulado Berichte der Durstigen Chemischen Gesellschaft (Revista de la Sociedad Química Sed), una parodia del Berichte der Deutschen Chemischen Gesellschaft , sólo que en la parodia los monos se agarraban unos a otros en un círculo, en lugar de serpientes como en la anécdota de Kekulé. [41] Algunos historiadores han sugerido que la parodia era una satirización de la anécdota de la serpiente, posiblemente ya bien conocida a través de la transmisión oral, incluso si aún no había aparecido impresa. [18] El discurso de Kekulé de 1890 [42] en el que apareció esta anécdota ha sido traducido al inglés. [43] Si la anécdota es el recuerdo de un hecho real, las circunstancias mencionadas en el relato sugieren que debió haber ocurrido a principios de 1862. [44]
En 1929, la cristalógrafa Kathleen Lonsdale finalmente confirmó la naturaleza cíclica del benceno utilizando métodos de difracción de rayos X. [45] [46] Utilizando grandes cristales de hexametilbenceno , un derivado del benceno con el mismo núcleo de seis átomos de carbono, Lonsdale obtuvo patrones de difracción. Mediante el cálculo de más de treinta parámetros, Lonsdale demostró que el anillo de benceno no podía ser más que un hexágono plano y proporcionó distancias precisas para todos los enlaces carbono-carbono de la molécula. [47]
El químico alemán Wilhelm Körner sugirió los prefijos orto-, meta-, para- para distinguir los derivados de benceno disustituidos en 1867; sin embargo, no utilizó los prefijos para distinguir las posiciones relativas de los sustituyentes en un anillo de benceno. [48] [49] Fue el químico alemán Carl Gräbe quien, en 1869, utilizó por primera vez los prefijos orto-, meta-, para- para denotar ubicaciones relativas específicas de los sustituyentes en un anillo aromático disustituido (es decir, naftaleno). . [50] En 1870, el químico alemán Viktor Meyer aplicó por primera vez la nomenclatura de Gräbe al benceno. [51]
En 1903, Ludwig Roselius popularizó el uso del benceno para descafeinar el café . Este descubrimiento condujo a la producción de Sanka . Este proceso fue posteriormente interrumpido. Históricamente, el benceno se ha utilizado como componente importante en muchos productos de consumo, como llaves líquidas , varios decapantes de pintura , cementos de caucho , quitamanchas y otros productos. La fabricación de algunas de estas formulaciones que contienen benceno cesó alrededor de 1950, aunque Liquid Wrench continuó conteniendo cantidades significativas de benceno hasta finales de los años 1970. [52]
Se encuentran trazas de benceno en el petróleo y el carbón. Es un subproducto de la combustión incompleta de muchos materiales. Para uso comercial, hasta la Segunda Guerra Mundial , gran parte del benceno se obtenía como subproducto de la producción de coque (o "aceite ligero de hornos de coque") para la industria del acero . Sin embargo, en la década de 1950, el aumento de la demanda de benceno, especialmente de la creciente industria de los polímeros , requirió la producción de benceno a partir del petróleo. Hoy en día, la mayor parte del benceno proviene de la industria petroquímica , y sólo una pequeña fracción se produce a partir del carbón. [53] Se ha detectado benceno en Marte . [54] [55] [56]
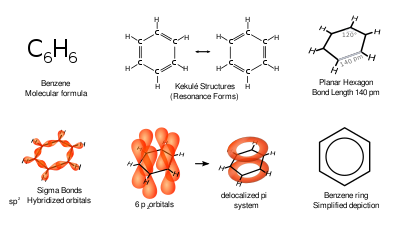
La difracción de rayos X muestra que los seis enlaces carbono-carbono del benceno tienen la misma longitud, 140 picometros (pm). [57] Las longitudes de los enlaces C-C son mayores que las de un enlace doble (135 pm) pero más cortas que las de un enlace simple (147 pm). Esta distancia intermedia es causada por la deslocalización de los electrones : los electrones para el enlace C=C se distribuyen equitativamente entre cada uno de los seis átomos de carbono. El benceno tiene 6 átomos de hidrógeno, menos que el alcano original correspondiente , el hexano , que tiene 14. El benceno y el ciclohexano tienen una estructura similar, sólo el anillo de electrones deslocalizados y la pérdida de un hidrógeno por carbono lo distinguen del ciclohexano. La molécula es plana. [58] La descripción del orbital molecular implica la formación de tres orbitales π deslocalizados que abarcan los seis átomos de carbono, mientras que la descripción del enlace de valencia implica una superposición de estructuras de resonancia . [59] [60] [61] [62] Es probable que esta estabilidad contribuya a las peculiares propiedades moleculares y químicas conocidas como aromaticidad . Para reflejar la naturaleza deslocalizada del enlace, el benceno suele representarse con un círculo dentro de una disposición hexagonal de átomos de carbono.
Los derivados del benceno se encuentran con bastante frecuencia como componente de moléculas orgánicas, hasta el punto de que el Consorcio Unicode ha asignado un símbolo en el bloque Técnico Misceláneo con el código U+232C (⌬) para representarlo con tres dobles enlaces, [63] y U+23E3 (⏣) para una versión deslocalizada. [64]
Muchos compuestos químicos importantes se derivan del benceno reemplazando uno o más de sus átomos de hidrógeno con otro grupo funcional . Ejemplos de derivados simples del benceno son el fenol , el tolueno y la anilina , abreviados como PhOH, PhMe y PhNH 2 , respectivamente. La unión de anillos de benceno da bifenilo , C 6 H 5 –C 6 H 5 . Una mayor pérdida de hidrógeno produce hidrocarburos aromáticos "fusionados", como naftaleno , antraceno , fenantreno y pireno . El límite del proceso de fusión es el alótropo del carbono libre de hidrógeno, el grafito .
En los heterociclos , los átomos de carbono del anillo de benceno se reemplazan por otros elementos. Las variaciones más importantes contienen nitrógeno . Reemplazar un CH con N da el compuesto piridina , C 5 H 5 N. Aunque el benceno y la piridina están relacionados estructuralmente , el benceno no se puede convertir en piridina. La sustitución de un segundo enlace CH por N da, dependiendo de la ubicación del segundo N, piridazina , pirimidina o pirazina . [sesenta y cinco]
Cuatro procesos químicos contribuyen a la producción industrial de benceno: reformado catalítico , hidrodesalquilación de tolueno , desproporción de tolueno y craqueo con vapor , etc. Según el Perfil Toxicológico del benceno de la ATSDR , entre 1978 y 1981, los reformados catalíticos representaron aproximadamente entre el 44% y el 50% del total de EE. UU. producción de benceno. [53]
En el reformado catalítico, una mezcla de hidrocarburos con puntos de ebullición entre 60 y 200 °C se mezcla con gas hidrógeno y luego se expone a un catalizador bifuncional de cloruro de platino o cloruro de renio a 500–525 °C y presiones que oscilan entre 8 y 50 atm. En estas condiciones, los hidrocarburos alifáticos forman anillos y pierden hidrógeno para convertirse en hidrocarburos aromáticos. Los productos aromáticos de la reacción luego se separan de la mezcla de reacción (o reformado) mediante extracción con cualquiera de varios disolventes , incluidos dietilenglicol o sulfolano , y luego el benceno se separa de los otros aromáticos mediante destilación. La etapa de extracción de aromáticos del reformado está diseñada para producir aromáticos con los componentes no aromáticos más bajos. La recuperación de los aromáticos, comúnmente denominados BTX (isómeros de benceno, tolueno y xileno), implica dichas etapas de extracción y destilación.
De manera similar a este reformado catalítico, UOP y BP comercializaron un método desde GLP (principalmente propano y butano) hasta aromáticos.
La hidrodesalquilación de tolueno convierte el tolueno en benceno. En este proceso intensivo en hidrógeno, el tolueno se mezcla con hidrógeno y luego se pasa sobre un catalizador de cromo , molibdeno u óxido de platino a 500-650 °C y 20-60 atm de presión. A veces, se utilizan temperaturas más altas en lugar de un catalizador (en condiciones de reacción similares). En estas condiciones, el tolueno sufre desalquilación a benceno y metano :
Esta reacción irreversible va acompañada de una reacción secundaria de equilibrio que produce bifenilo (también conocido como difenilo) a una temperatura más alta:
Si el flujo de materia prima contiene muchos componentes no aromáticos (parafinas o naftenos), es probable que se descompongan en hidrocarburos inferiores como el metano, lo que aumenta el consumo de hidrógeno.
Un rendimiento de reacción típico supera el 95%. A veces, se utilizan xilenos y aromáticos más pesados en lugar de tolueno, con una eficacia similar.
Esto a menudo se denomina metodología "específica" para producir benceno, en comparación con los procesos de extracción convencionales de BTX (benceno-tolueno-xileno).
La desproporción de tolueno ( TDP ) es la conversión de tolueno en benceno y xileno . [66]
Dado que la demanda de para -xileno ( p -xileno ) excede sustancialmente la demanda de otros isómeros de xileno, se puede utilizar un refinamiento del proceso TDP llamado TDP selectivo (STDP). En este proceso, la corriente de xileno que sale de la unidad TDP es aproximadamente 90% de p -xileno. En algunos sistemas, incluso la relación benceno-xilenos se modifica para favorecer a los xilenos.
El craqueo con vapor es el proceso para producir etileno y otros alquenos a partir de hidrocarburos alifáticos . Dependiendo de la materia prima utilizada para producir las olefinas, el craqueo con vapor puede producir un subproducto líquido rico en benceno llamado gasolina de pirólisis . La gasolina de pirólisis se puede mezclar con otros hidrocarburos como aditivo de la gasolina o pasar por un proceso de extracción para recuperar los aromáticos BTX (benceno, tolueno y xilenos).
Aunque no tiene importancia comercial, existen muchas otras rutas para obtener benceno. El fenol y los halobencenos se pueden reducir con metales. El ácido benzoico y sus sales se descarboxilan a benceno. La reacción del compuesto de diazonio derivado de la anilina con ácido hipofosforoso da benceno. La trimerización alquinada del acetileno da benceno. La descarboxilación completa del ácido melítico da benceno.
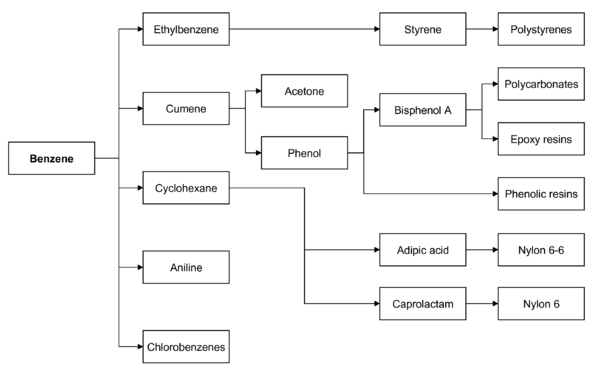
El benceno se utiliza principalmente como intermediario para fabricar otras sustancias químicas, sobre todo etilbenceno (y otros alquilbencenos ), cumeno , ciclohexano y nitrobenceno . En 1988 se informó que dos tercios de todas las sustancias químicas incluidas en las listas de la Sociedad Química Estadounidense contenían al menos un anillo de benceno. [67] Más de la mitad de toda la producción de benceno se procesa en etilbenceno, un precursor del estireno , que se utiliza para fabricar polímeros y plásticos como el poliestireno . Alrededor del 20% de la producción de benceno se utiliza para fabricar cumeno, necesario para producir fenol y acetona para resinas y adhesivos. El ciclohexano consume alrededor del 10% de la producción mundial de benceno; se utiliza principalmente en la fabricación de fibras de nailon, que se procesan para fabricar textiles y plásticos de ingeniería. Se utilizan cantidades más pequeñas de benceno para fabricar algunos tipos de cauchos , lubricantes , tintes , detergentes , medicamentos , explosivos y pesticidas . En 2013, el mayor país consumidor de benceno fue China, seguida de Estados Unidos. Actualmente la producción de benceno está aumentando en Oriente Medio y África, mientras que las capacidades de producción en Europa occidental y América del Norte están estancadas. [68]
El tolueno se utiliza ahora a menudo como sustituto del benceno, por ejemplo como aditivo para combustibles. Las propiedades disolventes de los dos son similares, pero el tolueno es menos tóxico y tiene un rango de líquidos más amplio. El tolueno también se transforma en benceno. [69]
Como aditivo de la gasolina , el benceno aumenta el octanaje y reduce la detonación . Como consecuencia, la gasolina a menudo contenía varios porcentajes de benceno antes de la década de 1950, cuando el tetraetilo de plomo la reemplazó como el aditivo antidetonante más utilizado. Con la eliminación mundial de la gasolina con plomo, el benceno ha regresado como aditivo de la gasolina en algunos países. En los Estados Unidos , la preocupación por sus efectos negativos para la salud y la posibilidad de que el benceno ingrese al agua subterránea ha llevado a una regulación estricta del contenido de benceno de la gasolina, con límites típicamente de alrededor del 1%. [70] Las especificaciones europeas para la gasolina contienen ahora el mismo límite del 1% en el contenido de benceno. La Agencia de Protección Ambiental de Estados Unidos introdujo nuevas regulaciones en 2011 que redujeron el contenido de benceno en la gasolina al 0,62%. [71]
En algunos idiomas europeos, la palabra petróleo o gasolina es un cognado exacto de "benceno". Por ejemplo, en catalán se puede utilizar la palabra 'benzina' para referirse a la gasolina, aunque ahora es relativamente raro.
Las reacciones más comunes del benceno implican la sustitución de un protón por otros grupos. [72] La sustitución aromática electrófila es un método general para derivatizar el benceno. El benceno es suficientemente nucleofílico como para sufrir sustitución por iones acilio y carbocationes de alquilo para dar derivados sustituidos.
El ejemplo más practicado de esta reacción es la etilación del benceno.
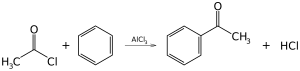
En 1999 se produjeron aproximadamente 24.700.000 toneladas. [73] Altamente instructivo pero de mucha menos importancia industrial es la alquilación de Friedel-Crafts de benceno (y muchos otros anillos aromáticos) utilizando un haluro de alquilo en presencia de un fuerte catalizador ácido de Lewis. De manera similar, la acilación de Friedel-Crafts es un ejemplo relacionado de sustitución aromática electrofílica . La reacción implica la acilación de benceno (o muchos otros anillos aromáticos) con un cloruro de acilo utilizando un catalizador ácido de Lewis fuerte como el cloruro de aluminio o el cloruro de hierro (III) .
Mediante sustitución aromática electrófila, se introducen muchos grupos funcionales en la estructura del benceno. La sulfonación del benceno implica el uso de óleum , una mezcla de ácido sulfúrico con trióxido de azufre . Los derivados de benceno sulfonados son detergentes útiles . En la nitración , el benceno reacciona con iones nitronio (NO 2 + ), que es un electrófilo fuerte producido al combinar ácidos sulfúrico y nítrico. El nitrobenceno es el precursor de la anilina . La cloración se logra con cloro para dar clorobenceno en presencia de un catalizador ácido de Lewis como el tricloruro de aluminio.
Mediante hidrogenación , el benceno y sus derivados se convierten en ciclohexano y derivados. Esta reacción se logra mediante el uso de altas presiones de hidrógeno en presencia de catalizadores heterogéneos , como el níquel finamente dividido . Mientras que los alquenos pueden hidrogenarse cerca de la temperatura ambiente, el benceno y los compuestos relacionados son sustratos más reacios y requieren temperaturas >100 °C. Esta reacción se practica a gran escala industrialmente. En ausencia del catalizador, el benceno es impermeable al hidrógeno. No se puede detener la hidrogenación para dar ciclohexeno o ciclohexadienos, ya que son sustratos superiores. La reducción con abedul , un proceso no catalítico, sin embargo, hidrogena selectivamente el benceno al dieno.
El benceno es un ligando excelente en la química organometálica de metales de baja valencia. Ejemplos importantes incluyen los complejos sándwich y medio sándwich, respectivamente, Cr(C 6 H 6 ) 2 y [RuCl 2 (C 6 H 6 )] 2 .

El benceno está clasificado como carcinógeno , lo que aumenta el riesgo de cáncer y otras enfermedades, y también es una causa notoria de insuficiencia de la médula ósea . Cantidades sustanciales de datos epidemiológicos, clínicos y de laboratorio vinculan el benceno con la anemia aplásica, la leucemia aguda , las anomalías de la médula ósea y las enfermedades cardiovasculares. [74] [75] [76] Las neoplasias malignas hematológicas específicas con las que se asocia el benceno incluyen: leucemia mieloide aguda (LMA), anemia aplásica, síndrome mielodisplásico (MDS), leucemia linfoblástica aguda (LLA) y leucemia mieloide crónica (LMC). . [77]
El Instituto Americano del Petróleo (API) afirmó ya en 1948 que "en general se considera que la única concentración absolutamente segura de benceno es cero". [78] No existe un nivel de exposición seguro; incluso pequeñas cantidades pueden causar daño. [79] El Departamento de Salud y Servicios Humanos de EE.UU. (DHHS) clasifica el benceno como carcinógeno humano. La exposición prolongada a niveles excesivos de benceno en el aire provoca leucemia, un cáncer potencialmente mortal de los órganos productores de sangre. En particular, la leucemia mieloide aguda o la leucemia aguda no linfocítica (AML y ANLL) es causada por el benceno. [80] La IARC calificó el benceno como "conocido por ser cancerígeno para los seres humanos" ( Grupo 1 ).
Como el benceno es omnipresente en la gasolina y los combustibles de hidrocarburos que se utilizan en todas partes, la exposición humana al benceno es un problema de salud mundial. El benceno se dirige al hígado, los riñones, los pulmones, el corazón y el cerebro y puede provocar roturas de cadenas de ADN y daños cromosómicos , por lo que es teratogénico y mutagénico . El benceno causa cáncer en animales, incluidos los humanos. Se ha demostrado que el benceno causa cáncer en ambos sexos de múltiples especies de animales de laboratorio expuestos por diversas vías. [81] [82]
Según la Agencia para el Registro de Sustancias Tóxicas y Enfermedades (ATSDR) (2007), el benceno es una sustancia química tanto sintética como natural a partir de procesos que incluyen: erupciones volcánicas, incendios forestales, síntesis de sustancias químicas como el fenol , producción de fibras sintéticas , y fabricación de cauchos , lubricantes , pesticidas , medicamentos y tintes . Las principales fuentes de exposición al benceno son el humo del tabaco , las estaciones de servicio de automóviles, los gases de escape de los vehículos de motor y las emisiones industriales; sin embargo, la ingestión y absorción dérmica del benceno también puede ocurrir a través del contacto con agua contaminada. El benceno se metaboliza hepáticamente y se excreta por la orina . La medición de los niveles de benceno en el aire y el agua se logra mediante la recolección a través de tubos de carbón activado , que luego se analizan con un cromatógrafo de gases . La medición del benceno en humanos se puede realizar mediante pruebas de orina , sangre y aliento ; sin embargo, todos estos tienen sus limitaciones porque el benceno se metaboliza rápidamente en el cuerpo humano. [83]
La exposición al benceno puede provocar progresivamente anemia aplásica , leucemia y mieloma múltiple . [84]
OSHA regula los niveles de benceno en el lugar de trabajo. [85] La cantidad máxima permitida de benceno en el aire del lugar de trabajo durante una jornada laboral de 8 horas y una semana laboral de 40 horas es 1 ppm. Como el benceno puede causar cáncer , NIOSH recomienda que todos los trabajadores usen equipo de respiración especial cuando sea probable que estén expuestos al benceno en niveles que excedan el límite de exposición recomendado (8 horas) de 0,1 ppm. [86]
La Agencia de Protección Ambiental de los Estados Unidos ha establecido un nivel máximo de contaminante para el benceno en el agua potable en 0,0005 mg/L (5 ppb), según lo promulgado a través de las Regulaciones Nacionales Primarias de Agua Potable de los Estados Unidos. [87] Esta regulación se basa en prevenir la leucemogénesis del benceno . El objetivo de nivel máximo de contaminante (MCLG), un objetivo de salud no exigible que permitiría un margen de seguridad adecuado para la prevención de efectos adversos, es una concentración cero de benceno en el agua potable. La EPA exige que se informen los derrames o liberaciones accidentales al medio ambiente de 10 libras (4,5 kg) o más de benceno.
La Administración de Salud y Seguridad Ocupacional de EE. UU. (OSHA) ha establecido un límite de exposición permisible de 1 parte de benceno por millón de partes de aire (1 ppm) en el lugar de trabajo durante una jornada laboral de 8 horas y una semana laboral de 40 horas. El límite de exposición a corto plazo al benceno en el aire es de 5 ppm durante 15 minutos. [88] Estos límites legales se basaron en estudios que demostraron evidencia convincente de riesgo para la salud de los trabajadores expuestos al benceno. Se ha estimado que el riesgo de exposición a 1 ppm durante toda la vida laboral es de cinco muertes por leucemia por cada 1.000 empleados expuestos. (Esta estimación no asume ningún umbral para los efectos cancerígenos del benceno). OSHA también ha establecido un nivel de acción de 0,5 ppm para fomentar exposiciones aún más bajas en el lugar de trabajo. [89]
El Instituto Nacional de Seguridad y Salud Ocupacional de EE. UU. (NIOSH) revisó la concentración de benceno inmediatamente peligroso para la vida y la salud (IDLH) a 500 ppm. La definición actual de NIOSH para una condición IDLH, como se indica en la Lógica de selección de respiradores de NIOSH, es aquella que representa una amenaza de exposición a contaminantes en el aire cuando es probable que esa exposición cause la muerte o efectos adversos permanentes inmediatos o retardados para la salud o impida el escape de dichos contaminantes. un ambiente. [90] El propósito de establecer un valor IDLH es (1) asegurar que el trabajador pueda escapar de un ambiente contaminado dado en caso de falla del equipo de protección respiratoria y (2) se considera un nivel máximo por encima del cual solo un Se permite el uso de aparatos de respiración confiables que brinden la máxima protección a los trabajadores. [90] [91] En septiembre de 1995, NIOSH emitió una nueva política para desarrollar límites de exposición recomendados (REL) para sustancias, incluidos los carcinógenos. Como el benceno puede causar cáncer, NIOSH recomienda que todos los trabajadores usen equipo de respiración especial cuando sea probable que estén expuestos al benceno en niveles que excedan el REL (10 horas) de 0,1 ppm. [92] El límite de exposición a corto plazo de NIOSH (STEL – 15 min) es de 1 ppm.
La Conferencia Americana de Higienistas Industriales Gubernamentales (ACGIH) adoptó valores límite umbral (TLV) para el benceno de 0,5 ppm TWA y 2,5 ppm STEL. [88]
Varias pruebas pueden determinar la exposición al benceno. El benceno en sí se puede medir en el aliento, la sangre o la orina, pero dichas pruebas generalmente se limitan a las primeras 24 horas posteriores a la exposición debido a la eliminación relativamente rápida de la sustancia química mediante exhalación o biotransformación. La mayoría de las personas en los países desarrollados tienen niveles básicos mensurables de benceno y otros hidrocarburos aromáticos del petróleo en la sangre. En el cuerpo, el benceno se convierte enzimáticamente en una serie de productos de oxidación que incluyen ácido mucónico , ácido fenilmercaptúrico, fenol , catecol , hidroquinona y 1,2,4-trihidroxibenceno . La mayoría de estos metabolitos tienen algún valor como biomarcadores de la exposición humana, ya que se acumulan en la orina en proporción al grado y la duración de la exposición, y pueden seguir presentes durante algunos días después de que haya cesado la exposición. Los límites de exposición biológica actuales de la ACGIH para la exposición ocupacional son 500 μg/g de creatinina para el ácido mucónico y 25 μg/g de creatinina para el ácido fenilmercaptúrico en una muestra de orina al final del turno. [93] [94] [95] [96]
Aunque no es un sustrato común para el metabolismo, el benceno puede ser oxidado tanto por bacterias como por eucariotas . En las bacterias, la enzima dioxigenasa puede agregar oxígeno al anillo y el producto inestable se reduce inmediatamente (mediante NADH ) a un diol cíclico con dos dobles enlaces, rompiendo la aromaticidad. A continuación, el NADH reduce nuevamente el diol a catecol . Luego, el catecol se metaboliza a acetil CoA y succinil CoA , utilizados por los organismos principalmente en el ciclo del ácido cítrico para la producción de energía.
La vía del metabolismo del benceno es compleja y comienza en el hígado. Varias enzimas están involucradas. Estos incluyen el citocromo P450 2E1 (CYP2E1), quinina oxidorreductasa (NQ01 o DT-diaforasa o NAD(P)H deshidrogenasa (quinona 1) ), GSH y mieloperoxidasa (MPO). CYP2E1 participa en múltiples pasos: convertir benceno en oxepina (óxido de benceno), fenol en hidroquinona e hidroquinona en bencenetriol y catecol . La hidroquinona, el bencenetriol y el catecol se convierten en polifenoles. En la médula ósea, la MPO convierte estos polifenoles en benzoquinonas. Estos intermediarios y metabolitos inducen genotoxicidad mediante múltiples mecanismos, incluida la inhibición de la topoisomerasa II (que mantiene la estructura cromosómica), la alteración de los microtúbulos (que mantiene la estructura y organización celular), la generación de radicales libres de oxígeno (especies inestables) que pueden conducir a mutaciones puntuales, aumentando estrés oxidativo, inducción de roturas de cadenas de ADN y alteración de la metilación del ADN (que puede afectar la expresión genética). NQ01 y GSH alejan el metabolismo de la toxicidad. NQ01 metaboliza la benzoquinona hacia polifenoles (contrarrestando el efecto de la MPO). El GSH participa en la formación de ácido fenilmercaptúrico. [77] [97]
Los polimorfismos genéticos en estas enzimas pueden inducir pérdida o ganancia de función. Por ejemplo, las mutaciones en CYP2E1 aumentan la actividad y dan como resultado una mayor generación de metabolitos tóxicos. Las mutaciones NQ01 provocan la pérdida de función y pueden provocar una disminución de la desintoxicación. Las mutaciones de mieloperoxidasa provocan pérdida de función y pueden provocar una disminución de la generación de metabolitos tóxicos. Las mutaciones o deleciones de GSH provocan una pérdida de función y una disminución de la desintoxicación. Estos genes pueden ser objetivos para la detección genética de susceptibilidad a la toxicidad del benceno. [98]
El paradigma de la evaluación toxicológica del benceno está cambiando hacia el dominio de la toxicología molecular, ya que permite comprender mejor los mecanismos biológicos fundamentales. El glutatión parece desempeñar un papel importante al proteger contra las roturas del ADN inducidas por el benceno y se está identificando como un nuevo biomarcador de exposición y efecto. [99] El benceno causa aberraciones cromosómicas en los leucocitos de la sangre periférica y la médula ósea, lo que explica la mayor incidencia de leucemia y mieloma múltiple causados por la exposición crónica. Estas aberraciones se pueden controlar mediante hibridación fluorescente in situ (FISH) con sondas de ADN para evaluar los efectos del benceno junto con las pruebas hematológicas como marcadores de hematotoxicidad. [100] El metabolismo del benceno implica enzimas codificadas por genes polimórficos. Los estudios han demostrado que el genotipo en estos loci puede influir en la susceptibilidad a los efectos tóxicos de la exposición al benceno. Los individuos portadores de una variante de NAD(P)H:quinona oxidorreductasa 1 (NQO1), epóxido hidrolasa microsomal (EPHX) y deleción de la glutatión S-transferasa T1 (GSTT1) mostraron una mayor frecuencia de roturas monocatenarias del ADN. [101]
Una forma de comprender los efectos cancerígenos del benceno es examinando los productos de la oxidación biológica. El benceno puro, por ejemplo, se oxida en el cuerpo para producir un epóxido, óxido de benceno , que no se excreta fácilmente y puede interactuar con el ADN para producir mutaciones dañinas.
El aire exterior puede contener niveles bajos de benceno procedente de estaciones de servicio de automóviles, humo de leña, humo de tabaco, transferencia de gasolina, gases de escape de vehículos motorizados y emisiones industriales. [102] Aproximadamente el 50% de toda la exposición a nivel nacional (Estados Unidos) al benceno se debe a fumar tabaco o a la exposición al humo del tabaco. [103] Después de fumar 32 cigarrillos por día, el fumador ingeriría aproximadamente 1,8 miligramos (mg) de benceno. Esta cantidad es aproximadamente 10 veces la ingesta diaria promedio de benceno por parte de los no fumadores. [104]
El benceno inhalado se expulsa principalmente sin cambios mediante la exhalación. En un estudio en humanos, del 16,4 al 41,6 % del benceno retenido se eliminó a través de los pulmones entre cinco y siete horas después de una exposición de dos a tres horas a 47 a 110 ppm y sólo del 0,07 al 0,2 % del benceno restante se excretó sin cambios en los pulmones. orina. Después de la exposición a 63 a 405 mg/m 3 de benceno durante 1 a 5 horas, del 51 al 87% se excretó en la orina como fenol durante un período de 23 a 50 horas. En otro estudio en humanos, el 30% del benceno absorbido aplicado por vía dérmica, que se metaboliza principalmente en el hígado, se excretó como fenol en la orina. [105]
En condiciones específicas y en presencia de otras sustancias químicas, el ácido benzoico (un conservante) y el ácido ascórbico (vitamina C) pueden interactuar para producir benceno. En marzo de 2006, la Agencia de Normas Alimentarias oficial del Reino Unido llevó a cabo una encuesta sobre 150 marcas de refrescos. Encontró que cuatro contenían niveles de benceno por encima de los límites de la Organización Mundial de la Salud . Los lotes afectados fueron retirados de la venta. La FDA informó problemas similares en los Estados Unidos. [106]
En 2005, el suministro de agua a la ciudad de Harbin en China, con una población de casi nueve millones de personas, se cortó debido a una importante exposición al benceno. [107] El benceno se filtró al río Songhua , que suministra agua potable a la ciudad, después de una explosión en una fábrica de la Corporación Nacional de Petróleo de China (CNPC) en la ciudad de Jilin el 13 de noviembre de 2005.
Cuando las tuberías de agua de plástico están expuestas a altas temperaturas, el agua puede estar contaminada con benceno. [108]
El gobierno alemán nazi utilizó benceno administrado mediante inyección como uno de sus muchos métodos para matar . [109] [110]
La existencia y el modo de formación del ácido insolínico demuestran que para la serie de ácidos aromáticos monobásicos, C
n2
H
n2-8
O
4
, cuyo término más bajo conocido es el ácido benzoico,….
[Nota: Las fórmulas empíricas de compuestos orgánicos que aparecen en el artículo de Hofmann (p. 3) se basan en una masa atómica de carbono de 6 (en lugar de 12) y una masa atómica de oxígeno de 8 (en lugar de 16).]
La identificación de moléculas orgánicas en las rocas del planeta rojo no necesariamente indica que haya vida allí, pasada o presente, pero sí indica que algunos de los componentes básicos estaban presentes.