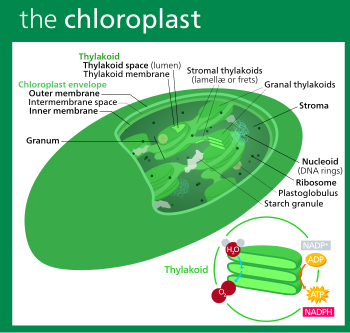

Un cloroplasto ( / ˈ k l ɔːr ə ˌ p l æ s t , - p l ɑː s t / ) [1] [2] es un tipo de orgánulo conocido como plástido que realiza la fotosíntesis principalmente en células de plantas y algas . Los cloroplastos tienen una alta concentración de pigmentos de clorofila que capturan la energía de la luz solar y la convierten en energía química y liberan oxígeno . La energía química creada luego se utiliza para producir azúcar y otras moléculas orgánicas a partir de dióxido de carbono en un proceso llamado ciclo de Calvin . Los cloroplastos llevan a cabo una serie de otras funciones, incluida la síntesis de ácidos grasos , la síntesis de aminoácidos y la respuesta inmune en las plantas. El número de cloroplastos por célula varía desde uno, en algunas algas unicelulares, hasta 100 en plantas como Arabidopsis y el trigo .
Los cloroplastos son muy dinámicos: circulan y se desplazan dentro de las células. Su comportamiento está fuertemente influenciado por factores ambientales como el color y la intensidad de la luz. La célula vegetal no puede volver a generar cloroplastos, y cada célula hija debe heredarlos durante la división celular, lo que se cree que se hereda de su antecesor, una cianobacteria fotosintética que fue engullida por una célula eucariota primitiva . [3]
Los cloroplastos evolucionaron a partir de una antigua cianobacteria que fue engullida por una célula eucariota primitiva. Debido a sus orígenes endosimbióticos, los cloroplastos, al igual que las mitocondrias , contienen su propio ADN separado del núcleo celular . Con una excepción (la ameboide Paulinella chromatophora ), todos los cloroplastos pueden rastrearse hasta un único evento endosimbiótico . A pesar de esto, los cloroplastos se pueden encontrar en organismos extremadamente diversos que no están directamente relacionados entre sí, una consecuencia de muchos eventos endosimbióticos secundarios e incluso terciarios .
La primera descripción definitiva de un cloroplasto ( Chlorophyllkörnen , "grano de clorofila") fue dada por Hugo von Mohl en 1837 como cuerpos discretos dentro de la célula de la planta verde. [4] En 1883, Andreas Franz Wilhelm Schimper nombró a estos cuerpos como "cloroplastidios" ( Chloroplastiden ). [5] En 1884, Eduard Strasburger adoptó el término "cloroplastos" ( Chloroplasten ). [6] [7] [8]
La palabra cloroplasto deriva de las palabras griegas chloros (χλωρός), que significa verde, y plastes (πλάστης), que significa "el que forma". [9]
Los cloroplastos son uno de los muchos tipos de orgánulos en las células eucariotas fotosintéticas. Evolucionaron a partir de las cianobacterias a través de un proceso llamado organelogénesis . [10] Las cianobacterias son un filo diverso de bacterias gramnegativas capaces de llevar a cabo la fotosíntesis oxigénica . Al igual que los cloroplastos, tienen tilacoides . [11] Las membranas tilacoides contienen pigmentos fotosintéticos , incluida la clorofila a . [12] [13] Este origen de los cloroplastos fue sugerido por primera vez por el biólogo ruso Konstantin Mereschkowski en 1905 [14] después de que Andreas Franz Wilhelm Schimper observara en 1883 que los cloroplastos se parecen mucho a las cianobacterias . [5] Los cloroplastos solo se encuentran en plantas , algas , [15] y algunas especies de la ameboide Paulinella . [16]
Se cree que las mitocondrias provienen de un evento de endosimbiosis similar , donde un procariota aeróbico fue engullido. [17]
![Endosimbiosis primaria Un eucariota con mitocondrias envolvió una cianobacteria en un evento de endosimbiosis primaria en serie, creando un linaje de células con ambos orgánulos.[17]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b8/Chloroplast_endosymbiosis_simple.svg/400px-Chloroplast_endosymbiosis_simple.svg.png)
Hace aproximadamente dos mil millones de años, [18] [19] [20] una cianobacteria de vida libre entró en una célula eucariota temprana, ya sea como alimento o como parásito interno , [17] pero logró escapar de la vacuola fagocítica en la que estaba contenida y persistir dentro de la célula. [12] Este evento se llama endosimbiosis , o "célula que vive dentro de otra célula con un beneficio mutuo para ambas". La célula externa se conoce comúnmente como el huésped, mientras que la célula interna se llama endosimbionte . [17] La cianobacteria engullida proporcionó una ventaja al huésped al proporcionar azúcar de la fotosíntesis. [17] Con el tiempo, la cianobacteria fue asimilada y muchos de sus genes se perdieron o se transfirieron al núcleo del huésped. [21] Algunas de las proteínas cianobacterianas fueron luego sintetizadas por la célula huésped e importadas nuevamente al cloroplasto (anteriormente la cianobacteria), lo que le permitió al huésped controlar el cloroplasto. [21] [22]
Los cloroplastos que se pueden rastrear directamente hasta un ancestro cianobacteriano (es decir, sin un evento endosimbiótico posterior) se conocen como plástidos primarios (" plástido " en este contexto significa casi lo mismo que cloroplasto [17] ). [23] Los cloroplastos que se pueden rastrear hasta otro endosimbionte eucariota fotosintético se denominan plástidos secundarios o plástidos terciarios (que se analizan a continuación).
Durante mucho tiempo se debatió si los cloroplastos primarios surgieron de un único evento endosimbiótico o de múltiples engullimientos independientes a lo largo de varios linajes eucariotas. Ahora se sostiene generalmente que con una excepción (el ameboide Paulinella chromatophora ), los cloroplastos surgieron de un único evento endosimbiótico hace unos dos mil millones de años y todos estos cloroplastos comparten un único ancestro . [19] Se ha propuesto que el pariente vivo más cercano de la cianobacteria ancestral engullida es Gloeomargarita lithophora . [24] [25] [26] Por otra parte, en algún momento hace unos 90-140 millones de años, este proceso ocurrió de nuevo en el ameboide Paulinella con una cianobacteria del género Prochlorococcus . Este cloroplasto evolucionado independientemente a menudo se llama cromatóforo en lugar de cloroplasto. [27] [Nota 1]
Se cree que los cloroplastos surgieron después de las mitocondrias , ya que todos los eucariotas contienen mitocondrias, pero no todos tienen cloroplastos. [17] [28] Esto se llama endosimbiosis en serie , donde un eucariota temprano engulló al ancestro mitocondrial , y luego sus descendientes engulleron al ancestro cloroplasto, creando una célula con cloroplastos y mitocondrias. [17]
Muchos otros organismos obtuvieron cloroplastos de los linajes de cloroplastos primarios a través de la endosimbiosis secundaria, envolviendo un alga roja o verde con un cloroplasto primario. Estos cloroplastos se conocen como plástidos secundarios . [23]
Como resultado del evento endosimbiótico secundario, los cloroplastos secundarios tienen membranas adicionales fuera de las dos originales en los cloroplastos primarios. [29] En los plástidos secundarios, típicamente solo el cloroplasto, y a veces su membrana celular y núcleo permanecen, formando un cloroplasto con tres o cuatro membranas [30] —las dos membranas de las cianobacterias, a veces la membrana celular del alga ingerida y la vacuola fagosómica de la membrana celular del huésped. [29]
Los genes en el núcleo del eucariota fagocitado a menudo se transfieren al núcleo del huésped secundario. [29] Las criptomonas y las clorraracniofitas retienen el núcleo del eucariota fagocitado, un objeto llamado nucleomorfo , [29] ubicado entre la segunda y tercera membranas del cloroplasto. [12] [22]
Todos los cloroplastos secundarios proceden de algas verdes y rojas . No se han observado cloroplastos secundarios de glaucófitas , probablemente porque estas últimas son relativamente raras en la naturaleza, lo que hace menos probable que hayan sido absorbidas por otro eucariota. [29]
Otros organismos, incluidos los dinoflagelados Karlodinium y Karenia , obtuvieron cloroplastos al engullir un organismo con un plástido secundario. Estos se denominan plástidos terciarios . [23]

Todos los cloroplastos primarios pertenecen a uno de los cuatro linajes de cloroplastos: el linaje de cloroplastos glaucófitos , el linaje de cloroplastos rodófitos ("rojos") y el linaje de cloroplastos cloroplastídeos ("verdes"), el linaje ameboide Paulinella chromatophora . [33] Los linajes glaucófitos, rodófitos y cloroplastídeos descienden del mismo evento endosimbiótico ancestral y todos pertenecen al grupo Archaeplastida . [29]

El grupo de cloroplastos glaucófitos es el más pequeño de los tres linajes primarios de cloroplastos, ya que solo hay 25 especies de glaucofitos descritas. [34] Los glaucófitos divergieron primero antes de que divergieran los linajes de cloroplastos rojo y verde. [35] Debido a esto, a veces se los considera intermedios entre las cianobacterias y los cloroplastos rojo y verde. [36] Esta divergencia temprana está respaldada tanto por estudios filogenéticos como por características físicas presentes en los cloroplastos glaucófitos y las cianobacterias, pero no en los cloroplastos rojo y verde. En primer lugar, los cloroplastos glaucófitos tienen una pared de peptidoglicano , un tipo de pared celular que de otro modo solo se encuentra en bacterias (incluidas las cianobacterias). [Nota 2] En segundo lugar, los cloroplastos glaucófitos contienen tilacoides concéntricos no apilados que rodean un carboxisoma , una estructura icosaédrica que contiene la enzima RuBisCO responsable de la fijación de carbono . En tercer lugar, el almidón creado por el cloroplasto se recoge fuera del cloroplasto. [37] Además, al igual que las cianobacterias, tanto los tilacoides glaucofitos como los rodofitos están repletos de estructuras recolectoras de luz llamadas ficobilisomas .
El grupo de las rodofitas, o algas rojas , es un linaje grande y diverso. [29] Los cloroplastos rodofitos también se denominan rodoplastos , [23] literalmente "cloroplastos rojos". [38] Los rodoplastos tienen una membrana doble con un espacio intermembrana y pigmentos de ficobilina organizados en ficobilisomas en las membranas tilacoides, lo que evita que sus tilacoides se apilen. [12] Algunos contienen pirenoides . [23] Los rodoplastos tienen clorofila a y ficobilinas [32] para pigmentos fotosintéticos; la ficobilina ficoeritrina es responsable de dar a muchas algas rojas su color rojo distintivo . [39] Sin embargo, dado que también contienen la clorofila a verde azulada y otros pigmentos, muchos son de color rojizo a púrpura por la combinación. [23] [ dudoso – discutir ] El pigmento rojo ficoeritrina es una adaptación para ayudar a las algas rojas a captar más luz solar en aguas profundas [23] —como tal, algunas algas rojas que viven en aguas poco profundas tienen menos ficoeritrina en sus rodoplastos y pueden parecer más verdosas. [39] Los rodoplastos sintetizan una forma de almidón llamada almidón floridiano , [23] que se acumula en gránulos fuera del rodoplasto, en el citoplasma del alga roja. [12]
El grupo cloroplastida es otro linaje grande y muy diverso que incluye tanto algas verdes como plantas terrestres . [40] Este grupo también se llama Viridiplantae , que incluye dos clados principales: Chlorophyta y Streptophyta .
La mayoría de los cloroplastos verdes son de color verde , aunque algunos no lo son debido a pigmentos accesorios que anulan el verde de las clorofilas, como en las células en reposo de Haematococcus pluvialis . Los cloroplastos verdes se diferencian de los cloroplastos de las glaucofitas y las algas rojas en que han perdido sus ficobilisomas y contienen clorofila b . [12] También han perdido la pared de peptidoglicano entre su doble membrana, dejando un espacio intermembrana. [12] Algunas plantas han conservado algunos genes necesarios para la síntesis de peptidoglicano, pero los han reutilizado para su uso en la división de cloroplastos. [41] Los linajes de Chloroplastida también mantienen su almidón dentro de sus cloroplastos. [12] [32] [40] En las plantas y algunas algas, los tilacoides del cloroplasto están dispuestos en pilas de grana. Algunos cloroplastos de algas verdes contienen una estructura llamada pirenoide , [12] que concentra RuBisCO y CO 2 en el cloroplasto, funcionalmente similar al carboxisoma glaucófito . [42]
Existen algunos linajes de algas verdes parásitas no fotosintéticas que han perdido sus cloroplastos por completo, como Prototheca , [32] o no tienen cloroplastos pero conservan el genoma del cloroplasto separado, como en Helicosporidium . [43] Las similitudes morfológicas y fisiológicas, así como la filogenética , confirman que se trata de linajes que ancestralmente tenían cloroplastos pero que desde entonces los han perdido. [43] [44]
Los ameboides fotosintéticos del género Paulinella —P. chromatophora, P. micropora y P. longichromatophora marina— tienen el único cloroplasto conocido que evolucionó de forma independiente, a menudo llamado cromatóforo . [Nota 1] Mientras que todos los demás cloroplastos se originan a partir de un único evento endosimbiótico antiguo, Paulinella adquirió de forma independiente una cianobacteria endosimbiótica del género Synechococcus hace unos 90 a 140 millones de años. [27] [29] Cada célula de Paulinella contiene uno o dos cloroplastos con forma de salchicha; [21] [45] fueron descritos por primera vez en 1894 por el biólogo alemán Robert Lauterborn. [46]
El cromatóforo es muy reducido en comparación con sus parientes cianobacterianos de vida libre y tiene funciones limitadas. Por ejemplo, tiene un genoma de alrededor de 1 millón de pares de bases , un tercio del tamaño de los genomas de Synechococcus , y solo codifica alrededor de 850 proteínas. [21] Sin embargo, esto sigue siendo mucho más grande que otros genomas de cloroplastos, que suelen tener alrededor de 150.000 pares de bases. Los cromatóforos también han transferido mucho menos de su ADN al núcleo de sus huéspedes. Alrededor del 0,3-0,8% del ADN nuclear en Paulinella proviene del cromatóforo, en comparación con el 11-14% del cloroplasto en las plantas. [45] Al igual que otros cloroplastos, Paulinella proporciona proteínas específicas al cromatóforo utilizando una secuencia de orientación específica. [47] Debido a que los cromatóforos son mucho más jóvenes en comparación con los cloroplastos canónicos, se estudia Paulinella chromatophora para comprender cómo evolucionaron los primeros cloroplastos. [21]
Las algas verdes han sido absorbidas por muchos grupos en tres o cuatro eventos separados. [48] Principalmente, los cloroplastos secundarios derivados de las algas verdes se encuentran en los euglenidos y cloraracniofitos . También se encuentran en un linaje de dinoflagelados [32] y posiblemente en el ancestro del linaje CASH ( criptomonas , alveolados , estramenopilos y haptofitos ) [49] Muchos cloroplastos derivados de algas verdes contienen pirenoides , pero a diferencia de los cloroplastos en sus ancestros de algas verdes, el producto de almacenamiento se acumula en gránulos fuera del cloroplasto. [12]

Los euglenofitos son un grupo de protistos flagelados comunes que contienen cloroplastos derivados de un alga verde. [29] Los euglenofitos son el único grupo fuera de Diaphoretickes que tienen cloroplastos sin realizar cleptoplastia . [50] [51] Los cloroplastos euglenofitos tienen tres membranas. Se piensa que la membrana del huésped endosimbionte primario se perdió (por ejemplo, la membrana del alga verde), dejando las dos membranas cianobacterianas y la membrana fagosómica del huésped secundario. [29] Los cloroplastos euglenofitos tienen un pirenoide y tilacoides apilados en grupos de tres. El carbono fijado a través de la fotosíntesis se almacena en forma de paramilón , que está contenido en gránulos unidos a la membrana en el citoplasma del euglenofito. [12] [32]

Las cloraracniófitas son un grupo poco común de organismos que también contienen cloroplastos derivados de algas verdes, [29] aunque su historia es más complicada que la de las euglenófitas. Se cree que el ancestro de las cloraracniófitas fue un eucariota con un cloroplasto derivado de algas rojas . Se cree que luego perdió su primer cloroplasto de algas rojas y luego engulló un alga verde, lo que le dio su segundo cloroplasto derivado de algas verdes. [32]
Los cloroplastos de las cloraracniofitas están delimitados por cuatro membranas, excepto cerca de la membrana celular, donde las membranas del cloroplasto se fusionan en una membrana doble. [12] Sus tilacoides están dispuestos en pilas sueltas de tres. [12] Las cloraracniofitas tienen una forma de polisacárido llamado crisolaminarina , que almacenan en el citoplasma, [32] a menudo se acumula alrededor del pirenoide del cloroplasto , que sobresale hacia el citoplasma. [12]
Los cloroplastos cloraracniófitos son notables porque el alga verde del que derivan no se ha descompuesto completamente: su núcleo aún persiste como un nucleomorfo [29] que se encuentra entre la segunda y tercera membranas del cloroplasto [12] , el espacio periplastídeo, que corresponde al citoplasma del alga verde. [32]
Los dinoflagelados del género Lepidodinium han perdido su cloroplasto peridinina original y lo han reemplazado por un cloroplasto derivado de algas verdes (más específicamente, un prasinofito ). [12] [52] Lepidodinium es el único dinoflagelado que tiene un cloroplasto que no es del linaje de los rodoplastos . El cloroplasto está rodeado por dos membranas y no tiene nucleomorfo: todos los genes nucleomorfos se han transferido al núcleo del dinofito . [52] El evento endosimbiótico que condujo a este cloroplasto fue una endosimbiosis secundaria en serie en lugar de una endosimbiosis terciaria: el endosimbionte era un alga verde que contenía un cloroplasto primario (que formaba un cloroplasto secundario). [32]
Los cloroplastos secundarios derivados de las algas rojas parecen haber sido absorbidos solo una vez, y luego se diversificaron en un gran grupo llamado cromalveolados . Hoy en día se encuentran en las haptofitas , criptomonas , heterokontes , dinoflagelados y apicomplejos . [32] Los cloroplastos secundarios de las algas rojas contienen clorofila c y están rodeados por cuatro membranas. [12]
Las criptofitas , o criptomonas, son un grupo de algas que contienen un cloroplasto derivado de algas rojas. Los cloroplastos criptofitos contienen un nucleomorfo que superficialmente se parece al de las cloraracniófitas . [29] Los cloroplastos criptofitos tienen cuatro membranas, la más externa de las cuales es continua con el retículo endoplasmático rugoso . Sintetizan almidón ordinario , que se almacena en gránulos que se encuentran en el espacio periplastídeo, fuera de la doble membrana original, en el lugar que corresponde al citoplasma del alga roja. Dentro de los cloroplastos criptofitos hay un pirenoide y tilacoides en pilas de dos. [12]
Sus cloroplastos no tienen ficobilisomas , [12] pero sí tienen pigmentos de ficobilina que mantienen en su espacio tilacoide, en lugar de anclados en el exterior de sus membranas tilacoides. [12] [29]
Las criptofitas pueden haber desempeñado un papel clave en la propagación de los cloroplastos basados en algas rojas. [53] [54]

Las haptofitas son similares y están estrechamente relacionadas con las criptofitas o heterocontofitas. [32] Sus cloroplastos carecen de un nucleomorfo, [12] [29] sus tilacoides están en pilas de tres y sintetizan el azúcar crisolaminarina , que almacenan completamente fuera del cloroplasto, en el citoplasma de la haptofita. [12]

Los estramenopilos , también conocidos como heterocontofitos, son un grupo muy grande y diverso de eucariotas. Incluye Ochrophyta , que incluye diatomeas , algas pardas (algas marinas) y algas doradas (crisofitas) [39] , y Xanthophyceae (también llamadas algas verdeamarillas). [32]
Los cloroplastos heterokont son muy similares a los cloroplastos haptofitos. Tienen un pirenoide , tilacoides tripletes y, con algunas excepciones, [12] una envoltura plastídica de cuatro capas (la membrana epiplastídica más externa conectada al retículo endoplasmático ). Al igual que los haptofitos, los stramenopiles almacenan azúcar en gránulos de crisolaminarina en el citoplasma. [12] Los cloroplastos de stramenopiles contienen clorofila a y, con algunas excepciones [12], clorofila c , [29] pero también tienen carotenoides que les dan sus muchos colores. [39]
Los alveolados son un clado importante de eucariotas unicelulares con miembros tanto autótrofos como heterótrofos. La característica compartida más notable es la presencia de alvéolos (sacos) corticales (región externa). Estos son vesículas (sacos) aplanadas empaquetadas en una capa continua justo debajo de la membrana y que la sostienen, formando típicamente una película flexible (piel delgada). En los dinoflagelados, a menudo forman placas de armadura. Muchos miembros contienen un plástido derivado de algas rojas. Una característica notable de este grupo diverso es la pérdida frecuente de la fotosíntesis. Sin embargo, la mayoría de estos heterótrofos continúan procesando un plástido no fotosintético. [55]
Los apicomplejos son un grupo de alveolados. Al igual que los helicosproidia , son parásitos y tienen un cloroplasto no fotosintético. [32] Alguna vez se pensó que estaban relacionados con los helicosproidia, pero ahora se sabe que los helicosproida son algas verdes en lugar de parte del linaje CASH. [32] Los apicomplejos incluyen Plasmodium , el parásito de la malaria . Muchos apicomplejos mantienen un cloroplasto vestigial derivado de algas rojas [56] [32] llamado apicoplasto , que heredaron de sus antepasados. Otros apicomplejos como Cryptosporidium han perdido el cloroplasto por completo. [56] Los apicomplejos almacenan su energía en gránulos de amilopectina que se encuentran en su citoplasma, a pesar de que no son fotosintéticos. [12]
Los apicoplastos han perdido toda función fotosintética y no contienen pigmentos fotosintéticos ni tilacoides verdaderos. Están delimitados por cuatro membranas, pero las membranas no están conectadas al retículo endoplasmático . [12] El hecho de que los apicomplejos aún mantengan su cloroplasto no fotosintético demuestra cómo el cloroplasto lleva a cabo funciones importantes además de la fotosíntesis . Los cloroplastos vegetales proporcionan a las células vegetales muchas cosas importantes además del azúcar, y los apicoplastos no son diferentes: sintetizan ácidos grasos , pirofosfato de isopentenilo , grupos de hierro-azufre y llevan a cabo parte de la vía del hemo . [56] Esto hace que el apicoplasto sea un objetivo atractivo para los medicamentos para curar enfermedades relacionadas con los apicomplejos. [23] La función más importante del apicoplasto es la síntesis de pirofosfato de isopentenilo ; de hecho, los apicomplejos mueren cuando algo interfiere con esta función del apicoplasto, y cuando los apicomplejos se cultivan en un medio rico en pirofosfato de isopentenilo, desechan el orgánulo. [56]
Chromerida es un grupo de algas recién descubierto en los corales australianos que comprende algunos parientes fotosintéticos cercanos de los apicomplexanos. El primer miembro, Chromera velia , fue descubierto y aislado por primera vez en 2001. El descubrimiento de Chromera velia con una estructura similar a los apicomplexanos, proporciona un vínculo importante en la historia evolutiva de los apicomplexanos y los dinófitos. Sus plástidos tienen cuatro membranas, carecen de clorofila c y utilizan la forma tipo II de RuBisCO obtenida a partir de un evento de transferencia horizontal. [57]
Los dinoflagelados son otro grupo muy grande y diverso de protistas , aproximadamente la mitad de los cuales son (al menos parcialmente ) fotosintéticos . [39] [52]
La mayoría de los cloroplastos de los dinófitos son cloroplastos secundarios derivados de algas rojas . Muchos otros dinófitos han perdido el cloroplasto (convirtiéndose en el tipo no fotosintético de dinoflagelado), o lo han reemplazado a través de la endosimbiosis terciaria [58] —la absorción de otra alga eucariota que contiene un cloroplasto derivado de algas rojas. Otros reemplazaron su cloroplasto original con uno derivado de algas verdes . [29] [32] [52]
La mayoría de los cloroplastos de los dinófitos contienen RuBisCO de forma II, al menos los pigmentos fotosintéticos clorofila a , clorofila c 2 , betacaroteno y al menos una xantofila exclusiva de los dinófitos ( peridinina , dinoxantina o diadinoxantina ), lo que les da a muchos un color marrón dorado. [55] [52] Todos los dinófitos almacenan almidón en su citoplasma y la mayoría tienen cloroplastos con tilacoides dispuestos en pilas de tres. [12]

El cloroplasto de dinófito más común es el cloroplasto de tipo peridinina , caracterizado por el pigmento carotenoide peridinina en sus cloroplastos, junto con clorofila a y clorofila c 2 . [29] [52] La peridinina no se encuentra en ningún otro grupo de cloroplastos. [52] El cloroplasto de peridinina está delimitado por tres membranas (ocasionalmente dos), [12] habiendo perdido la membrana celular original del endosimbionte de algas rojas. [29] [32] La membrana más externa no está conectada al retículo endoplásmico. [12] [52] Contienen un pirenoide y tienen tilacoides apilados en tripletes. El almidón se encuentra fuera del cloroplasto. [12] Una característica importante de estos cloroplastos es que su ADN de cloroplasto está altamente reducido y fragmentado en muchos círculos pequeños. La mayor parte del genoma ha migrado al núcleo y sólo los genes críticos relacionados con la fotosíntesis permanecen en el cloroplasto. [52]
Se cree que el cloroplasto de peridinina es el cloroplasto "original" de los dinófitos, [52] que se ha perdido, reducido, reemplazado o está presente en varios otros linajes de dinófitos. [32]

Los linajes de dinófitos fucoxantínicos (incluidos Karlodinium y Karenia ) [32] perdieron su cloroplasto original derivado de algas rojas y lo reemplazaron con un nuevo cloroplasto derivado de un endosimbionte haptofito , lo que produjo estos plástidos terciarios. Karlodinium y Karenia probablemente adoptaron diferentes heterocontofitos. [32] Debido a que el cloroplasto haptofito tiene cuatro membranas, se esperaría que la endosimbiosis terciaria creara un cloroplasto de seis membranas, agregando la membrana celular del haptofito y la vacuola fagosómica del dinófito . [60] Sin embargo, el haptofito se redujo en gran medida, se le quitaron algunas membranas y su núcleo, dejando solo su cloroplasto (con su doble membrana original) y posiblemente una o dos membranas adicionales a su alrededor. [32] [60]
Los cloroplastos que contienen fucoxantina se caracterizan por tener el pigmento fucoxantina (en realidad 19′-hexanoiloxi-fucoxantina y/o 19′-butanoiloxi-fucoxantina) y no tener peridinina. La fucoxantina también se encuentra en los cloroplastos de haptofitas, lo que proporciona evidencia de ascendencia. [52]

Algunos dinófitos, como Kryptoperidinium y Durinskia , [32] tienen un cloroplasto derivado de diatomeas ( heterocontofito ). [29] Estos cloroplastos están delimitados por hasta cinco membranas, [29] (dependiendo de si todo el endosimbionte de diatomeas se cuenta como cloroplasto, o solo el cloroplasto derivado de algas rojas en su interior). El endosimbionte de diatomeas se ha reducido relativamente poco: todavía conserva sus mitocondrias originales , [32] y tiene retículo endoplasmático , ribosomas , un núcleo y, por supuesto, cloroplastos derivados de algas rojas, prácticamente una célula completa , [61] todo dentro del lumen del retículo endoplasmático del huésped . [32] Sin embargo, el endosimbionte de diatomeas no puede almacenar su propio alimento: su polisacárido de almacenamiento se encuentra en gránulos en el citoplasma del huésped dinófito. [12] [61] El núcleo del endosimbionte de diatomeas está presente, pero probablemente no se lo pueda llamar nucleomorfo porque no muestra signos de reducción del genoma , e incluso podría haberse expandido . [32] Las diatomeas han sido engullidas por dinoflagelados al menos tres veces. [32]
El endosimbionte diatomea está delimitado por una sola membrana, [52] en su interior hay cloroplastos con cuatro membranas. Al igual que el ancestro diatomea del endosimbionte diatomea, los cloroplastos tienen tilacoides y pirenoides tripletes . [61]
En algunos de estos géneros , los cloroplastos del endosimbionte diatomea no son los únicos cloroplastos en el dinófito. El cloroplasto peridinínico original de tres membranas todavía está presente, convertido en una mancha ocular . [29] [32]
En algunos grupos de protistos mixotróficos , como algunos dinoflagelados (por ejemplo, Dinophysis ), los cloroplastos se separan de un alga capturada y se utilizan temporalmente. Estos cloroplastos clepto pueden tener una vida útil de solo unos pocos días y luego se reemplazan. [62] [63]
Los miembros del género Dinophysis tienen un cloroplasto que contiene ficobilina [60] tomado de un criptofito . [29] Sin embargo, el criptofito no es un endosimbionte: solo parece que se le ha quitado el cloroplasto, y se le ha quitado el nucleomorfo y las dos membranas más externas, dejando solo un cloroplasto de dos membranas. Los cloroplastos de criptofitas requieren su nucleomorfo para mantenerse, y las especies de Dinophysis cultivadas en cultivos celulares por sí solas no pueden sobrevivir, por lo que es posible (pero no confirmado) que el cloroplasto de Dinophysis sea un cleptoplasto ; si es así, los cloroplastos de Dinophysis se desgastan y las especies de Dinophysis deben engullir continuamente criptofitas para obtener nuevos cloroplastos para reemplazar los viejos. [52]
Los cloroplastos, al igual que otros orgánulos endosimbióticos, contienen un genoma separado del del núcleo celular . La existencia del ADN del cloroplasto (cpDNA) se identificó bioquímicamente en 1959, [64] y se confirmó mediante microscopía electrónica en 1962. [65] Los descubrimientos de que el cloroplasto contiene ribosomas [66] y realiza la síntesis de proteínas [67] revelaron que el cloroplasto es genéticamente semiautónomo. El ADN del cloroplasto se secuenció por primera vez en 1986. [68] Desde entonces, se han secuenciado cientos de genomas de cloroplastos de varias especies , pero en su mayoría son de plantas terrestres y algas verdes : las glaucófitas , las algas rojas y otros grupos de algas están extremadamente subrepresentadas, lo que potencialmente introduce algún sesgo en las opiniones sobre la estructura y el contenido "típicos" del ADN del cloroplasto. [69]
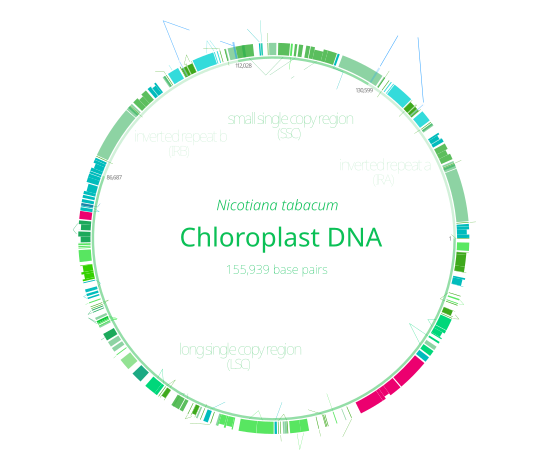
Con pocas excepciones, la mayoría de los cloroplastos tienen todo su genoma cloroplástico combinado en una única molécula grande de ADN circular, [69] típicamente de 120.000 a 170.000 pares de bases de longitud [70] [71] [72] [18] y una masa de alrededor de 80 a 130 millones de daltons . [73] Mientras que los genomas de los cloroplastos casi siempre se pueden ensamblar en un mapa circular, las moléculas físicas de ADN dentro de las células toman una variedad de formas lineales y ramificadas. [69] [74] Los nuevos cloroplastos pueden contener hasta 100 copias de su genoma, [70] aunque el número de copias disminuye a alrededor de 15 a 20 a medida que los cloroplastos envejecen. [75]
El ADN del cloroplasto suele estar condensado en nucleoides , que pueden contener múltiples copias del genoma del cloroplasto. Se pueden encontrar muchos nucleoides en cada cloroplasto. [73] En las algas rojas primitivas , los nucleoides del ADN del cloroplasto se agrupan en el centro del cloroplasto, mientras que en las plantas verdes y las algas verdes , los nucleoides se encuentran dispersos por todo el estroma . [76] El ADN del cloroplasto no está asociado con histonas verdaderas , proteínas que se utilizan para empaquetar firmemente las moléculas de ADN en los núcleos eucariotas. [17] Aunque en las algas rojas , proteínas similares empaquetan firmemente cada anillo de ADN del cloroplasto en un nucleoide . [76]
Muchos genomas de cloroplastos contienen dos repeticiones invertidas , que separan una sección de copia única larga (LSC) de una sección de copia única corta (SSC). [72] Un par dado de repeticiones invertidas rara vez son idénticas, pero siempre son muy similares entre sí, aparentemente como resultado de una evolución concertada . [69] Las repeticiones invertidas varían enormemente en longitud, desde 4000 a 25 000 pares de bases de longitud cada una y contienen tan solo cuatro o hasta más de 150 genes. [69] Las regiones de repetición invertida están altamente conservadas en plantas terrestres y acumulan pocas mutaciones. [72] [77]
Existen repeticiones invertidas similares en los genomas de las cianobacterias y los otros dos linajes de cloroplastos ( glaucophyta y rhodophyceae ), lo que sugiere que son anteriores al cloroplasto. [69] Algunos genomas de cloroplastos han perdido desde entonces [77] [78] o han invertido las repeticiones invertidas (convirtiéndolas en repeticiones directas ). [69] Es posible que las repeticiones invertidas ayuden a estabilizar el resto del genoma del cloroplasto, ya que los genomas de cloroplastos que han perdido algunos de los segmentos de repetición invertidos tienden a reorganizarse más. [78]
En los cloroplastos del musgo Physcomitrella patens , la proteína de reparación de desajustes de ADN Msh1 interactúa con las proteínas de reparación recombinacionales RecA y RecG para mantener la estabilidad del genoma del cloroplasto . [79] En los cloroplastos de la planta Arabidopsis thaliana, la proteína RecA mantiene la integridad del ADN del cloroplasto mediante un proceso que probablemente implica la reparación recombinacional del daño del ADN . [80]

El mecanismo de replicación del ADN del cloroplasto (cpDNA) no se ha determinado de manera concluyente, pero se han propuesto dos modelos principales. Los científicos han intentado observar la replicación del cloroplasto mediante microscopía electrónica desde la década de 1970. [81] [82] Los resultados de los experimentos de microscopía llevaron a la idea de que el ADN del cloroplasto se replica utilizando un bucle de doble desplazamiento (D-loop). A medida que el D-loop se mueve a través del ADN circular, adopta una forma intermediaria theta, también conocida como intermediario de replicación de Cairns, y completa la replicación con un mecanismo de círculo rodante. [81] [83] La transcripción comienza en puntos de origen específicos. Se abren múltiples horquillas de replicación, lo que permite que la maquinaria de replicación transcriba el ADN. A medida que continúa la replicación, las horquillas crecen y finalmente convergen. Las nuevas estructuras de cpDNA se separan, creando cromosomas cpDNA hijos.
Además de los primeros experimentos de microscopía, este modelo también está respaldado por las cantidades de desaminación observadas en el cpDNA. [81] La desaminación ocurre cuando se pierde un grupo amino y es una mutación que a menudo da como resultado cambios de bases. Cuando se desamina la adenina, se convierte en hipoxantina . La hipoxantina puede unirse a la citosina y, cuando se replica el par de bases XC, se convierte en un GC (por lo tanto, un cambio de base A → G). [84]

En el cpDNA, hay varios gradientes de desaminación A → G. El ADN se vuelve susceptible a eventos de desaminación cuando es monocatenario. Cuando se forman horquillas de replicación, la hebra que no se copia es monocatenaria y, por lo tanto, corre el riesgo de desaminación A → G. Por lo tanto, los gradientes en la desaminación indican que las horquillas de replicación probablemente estaban presentes y la dirección en la que se abrieron inicialmente (el gradiente más alto es probablemente el más cercano al sitio de inicio porque fue monocatenario durante la mayor cantidad de tiempo). [81] Este mecanismo sigue siendo la teoría principal en la actualidad; sin embargo, una segunda teoría sugiere que la mayor parte del cpDNA es en realidad lineal y se replica a través de recombinación homóloga. Además, sostiene que solo una minoría del material genético se mantiene en cromosomas circulares, mientras que el resto está en estructuras ramificadas, lineales u otras estructuras complejas. [81] [83]
Uno de los modelos competitivos para la replicación del cpDNA afirma que la mayor parte del cpDNA es lineal y participa en estructuras de recombinación homóloga y replicación similares a las estructuras de ADN lineal y circular del bacteriófago T4 . [83] [85] Se ha establecido que algunas plantas tienen cpDNA lineal, como el maíz, y que más especies aún contienen estructuras complejas que los científicos aún no comprenden. [83] Cuando se realizaron los experimentos originales con cpDNA, los científicos notaron estructuras lineales; sin embargo, atribuyeron estas formas lineales a círculos rotos. [83] Si las estructuras ramificadas y complejas observadas en los experimentos con cpDNA son reales y no artefactos de ADN circular concatenado o círculos rotos, entonces un mecanismo de replicación de bucle D es insuficiente para explicar cómo se replicarían esas estructuras. [83] Al mismo tiempo, la recombinación homóloga no expande los gradientes múltiples A --> G observados en los plastomas. [81] Debido a la imposibilidad de explicar el gradiente de desaminación, así como las numerosas especies de plantas que han demostrado tener cpDNA circular, la teoría predominante sigue sosteniendo que la mayor parte del cpDNA es circular y muy probablemente se replica a través de un mecanismo de bucle D.
Las cianobacterias ancestrales que dieron origen a los cloroplastos probablemente tenían un genoma que contenía más de 3000 genes, pero solo quedan aproximadamente 100 genes en los genomas de cloroplastos contemporáneos. [18] [22] [71] Estos genes codifican una variedad de cosas, principalmente relacionadas con la cadena de proteínas y la fotosíntesis . Al igual que en los procariotas , los genes en el ADN del cloroplasto están organizados en operones . [22] A diferencia de las moléculas de ADN procariota , las moléculas de ADN del cloroplasto contienen intrones ( el ADN mitocondrial de las plantas también, pero no el ADNmt humano). [86]
Entre las plantas terrestres, el contenido del genoma del cloroplasto es bastante similar. [72]
Con el tiempo, muchas partes del genoma del cloroplasto se transfirieron al genoma nuclear del huésped, [70] [71] [87] un proceso llamado transferencia genética endosimbiótica . Como resultado, el genoma del cloroplasto se reduce considerablemente en comparación con el de las cianobacterias de vida libre. Los cloroplastos pueden contener entre 60 y 100 genes, mientras que las cianobacterias a menudo tienen más de 1500 genes en su genoma. [88] Recientemente, se encontró un plástido sin genoma, lo que demuestra que los cloroplastos pueden perder su genoma durante el proceso de transferencia genética endosimbiótica. [89]
La transferencia de genes endosimbióticos es la forma en que conocemos los cloroplastos perdidos en muchos linajes CASH. Incluso si un cloroplasto finalmente se pierde, los genes que donó al núcleo del huésped anterior persisten, lo que proporciona evidencia de la existencia del cloroplasto perdido. Por ejemplo, mientras que las diatomeas (un heterocontofito ) ahora tienen un cloroplasto derivado de algas rojas , la presencia de muchos genes de algas verdes en el núcleo de la diatomea proporciona evidencia de que el ancestro de la diatomea tuvo un cloroplasto derivado de algas verdes en algún momento, que posteriormente fue reemplazado por el cloroplasto rojo. [49]
En las plantas terrestres, entre el 11 y el 14 % del ADN de sus núcleos se puede rastrear hasta el cloroplasto, [45] hasta el 18 % en Arabidopsis , lo que corresponde a unos 4500 genes codificadores de proteínas. [90] Ha habido algunas transferencias recientes de genes del ADN del cloroplasto al genoma nuclear en plantas terrestres. [71]
De las aproximadamente 3000 proteínas que se encuentran en los cloroplastos, alrededor del 95% de ellas están codificadas por genes nucleares. Muchos de los complejos proteicos del cloroplasto consisten en subunidades tanto del genoma del cloroplasto como del genoma nuclear del huésped. Como resultado, la síntesis de proteínas debe coordinarse entre el cloroplasto y el núcleo. El cloroplasto está en su mayor parte bajo control nuclear, aunque los cloroplastos también pueden emitir señales que regulan la expresión genética en el núcleo, llamadas señalización retrógrada . [91] Investigaciones recientes indican que partes de la red de señalización retrógrada que alguna vez se consideraron características de las plantas terrestres surgieron ya en un progenitor de algas, [92] [93] [94] integrándose en cohortes de genes coexpresados en los parientes algales más cercanos de las plantas terrestres. [95]
La síntesis de proteínas en los cloroplastos depende de dos ARN polimerasas . Una está codificada por el ADN del cloroplasto y la otra es de origen nuclear . Las dos ARN polimerasas pueden reconocer y unirse a diferentes tipos de promotores dentro del genoma del cloroplasto. [96] Los ribosomas de los cloroplastos son similares a los ribosomas bacterianos. [97]
Debido a que muchos genes del cloroplasto se han trasladado al núcleo, muchas proteínas que originalmente se habrían traducido en el cloroplasto ahora se sintetizan en el citoplasma de la célula vegetal. Estas proteínas deben ser dirigidas de vuelta al cloroplasto y ser importadas a través de al menos dos membranas del cloroplasto. [98]
Curiosamente, alrededor de la mitad de los productos proteicos de los genes transferidos ni siquiera se dirigen de nuevo al cloroplasto. Muchos se convirtieron en exaptaciones , asumiendo nuevas funciones como participar en la división celular , el enrutamiento de proteínas e incluso la resistencia a las enfermedades . Unos pocos genes del cloroplasto encontraron nuevos hogares en el genoma mitocondrial ; la mayoría se convirtieron en pseudogenes no funcionales , aunque unos pocos genes de ARNt todavía funcionan en la mitocondria . [88] Algunos productos proteicos del ADN del cloroplasto transferidos se dirigen a la vía secretora , [88] aunque muchos plástidos secundarios están delimitados por una membrana más externa derivada de la membrana celular del huésped y, por lo tanto, topológicamente fuera de la célula porque para llegar al cloroplasto desde el citosol , se debe cruzar la membrana celular , lo que significa la entrada al espacio extracelular . En esos casos, las proteínas dirigidas al cloroplasto viajan inicialmente a lo largo de la vía secretora. [32]
Debido a que la célula que adquiere un cloroplasto ya tenía mitocondrias (y peroxisomas , y una membrana celular para la secreción), el nuevo huésped del cloroplasto tuvo que desarrollar un sistema de orientación de proteínas único para evitar que las proteínas del cloroplasto se enviaran al orgánulo equivocado . [98]
![Los dos extremos de un polipéptido se denominan extremo N, o amino, y extremo C, o carboxilo.[99] Este polipéptido tiene cuatro aminoácidos unidos entre sí. A la izquierda se encuentra el extremo N, con su grupo amino (H2N) en verde. El extremo C, en azul, con su grupo carboxilo (CO2H), se encuentra a la derecha.](http://upload.wikimedia.org/wikipedia/commons/thumb/c/c0/Tetrapeptide_structural_formulae.svg/370px-Tetrapeptide_structural_formulae.svg.png)
En la mayoría de los casos, aunque no en todos, las proteínas de cloroplasto codificadas en el núcleo se traducen con un péptido de tránsito escindible que se agrega al extremo N del precursor proteico. A veces, la secuencia de tránsito se encuentra en el extremo C de la proteína [100] o dentro de la parte funcional de la proteína [98] .
Después de que un polipéptido de cloroplasto se sintetiza en un ribosoma en el citosol , una enzima específica para las proteínas del cloroplasto [101] fosforila o agrega un grupo fosfato a muchas (pero no todas) de ellas en sus secuencias de tránsito. [98] La fosforilación ayuda a muchas proteínas a unirse al polipéptido, evitando que se pliegue prematuramente. [98] Esto es importante porque evita que las proteínas del cloroplasto asuman su forma activa y realicen sus funciones de cloroplasto en el lugar equivocado: el citosol . [102] [103] Al mismo tiempo, tienen que mantener la forma suficiente para que el cloroplasto pueda reconocerlas. [102] Estas proteínas también ayudan a que el polipéptido se importe al cloroplasto. [98]
Desde aquí, las proteínas del cloroplasto destinadas al estroma deben pasar a través de dos complejos proteicos: el complejo TOC , o translocón en la membrana externa del cloroplasto , y el translocón TIC , o translocón en el translocón de la membrana interna del cloroplasto . [ 98 ] Las cadenas polipeptídicas del cloroplasto probablemente viajan a menudo a través de los dos complejos al mismo tiempo, pero el complejo TIC también puede recuperar preproteínas perdidas en el espacio intermembrana . [98]
En las plantas terrestres , los cloroplastos generalmente tienen forma de lente, de 3 a 10 μm de diámetro y 1 a 3 μm de espesor. [104] [18] Los cloroplastos de las plántulas de maíz tienen un volumen de ≈20 μm 3 . [18] Existe una mayor diversidad en las formas de los cloroplastos entre las algas , que a menudo contienen un solo cloroplasto [12] que puede tener forma de red (p. ej., Oedogonium ), [105] de copa (p. ej., Chlamydomonas ), [106] de espiral en forma de cinta alrededor de los bordes de la célula (p. ej., Spirogyra ), [107] o de bandas ligeramente retorcidas en los bordes de la célula (p. ej., Sirogonium ). [108] Algunas algas tienen dos cloroplastos en cada célula; tienen forma de estrella en Zygnema , [109] o pueden seguir la forma de la mitad de la célula en el orden Desmidiales . [110] En algunas algas, el cloroplasto ocupa la mayor parte de la célula, con cavidades para el núcleo y otros orgánulos, [12] por ejemplo, algunas especies de Chlorella tienen un cloroplasto en forma de copa que ocupa gran parte de la célula. [111]
Todos los cloroplastos tienen al menos tres sistemas de membrana: la membrana externa del cloroplasto, la membrana interna del cloroplasto y el sistema tilacoide . Las dos membranas de bicapa lipídica más internas [112] que rodean a todos los cloroplastos corresponden a las membranas externa e interna de la pared celular gramnegativa de la cianobacteria ancestral, [29] [113] [114] y no a la membrana fagosómica del huésped, que probablemente se perdió. [29] Los cloroplastos que son el producto de la endosimbiosis secundaria pueden tener membranas adicionales que rodean a estas tres. [30] Dentro de las membranas externa e interna del cloroplasto se encuentra el estroma del cloroplasto , un fluido semigelificado [23] que constituye gran parte del volumen de un cloroplasto y en el que flota el sistema tilacoide.

Existen algunos conceptos erróneos comunes sobre las membranas externa e interna de los cloroplastos. El hecho de que los cloroplastos estén rodeados por una membrana doble se cita a menudo como evidencia de que son descendientes de cianobacterias endosimbióticas . Esto a menudo se interpreta como que la membrana externa del cloroplasto es el producto del plegamiento de la membrana celular del huésped para formar una vesícula que rodea a la cianobacteria ancestral , lo cual no es cierto: ambas membranas de cloroplasto son homólogas a las membranas dobles originales de la cianobacteria. [29]
La doble membrana del cloroplasto también se compara a menudo con la doble membrana mitocondrial . Esta no es una comparación válida: la membrana mitocondrial interna se utiliza para hacer funcionar las bombas de protones y llevar a cabo la fosforilación oxidativa para generar energía ATP . La única estructura del cloroplasto que se puede considerar análoga a ella es el sistema tilacoide interno. Aun así, en términos de "entrada-salida", la dirección del flujo de iones H + del cloroplasto es en la dirección opuesta en comparación con la fosforilación oxidativa en las mitocondrias. [23] [115] Además, en términos de función, la membrana interna del cloroplasto, que regula el paso de metabolitos y sintetiza algunos materiales, no tiene equivalente en la mitocondria. [23]
La membrana externa del cloroplasto es una membrana semiporosa a través de la cual las moléculas pequeñas y los iones pueden difundirse fácilmente. [116] Sin embargo, no es permeable a proteínas más grandes, por lo que los polipéptidos del cloroplasto que se sintetizan en el citoplasma celular deben ser transportados a través de la membrana externa del cloroplasto por el complejo TOC , o translocón en la membrana externa del cloroplasto . [98]
Las membranas de los cloroplastos a veces sobresalen hacia el citoplasma, formando un estrómulo o un túbulo que contiene un estrómulo . Los estrómulos son muy raros en los cloroplastos, y son mucho más comunes en otros plástidos como los cromoplastos y amiloplastos en pétalos y raíces, respectivamente. [117] [118] Pueden existir para aumentar el área de superficie del cloroplasto para el transporte a través de la membrana, porque a menudo están ramificados y enredados con el retículo endoplasmático . [119] Cuando se observaron por primera vez en 1962, algunos biólogos vegetales descartaron las estructuras como artefactos, afirmando que los estrómulos eran simplemente cloroplastos de forma extraña con regiones constreñidas o cloroplastos en división . [120] Sin embargo, hay un creciente cuerpo de evidencia de que los estrómulos son características funcionales e integrales de los plástidos de las células vegetales, no simplemente artefactos. [121]

Generalmente, existe un espacio intermembrana delgado de unos 10 a 20 nanómetros de espesor entre las membranas externa e interna del cloroplasto. [122]
Los cloroplastos de las algas glaucófitas tienen una capa de peptidoglicano entre las membranas de los cloroplastos. Corresponde a la pared celular de peptidoglicano de sus ancestros cianobacterianos , que se encuentra entre sus dos membranas celulares. Estos cloroplastos se denominan muroplastos (del latín "mura" , que significa "pared"). Se suponía que otros cloroplastos habían perdido la pared de las cianobacterias, dejando un espacio intermembrana entre las dos membranas de la envoltura del cloroplasto, [23] pero desde entonces se ha encontrado también en musgos, licofitas y helechos. [123]
La membrana interna del cloroplasto limita el estroma y regula el paso de materiales hacia dentro y hacia fuera del cloroplasto. Después de pasar por el complejo TOC en la membrana externa del cloroplasto, los polipéptidos deben pasar por el complejo TIC ( translocón en la membrana interna del cloroplasto ) que se encuentra en la membrana interna del cloroplasto. [98]
Además de regular el paso de materiales, la membrana interna del cloroplasto es donde se sintetizan los ácidos grasos , los lípidos y los carotenoides . [23]
Algunos cloroplastos contienen una estructura llamada retículo periférico del cloroplasto . [122] A menudo se encuentra en los cloroplastos de las plantas C 4 , aunque también se ha encontrado en algunas angiospermas C 3 , [23] e incluso algunas gimnospermas . [124] El retículo periférico del cloroplasto consiste en un laberinto de tubos membranosos y vesículas continuas con la membrana interna del cloroplasto que se extiende hacia el líquido estromal interno del cloroplasto. Se cree que su propósito es aumentar el área de superficie del cloroplasto para el transporte a través de la membrana entre su estroma y el citoplasma celular . Las pequeñas vesículas observadas a veces pueden servir como vesículas de transporte para transportar material entre los tilacoides y el espacio intermembrana. [125]
El fluido acuoso , alcalino y rico en proteínas [23] , [115] dentro de la membrana interna del cloroplasto y fuera del espacio tilacoide se llama estroma, [23] que corresponde al citosol de la cianobacteria original . Los nucleoides del ADN del cloroplasto , los ribosomas del cloroplasto , el sistema tilacoide con plastoglobulinas , gránulos de almidón y muchas proteínas se pueden encontrar flotando en él. El ciclo de Calvin , que fija el CO 2 en G3P, tiene lugar en el estroma.
Los cloroplastos tienen sus propios ribosomas, que utilizan para sintetizar una pequeña fracción de sus proteínas. Los ribosomas de los cloroplastos tienen aproximadamente dos tercios del tamaño de los ribosomas citoplasmáticos (alrededor de 17 nm frente a 25 nm ). [122] Toman los ARNm transcritos del ADN del cloroplasto y los traducen en proteínas. Si bien son similares a los ribosomas bacterianos , [17] la traducción en los cloroplastos es más compleja que en las bacterias, por lo que los ribosomas de los cloroplastos incluyen algunas características exclusivas de los cloroplastos. [126] [127]
Los ARN ribosómicos de subunidades pequeñas en varios cloroplastos de Chlorophyta y euglenid carecen de motivos para el reconocimiento de la secuencia Shine-Dalgarno , [128] que se considera esencial para el inicio de la traducción en la mayoría de los cloroplastos y procariotas . [129] [130] Dicha pérdida también se observa raramente en otros plástidos y procariotas. [128] [131] Un ARNr 4.5S adicional con homología con la cola 3' de 23S se encuentra en plantas "superiores". [127]
Los plastoglobuli ( singular plastoglobulus , a veces escrito plastoglobule(s) ) son burbujas esféricas de lípidos y proteínas [23] de unos 45–60 nanómetros de diámetro. [132] Están rodeados por una monocapa lipídica. [132] Los plastoglobuli se encuentran en todos los cloroplastos, [122] pero se vuelven más comunes cuando el cloroplasto está bajo estrés oxidativo , [132] o cuando envejece y se transforma en un gerontoplasto . [23] Los plastoglobuli también exhiben una mayor variación de tamaño en estas condiciones. [132] También son comunes en los etioplastos , pero disminuyen en número a medida que los etioplastos maduran y se convierten en cloroplastos. [132]
Los plastoglobuli contienen proteínas estructurales y enzimas involucradas en la síntesis y el metabolismo de los lípidos . Contienen muchos tipos de lípidos , entre ellos plastoquinona , vitamina E , carotenoides y clorofilas . [132]
Antes se pensaba que los plastoglobulos flotaban libremente en el estroma , pero ahora se piensa que están permanentemente unidos a un tilacoide o a otro plastoglobulus unido a un tilacoide, una configuración que permite que un plastoglobulus intercambie su contenido con la red de tilacoide. [132] En los cloroplastos verdes normales, la gran mayoría de los plastoglobuli se presentan de forma singular, unidos directamente a su tilacoide original. En los cloroplastos viejos o estresados, los plastoglobuli tienden a presentarse en grupos o cadenas enlazadas, todavía siempre anclados a un tilacoide. [132]
Los plastoglobulos se forman cuando aparece una burbuja entre las capas de la bicapa lipídica de la membrana del tilacoide, o brotan de plastoglobulos existentes, aunque nunca se desprenden y flotan hacia el estroma. [132] Prácticamente todos los plastoglobulos se forman en los bordes muy curvados de los discos o láminas de los tilacoides o cerca de ellos. También son más comunes en los tilacoides del estroma que en los granulares . [132]

Los gránulos de almidón son muy comunes en los cloroplastos, y normalmente ocupan el 15% del volumen del orgánulo, [133] aunque en algunos otros plástidos como los amiloplastos , pueden ser lo suficientemente grandes como para distorsionar la forma del orgánulo. [122] Los gránulos de almidón son simplemente acumulaciones de almidón en el estroma y no están delimitados por una membrana. [122]
Los gránulos de almidón aparecen y crecen durante todo el día, a medida que el cloroplasto sintetiza azúcares , y se consumen durante la noche para alimentar la respiración y continuar la exportación de azúcar al floema , [134] aunque en los cloroplastos maduros, es raro que un gránulo de almidón se consuma completamente o que se acumule un nuevo gránulo. [133]
Los gránulos de almidón varían en composición y ubicación en los diferentes linajes de cloroplastos. En las algas rojas , los gránulos de almidón se encuentran en el citoplasma en lugar de en el cloroplasto. [135] En las plantas C 4 , los cloroplastos del mesófilo , que no sintetizan azúcares, carecen de gránulos de almidón. [23]
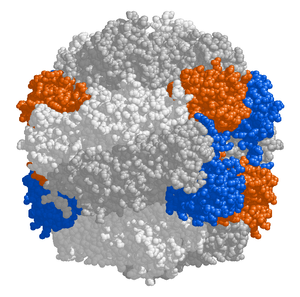
El estroma del cloroplasto contiene muchas proteínas, aunque la más común e importante es la RuBisCO , que probablemente también sea la proteína más abundante del planeta. [115] La RuBisCO es la enzima que fija el CO2 en moléculas de azúcar. En las plantas C3 , la RuBisCO es abundante en todos los cloroplastos, aunque en las plantas C4 , se limita a los cloroplastos de la vaina del haz , donde se lleva a cabo el ciclo de Calvin en las plantas C4 . [136]
Los cloroplastos de algunas antocerotas [137] y algas contienen estructuras llamadas pirenoides . No se encuentran en plantas superiores. [138] Los pirenoides son cuerpos aproximadamente esféricos y altamente refractarios que son un sitio de acumulación de almidón en las plantas que los contienen. Consisten en una matriz opaca a los electrones, rodeada por dos placas de almidón hemisféricas. El almidón se acumula a medida que maduran los pirenoides. [139] En algas con mecanismos de concentración de carbono , la enzima RuBisCO se encuentra en los pirenoides. El almidón también puede acumularse alrededor de los pirenoides cuando el CO 2 es escaso. [138] Los pirenoides pueden dividirse para formar nuevos pirenoides, o producirse "de novo" . [139] [140]

Los tilacoides (a veces escritos tilacoideos ) [142] son pequeños sacos interconectados que contienen las membranas en las que se producen las reacciones luminosas de la fotosíntesis. La palabra tilacoide proviene del griego thylakos , que significa "saco". [143]
Suspendido dentro del estroma del cloroplasto se encuentra el sistema tilacoidal , una colección altamente dinámica de sacos membranosos llamados tilacoides donde se encuentra la clorofila y ocurren las reacciones luminosas de la fotosíntesis . [11] En la mayoría de los cloroplastos de plantas vasculares , los tilacoides están dispuestos en pilas llamadas grana, [144] aunque en ciertos cloroplastos de plantas C 4 [136] y algunos cloroplastos de algas , los tilacoides flotan libremente. [12]

Usando un microscopio óptico , apenas es posible ver pequeños gránulos verdes, que fueron llamados grana . [122] Con la microscopía electrónica , se hizo posible ver el sistema tilacoidal con más detalle, revelando que consiste en pilas de tilacoides planos que formaban la grana, y largos tilacoides estromales interconectados que unían diferentes grana. [122] En el microscopio electrónico de transmisión , las membranas tilacoides aparecen como bandas alternas de luz y oscuridad, de 8,5 nanómetros de espesor. [122]
La estructura tridimensional del sistema de membranas tilacoidales ha sido objeto de debate. Se han propuesto muchos modelos, siendo el más frecuente el modelo helicoidal , en el que las pilas de tilacoides granum están envueltas por tilacoides estromales helicoidales. [145] Otro modelo conocido como "modelo de bifurcación", que se basó en el primer estudio de tomografía electrónica de las membranas tilacoides de las plantas, representa las membranas estromales como láminas lamelares anchas perpendiculares a las columnas granum que se bifurcan en múltiples discos paralelos que forman el conjunto granum-estroma. [146] El modelo helicoidal fue respaldado por varios trabajos adicionales, [144] [147] pero finalmente se determinó en 2019 que las características de los modelos helicoidal y de bifurcación se consolidan mediante uniones de membrana helicoidales zurdas recién descubiertas. [141] Probablemente para facilitar la comprensión, el sistema tilacoideo todavía se representa comúnmente mediante modelos más antiguos de "centro y radios" donde los grana están conectados entre sí por tubos de tilacoides estromales. [148]
Las granas consisten en pilas de tilacoides granulares circulares aplanados que se parecen a panqueques. Cada grana puede contener entre dos y cien tilacoides, [122] aunque las granas con 10-20 tilacoides son las más comunes. [144] Alrededor de las granas hay múltiples tilacoides estromales helicoidales dextrógiros paralelos, también conocidos como trastes o tilacoides lamelares. Las hélices ascienden en un ángulo de ~20°, conectándose a cada tilacoide granal en una unión de hendidura en forma de puente. [144] [147] [141]
Las láminas del estroma se extienden como grandes láminas perpendiculares a las columnas de grana. Estas láminas están conectadas a las hélices dextrógiras ya sea directamente o a través de bifurcaciones que forman superficies de membrana helicoidales levógiras. [141] Las superficies helicoidales levógiras tienen un ángulo de inclinación similar al de las hélices dextrógiras (~20°), pero ¼ del paso. Aproximadamente 4 uniones helicoidales levógiras están presentes por granum, lo que da como resultado una matriz equilibrada en el paso de superficies de membrana helicoidales dextrógiras e levógiras de diferentes radios y pasos que consolidan la red con energías mínimas de superficie y flexión. [141] Si bien las diferentes partes del sistema tilacoidal contienen diferentes proteínas de membrana, las membranas tilacoidales son continuas y el espacio tilacoide que encierran forma un único laberinto continuo. [144]
En las membranas tilacoidales se encuentran importantes complejos proteicos que llevan a cabo las reacciones luminosas de la fotosíntesis . El fotosistema II y el fotosistema I contienen complejos de captación de luz con clorofila y carotenoides que absorben la energía luminosa y la utilizan para energizar los electrones. Las moléculas de la membrana tilacoidal utilizan los electrones energizados para bombear iones de hidrógeno al espacio tilacoideo, lo que disminuye el pH y lo vuelve ácido. La ATP sintasa es un gran complejo proteico que aprovecha el gradiente de concentración de los iones de hidrógeno en el espacio tilacoideo para generar energía ATP a medida que los iones de hidrógeno fluyen de regreso al estroma, de manera muy similar a la turbina de una presa. [115]
Existen dos tipos de tilacoides: los tilacoides granales, que se disponen en grana, y los tilacoides estromales, que están en contacto con el estroma . Los tilacoides granales son discos circulares con forma de panqueque de unos 300 a 600 nanómetros de diámetro. Los tilacoides estromales son láminas helicoidales que giran en espiral alrededor de la grana. [144] Las partes superiores e inferiores planas de los tilacoides granales contienen solo el complejo proteico del fotosistema II relativamente plano . Esto les permite apilarse firmemente, formando grana con muchas capas de membrana fuertemente presionada, llamada membrana granal, lo que aumenta la estabilidad y el área de superficie para la captura de luz. [144]
En cambio, el fotosistema I y la ATP sintasa son grandes complejos proteicos que sobresalen hacia el estroma. No caben en las membranas granales adpresas, por lo que se encuentran en la membrana tilacoidal estromal (los bordes de los discos tilacoidales granales y los tilacoides estromales). Estos grandes complejos proteicos pueden actuar como espaciadores entre las láminas de tilacoides estromales. [144]
La cantidad de tilacoides y el área total de tilacoides de un cloroplasto se ven influenciados por la exposición a la luz. Los cloroplastos sombreados contienen grana más grande y en mayor cantidad , con una mayor área de membrana tilacoide que los cloroplastos expuestos a la luz brillante, que tienen grana más pequeña y en menor cantidad, y una menor área tilacoide. La extensión de los tilacoides puede cambiar en cuestión de minutos después de la exposición a la luz o de la eliminación de la misma. [125]
Dentro de los fotosistemas incrustados en las membranas tilacoides de los cloroplastos se encuentran diversos pigmentos fotosintéticos , que absorben y transfieren la energía de la luz . Los tipos de pigmentos que se encuentran son diferentes en varios grupos de cloroplastos, y son responsables de una amplia variedad de coloraciones de los cloroplastos. Otros tipos de plastidios , como el leucoplasto y el cromoplasto , contienen poca clorofila y no realizan la fotosíntesis.
La clorofila a se encuentra en todos los cloroplastos, así como en sus ancestros cianobacterianos . La clorofila a es un pigmento azul verdoso [149] parcialmente responsable de dar a la mayoría de las cianobacterias y cloroplastos su color. Existen otras formas de clorofila, como los pigmentos accesorios clorofila b , clorofila c , clorofila d , [12] y clorofila f .
La clorofila b es un pigmento verde oliva que se encuentra únicamente en los cloroplastos de las plantas , las algas verdes , cualquier cloroplasto secundario obtenido a través de la endosimbiosis secundaria de un alga verde y algunas cianobacterias . [12] Son las clorofilas a y b juntas las que hacen que la mayoría de los cloroplastos de las plantas y las algas verdes sean verdes. [149]
La clorofila c se encuentra principalmente en cloroplastos endosimbióticos secundarios que se originaron a partir de un alga roja , aunque no se encuentra en los cloroplastos de las propias algas rojas. La clorofila c también se encuentra en algunas algas verdes y cianobacterias . [12]
Las clorofilas d y f son pigmentos que se encuentran sólo en algunas cianobacterias. [12] [150]
![Delesseria sanguinea, un alga roja, tiene cloroplastos que contienen pigmentos rojos como la ficoeriterina que enmascaran su clorofila a azul verdosa.[39]](http://upload.wikimedia.org/wikipedia/commons/thumb/1/19/Delesseria_sanguinea_Helgoland.JPG/440px-Delesseria_sanguinea_Helgoland.JPG)
Además de las clorofilas, en los fotosistemas también se encuentran otro grupo de pigmentos de color amarillo anaranjado [149] llamados carotenoides . Hay unos treinta carotenoides fotosintéticos [151] . Ayudan a transferir y disipar el exceso de energía [12] y sus colores brillantes a veces anulan el verde de la clorofila, como durante el otoño , cuando las hojas de algunas plantas terrestres cambian de color. [152] El β-caroteno es un carotenoide rojo anaranjado brillante que se encuentra en casi todos los cloroplastos, como la clorofila a [12] Las xantofilas , especialmente la zeaxantina de color rojo anaranjado , también son comunes [151] Existen muchas otras formas de carotenoides que solo se encuentran en ciertos grupos de cloroplastos [12]
Las ficobilinas son un tercer grupo de pigmentos que se encuentran en las cianobacterias y en los cloroplastos de las glaucofitas , las algas rojas y las criptofitas . [12] [153] Las ficobilinas vienen en todos los colores, aunque la ficoeriterina es uno de los pigmentos que hace que muchas algas rojas sean rojas. [154] Las ficobilinas a menudo se organizan en complejos proteicos relativamente grandes de unos 40 nanómetros de diámetro llamados ficobilisomas . [12] Al igual que el fotosistema I y la ATP sintasa , los ficobilisomas sobresalen del estroma, evitando el apilamiento de tilacoides en los cloroplastos de las algas rojas. [12] Los cloroplastos de las criptofitas y algunas cianobacterias no tienen sus pigmentos de ficobilina organizados en ficobilisomas, y los mantienen en su espacio tilacoide. [12]
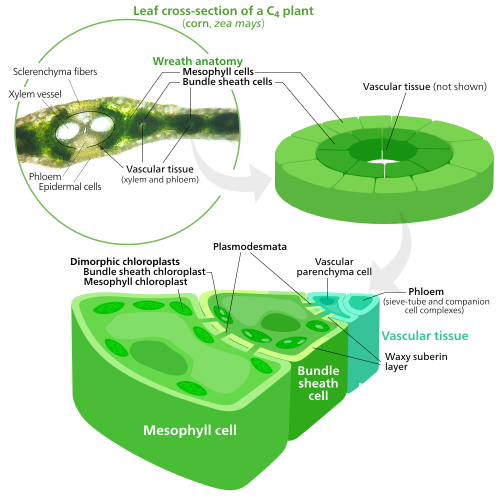
Para fijar el dióxido de carbono en moléculas de azúcar en el proceso de fotosíntesis , los cloroplastos utilizan una enzima llamada RuBisCO . RuBisCO tiene problemas para distinguir entre dióxido de carbono y oxígeno , por lo que en altas concentraciones de oxígeno, RuBisCO comienza a agregar oxígeno accidentalmente a los precursores de azúcar. Esto tiene como resultado que se desperdicie energía ATP y se libere CO2 , todo sin que se produzca azúcar. Este es un gran problema, ya que el O2 se produce por las reacciones luminosas iniciales de la fotosíntesis, lo que causa problemas más adelante en el ciclo de Calvin que utiliza RuBisCO. [155]
Las plantas C4 desarrollaron una forma de resolver esto: separando espacialmente las reacciones luminosas y el ciclo de Calvin. Las reacciones luminosas, que almacenan energía luminosa en ATP y NADPH , se realizan en las células del mesófilo de una hoja C4 . El ciclo de Calvin, que utiliza la energía almacenada para producir azúcar utilizando RuBisCO, se realiza en las células de la vaina del haz , una capa de células que rodea una vena en una hoja . [155]
Como resultado, los cloroplastos en las células del mesófilo C 4 y las células de la vaina del haz están especializados para cada etapa de la fotosíntesis. En las células del mesófilo, los cloroplastos están especializados para las reacciones de luz, por lo que carecen de RuBisCO , y tienen grana y tilacoides normales , [136] que utilizan para producir ATP y NADPH, así como oxígeno. Almacenan CO 2 en un compuesto de cuatro carbonos, por lo que el proceso se llama fotosíntesis C 4 . El compuesto de cuatro carbonos luego se transporta a los cloroplastos de la vaina del haz, donde deja caer CO 2 y regresa al mesófilo. Los cloroplastos de la vaina del haz no llevan a cabo las reacciones de luz, lo que evita que el oxígeno se acumule en ellos e interrumpe la actividad de RuBisCO. [155] Debido a esto, carecen de tilacoides organizados en pilas de grana , aunque los cloroplastos de la vaina del haz aún tienen tilacoides flotando libremente en el estroma donde aún llevan a cabo el flujo cíclico de electrones , un método impulsado por la luz para sintetizar ATP para impulsar el ciclo de Calvin sin generar oxígeno. Carecen del fotosistema II y solo tienen el fotosistema I , el único complejo proteico necesario para el flujo cíclico de electrones. [136] [155] Debido a que el trabajo de los cloroplastos de la vaina del haz es llevar a cabo el ciclo de Calvin y producir azúcar, a menudo contienen grandes granos de almidón . [136]
Ambos tipos de cloroplastos contienen grandes cantidades de retículo periférico de cloroplasto , [136] que utilizan para obtener más área de superficie para transportar material dentro y fuera de ellos. [124] [125] Los cloroplastos del mesófilo tienen un poco más de retículo periférico que los cloroplastos de la vaina del haz. [156]
A diferencia de la mayoría de las células epidérmicas, las células guardianas de los estomas de las plantas contienen cloroplastos relativamente bien desarrollados. [157] Sin embargo, lo que hacen exactamente es controvertido. [158]
Las plantas carecen de células inmunitarias especializadas : todas las células vegetales participan en la respuesta inmunitaria de la planta . Los cloroplastos, junto con el núcleo , la membrana celular y el retículo endoplasmático [159] son actores clave en la defensa contra los patógenos . Debido a su papel en la respuesta inmunitaria de una célula vegetal, los patógenos con frecuencia atacan al cloroplasto. [159]
Las plantas tienen dos respuestas inmunes principales: la respuesta hipersensible , en la que las células infectadas se aíslan y experimentan una muerte celular programada , y la resistencia sistémica adquirida , en la que las células infectadas liberan señales que advierten al resto de la planta de la presencia de un patógeno. Los cloroplastos estimulan ambas respuestas dañando deliberadamente su sistema fotosintético, produciendo especies reactivas de oxígeno . Los niveles altos de especies reactivas de oxígeno causarán la respuesta hipersensible . Las especies reactivas de oxígeno también matan directamente a cualquier patógeno dentro de la célula. Los niveles más bajos de especies reactivas de oxígeno inician la resistencia sistémica adquirida , lo que desencadena la producción de moléculas de defensa en el resto de la planta. [159]
Se sabe que en algunas plantas los cloroplastos se acercan al sitio de la infección y al núcleo durante una infección. [159]
Los cloroplastos pueden actuar como sensores celulares. Tras detectar estrés en una célula, que puede deberse a un patógeno, los cloroplastos comienzan a producir moléculas como ácido salicílico , ácido jasmónico , óxido nítrico y especies reactivas de oxígeno que pueden actuar como señales de defensa. Como señales celulares, las especies reactivas de oxígeno son moléculas inestables, por lo que probablemente no abandonen el cloroplasto, sino que transmitan su señal a una molécula mensajera desconocida. Todas estas moléculas inician una señalización retrógrada : señales del cloroplasto que regulan la expresión génica en el núcleo. [159]
Además de la señalización de defensa, los cloroplastos, con la ayuda de los peroxisomas , [160] ayudan a sintetizar una importante molécula de defensa, el jasmonato . Los cloroplastos sintetizan todos los ácidos grasos de una célula vegetal [159] [161] — el ácido linoleico , un ácido graso, es un precursor del jasmonato. [159]
Una de las principales funciones del cloroplasto es su papel en la fotosíntesis , proceso por el cual la luz se transforma en energía química, para posteriormente producir alimentos en forma de azúcares . En la fotosíntesis se utilizan agua (H 2 O) y dióxido de carbono (CO 2 ), y se fabrican azúcar y oxígeno (O 2 ), utilizando la energía de la luz . La fotosíntesis se divide en dos etapas: las reacciones luminosas , donde el agua se divide para producir oxígeno, y las reacciones oscuras , o ciclo de Calvin , que construye moléculas de azúcar a partir del dióxido de carbono. Las dos fases están unidas por los portadores de energía trifosfato de adenosina (ATP) y fosfato de dinucleótido de nicotinamida y adenina (NADP + ). [162] [163]

Las reacciones luminosas tienen lugar en las membranas de los tilacoides, que captan la energía luminosa y la almacenan en NADPH , una forma de NADP + , y ATP para alimentar las reacciones oscuras .
El ATP es la versión fosforilada del difosfato de adenosina (ADP), que almacena energía en una célula y potencia la mayoría de las actividades celulares. El ATP es la forma energizada, mientras que el ADP es la forma (parcialmente) agotada. El NADP + es un transportador de electrones que transporta electrones de alta energía. En las reacciones luminosas, se reduce , lo que significa que recoge electrones y se convierte en NADPH .
Al igual que las mitocondrias, los cloroplastos utilizan la energía potencial almacenada en un gradiente de H + , o iones de hidrógeno, para generar energía ATP. Los dos fotosistemas capturan la energía de la luz para energizar los electrones tomados del agua y los liberan por una cadena de transporte de electrones . Las moléculas entre los fotosistemas aprovechan la energía de los electrones para bombear iones de hidrógeno al espacio tilacoide, creando un gradiente de concentración , con más iones de hidrógeno (hasta mil veces más) [115] dentro del sistema tilacoide que en el estroma. Los iones de hidrógeno en el espacio tilacoide luego se difunden de regreso a lo largo de su gradiente de concentración, fluyendo de regreso hacia el estroma a través de la ATP sintasa . La ATP sintasa utiliza la energía de los iones de hidrógeno que fluyen para fosforilar el difosfato de adenosina en trifosfato de adenosina o ATP. [115] [164] Debido a que la ATP sintasa del cloroplasto se proyecta hacia el estroma, el ATP se sintetiza allí, en posición de ser utilizado en las reacciones oscuras. [165]
A menudo, se eliminan electrones de las cadenas de transporte de electrones para cargar el NADP + con electrones, reduciéndolo a NADPH . Al igual que la ATP sintasa, la ferredoxina-NADP + reductasa , la enzima que reduce el NADP + , libera el NADPH que produce en el estroma, justo donde se necesita para las reacciones oscuras. [165]
Debido a que la reducción de NADP + elimina electrones de las cadenas de transporte de electrones, estos deben ser reemplazados (el trabajo del fotosistema II , que divide las moléculas de agua (H 2 O) para obtener los electrones de sus átomos de hidrógeno ). [115] [162]
Mientras que el fotosistema II fotoliza el agua para obtener y energizar nuevos electrones, el fotosistema I simplemente reenergiza los electrones agotados al final de una cadena de transporte de electrones. Normalmente, los electrones reenergizados son tomados por NADP + , aunque a veces pueden fluir de regreso por más cadenas de transporte de electrones que bombean H + para transportar más iones de hidrógeno al espacio tilacoide para generar más ATP. Esto se denomina fotofosforilación cíclica porque los electrones se reciclan. La fotofosforilación cíclica es común en las plantas C4 , que necesitan más ATP que NADPH . [155]
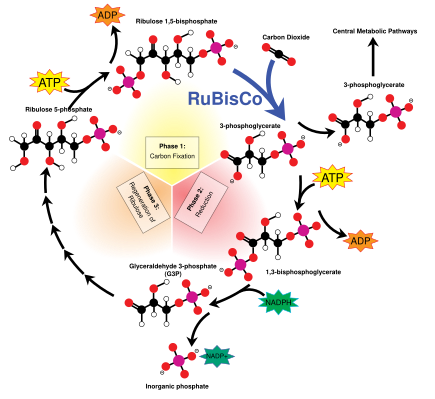
El ciclo de Calvin , también conocido como reacciones oscuras , es una serie de reacciones bioquímicas que fijan el CO2 en moléculas de azúcar G3P y utilizan la energía y los electrones del ATP y el NADPH producidos en las reacciones luminosas. El ciclo de Calvin tiene lugar en el estroma del cloroplasto. [155]
Aunque se denominan "reacciones oscuras" , en la mayoría de las plantas tienen lugar en la luz, ya que las reacciones oscuras dependen de los productos de las reacciones luminosas. [11]
El ciclo de Calvin comienza con el uso de la enzima RuBisCO para fijar el CO2 en moléculas de ribulosa bisfosfato (RuBP) de cinco carbonos. El resultado son moléculas inestables de seis carbonos que se descomponen inmediatamente en moléculas de tres carbonos llamadas ácido 3-fosfoglicérico o 3-PGA. El ATP y el NADPH producidos en las reacciones luminosas se utilizan para convertir el 3-PGA en gliceraldehído-3-fosfato o moléculas de azúcar G3P. La mayoría de las moléculas de G3P se reciclan de nuevo en RuBP utilizando energía de más ATP, pero una de cada seis producidas abandona el ciclo: el producto final de las reacciones oscuras. [155]

El gliceraldehído-3-fosfato puede duplicarse para formar moléculas de azúcar más grandes, como la glucosa y la fructosa . Estas moléculas se procesan y, a partir de ellas, se forma la sacarosa , un disacárido conocido comúnmente como azúcar de mesa, de mayor tamaño, aunque este proceso tiene lugar fuera del cloroplasto, en el citoplasma . [166]
Alternativamente, los monómeros de glucosa en el cloroplasto pueden unirse para formar almidón , que se acumula en los granos de almidón que se encuentran en el cloroplasto. [166] En condiciones como altas concentraciones atmosféricas de CO2 , estos granos de almidón pueden crecer mucho, distorsionando los granos y los tilacoides. Los gránulos de almidón desplazan a los tilacoides, pero los dejan intactos. [167] Las raíces anegadas también pueden causar la acumulación de almidón en los cloroplastos, posiblemente debido a que se exporta menos sacarosa fuera del cloroplasto (o más exactamente, de la célula vegetal ). Esto agota el suministro de fosfato libre de una planta , lo que estimula indirectamente la síntesis de almidón del cloroplasto. [167] Si bien están vinculados a bajas tasas de fotosíntesis, los granos de almidón en sí mismos pueden no interferir necesariamente de manera significativa con la eficiencia de la fotosíntesis, [168] y podrían ser simplemente un efecto secundario de otro factor que deprime la fotosíntesis. [167]
La fotorrespiración puede ocurrir cuando la concentración de oxígeno es demasiado alta. RuBisCO no puede distinguir muy bien entre oxígeno y dióxido de carbono, por lo que puede agregar accidentalmente O 2 en lugar de CO 2 a RuBP . Este proceso reduce la eficiencia de la fotosíntesis: consume ATP y oxígeno, libera CO 2 y no produce azúcar. Puede desperdiciar hasta la mitad del carbono fijado por el ciclo de Calvin. [162] Varios mecanismos han evolucionado en diferentes linajes que aumentan la concentración de dióxido de carbono en relación con el oxígeno dentro del cloroplasto, lo que aumenta la eficiencia de la fotosíntesis. Estos mecanismos se denominan mecanismos de concentración de dióxido de carbono o CCM. Estos incluyen el metabolismo ácido de las crasuláceas , la fijación de carbono C 4 , [162] y los pirenoides . Los cloroplastos en las plantas C 4 son notables ya que exhiben un dimorfismo de cloroplasto distintivo.
Debido al gradiente de H + a través de la membrana del tilacoide, el interior del tilacoide es ácido , con un pH de alrededor de 4, [169] mientras que el estroma es ligeramente básico, con un pH de alrededor de 8. [170] El pH óptimo del estroma para el ciclo de Calvin es 8,1, y la reacción casi se detiene cuando el pH cae por debajo de 7,3. [171]
El CO2 en el agua puede formar ácido carbónico , que puede alterar el pH de los cloroplastos aislados, interfiriendo con la fotosíntesis, aunque el CO2 se utiliza en la fotosíntesis. Sin embargo, los cloroplastos en las células vegetales vivas no se ven tan afectados por esto. [170]
Los cloroplastos pueden bombear iones K + y H + dentro y fuera de sí mismos utilizando un sistema de transporte impulsado por luz poco conocido. [170]
En presencia de luz, el pH del lumen del tilacoide puede caer hasta 1,5 unidades de pH, mientras que el pH del estroma puede aumentar casi una unidad de pH. [171]
Los cloroplastos por sí solos producen casi todos los aminoácidos de una célula vegetal en su estroma [172] excepto los que contienen azufre como la cisteína y la metionina . [173] [174] La cisteína se produce en el cloroplasto (también en el proplástido ), pero también se sintetiza en el citosol y las mitocondrias , probablemente porque tiene problemas para cruzar las membranas para llegar a donde se necesita. [174] Se sabe que el cloroplasto produce los precursores de la metionina, pero no está claro si el orgánulo lleva a cabo la última etapa de la vía o si ocurre en el citosol . [175]
Los cloroplastos producen todas las purinas y pirimidinas de una célula (las bases nitrogenadas que se encuentran en el ADN y el ARN) . [172] También convierten el nitrito (NO 2 − ) en amoníaco (NH 3 ), que proporciona a la planta nitrógeno para producir sus aminoácidos y nucleótidos . [172]
El plástido es el sitio de síntesis lipídica diversa y compleja en las plantas. [176] [177] El carbono utilizado para formar la mayoría del lípido proviene del acetil-CoA , que es el producto de descarboxilación del piruvato . [176] El piruvato puede ingresar al plástido desde el citosol por difusión pasiva a través de la membrana después de la producción en la glucólisis . [178] El piruvato también se produce en el plástido a partir del fosfoenolpiruvato, un metabolito producido en el citosol a partir del piruvato o PGA . [176] El acetato en el citosol no está disponible para la biosíntesis de lípidos en el plástido. [179] La longitud típica de los ácidos grasos producidos en el plástido son 16 o 18 carbonos, con 0-3 dobles enlaces cis . [180]
La biosíntesis de ácidos grasos a partir de acetil-CoA requiere principalmente dos enzimas. La acetil-CoA carboxilasa crea malonil-CoA, que se utiliza tanto en el primer paso como en los pasos de extensión de la síntesis. La sintetasa de ácidos grasos (FAS) es un gran complejo de enzimas y cofactores que incluye la proteína transportadora de acilo (ACP) que sostiene la cadena de acilo a medida que se sintetiza. El inicio de la síntesis comienza con la condensación de malonil-ACP con acetil-CoA para producir cetobutiril-ACP. Dos reducciones que implican el uso de NADPH y una deshidratación crean butiril-ACP. La extensión del ácido graso proviene de ciclos repetidos de condensación, reducción y deshidratación de malonil-ACP. [176]
Otros lípidos se derivan de la vía del metil-eritritol fosfato (MEP) y consisten en giberelinas , esteroles , ácido abscísico , fitol e innumerables metabolitos secundarios . [176]

No todas las células de una planta multicelular contienen cloroplastos. Todas las partes verdes de una planta contienen cloroplastos, ya que el color proviene de la clorofila . [11] Las células vegetales que contienen cloroplastos son generalmente células del parénquima , aunque también se pueden encontrar cloroplastos en el tejido del colénquima . [181] Una célula vegetal que contiene cloroplastos se conoce como célula de clorénquima . Una célula de clorénquima típica de una planta terrestre contiene alrededor de 10 a 100 cloroplastos.
En algunas plantas como los cactus , los cloroplastos se encuentran en los tallos , [182] aunque en la mayoría de las plantas, los cloroplastos se concentran en las hojas . Un milímetro cuadrado de tejido foliar puede contener medio millón de cloroplastos. [11] Dentro de una hoja, los cloroplastos se encuentran principalmente en las capas del mesófilo de una hoja y en las células de guarda de los estomas . Las células del mesófilo en empalizada pueden contener entre 30 y 70 cloroplastos por célula, mientras que las células de guarda de los estomas contienen solo alrededor de 8 a 15 por célula, así como mucha menos clorofila . Los cloroplastos también se pueden encontrar en las células de la vaina del haz de una hoja, especialmente en las plantas C 4 , que llevan a cabo el ciclo de Calvin en sus células de la vaina del haz. A menudo están ausentes de la epidermis de una hoja. [157]
Los cloroplastos de las células de las plantas y las algas pueden orientarse para adaptarse mejor a la luz disponible. En condiciones de poca luz, se extienden formando una lámina, maximizando la superficie para absorber la luz. En condiciones de luz intensa, buscan refugio alineándose en columnas verticales a lo largo de la pared celular de la célula vegetal o girándose hacia los lados para que la luz los golpee de canto. Esto reduce la exposición y los protege del daño fotooxidativo. [183] Esta capacidad de distribuir los cloroplastos de modo que puedan refugiarse unos detrás de otros o extenderse puede ser la razón por la que las plantas terrestres evolucionaron para tener muchos cloroplastos pequeños en lugar de unos pocos grandes. [184] El movimiento de los cloroplastos se considera uno de los sistemas de estímulo-respuesta más estrechamente regulados que se pueden encontrar en las plantas. [185] También se ha observado que las mitocondrias siguen a los cloroplastos mientras se mueven. [186]
En las plantas superiores, el movimiento de los cloroplastos está controlado por las fototropinas , fotorreceptores de luz azul también responsables del fototropismo de las plantas . En algunas algas, musgos , helechos y plantas con flores , el movimiento de los cloroplastos está influenciado por la luz roja además de la luz azul, [183] aunque las longitudes de onda rojas muy largas inhiben el movimiento en lugar de acelerarlo. La luz azul generalmente hace que los cloroplastos busquen refugio, mientras que la luz roja los atrae para maximizar la absorción de luz. [186]
Los estudios de Vallisneria gigantea , una planta acuática con flores , han demostrado que los cloroplastos pueden empezar a moverse cinco minutos después de la exposición a la luz, aunque inicialmente no muestran ninguna direccionalidad neta. Pueden moverse a lo largo de pistas de microfilamentos , y el hecho de que la malla de microfilamentos cambie de forma para formar una estructura de panal que rodea a los cloroplastos después de que se hayan movido sugiere que los microfilamentos pueden ayudar a anclar los cloroplastos en su lugar. [185] [186]
Los cloroplastos son un tipo especial de orgánulo celular vegetal llamado plástido , aunque a veces ambos términos se usan indistintamente. Existen muchos otros tipos de plástidos, que llevan a cabo diversas funciones. Todos los cloroplastos de una planta descienden de proplástidos indiferenciados que se encuentran en el cigoto [172] o en el óvulo fertilizado. Los proplástidos se encuentran comúnmente en los meristemos apicales de una planta adulta . Los cloroplastos normalmente no se desarrollan a partir de proplástidos en los meristemos de la punta de la raíz [187] —en cambio, es más común la formación de amiloplastos que almacenan almidón . [172]
En los brotes , los proplástidos de los meristemos apicales de los brotes pueden convertirse gradualmente en cloroplastos en los tejidos fotosintéticos de las hojas a medida que la hoja madura, si se expone a la luz necesaria. [15] Este proceso implica invaginaciones de la membrana interna del plástido, formando láminas de membrana que se proyectan hacia el estroma interno . Estas láminas de membrana luego se pliegan para formar tilacoides y grana . [188]
Si los brotes de las angiospermas no se exponen a la luz necesaria para la formación de cloroplastos, los proplástidos pueden desarrollarse hasta una etapa de etioplasto antes de convertirse en cloroplastos. Un etioplasto es un plástido que carece de clorofila y tiene invaginaciones en la membrana interna que forman una red de tubos en su estroma, llamada cuerpo prolamelar . Si bien los etioplastos carecen de clorofila, tienen almacenado un precursor de clorofila amarilla . [15] A los pocos minutos de exposición a la luz, el cuerpo prolamelar comienza a reorganizarse en pilas de tilacoides y comienza a producirse clorofila. Este proceso, en el que el etioplasto se convierte en cloroplasto, lleva varias horas. [188] Las gimnospermas no requieren luz para formar cloroplastos. [188]
Sin embargo, la luz no garantiza que un proplástido se convierta en un cloroplasto. El hecho de que un proplástido se convierta en un cloroplasto o en otro tipo de plástido depende en gran medida del núcleo [15] y del tipo de célula en la que reside. [172]
La diferenciación de los plastidios no es permanente, de hecho, son posibles muchas interconversiones. Los cloroplastos pueden convertirse en cromoplastos , que son plastidios llenos de pigmento responsables de los colores brillantes que se ven en las flores y la fruta madura . Los amiloplastos que almacenan almidón también pueden convertirse en cromoplastos, y es posible que los proplástidos se desarrollen directamente en cromoplastos. Los cromoplastos y amiloplastos también pueden convertirse en cloroplastos, como lo que sucede cuando se ilumina una zanahoria o una papa . Si una planta se lesiona, o algo más hace que una célula vegetal vuelva a un estado meristemático , los cloroplastos y otros plastidios pueden volver a convertirse en proplástidos. El cloroplasto, el amiloplasto, el cromoplasto y el proplástido no son absolutos; las formas intermedias de estado son comunes. [172]
La mayoría de los cloroplastos en una célula fotosintética no se desarrollan directamente a partir de proplastidios o etioplastos. De hecho, una célula vegetal meristemática típica de un brote contiene solo entre 7 y 20 proplastidios . Estos proplastidios se diferencian en cloroplastos, que se dividen para crear los 30 a 70 cloroplastos que se encuentran en una célula vegetal fotosintética madura. Si la célula se divide , la división de cloroplastos proporciona los cloroplastos adicionales para repartirse entre las dos células hijas. [189]
En las algas unicelulares , la división de cloroplastos es la única forma de formar nuevos cloroplastos. No hay diferenciación de proplástidos: cuando una célula de alga se divide, su cloroplasto se divide junto con ella y cada célula hija recibe un cloroplasto maduro. [188]
Casi todos los cloroplastos de una célula se dividen, en lugar de un pequeño grupo de cloroplastos que se dividen rápidamente. [190] Los cloroplastos no tienen una fase S definida : su replicación de ADN no está sincronizada ni limitada a la de sus células huésped. [191] Gran parte de lo que sabemos sobre la división de cloroplastos proviene del estudio de organismos como Arabidopsis y el alga roja Cyanidioschyzon merolæ . [184]
![La mayoría de los cloroplastos en las células vegetales y todos los cloroplastos en las algas surgen de la división de cloroplastos.[188] Referencias de imágenes,[184][192]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/df/Chloroplast_division.svg/800px-Chloroplast_division.svg.png)
El proceso de división comienza cuando las proteínas FtsZ1 y FtsZ2 se ensamblan en filamentos y, con la ayuda de una proteína ARC6, forman una estructura llamada anillo Z dentro del estroma del cloroplasto. [184] [192] El sistema Min gestiona la colocación del anillo Z, asegurando que el cloroplasto se escinda más o menos uniformemente. La proteína MinD evita que FtsZ se una y forme filamentos. Otra proteína ARC3 también puede estar involucrada, pero no se entiende muy bien. Estas proteínas son activas en los polos del cloroplasto, evitando la formación del anillo Z allí, pero cerca del centro del cloroplasto, MinE las inhibe, permitiendo que se forme el anillo Z. [184]
A continuación, se forman los dos anillos divisores de plástidos, o anillos PD. El anillo divisor de plástidos interno se encuentra en el lado interno de la membrana interna del cloroplasto y se forma primero. [184] El anillo divisor de plástidos externo se encuentra envuelto alrededor de la membrana externa del cloroplasto. Consiste en filamentos de aproximadamente 5 nanómetros de ancho, [184] dispuestos en filas separadas por 6,4 nanómetros, y se encoge para comprimir el cloroplasto. Aquí es cuando comienza la constricción del cloroplasto. [192]
En algunas especies como Cyanidioschyzon merolæ , los cloroplastos tienen un tercer anillo divisor de plástidos ubicado en el espacio intermembrana del cloroplasto. [184] [192]
En etapas avanzadas de la fase de constricción, las proteínas dinamina se reúnen alrededor del anillo divisor externo del plástido, [192] lo que ayuda a proporcionar fuerza para comprimir el cloroplasto. [184] Mientras tanto, el anillo Z y el anillo divisor interno del plástido se descomponen. [192] Durante esta etapa, los numerosos plásmidos de ADN del cloroplasto que flotan en el estroma se dividen y se distribuyen entre los dos cloroplastos hijos en formación. [193]
Más tarde, las dinaminas migran debajo del anillo divisor externo del plástido, en contacto directo con la membrana externa del cloroplasto, [192] para dividir el cloroplasto en dos cloroplastos hijos. [184]
Un resto del anillo divisor externo del plástido permanece flotando entre los dos cloroplastos hijos, y un resto del anillo de dinamina permanece unido a uno de los cloroplastos hijos. [192]
De los cinco o seis anillos involucrados en la división del cloroplasto, solo el anillo divisor externo del plástido está presente durante toda la fase de constricción y división; si bien el anillo Z se forma primero, la constricción no comienza hasta que se forma el anillo divisor externo del plástido. [192]


En las especies de algas que contienen un solo cloroplasto, la regulación de la división de cloroplastos es extremadamente importante para garantizar que cada célula hija reciba un cloroplasto (los cloroplastos no pueden crearse desde cero). [86] [184] En organismos como las plantas, cuyas células contienen múltiples cloroplastos, la coordinación es más laxa y menos importante. Es probable que la división celular y de cloroplastos esté algo sincronizada, aunque los mecanismos para ello son en su mayoría desconocidos. [184]
Se ha demostrado que la luz es un requisito para la división de los cloroplastos. Los cloroplastos pueden crecer y progresar a través de algunas de las etapas de constricción bajo luz verde de mala calidad , pero son lentos para completar la división: requieren exposición a luz blanca brillante para completar la división. Se ha observado que las hojas de espinaca cultivadas bajo luz verde contienen muchos cloroplastos grandes con forma de mancuerna. La exposición a la luz blanca puede estimular la división de estos cloroplastos y reducir la población de cloroplastos con forma de mancuerna. [190] [193]
Al igual que las mitocondrias , los cloroplastos suelen heredarse de un solo progenitor. La herencia biparental de los cloroplastos (en la que los genes de los plástidos se heredan de ambas plantas progenitoras) se da en niveles muy bajos en algunas plantas con flores. [194]
Existen muchos mecanismos que impiden la herencia del ADN de los cloroplastos biparentales, entre ellos la destrucción selectiva de los cloroplastos o sus genes dentro del gameto o cigoto , y la exclusión de los cloroplastos de uno de los padres del embrión. Los cloroplastos parentales pueden clasificarse de modo que solo un tipo esté presente en cada descendencia. [195]
Las gimnospermas , como los pinos , suelen transmitir los cloroplastos por vía paterna, [196] mientras que las plantas con flores suelen heredar los cloroplastos por vía materna. [197] [198] Antes se creía que las plantas con flores solo heredaban los cloroplastos por vía materna. Sin embargo, ahora hay muchos casos documentados de angiospermas que heredan los cloroplastos por vía paterna. [194]
Las angiospermas , que transmiten los cloroplastos por vía materna, tienen muchas formas de evitar la herencia paterna. La mayoría de ellas producen espermatozoides que no contienen ningún plástido. Existen muchos otros mecanismos documentados que impiden la herencia paterna en estas plantas con flores, como las diferentes tasas de replicación de los cloroplastos dentro del embrión. [194]
Entre las angiospermas, la herencia paterna de cloroplastos se observa con mayor frecuencia en híbridos que en descendientes de progenitores de la misma especie. Esto sugiere que los genes híbridos incompatibles podrían interferir con los mecanismos que impiden la herencia paterna. [194]
Recientemente, los cloroplastos han llamado la atención de los desarrolladores de cultivos modificados genéticamente . Dado que, en la mayoría de las plantas con flores, los cloroplastos no se heredan del progenitor masculino, los transgenes en estos plástidos no pueden diseminarse por el polen . Esto hace que la transformación de plástidos sea una herramienta valiosa para la creación y el cultivo de plantas modificadas genéticamente que están biológicamente contenidas, lo que plantea riesgos ambientales significativamente menores. Por lo tanto, esta estrategia de contención biológica es adecuada para establecer la coexistencia de la agricultura convencional y orgánica . Si bien la confiabilidad de este mecanismo aún no se ha estudiado para todas las especies de cultivos relevantes, los resultados recientes en plantas de tabaco son prometedores, mostrando una tasa de contención fallida de plantas transplastómicas de 3 en 1.000.000. [198]
número de copias de ctDNA por cloroplasto.
En los pinos, el genoma del cloroplasto se transmite a través del polen.