La colina ( / ˈ k oʊ l iː n / KOH -leen ) [4] es un nutriente esencial para los humanos y muchos otros animales, que anteriormente se clasificaba como vitamina B ( vitamina B4 ). [5] [6] Es una parte estructural de los fosfolípidos y un donante de metilo en la química metabólica de un carbono. El compuesto está relacionado con la trimetilglicina en este último aspecto. Es un catión con la fórmula química [(CH 3 ) 3 NCH 2 CH 2 OH] + . La colina forma diversas sales , por ejemplo cloruro de colina y bitartrato de colina .
La colina es un catión de amonio cuaternario . Las colinas son una familia de compuestos de amonio cuaternario solubles en agua . [6] [7] La colina es el compuesto original de la clase de colinas, que consiste en un residuo de etanolamina que tiene tres grupos metilo unidos al mismo átomo de nitrógeno . [1] El hidróxido de colina se conoce como base de colina. Es higroscópico y, por lo tanto, a menudo se encuentra como un jarabe hidratado viscoso incoloro que huele a trimetilamina (TMA). Las soluciones acuosas de colina son estables, pero el compuesto se descompone lentamente en etilenglicol , polietilenglicoles y TMA. [2]
El cloruro de colina se puede producir tratando TMA con 2-cloroetanol : [2]
El 2-cloroetanol se puede generar a partir de óxido de etileno . [ ¿ cómo? ] Históricamente, la colina se ha producido a partir de fuentes naturales, como mediante la hidrólisis de la lecitina . [2]
La colina está muy extendida en la naturaleza entre los seres vivos. En la mayoría de los animales, los fosfolípidos de colina son componentes necesarios en las membranas celulares , en las membranas de los orgánulos celulares y en las lipoproteínas de muy baja densidad . [5]
La colina es un nutriente esencial para los humanos y muchos otros animales. [5] [6] Los seres humanos son capaces de realizar cierta síntesis de novo de colina, pero requieren colina adicional en la dieta para mantener la salud. Las necesidades dietéticas pueden cubrirse con colina sola o en forma de fosfolípidos de colina , como la fosfatidilcolina . [5] La colina no está clasificada formalmente como una vitamina a pesar de ser un nutriente esencial con una estructura y un metabolismo similares a los de los aminoácidos . [3]
Se necesita colina para producir acetilcolina , un neurotransmisor , y S -adenosilmetionina (SAM), un donante universal de metilo . Tras la metilación, SAM se transforma en S-adenosil homocisteína . [5]
La deficiencia sintomática de colina causa enfermedad del hígado graso no alcohólico y daño muscular. [5] El consumo excesivo de colina (más de 7,5 gramos por día) puede causar presión arterial baja , sudoración , diarrea y olor corporal a pescado debido a la trimetilamina , que se forma en el metabolismo de la colina. [5] [8] Las fuentes dietéticas ricas en colina y fosfolípidos de colina incluyen vísceras , yemas de huevo , productos lácteos , maní , ciertos frijoles , nueces y semillas . Las verduras con pasta y arroz también contribuyen a la ingesta de colina en la dieta estadounidense . [5] [9]
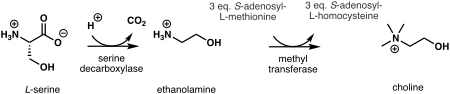
En las plantas, el primer paso en la biosíntesis de novo de colina es la descarboxilación de serina en etanolamina , que es catalizada por una serina descarboxilasa . [10] La síntesis de colina a partir de etanolamina puede tener lugar en tres vías paralelas, donde tres pasos consecutivos de N -metilación catalizados por una metil transferasa se llevan a cabo en la base libre, [11] fosfobases, [12] o fosfatidil-bases. [13] La fuente del grupo metilo es S -adenosil- L -metionina y S -adenosil- L -homocisteína se genera como producto secundario. [14]

En los seres humanos y en la mayoría de los demás animales, la síntesis de novo de colina se realiza a través de la vía de la fosfatidiletanolamina N-metiltransferasa (PEMT), [8] pero la biosíntesis no es suficiente para satisfacer las necesidades humanas. [15] En la ruta PEMT hepática, el 3-fosfoglicerato (3PG) recibe 2 grupos acilo de la acil-CoA formando un ácido fosfatídico . Reacciona con trifosfato de citidina para formar difosfato de citidina-diacilglicerol. Su grupo hidroxilo reacciona con la serina para formar fosfatidilserina que se descarboxila en formas de etanolamina y fosfatidiletanolamina (PE). Una enzima PEMT mueve tres grupos metilo de tres donantes de S -adenosil metioninas (SAM) al grupo etanolamina de la fosfatidiletanolamina para formar colina en forma de fosfatidilcolina. Como subproducto se forman tres S -adenosilhomocisteínas (SAH). [8]
La colina también se puede liberar a partir de moléculas más complejas que contienen colina. Por ejemplo, las fosfatidilcolinas (PC) se pueden hidrolizar a colina (Chol) en la mayoría de los tipos de células. La colina también se puede producir por la ruta CDP-colina, las colina quinasas citosólicas (CK) fosforilan la colina con ATP para formar fosfocolina (PChol). [3] Esto sucede en algunos tipos de células como el hígado y el riñón. Las citidililtransferasas de colina-fosfato (CPCT) transforman PChol en CDP-colina (CDP-Chol) con trifosfato de citidina (CTP). La CDP-colina y el diglicérido se transforman en PC mediante la diacilglicerolcolinefosfotransferasa (CPT). [8]
En los seres humanos, ciertas mutaciones de la enzima PEMT y la deficiencia de estrógenos (a menudo debido a la menopausia ) aumentan la necesidad dietética de colina. En los roedores, el 70% de las fosfatidilcolinas se forman por vía PEMT y sólo el 30% por vía CDP-colina. [8] En ratones knockout , la inactivación de PEMT los hace completamente dependientes de la colina en la dieta. [3]
En los seres humanos, la colina se absorbe en los intestinos a través de la proteína de membrana SLC44A1 (CTL1) mediante difusión facilitada gobernada por el gradiente de concentración de colina y el potencial eléctrico a través de las membranas de los enterocitos . SLC44A1 tiene una capacidad limitada para transportar colina: en concentraciones elevadas, parte de ella queda sin absorber. La colina absorbida sale de los enterocitos a través de la vena porta , pasa por el hígado y entra en la circulación sistémica . Los microbios intestinales degradan la colina no absorbida a trimetilamina, que se oxida en el hígado a N -óxido de trimetilamina . [8]
La fosfocolina y las glicerofosfocolinas se hidrolizan mediante fosfolipasas a colina, que ingresa a la vena porta. Debido a su solubilidad en agua, algunos de ellos escapan sin cambios a la vena porta. Los compuestos liposolubles que contienen colina (fosfatidilcolinas y esfingomielinas ) son hidrolizados por fosfolipasas o ingresan a la linfa incorporados en los quilomicrones . [8]
En los seres humanos, la colina se transporta como molécula libre en la sangre. Los fosfolípidos que contienen colina y otras sustancias, como las glicerofosfocolinas, se transportan en las lipoproteínas sanguíneas . Los niveles de colina en plasma sanguíneo en adultos sanos en ayunas son de 7 a 20 micromoles por litro (μmol/L) y 10 μmol/L en promedio. Los niveles están regulados, pero la ingesta y la deficiencia de colina alteran estos niveles. Los niveles se elevan durante aproximadamente 3 horas después del consumo de colina. Los niveles de fosfatidilcolina en el plasma de adultos en ayunas son de 1,5 a 2,5 mmol/L. Su consumo eleva los niveles de colina libre durante unas 8 a 12 horas, pero no afecta significativamente los niveles de fosfatidilcolina. [8]
La colina es un ion soluble en agua y, por lo tanto, requiere transportadores para atravesar las membranas celulares liposolubles . Se conocen tres tipos de transportadores de colina: [16]
Los SLC5A7 son transportadores dependientes de sodio - (Na + ) y ATP. [16] [8] Tienen una alta afinidad de unión por la colina, la transportan principalmente a las neuronas y están indirectamente asociados con la producción de acetilcolina . [8] Su función deficiente causa debilidad hereditaria en los músculos pulmonares y otros músculos en humanos a través de la deficiencia de acetilcolina. En ratones knockout , su disfunción resulta fácilmente en la muerte con cianosis y parálisis . [17]
Los CTL1 tienen una afinidad moderada por la colina y la transportan en casi todos los tejidos, incluidos los intestinos, el hígado, los riñones, la placenta y las mitocondrias . Los CTL1 suministran colina para la producción de fosfatidilcolina y trimetilglicina . [8] Los CTL2 se producen especialmente en las mitocondrias de la lengua, los riñones, los músculos y el corazón. Están asociados con la oxidación mitocondrial de colina a trimetilglicina. Los CTL1 y CTL2 no están asociados con la producción de acetilcolina, pero transportan colina juntos a través de la barrera hematoencefálica . Sólo los CTL2 se encuentran en el lado cerebral de la barrera. También eliminan el exceso de colina de las neuronas a la sangre. Los CTL1 se encuentran sólo en el lado sanguíneo de la barrera, pero también en las membranas de los astrocitos y las neuronas. [dieciséis]
Los OCT1 y OCT2 no están asociados con la producción de acetilcolina. [8] Transportan colina con baja afinidad. Los OCT1 transportan colina principalmente en el hígado y los riñones; OCT2 en riñones y cerebro. [dieciséis]
La colina se almacena en las membranas celulares y orgánulos como fosfolípidos, y en el interior de las células como fosfatidilcolinas y glicerofosfocolinas. [8]
Incluso con dosis de colina de 2 a 8 g, en los seres humanos se excreta poca colina en la orina. La excreción se produce a través de transportadores que se encuentran dentro de los riñones (ver transporte). La trimetilglicina se desmetila en el hígado y los riñones a dimetilglicina ( el tetrahidrofolato recibe uno de los grupos metilo). La metilglicina se forma, se excreta en la orina o se desmetila a glicina . [8]
La colina y sus derivados tienen muchas funciones en los seres humanos y en otros organismos. La función más notable es que la colina sirve como precursor sintético de otros componentes celulares esenciales y moléculas de señalización, como los fosfolípidos que forman las membranas celulares, el neurotransmisor acetilcolina y el osmorregulador trimetilglicina ( betaína ). La trimetilglicina, a su vez, sirve como fuente de grupos metilo al participar en la biosíntesis de S -adenosilmetionina . [18] [19]
La colina se transforma en diferentes fosfolípidos, como fosfatidilcolinas y esfingomielinas. Estos se encuentran en todas las membranas celulares y en las membranas de la mayoría de los orgánulos celulares. [3] Las fosfatidilcolinas son una parte estructuralmente importante de las membranas celulares. En los seres humanos, entre el 40 y el 50% de sus fosfolípidos son fosfatidilcolinas. [8]
Los fosfolípidos de colina también forman balsas lipídicas en las membranas celulares junto con el colesterol . Las balsas son centros, por ejemplo, para receptores y enzimas de transducción de señales de receptores . [3]
Las fosfatidilcolinas son necesarias para la síntesis de VLDL : entre el 70% y el 95% de sus fosfolípidos son fosfatidilcolinas en humanos. [8]
La colina también es necesaria para la síntesis de surfactante pulmonar , que es una mezcla compuesta principalmente de fosfatidilcolinas. El surfactante es responsable de la elasticidad pulmonar, es decir, de la capacidad del tejido pulmonar para contraerse y expandirse. Por ejemplo, la deficiencia de fosfatidilcolinas en los tejidos pulmonares se ha relacionado con el síndrome de dificultad respiratoria aguda . [20]
Las fosfatidilcolinas se excretan en la bilis y actúan junto con las sales de ácidos biliares como tensioactivos , ayudando así a la absorción intestinal de lípidos . [3]
Se necesita colina para producir acetilcolina. Se trata de un neurotransmisor que desempeña un papel necesario en la contracción muscular , la memoria y el desarrollo neuronal , por ejemplo. [8] Sin embargo, hay poca acetilcolina en el cuerpo humano en comparación con otras formas de colina. [3] Las neuronas también almacenan colina en forma de fosfolípidos en sus membranas celulares para la producción de acetilcolina. [8]
En los seres humanos, la colina se oxida irreversiblemente en las mitocondrias del hígado a glicina betaína aldehído mediante colina oxidasas . Este es oxidado por betaína-aldehído deshidrogenasas mitocondriales o citosólicas a trimetilglicina. [8] La trimetilglicina es un osmorregulador necesario. También funciona como sustrato para la enzima BHMT , que metila la homocisteína en metionina . Este es un precursor de S -adenosilmetionina (SAM). SAM es un reactivo común en reacciones de metilación biológica . Por ejemplo, metila guanidinas del ADN y determinadas lisinas de las histonas . Por tanto, forma parte de la expresión genética y la regulación epigenética . Por lo tanto, la deficiencia de colina conduce a niveles elevados de homocisteína y niveles reducidos de SAM en sangre. [8]
La colina se encuentra en los alimentos como molécula libre y en forma de fosfolípidos, especialmente como fosfatidilcolinas. La colina es más alta en las vísceras y las yemas de huevo , aunque se encuentra en menor grado en las vísceras, los cereales, las verduras, las frutas y los productos lácteos . Los aceites de cocina y otras grasas alimentarias tienen aproximadamente 5 mg/100 g de colina total. [8] En los Estados Unidos, las etiquetas de los alimentos expresan la cantidad de colina en una porción como porcentaje del valor diario (%DV) basado en la ingesta adecuada de 550 mg/día. El 100% del valor diario significa que una ración de alimento tiene 550 mg de colina. [21] La "colina total" se define como la suma de la colina libre y los fosfolípidos que contienen colina, sin tener en cuenta la fracción de masa. [22] [23] [8]
La leche materna humana es rica en colina. La lactancia materna exclusiva corresponde a unos 120 mg de colina al día para el bebé. El aumento en la ingesta de colina de la madre aumenta el contenido de colina en la leche materna y una ingesta baja lo disminuye. [8] Las fórmulas infantiles pueden contener o no suficiente colina. En la UE y EE. UU., es obligatorio añadir al menos 7 mg de colina por cada 100 kilocalorías (kcal) a cada fórmula infantil. En la UE no se permiten niveles superiores a 50 mg/100 kcal. [8] [24]
La trimetilglicina es un metabolito funcional de la colina. Sustituye nutricionalmente a la colina, pero sólo parcialmente. [3] Se encuentran altas cantidades de trimetilglicina en el salvado de trigo (1339 mg/100 g), el germen de trigo tostado (1240 mg/100 g) y las espinacas (600–645 mg/100 g), por ejemplo. [22]
La siguiente tabla contiene fuentes actualizadas de colina para reflejar el nuevo valor diario y las nuevas etiquetas de información nutricional y de suplementos. [21] Refleja datos del Servicio de Investigación Agrícola del Departamento de Agricultura de EE. UU. Central de datos alimentarios, 2019. [21]
VD = Valor Diario. La Administración de Alimentos y Medicamentos de EE. UU. (FDA) desarrolló VD para ayudar a los consumidores a comparar el contenido de nutrientes de los alimentos y suplementos dietéticos en el contexto de una dieta total. El valor diario de colina es de 550 mg para adultos y niños de 4 años en adelante. [ cita necesaria ] La FDA no exige que las etiquetas de los alimentos indiquen el contenido de colina a menos que se haya agregado colina al alimento. Los alimentos que proporcionan el 20% o más del VD se consideran fuentes altas de un nutriente, pero los alimentos que proporcionan porcentajes más bajos del VD también contribuyen a una dieta saludable. [21]
FoodData Central del Departamento de Agricultura de EE. UU. (USDA) enumera el contenido de nutrientes de muchos alimentos y proporciona una lista completa de alimentos que contienen colina ordenados por contenido de nutrientes. [21]
No hay datos suficientes disponibles para establecer un requerimiento promedio estimado (EAR) de colina, por lo que la Junta de Alimentos y Nutrición (FNB) estableció ingestas adecuadas (AI). [25] Para los adultos, la IA de colina se fijó en 550 mg/día para los hombres y 425 mg/día para las mujeres. Se ha demostrado que estos valores previenen la alteración hepática en los hombres. Sin embargo, el estudio utilizado para derivar estos valores no evaluó si sería eficaz menos colina, ya que los investigadores sólo compararon una dieta sin colina con una dieta que contenía 550 mg de colina por día. A partir de esto, se extrapolaron las IA para niños y adolescentes. [26] [27]
Las recomendaciones están en miligramos por día (mg/día). Las recomendaciones de la Autoridad Europea de Seguridad Alimentaria (EFSA) son recomendaciones generales para los países de la UE . La EFSA no ha fijado límites máximos de ingesta. [8] Los países individuales de la UE pueden tener recomendaciones más específicas. Las recomendaciones de la Academia Nacional de Medicina (NAM) se aplican en los Estados Unidos, [21] Australia y Nueva Zelanda. [28]
Doce encuestas realizadas en nueve países de la UE entre 2000 y 2011 estimaron que la ingesta de colina de los adultos en estos países era de 269 a 468 miligramos por día. La ingesta fue de 269 a 444 mg/día en mujeres adultas y de 332 a 468 mg/día en hombres adultos. La ingesta fue de 75 a 127 mg/día en los lactantes, de 151 a 210 mg/día en los niños de 1 a 3 años, de 177 a 304 mg/día en los de 3 a 10 años y de 244 a 373 mg/día en los niños de 3 a 10 años. Jóvenes de 10 a 18 años. La ingesta media estimada de colina total fue de 336 mg/día en adolescentes embarazadas y de 356 mg/día en mujeres embarazadas. [8]
Un estudio basado en la encuesta NHANES 2009-2012 estimó que la ingesta de colina era demasiado baja en algunas subpoblaciones de EE. UU. La ingesta fue de 315,2 a 318,8 mg/d en niños mayores de 2 años entre este período. De los niños mayores de 2 años, sólo15,6 ± 0,8 % de los varones y6,1 ± 0,6 % de las hembras excedieron el consumo adecuado (IA). La IA fue superada por62,9 ± 3,1 % de niños de 2 a 3 años,45,4 ± 1,6 % de niños de 4 a 8 años,9,0 ± 1,0 % de niños de 9 a 13 años,1,8 ± 0,4 % de 14 a 18 años y6,6 ± 0,5 % de mayores de 19 años. El nivel máximo de ingesta no se superó en ninguna subpoblación. [29]
Un estudio NHANES de 2013-2014 sobre la población estadounidense encontró que la ingesta de colina de los jóvenes de 2 a 19 años era256 ± 3,8 mg/día y339 ± 3,9 mg/día en adultos de 20 años y más. La ingesta fue402 ± 6,1 mg/d en hombres de 20 y más años y 278 mg/d en mujeres de 20 y más años. [30]
La deficiencia sintomática de colina es rara en humanos. La mayoría obtiene cantidades suficientes de la dieta y son capaces de biosintetizar cantidades limitadas a través de PEMT . [3] La deficiencia sintomática suele ser causada por ciertas enfermedades o por otras causas indirectas. Una deficiencia grave causa daño muscular y enfermedad del hígado graso no alcohólico , que puede convertirse en cirrosis . [31]
Además de en los humanos, el hígado graso también es un signo típico de deficiencia de colina en otros animales. En algunas especies también puede producirse sangrado en los riñones. Se sospecha que esto se debe a una deficiencia de trimetilglicina derivada de colina, que funciona como osmorregulador. [3]
La producción de estrógeno es un factor relevante que predispone a las personas a una deficiencia junto con una ingesta baja de colina en la dieta. Los estrógenos activan la fosfatidilcolina produciendo enzimas PEMT. Las mujeres antes de la menopausia tienen una menor necesidad dietética de colina que los hombres debido a la mayor producción de estrógeno de las mujeres. Sin terapia con estrógenos , las necesidades de colina de las mujeres posmenopáusicas son similares a las de los hombres. También son relevantes algunos polimorfismos de un solo nucleótido (factores genéticos) que afectan el metabolismo de la colina y el folato . Ciertos microbios intestinales también degradan la colina de manera más eficiente que otros, por lo que también son relevantes. [31]
En caso de deficiencia, disminuye la disponibilidad de fosfatidilcolinas en el hígado, que son necesarias para la formación de VLDL. Por lo tanto, el transporte de ácidos grasos fuera del hígado mediado por VLDL disminuye, lo que conduce a la acumulación de grasa en el hígado. [8] También se han sugerido otros mecanismos que ocurren simultáneamente y que explican el daño hepático observado. Por ejemplo, los fosfolípidos de colina también son necesarios en las membranas mitocondriales . Su indisponibilidad conduce a la incapacidad de las membranas mitocondriales para mantener el gradiente electroquímico adecuado , que, entre otras cosas, es necesario para degradar los ácidos grasos mediante β-oxidación . Por tanto, el metabolismo de las grasas en el hígado disminuye. [31]
Dosis excesivas de colina pueden tener efectos adversos. Por ejemplo, se ha descubierto que dosis diarias de colina de 8 a 20 g causan presión arterial baja , náuseas , diarrea y olor corporal parecido al del pescado . El olor se debe a la trimetilamina (TMA) formada por los microbios intestinales a partir de la colina no absorbida (ver trimetilaminuria ). [8]
El hígado oxida la TMA a N -óxido de trimetilamina (TMAO). Los niveles elevados de TMA y TMAO en el cuerpo se han relacionado con un mayor riesgo de aterosclerosis y mortalidad. Por lo tanto, se ha planteado la hipótesis de que la ingesta excesiva de colina aumenta estos riesgos, además de la carnitina , que también se forma en TMA y TMAO por las bacterias intestinales. Sin embargo, no se ha demostrado que la ingesta de colina aumente el riesgo de morir por enfermedades cardiovasculares . [32] Es posible que los niveles elevados de TMA y TMAO sean solo un síntoma de otras enfermedades subyacentes o factores genéticos que predisponen a las personas a una mayor mortalidad. Es posible que dichos factores no se hayan tenido en cuenta adecuadamente en ciertos estudios que observaron la mortalidad relacionada con los niveles de TMA y OTMA. La causalidad puede ser inversa o confusa y es posible que una ingesta elevada de colina no aumente la mortalidad en humanos. Por ejemplo, la disfunción renal predispone a enfermedades cardiovasculares, pero también puede disminuir la excreción de TMA y TMAO. [33]
La baja ingesta materna de colina se asocia con un mayor riesgo de defectos del tubo neural . Es probable que una mayor ingesta materna de colina se asocie con una mejor neurocognición y neurodesarrollo en los niños. [34] [5] La colina y el folato, al interactuar con la vitamina B 12 , actúan como donantes de metilo para la homocisteína para formar metionina, que luego puede formar SAM ( S -adenosilmetionina). [5] SAM es el sustrato de casi todas las reacciones de metilación en mamíferos. Se ha sugerido que la alteración de la metilación a través de SAM podría ser responsable de la relación entre el folato y los defectos del tubo neural. [35] Esto también puede aplicarse a la colina. [ cita necesaria ] Ciertas mutaciones que alteran el metabolismo de la colina aumentan la prevalencia de defectos del tubo neural en los recién nacidos, pero el papel de la deficiencia de colina en la dieta aún no está claro, a partir de 2015. [5][actualizar]
La deficiencia de colina puede provocar hígado graso , lo que aumenta el riesgo de cáncer y enfermedades cardiovasculares. La deficiencia de colina también disminuye la producción de SAM, que participa en la metilación del ADN ; esta disminución también puede contribuir a la carcinogénesis . Así, se ha estudiado la deficiencia y su asociación con dichas enfermedades. [8] Sin embargo, los estudios observacionales de poblaciones libres no han demostrado de manera convincente una asociación entre la ingesta baja de colina y las enfermedades cardiovasculares o la mayoría de los cánceres. [5] [8] Los estudios sobre el cáncer de próstata han sido contradictorios. [36] [37]
Se han realizado estudios en humanos adultos que observan el efecto entre una mayor ingesta de colina y la cognición , con resultados contradictorios. [5] [38] Estudios similares sobre bebés y niños humanos han sido contradictorios y también limitados. [5]
Tanto el embarazo como la lactancia aumentan drásticamente la demanda de colina. Esta demanda puede satisfacerse mediante la regulación positiva de PEMT mediante el aumento de los niveles de estrógeno para producir más colina de novo , pero incluso con una mayor actividad de PEMT, la demanda de colina sigue siendo tan alta que las reservas corporales generalmente se agotan. Esto se ejemplifica con la observación de que los ratones Pemt -/- (ratones que carecen de PEMT funcional) abortarán a los 9-10 días a menos que se les alimente colina suplementaria. [39]
Mientras que las reservas maternas de colina se agotan durante el embarazo y la lactancia, la placenta acumula colina bombeándola contra el gradiente de concentración hacia el tejido, donde luego se almacena en diversas formas, principalmente como acetilcolina. Las concentraciones de colina en el líquido amniótico pueden ser diez veces mayores que en la sangre materna. [39]
La colina tiene una gran demanda durante el embarazo como sustrato para la construcción de membranas celulares (rápida expansión del tejido materno y fetal), mayor necesidad de restos de un carbono (un sustrato para la metilación del ADN y otras funciones), aumento de las reservas de colina en los tejidos fetales y placentarios. y para una mayor producción de lipoproteínas (proteínas que contienen porciones "grasas"). [40] [41] [42] En particular, existe interés en el impacto del consumo de colina en el cerebro. Esto se debe al uso de la colina como material para fabricar membranas celulares (particularmente para producir fosfatidilcolina). El crecimiento del cerebro humano es más rápido durante el tercer trimestre del embarazo y continúa siendo rápido hasta aproximadamente los cinco años de edad. [43] Durante este tiempo, la demanda es alta de esfingomielina, que está hecha de fosfatidilcolina (y por lo tanto de colina), porque este material se usa para mielinizar (aislar) las fibras nerviosas . [44] La colina también es necesaria para la producción del neurotransmisor acetilcolina, que puede influir en la estructura y organización de las regiones del cerebro, la neurogénesis , la mielinización y la formación de sinapsis . La acetilcolina incluso está presente en la placenta y puede ayudar a controlar la proliferación y diferenciación celular (aumentos en el número de células y cambios de células multiuso en funciones celulares dedicadas) y el parto . [45] [46]
La absorción de colina en el cerebro está controlada por un transportador de baja afinidad ubicado en la barrera hematoencefálica. [47] El transporte ocurre cuando las concentraciones de colina en el plasma sanguíneo arterial aumentan por encima de 14 μmol/L, lo que puede ocurrir durante un aumento en la concentración de colina después de consumir alimentos ricos en colina. Las neuronas, por el contrario, adquieren colina mediante transportadores de alta y baja afinidad. La colina se almacena como fosfatidilcolina unida a la membrana, que luego puede usarse para la síntesis del neurotransmisor acetilcolina. La acetilcolina se forma según sea necesario, viaja a través de la sinapsis y transmite la señal a la siguiente neurona. Posteriormente, la acetilcolinesterasa la degrada y la colina libre es absorbida nuevamente por un transportador de alta afinidad hacia la neurona. [48]
El cloruro de colina y el bitartrato de colina se utilizan en suplementos dietéticos . El bitartrato se utiliza con más frecuencia debido a su menor higroscopicidad. [3] Ciertas sales de colina se utilizan para complementar los alimentos para pollos, pavos y otros animales . Algunas sales también se utilizan como productos químicos industriales: por ejemplo, en fotolitografía para eliminar fotoprotectores . [2] El teofilinato de colina y el salicilato de colina se utilizan como medicamentos, [2] [49] así como análogos estructurales , como metacolina y carbacol . [50] Las colinas radiomarcadas , como la 11 C-colina , se utilizan en imágenes médicas . [51] Otras sales utilizadas comercialmente incluyen el citrato de tricolina y el bicarbonato de colina . [2]
Se han desarrollado cientos de antagonistas de colina e inhibidores de enzimas con fines de investigación. El aminometilpropanol se encuentra entre los primeros utilizados como herramienta de investigación. Inhibe la síntesis de colina y trimetilglicina. Es capaz de inducir una deficiencia de colina que a su vez provoca hígado graso en los roedores. La dietanolamina es otro de esos compuestos, pero también un contaminante ambiental. La N-ciclohexilcolina inhibe la absorción de colina principalmente en el cerebro. El hemicolinio-3 es un inhibidor más general, pero también inhibe moderadamente las colina quinasas. También se han desarrollado inhibidores de la colina quinasa más específicos. También existen inhibidores de la síntesis de trimetilglicina: la carboxibutilhomocisteína es un ejemplo de inhibidor específico de BHMT. [3]
La hipótesis colinérgica de la demencia no sólo ha dado lugar a los inhibidores medicinales de la acetilcolinesterasa , sino también a una variedad de inhibidores de la acetilcolina. Ejemplos de tales sustancias químicas de investigación inhibidoras incluyen trietilcolina , homocolina y muchos otros derivados N -etílicos de la colina, que son falsos neurotransmisores análogos de la acetilcolina. También se han desarrollado inhibidores de la colina acetiltransferasa . [3]
En 1849, Adolph Strecker fue el primero en aislar la colina de la bilis de cerdo. [52] [53] En 1852, L. Babo y M. Hirschbrunn extrajeron colina de semillas de mostaza blanca y la llamaron sinkalina . [53] En 1862, Strecker repitió su experimento con bilis de cerdo y de buey, llamando a la sustancia colina por primera vez, después de la palabra griega para bilis, chole , e identificándola con la fórmula química C 5 H 13 NO. [54] [15] En 1850, Theodore Nicolas Gobley extrajo de los cerebros y huevas de carpas una sustancia a la que llamó lecitina por la palabra griega para yema de huevo , lekithos , demostrando en 1874 que era una mezcla de fosfatidilcolinas . [55] [56]
En 1865, Oscar Liebreich aisló la " neurina " de cerebros de animales. [57] [15] Las fórmulas estructurales de la acetilcolina y la "neurina" de Liebreich fueron resueltas por Adolf von Baeyer en 1867. [58] [53] Más tarde, ese mismo año, se demostró que la "neurina" y la sinkalina eran las mismas sustancias que la colina de Strecker. Así, Bayer fue el primero en resolver la estructura de la colina. [59] [60] [53] El compuesto ahora conocido como neurina no está relacionado con la colina. [15]
A principios de la década de 1930, Charles Best y sus colegas observaron que el hígado graso en ratas con una dieta especial y en perros diabéticos se podía prevenir alimentándolos con lecitina, [15] demostrando en 1932 que la colina en la lecitina era la única responsable de este efecto preventivo. [61] En 1998, la Academia Nacional de Medicina de EE. UU. informó sus primeras recomendaciones para la colina en la dieta humana. [62]
{{cite encyclopedia}}: |website=ignorado ( ayuda )En esta Opinión, el Panel considera la colina dietética, incluidos los compuestos de colina (por ejemplo, glicerofosfocolina, fosfocolina, fosfatidilcolina, esfingomielina).
El contenido total de colina se calculó como la suma de Cho, GPC, Pcho, Ptdcho y SM.