La guanidina es el compuesto de fórmula HNC(NH 2 ) 2 . Es un sólido incoloro que se disuelve en disolventes polares . Es una base fuerte que se utiliza en la producción de plásticos y explosivos . Se encuentra en la orina predominantemente en pacientes con insuficiencia renal. [3] Un resto de guanidina también aparece en moléculas orgánicas más grandes, incluso en la cadena lateral de la arginina .
Se puede considerar a la guanidina como un análogo nitrogenado del ácido carbónico . Es decir, el grupo C=O en el ácido carbónico se reemplaza por un grupo C=NH y cada OH se reemplaza por un NH.
2grupo. [4] El isobuteno puede verse como el análogo del carbono de la misma manera. Un análisis cristalográfico detallado de la guanidina fue dilucidado 148 años después de su primera síntesis, a pesar de la simplicidad de la molécula. [5] En 2013, las posiciones de los átomos de hidrógeno y sus parámetros de desplazamiento se determinaron con precisión mediante difracción de neutrones monocristalinos. [6]
La guanidina se puede obtener de fuentes naturales, siendo aislada por primera vez en 1861 por Adolph Strecker mediante la degradación oxidativa de un producto natural aromático, la guanina , aislada del guano peruano . [7] [8]
Un método de laboratorio para producir guanidina es la descomposición térmica suave (180-190 °C) de tiocianato de amonio seco en condiciones anhidras:
La ruta comercial implica un proceso de dos pasos que comienza con la reacción de diciandiamida con sales de amonio . A través de la intermediación de biguanidina , este paso de amonólisis produce sales del catión guanidinio (ver más abajo). En el segundo paso, la sal se trata con una base, como metóxido de sodio . [7]
El ácido conjugado se llama catión guanidinio , ( C(NH
2)+
3). Este ion plano y simétrico consta de tres grupos amino , cada uno de ellos unido al átomo de carbono central con un enlace covalente de orden 4/3. Es un catión +1 altamente estable en solución acuosa debido a la eficiente estabilización por resonancia de la carga y la eficiente solvatación por las moléculas de agua. Como resultado, su p K aH es 13,6 [9] (p K b de 0,4), lo que significa que la guanidina es una base muy fuerte en agua; en agua neutra, existe casi exclusivamente como guanidinio. Debido a esto, la mayoría de los derivados de guanidina son sales que contienen el ácido conjugado.
La guanidina se puede detectar selectivamente utilizando ácido 1,2-naftoquinona-4-sulfónico de sodio ( reactivo de Folin ) y urea acidificada. [10]
La principal sal de interés comercial es el nitrato [C( NH
2) 3 ] NO
3. Se utiliza como propulsor, por ejemplo en bolsas de aire .
Desde la Edad Media en Europa, la guanidina se ha utilizado para tratar la diabetes como ingrediente activo antihiperglucemiante de la lila francesa . Debido a su hepatotoxicidad a largo plazo , al principio se suspendieron más investigaciones sobre el control del azúcar en sangre después del descubrimiento de la insulina. El desarrollo posterior de biguanidas seguras y no tóxicas condujo al medicamento de primera línea para el control de la diabetes, metformina , utilizado durante mucho tiempo , introducido en Europa en la década de 1950 y en Estados Unidos en 1995 y ahora recetado a más de 17 millones de pacientes por año en Estados Unidos. [11] [12]
El cloruro de guanidinio [11] es un coadyuvante ahora controvertido en el tratamiento del botulismo . Estudios recientes han demostrado que algunos subconjuntos importantes de pacientes no ven ninguna mejora después de la administración de este fármaco. [13]
La guanidina existe protonada, como guanidinio, en solución a pH fisiológico.
El cloruro de guanidinio (también conocido como clorhidrato de guanidina) tiene propiedades caotrópicas y se utiliza para desnaturalizar proteínas. Se sabe que el cloruro de guanidinio desnaturaliza las proteínas con una relación lineal entre la concentración y la energía libre de desarrollo. En soluciones acuosas que contienen cloruro de guanidinio 6 M , casi todas las proteínas pierden toda su estructura secundaria y se convierten en cadenas peptídicas enrolladas al azar . El tiocianato de guanidinio también se utiliza por su efecto desnaturalizante en diversas muestras biológicas.
Estudios recientes sugieren que el guanidinio es producido por bacterias como un subproducto tóxico. Para aliviar la toxicidad del guanidinio, las bacterias han desarrollado una clase de transportadores conocidos como exportadores de guanidinio o proteínas Gdx para expulsar las cantidades adicionales de este ion al exterior de la célula. [14] Las proteínas Gdx son altamente selectivas para guanidinio y compuestos de guanidinilo monosustituidos y comparten un conjunto superpuesto de sustratos no canónicos con el exportador de fármacos EmrE. [15]
El hidróxido de guanidinio es el ingrediente activo de algunos alisantes para el cabello sin lejía .
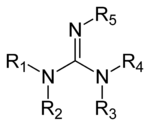
Las guanidinas son un grupo de compuestos orgánicos que comparten un grupo funcional común con la estructura general (R
1R
2norte)(r
3R
4N)C=N-R
5. El enlace central dentro de este grupo es el de una imina , y el grupo está relacionado estructuralmente con amidinas y ureas. Ejemplos de guanidinas son la arginina , el triazabiciclodeceno , la saxitoxina y la creatina .
Galegine es una isoamileno guanidina. [dieciséis]