La quimioterapia (a menudo abreviada quimio , a veces CTX y CTx ) es el tipo de tratamiento contra el cáncer que utiliza uno o más medicamentos contra el cáncer ( agentes quimioterapéuticos o agentes alquilantes ) en un régimen estándar . La quimioterapia se puede administrar con una intención curativa (que casi siempre implica combinaciones de medicamentos), o puede tener como objetivo únicamente prolongar la vida o reducir los síntomas ( quimioterapia paliativa ). La quimioterapia es una de las principales categorías de la disciplina médica dedicada específicamente a la farmacoterapia para el cáncer , que se denomina oncología médica . [1] [2]
El término quimioterapia ahora significa el uso no específico de venenos intracelulares para inhibir la mitosis (división celular) o inducir daño al ADN (para que la reparación del ADN pueda aumentar la quimioterapia). [3] Este significado excluye los agentes más selectivos que bloquean las señales extracelulares ( transducción de señales ). Las terapias con objetivos moleculares o genéticos específicos, que inhiben las señales promotoras del crecimiento de las hormonas endocrinas clásicas (principalmente estrógenos para el cáncer de mama y andrógenos para el cáncer de próstata), ahora se denominan terapias hormonales . Otras inhibiciones de las señales de crecimiento, como las asociadas con los receptores tirosina quinasas , son terapias dirigidas .
El uso de medicamentos (ya sea quimioterapia, terapia hormonal o terapia dirigida) es una terapia sistémica para el cáncer: se introducen en el torrente sanguíneo (el sistema) y, por lo tanto, pueden tratar el cáncer en cualquier parte del cuerpo. La terapia sistémica a menudo se usa con otras terapias locales (tratamientos que funcionan solo donde se aplican), como radiación , cirugía e hipertermia .
Los agentes quimioterapéuticos tradicionales son citotóxicos al interferir con la división celular (mitosis), pero las células cancerosas varían ampliamente en su susceptibilidad a estos agentes. En gran medida, se puede considerar la quimioterapia como una forma de dañar o estresar las células, lo que luego puede conducir a la muerte celular si se inicia la apoptosis . Muchos de los efectos secundarios de la quimioterapia se deben al daño a las células normales que se dividen rápidamente y, por lo tanto, son sensibles a los fármacos antimitóticos: células de la médula ósea , el tracto digestivo y los folículos pilosos . Esto produce los efectos secundarios más comunes de la quimioterapia: mielosupresión (disminución de la producción de células sanguíneas, de ahí también inmunosupresión ), mucositis (inflamación del revestimiento del tracto digestivo) y alopecia (pérdida de cabello). Debido al efecto sobre las células inmunes (especialmente los linfocitos), los medicamentos de quimioterapia a menudo encuentran uso en una serie de enfermedades que resultan de una hiperactividad dañina del sistema inmunológico contra uno mismo (la llamada autoinmunidad ). Estos incluyen artritis reumatoide , lupus eritematoso sistémico , esclerosis múltiple , vasculitis y muchos otros.
Existen varias estrategias en la administración de fármacos quimioterapéuticos que se utilizan en la actualidad. La quimioterapia puede administrarse con intención curativa o puede tener como objetivo prolongar la vida o paliar los síntomas .
Todos los regímenes de quimioterapia requieren que el receptor sea capaz de someterse al tratamiento. El estado funcional se utiliza a menudo como medida para determinar si una persona puede recibir quimioterapia o si es necesaria una reducción de la dosis. Debido a que solo una fracción de las células de un tumor muere con cada tratamiento ( muerte fraccionada ), se deben administrar dosis repetidas para continuar reduciendo el tamaño del tumor. [10] Los regímenes de quimioterapia actuales aplican el tratamiento farmacológico en ciclos, con la frecuencia y duración de los tratamientos limitadas por la toxicidad. [11]
La eficacia de la quimioterapia depende del tipo de cáncer y del estadio. La eficacia general varía desde ser curativo para algunos cánceres, como algunas leucemias , [12] [13] hasta ser ineficaz, como en algunos tumores cerebrales , [14] y ser innecesario en otros, como la mayoría de los cánceres de piel no melanoma . [15]

La dosificación de la quimioterapia puede resultar difícil: si la dosis es demasiado baja, será ineficaz contra el tumor, mientras que, en dosis excesivas, la toxicidad ( efectos secundarios ) será intolerable para la persona que la recibe. [4] El método estándar para determinar la dosis de quimioterapia se basa en el área de superficie corporal (BSA) calculada. El BSA generalmente se calcula con una fórmula matemática o un nomograma , utilizando el peso y la altura del destinatario, en lugar de medir directamente el área corporal. Esta fórmula se derivó originalmente en un estudio de 1916 e intentó traducir las dosis medicinales establecidas con animales de laboratorio a dosis equivalentes para humanos. [16] El estudio solo incluyó nueve sujetos humanos. [17] Cuando se introdujo la quimioterapia en la década de 1950, la fórmula BSA se adoptó como el estándar oficial para la dosificación de quimioterapia a falta de una mejor opción. [18] [19]
Se ha cuestionado la validez de este método para calcular dosis uniformes porque la fórmula sólo tiene en cuenta el peso y la altura del individuo. La absorción y eliminación de medicamentos están influenciadas por múltiples factores, incluidos la edad, el sexo, el metabolismo, el estado de la enfermedad, la función de los órganos, las interacciones entre medicamentos, la genética y la obesidad, que tienen un impacto importante en la concentración real del medicamento en el torrente sanguíneo de la persona. . [18] [20] [21] Como resultado, existe una alta variabilidad en la concentración del fármaco de quimioterapia sistémica en personas a las que se les administra BSA, y se ha demostrado que esta variabilidad es más de diez veces mayor para muchos fármacos. [17] [22] En otras palabras, si dos personas reciben la misma dosis de un medicamento determinado según su BSA, la concentración de ese medicamento en el torrente sanguíneo de una persona puede ser 10 veces mayor o menor en comparación con la de la otra persona. . [22] Esta variabilidad es típica de muchos medicamentos de quimioterapia dosificados con BSA y, como se muestra a continuación, se demostró en un estudio de 14 medicamentos de quimioterapia comunes. [17]

El resultado de esta variabilidad farmacocinética entre las personas es que muchas personas no reciben la dosis adecuada para lograr una eficacia óptima del tratamiento con efectos secundarios tóxicos minimizados. Algunas personas sufren una sobredosis mientras que otras reciben una dosis insuficiente. [18] [20] [21] [23] [24] [25] [26] Por ejemplo, en un ensayo clínico aleatorizado, los investigadores encontraron que el 85 % de los pacientes con cáncer colorrectal metastásico tratados con 5-fluorouracilo (5-FU) no no recibieron la dosis terapéutica óptima cuando se les administró según el estándar BSA: el 68 % recibió una dosis insuficiente y el 17 % una sobredosis. [23]
Ha habido controversia sobre el uso de BSA para calcular las dosis de quimioterapia para personas obesas . [27] Debido a su BSA más alta, los médicos a menudo reducen arbitrariamente la dosis prescrita por la fórmula de BSA por temor a una sobredosis . [27] En muchos casos, esto puede resultar en un tratamiento subóptimo. [27]
Varios estudios clínicos han demostrado que cuando la dosis de quimioterapia se individualiza para lograr una exposición sistémica óptima al fármaco, los resultados del tratamiento mejoran y se reducen los efectos secundarios tóxicos. [23] [25] En el estudio clínico de 5-FU citado anteriormente, las personas cuya dosis se ajustó para lograr una exposición objetivo predeterminada obtuvieron una mejora del 84 % en la tasa de respuesta al tratamiento y una mejora de seis meses en la supervivencia general (SG). en comparación con aquellos a los que se les administró BSA. [23]
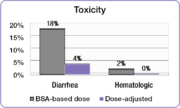
En el mismo estudio, los investigadores compararon la incidencia de toxicidades comunes de grado 3/4 asociadas con el 5-FU entre las personas que recibieron dosis ajustadas y las personas que recibieron dosis según BSA. [23] La incidencia de grados debilitantes de diarrea se redujo del 18% en el grupo que recibió dosis de BSA al 4% en el grupo con dosis ajustada y se eliminaron los efectos secundarios hematológicos graves. [23] Debido a la toxicidad reducida, los pacientes con dosis ajustadas pudieron ser tratados durante períodos de tiempo más prolongados. [23] Las personas que recibieron dosis de BSA fueron tratadas durante un total de 680 meses, mientras que las personas en el grupo con dosis ajustada fueron tratadas durante un total de 791 meses. [23] Completar el curso del tratamiento es un factor importante para lograr mejores resultados del tratamiento.
Se encontraron resultados similares en un estudio en el que participaron personas con cáncer colorrectal que fueron tratadas con el popular régimen FOLFOX . [25] La incidencia de diarrea grave se redujo del 12 % en el grupo de pacientes que recibió la dosis de BSA al 1,7 % en el grupo con dosis ajustada, y la incidencia de mucositis grave se redujo del 15 % al 0,8 %. [25]
El estudio FOLFOX también demostró una mejora en los resultados del tratamiento. [25] La respuesta positiva aumentó del 46% en el grupo que recibió la dosis de BSA al 70% en el grupo con la dosis ajustada. La mediana de la supervivencia libre de progresión (SLP) y la supervivencia general (SG) mejoraron seis meses en el grupo con dosis ajustada. [25]
Un enfoque que puede ayudar a los médicos a individualizar la dosis de quimioterapia es medir los niveles del fármaco en el plasma sanguíneo a lo largo del tiempo y ajustar la dosis según una fórmula o algoritmo para lograr una exposición óptima. Con una exposición objetivo establecida para optimizar la eficacia del tratamiento con toxicidades minimizadas, la dosificación se puede personalizar para lograr la exposición objetivo y resultados óptimos para cada persona. Este algoritmo se utilizó en los ensayos clínicos citados anteriormente y dio como resultado resultados de tratamiento significativamente mejores. [28]
Los oncólogos ya están individualizando las dosis de algunos medicamentos contra el cáncer en función de la exposición. La dosificación de carboplatino [29] : 4 y busulfán [30] [31] depende de los resultados de los análisis de sangre para calcular la dosis óptima para cada persona. También se encuentran disponibles análisis de sangre simples para optimizar la dosis de metotrexato , [32] 5-FU, paclitaxel y docetaxel . [33] [34]
El nivel de albúmina sérica inmediatamente antes de la administración de quimioterapia es un predictor pronóstico independiente de supervivencia en varios tipos de cáncer. [35]

Los agentes alquilantes son el grupo más antiguo de quimioterapéuticos que se utilizan en la actualidad. Originalmente derivado del gas mostaza utilizado en la Primera Guerra Mundial , ahora se utilizan muchos tipos de agentes alquilantes. [4] Se llaman así debido a su capacidad para alquilar muchas moléculas, incluidas proteínas , ARN y ADN . Esta capacidad de unirse covalentemente al ADN a través de su grupo alquilo es la causa principal de sus efectos anticancerígenos. [37] El ADN está formado por dos cadenas y las moléculas pueden unirse dos veces a una cadena de ADN (entrecruzamiento intracadena) o pueden unirse una vez a ambas cadenas (entrecruzamiento entre cadenas). Si la célula intenta replicar el ADN reticulado durante la división celular , o intenta repararlo, las hebras de ADN pueden romperse. Esto conduce a una forma de muerte celular programada llamada apoptosis . [36] [38] Los agentes alquilantes funcionarán en cualquier punto del ciclo celular y, por lo tanto, se conocen como fármacos independientes del ciclo celular. Por esta razón, el efecto sobre la célula depende de la dosis; la fracción de células que mueren es directamente proporcional a la dosis del fármaco. [39]
Los subtipos de agentes alquilantes son las mostazas nitrogenadas , nitrosoureas , tetrazinas , aziridinas , [40] cisplatinos y derivados, y agentes alquilantes no clásicos. Las mostazas nitrogenadas incluyen mecloretamina , ciclofosfamida , melfalán , clorambucilo , ifosfamida y busulfán . Las nitrosoureas incluyen N-nitroso-N-metilurea (MNU), carmustina (BCNU), lomustina (CCNU) y semustina (MeCCNU), fotemustina y estreptozotocina . Las tetrazinas incluyen dacarbazina , mitozolomida y temozolomida . Las aziridinas incluyen tiotepa , mitomicina y diazicuona (AZQ). El cisplatino y sus derivados incluyen cisplatino , carboplatino y oxaliplatino . [37] [38] Afectan la función celular al formar enlaces covalentes con los grupos amino , carboxilo , sulfhidrilo y fosfato en moléculas biológicamente importantes. [41] Los agentes alquilantes no clásicos incluyen procarbazina y hexametilmelamina. [37] [38]

Los antimetabolitos son un grupo de moléculas que impiden la síntesis de ADN y ARN. Muchos de ellos tienen una estructura similar a los componentes básicos del ADN y el ARN. Los componentes básicos son los nucleótidos ; Molécula que comprende una nucleobase , un azúcar y un grupo fosfato . Las nucleobases se dividen en purinas ( guanina y adenina ) y pirimidinas ( citosina , timina y uracilo ). Los antimetabolitos se parecen a las nucleobases o a los nucleósidos (un nucleótido sin el grupo fosfato), pero tienen grupos químicos alterados . [42] Estos fármacos ejercen su efecto bloqueando las enzimas necesarias para la síntesis de ADN o incorporándose al ADN o al ARN. Al inhibir las enzimas implicadas en la síntesis del ADN, previenen la mitosis porque el ADN no puede duplicarse. Además, después de una mala incorporación de las moléculas al ADN, se puede producir daño en el ADN y se induce la muerte celular programada ( apoptosis ). A diferencia de los agentes alquilantes, los antimetabolitos dependen del ciclo celular. Esto significa que sólo funcionan durante una parte específica del ciclo celular, en este caso la fase S (la fase de síntesis de ADN). Por esta razón, a una dosis determinada, el efecto se estabiliza y, proporcionalmente, no se produce más muerte celular con dosis aumentadas. Los subtipos de antimetabolitos son los antifolatos , las fluoropirimidinas, los análogos de desoxinucleósidos y las tiopurinas . [37] [42]
Los antifolatos incluyen metotrexato y pemetrexed . El metotrexato inhibe la dihidrofolato reductasa (DHFR), una enzima que regenera el tetrahidrofolato a partir del dihidrofolato . Cuando la enzima es inhibida por el metotrexato, los niveles celulares de coenzimas de folato disminuyen. Estos son necesarios para la producción de timidilato y purina, que son esenciales para la síntesis de ADN y la división celular. [6] : 55–59 [7] : 11 El pemetrexed es otro antimetabolito que afecta la producción de purinas y pirimidinas y, por lo tanto, también inhibe la síntesis de ADN. Inhibe principalmente la enzima timidilato sintasa , pero también tiene efectos sobre la DHFR, la aminoimidazol carboxamida ribonucleótido formiltransferasa y la glicinamida ribonucleótido formiltransferasa . [43] Las fluoropirimidinas incluyen fluorouracilo y capecitabina . El fluorouracilo es un análogo de nucleobase que se metaboliza en las células para formar al menos dos productos activos; Monofosfato de 5-fluorouridina (FUMP) y 5'-fosfato de 5-fluoro-2'-desoxiuridina (fdUMP). FUMP se incorpora al ARN y fdUMP inhibe la enzima timidilato sintasa; ambos conducen a la muerte celular. [7] : 11 La capecitabina es un profármaco del 5-fluorouracilo que se descompone en las células para producir el fármaco activo. [44] Los análogos de desoxinucleósidos incluyen citarabina , gemcitabina , decitabina , azacitidina , fludarabina , nelarabina , cladribina , clofarabina y pentostatina . Las tiopurinas incluyen tioguanina y mercaptopurina . [37] [42]

Los agentes antimicrotúbulos son sustancias químicas de origen vegetal que bloquean la división celular impidiendo la función de los microtúbulos . Los microtúbulos son una estructura celular importante compuesta por dos proteínas, α-tubulina y β-tubulina . Son estructuras huecas con forma de varilla que son necesarias para la división celular, entre otras funciones celulares. [45] Los microtúbulos son estructuras dinámicas, lo que significa que están permanentemente en estado de montaje y desmontaje. Los alcaloides de la vinca y los taxanos son los dos grupos principales de agentes antimicrotúbulos, y aunque ambos grupos de fármacos causan disfunción de los microtúbulos, sus mecanismos de acción son completamente opuestos: los alcaloides de la vinca impiden el ensamblaje de los microtúbulos, mientras que los taxanos impiden su desmontaje. Al hacerlo, pueden inducir una catástrofe mitótica en las células cancerosas. [46] Después de esto, se produce la detención del ciclo celular, lo que induce la muerte celular programada ( apoptosis ). [37] [47] Estos medicamentos también pueden afectar el crecimiento de los vasos sanguíneos , un proceso esencial que los tumores utilizan para crecer y metastatizar. [47]
Los alcaloides de la vinca se derivan del bígaro de Madagascar , Catharanthus roseus , [48] [49] anteriormente conocido como Vinca rosea . Se unen a sitios específicos de la tubulina, inhibiendo el ensamblaje de la tubulina en microtúbulos. Los alcaloides originales de la vinca son productos naturales que incluyen vincristina y vinblastina . [50] [51] [52] [53] Tras el éxito de estos fármacos, se produjeron alcaloides de vinca semisintéticos : vinorelbina (utilizado en el tratamiento del cáncer de pulmón de células no pequeñas [52] [54] [55] ), vindesina y vinflunina . [47] Estos medicamentos son específicos del ciclo celular . Se unen a las moléculas de tubulina en la fase S e impiden la formación adecuada de microtúbulos necesaria para la fase M. [39]
Los taxanos son drogas naturales y semisintéticas. El primer fármaco de su clase, el paclitaxel , se extrajo originalmente del Taxus brevifolia , el tejo del Pacífico. Ahora bien, este fármaco y otro de esta clase, el docetaxel , se producen de forma semisintética a partir de una sustancia química que se encuentra en la corteza de otro tejo, Taxus baccata . [56]
La podofilotoxina es un lignano antineoplásico obtenido principalmente del mayapple americano ( Podophyllum peltatum ) y del mayapple del Himalaya ( Sinopodophyllum hexandrum ). Tiene actividad antimicrotúbulos y su mecanismo es similar al de los alcaloides de la vinca en el sentido de que se unen a la tubulina, inhibiendo la formación de microtúbulos. La podofilotoxina se utiliza para producir otros dos fármacos con diferentes mecanismos de acción: etopósido y tenipósido . [57] [58]

Los inhibidores de la topoisomerasa son fármacos que afectan la actividad de dos enzimas: la topoisomerasa I y la topoisomerasa II . Cuando la hélice de doble hebra del ADN se desenrolla, durante la replicación o transcripción del ADN , por ejemplo, el ADN adyacente sin abrir se enrolla más apretado (superenrollamientos), como si se abriera la mitad de una cuerda retorcida. El estrés causado por este efecto se ve favorecido en parte por las enzimas topoisomerasas. Producen roturas de una o dos hebras en el ADN, reduciendo la tensión en la hebra de ADN. Esto permite que se produzca el desenrollado normal del ADN durante la replicación o transcripción. La inhibición de la topoisomerasa I o II interfiere con ambos procesos. [59] [60]
Dos inhibidores de la topoisomerasa I, el irinotecán y el topotecán , se derivan de forma semisintética de la camptotecina , que se obtiene del árbol ornamental chino Camptotheca acuminata . [39] Los medicamentos que se dirigen a la topoisomerasa II se pueden dividir en dos grupos. Los venenos de topoisomerasa II provocan niveles elevados de enzimas unidas al ADN. Esto previene la replicación y transcripción del ADN, provoca roturas en las cadenas de ADN y conduce a la muerte celular programada ( apoptosis ). Estos agentes incluyen etopósido , doxorrubicina , mitoxantrona y tenipósido . El segundo grupo, los inhibidores catalíticos, son fármacos que bloquean la actividad de la topoisomerasa II y, por tanto, impiden la síntesis y traducción del ADN porque el ADN no puede desenrollarse correctamente. Este grupo incluye novobiocina , merbarona y aclarubicina , que también tienen otros mecanismos de acción importantes. [61]
Los antibióticos citotóxicos son un grupo variado de fármacos que tienen diversos mecanismos de acción. El tema común que comparten en su indicación de quimioterapia es que interrumpen la división celular . El subgrupo más importante son las antraciclinas y las bleomicinas ; otros ejemplos destacados incluyen la mitomicina C y la actinomicina . [62]
Entre las antraciclinas, la doxorrubicina y la daunorrubicina fueron las primeras, y se obtuvieron de la bacteria Streptomyces peucetius . [63] Los derivados de estos compuestos incluyen epirrubicina e idarrubicina . Otros fármacos del grupo de las antraciclinas de uso clínico son la pirarubicina , la aclarubicina y la mitoxantrona . [64] Los mecanismos de las antraciclinas incluyen la intercalación de ADN (las moléculas se insertan entre las dos hebras de ADN), la generación de radicales libres altamente reactivos que dañan las moléculas intercelulares y la inhibición de la topoisomerasa. [sesenta y cinco]
La actinomicina es una molécula compleja que intercala el ADN e impide la síntesis de ARN . [66]
La bleomicina, un glicopéptido aislado de Streptomyces verticillus , también intercala el ADN, pero produce radicales libres que dañan el ADN. Esto ocurre cuando la bleomicina se une a un ion metálico , se reduce químicamente y reacciona con el oxígeno . [67] [6] : 87
La mitomicina es un antibiótico citotóxico con la capacidad de alquilar el ADN. [68]

La mayor parte de la quimioterapia se administra por vía intravenosa , aunque varios agentes se pueden administrar por vía oral (p. ej., melfalán , busulfán , capecitabina ). Según una revisión sistemática reciente (2016), las terapias orales presentan desafíos adicionales para que los pacientes y los equipos de atención mantengan y respalden el cumplimiento de los planes de tratamiento. [69]
Existen muchos métodos intravenosos de administración de medicamentos, conocidos como dispositivos de acceso vascular. Estos incluyen el dispositivo de infusión con alas , el catéter venoso periférico , el catéter de línea media, el catéter central de inserción periférica (PICC), el catéter venoso central y el puerto implantable . Los dispositivos tienen diferentes aplicaciones en cuanto a la duración del tratamiento de quimioterapia, el método de administración y los tipos de agente quimioterapéutico. [7] : 94–95
Dependiendo de la persona, el cáncer, la etapa del cáncer, el tipo de quimioterapia y la dosis, la quimioterapia intravenosa se puede administrar de forma hospitalaria o ambulatoria . Para la administración de quimioterapia intravenosa continua, frecuente o prolongada, se pueden insertar quirúrgicamente varios sistemas en la vasculatura para mantener el acceso. [7] : 113–118 Los sistemas más utilizados son la línea Hickman , el Port-a-Cath y la línea PICC . Tienen un menor riesgo de infección, son mucho menos propensos a la flebitis o extravasación y eliminan la necesidad de insertar repetidamente cánulas periféricas. [70]
Para tratar algunos tumores se ha utilizado la perfusión aislada de las extremidades (a menudo utilizada en el melanoma ), [71] o la infusión aislada de quimioterapia en el hígado [72] o el pulmón. El objetivo principal de estos enfoques es administrar una dosis muy alta de quimioterapia en los sitios del tumor sin causar un daño sistémico abrumador. [73] Estos enfoques pueden ayudar a controlar las metástasis solitarias o limitadas, pero, por definición, no son sistémicos y, por lo tanto, no tratan las metástasis distribuidas ni las micrometástasis . [ cita necesaria ]
Las quimioterapias tópicas, como el 5-fluorouracilo , se utilizan para tratar algunos casos de cáncer de piel no melanoma . [74]
Si el cáncer afecta el sistema nervioso central o tiene enfermedad meníngea, se puede administrar quimioterapia intratecal . [4]
Las técnicas de quimioterapia tienen una variedad de efectos secundarios que dependen del tipo de medicamento utilizado. Los medicamentos más comunes afectan principalmente a las células del cuerpo que se dividen rápidamente , como las células sanguíneas y las células que recubren la boca, el estómago y los intestinos. Las toxicidades relacionadas con la quimioterapia pueden ocurrir de forma aguda después de la administración, en cuestión de horas o días, o de forma crónica, de semanas a años. [6] : 265
Prácticamente todos los regímenes quimioterapéuticos pueden causar depresión del sistema inmunológico , a menudo paralizando la médula ósea y provocando una disminución de los glóbulos blancos , rojos y plaquetas . La anemia y la trombocitopenia pueden requerir transfusión de sangre . La neutropenia (una disminución del recuento de granulocitos de neutrófilos por debajo de 0,5 x 10 9 / litro ) se puede mejorar con G-CSF sintético ( factor estimulante de colonias de granulocitos , por ejemplo, filgrastim , lenograstim , efbemalenograstim alfa ). [75]
En la mielosupresión muy grave , que ocurre en algunos regímenes, casi todas las células madre de la médula ósea (células que producen glóbulos blancos y rojos ) se destruyen, lo que significa que son necesarios trasplantes alogénicos o autólogos de células de la médula ósea . (En los TMO autólogos, las células se extraen de la persona antes del tratamiento, se multiplican y luego se reinyectan; en los TMO alogénicos , la fuente es un donante). Sin embargo, algunas personas aún desarrollan enfermedades debido a esta interferencia con la médula ósea. [76]
Aunque se anima a las personas que reciben quimioterapia a lavarse las manos, evitar a las personas enfermas y tomar otras medidas para reducir las infecciones, alrededor del 85% de las infecciones se deben a microorganismos que se encuentran naturalmente en el propio tracto gastrointestinal (incluida la cavidad bucal ) y la piel de la persona. [77] : 130 Esto puede manifestarse como infecciones sistémicas, como sepsis , o como brotes localizados, como herpes simple , culebrilla u otros miembros de Herpesviridea . [78] El riesgo de enfermedad y muerte se puede reducir tomando antibióticos comunes como quinolonas o trimetoprim/sulfametoxazol antes de que aparezca cualquier fiebre o signo de infección. [79] Las quinolonas muestran una profilaxis eficaz principalmente en el cáncer hematológico. [79] Sin embargo, en general, por cada cinco personas inmunodeprimidas después de la quimioterapia que toman un antibiótico, se puede prevenir una fiebre; por cada 34 que toman un antibiótico, se puede evitar una muerte. [79] A veces, los tratamientos de quimioterapia se posponen porque el sistema inmunológico está suprimido a un nivel críticamente bajo. [ cita necesaria ]
En Japón , el gobierno ha aprobado el uso de algunos hongos medicinales como Trametes versicolor , para contrarrestar la depresión del sistema inmunológico en personas sometidas a quimioterapia. [80]
Trilaciclib es un inhibidor de la quinasa 4/6 dependiente de ciclina aprobado para la prevención de la mielosupresión causada por la quimioterapia. El medicamento se administra antes de la quimioterapia para proteger la función de la médula ósea. [81]
Debido a la supresión del sistema inmunológico, la enterocolitis neutropénica (tiflitis) es una "complicación gastrointestinal de la quimioterapia que pone en peligro la vida". [82] La tiflitis es una infección intestinal que puede manifestarse a través de síntomas que incluyen náuseas , vómitos , diarrea , abdomen distendido , fiebre , escalofríos o dolor y sensibilidad abdominal . [83]
La tiflitis es una emergencia médica . Tiene un pronóstico muy malo y a menudo es fatal a menos que se reconozca rápidamente y se trate agresivamente. [84] El tratamiento exitoso depende del diagnóstico temprano proporcionado por un alto índice de sospecha y el uso de tomografía computarizada, tratamiento no quirúrgico para casos no complicados y, a veces, hemicolectomía derecha electiva para prevenir la recurrencia. [84]
Náuseas , vómitos , anorexia , diarrea , calambres abdominales y estreñimiento son efectos secundarios comunes de los medicamentos quimioterapéuticos que matan las células que se dividen rápidamente. [85] La desnutrición y la deshidratación pueden ocurrir cuando el receptor no come o bebe lo suficiente, o cuando la persona vomita con frecuencia, debido a daño gastrointestinal. Esto puede resultar en una rápida pérdida de peso, o en ocasiones en un aumento de peso, si la persona come demasiado en un esfuerzo por aliviar las náuseas o la acidez de estómago. El aumento de peso también puede deberse a algunos medicamentos esteroides. Estos efectos secundarios frecuentemente pueden reducirse o eliminarse con fármacos antieméticos . La evidencia de certeza baja también sugiere que los probióticos pueden tener un efecto preventivo y de tratamiento de la diarrea relacionada con la quimioterapia sola y con la radioterapia. [86] Sin embargo, es apropiado un alto índice de sospecha, ya que la diarrea y la hinchazón también son síntomas de tiflitis , una emergencia médica muy grave y potencialmente mortal que requiere tratamiento inmediato. [87]
La anemia puede ser un resultado combinado causado por la quimioterapia mielosupresora y posibles causas relacionadas con el cáncer, como sangrado , destrucción de células sanguíneas ( hemólisis ), enfermedades hereditarias, disfunción renal, deficiencias nutricionales o anemia de enfermedades crónicas . Los tratamientos para mitigar la anemia incluyen hormonas para estimular la producción de sangre ( eritropoyetina ), suplementos de hierro y transfusiones de sangre . [88] [89] [90] La terapia mielosupresora puede provocar una tendencia a sangrar fácilmente, lo que provoca anemia. Los medicamentos que matan las células sanguíneas o las células que se dividen rápidamente pueden reducir la cantidad de plaquetas en la sangre, lo que puede provocar hematomas y sangrado . Los recuentos de plaquetas extremadamente bajos pueden aumentar temporalmente mediante transfusiones de plaquetas y se están desarrollando nuevos medicamentos para aumentar los recuentos de plaquetas durante la quimioterapia. [91] [92] [93] [94] A veces, los tratamientos de quimioterapia se posponen para permitir que se recuperen los recuentos de plaquetas.
La fatiga puede ser una consecuencia del cáncer o de su tratamiento y puede durar meses o años después del tratamiento. Una causa fisiológica de la fatiga es la anemia, que puede ser causada por quimioterapia, cirugía , radioterapia , enfermedad primaria y metastásica o por agotamiento nutricional. [95] [96] Se ha descubierto que el ejercicio aeróbico es beneficioso para reducir la fatiga en personas con tumores sólidos . [97]
Las náuseas y los vómitos son dos de los efectos secundarios relacionados con el tratamiento del cáncer más temidos por las personas con cáncer y sus familias. En 1983, Coates et al. descubrió que las personas que recibían quimioterapia clasificaron las náuseas y los vómitos como el primer y segundo efecto secundario más grave, respectivamente. [98] Hasta el 20% de las personas que recibían agentes altamente emetógenos en esta época pospusieron, o incluso rechazaron, tratamientos potencialmente curativos. [99] Las náuseas y los vómitos inducidos por la quimioterapia (CINV) son comunes en muchos tratamientos y en algunas formas de cáncer. Desde la década de 1990, se han desarrollado y comercializado varias clases novedosas de antieméticos , que se han convertido en un estándar casi universal en los regímenes de quimioterapia y han ayudado a controlar con éxito estos síntomas en muchas personas. La mediación efectiva de estos síntomas desagradables y a veces debilitantes da como resultado una mayor calidad de vida para el receptor y ciclos de tratamiento más eficientes, debido a una menor interrupción del tratamiento debido a una mejor tolerancia y una mejor salud general. [100]

La caída del cabello (alopecia) puede ser causada por la quimioterapia que mata las células que se dividen rápidamente; Otros medicamentos pueden hacer que el cabello se adelgace. La mayoría de las veces se trata de efectos temporales: el cabello suele empezar a volver a crecer unas semanas después del último tratamiento, pero a veces con un cambio de color, textura, grosor o estilo. A veces, el cabello tiende a rizarse después de volver a crecer, lo que resulta en "rizos de quimioterapia". La caída severa del cabello ocurre con mayor frecuencia con medicamentos como doxorrubicina , daunorrubicina , paclitaxel , docetaxel , ciclofosfamida , ifosfamida y etopósido . Algunos regímenes de quimioterapia estándar pueden provocar debilitamiento o caída permanente del cabello. [101]
La caída del cabello inducida por la quimioterapia se produce mediante un mecanismo no androgénico y puede manifestarse como alopecia total , efluvio telógeno o, con menor frecuencia, alopecia areata . [102] Generalmente se asocia con tratamiento sistémico debido a la alta tasa mitótica de los folículos pilosos, y es más reversible que la caída del cabello androgénica, [103] [104] aunque pueden ocurrir casos permanentes. [105] La quimioterapia induce la caída del cabello en las mujeres con más frecuencia que en los hombres. [106]
El enfriamiento del cuero cabelludo ofrece un medio para prevenir la caída del cabello tanto permanente como temporal; sin embargo, han surgido preocupaciones sobre este método. [107] [108]
Puede ocurrir el desarrollo de neoplasia secundaria después de un tratamiento exitoso de quimioterapia o radioterapia. La neoplasia secundaria más común es la leucemia mieloide aguda secundaria, que se desarrolla principalmente después del tratamiento con agentes alquilantes o inhibidores de la topoisomerasa. [109] Los sobrevivientes de cáncer infantil tienen más de 13 veces más probabilidades de sufrir una neoplasia secundaria durante los 30 años posteriores al tratamiento que la población general. [110] No todo este aumento puede atribuirse a la quimioterapia.
Algunos tipos de quimioterapia son gonadotóxicos y pueden causar infertilidad . [111] Las quimioterapias con alto riesgo incluyen procarbazina y otros fármacos alquilantes como ciclofosfamida, ifosfamida, busulfán, melfalán, clorambucilo y clormetina. [111] Los medicamentos con riesgo medio incluyen la doxorrubicina y los análogos del platino, como el cisplatino y el carboplatino. [111] Por otro lado, las terapias con bajo riesgo de gonadotoxicidad incluyen derivados vegetales como vincristina y vinblastina, antibióticos como bleomicina y dactinomicina, y antimetabolitos como metotrexato, mercaptopurina y 5-fluorouracilo. [111]
La infertilidad femenina por quimioterapia parece ser secundaria a una falla ovárica prematura por pérdida de folículos primordiales . [112] Esta pérdida no es necesariamente un efecto directo de los agentes quimioterapéuticos, pero podría deberse a una mayor tasa de inicio del crecimiento para reemplazar los folículos en desarrollo dañados. [112]
Las personas pueden elegir entre varios métodos de preservación de la fertilidad antes de la quimioterapia, incluida la criopreservación de semen, tejido ovárico, ovocitos o embriones. [113] Como más de la mitad de los pacientes con cáncer son ancianos, este efecto adverso sólo es relevante para una minoría de pacientes. Un estudio realizado en Francia entre 1999 y 2011 llegó a la conclusión de que la congelación de embriones antes de la administración de agentes gonadotóxicos a las hembras provocaba un retraso en el tratamiento en el 34% de los casos, y un nacimiento vivo en el 27% de los casos supervivientes que querían quedar embarazadas, con el tiempo de seguimiento varía entre 1 y 13 años. [114]
Los posibles agentes protectores o atenuantes incluyen análogos de GnRH , donde varios estudios han demostrado un efecto protector in vivo en humanos, pero algunos estudios no muestran tal efecto. La esfingosina-1-fosfato (S1P) ha mostrado un efecto similar, pero su mecanismo de inhibición de la vía apoptótica de la esfingomielina también puede interferir con la acción de apoptosis de los fármacos quimioterapéuticos. [115]
En el caso de la quimioterapia como régimen de acondicionamiento en el trasplante de células madre hematopoyéticas, un estudio de personas condicionadas con ciclofosfamida sola para la anemia aplásica grave llegó al resultado de que la recuperación ovárica se produjo en todas las mujeres menores de 26 años en el momento del trasplante, pero sólo en cinco de 16 mujeres mayores de 26 años. [116]
La quimioterapia es teratogénica durante el embarazo , especialmente durante el primer trimestre , al punto que generalmente se recomienda el aborto si se detecta embarazo en este período durante la quimioterapia. [117] La exposición durante el segundo y tercer trimestre generalmente no aumenta el riesgo teratogénico ni los efectos adversos sobre el desarrollo cognitivo, pero puede aumentar el riesgo de diversas complicaciones del embarazo y mielosupresión fetal. [117]
Las pacientes femeninas en edad fértil deben utilizar métodos anticonceptivos eficaces durante la quimioterapia y durante algunos meses después de la última dosis (p. ej., 6 meses para doxorrubicina [118] ).
En los varones que previamente se han sometido a quimioterapia o radioterapia, no parece haber ningún aumento de defectos genéticos o malformaciones congénitas en sus hijos concebidos después de la terapia. [117] El uso de tecnologías de reproducción asistida y técnicas de micromanipulación podría aumentar este riesgo. [117] En mujeres que se han sometido previamente a quimioterapia, los abortos espontáneos y las malformaciones congénitas no aumentan en concepciones posteriores. [117] Sin embargo, cuando se practica la fertilización in vitro y la criopreservación de embriones entre el tratamiento o poco después, existen posibles riesgos genéticos para los ovocitos en crecimiento y, por lo tanto, se ha recomendado que los bebés sean examinados. [117]
Entre el 30 y el 40 por ciento de las personas que reciben quimioterapia experimentan neuropatía periférica inducida por la quimioterapia (CIPN), una afección progresiva, duradera y a menudo irreversible, que causa dolor, hormigueo, entumecimiento y sensibilidad al frío, que comienza en las manos y los pies y a veces progresa hasta los brazos y las piernas. [119] Los medicamentos de quimioterapia asociados con la CIPN incluyen talidomida , epotilonas , alcaloides de la vinca , taxanos, inhibidores del proteasoma y medicamentos a base de platino. [119] [120] Si surge CIPN y en qué grado, está determinado por la elección del medicamento, la duración del uso, la cantidad total consumida y si la persona ya tiene neuropatía periférica . Aunque los síntomas son principalmente sensoriales, en algunos casos se ven afectados los nervios motores y el sistema nervioso autónomo . [121] La CIPN a menudo sigue a la primera dosis de quimioterapia y su gravedad aumenta a medida que continúa el tratamiento, pero esta progresión generalmente se estabiliza al finalizar el tratamiento. Los medicamentos a base de platino son la excepción; Con estos medicamentos, la sensación puede continuar deteriorándose durante varios meses después de finalizar el tratamiento. [122] Algunas CIPN parecen ser irreversibles. [122] El dolor a menudo se puede controlar con medicamentos u otro tratamiento, pero el entumecimiento suele ser resistente al tratamiento. [123]
Algunas personas que reciben quimioterapia informan fatiga o problemas neurocognitivos no específicos, como incapacidad para concentrarse; A esto a veces se le llama deterioro cognitivo posquimioterapia , denominado "cerebro de quimioterapia" en las redes sociales y populares. [124]
En tumores particularmente grandes y cánceres con recuentos elevados de glóbulos blancos , como linfomas , teratomas y algunas leucemias , algunas personas desarrollan síndrome de lisis tumoral . La rápida degradación de las células cancerosas provoca la liberación de sustancias químicas desde el interior de las células. A continuación, se encuentran niveles elevados de ácido úrico , potasio y fosfato en la sangre. Los niveles altos de fosfato inducen hipoparatiroidismo secundario, lo que resulta en niveles bajos de calcio en la sangre. [125] Esto causa daño renal y los altos niveles de potasio pueden causar arritmia cardíaca . Aunque la profilaxis está disponible y a menudo se inicia en personas con tumores grandes, este es un efecto secundario peligroso que puede provocar la muerte si no se trata. [7] : 202
La cardiotoxicidad (daño cardíaco) es especialmente prominente con el uso de antraciclinas ( doxorrubicina , epirrubicina , idarrubicina y doxorrubicina liposomal ). Lo más probable es que la causa de esto se deba a la producción de radicales libres en la célula y al daño posterior del ADN . Otros agentes quimioterapéuticos que causan cardiotoxicidad, pero con menor incidencia, son la ciclofosfamida , el docetaxel y la clofarabina . [126]
La hepatotoxicidad (daño hepático) puede ser causada por muchos fármacos citotóxicos. La susceptibilidad de un individuo al daño hepático puede verse alterada por otros factores como el propio cáncer, la hepatitis viral , la inmunosupresión y la deficiencia nutricional . El daño hepático puede consistir en daño a las células del hígado, síndrome sinusoidal hepático (obstrucción de las venas del hígado), colestasis (donde la bilis no fluye del hígado al intestino) y fibrosis hepática . [127] [128]
La nefrotoxicidad (daño renal) puede ser causada por el síndrome de lisis tumoral y también por los efectos directos de la eliminación del fármaco por los riñones. Diferentes medicamentos afectarán diferentes partes del riñón y la toxicidad puede ser asintomática (solo se observa en análisis de sangre u orina) o puede causar lesión renal aguda . [129] [130]
La ototoxicidad (daño al oído interno) es un efecto secundario común de los medicamentos a base de platino que puede producir síntomas como mareos y vértigo . [131] [132] Se ha descubierto que los niños tratados con análogos del platino corren riesgo de desarrollar pérdida auditiva. [133] [134] [135]
Los efectos secundarios menos comunes incluyen enrojecimiento de la piel ( eritema ), piel seca, uñas dañadas, boca seca ( xerostomía ), retención de líquidos e impotencia sexual . Algunos medicamentos pueden desencadenar reacciones alérgicas o pseudoalérgicas .
Los agentes quimioterapéuticos específicos se asocian con toxicidades específicas de órganos, incluidas enfermedades cardiovasculares (p. ej., doxorrubicina ), enfermedad pulmonar intersticial (p. ej., bleomicina ) y ocasionalmente neoplasias secundarias (p. ej., terapia MOPP para la enfermedad de Hodgkin). [136]
El síndrome mano-pie es otro efecto secundario de la quimioterapia citotóxica. [137]
Los problemas nutricionales también se observan con frecuencia en pacientes con cáncer en el momento del diagnóstico y durante el tratamiento de quimioterapia. Las investigaciones sugieren que en niños y jóvenes sometidos a tratamiento contra el cáncer, la nutrición parenteral puede ayudar a lograr un aumento de peso y una mayor ingesta de calorías y proteínas, en comparación con la nutrición enteral. [138]
La quimioterapia no siempre funciona e incluso cuando es útil, es posible que no destruya completamente el cáncer. La gente frecuentemente no comprende sus limitaciones. En un estudio de personas a las que se les había diagnosticado recientemente cáncer incurable en etapa 4 , más de dos tercios de las personas con cáncer de pulmón y más de cuatro quintas partes de las personas con cáncer colorrectal todavía creían que la quimioterapia probablemente curaría su cáncer. [139]
La barrera hematoencefálica plantea un obstáculo para la administración de quimioterapia al cerebro . Esto se debe a que el cerebro cuenta con un extenso sistema para protegerlo de sustancias químicas nocivas. Los transportadores de fármacos pueden bombear fármacos desde el cerebro y las células de los vasos sanguíneos del cerebro hacia el líquido cefalorraquídeo y la circulación sanguínea. Estos transportadores bombean la mayoría de los fármacos de quimioterapia, lo que reduce su eficacia en el tratamiento de tumores cerebrales. Sólo los agentes alquilantes lipófilos pequeños , como la lomustina o la temozolomida , pueden cruzar esta barrera hematoencefálica. [140] [141] [142]
Los vasos sanguíneos de los tumores son muy diferentes de los que se observan en los tejidos normales. A medida que un tumor crece, las células tumorales más alejadas de los vasos sanguíneos pierden oxígeno ( hipóxicas ). Para contrarrestar esto, envían señales para que crezcan nuevos vasos sanguíneos. La vasculatura tumoral recién formada está mal formada y no suministra un suministro de sangre adecuado a todas las áreas del tumor. Esto genera problemas con la administración de medicamentos porque el sistema circulatorio entregará muchos medicamentos al tumor . [143]
La resistencia es una de las principales causas del fracaso del tratamiento con fármacos quimioterapéuticos. Existen algunas causas posibles de resistencia en el cáncer, una de las cuales es la presencia de pequeñas bombas en la superficie de las células cancerosas que mueven activamente la quimioterapia desde el interior de la célula hacia el exterior. Las células cancerosas producen grandes cantidades de estas bombas, conocidas como glicoproteína p , para protegerse de la quimioterapia. Actualmente se están llevando a cabo investigaciones sobre la glicoproteína p y otras bombas de eflujo de quimioterapia similares. Se están investigando medicamentos para inhibir la función de la glicoproteína p, pero debido a las toxicidades y las interacciones con medicamentos contra el cáncer su desarrollo ha sido difícil. [144] [145] Otro mecanismo de resistencia es la amplificación genética , un proceso en el que las células cancerosas producen múltiples copias de un gen. Esto supera el efecto de los fármacos que reducen la expresión de genes implicados en la replicación. Con más copias del gen, el fármaco no puede impedir toda la expresión del gen y, por tanto, la célula puede restaurar su capacidad proliferativa. Las células cancerosas también pueden causar defectos en las vías celulares de apoptosis (muerte celular programada). Como la mayoría de los medicamentos de quimioterapia matan las células cancerosas de esta manera, la apoptosis defectuosa permite la supervivencia de estas células, haciéndolas resistentes. Muchos medicamentos de quimioterapia también causan daños en el ADN, que pueden repararse mediante enzimas en la célula que llevan a cabo la reparación del ADN . La regulación positiva de estos genes puede superar el daño del ADN y prevenir la inducción de la apoptosis. Pueden ocurrir mutaciones en los genes que producen proteínas diana de los fármacos, como la tubulina , que impiden que los fármacos se unan a la proteína, lo que genera resistencia a este tipo de fármacos. [146] Los medicamentos utilizados en la quimioterapia pueden inducir estrés celular, que puede matar una célula cancerosa; sin embargo, bajo ciertas condiciones, el estrés de las células puede inducir cambios en la expresión genética que permiten la resistencia a varios tipos de fármacos. [147] En el cáncer de pulmón , se cree que el factor de transcripción NFκB desempeña un papel en la resistencia a la quimioterapia, a través de vías inflamatorias. [148] [149] [150]
Las terapias dirigidas son una clase relativamente nueva de medicamentos contra el cáncer que pueden superar muchos de los problemas observados con el uso de citotóxicos. Se dividen en dos grupos: moléculas pequeñas y anticuerpos. La toxicidad masiva observada con el uso de citotóxicos se debe a la falta de especificidad celular de los fármacos. Matarán cualquier célula, tumoral o normal, que se divida rápidamente. Las terapias dirigidas están diseñadas para afectar las proteínas o procesos celulares que utilizan las células cancerosas. [151] Esto permite una dosis alta para los tejidos cancerosos con una dosis relativamente baja para otros tejidos. Aunque los efectos secundarios suelen ser menos graves que los observados con los quimioterapéuticos citotóxicos, pueden producirse efectos potencialmente mortales. Inicialmente, se suponía que las terapias dirigidas serían selectivas únicamente para una proteína. Ahora está claro que a menudo existe una variedad de objetivos proteicos a los que el fármaco puede unirse. Un ejemplo de objetivo para la terapia dirigida es la proteína BCR-ABL1 producida a partir del cromosoma Filadelfia , una lesión genética que se encuentra comúnmente en la leucemia mielógena crónica y en algunos pacientes con leucemia linfoblástica aguda . Esta proteína de fusión tiene actividad enzimática que puede ser inhibida por imatinib , un fármaco de molécula pequeña . [152] [153] [154] [155]

El cáncer es el crecimiento descontrolado de células junto con un comportamiento maligno : invasión y metástasis (entre otras características). [156] Es causada por la interacción entre la susceptibilidad genética y factores ambientales. [157] [158] Estos factores conducen a acumulaciones de mutaciones genéticas en oncogenes (genes que controlan la tasa de crecimiento de las células) y genes supresores de tumores (genes que ayudan a prevenir el cáncer), lo que da a las células cancerosas sus características malignas, como la proliferación descontrolada. crecimiento. [159] : 93–94
En sentido amplio, la mayoría de los fármacos quimioterapéuticos actúan alterando la mitosis ( división celular ), dirigiéndose eficazmente a las células que se dividen rápidamente . Como estos fármacos dañan las células, se denominan citotóxicos . Previenen la mitosis mediante diversos mecanismos, incluido el daño al ADN y la inhibición de la maquinaria celular implicada en la división celular. [39] [160] Una teoría de por qué estos medicamentos matan las células cancerosas es que inducen una forma programada de muerte celular conocida como apoptosis . [161]
Como la quimioterapia afecta la división celular, los tumores con altas tasas de crecimiento (como la leucemia mielógena aguda y los linfomas agresivos , incluida la enfermedad de Hodgkin ) son más sensibles a la quimioterapia, ya que una mayor proporción de las células diana están experimentando división celular en cualquier momento. Las neoplasias malignas con tasas de crecimiento más lentas, como los linfomas indolentes, tienden a responder a la quimioterapia de manera mucho más modesta. [4] Los tumores heterogénicos también pueden mostrar diferentes sensibilidades a los agentes quimioterapéuticos, dependiendo de las poblaciones subclonales dentro del tumor. [162]
Las células del sistema inmunológico también contribuyen de manera crucial a los efectos antitumorales de la quimioterapia. [163] Por ejemplo, los fármacos quimioterapéuticos oxaliplatino y ciclofosfamida pueden provocar la muerte de las células tumorales de una manera detectable por el sistema inmunitario (llamada muerte celular inmunogénica ), que moviliza células inmunitarias con funciones antitumorales. [164] Los medicamentos quimioterapéuticos que causan la muerte inmunogénica de las células tumorales cancerosas pueden hacer que los tumores que no responden sean sensibles a la terapia de puntos de control inmunológico . [165]
Algunos fármacos de quimioterapia se utilizan en enfermedades distintas del cáncer, como los trastornos autoinmunes [166] y la discrasia de células plasmáticas no cancerosas . En algunos casos se suelen utilizar en dosis más bajas, lo que significa que se minimizan los efectos secundarios, [166] mientras que en otros casos se utilizan dosis similares a las que se utilizan para tratar el cáncer. El metotrexato se utiliza en el tratamiento de la artritis reumatoide (AR), [167] psoriasis , [168] espondilitis anquilosante [169] y esclerosis múltiple . [170] [171] Se cree que la respuesta antiinflamatoria observada en la AR se debe a aumentos en la adenosina , que causa inmunosupresión ; efectos sobre las vías de la enzima ciclooxigenasa -2 inmunorreguladora ; reducción de citoquinas proinflamatorias ; y propiedades antiproliferativas. [167] Aunque el metotrexato se usa para tratar tanto la esclerosis múltiple como la espondilitis anquilosante, su eficacia en estas enfermedades aún es incierta. [169] [170] [171] La ciclofosfamida a veces se usa para tratar la nefritis lúpica , un síntoma común del lupus eritematoso sistémico . [172] La dexametasona junto con bortezomib o melfalán se usa comúnmente como tratamiento para la amiloidosis AL . Recientemente, la bortezomida en combinación con ciclofosfamida y dexametasona también se ha mostrado prometedora como tratamiento para la amiloidosis AL. Otros medicamentos utilizados para tratar el mieloma, como la lenalidomida, se han mostrado prometedores en el tratamiento de la amiloidosis AL. [173]
Los fármacos de quimioterapia también se utilizan en regímenes de acondicionamiento previos al trasplante de médula ósea ( trasplante de células madre hematopoyéticas ). Los regímenes de acondicionamiento se utilizan para suprimir el sistema inmunológico del receptor a fin de permitir que se injerte un trasplante. La ciclofosfamida es un fármaco citotóxico común que se utiliza de esta manera y a menudo se utiliza junto con la irradiación corporal total . Los medicamentos quimioterapéuticos se pueden usar en dosis altas para eliminar permanentemente las células de la médula ósea del receptor (condicionamiento mieloablativo) o en dosis más bajas que evitarán la pérdida permanente de la médula ósea (condicionamiento no mieloablativo y de intensidad reducida). [174] Cuando se utiliza en entornos no relacionados con el cáncer, el tratamiento todavía se denomina "quimioterapia" y, a menudo, se realiza en los mismos centros de tratamiento que se utilizan para las personas con cáncer.
En la década de 1970, los medicamentos antineoplásicos (quimioterapia) fueron identificados como peligrosos, y desde entonces la Sociedad Estadounidense de Farmacéuticos del Sistema de Salud (ASHP) ha introducido el concepto de medicamentos peligrosos después de publicar una recomendación en 1983 sobre el manejo de medicamentos peligrosos. La adaptación de las regulaciones federales se produjo cuando la Administración de Salud y Seguridad Ocupacional (OSHA) de EE. UU. publicó por primera vez sus directrices en 1986 y luego las actualizó en 1996, 1999 y, más recientemente, en 2006. [175]
El Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) ha estado realizando desde entonces una evaluación en el lugar de trabajo con respecto a estos medicamentos. La exposición ocupacional a medicamentos antineoplásicos se ha relacionado con múltiples efectos sobre la salud, incluida la infertilidad y posibles efectos cancerígenos. El informe de alerta del NIOSH ha informado algunos casos, como uno en el que a una farmacéutica se le diagnosticó carcinoma papilar de células de transición. Doce años antes de que a la farmacéutica le diagnosticaran la enfermedad, había trabajado durante 20 meses en un hospital donde era responsable de preparar múltiples fármacos antineoplásicos. [176] La farmacéutica no tenía ningún otro factor de riesgo de cáncer y, por lo tanto, su cáncer se atribuyó a la exposición a los medicamentos antineoplásicos, aunque no se ha establecido una relación de causa y efecto en la literatura. Otro caso ocurrió cuando se cree que un mal funcionamiento en los gabinetes de bioseguridad expuso al personal de enfermería a medicamentos antineoplásicos. Las investigaciones revelaron evidencia de biomarcadores genotóxicos dos y nueve meses después de esa exposición.
Los fármacos antineoplásicos generalmente se administran por vía intravenosa , intramuscular , intratecal o subcutánea . En la mayoría de los casos, antes de administrar el medicamento al paciente, es necesario que varios trabajadores lo preparen y manipulen. Cualquier trabajador que participe en la manipulación, preparación o administración de medicamentos, o en la limpieza de objetos que hayan estado en contacto con medicamentos antineoplásicos, está potencialmente expuesto a medicamentos peligrosos [177] . Los trabajadores de la salud están expuestos a los medicamentos en diferentes circunstancias, como cuando los farmacéuticos y técnicos de farmacia preparan y manipulan medicamentos antineoplásicos y cuando las enfermeras y los médicos administran los medicamentos a los pacientes. Además, quienes son responsables de eliminar los medicamentos antineoplásicos en los centros de atención médica también corren riesgo de exposición. [178]
Se cree que la exposición dérmica es la principal vía de exposición debido al hecho de que se han encontrado cantidades significativas de agentes antineoplásicos en los guantes que usan los trabajadores de la salud que preparan, manipulan y administran los agentes. Otra vía de exposición digna de mención es la inhalación de los vapores de la droga. Múltiples estudios han investigado la inhalación como vía de exposición y, aunque las muestras de aire no han mostrado niveles peligrosos, sigue siendo una vía potencial de exposición. La ingestión de la mano a la boca es una vía de exposición menos probable en comparación con otras debido a las normas de higiene aplicadas en las instituciones de salud. Sin embargo, sigue siendo una vía potencial, especialmente en el lugar de trabajo, fuera de un instituto de salud. Uno también puede estar expuesto a estas drogas peligrosas mediante inyecciones mediante pinchazos con agujas . Las investigaciones realizadas en esta área han establecido que la exposición ocupacional ocurre al examinar evidencia en múltiples muestras de orina de trabajadores de la salud. [179]
Las drogas peligrosas exponen a los trabajadores de la salud a graves riesgos para la salud. Muchos estudios muestran que los fármacos antineoplásicos podrían tener muchos efectos secundarios en el sistema reproductivo, como pérdida fetal, malformaciones congénitas e infertilidad. Los trabajadores de la salud que están expuestos a medicamentos antineoplásicos en muchas ocasiones tienen resultados reproductivos adversos, como abortos espontáneos, muertes fetales y malformaciones congénitas. Además, los estudios han demostrado que la exposición a estos medicamentos provoca irregularidades en el ciclo menstrual. Los medicamentos antineoplásicos también pueden aumentar el riesgo de problemas de aprendizaje entre los hijos de trabajadores de la salud que están expuestos a estas sustancias peligrosas. [180]
Además, estos fármacos tienen efectos cancerígenos . En las últimas cinco décadas, múltiples estudios han demostrado los efectos cancerígenos de la exposición a fármacos antineoplásicos. De manera similar, se han realizado estudios de investigación que relacionan los agentes alquilantes con el desarrollo de leucemias en humanos. Los estudios han informado un riesgo elevado de cáncer de mama, cáncer de piel no melanoma y cáncer de recto entre las enfermeras expuestas a estos medicamentos. Otras investigaciones revelaron que existe un posible efecto genotóxico de los medicamentos antineoplásicos en los trabajadores de entornos de atención médica. [176]
A partir de 2018, no había límites de exposición ocupacional establecidos para medicamentos antineoplásicos, es decir, OSHA o la Conferencia Estadounidense de Higienistas Industriales Gubernamentales (ACGIH) no han establecido pautas de seguridad en el lugar de trabajo. [181]
NIOSH recomienda utilizar un gabinete ventilado diseñado para disminuir la exposición de los trabajadores. Además, recomienda la capacitación de todo el personal, el uso de gabinetes, implementar una evaluación inicial de la técnica del programa de seguridad y el uso de guantes y batas protectoras al abrir envases de medicamentos, manipular viales o etiquetar. Al usar equipo de protección personal , se deben inspeccionar los guantes para detectar defectos físicos antes de usarlos y siempre usar guantes dobles y batas protectoras. Los trabajadores de la salud también deben lavarse las manos con agua y jabón antes y después de trabajar con medicamentos antineoplásicos, cambiarse los guantes cada 30 minutos o cada vez que se pinchen y desecharlos inmediatamente en un contenedor de desechos de quimioterapia. [182]
Las batas utilizadas deben ser batas desechables hechas de polipropileno recubierto de polietileno. Al usar batas, las personas deben asegurarse de que estén cerradas y tengan mangas largas. Cuando finalice la preparación, el producto final debe estar completamente sellado en una bolsa de plástico. [183]
El trabajador de la salud también debe limpiar todos los contenedores de desechos dentro del gabinete ventilado antes de sacarlos del gabinete. Finalmente, los trabajadores deben quitarse toda la ropa protectora y colocarla en una bolsa para su eliminación dentro del gabinete ventilado. [178]
Los medicamentos solo deben administrarse utilizando dispositivos médicos de protección, como listas de agujas y sistemas y técnicas cerrados, como el cebado de tubos intravenosos, por parte del personal de farmacia dentro de un gabinete ventilado. Los trabajadores siempre deben usar equipo de protección personal, como guantes dobles, gafas protectoras y batas protectoras al abrir la bolsa exterior y ensamblar el sistema de administración para entregar el medicamento al paciente, y al desechar todo el material utilizado en la administración de los medicamentos. [181]
Los trabajadores del hospital nunca deben quitar el tubo de una bolsa intravenosa que contenga un fármaco antineoplásico y, al desconectar el tubo del sistema, deben asegurarse de que se haya lavado completamente. Después de retirar la bolsa intravenosa, los trabajadores deben colocarla junto con otros artículos desechables directamente en el contenedor amarillo de desechos de quimioterapia con la tapa cerrada. Se debe quitar el equipo de protección y colocarlo en un recipiente desechable para desechos de quimioterapia. Una vez hecho esto, se deben colocar en bolsas dobles los desechos de la quimioterapia antes o después de quitarse los guantes internos. Además, siempre hay que lavarse las manos con agua y jabón antes de abandonar el lugar de administración del medicamento. [184]
Todos los empleados cuyos trabajos en centros de atención médica los exponen a medicamentos peligrosos deben recibir capacitación. La capacitación debe incluir al personal de envío y recepción, amas de llaves, farmacéuticos, asistentes y todas las personas involucradas en el transporte y almacenamiento de medicamentos antineoplásicos. Estas personas deben recibir información y capacitación para informarles sobre los peligros de las drogas presentes en sus áreas de trabajo. Deben ser informados y capacitados sobre las operaciones y procedimientos en sus áreas de trabajo donde pueden encontrar peligros, los diferentes métodos utilizados para detectar la presencia de drogas peligrosas y cómo se liberan los peligros, y los peligros físicos y para la salud de las drogas, incluidos sus efectos reproductivos. y potencial de riesgo cancerígeno. Además, se les debe informar y capacitar sobre las medidas que deben tomar para evitar y protegerse de estos peligros. Esta información debe proporcionarse cuando los trabajadores de la salud entran en contacto con los medicamentos, es decir, cuando realizan la tarea inicial en un área de trabajo con medicamentos peligrosos. Además, también se debe brindar capacitación cuando surjan nuevos peligros, así como cuando se introduzcan nuevos medicamentos, procedimientos o equipos. [181]
Al realizar la limpieza y descontaminación del área de trabajo donde se utilizan medicamentos antineoplásicos, se debe asegurarse de que haya suficiente ventilación para evitar la acumulación de concentraciones de medicamentos en el aire. Al limpiar la superficie de trabajo, los trabajadores del hospital deben utilizar agentes de desactivación y limpieza antes y después de cada actividad, así como al final de sus turnos. La limpieza debe realizarse siempre utilizando guantes de doble protección y batas desechables. Una vez que los empleados terminen de limpiar, deben desechar los elementos utilizados en la actividad en un contenedor amarillo de desechos de quimioterapia mientras aún usan guantes protectores. Después de quitarse los guantes, deben lavarse bien las manos con agua y jabón. Todo lo que entre en contacto o tenga rastros de los medicamentos antineoplásicos, como agujas, viales vacíos, jeringas, batas y guantes, debe depositarse en el contenedor de desechos de quimioterapia. [185]
Es necesario contar con una política escrita en caso de derrame de productos antineoplásicos. La política debe abordar la posibilidad de derrames de distintos tamaños, así como el procedimiento y el equipo de protección personal necesarios para cada tamaño. Un trabajador capacitado debe manejar un derrame grande y siempre desechar todos los materiales de limpieza en el contenedor de desechos químicos de acuerdo con las regulaciones de la EPA, no en un contenedor amarillo de desechos de quimioterapia. [186]
Se debe establecer un programa de vigilancia médica . En caso de exposición, los profesionales de la salud ocupacional deben solicitar una historia detallada y realizar un examen físico completo. Deben analizar la orina del trabajador potencialmente expuesto mediante una tira reactiva de orina o un examen microscópico, principalmente buscando sangre, ya que se sabe que varios medicamentos antineoplásicos causan daño a la vejiga. [176]
La mutagenicidad urinaria es un marcador de exposición a fármacos antineoplásicos que fue utilizado por primera vez por Falck y sus colegas en 1979 y utiliza ensayos de mutagenicidad bacteriana. Además de ser inespecífica, la prueba puede verse influenciada por factores extraños como la ingesta dietética y el tabaquismo y, por lo tanto, se utiliza con moderación. Sin embargo, la prueba jugó un papel importante en el cambio del uso de cabinas de flujo horizontal a cabinas de seguridad biológica de flujo vertical durante la preparación de medicamentos antineoplásicos porque las primeras exponían a los trabajadores de la salud a altos niveles de medicamentos. Esto cambió el manejo de los medicamentos y redujo efectivamente la exposición de los trabajadores a los medicamentos antineoplásicos. [176]
Los biomarcadores de exposición a fármacos antineoplásicos comúnmente incluyen platino en orina , metotrexato , ciclofosfamida e ifosfamida en orina y el metabolito urinario de 5-fluorouracilo . Además de esto, existen otros fármacos que se utilizan para medir los fármacos directamente en la orina, aunque rara vez se utilizan. Una medición de estos medicamentos directamente en la orina es un signo de altos niveles de exposición y de que la absorción de los medicamentos se produce por inhalación o por vía dérmica. [176]
Existe una extensa lista de agentes antineoplásicos . Se han utilizado varios esquemas de clasificación para subdividir los medicamentos utilizados contra el cáncer en varios tipos diferentes. [187] [188]


El primer uso de fármacos de molécula pequeña para tratar el cáncer se produjo a principios del siglo XX, aunque los productos químicos específicos que se utilizaron por primera vez no estaban destinados originalmente a ese fin. El gas mostaza se utilizó como agente de guerra química durante la Primera Guerra Mundial y se descubrió que era un potente supresor de la hematopoyesis (producción de sangre). [189] Una familia similar de compuestos conocidos como mostazas nitrogenadas se estudió más a fondo durante la Segunda Guerra Mundial en la Escuela de Medicina de Yale . [190] Se razonó que un agente que dañaba los glóbulos blancos de rápido crecimiento podría tener un efecto similar sobre el cáncer. [190] Por lo tanto, en diciembre de 1942, varias personas con linfomas avanzados (cánceres del sistema linfático y de los ganglios linfáticos) recibieron el fármaco por vía intravenosa, en lugar de respirar el gas irritante. [190] Su mejora, aunque temporal, fue notable. [191] Al mismo tiempo, durante una operación militar en la Segunda Guerra Mundial, tras un ataque aéreo alemán en el puerto italiano de Bari , varios cientos de personas quedaron expuestas accidentalmente al gas mostaza, que había sido transportado allí por las fuerzas aliadas para prepararse para posibles represalias. en caso de que Alemania utilice armas químicas. Más tarde se descubrió que los supervivientes tenían recuentos de glóbulos blancos muy bajos. [192] Después de que terminó la Segunda Guerra Mundial y los informes se desclasificaron, las experiencias convergieron y llevaron a los investigadores a buscar otras sustancias que pudieran tener efectos similares contra el cáncer. El primer fármaco de quimioterapia que se desarrolló a partir de esta línea de investigación fue la mustina . Desde entonces, se han desarrollado muchos otros medicamentos para tratar el cáncer, y el desarrollo de fármacos se ha convertido en una industria multimillonaria, aunque los principios y limitaciones de la quimioterapia descubiertos por los primeros investigadores todavía se aplican. [193]
La palabra quimioterapia sin modificador suele referirse al tratamiento del cáncer, pero su significado histórico era más amplio. El término fue acuñado a principios del siglo XX por Paul Ehrlich para referirse a cualquier uso de productos químicos para tratar cualquier enfermedad ( quimio- + -terapia ), como el uso de antibióticos ( quimioterapia antibacteriana ). [194] Ehrlich no se mostró optimista en cuanto a que se encontrarían fármacos de quimioterapia eficaces para el tratamiento del cáncer. [194] El primer agente quimioterapéutico moderno fue la arsfenamina , un compuesto de arsénico descubierto en 1907 y utilizado para tratar la sífilis . [195] A esto le siguieron más tarde las sulfonamidas (sulfamidas) y la penicilina . En el uso actual , el sentido "cualquier tratamiento de una enfermedad con fármacos" suele expresarse con la palabra farmacoterapia . En términos de lenguaje metafórico, la "quimioterapia" puede compararse con la idea de una "tormenta", ya que ambas pueden causar angustia pero después pueden tener un efecto curativo/limpiador.

Los vehículos de administración especialmente dirigidos tienen como objetivo aumentar los niveles efectivos de quimioterapia para las células tumorales y al mismo tiempo reducir los niveles efectivos para otras células. Esto debería dar como resultado una mayor destrucción de tumores, una reducción de la toxicidad o ambas. [196]
Los conjugados anticuerpo-fármaco (ADC) comprenden un anticuerpo , un fármaco y un conector entre ellos. El anticuerpo se dirigirá a una proteína expresada preferentemente en las células tumorales (conocida como antígeno tumoral ) o en células que el tumor puede utilizar, como las células endoteliales de los vasos sanguíneos . Se unen al antígeno tumoral y se internalizan, donde el conector libera el fármaco en la célula. Estos vehículos de administración especialmente dirigidos varían en su estabilidad, selectividad y elección del objetivo, pero, en esencia, todos apuntan a aumentar la dosis máxima efectiva que se puede administrar a las células tumorales. [197] La toxicidad sistémica reducida significa que también se pueden utilizar en personas más enfermas y que pueden portar nuevos agentes quimioterapéuticos que habrían sido demasiado tóxicos para administrarse mediante enfoques sistémicos tradicionales. [198]
El primer fármaco aprobado de este tipo fue gemtuzumab ozogamicina (Mylotarg), lanzado por Wyeth (ahora Pfizer ). El medicamento fue aprobado para tratar la leucemia mieloide aguda . [199] Otros dos fármacos, trastuzumab emtansina y brentuximab vedotin , se encuentran en ensayos clínicos tardíos, y a este último se le ha concedido aprobación acelerada para el tratamiento del linfoma de Hodgkin refractario y del linfoma anaplásico de células grandes sistémico . [197]
Las nanopartículas son partículas de tamaño de 1 a 1000 nanómetros (nm) que pueden promover la selectividad tumoral y ayudar a administrar medicamentos de baja solubilidad . Las nanopartículas pueden atacarse de forma pasiva o activa. La focalización pasiva aprovecha la diferencia entre los vasos sanguíneos tumorales y los vasos sanguíneos normales. Los vasos sanguíneos de los tumores tienen "fugas" porque tienen espacios de 200 a 2000 nm, que permiten que las nanopartículas escapen al interior del tumor. La orientación activa utiliza moléculas biológicas ( anticuerpos , proteínas , ADN y ligandos de receptores ) para dirigir preferentemente las nanopartículas a las células tumorales. Existen muchos tipos de sistemas de administración de nanopartículas, como sílice , polímeros , liposomas [200] y partículas magnéticas. Las nanopartículas hechas de material magnético también se pueden usar para concentrar agentes en sitios de tumores utilizando un campo magnético aplicado externamente. [196] Han surgido como un vehículo útil en la administración magnética de fármacos para agentes poco solubles como el paclitaxel . [201]
La electroquimioterapia es el tratamiento combinado en el que a la inyección de un fármaco quimioterapéutico le sigue la aplicación de pulsos eléctricos de alto voltaje localmente al tumor. El tratamiento permite que los fármacos quimioterapéuticos, que de otro modo no podrían o apenas atravesarían la membrana de las células (como la bleomicina y el cisplatino), entren en las células cancerosas. De ahí que se consiga una mayor eficacia del tratamiento antitumoral. [202]
La electroquimioterapia clínica se ha utilizado con éxito para el tratamiento de tumores cutáneos y subcutáneos independientemente de su origen histológico. [203] [204] Se ha informado que el método es seguro, simple y altamente efectivo en todos los informes sobre el uso clínico de la electroquimioterapia. Según el proyecto ESOPE (Procedimientos Operativos Estándar Europeos de Electroquimioterapia), se elaboraron los Procedimientos Operativos Estándar (SOP) para electroquimioterapia, basados en la experiencia de los principales centros oncológicos europeos en electroquimioterapia. [205] [206] Recientemente, se han desarrollado nuevas modalidades de electroquimioterapia para el tratamiento de tumores internos mediante procedimientos quirúrgicos, vías endoscópicas o abordajes percutáneos para acceder al área de tratamiento. [207] [208]
La terapia de hipertermia es un tratamiento térmico para el cáncer que puede ser una herramienta poderosa cuando se usa en combinación con quimioterapia (termoquimioterapia) o radiación para el control de una variedad de cánceres. El calor se puede aplicar localmente al sitio del tumor, lo que dilatará los vasos sanguíneos del tumor, permitiendo que entre más medicamento quimioterapéutico al tumor. Además, la membrana de la célula tumoral se volverá más porosa, lo que permitirá que entre más medicamento quimioterapéutico en la célula tumoral.
También se ha demostrado que la hipertermia ayuda a prevenir o revertir la "quimiorresistencia". La resistencia a la quimioterapia a veces se desarrolla con el tiempo a medida que los tumores se adaptan y pueden superar la toxicidad de la quimioterapia. "La superación de la quimiorresistencia se ha estudiado ampliamente en el pasado, especialmente usando células resistentes al CDDP. En cuanto al beneficio potencial de que se puedan reclutar células resistentes a los medicamentos para una terapia efectiva combinando quimioterapia con hipertermia, era importante demostrar que la quimiorresistencia contra varios Los medicamentos contra el cáncer (por ejemplo, mitomicina C, antraciclinas, BCNU, melfalán), incluido el CDDP, podrían revertirse al menos parcialmente mediante la adición de calor [209] .
La quimioterapia se usa en medicina veterinaria de manera similar a como se usa en medicina humana. [210]
Las náuseas y los vómitos son dos de los efectos secundarios relacionados con el tratamiento del cáncer más temidos por los pacientes con cáncer y sus familias.