La inmunoterapia contra el cáncer ( inmuno-oncoterapia ) es la estimulación del sistema inmunológico para tratar el cáncer , mejorando la capacidad natural del sistema inmunológico para combatir la enfermedad. [1] Es una aplicación de la investigación fundamental de la inmunología del cáncer ( inmunoncología ) y una creciente subespecialidad de la oncología .
La inmunoterapia contra el cáncer aprovecha el hecho de que las células cancerosas a menudo tienen antígenos tumorales , moléculas en su superficie que pueden unirse a proteínas de anticuerpos o receptores de células T , desencadenando una respuesta del sistema inmunológico. Los antígenos tumorales suelen ser proteínas u otras macromoléculas (p. ej., carbohidratos ). Los anticuerpos normales se unen a patógenos externos, pero los anticuerpos de inmunoterapia modificados se unen a los antígenos tumorales, marcando e identificando las células cancerosas para que el sistema inmunológico las inhiba o las elimine. El éxito clínico de la inmunoterapia contra el cáncer varía mucho entre las diferentes formas de cáncer; por ejemplo, ciertos subtipos de cáncer gástrico reaccionan bien al enfoque, mientras que la inmunoterapia no es eficaz para otros subtipos. [2]
En 2018, el inmunólogo estadounidense James P. Allison y el inmunólogo japonés Tasuku Honjo recibieron el Premio Nobel de Fisiología o Medicina por su descubrimiento de la terapia contra el cáncer mediante la inhibición de la regulación inmune negativa. [3]
"Durante los siglos XVII y XVIII, se generalizaron diversas formas de inmunoterapia contra el cáncer... En los siglos XVIII y XIX, para el tratamiento del cáncer se utilizaban vendajes sépticos que envolvían tumores ulcerosos. Las heridas quirúrgicas se dejaban abiertas para facilitar el desarrollo de la infección. , y se crearon llagas purulentas deliberadamente... Uno de los efectos más conocidos de los microorganismos sobre... el cáncer se informó en 1891, cuando un cirujano estadounidense, William Coley , inoculó a pacientes que tenían tumores inoperables con [ Streptococcus pyogenes ]." [4] "Coley [había] revisado minuciosamente la literatura disponible en ese momento y encontró 38 informes de pacientes con cáncer con erisipela febril accidental o iatrogénica . En 12 pacientes, el sarcoma o carcinoma había desaparecido por completo; los demás habían mejorado sustancialmente. Coley decidió para intentar el uso terapéutico de la erisipela iatrogénica..." [5] "Coley desarrolló una toxina que contenía bacterias muertas por calor [ Streptococcus pyogenes y Serratia marcescens ]. Hasta 1963, este tratamiento se usaba para el tratamiento del sarcoma". [4] "Coley inyectó bacterias o productos bacterianos a más de 1000 pacientes con cáncer". [6] El 51,9% de los pacientes [de Coley] con sarcomas de tejido blando inoperables mostraron una regresión tumoral completa y sobrevivieron durante más de 5 años, y el 21,2% de los pacientes no tuvieron evidencia clínica de tumor al menos 20 años después de este tratamiento... " [4] La investigación continuó en el siglo XX bajo la dirección de Maria O'Connor Hornung en la Facultad de Medicina de Tulane [7] [8]
Existen varios tipos de inmunoterapia que se utilizan para tratar el cáncer: [9] [10]
Las inmunoterapias se pueden clasificar como activas o pasivas según su capacidad para activar el sistema inmunológico del huésped contra el cáncer. [11] [12] La inmunoterapia activa se dirige específicamente a las células tumorales a través del sistema inmunológico. Los ejemplos incluyen vacunas terapéuticas contra el cáncer (también conocidas como vacunas de tratamiento, [13] que están diseñadas para estimular el sistema inmunológico del cuerpo para combatir el cáncer), células CAR-T y terapias con anticuerpos dirigidos. Por el contrario, la inmunoterapia pasiva no se dirige directamente a las células tumorales, sino que mejora la capacidad del sistema inmunológico para atacar las células cancerosas. Los ejemplos incluyen inhibidores de puntos de control y citocinas .
Las terapias celulares activas tienen como objetivo destruir las células cancerosas mediante el reconocimiento de distintos marcadores conocidos como antígenos . En las vacunas contra el cáncer, el objetivo es generar una respuesta inmune a estos antígenos a través de una vacuna. Actualmente, sólo se ha aprobado una vacuna ( sipuleucel-T para el cáncer de próstata). En las terapias mediadas por células, como la terapia con células CAR-T, las células inmunitarias se extraen del paciente, se modifican genéticamente para reconocer antígenos específicos del tumor y se devuelven al paciente. Los tipos de células que se pueden utilizar de esta manera son las células asesinas naturales (NK) , las células asesinas activadas por linfocinas , las células T citotóxicas y las células dendríticas . Finalmente, se pueden desarrollar anticuerpos específicos que reconozcan las células cancerosas y se dirijan a ellas para que el sistema inmunológico las destruya. Ejemplos de tales anticuerpos incluyen rituximab (dirigido a CD-20), trastuzumab (dirigido a HER-2) y cetuximab (dirigido a EGFR).
Las terapias pasivas con anticuerpos tienen como objetivo aumentar la actividad del sistema inmunológico sin apuntar específicamente a las células cancerosas. Por ejemplo, las citoquinas estimulan directamente el sistema inmunológico y aumentan la actividad inmune. Los inhibidores de puntos de control se dirigen a proteínas ( puntos de control inmunitarios ) que normalmente amortiguan la respuesta inmunitaria. Esto mejora la capacidad del sistema inmunológico para atacar las células cancerosas. La investigación actual está identificando nuevos objetivos potenciales para mejorar la función inmune. Los inhibidores de puntos de control aprobados incluyen anticuerpos como ipilimumab , nivolumab y pembrolizumab .

La terapia con células dendríticas provoca respuestas antitumorales al hacer que las células dendríticas presenten antígenos tumorales a los linfocitos, lo que los activa y los prepara para matar otras células que presentan el antígeno. Las células dendríticas son células presentadoras de antígenos (APC) en el sistema inmunológico de los mamíferos. [14] En el tratamiento del cáncer, ayudan a atacar el antígeno del cáncer. [15] La única terapia contra el cáncer celular aprobada basada en células dendríticas es el sipuleucel-T .
Un método para inducir que las células dendríticas presenten antígenos tumorales es mediante la vacunación con lisados tumorales autólogos [16] o péptidos cortos (pequeñas partes de la proteína que corresponden a los antígenos proteicos de las células cancerosas). Estos péptidos suelen administrarse en combinación con adyuvantes (sustancias altamente inmunogénicas ) para aumentar las respuestas inmunitarias y antitumorales. Otros adyuvantes incluyen proteínas u otras sustancias químicas que atraen y/o activan las células dendríticas, como el factor estimulante de colonias de granulocitos y macrófagos (GM-CSF). Las fuentes más comunes de antígenos utilizados para la vacuna de células dendríticas en el glioblastoma (GBM) como un tumor cerebral agresivo fueron el lisado tumoral completo, el ARN del antígeno CMV y los péptidos asociados a tumores como EGFRvIII . [17]
Las células dendríticas también pueden activarse in vivo haciendo que las células tumorales expresen GM-CSF. Esto se puede lograr mediante ingeniería genética de células tumorales para producir GM-CSF o infectando células tumorales con un virus oncolítico que exprese GM-CSF.
Otra estrategia consiste en eliminar las células dendríticas de la sangre de un paciente y activarlas fuera del cuerpo. Las células dendríticas se activan en presencia de antígenos tumorales, que pueden ser un único péptido/proteína específico del tumor o un lisado de células tumorales (una solución de células tumorales descompuestas). Estas células (con adyuvantes opcionales) se infunden y provocan una respuesta inmune.
Las terapias con células dendríticas incluyen el uso de anticuerpos que se unen a receptores en la superficie de las células dendríticas. Se pueden agregar antígenos al anticuerpo y pueden inducir la maduración de las células dendríticas y proporcionar inmunidad al tumor. Se han utilizado como dianas de anticuerpos receptores de células dendríticas como TLR3 , TLR7 , TLR8 o CD40 . [15] La interfaz entre células dendríticas y células NK también tiene un papel importante en la inmunoterapia. El diseño de nuevas estrategias de vacunación basadas en células dendríticas también debería abarcar la potencia estimulante de las células NK. Es fundamental incorporar sistemáticamente la monitorización de las células NK como resultado de los ensayos clínicos antitumorales basados en CD. [ cita necesaria ]
Sipuleucel-T (Provenge) fue aprobado para el tratamiento del cáncer de próstata metastásico resistente a la castración asintomático o mínimamente sintomático en 2010. El tratamiento consiste en la eliminación de células presentadoras de antígenos de la sangre mediante leucoféresis y su cultivo con la proteína de fusión PA2024 elaborada a partir de GM- LCR y fosfatasa ácida prostática (PAP) específica de la próstata y reinfusión. Este proceso se repite tres veces. [18] [19] [20] [21]

La terapia adoptiva con células T es una forma de inmunización pasiva mediante la transfusión de células T. Se encuentran en la sangre y los tejidos y normalmente se activan cuando encuentran patógenos extraños . La activación ocurre cuando los receptores de superficie de las células T encuentran células que muestran partes de proteínas extrañas (ya sea en su superficie o intracelularmente). Pueden ser células infectadas u otras células presentadoras de antígenos (APC). Estos últimos se encuentran en el tejido normal y en el tejido tumoral, donde se les conoce como linfocitos infiltrantes de tumores (TIL). Se activan por la presencia de APC como las células dendríticas que presentan antígenos tumorales . Aunque estas células pueden atacar los tumores, el microambiente del tumor es altamente inmunosupresor, lo que interfiere con la muerte del tumor mediada por el sistema inmunológico. [22]
Se han desarrollado múltiples formas de producir células T que destruyen tumores. Lo más común es que las células T específicas de un antígeno tumoral se puedan extraer de una muestra de tumor (TIL) o filtrar de la sangre. Opcionalmente, las células T pueden modificarse de diversas formas, cultivarse e infundirse en pacientes. Las células T se pueden modificar mediante ingeniería genética, produciendo células CAR-T o células T TCR o exponiendo las células T a antígenos tumorales en un entorno no inmunosupresor, que reconocen como extraños y aprenden a atacar.
Otro enfoque es la transferencia de células T γδ haploidénticas o células asesinas naturales de un donante sano. [23] La principal ventaja de este enfoque es que estas células no causan enfermedad de injerto contra huésped . La desventaja es que las células transferidas frecuentemente tienen una función deteriorada. [24]
El ejemplo más simple consiste en extraer TIL de un tumor, cultivarlos pero sin modificarlos e infundir el resultado nuevamente en el tumor. La primera terapia de este tipo, Lifileucel , que obtuvo la aprobación de la FDA en febrero de 2024.
La premisa de la inmunoterapia CAR-T es modificar las células T para que reconozcan las células cancerosas con el fin de atacarlas y destruirlas. Los científicos recolectan células T de personas, las alteran genéticamente para agregarles un receptor de antígeno quimérico (CAR) que reconoce específicamente las células cancerosas y luego infunden las células CAR-T resultantes en los pacientes para atacar sus tumores.
Tisagenlecleucel (Kymriah), una terapia con receptor de antígeno quimérico (CAR-T), fue aprobada por la FDA en 2017 para tratar la leucemia linfoblástica aguda (LLA). [25] Este tratamiento elimina las células CD19 positivas (células B) del cuerpo (incluidas las células enfermas, pero también las células normales productoras de anticuerpos).
Axicabtagene ciloleucel (Yescarta) es otro terapéutico CAR-T, aprobado en 2017 para el tratamiento del linfoma difuso de células B grandes (DLBCL). [26]
Los andamios de alginato multifuncionales para la ingeniería y liberación de células T (MASTER) son una técnica para la ingeniería, replicación y liberación in situ de células T genéticamente modificadas. Es una evolución de la terapia con células T CAR . Las células T se extraen del paciente y se mezclan con un virus modificado genéticamente que contiene un gen dirigido al cáncer (como ocurre con el CAR T). Luego se añade la mezcla a un MASTER (andamio), que los absorbe. El MASTER contiene anticuerpos que activan las células T e interleucinas que desencadenan la proliferación celular. Luego se implanta el MASTER en el paciente. Las células T activadas interactúan con los virus para convertirse en células T CAR. Las interleucinas estimulan la proliferación de estas células CAR T y las células CAR T salen del MAESTRO para atacar el cáncer. La técnica lleva horas en lugar de semanas. Y como las células son más jóvenes, duran más en el cuerpo, muestran una mayor potencia contra el cáncer y muestran menos marcadores de agotamiento. Estas características se demostraron en modelos de ratón. El tratamiento fue más eficaz y duradero contra el linfoma . [27] [28]
La terapia con células T con receptores de células T (TCR-T) es un tipo de terapia adoptiva con células T que se dirige a algunos cánceres. Las terapias TCR-T utilizan heterodímeros formados por cadenas peptídicas alfa y beta para reconocer moléculas de fragmentos polipeptídicos presentados por MHC . A diferencia de CAR-T, que utiliza antígenos de la superficie celular, TCR-T puede reconocer el conjunto más grande de fragmentos de antígenos intracelulares del MHC. Sin embargo, la terapia con células TCR-T depende de moléculas MHC, lo que limita su utilidad. [29] [30]
El TCR de cada célula T es específico de un antígeno y se encuentra en la superficie de la célula T. La afinidad de los TCR humanos por los antígenos tumorales es relativamente baja, lo que los hace incapaces de reconocer y destruir células tumorales de manera efectiva. La célula T modificada tiene una afinidad mucho mayor, lo que mejora tanto el reconocimiento como la afinidad que respalda el reconocimiento de las células tumorales. [29]
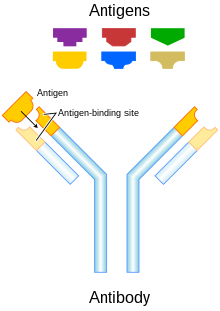
Se utilizan dos tipos en los tratamientos contra el cáncer: [32]
La capacidad de Fc para unirse a los receptores Fc es importante porque permite que los anticuerpos activen el sistema inmunológico. Las regiones Fc son variadas: existen en numerosos subtipos y pueden modificarse aún más, por ejemplo, con la adición de azúcares en un proceso llamado glicosilación . Los cambios en la región Fc pueden alterar la capacidad de un anticuerpo para activar los receptores Fc y, por extensión, determinarán el tipo de respuesta inmune que desencadena el anticuerpo. [35] Por ejemplo, los bloqueadores de puntos de control inmunitarios dirigidos a PD-1 son anticuerpos diseñados para unirse a PD-1 expresado por células T y reactivar estas células para eliminar tumores . [36] Los fármacos anti-PD-1 contienen no sólo una región Fab que se une a PD-1 sino también una región Fc. El trabajo experimental indica que la porción Fc de los medicamentos de inmunoterapia contra el cáncer puede afectar el resultado del tratamiento. Por ejemplo, los fármacos anti-PD-1 con regiones Fc que se unen a receptores Fc inhibidores pueden tener una eficacia terapéutica disminuida. [37] Los estudios de imágenes han demostrado además que la región Fc de los fármacos anti-PD-1 puede unirse a los receptores Fc expresados por macrófagos asociados a tumores. Este proceso elimina los fármacos de sus objetivos previstos (es decir, moléculas PD-1 expresadas en la superficie de las células T) y limita la eficacia terapéutica. [38] Además, los anticuerpos dirigidos a la proteína coestimuladora CD40 requieren la interacción con receptores Fc selectivos para una eficacia terapéutica óptima. [39] En conjunto, estos estudios subrayan la importancia del estado de Fc en las estrategias de focalización de puntos de control inmunológico basadas en anticuerpos .
Los anticuerpos pueden provenir de diversas fuentes, incluidas células humanas, ratones y una combinación de ambos (anticuerpos quiméricos). Diferentes fuentes de anticuerpos pueden provocar diferentes tipos de respuestas inmunitarias. Por ejemplo, el sistema inmunológico humano puede reconocer anticuerpos de ratón (también conocidos como anticuerpos murinos) y desencadenar una respuesta inmune contra ellos. Esto podría reducir la eficacia de los anticuerpos como tratamiento y provocar una reacción inmune. Los anticuerpos quiméricos intentan reducir la inmunogenicidad de los anticuerpos murinos reemplazando parte del anticuerpo con su contraparte humana correspondiente. Los anticuerpos humanizados son casi completamente humanos; sólo las regiones determinantes de la complementariedad de las regiones variables se derivan de fuentes murinas. Se han producido anticuerpos humanos utilizando ADN humano no modificado. [33]

La citotoxicidad mediada por células dependiente de anticuerpos (ADCC) requiere que los anticuerpos se unan a las superficies de las células diana. Los anticuerpos están formados por una región de unión (Fab) y la región Fc que pueden ser detectadas por las células del sistema inmunológico a través de sus receptores de superficie Fc . Los receptores Fc se encuentran en muchas células del sistema inmunológico, incluidas las células NK. Cuando las células NK encuentran células recubiertas de anticuerpos, las regiones Fc de estas últimas interactúan con sus receptores Fc, liberando perforina y granzima B para matar la célula tumoral. Los ejemplos incluyen rituximab , ofatumumab , elotuzumab y alemtuzumab . Los anticuerpos en desarrollo tienen regiones Fc alteradas que tienen mayor afinidad por un tipo específico de receptor Fc, FcγRIIIA, lo que puede aumentar drásticamente la eficacia. [40] [41]
Muchas células tumorales sobreexpresan CD47 para escapar de la inmunovigilancia del sistema inmunológico del huésped. CD47 se une a su receptor de proteína alfa reguladora de señales (SIRPα) y regula negativamente la fagocitosis de las células tumorales. [42] Por lo tanto, la terapia anti-CD47 tiene como objetivo restaurar la eliminación de las células tumorales. Además, cada vez hay más pruebas que respaldan el empleo de una respuesta de células T específicas de antígeno tumoral en respuesta a la terapia anti-CD47. [43] [44] Se están desarrollando varias terapias, incluidos anticuerpos anti-CD47 , receptores señuelo diseñados, anticuerpos anti-SIRPα y agentes biespecíficos. [43] A partir de 2017, se estaban probando clínicamente una amplia gama de neoplasias malignas sólidas y hematológicas. [43] [45]

Los antígenos de carbohidratos en la superficie de las células se pueden utilizar como objetivos para la inmunoterapia. GD2 es un gangliósido que se encuentra en la superficie de muchos tipos de células cancerosas, incluidos neuroblastoma , retinoblastoma , melanoma , cáncer de pulmón de células pequeñas , tumores cerebrales , osteosarcoma , rabdomiosarcoma , sarcoma de Ewing , liposarcoma , fibrosarcoma , leiomiosarcoma y otros sarcomas de tejidos blandos . Generalmente no se expresa en la superficie de los tejidos normales, lo que lo convierte en un buen objetivo para la inmunoterapia. En 2014, se estaban realizando ensayos clínicos. [46]
El sistema del complemento incluye proteínas sanguíneas que pueden provocar la muerte celular después de que un anticuerpo se une a la superficie celular (la vía clásica del complemento , entre las formas de activación del complemento). Generalmente, el sistema se ocupa de patógenos extraños, pero puede activarse con anticuerpos terapéuticos en el cáncer. El sistema puede activarse si el anticuerpo es quimérico, humanizado o humano; siempre que contenga la región Fc de IgG1 . El complemento puede provocar la muerte celular mediante la activación del complejo de ataque a la membrana , conocido como citotoxicidad dependiente del complemento ; mejora de la citotoxicidad mediada por células dependiente de anticuerpos ; y citotoxicidad celular dependiente de CR3. La citotoxicidad dependiente del complemento ocurre cuando los anticuerpos se unen a la superficie de la célula cancerosa, el complejo C1 se une a estos anticuerpos y, posteriormente, se forman poros de proteínas en la membrana de la célula cancerosa . [47]
Bloqueo
Las terapias con anticuerpos también pueden funcionar uniéndose a proteínas y bloqueando físicamente su interacción con otras proteínas. Los inhibidores de puntos de control (CTLA-4, PD-1 y PD-L1) operan mediante este mecanismo. Brevemente, los inhibidores de puntos de control son proteínas que normalmente ayudan a ralentizar las respuestas inmunitarias y evitan que el sistema inmunitario ataque las células normales. Los inhibidores de puntos de control se unen a estas proteínas y evitan que funcionen normalmente, lo que aumenta la actividad del sistema inmunológico. Los ejemplos incluyen durvalumab , ipilimumab , nivolumab y pembrolizumab .
Alemtuzumab (Campath-1H) es un anticuerpo monoclonal IgG1 humanizado anti- CD52 indicado para el tratamiento de la leucemia linfocítica crónica (LLC) refractaria a fludarabina , el linfoma cutáneo de células T , el linfoma periférico de células T y la leucemia prolinfocítica de células T. CD52 se encuentra en >95% de los linfocitos de sangre periférica (tanto células T como B) y monocitos , pero se desconoce su función en los linfocitos. Se une a CD52 e inicia su efecto citotóxico mediante mecanismos de fijación del complemento y ADCC. Debido al objetivo de los anticuerpos (células del sistema inmunológico), las complicaciones comunes del tratamiento con alemtuzumab son infección, toxicidad y mielosupresión . [65] [66] [67]
Durvalumab (Imfinzi) es un anticuerpo monoclonal de inmunoglobulina humana G1 kappa (IgG1κ) que bloquea la interacción del ligando 1 de muerte celular programada (PD-L1) con las moléculas PD-1 y CD80 (B7.1). Durvalumab está aprobado para el tratamiento de pacientes con carcinoma urotelial localmente avanzado o metastásico que:
El 16 de febrero de 2018, la Administración de Alimentos y Medicamentos aprobó durvalumab para pacientes con cáncer de pulmón de células no pequeñas (CPCNP) en estadio III irresecable cuya enfermedad no ha progresado después de quimioterapia y radioterapia simultáneas a base de platino. [68]
Ipilimumab (Yervoy) es un anticuerpo IgG1 humano que se une a la proteína de superficie CTLA4 . En la fisiología normal, las células T se activan mediante dos señales: el receptor de células T que se une a un antígeno : complejo MHC y el receptor de superficie de células T CD28 que se une a las proteínas CD80 o CD86 . CTLA4 se une a CD80 o CD86, impidiendo la unión de CD28 a estas proteínas de superficie y, por tanto, regula negativamente la activación de las células T. [69] [70] [71] [72]
Se necesitan células T citotóxicas activas para que el sistema inmunológico ataque las células del melanoma. Las células T citotóxicas activas específicas del melanoma normalmente inhibidas pueden producir una respuesta antitumoral eficaz. Ipilimumab puede provocar un cambio en la proporción de células T reguladoras y células T citotóxicas para aumentar la respuesta antitumoral. Las células T reguladoras inhiben otras células T, lo que puede beneficiar al tumor. [69] [70] [71] [72]
Nivolumab es un anticuerpo IgG4 humano que previene la inactivación de las células T al bloquear la unión del ligando 1 de muerte celular programada 1 o del ligando 2 de muerte celular programada 1 (PD-L1 o PD-L2), una proteína expresada por células cancerosas, con PD- 1 , una proteína que se encuentra en la superficie de las células T activadas. [73] [74] Nivolumab se usa en melanoma avanzado, carcinoma de células renales metastásico, cáncer de pulmón avanzado, cáncer de cabeza y cuello avanzado y linfoma de Hodgkin. [75]
Ofatumumab es un anticuerpo IgG1 humano de segunda generación que se une a CD20 . Se utiliza en el tratamiento de la leucemia linfocítica crónica (LLC) porque las células cancerosas de la LLC suelen ser células B que expresan CD20. A diferencia de rituximab , que se une a un bucle grande de la proteína CD20, ofatumumab se une a un bucle pequeño separado. Esto puede explicar sus diferentes características. En comparación con rituximab, ofatumumab induce citotoxicidad dependiente del complemento en una dosis más baja con menos inmunogenicidad . [76] [77]
A partir de 2019, pembrolizumab , que bloquea PD-1 , la proteína 1 de muerte celular programada, se ha utilizado mediante infusión intravenosa para tratar el melanoma inoperable o metastásico , el cáncer de pulmón de células no pequeñas (CPCNP) metastásico en determinadas situaciones, como segunda línea. tratamiento del carcinoma de células escamosas de cabeza y cuello (HNSCC), después de quimioterapia basada en platino , y para el tratamiento de pacientes adultos y pediátricos con linfoma de Hodgkin clásico refractario (cHL). [78] [79] También está indicado para ciertos pacientes con carcinoma urotelial , cáncer de estómago y cáncer de cuello uterino . [80]
Rituximab es un anticuerpo monoclonal quimérico IgG1 específico para CD20, desarrollado a partir de su anticuerpo original Ibritumomab . Al igual que ibritumomab, rituximab se dirige al CD20, lo que lo hace eficaz en el tratamiento de determinadas neoplasias malignas de células B. Estos incluyen linfomas agresivos e indolentes, como el linfoma difuso de células B grandes y el linfoma folicular, y leucemias como la leucemia linfocítica crónica de células B. Aunque la función de CD20 es relativamente desconocida, CD20 puede ser un canal de calcio implicado en la activación de las células B. El modo de acción del anticuerpo es principalmente a través de la inducción de ADCC y citotoxicidad mediada por el complemento. Otros mecanismos incluyen la apoptosis [ se necesita aclaración ] y la detención del crecimiento celular. Rituximab también aumenta la sensibilidad de las células B cancerosas a la quimioterapia. [81] [82] [83] [84] [85]

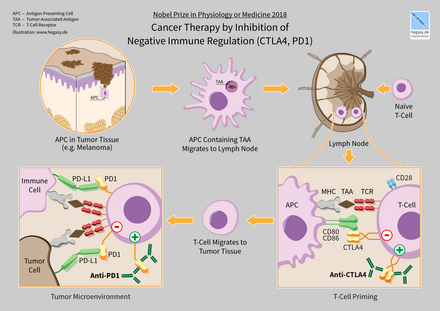
Los puntos de control inmunológico afectan la función del sistema inmunológico. Los puntos de control inmunológico pueden ser estimulantes o inhibidores. Los tumores pueden utilizar estos puntos de control para protegerse de los ataques del sistema inmunológico. Las terapias de puntos de control aprobadas a partir de 2012 bloquean los receptores de puntos de control inhibidores. El bloqueo de la señalización de retroalimentación negativa a las células inmunitarias da como resultado una respuesta inmunitaria mejorada contra los tumores. [74] A partir de 2020, las terapias de bloqueo de puntos de control inmunológico tienen una eficacia variada. En el linfoma de Hodgkin y el linfoma de células T asesinas naturales , las tasas de respuesta son altas, del 50 al 60 %. Sin embargo, las tasas de respuesta son bastante bajas para los cánceres de mama y próstata. [86] Un desafío importante son las grandes variaciones en las respuestas a los inhibidores de puntos de control inmunológico: algunos pacientes muestran respuestas clínicas espectaculares mientras que en otros no se observan efectos positivos. Se han propuesto multitud de posibles razones para la ausencia de eficacia en muchos pacientes, pero la comunidad biomédica aún tiene que empezar a encontrar un consenso al respecto. Por ejemplo, un artículo reciente documentó que la infección por Helicobacter pylori influiría negativamente en los efectos de los inhibidores de puntos de control inmunológico en el cáncer gástrico , [87] pero otros rápidamente cuestionaron esta noción. [88]
Una interacción ligando-receptor que se está investigando es la interacción entre la proteína transmembrana de muerte celular programada 1 (PDCD1, PD-1; también conocida como CD279) y su ligando, el ligando 1 de PD-1 (PD-L1, CD274). PD-L1 en la superficie celular se une a PD1 en la superficie de una célula inmune, lo que inhibe la actividad de las células inmunes. Entre las funciones de PD-L1 se encuentra una función reguladora clave de las actividades de las células T. Parece que la regulación positiva (mediada por el cáncer) de PD-L1 en la superficie celular puede inhibir las células T que de otro modo podrían atacar. PD-L1 en las células cancerosas también inhibe la apoptosis dependiente de FAS y de interferón, protegiendo a las células de las moléculas citotóxicas producidas por las células T. Los anticuerpos que se unen a PD-1 o PD-L1 y, por lo tanto, bloquean la interacción pueden permitir que las células T ataquen el tumor. [89]
El primer anticuerpo de punto de control aprobado por la FDA fue el ipilimumab , aprobado en 2011 para tratar el melanoma. [90] Bloquea la molécula del punto de control inmunológico CTLA-4 . A partir de 2012, los ensayos clínicos también han demostrado algunos beneficios de la terapia anti-CTLA-4 en el cáncer de pulmón o de páncreas , específicamente en combinación con otros fármacos. [91] [92] En ensayos en curso, la combinación del bloqueo de CTLA-4 con inhibidores de PD-1 o PD-L1 se prueba en diferentes tipos de cáncer. [93]
Sin embargo, a partir de 2015 se sabe que los pacientes tratados con bloqueo de puntos de control (específicamente anticuerpos bloqueadores CTLA-4), o una combinación de anticuerpos bloqueadores de puntos de control, tienen un alto riesgo de sufrir eventos adversos relacionados con el sistema inmunológico, como dermatológicos, gastrointestinales, reacciones autoinmunes endocrinas o hepáticas . [73] Lo más probable es que esto se deba a la amplitud de la activación de las células T inducida cuando los anticuerpos anti-CTLA-4 se administran mediante inyección en el torrente sanguíneo.
Curiosamente, un estudio de cohorte de 2024 sobre el uso de ICI durante el embarazo no mostró informes excesivos de efectos adversos específicos sobre los resultados del embarazo, el feto y/o el recién nacido. [94]
Utilizando un modelo de ratón de cáncer de vejiga, los investigadores han descubierto que una inyección local de una dosis baja de anti-CTLA-4 en el área del tumor tenía la misma capacidad inhibidora del tumor que cuando el anticuerpo se administraba en la sangre. [95] Al mismo tiempo, los niveles de anticuerpos circulantes eran más bajos, lo que sugiere que la administración local de la terapia anti-CTLA-4 podría provocar menos eventos adversos. [95]
Los resultados del ensayo clínico inicial con nivolumab , anticuerpo IgG4 PD1 , se publicaron en 2010. [74] Fue aprobado en 2014. Nivolumab está aprobado para tratar el melanoma, el cáncer de pulmón, el cáncer de riñón, el cáncer de vejiga, el cáncer de cabeza y cuello y el linfoma de Hodgkin . [96] Un ensayo clínico realizado en 2016 para el cáncer de pulmón de células no pequeñas no logró alcanzar su criterio de valoración principal para el tratamiento en el entorno de primera línea, pero cuenta con la aprobación de la FDA para líneas de terapia posteriores. [97]
Pembrolizumab (Keytruda) es otro inhibidor de PD1 aprobado por la FDA en 2014. Pembrolizumab está aprobado para tratar el melanoma y el cáncer de pulmón. [96]
El anticuerpo BGB-A317 es un inhibidor de PD-1 (diseñado para no unirse al receptor I de Fc gamma) en los primeros ensayos clínicos. [98]
En mayo de 2016, se aprobó el inhibidor de PD-L1 atezolizumab [99] para el tratamiento del cáncer de vejiga.
Los anticuerpos anti-PD-L1 actualmente en desarrollo incluyen avelumab [100] y durvalumab , [101] además de un affimer inhibidor. [102]
Muchos pacientes con cáncer no responden al bloqueo de los puntos de control inmunológico. La tasa de respuesta se puede mejorar combinándola con terapias adicionales, incluidas aquellas que estimulan la infiltración de células T. Por ejemplo, las terapias dirigidas como la radioterapia, los agentes dirigidos a la vasculatura y la quimioterapia inmunogénica [107] pueden mejorar la respuesta de bloqueo de los puntos de control inmunológico en modelos animales.
La combinación de inmunoterapias como los inhibidores de PD1 y CTLA4 puede generar respuestas duraderas. [108] [109]
La ablación combinada y la inmunoterapia mejoran la respuesta inmunoestimulante y tienen efectos sinérgicos para el tratamiento del cáncer metastásico. [110]
La combinación de inmunoterapias de punto de control con agentes farmacéuticos tiene el potencial de mejorar la respuesta y, a partir de 2018, fueron objeto de investigación clínica. [111] Los fármacos inmunoestimulantes, como los inhibidores del CSF-1R y los agonistas de TLR , han resultado eficaces. [112] [113]
Dos ensayos clínicos independientes realizados en 2024 informaron que las combinaciones de inhibidores de JAK con inmunoterapia anti-PD-1 podrían mejorar la eficacia. Un ensayo de fase 2 investigó la combinación como terapia de primera línea para el cáncer de pulmón de células no pequeñas metastásico. La administración de itacitinib después del tratamiento con pembrolizumab mejoró la respuesta terapéutica. Un ensayo de fase 1/2 independiente con pacientes con linfoma de Hodgkin en recaída/refractario combinó ruxolitinib y nivolumab , lo que produjo una eficacia clínica mejorada en pacientes en los que previamente había fracasado la inmunoterapia de bloqueo de puntos de control. [114]
Las citoquinas son proteínas producidas por muchos tipos de células presentes dentro de un tumor. Pueden modular las respuestas inmunes. El tumor a menudo los emplea para permitirle crecer y reducir la respuesta inmune. Estos efectos inmunomoduladores permiten que se utilicen como fármacos para provocar una respuesta inmunitaria. Dos citocinas de uso común son los interferones y las interleucinas. [115]
La interleucina-2 y el interferón -α son citocinas, proteínas que regulan y coordinan el comportamiento del sistema inmunológico. Tienen la capacidad de mejorar la actividad antitumoral y, por tanto, pueden utilizarse como tratamientos pasivos contra el cáncer. El interferón-α se utiliza en el tratamiento de la leucemia de células pilosas , el sarcoma de Kaposi relacionado con el SIDA , el linfoma folicular , la leucemia mieloide crónica y el melanoma maligno . La interleucina-2 se utiliza en el tratamiento del melanoma maligno y del carcinoma de células renales . [116]
Los interferones son producidos por el sistema inmunológico. Por lo general, participan en la respuesta antiviral, pero también se utilizan para el cáncer. Se dividen en tres grupos: tipo I (IFNα e IFNβ), tipo II (IFNγ) y tipo III (IFNλ). El IFNα ha sido aprobado para su uso en la leucemia de células pilosas , el sarcoma de Kaposi relacionado con el SIDA, el linfoma folicular, la leucemia mieloide crónica y el melanoma. Los IFN de tipo I y II se han investigado exhaustivamente y, aunque ambos tipos promueven efectos antitumorales en el sistema inmunológico, sólo los IFN de tipo I han demostrado ser clínicamente eficaces. "IFNλ se muestra prometedor por sus efectos antitumorales en modelos animales ". [117] [118]
A diferencia de los IFN tipo I, el interferón gamma aún no está aprobado para el tratamiento de ningún cáncer. Sin embargo, se observó una mejor supervivencia cuando se administró interferón gamma a pacientes con carcinoma de vejiga y melanoma . El resultado más prometedor se logró en pacientes con carcinoma de ovario en estadios 2 y 3 . El estudio in vitro del IFN-gamma en células cancerosas es más extenso y los resultados indican una actividad antiproliferativa del IFN-gamma que conduce a la inhibición del crecimiento o la muerte celular, generalmente inducida por apoptosis pero a veces por autofagia . [119]
Las interleucinas tienen una variedad de efectos sobre el sistema inmunológico. La interleucina-2 se utiliza en el tratamiento del melanoma maligno y del carcinoma de células renales . En fisiología normal promueve tanto las células T efectoras como las células T reguladoras, pero se desconoce su mecanismo de acción exacto. [115] [120]
Debido al alto costo de muchos medicamentos de inmunoterapia y la renuencia de las compañías de seguros médicos a pagar por adelantado sus recetas, se han propuesto varios métodos de prueba para intentar pronosticar la efectividad de estos medicamentos. En algunos casos, la FDA ha aprobado pruebas genéticas para medicamentos específicos de ciertos marcadores genéticos. Por ejemplo, la FDA aprobó el medicamento asociado a BRAF para el melanoma metastásico, que se administrará a los pacientes después de realizar pruebas para detectar la mutación genética BRAF. [121]
A partir de 2018, la detección de la proteína PD-L1 parecía ser un indicio de cáncer susceptible a varios medicamentos de inmunoterapia, pero las investigaciones encontraron que tanto la falta de esta proteína como su inclusión en el tejido canceroso no eran concluyentes, debido a la falta de comprensión de la enfermedad. cantidades variables de proteína durante diferentes momentos y ubicaciones dentro de las células y tejidos infectados. [122] [123] [124]
En 2018, se han analizado algunas indicaciones genéticas, como la carga mutacional tumoral (TMB, el número de mutaciones dentro de una región genética específica en el ADN de la célula cancerosa) y la inestabilidad de microsatélites (MSI, la cantidad de desajustes de ADN alterados que conducen a probables mutaciones). aprobados por la FDA como buenos indicadores de la probabilidad de un tratamiento eficaz con medicamentos de inmunoterapia para ciertos cánceres, pero la investigación aún está en progreso. [125] [126] A partir de 2020, la priorización de pacientes para la inmunoterapia basada en TMB todavía era muy controvertida. [127] [128]
Se están publicitando ampliamente pruebas de este tipo para el tratamiento general del cáncer y son caras. En el pasado, algunas pruebas genéticas para el tratamiento del cáncer han estado involucradas en estafas como el escándalo de fraude contra el cáncer de la Universidad de Duke , o se han afirmado que son engaños. [129] [130] [131]
Un virus oncolítico es un virus que preferentemente infecta y mata las células cancerosas. A medida que la oncólisis destruye las células cancerosas infectadas , liberan nuevas partículas de virus infecciosos o viriones para ayudar a destruir el tumor restante. Se cree que los virus oncolíticos no sólo causan la destrucción directa de las células tumorales, sino que también estimulan las respuestas inmunitarias antitumorales del huésped para la inmunoterapia a largo plazo. [132] [133] [134]
El potencial de los virus como agentes anticancerígenos se descubrió por primera vez a principios del siglo XX, aunque los esfuerzos coordinados de investigación no comenzaron hasta los años sesenta. Actualmente se han probado clínicamente como agentes oncolíticos varios virus, incluidos el adenovirus , el reovirus , el sarampión , el herpes simple , el virus de la enfermedad de Newcastle y la vaccinia . T-Vec es el primer virus oncolítico aprobado por la FDA para el tratamiento del melanoma. Varios otros virus oncolíticos se encuentran en la fase II-III de desarrollo. [135]
Ciertos compuestos que se encuentran en los hongos , principalmente polisacáridos , pueden regular positivamente el sistema inmunológico y pueden tener propiedades anticancerígenas. Por ejemplo, se ha demostrado en estudios de laboratorio que los betaglucanos como el lentinano estimulan los macrófagos , las células NK , las células T y las citoquinas del sistema inmunológico y se han investigado en ensayos clínicos como adyuvantes inmunológicos . [136]
Muchos tumores expresan mutaciones. Estas mutaciones crean potencialmente nuevos antígenos atacables (neoantígenos) para su uso en la inmunoterapia con células T. La presencia de células T CD8+ en las lesiones cancerosas, identificada mediante datos de secuenciación de ARN, es mayor en tumores con una alta carga mutacional. El nivel de transcripciones asociadas con la actividad citolítica de las células asesinas naturales y las células T se correlaciona positivamente con la carga mutacional en muchos tumores humanos. En pacientes con cáncer de pulmón de células no pequeñas tratados con lambrolizumab, la carga mutacional muestra una fuerte correlación con la respuesta clínica. En pacientes con melanoma tratados con ipilimumab, el beneficio a largo plazo también se asocia con una mayor carga mutacional, aunque de manera menos significativa. Los neoantígenos de unión al MHC previstos en pacientes con un beneficio clínico a largo plazo se enriquecieron con una serie de motivos tetrapeptídicos que no se encontraron en tumores de pacientes con beneficio clínico mínimo o nulo. [137] Sin embargo, los neoantígenos humanos identificados en otros estudios no muestran el sesgo hacia las firmas tetrapeptídicas. [138]
En la década de 1980, el Ministerio de Salud, Trabajo y Bienestar de Japón aprobó el polisacárido K extraído del hongo Coriolus versicolor para estimular el sistema inmunológico de los pacientes sometidos a quimioterapia. Es un suplemento dietético en los EE. UU. y otras jurisdicciones. [139]
Aquí demostramos por primera vez la conjugación exitosa de una molécula pequeña agonista de TLR7 con un mAb antitumoral (el rituximab anti-hCD20) sin comprometer la especificidad del antígeno.