La influenza , comúnmente conocida como gripe , es una enfermedad infecciosa causada por los virus de la influenza . Los síntomas varían de leves a graves y a menudo incluyen fiebre , secreción nasal , dolor de garganta , dolor muscular , dolor de cabeza , tos y fatiga . Estos síntomas comienzan de uno a cuatro (normalmente dos) días después de la exposición al virus y duran aproximadamente de dos a ocho días. Pueden producirse diarrea y vómitos , especialmente en niños. La influenza puede progresar a neumonía por el virus o una infección bacteriana posterior . Otras complicaciones incluyen síndrome de dificultad respiratoria aguda , meningitis , encefalitis y empeoramiento de problemas de salud preexistentes, como asma y enfermedad cardiovascular .
Existen cuatro tipos de virus de la influenza: tipos A, B, C y D. Las aves acuáticas son la fuente principal del virus de la influenza A (IAV), que también está muy extendido en varios mamíferos, incluidos los humanos y los cerdos. El virus de la influenza B (IBV) y el virus de la influenza C (ICV) infectan principalmente a los humanos, y el virus de la influenza D (IDV) se encuentra en el ganado vacuno y los cerdos. El virus de la influenza A y el virus de la influenza B circulan en los humanos y causan epidemias estacionales , y el virus de la influenza C causa una infección leve, principalmente en los niños. El virus de la influenza D puede infectar a los humanos, pero no se sabe que cause enfermedad. En los humanos, los virus de la influenza se transmiten principalmente a través de gotitas respiratorias de la tos y los estornudos. También se produce la transmisión a través de aerosoles y superficies contaminadas por el virus.
El lavado frecuente de manos y cubrirse la boca y la nariz al toser o estornudar reducen la transmisión. La vacunación anual puede ayudar a proporcionar protección contra la gripe. Los virus de la gripe, en particular el virus de la gripe A, evolucionan rápidamente, por lo que las vacunas contra la gripe se actualizan periódicamente para que coincidan con las cepas de gripe que están en circulación. Las vacunas proporcionan protección contra los subtipos H1N1 y H3N2 del virus de la gripe A y uno o dos subtipos del virus de la gripe B. La infección por gripe se diagnostica con métodos de laboratorio como pruebas de anticuerpos o antígenos y una reacción en cadena de la polimerasa ( PCR ) para identificar el ácido nucleico viral . La enfermedad puede tratarse con medidas de apoyo y, en casos graves, con medicamentos antivirales como el oseltamivir . En individuos sanos, la gripe suele ser autolimitante y rara vez es mortal, pero puede ser mortal en grupos de alto riesgo.
En un año típico, entre el 5 y el 15 por ciento de la población contrae la gripe. Anualmente se producen entre 3 y 5 millones de casos graves, con hasta 650.000 muertes relacionadas con las vías respiratorias en todo el mundo cada año. Las muertes se producen con mayor frecuencia en grupos de alto riesgo, incluidos los niños pequeños, los ancianos y las personas con enfermedades crónicas. En las regiones templadas , el número de casos de gripe alcanza su punto máximo durante el invierno, mientras que en los trópicos , la gripe puede producirse durante todo el año. Desde finales del siglo XIX, se han producido brotes pandémicos de nuevas cepas de gripe cada 10 a 50 años. Desde 1900 se han producido cinco pandemias de gripe : la gripe española de 1918 a 1920, que fue la más grave; la gripe asiática en 1957; la gripe de Hong Kong en 1968; la gripe rusa en 1977; y la pandemia de gripe porcina en 2009.

Los síntomas de la gripe son similares a los de un resfriado, aunque suelen ser más graves y es menos probable que incluyan secreción nasal . [8] [9] El tiempo entre la exposición al virus y el desarrollo de los síntomas (el período de incubación ) es de uno a cuatro días, lo más común es de uno a dos días. Muchas infecciones son asintomáticas. [10] El inicio de los síntomas es repentino y los síntomas iniciales son predominantemente inespecíficos, incluyendo fiebre, escalofríos, dolores de cabeza, dolor muscular , malestar , pérdida de apetito , falta de energía y confusión. Estos suelen ir acompañados de síntomas respiratorios como tos seca , dolor o sequedad de garganta , voz ronca y congestión o secreción nasal . La tos es el síntoma más común. [1] También pueden presentarse síntomas gastrointestinales, incluyendo náuseas, vómitos, diarrea, [11] y gastroenteritis, [12] especialmente en niños. Los síntomas estándar de la gripe suelen durar de dos a ocho días. [13] Algunos estudios sugieren que la influenza puede causar síntomas duraderos de manera similar a la COVID prolongada . [14] [15] [16]
Las infecciones sintomáticas suelen ser leves y limitadas al tracto respiratorio superior , pero la progresión a neumonía es relativamente común. La neumonía puede ser causada por la infección viral primaria o una infección bacteriana secundaria . La neumonía primaria se caracteriza por una rápida progresión de fiebre, tos, dificultad para respirar y bajos niveles de oxígeno que causan piel azulada . Es especialmente común entre quienes tienen una enfermedad cardiovascular subyacente, como la cardiopatía reumática . La neumonía secundaria generalmente tiene un período de mejoría de los síntomas de una a tres semanas [17] seguido de fiebre recurrente, producción de esputo y acumulación de líquido en los pulmones , [1] pero también puede ocurrir solo unos días después de que aparezcan los síntomas de la gripe. [17] Aproximadamente un tercio de los casos de neumonía primaria son seguidos por neumonía secundaria, que es causada con mayor frecuencia por las bacterias Streptococcus pneumoniae y Staphylococcus aureus . [10] [1]

Los virus de la gripe comprenden cuatro especies, cada una de ellas miembro exclusivo de su propio género. Los cuatro géneros de la gripe comprenden cuatro de los siete géneros de la familia Orthomyxoviridae . Son: [1] [18]
El virus de la influenza A es responsable de la mayoría de los casos de enfermedad grave, así como de epidemias estacionales y pandemias ocasionales. Infecta a personas de todas las edades, pero tiende a causar enfermedades graves de manera desproporcionada en los ancianos, los muy jóvenes y aquellos con problemas de salud crónicos. Las aves son el reservorio principal del virus de la influenza A, especialmente las aves acuáticas como patos, gansos, aves playeras y gaviotas, [19] [20] pero el virus también circula entre mamíferos, incluidos cerdos, caballos y mamíferos marinos.
Los subtipos de influenza A se definen por la combinación de las proteínas virales antigénicas hemaglutinina (H) y neuraminidasa (N) en la envoltura viral ; por ejemplo, " H1N1 " designa un subtipo de IAV que tiene una proteína hemaglutinina (H) tipo 1 y una proteína neuraminidasa (N) tipo 1. [21] Casi todas las combinaciones posibles de H (1 a 16) y N (1 a 11) se han aislado de aves silvestres. [22] [23] Además, se han encontrado H17, H18, N10 y N11 en murciélagos. [24] [23] Los subtipos del virus de influenza A en circulación entre humanos a partir de 2018 [actualizar]son H1N1 y H3N2. [2]
El virus de la influenza B infecta principalmente a los humanos, pero se ha identificado en focas, caballos, perros y cerdos. [23] El virus de la influenza B no tiene subtipos como el virus de la influenza A, pero tiene dos linajes antigénicamente distintos, denominados linajes similares a B/Victoria/2/1987 y similares a B/Yamagata/16/1988, [1] o simplemente (B/)Victoria(-like) y (B/)Yamagata(-like). [23] [2] Ambos linajes están en circulación en humanos, [1] afectando desproporcionadamente a los niños. [11] Sin embargo, el linaje B/Yamagata podría haberse extinguido en 2020/2021 debido a las medidas pandémicas de COVID-19 . [25] Los virus de la influenza B contribuyen a las epidemias estacionales junto con los virus de la influenza A, pero nunca se han asociado con una pandemia. [23]
El virus de la influenza C, al igual que el virus de la influenza B, se encuentra principalmente en humanos, aunque se ha detectado en cerdos, perros salvajes, camellos dromedarios , ganado y perros. [12] [23] La infección por el virus de la influenza C afecta principalmente a los niños y suele ser asintomática [1] [11] o presenta síntomas leves similares a los de un resfriado, aunque pueden presentarse síntomas más graves como gastroenteritis y neumonía. [12] A diferencia del virus de la influenza A y el virus de la influenza B, el virus de la influenza C no ha sido un foco principal de investigación relacionada con medicamentos antivirales, vacunas y otras medidas contra la influenza. [23] El virus de la influenza C se subclasifica en seis linajes genéticos/antigénicos. [12] [26]
El virus de la influenza D se ha aislado de cerdos y ganado vacuno, siendo este último el reservorio natural. También se ha observado la infección en humanos, caballos, camellos dromedarios y pequeños rumiantes como cabras y ovejas. [23] [26] El virus de la influenza D está distantemente relacionado con el virus de la influenza C. Si bien los trabajadores del ganado han dado positivo ocasionalmente a una infección previa por el virus de la influenza D, no se sabe que cause enfermedad en humanos. [1] [11] [12] El virus de la influenza C y el virus de la influenza D experimentan una tasa más lenta de evolución antigénica que el virus de la influenza A y el virus de la influenza B. Debido a esta estabilidad antigénica, surgen relativamente pocos linajes nuevos. [26]

Cada año se analizan millones de muestras del virus de la gripe para monitorear los cambios en las propiedades antigénicas del virus y para informar el desarrollo de vacunas. [27]
Para describir de forma inequívoca un aislamiento específico del virus, los investigadores utilizan la nomenclatura del virus de la gripe aceptada internacionalmente,i [28] que describe, entre otras cosas, la especie animal de la que se aisló el virus y el lugar y año de recolección. A modo de ejemplo: A/pollo/Nakorn-Patom/Tailandia/CU-K2/04(H5N1) :
La nomenclatura de los virus de influenza B, C y D, que son menos variables, es más sencilla. Algunos ejemplos son B/Santiago/29615/2020 y C/Minnesota/10/2015. [29]

Los virus de la gripe tienen un genoma de ARN monocatenario de sentido negativo que está segmentado. El sentido negativo del genoma significa que puede usarse como plantilla para sintetizar ARN mensajero (ARNm). [10] El virus de la gripe A y el virus de la gripe B tienen ocho segmentos genómicos que codifican 10 proteínas principales. El virus de la gripe C y el virus de la gripe D tienen siete segmentos genómicos que codifican nueve proteínas principales. [12]
Tres segmentos codifican tres subunidades de un complejo ARN polimerasa dependiente de ARN (RdRp): PB1, una transcriptasa, PB2, que reconoce tapas 5' , y PA (P3 para el virus de la influenza C y el virus de la influenza D), una endonucleasa . [30] La proteína de matriz M1 y el canal de protones M2 comparten un segmento, al igual que la proteína no estructural (NS1) y la proteína de exportación nuclear (NEP). [1] Para el virus de la influenza A y el virus de la influenza B, la hemaglutinina (HA) y la neuraminidasa (NA) se codifican en un segmento cada una, mientras que el virus de la influenza C y el virus de la influenza D codifican una proteína de fusión hemaglutinina-esterasa (HEF) en un segmento que fusiona las funciones de HA y NA. El segmento final del genoma codifica la nucleoproteína viral (NP). [30] Los virus de la influenza también codifican varias proteínas accesorias, como PB1-F2 y PA-X, que se expresan a través de marcos de lectura abiertos alternativos [1] [31] y que son importantes en la supresión de la defensa del huésped, la virulencia y la patogenicidad. [32]
La partícula viral, llamada virión, es pleomórfica y varía entre filamentosa, baciliforme o esférica. Los aislados clínicos tienden a ser pleomórficos, mientras que las cepas adaptadas al crecimiento en laboratorio suelen producir viriones esféricos. Los viriones filamentosos tienen un diámetro de aproximadamente 250 nanómetros (nm) por 80 nm, los baciliformes de 120 a 250 por 95 nm y los esféricos de 120 nm. [33]
El núcleo del virión comprende una copia de cada segmento del genoma unido a nucleoproteínas NP en complejos de ribonucleoproteína (RNP) separados para cada segmento. Hay una copia de la RdRp, incluidas todas las subunidades, unida a cada RNP. El material genético está encapsulado por una capa de proteína de matriz M1 que proporciona refuerzo estructural a la capa externa, la envoltura viral . [3] La envoltura comprende una membrana de bicapa lipídica que incorpora proteínas HA y NA (o HEF [26] ) que se extienden hacia afuera desde su superficie exterior. Las proteínas HA y HEF [26] tienen una estructura de "cabeza" y "tallo" distintas. Las proteínas M2 forman canales de protones a través de la envoltura viral que son necesarios para la entrada y salida viral. Los virus de la influenza B contienen una proteína de superficie llamada NB que está anclada en la envoltura, pero se desconoce su función. [1]

El ciclo de vida viral comienza con la unión a una célula diana. La unión está mediada por las proteínas HA virales en la superficie de la envoltura, que se unen a las células que contienen receptores de ácido siálico en la superficie de la membrana celular. [1] [19] [3] Para los subtipos N1 con la mutación "G147R" y los subtipos N2, la proteína NA puede iniciar la entrada. Antes de la unión, las proteínas NA promueven el acceso a las células diana degradando el moco, lo que ayuda a eliminar los receptores señuelo extracelulares que impedirían el acceso a las células diana. [3] Después de la unión, el virus es internalizado en la célula por un endosoma que contiene el virión en su interior. El endosoma es acidificado por la vATPasa celular [31] para tener un pH más bajo, lo que desencadena un cambio conformacional en HA que permite la fusión de la envoltura viral con la membrana endosómica. [32] Al mismo tiempo, los iones de hidrógeno se difunden en el virión a través de los canales iónicos M2, lo que altera las interacciones proteína-proteína internas y libera las RNP en el citosol de la célula huésped . La capa de proteína M1 que rodea a las RNP se degrada, lo que hace que las RNP queden completamente desprovistas de su envoltura en el citosol. [31] [3]
Las RNP se importan luego al núcleo con la ayuda de señales de localización viral. Allí, la ARN polimerasa viral transcribe el ARNm utilizando la cadena genómica de sentido negativo como plantilla. La polimerasa arrebata las tapas 5' para el ARNm viral del ARN celular para iniciar la síntesis de ARNm y el extremo 3' del ARNm se poliadenila al final de la transcripción. [30] Una vez que el ARNm viral se transcribe, se exporta fuera del núcleo y los ribosomas del huésped lo traducen de una manera dependiente de la tapa para sintetizar proteínas virales. [31] RdRp también sintetiza cadenas complementarias de sentido positivo del genoma viral en un complejo RNP complementario que luego se utilizan como plantillas por las polimerasas virales para sintetizar copias del genoma de sentido negativo. [1] [3] Durante estos procesos, las RdRp de los virus de la influenza aviar (AIV) funcionan de manera óptima a una temperatura más alta que los virus de la influenza de los mamíferos. [13]
Las subunidades de polimerasa viral recién sintetizadas y las proteínas NP se importan al núcleo para aumentar aún más la tasa de replicación viral y formar RNP. [30] Las proteínas HA, NA y M2 se transportan con la ayuda de las proteínas M1 y NEP [32] a la membrana celular a través del aparato de Golgi [30] y se insertan en la membrana de la célula. Las proteínas no estructurales virales, incluidas NS1, PB1-F2 y PA-X, regulan los procesos celulares del huésped para desactivar las respuestas antivirales. [1] [32] [3] PB1-F2 también interactúa con PB1 para mantener las polimerasas en el núcleo durante más tiempo. [20] Las proteínas M1 y NEP se localizan en el núcleo durante las últimas etapas de la infección, se unen a las RNP virales y median su exportación al citoplasma, donde migran a la membrana celular con la ayuda de endosomas reciclados y se agrupan en los segmentos del genoma. [1] [3]
Los virus progenie abandonan la célula mediante gemación desde la membrana celular, que se inicia con la acumulación de proteínas M1 en el lado citoplasmático de la membrana. El genoma viral se incorpora dentro de una envoltura viral derivada de porciones de la membrana celular que tienen proteínas HA, NA y M2. Al final de la gemación, las proteínas HA permanecen unidas al ácido siálico celular hasta que son escindidas por la actividad sialidasa de las proteínas NA. Luego, el virión se libera de la célula. La actividad sialidasa de NA también escinde cualquier residuo de ácido siálico de la superficie viral, lo que ayuda a evitar que los virus recién ensamblados se agreguen cerca de la superficie celular y mejore la infectividad. [1] [3] De manera similar a otros aspectos de la replicación de la influenza, la actividad óptima de NA depende de la temperatura y el pH. [13] En última instancia, la presencia de grandes cantidades de ARN viral en la célula desencadena la apoptosis (muerte celular programada), que es iniciada por factores celulares para restringir la replicación viral. [31]

Dos procesos clave por los que evolucionan los virus de la gripe son la deriva antigénica y el cambio antigénico . La deriva antigénica es cuando los antígenos de un virus de la gripe cambian debido a la acumulación gradual de mutaciones en el gen del antígeno (HA o NA). [19] Esto puede ocurrir en respuesta a la presión evolutiva ejercida por la respuesta inmune del huésped. La deriva antigénica es especialmente común para la proteína HA, en la que solo unos pocos cambios de aminoácidos en la región de la cabeza pueden constituir una deriva antigénica. [2] [26] El resultado es la producción de nuevas cepas que pueden evadir la inmunidad mediada por anticuerpos preexistente. [1] [11] La deriva antigénica ocurre en todas las especies de influenza, pero es más lenta en B que en A y más lenta en C y D. [26] La deriva antigénica es una causa importante de influenza estacional, [34] y requiere que las vacunas contra la gripe se actualicen anualmente. HA es el componente principal de las vacunas inactivadas, por lo que la vigilancia monitorea la deriva antigénica de este antígeno entre las cepas circulantes. La evolución antigénica de los virus de la gripe de humanos parece ser más rápida que en cerdos y equinos. En las aves silvestres, la variación antigénica dentro del subtipo parece ser limitada, pero se ha observado en aves de corral. [1] [11]
El cambio antigénico es un cambio repentino y drástico en el antígeno del virus de la influenza, generalmente HA. Durante el cambio antigénico, cepas antigénicamente diferentes que infectan la misma célula pueden reasociar segmentos genómicos entre sí, produciendo una progenie híbrida. Dado que todos los virus de la influenza tienen genomas segmentados, todos son capaces de reasociarse. [12] [26] El cambio antigénico solo ocurre entre virus de influenza del mismo género [30] y ocurre más comúnmente entre virus de influenza A. En particular, la reasociación es muy común en los virus de influenza aviar, lo que crea una gran diversidad de virus de influenza en aves, pero es poco común en linajes humanos, equinos y caninos. [35] Los cerdos, murciélagos y codornices tienen receptores para los virus de influenza A tanto de mamíferos como de aves, por lo que son "recipientes de mezcla" potenciales para la reasociación. [23] Si una cepa animal se reasocia con una cepa humana, [2] entonces puede surgir una nueva cepa que sea capaz de transmitirse de humano a humano. Esto ha causado pandemias, pero sólo un número limitado, por lo que es difícil predecir cuándo ocurrirá la próxima. [1] [11] El Sistema Mundial de Vigilancia y Respuesta a la Gripe de la Organización Mundial de la Salud (GISRS) analiza varios millones de muestras al año para monitorear la propagación y evolución de los virus de la gripe. [36] [37] [38]
Las personas infectadas pueden transmitir los virus de la gripe al respirar, hablar, toser y estornudar, lo que propaga gotitas respiratorias y aerosoles que contienen partículas del virus en el aire. Una persona susceptible a la infección puede contraer la gripe al entrar en contacto con estas partículas. [17] [39] Las gotitas respiratorias son relativamente grandes y viajan menos de dos metros antes de caer sobre superficies cercanas. Los aerosoles son más pequeños y permanecen suspendidos en el aire durante más tiempo, por lo que tardan más en asentarse y pueden viajar más lejos. [39] [4] La inhalación de aerosoles puede provocar una infección, [40] pero la mayor parte de la transmisión se produce en el área de unos dos metros alrededor de una persona infectada a través de gotitas respiratorias [10] que entran en contacto con la mucosa del tracto respiratorio superior. [40] También puede producirse la transmisión a través del contacto con una persona, fluidos corporales u objetos intermedios ( fómites ), [10] [39] ya que los virus de la gripe pueden sobrevivir durante horas en superficies no porosas. [4] Si las manos están contaminadas, tocarse la cara puede provocar la infección. [41]
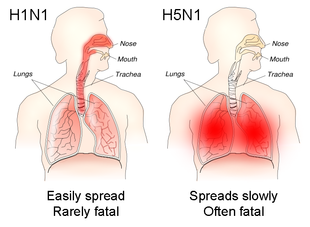
La gripe suele transmitirse desde un día antes de la aparición de los síntomas hasta 5-7 días después. [11] En los adultos sanos, el virus se elimina durante 3-5 días. En los niños y las personas inmunodeprimidas, el virus puede transmitirse durante varias semanas. [10] Se considera que los niños de 2 a 17 años son los principales y más eficientes propagadores de la gripe. [1] [11] Los niños que no han estado expuestos previamente a múltiples virus de la gripe eliminan el virus en mayores cantidades y durante más tiempo que otros niños. [1] Las personas en riesgo de exposición a la gripe incluyen a los trabajadores de la salud, los trabajadores de asistencia social y aquellos que viven con personas vulnerables a la gripe o las cuidan. En los centros de atención a largo plazo, la gripe puede propagarse rápidamente. [11] Es probable que una variedad de factores fomenten la transmisión de la gripe, incluida la temperatura más baja, la humedad absoluta y relativa más baja , menos radiación ultravioleta del sol, [40] [42] y el hacinamiento. [39] Los virus de influenza que infectan el tracto respiratorio superior, como el H1N1, tienden a ser más leves pero más transmisibles, mientras que los que infectan el tracto respiratorio inferior, como el H5N1, tienden a causar una enfermedad más grave pero son menos contagiosos. [10]
En los seres humanos, los virus de la gripe causan primero la infección al infectar las células epiteliales del tracto respiratorio. La enfermedad durante la infección es principalmente el resultado de la inflamación y el compromiso pulmonar causados por la infección y muerte de las células epiteliales, combinados con la inflamación causada por la respuesta del sistema inmunológico a la infección. Los órganos no respiratorios pueden verse afectados, pero se desconocen los mecanismos por los que la gripe está involucrada en estos casos. La enfermedad respiratoria grave puede ser causada por múltiples mecanismos no exclusivos, entre ellos la obstrucción de las vías respiratorias, la pérdida de la estructura alveolar , la pérdida de la integridad epitelial pulmonar debido a la infección y muerte de las células epiteliales y la degradación de la matriz extracelular que mantiene la estructura pulmonar. En particular, la infección de las células alveolares parece provocar síntomas graves, ya que esto da lugar a un intercambio de gases deficiente y permite que los virus infecten las células endoteliales, que producen grandes cantidades de citocinas proinflamatorias . [17]
La neumonía causada por los virus de la influenza se caracteriza por altos niveles de replicación viral en el tracto respiratorio inferior, acompañados de una fuerte respuesta proinflamatoria llamada tormenta de citocinas . [1] La infección con H5N1 o H7N9 produce especialmente altos niveles de citocinas proinflamatorias. [19] En las infecciones bacterianas, el agotamiento temprano de los macrófagos durante la influenza crea un entorno favorable en los pulmones para el crecimiento bacteriano, ya que estos glóbulos blancos son importantes para responder a la infección bacteriana. Los mecanismos del huésped para estimular la reparación tisular pueden permitir inadvertidamente la infección bacteriana. La infección también induce la producción de glucocorticoides sistémicos que pueden reducir la inflamación para preservar la integridad del tejido pero permitir un mayor crecimiento bacteriano. [17]
La fisiopatología de la gripe está significativamente influenciada por los receptores a los que se unen los virus de la gripe durante la entrada en las células. Los virus de la gripe de los mamíferos se unen preferentemente a los ácidos siálicos conectados al resto del oligosacárido por un enlace α-2,6, que se encuentran más comúnmente en varias células respiratorias, [1] [19] [3] como las células epiteliales respiratorias y de la retina. [31] Los AIV prefieren los ácidos siálicos con un enlace α-2,3, que son más comunes en las aves en las células epiteliales gastrointestinales [1] [19] [3] y en los humanos en el tracto respiratorio inferior. [44] La escisión de la proteína HA en HA 1 , la subunidad de unión, y HA 2 , la subunidad de fusión, es realizada por diferentes proteasas, lo que afecta a qué células pueden infectarse. En el caso de los virus de influenza mamífera y los virus de influenza aviar de baja patogenicidad, la escisión es extracelular, lo que limita la infección a las células que tienen las proteasas adecuadas, mientras que en el caso de los virus de influenza aviar de alta patogenicidad, la escisión es intracelular y la realizan proteasas ubicuas, lo que permite la infección de una mayor variedad de células, contribuyendo así a una enfermedad más grave. [1] [35] [45]
Las células poseen sensores para detectar el ARN viral, que luego puede inducir la producción de interferón . Los interferones median la expresión de proteínas antivirales y proteínas que reclutan células inmunes al sitio de la infección, y notifican la infección a las células cercanas no infectadas. Algunas células infectadas liberan citocinas proinflamatorias que reclutan células inmunes al sitio de la infección. Las células inmunes controlan la infección viral matando células infectadas y fagocitando partículas virales y células apoptóticas. Una respuesta inmune exacerbada puede dañar al organismo huésped a través de una tormenta de citocinas. [1] [13] [31] Para contrarrestar la respuesta inmune, los virus de la influenza codifican varias proteínas no estructurales, incluidas NS1, NEP, PB1-F2 y PA-X, que están involucradas en la reducción de la respuesta inmune del huésped al suprimir la producción de interferón y la expresión génica del huésped. [1] [32]
Las células B , un tipo de glóbulo blanco, producen anticuerpos que se unen a los antígenos de influenza HA y NA (o HEF [26] ) y otras proteínas en menor grado. Una vez unidos a estas proteínas, los anticuerpos impiden que los viriones se unan a los receptores celulares, neutralizando el virus. En los humanos, se produce una respuesta de anticuerpos considerable aproximadamente una semana después de la exposición viral. [46] Esta respuesta de anticuerpos suele ser robusta y duradera, especialmente para el virus de la influenza C y el virus de la influenza D. [1] [26] Las personas expuestas a una determinada cepa en la infancia aún poseen anticuerpos contra esa cepa en un nivel razonable más tarde en la vida, lo que puede proporcionar cierta protección contra cepas relacionadas. [1] Sin embargo, existe un " pecado antigénico original ", en el que el primer subtipo de HA al que se expone una persona influye en la respuesta inmunitaria basada en anticuerpos a futuras infecciones y vacunas. [2]

La vacunación anual es la forma principal y más eficaz de prevenir la gripe y las complicaciones asociadas a ella, especialmente en los grupos de alto riesgo. [10] [1] [47] Las vacunas contra la gripe son trivalentes o cuadrivalentes y proporcionan protección contra una cepa H1N1, una cepa H3N2 y una o dos cepas del virus de la gripe B correspondientes a los dos linajes del virus de la gripe B. [10] [2] Se utilizan dos tipos de vacunas: las vacunas inactivadas que contienen virus "muertos" (es decir, inactivados) y las vacunas vivas atenuadas contra la gripe (LAIV) que contienen virus debilitados. [1] Hay tres tipos de vacunas inactivadas: de virus completo, de virus dividido, en el que el virus se altera con un detergente, y de subunidades, que solo contiene los antígenos virales HA y NA. [48] La mayoría de las vacunas contra la gripe se inactivan y se administran mediante inyección intramuscular. Las LAIV se rocían en la cavidad nasal. [1]
Las recomendaciones de vacunación varían según el país. Algunos países recomiendan la vacunación para todas las personas mayores de una determinada edad, como los 6 meses, [47] mientras que otros países limitan las recomendaciones a los grupos de alto riesgo. [1] [11] Los bebés pequeños no pueden recibir vacunas contra la gripe por razones de seguridad, pero pueden heredar inmunidad pasiva de su madre si se vacunan durante el embarazo. [49] La vacunación contra la gripe ayuda a reducir la probabilidad de redistribución. [13]

En general, las vacunas contra la gripe solo son eficaces si existe una coincidencia antigénica entre las cepas de la vacuna y las cepas circulantes. [10] [2] La mayoría de las vacunas contra la gripe disponibles comercialmente se fabrican mediante la propagación de virus de la gripe en huevos de gallina embrionados, lo que lleva de 6 a 8 meses. [2] Las temporadas de gripe son diferentes en el hemisferio norte y sur, por lo que la OMS se reúne dos veces al año, una para cada hemisferio, para discutir qué cepas deben incluirse en función de la observación de los ensayos de inhibición de HA. [10] [3] Otros métodos de fabricación incluyen una vacuna inactivada basada en cultivo de células MDCK y una vacuna de subunidad recombinante fabricada a partir de la sobreexpresión de baculovirus en células de insectos. [2] [50]
La gripe se puede prevenir o reducir en gravedad mediante profilaxis posterior a la exposición con los medicamentos antivirales oseltamivir , que puede tomarse por vía oral a partir de los tres meses de edad, y zanamivir , que puede inhalarse a partir de los siete años. La quimioprofilaxis es más útil para las personas con alto riesgo de complicaciones y para aquellas que no pueden recibir la vacuna contra la gripe. [10] La quimioprofilaxis posterior a la exposición solo se recomienda si el oseltamivir se toma dentro de las 48 horas posteriores al contacto con un caso confirmado o sospechoso y el zanamivir dentro de las 36 horas. [10] [11] Se recomienda para las personas que aún no han recibido una vacuna para la temporada de gripe actual, que se han vacunado menos de dos semanas después del contacto, si hay un desajuste significativo entre la vacuna y las cepas circulantes, o durante un brote en un entorno cerrado independientemente del historial de vacunación. [11]
La higiene de las manos es importante para reducir la propagación de la gripe. Esto incluye lavarse las manos con frecuencia con agua y jabón, usar desinfectantes para manos a base de alcohol y no tocarse los ojos, la nariz y la boca con las manos. Es importante cubrirse la nariz y la boca al toser o estornudar. [51] Otros métodos para limitar la transmisión de la gripe incluyen quedarse en casa cuando se está enfermo, [1] evitar el contacto con otras personas hasta un día después de que desaparezcan los síntomas, [11] y desinfectar las superficies que puedan estar contaminadas por el virus. [1]
Hasta el momento, las investigaciones no han demostrado una reducción significativa de la gripe estacional con el uso de mascarillas. La eficacia de las pruebas de detección en los puntos de entrada a los países no se ha investigado en profundidad. [51] Las medidas de distanciamiento social , como el cierre de escuelas, el aislamiento o la cuarentena y la limitación de las reuniones multitudinarias, pueden reducir la transmisión, [1] [51] pero estas medidas suelen ser caras, impopulares y difíciles de implementar. En consecuencia, los métodos de control de infecciones que se recomiendan habitualmente son la etiqueta respiratoria, la higiene de manos y el uso de mascarillas, que son económicos y fáciles de aplicar. Las medidas farmacéuticas son eficaces, pero pueden no estar disponibles en las primeras etapas de un brote. [52]
En los centros de atención de salud, las personas infectadas pueden ser agrupadas o asignadas a habitaciones individuales. Se recomienda el uso de ropa protectora, como mascarillas, guantes y batas, al entrar en contacto con personas infectadas si existe riesgo de exposición a fluidos corporales infectados. Mantener a los pacientes en habitaciones con presión negativa y evitar actividades que produzcan aerosoles puede ayudar, [10] pero no se consideran necesarios sistemas especiales de ventilación y manejo del aire para prevenir la propagación de la gripe en el aire. [4] En los hogares residenciales, puede ser necesario cerrar las nuevas admisiones hasta que se controle la propagación de la gripe. [11]
Dado que los virus de la gripe circulan en animales como las aves y los cerdos, es importante prevenir la transmisión a partir de estos animales. El tratamiento del agua , la crianza de los animales en interiores, la cuarentena de los animales enfermos, la vacunación y la bioseguridad son las principales medidas que se utilizan. La ubicación de los gallineros y las porquerizas en terrenos elevados, lejos de granjas de alta densidad, granjas de traspatio, mercados de aves de corral vivas y masas de agua, ayuda a minimizar el contacto con las aves silvestres. [1] El cierre de los mercados de aves de corral vivas parece ser la medida más eficaz [19] y ha demostrado ser eficaz para controlar la propagación de H5N1, H7N9 y H9N2 . [20] Otras medidas de bioseguridad incluyen la limpieza y desinfección de las instalaciones y los vehículos, la prohibición de las visitas a las granjas avícolas, no llevar a las granjas aves destinadas al sacrificio, [53] cambiar la ropa, desinfectar los baños de pies y tratar los alimentos y el agua. [1]
Si no se cierran los mercados de aves de corral vivas, se pueden utilizar "días limpios" en los que se retiran las aves de corral no vendidas y se desinfectan las instalaciones, y se pueden utilizar políticas de "no transferencia" para eliminar el material infeccioso antes de que lleguen nuevas aves de corral para reducir la propagación de los virus de la influenza. Si un nuevo virus de influenza ha violado las medidas de bioseguridad antes mencionadas, puede ser necesaria una detección rápida para erradicarlo mediante cuarentena, descontaminación y sacrificio para evitar que el virus se vuelva endémico. [1] Existen vacunas para los subtipos aviares H5, H7 y H9 que se utilizan en algunos países. [19] En China, por ejemplo, la vacunación de aves domésticas contra el H7N9 limitó con éxito su propagación, lo que indica que la vacunación puede ser una estrategia eficaz [35] si se utiliza en combinación con otras medidas para limitar la transmisión. [1] En cerdos y caballos, el manejo de la influenza depende de la vacunación con bioseguridad. [1]

El diagnóstico basado en los síntomas es bastante preciso en personas sanas durante las epidemias estacionales y debe sospecharse en casos de neumonía, síndrome de dificultad respiratoria aguda (SDRA), sepsis o si se produce encefalitis, miocarditis o deterioro del tejido muscular . [17] Debido a que la gripe es similar a otras enfermedades virales del tracto respiratorio, es necesario un diagnóstico de laboratorio para la confirmación. Los métodos comunes de recolección de muestras para la prueba incluyen hisopados nasales y de garganta. [1] Las muestras se pueden tomar del tracto respiratorio inferior si la infección ha despejado el tracto respiratorio superior pero no el inferior. Se recomienda la prueba de la gripe para cualquier persona hospitalizada con síntomas similares a la gripe durante la temporada de gripe o que esté relacionada con un caso de gripe. Para los casos graves, el diagnóstico temprano mejora el pronóstico del paciente. [47] Los métodos de diagnóstico que pueden identificar la gripe incluyen cultivos virales , pruebas de detección de anticuerpos y antígenos y pruebas basadas en ácidos nucleicos. [54]
Los virus pueden cultivarse en un cultivo de células de mamíferos o huevos embrionados durante 3 a 10 días para monitorear el efecto citopático. Luego, se puede realizar la confirmación final mediante tinción de anticuerpos, hemadsorción con glóbulos rojos o microscopía de inmunofluorescencia . Los cultivos en viales de vidrio, que pueden identificar la infección mediante inmunotinción antes de que aparezca un efecto citopático, son más sensibles que los cultivos tradicionales con resultados en 1 a 3 días. [1] [47] [54] Los cultivos se pueden utilizar para caracterizar virus nuevos, observar la sensibilidad a los medicamentos antivirales y monitorear la deriva antigénica, pero son relativamente lentos y requieren habilidades y equipos especializados. [1]
Los ensayos serológicos se pueden utilizar para detectar una respuesta de anticuerpos a la gripe después de una infección natural o una vacunación. Los ensayos serológicos más comunes incluyen los ensayos de inhibición de la hemaglutinación que detectan anticuerpos específicos de la HA, los ensayos de neutralización del virus que comprueban si los anticuerpos han neutralizado el virus y los ensayos inmunoabsorbentes ligados a enzimas. Estos métodos tienden a ser relativamente económicos y rápidos, pero son menos confiables que las pruebas basadas en ácidos nucleicos. [1] [54]
Las pruebas de inmunofluorescencia directa o de anticuerpos inmunofluorescentes (IFA/DFA) implican la tinción de células epiteliales respiratorias en muestras con anticuerpos específicos de influenza marcados con fluorescencia, seguido del examen bajo un microscopio de fluorescencia. Pueden diferenciar entre el virus de influenza A y el virus de influenza B, pero no pueden subtipificar el virus de influenza A. [54] Las pruebas de diagnóstico rápido de influenza (RIDT) son una forma sencilla de obtener resultados de análisis, son de bajo costo y producen resultados en menos de 30 minutos, por lo que se usan comúnmente, pero no pueden distinguir entre el virus de influenza A y el virus de influenza B o entre subtipos de virus de influenza A y no son tan sensibles como las pruebas basadas en ácidos nucleicos. [1] [54]
Las pruebas basadas en ácidos nucleicos (NAT) amplifican y detectan el ácido nucleico viral. La mayoría de estas pruebas tardan unas pocas horas, [54] pero los ensayos moleculares rápidos son tan rápidos como las RIDT. [47] Entre las NAT, la reacción en cadena de la polimerasa con transcripción inversa (RT-PCR) es la más tradicional y se considera el estándar de oro para diagnosticar la influenza [54] porque es rápida y puede subtipificar el virus de la influenza A, pero es relativamente cara y más propensa a falsos positivos que los cultivos. [1] Otras NAT que se han utilizado incluyen ensayos basados en amplificación isotérmica mediada por bucle , ensayos basados en amplificación simple y amplificación basada en secuencia de ácidos nucleicos. Los métodos de secuenciación de ácidos nucleicos pueden identificar la infección al obtener la secuencia de ácidos nucleicos de muestras virales para identificar el virus y la resistencia a los medicamentos antivirales. El método tradicional es la secuenciación de Sanger , pero ha sido reemplazado en gran medida por métodos de próxima generación que tienen mayor velocidad y rendimiento de secuenciación. [54]
El tratamiento en casos de enfermedad leve o moderada es de apoyo e incluye medicamentos antifebriles como paracetamol e ibuprofeno , [55] ingesta adecuada de líquidos para evitar la deshidratación y descanso. [11] Las pastillas para la tos y los aerosoles para la garganta pueden ser beneficiosos para el dolor de garganta. Se recomienda evitar el consumo de alcohol y tabaco mientras se está enfermo. [55] No se recomienda la aspirina para tratar la gripe en niños debido a un riesgo elevado de desarrollar síndrome de Reye . [56] No se recomiendan los corticosteroides excepto cuando se trata el choque séptico o una condición médica subyacente, como la enfermedad pulmonar obstructiva crónica o la exacerbación del asma, ya que están asociados con un aumento de la mortalidad. [47] Si ocurre una infección bacteriana secundaria, pueden ser necesarios antibióticos. [11]
Los medicamentos antivirales se utilizan principalmente para tratar a pacientes gravemente enfermos, especialmente aquellos con sistemas inmunológicos comprometidos. Los antivirales son más eficaces cuando se inician en las primeras 48 horas después de que aparecen los síntomas. La administración más tardía aún puede ser beneficiosa para aquellos que tienen defectos inmunológicos subyacentes, aquellos con síntomas más graves o aquellos que tienen un mayor riesgo de desarrollar complicaciones si estos individuos todavía están eliminando el virus. El tratamiento antiviral también se recomienda si una persona es hospitalizada con sospecha de influenza en lugar de esperar los resultados de las pruebas y si los síntomas están empeorando. [1] [47] La mayoría de los medicamentos antivirales contra la influenza se dividen en dos categorías: inhibidores de la neuraminidasa (NA) e inhibidores de M2. [13] El baloxavir marboxil es una excepción notable, que se dirige a la actividad de la endonucleasa de la ARN polimerasa viral y se puede utilizar como una alternativa a los inhibidores de NA y M2 para el virus de la influenza A y el virus de la influenza B. [10] [19] [4]
Los inhibidores de NA se dirigen a la actividad enzimática de los receptores de NA, imitando la unión del ácido siálico en el sitio activo de NA en los viriones del virus de la influenza A y del virus de la influenza B [1] de modo que la liberación viral de las células infectadas y la tasa de replicación viral se ven afectadas. [11] Los inhibidores de NA incluyen oseltamivir, que se consume por vía oral en forma de profármaco y se convierte a su forma activa en el hígado, y zanamivir, que es un polvo que se inhala por vía nasal. El oseltamivir y el zanamivir son eficaces para la profilaxis y la profilaxis posterior a la exposición, y la investigación en general indica que los inhibidores de NA son eficaces para reducir las tasas de complicaciones, hospitalización y mortalidad [1] y la duración de la enfermedad. [13] [47] [4] Además, cuanto antes se administren los inhibidores de NA, mejor será el resultado, [4] aunque la administración tardía aún puede ser beneficiosa en casos graves. [1] [47] Otros inhibidores de NA incluyen laninamivir [1] y peramivir, este último puede usarse como alternativa al oseltamivir para personas que no pueden tolerarlo o absorberlo. [47]
Los adamantanos amantadina y rimantadina son fármacos administrados por vía oral que bloquean el canal iónico M2 del virus de la gripe, [1] impidiendo la pérdida de la envoltura viral. [4] Estos fármacos sólo son funcionales contra el virus de la gripe A [47] pero ya no se recomienda su uso debido a la resistencia generalizada a ellos entre los virus de la gripe A. [4] La resistencia al adamantano surgió por primera vez en H3N2 en 2003, y se volvió mundial en 2008. La resistencia al oseltamivir ya no está generalizada porque la cepa pandémica H1N1 de 2009 (H1N1 pdm09), que es resistente a los adamantanos, aparentemente reemplazó a las cepas resistentes en circulación. Desde la pandemia de 2009, la resistencia al oseltamivir se ha observado principalmente en pacientes sometidos a terapia, [1] especialmente en los inmunodeprimidos y los niños pequeños. [4] La resistencia al oseltamivir generalmente se informa en H1N1, pero se ha informado en H3N2 y virus de la gripe B con menor frecuencia. [1] Por este motivo, se recomienda el oseltamivir como fármaco de primera elección para personas inmunocompetentes, mientras que para las inmunodeprimidas se recomienda el oseltamivir contra el virus H3N2 y el virus de la influenza B y el zanamivir contra el virus H1N1 pdm09. La resistencia al zanamivir se observa con menos frecuencia, y es posible la resistencia al peramivir y al baloxavir marboxil. [4]
En las personas sanas, la infección por influenza suele ser autolimitante y rara vez es mortal. [10] [11] Los síntomas suelen durar entre 2 y 8 días. [13] La influenza puede provocar que las personas falten al trabajo o a la escuela, y se asocia con una disminución del rendimiento laboral y, en los adultos mayores, una menor independencia. La fatiga y el malestar pueden durar varias semanas después de la recuperación, y los adultos sanos pueden experimentar anomalías pulmonares que pueden tardar varias semanas en resolverse. Las complicaciones y la mortalidad se producen principalmente en las poblaciones de alto riesgo y en las personas hospitalizadas. La enfermedad grave y la mortalidad suelen atribuirse a la neumonía causada por la infección viral primaria o una infección bacteriana secundaria, [1] [11] que puede progresar a SDRA. [13]
Otras complicaciones respiratorias que pueden ocurrir incluyen sinusitis , bronquitis , bronquiolitis , acumulación excesiva de líquido en los pulmones y exacerbación de bronquitis crónica y asma. Puede ocurrir infección del oído medio y crup , más comúnmente en niños. [10] [1] Se ha observado que la infección secundaria por S. aureus , principalmente en niños, causa síndrome de choque tóxico después de la gripe, con hipotensión, fiebre y enrojecimiento y descamación de la piel. [1] Las complicaciones que afectan al sistema cardiovascular son raras e incluyen pericarditis, miocarditis fulminante con latidos cardíacos rápidos, lentos o irregulares y exacerbación de una enfermedad cardiovascular preexistente. [10] [11] La inflamación o hinchazón de los músculos acompañada de descomposición del tejido muscular ocurre raramente, generalmente en niños, que se presenta como dolor muscular y sensibilidad extrema en las piernas y una renuencia a caminar durante 2 a 3 días. [1] [11] [17]
La influenza puede afectar el embarazo, incluyendo causar un tamaño neonatal más pequeño, mayor riesgo de parto prematuro y un mayor riesgo de muerte infantil poco antes o después del nacimiento. [11] Las complicaciones neurológicas se han asociado con la influenza en raras ocasiones, incluyendo meningitis aséptica, encefalitis, encefalomielitis diseminada, mielitis transversa y síndrome de Guillain-Barré . [17] Además, pueden ocurrir convulsiones febriles y síndrome de Reye, más comúnmente en niños. [1] [11] La encefalopatía asociada a la influenza puede ocurrir directamente de la infección del sistema nervioso central por la presencia del virus en la sangre y se presenta como la aparición repentina de fiebre con convulsiones, seguida de una rápida progresión al coma. [10] Una forma atípica de encefalitis llamada encefalitis letárgica, caracterizada por dolor de cabeza, somnolencia y coma, puede ocurrir raramente en algún momento después de la infección. [1] En los sobrevivientes de la encefalopatía asociada a la influenza, pueden ocurrir defectos neurológicos. [10] Principalmente en niños, en casos graves el sistema inmunológico puede, en raras ocasiones, sobreproducir glóbulos blancos que liberan citocinas, lo que causa una inflamación grave. [10]
Las personas que tienen al menos 65 años de edad, [11] debido a un sistema inmunológico debilitado por el envejecimiento o una enfermedad crónica, son un grupo de alto riesgo para desarrollar complicaciones, al igual que los niños menores de un año de edad y los niños que no han estado expuestos previamente a los virus de la influenza varias veces. Las mujeres embarazadas tienen un riesgo elevado, que aumenta por trimestre [1] y dura hasta dos semanas después del parto. [11] [47] La obesidad, en particular un índice de masa corporal mayor de 35-40, se asocia con mayores cantidades de replicación viral, mayor gravedad de la infección bacteriana secundaria y menor eficacia de la vacunación. Las personas que tienen condiciones de salud subyacentes también se consideran en riesgo, incluidas aquellas que tienen problemas cardíacos congénitos o crónicos o trastornos pulmonares (p. ej., asma), renales, hepáticos, sanguíneos, neurológicos o metabólicos (p. ej., diabetes ), [10] [1] [11] al igual que las personas inmunodeprimidas por quimioterapia, asplenia , tratamiento prolongado con esteroides, disfunción esplénica o infección por VIH . [11] El consumo de tabaco, incluido el consumo en el pasado, pone a la persona en riesgo. [47] El papel de la genética en la gripe no se ha investigado bien, [1] pero puede ser un factor en la mortalidad por gripe. [13]

La gripe se caracteriza típicamente por epidemias estacionales y pandemias esporádicas. La mayor parte de la carga de gripe es resultado de temporadas de gripe causadas por el virus de la gripe A y el virus de la gripe B. Entre los subtipos del virus de la gripe A, el H1N1 y el H3N2 circulan en humanos y son responsables de la gripe estacional. Los casos se producen desproporcionadamente en niños, pero las causas más graves se dan entre los ancianos, los muy jóvenes [1] y los inmunodeprimidos [4] . En un año típico, los virus de la gripe infectan entre el 5 y el 15 % de la población mundial [3] [54], causando entre 3 y 5 millones de casos de enfermedad grave al año [1] [2] y representando entre 290 000 y 650 000 muertes cada año debido a enfermedades respiratorias [3] [4] [59] Entre el 5 y el 10 % de los adultos y el 20 y el 30 % de los niños contraen gripe cada año [23] . El número de casos de gripe notificados suele ser mucho menor que el número real [1] [49]
Durante las epidemias estacionales, se estima que alrededor del 80% de las personas sanas que tienen tos o dolor de garganta tienen gripe. [1] Aproximadamente entre el 30% y el 40% de las personas hospitalizadas por gripe desarrollan neumonía, y alrededor del 5% de todos los casos graves de neumonía en los hospitales se deben a la gripe, que también es la causa más común de SDRA en adultos. En los niños, la gripe y el virus respiratorio sincitial son las dos causas más comunes de SDRA. [17] Alrededor del 3% al 5% de los niños cada año desarrollan otitis media debido a la gripe. [10] Los adultos que desarrollan insuficiencia orgánica a causa de la gripe y los niños que tienen puntuaciones PIM e insuficiencia renal aguda tienen tasas más altas de mortalidad. [17] Durante la gripe estacional, la mortalidad se concentra en los muy jóvenes y los ancianos, mientras que durante las pandemias de gripe, los adultos jóvenes suelen verse afectados en una tasa alta. [13]

En las regiones templadas, el número de casos de gripe varía de una estación a otra. Los niveles más bajos de vitamina D , presumiblemente debido a menos luz solar, [42] menor humedad, temperatura más baja y cambios menores en las proteínas del virus causados por la deriva antigénica contribuyen a las epidemias anuales que alcanzan su punto máximo durante la temporada de invierno. En el hemisferio norte, esto es de octubre a mayo (más específicamente de diciembre a abril [13] ), y en el hemisferio sur, esto es de mayo a octubre (más específicamente de junio a septiembre [13] ). Por lo tanto, hay dos temporadas de gripe distintas cada año en las regiones templadas, una en el hemisferio norte y otra en el hemisferio sur. [1] [11] [2] En las regiones tropicales y subtropicales, la estacionalidad es más compleja y parece estar afectada por varios factores climáticos como la temperatura mínima, las horas de sol, las precipitaciones máximas y la alta humedad. [1] [60] Por lo tanto, la gripe puede ocurrir durante todo el año en estas regiones. [13] Las epidemias de gripe en los tiempos modernos tienden a comenzar en el hemisferio oriental o sur, [60] siendo Asia un reservorio clave. [13]
El virus de la influenza A y el virus de la influenza B circulan al mismo tiempo, por lo que tienen los mismos patrones de transmisión. [1] Sin embargo, la estacionalidad del virus de la influenza C no se conoce bien. La infección por el virus de la influenza C es más común en niños menores de dos años y, en la edad adulta, la mayoría de las personas han estado expuestas a él. La hospitalización asociada al virus de la influenza C ocurre con mayor frecuencia en niños menores de tres años y con frecuencia está acompañada de coinfección con otro virus o bacteria, lo que puede aumentar la gravedad de la enfermedad. Al considerar todas las hospitalizaciones por enfermedades respiratorias entre niños pequeños, el virus de la influenza C parece representar solo un pequeño porcentaje de dichos casos. Pueden ocurrir grandes brotes de infección por el virus de la influenza C, por lo que la incidencia varía significativamente. [12]
Los brotes de gripe causados por nuevos virus de la gripe son frecuentes. [30] Según el nivel de inmunidad preexistente en la población, los nuevos virus de la gripe pueden propagarse rápidamente y causar pandemias con millones de muertes. Estas pandemias, a diferencia de la gripe estacional, son causadas por cambios antigénicos que involucran virus de la gripe animal. Hasta la fecha, todas las pandemias de gripe conocidas han sido causadas por virus de la gripe A, y siguen el mismo patrón de propagación desde un punto de origen al resto del mundo en el transcurso de múltiples olas en un año. [1] [11] [47] Las cepas pandémicas tienden a estar asociadas con tasas más altas de neumonía en individuos por lo demás sanos. [17] Generalmente, después de cada pandemia de gripe, la cepa pandémica continúa circulando como la causa de la gripe estacional, reemplazando a las cepas anteriores. [1] Desde 1700 hasta 1889, las pandemias de gripe ocurrieron aproximadamente una vez cada 50 a 60 años. Desde entonces, las pandemias han ocurrido aproximadamente una vez cada 10 a 50 años, por lo que es posible que se estén volviendo más frecuentes con el tiempo. [60]
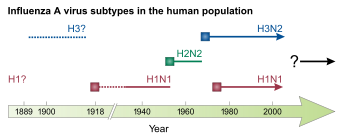
La primera epidemia de gripe puede haber ocurrido alrededor del año 6000 a. C. en China, [62] y existen posibles descripciones de la gripe en escritos griegos del siglo V a. C. [60] [63] Tanto en 1173-1174 d. C. como en 1387 d. C., ocurrieron epidemias en toda Europa que recibieron el nombre de "influenza". No está claro si estas epidemias u otras fueron causadas por la gripe, ya que entonces no había un patrón de denominación consistente para las enfermedades respiratorias epidémicas, y la "gripe" no se asoció claramente con la enfermedad respiratoria hasta siglos después. [64] La gripe puede haber llegado a las Américas ya en 1493, cuando una enfermedad epidémica parecida a la gripe mató a la mayor parte de la población de las Antillas . [65] [66]
El primer registro convincente de una pandemia de gripe fue en 1510. Comenzó en el este de Asia antes de propagarse al norte de África y luego a Europa. [67] Después de la pandemia, se produjo la gripe estacional, con pandemias posteriores en 1557 y 1580. [64] La pandemia de gripe de 1557 fue potencialmente la primera vez que la gripe se relacionó con el aborto espontáneo y la muerte de mujeres embarazadas. [68] La pandemia de gripe de 1580 se originó en Asia durante el verano, se propagó a África, luego a Europa y finalmente a América. [60] A finales del siglo XVI, la gripe comenzaba a entenderse como una enfermedad específica y reconocible con formas epidémicas y endémicas. [64] En 1648, se descubrió que los caballos también padecen gripe. [67]
Los datos sobre la gripe posteriores a 1700 son más precisos, por lo que es más fácil identificar pandemias de gripe después de este punto. [69] La primera pandemia de gripe del siglo XVIII comenzó en 1729 en Rusia en primavera, propagándose por todo el mundo en el transcurso de tres años con olas distintas, siendo las últimas más letales. Otra pandemia de gripe ocurrió en 1781-1782, comenzando en China en otoño. [60] A partir de esta pandemia, la gripe se asoció con brotes repentinos de enfermedad febril. [69] La siguiente pandemia de gripe fue de 1830 a 1833, comenzando en China en invierno. Esta pandemia tuvo una alta tasa de ataque, pero la tasa de mortalidad fue baja. [34] [60]
Una pandemia de gripe menor ocurrió entre 1847 y 1851 al mismo tiempo que la tercera pandemia de cólera y fue la primera pandemia de gripe en la que se registraron estadísticas vitales, por lo que la mortalidad por gripe se registró claramente por primera vez. [69] La peste aviar (ahora reconocida como gripe aviar altamente patógena) fue reconocida en 1878 [69] y pronto se relacionó con la transmisión a los humanos. [67] En el momento de la pandemia de 1889 , que puede haber sido causada por una cepa H2N2, [70] la gripe se había convertido en una enfermedad fácilmente reconocible. [67]
El agente microbiano responsable de la gripe fue identificado incorrectamente en 1892 por RFJ Pfeiffer como la especie bacteriana Haemophilus influenzae , que conserva "influenza" en su nombre. [67] [69] Entre 1901 y 1903, investigadores italianos y austríacos pudieron demostrar que la gripe aviar, entonces llamada "peste aviar", [35] era causada por un agente microscópico más pequeño que las bacterias mediante el uso de filtros con poros demasiado pequeños para que las bacterias pasaran a través de ellos. Sin embargo, las diferencias fundamentales entre virus y bacterias aún no se comprendían por completo. [69]

Entre 1918 y 1920, la pandemia de gripe española se convirtió en la pandemia de gripe más devastadora y una de las más letales de la historia. La pandemia, causada por una cepa H1N1 de la gripe A, [72] probablemente comenzó en los Estados Unidos antes de propagarse por todo el mundo a través de los soldados durante y después de la Primera Guerra Mundial . La ola inicial en la primera mitad de 1918 fue relativamente menor y se parecía a las pandemias de gripe anteriores, pero la segunda ola más tarde ese año tuvo una tasa de mortalidad mucho más alta. [60] Una tercera ola con menor mortalidad ocurrió en muchos lugares unos meses después de la segunda. [34] Para fines de 1920, se estima que aproximadamente un tercio [13] a la mitad de todas las personas en el mundo habían sido infectadas, con decenas de millones de muertes, desproporcionadamente adultos jóvenes. [60] Durante la pandemia de 1918, se identificó claramente la vía respiratoria de transmisión [34] y se demostró que la influenza era causada por un "pasador de filtro", no por una bacteria, pero la falta de acuerdo sobre la causa de la influenza persistió durante otra década y la investigación sobre la influenza disminuyó. [69] Después de la pandemia, el H1N1 circuló en humanos en forma estacional [1] hasta la siguiente pandemia. [69]
En 1931, Richard Shope publicó tres artículos que identificaban un virus como la causa de la influenza porcina, una enfermedad entonces recién reconocida entre los cerdos que se caracterizó durante la segunda ola de la pandemia de 1918. [68] [69] La investigación de Shope revigorizó la investigación sobre la influenza humana, y desde entonces han surgido muchos avances en virología, serología, inmunología, modelos animales experimentales, vaccinología e inmunoterapia a partir de la investigación sobre la influenza. [69] Solo dos años después de que se descubrieran los virus de la influenza, en 1933, se identificó al virus de la influenza A como el agente responsable de la influenza humana. [68] [73] Se descubrieron subtipos del virus de la influenza A a lo largo de la década de 1930, [69] y el virus de la influenza B se descubrió en 1940. [23]
Durante la Segunda Guerra Mundial , el gobierno de los EE. UU. trabajó en el desarrollo de vacunas inactivadas contra la gripe, lo que resultó en la autorización de la primera vacuna contra la gripe en 1945 en los Estados Unidos. [1] El virus de la gripe C se descubrió dos años después, en 1947. [23] En 1955, se confirmó que la gripe aviar era causada por el virus de la gripe A. [35] Se han producido cuatro pandemias de gripe desde la Segunda Guerra Mundial. La primera de ellas fue la gripe asiática de 1957 a 1958, causada por una cepa H2N2 [1] [52] y que comenzó en la provincia china de Yunnan . El número de muertes probablemente superó el millón, principalmente entre los muy jóvenes y los muy ancianos. [60] Esta fue la primera pandemia de gripe que se produjo en presencia de un sistema de vigilancia mundial y laboratorios capaces de estudiar el nuevo virus de la gripe. [34] Después de la pandemia, el H2N2 fue el subtipo del virus de la gripe A responsable de la gripe estacional. [1] El primer fármaco antiviral contra la gripe, la amantadina , fue aprobado en 1966, y desde la década de 1990 se han utilizado otros fármacos antivirales. [4]
En 1968, el H3N2 se introdujo en los seres humanos a través de un reordenamiento entre una cepa aviar H3N2 y una cepa H2N2 que circulaba en humanos. La nueva cepa H3N2 surgió en Hong Kong y se propagó por todo el mundo, causando la pandemia de gripe de Hong Kong , que resultó en 500.000-2.000.000 de muertes. Esta fue la primera pandemia que se propagó significativamente por los viajes aéreos. [3] [34] El H2N2 y el H3N2 circularon conjuntamente después de la pandemia hasta 1971, cuando el H2N2 disminuyó en prevalencia y fue reemplazado por completo por el H3N2. [3] En 1977, el H1N1 resurgió en los seres humanos, posiblemente después de que se liberara de un congelador en un accidente de laboratorio, y causó una pseudopandemia . [34] [69] Esta cepa H1N1 era antigénicamente similar a las cepas H1N1 que circulaban antes de 1957. Desde 1977, tanto el H1N1 como el H3N2 han circulado en humanos como parte de la influenza estacional. [1] En 1980, se introdujo el sistema de clasificación utilizado para subtipificar los virus de la influenza. [74]

En algún momento, el virus de la influenza B se dividió en dos cepas, llamadas linajes B/Victoria-like y B/Yamagata-like, ambas circulando en humanos desde 1983. [23]
En 1996, se detectó un subtipo H5N1 altamente patógeno de influenza A en gansos en Guangdong , China [35] y un año después apareció en aves de corral en Hong Kong, propagándose gradualmente a nivel mundial desde allí. Entonces se produjo un pequeño brote de H5N1 en humanos en Hong Kong [45] y desde 1997 se han producido casos humanos esporádicos, con una alta tasa de letalidad. [19] [54]
La pandemia de gripe más reciente fue la pandemia de gripe porcina de 2009 , que se originó en México y causó cientos de miles de muertes. [34] Fue causada por una nueva cepa H1N1 que era una recombinación de virus de influenza humana, porcina y aviar. [20] [4] La pandemia de 2009 tuvo el efecto de reemplazar las cepas H1N1 anteriores en circulación con la nueva cepa, pero no con ningún otro virus de influenza. En consecuencia, H1N1, H3N2 y ambos linajes de virus de influenza B han estado en circulación en forma estacional desde la pandemia de 2009. [1] [34] [35]
En 2011, se descubrió el virus de la influenza D en cerdos en Oklahoma, EE. UU., y luego se identificó al ganado como el reservorio principal del virus de la influenza D. [12] [23]
En el mismo año, [54] se detectó el virus H7N9 aviar en China y comenzó a causar infecciones humanas en 2013, comenzando en Shanghái y Anhui y permaneciendo principalmente en China. El virus H7N9 altamente patógeno surgió en algún momento de 2016 y ocasionalmente ha infectado a humanos de manera incidental. Otros virus de influenza aviar han infectado a humanos con menor frecuencia desde la década de 1990, incluidos H5N1, H5N5, H5N6 , H5N8 , H6N1 , H7N2 , H7N7 y H10N7 , y han comenzado a propagarse por gran parte del mundo desde la década de 2010. [19] Las futuras pandemias de gripe, que pueden ser causadas por un virus de influenza de origen aviar, [35] se consideran casi inevitables, y la creciente globalización ha facilitado la propagación de un virus pandémico, [34] por lo que existen esfuerzos continuos para prepararse para futuras pandemias [68] y mejorar la prevención y el tratamiento de la influenza. [1]
La palabra influenza proviene de la palabra italiana influenza , del latín medieval influentia , que originalmente significaba 'visitación' o 'influencia'. Términos como influenza di freddo , que significa 'influencia del frío', e influenza di stelle , que significa 'influencia de las estrellas' están atestiguados desde el siglo XIV. Este último se refería a la causa de la enfermedad, que en ese momento algunos atribuían a condiciones astrológicas desfavorables . Ya en 1504, influenza comenzó a significar una 'visita' o 'brote' de cualquier enfermedad que afectara a muchas personas en un solo lugar a la vez. Durante un brote de influenza en 1743 que comenzó en Italia y se extendió por toda Europa, la palabra llegó al idioma inglés y se anglicanizó en la pronunciación. Desde mediados del siglo XIX, influenza también se ha utilizado para referirse a resfriados severos. [75] [76] [77] La forma abreviada de la palabra, "flu", se atestigua por primera vez en 1839 como flue con la ortografía flu confirmada en 1893. [78] Otros nombres que se han utilizado para la influenza incluyen catarro epidémico , la gripe del francés , enfermedad del sudor y, especialmente cuando se hace referencia a la cepa pandémica de 1918, fiebre española . [79]
Las aves acuáticas, como patos, gansos, aves playeras y gaviotas, son el reservorio principal de los virus de influenza A (IAV). [19] [20]
Debido al impacto de la influenza aviar en granjas avícolas económicamente importantes, en 1981 se ideó un sistema de clasificación que dividía las cepas del virus aviar en altamente patógenas (y por lo tanto potencialmente requiriendo medidas de control enérgicas) o poco patógenas. La prueba para esto se basa únicamente en el efecto sobre los pollos: una cepa de virus es influenza aviar altamente patógena (HPAI) si el 75% o más de los pollos mueren después de ser infectados deliberadamente con ella. La clasificación alternativa es influenza aviar de baja patogenicidad (LPAI) que produce síntomas leves o nulos. [80] Este sistema de clasificación se ha modificado desde entonces para tener en cuenta la estructura de la proteína hemaglutinina del virus. [81] A nivel genético, un AIV puede identificarse como un virus HPAI si tiene un sitio de escisión multibásico en la proteína HA, que contiene residuos adicionales en el gen HA. [20] [35] Otras especies de aves, especialmente aves acuáticas, pueden infectarse con el virus HPAI sin experimentar síntomas graves y pueden propagar la infección a grandes distancias; Los síntomas exactos dependen de la especie de ave y de la cepa del virus. [80] La clasificación de una cepa de virus aviar como IAAP o IABP no predice qué tan grave podría ser la enfermedad si infecta a humanos u otros mamíferos. [80] [82]
Los síntomas de la infección por HPAI en pollos incluyen falta de energía y apetito, disminución de la producción de huevos, huevos con cáscara blanda o deformados, hinchazón de la cabeza, cresta, barbillas y corvejones, decoloración púrpura de barbillas, crestas y patas, secreción nasal, tos, estornudos, falta de coordinación y diarrea; las aves infectadas con un virus HPAI también pueden morir repentinamente sin ningún signo de infección. [53] Los virus HPAI notables incluyen influenza A (H5N1) y A (H7N9). Los virus HPAI han sido una importante carga de enfermedad en el siglo XXI, resultando en la muerte de un gran número de aves. En el caso de H7N9, algunas cepas circulantes eran originalmente poco patógenas pero se volvieron altamente patógenas al mutar para adquirir el sitio de escisión multibásica HA. El H9N2 aviar también es motivo de preocupación porque, aunque es poco patógeno, es un donante común de genes para H5N1 y H7N9 durante la redistribución. [1]
Las aves migratorias pueden propagar la gripe a grandes distancias. Un ejemplo de ello fue cuando una cepa H5N1 en 2005 infectó a las aves del lago Qinghai (China), que es una zona de escala y cría para muchas aves migratorias, y posteriormente propagó el virus a más de 20 países de Asia, Europa y Oriente Medio. [19] [35] Los virus de influenza aviar pueden transmitirse de las aves silvestres a los patos domésticos criados en libertad y, a su vez, a las aves de corral a través del agua contaminada, los aerosoles y los fómites. [1] Por tanto, los patos actúan como intermediarios clave entre las aves silvestres y las domésticas. [35] La transmisión a las aves de corral se produce normalmente en las granjas de traspatio y en los mercados de animales vivos, donde interactúan varias especies entre sí. Desde allí, los virus de influenza aviar pueden propagarse a las granjas avícolas en ausencia de una bioseguridad adecuada. Entre las aves de corral, la transmisión de la IAAP se produce a través de aerosoles y heces contaminadas, [1] jaulas, piensos y animales muertos. [19] Se ha producido una retransmisión de los virus de la IAAP de las aves de corral a las aves silvestres, que está implicada en muertes masivas y propagación intercontinental. [20]
Los virus de influenza aviar han infectado ocasionalmente a humanos a través de aerosoles, fómites y agua contaminada. [1] La transmisión directa de aves silvestres es rara. [35] En cambio, la mayoría de la transmisión involucra aves de corral domésticas, principalmente pollos, patos y gansos, pero también una variedad de otras aves como gallinas de guinea, perdices, faisanes y codornices. [ 20] El principal factor de riesgo para la infección con virus de influenza aviar es la exposición a aves en granjas y mercados de aves de corral vivas. [19] Por lo general, la infección con un virus de influenza aviar tiene un período de incubación de 3 a 5 días, pero puede ser de hasta 9 días. H5N1 y H7N9 causan enfermedad grave del tracto respiratorio inferior, mientras que otros virus de influenza aviar como H9N2 causan una enfermedad más leve del tracto respiratorio superior, comúnmente con conjuntivitis. [1] Se ha producido una transmisión limitada de los subtipos aviares H2, H5-7, H9 y H10 de una persona a otra a través de gotitas respiratorias, aerosoles y fómites, pero no se ha producido una transmisión sostenida de virus de influenza aviar de persona a persona. [1] [2]

La influenza porcina es una enfermedad respiratoria similar a la influenza humana y se encuentra en todo el mundo. Las infecciones asintomáticas son comunes. Los síntomas suelen aparecer 1 a 3 días después de la infección e incluyen fiebre, letargo, anorexia, pérdida de peso, dificultad para respirar, tos, estornudos y secreción nasal. En las cerdas, la gestación puede ser abortada. Las complicaciones incluyen infecciones secundarias y bronconeumonía potencialmente fatal . Los cerdos se vuelven contagiosos al día siguiente de la infección y generalmente propagan el virus durante 7 a 10 días, que puede propagarse rápidamente dentro de una manada. Los cerdos generalmente se recuperan dentro de los 3 a 7 días posteriores a la aparición de los síntomas. Las medidas de prevención y control incluyen vacunas inactivadas y el sacrificio de las manadas infectadas. Los subtipos del virus de la influenza A H1N1, H1N2 y H3N2 suelen ser responsables de la gripe porcina. [83]
Algunos virus de la influenza A pueden transmitirse a través de aerosoles de cerdos a humanos y viceversa. [1] Los cerdos, junto con los murciélagos y las codornices, [23] son reconocidos como un recipiente de mezcla de virus de la influenza porque tienen receptores de ácido siálico α-2,3 y α-2,6 en su tracto respiratorio. Debido a eso, tanto los virus de la influenza aviar como los de los mamíferos pueden infectar a los cerdos. Si ocurre una coinfección, es posible la recombinación. [20] Un ejemplo notable de esto fue la recombinación de un virus de influenza porcina, aviar y humana que causó la pandemia de gripe de 2009. [20] [4] Los eventos de contagio de humanos a cerdos parecen ser más comunes que de cerdos a humanos. [20]
Se han encontrado virus de la influenza en muchos otros animales, incluidos el ganado, los caballos, los perros, los gatos y los mamíferos marinos. Casi todos los virus de influenza A descienden aparentemente de virus ancestrales de las aves. La excepción son los virus similares a la influenza de los murciélagos, que tienen un origen incierto. Estos virus de murciélagos tienen los subtipos HA y NA H17, H18, N10 y N11. H17N10 y H18N11 no pueden recombinarse con otros virus de influenza A, pero sí pueden replicarse en otros mamíferos. [1]
Los virus de influenza A equina incluyen H7N7 y dos linajes [1] de H3N8 . Sin embargo, H7N7 no se ha detectado en caballos desde fines de la década de 1970, [30] por lo que puede haberse extinguido en caballos. [20] H3N8 en equinos se propaga a través de aerosoles y causa enfermedades respiratorias. [1] El H3N8 equino se une preferentemente a los ácidos siálicos α-2,3, por lo que los caballos generalmente se consideran huéspedes finales, pero se ha producido la transmisión a perros y camellos, lo que genera inquietudes de que los caballos puedan estar mezclando recipientes para la recombinación. En caninos, los únicos virus de influenza A en circulación son H3N8 derivado de equinos y H3N2 derivado de aves. No se ha observado que el H3N8 canino se recombine con otros subtipos. H3N2 tiene un rango de huéspedes mucho más amplio y puede recombinarse con H1N1 y H5N1. Se encontró un caso aislado de H6N1, probablemente de un pollo, que infectó a un perro, por lo que es posible que surjan otros virus de influenza aviar en caninos. [20]
Una amplia gama de otros mamíferos se han visto afectados por los virus de la gripe aviar A, generalmente debido a que comieron aves que habían sido infectadas. [84] Ha habido casos en los que puede haber ocurrido la transmisión de la enfermedad entre mamíferos, incluidas focas y vacas. [85] [86] [30] Se han identificado varias mutaciones que están asociadas con la adaptación de los virus de influenza aviar a los mamíferos. Dado que las proteínas HA varían en los ácidos siálicos a los que se unen, las mutaciones en el sitio de unión del receptor de HA pueden permitir que los virus de influenza aviar infecten a los mamíferos. Otras mutaciones incluyen mutaciones que afectan a los ácidos siálicos que las proteínas NA escinden y una mutación en la subunidad de la polimerasa PB2 que mejora la tolerancia a temperaturas más bajas en los tractos respiratorios de los mamíferos y mejora el ensamblaje de RNP al estabilizar la unión de NP y PB2. [20]
El virus de la influenza B se encuentra principalmente en humanos, pero también se ha detectado en cerdos, perros, caballos y focas. [23] Del mismo modo, el virus de la influenza C infecta principalmente a humanos, pero se ha observado en cerdos, perros, ganado y camellos dromedarios. [12] [23] El virus de la influenza D causa una enfermedad similar a la influenza en cerdos, pero su impacto en su reservorio natural, el ganado, es relativamente desconocido. Puede causar una enfermedad respiratoria similar a la influenza humana por sí solo, o puede ser parte de un complejo de enfermedad respiratoria bovina (BRD) con otros patógenos durante la coinfección. BRD es una preocupación para la industria ganadera, por lo que la posible participación del virus de la influenza D en BRD ha llevado a la investigación sobre vacunas para el ganado que pueden brindar protección contra el virus de la influenza D. [23] [26] Hay dos linajes antigénicos en circulación: D/swine/Oklahoma/1334/2011 (D/OK) y D/bovine/Oklahoma/660/2013 (D/660). [23]
Este memorando fue redactado por los firmantes enumerados en la página 590 con ocasión de una reunión celebrada en Ginebra en febrero de 1980.