

Las estructuras metal-orgánicas ( MOF ) son una clase de polímeros porosos que consisten en grupos metálicos (también conocidos como SBU) coordinados con ligandos orgánicos para formar estructuras unidimensionales, bidimensionales o tridimensionales. Los ligandos orgánicos incluidos a veces se denominan "puntales" o "enlazadores", siendo un ejemplo el ácido 1,4-bencenodicarboxílico (BDC).
Más formalmente, una estructura organometálica es una estructura extendida potencialmente porosa hecha de iones metálicos y conectores orgánicos. Una estructura extendida es una estructura cuyas subunidades se presentan en una proporción constante y están dispuestas en un patrón repetitivo. Los MOF son una subclase de redes de coordinación, que es un compuesto de coordinación que se extiende, a través de entidades de coordinación repetidas, en una dimensión, pero con enlaces cruzados entre dos o más cadenas, bucles o espiroenlaces individuales, o un compuesto de coordinación que se extiende a través de redes de coordinación repetidas. entidades de coordinación en dos o tres dimensiones. Las redes de coordinación, incluidos los MOF, pertenecen además a los polímeros de coordinación , que son un compuesto de coordinación con entidades de coordinación repetidas que se extienden en una, dos o tres dimensiones. [1] La mayoría de los MOF reportados en la literatura son compuestos cristalinos , pero también hay MOF amorfos , [2] y otras fases desordenadas. [3]
En la mayoría de los casos de los MOF, los poros son estables durante la eliminación de las moléculas invitadas (a menudo disolventes) y podrían rellenarse con otros compuestos. Debido a esta propiedad, los MOF son interesantes para el almacenamiento de gases como el hidrógeno y el dióxido de carbono . Otras posibles aplicaciones de los MOF son la purificación de gases , la separación de gases , la remediación de agua , [4] en catálisis , como sólidos conductores y como supercondensadores . [5]
La síntesis y propiedades de los MOF constituyen el foco principal de la disciplina denominada química reticular (del latín reticulum , "pequeña red"). [6] A diferencia de los MOF, las estructuras orgánicas covalentes (COF) están hechas completamente de elementos ligeros (H, B, C, N y O) con estructuras extendidas. [7]
Los MOF se componen de dos componentes principales: un grupo de metales inorgánicos (a menudo denominado unidad de construcción secundaria o SBU) y una molécula orgánica llamada conector. Por esta razón, a los materiales se les suele denominar materiales híbridos orgánicos-inorgánicos. [1] Las unidades orgánicas suelen ser ligandos mono, di, tri o tetravalentes . [8] La elección del metal y del conector dicta la estructura y, por tanto, las propiedades del MOF. Por ejemplo, la preferencia de coordinación del metal influye en el tamaño y la forma de los poros al dictar cuántos ligandos pueden unirse al metal y en qué orientación.
Para describir y organizar las estructuras de los MOF, se ha desarrollado un sistema de nomenclatura. Las subunidades de un MOF, llamadas unidades de construcción secundarias (SBU), pueden describirse mediante topologías comunes a varias estructuras. A cada topología, también llamada red, se le asigna un símbolo, que consta de tres letras minúsculas en negrita. MOF-5 , por ejemplo, tiene una red pcu .
Adjuntos a las SBU hay ligandos puente . Para los MOF, los ligandos puente típicos son los ácidos di y tricarboxílicos. Estos ligandos suelen tener cadenas principales rígidas. Ejemplos de ello son el ácido benceno-1,4-dicarboxílico (BDC o ácido tereftálico), el ácido bifenil-4,4' - dicarboxílico (BPDC) y el ácido tricarboxílico, ácido trimésico .
El estudio de los MOF tiene sus raíces en la química de coordinación y la química inorgánica del estado sólido, pero se convirtió en un campo nuevo. Además, los MOF se construyen a partir de ligandos orgánicos puente que permanecen intactos durante toda la síntesis. [10] La síntesis de zeolita a menudo utiliza una "plantilla". Las plantillas son iones que influyen en la estructura de la estructura inorgánica en crecimiento. Los iones plantillas típicos son cationes de amonio cuaternario, que se eliminan posteriormente. En los MOF, el marco está modelado por la SBU (unidad de construcción secundaria) y los ligandos orgánicos. [11] [12] Un enfoque de plantilla que es útil para los MOF destinados al almacenamiento de gas es el uso de disolventes aglutinantes de metales como N , N- dietilformamida y agua. En estos casos, los sitios metálicos quedan expuestos cuando se evacua el disolvente, lo que permite que el hidrógeno se una a estos sitios. [13]
Cuatro avances fueron particularmente importantes para avanzar en la química de los MOF. [14] (1) El principio geométrico de la construcción donde las unidades que contenían metal se mantenían en formas rígidas. Los primeros MOF contenían átomos individuales unidos a enlazadores de coordinación ditópicos. El enfoque no solo condujo a la identificación de una pequeña cantidad de topologías preferidas que podrían incluirse en la síntesis diseñada, sino que también fue el punto central para lograr una porosidad permanente. (2) El uso del principio isoreticular donde el tamaño y la naturaleza de una estructura cambian sin cambiar su topología condujo a MOF con porosidad ultraalta y aperturas de poros inusualmente grandes. (3) La modificación post-sintética de los MOF aumentó su funcionalidad al hacer reaccionar unidades orgánicas y complejos organometálicos con conectores. (4) Los MOF multifuncionales incorporaron múltiples funcionalidades en un solo marco.
Dado que los ligandos en los MOF generalmente se unen de manera reversible, el lento crecimiento de los cristales a menudo permite que los defectos se vuelvan a disolver, lo que da como resultado un material con cristales de escala milimétrica y una densidad de defectos cercana al equilibrio. La síntesis solvotérmica es útil para hacer crecer cristales adecuados para la determinación de la estructura, porque los cristales crecen en el transcurso de horas o días. Sin embargo, el uso de MOF como materiales de almacenamiento para productos de consumo exige una inmensa ampliación de su síntesis. La ampliación de escala de los MOF no se ha estudiado ampliamente, aunque varios grupos han demostrado que se pueden utilizar microondas para nuclear rápidamente cristales de MOF a partir de una solución. [15] [16] Esta técnica, denominada "síntesis solvotérmica asistida por microondas", se usa ampliamente en la literatura sobre zeolitas, [10] y produce cristales a escala micrométrica en cuestión de segundos a minutos, [15] [16] en rendimientos similares a los métodos de crecimiento lento.
Algunos MOF, como el mesoporoso MIL-100(Fe), [17] se pueden obtener en condiciones suaves a temperatura ambiente y en disolventes verdes (agua, etanol) mediante métodos de síntesis escalables.
Se ha descrito una síntesis sin disolventes de una variedad de MOF cristalinos. [18] Por lo general, el acetato metálico y el proligando orgánico se mezclan y se muelen con un molino de bolas . De esta manera, Cu 3 (BTC) 2 se puede sintetizar rápidamente con un rendimiento cuantitativo. En el caso de Cu 3 (BTC) 2, la morfología del producto sintetizado sin disolventes fue la misma que la del Basolite C300 fabricado industrialmente. Se cree que la fusión localizada de los componentes debido a la alta energía de colisión en el molino de bolas puede favorecer la reacción. La formación de ácido acético como subproducto en las reacciones en el molino de bolas también puede ayudar en la reacción que tiene efecto disolvente [19] en el molino de bolas. Se ha demostrado que la adición de pequeñas cantidades de etanol para la síntesis mecanoquímica de Cu 3 (BTC) 2 reduce significativamente la cantidad de defectos estructurales en el material obtenido. [20]
Un avance reciente en la preparación sin disolventes de películas y compuestos de MOF es su síntesis mediante deposición química de vapor . Este proceso, MOF-CVD, [21] se demostró por primera vez para ZIF-8 y consta de dos pasos. En una primera etapa se depositan capas precursoras de óxido metálico. En el segundo paso, estas capas precursoras se exponen a moléculas de ligando sublimadas , que inducen una transformación de fase en la red cristalina MOF. La formación de agua durante esta reacción juega un papel crucial en la dirección de la transformación. Este proceso se amplió con éxito a un proceso de sala limpia integrado, conforme a los estándares de microfabricación industrial. [22]
Se han informado numerosos métodos para el crecimiento de MOF como películas delgadas orientadas. Sin embargo, estos métodos sólo son adecuados para la síntesis de un pequeño número de topologías MOF. Un ejemplo de ello es la conversión asistida por vapor (VAC), que se puede utilizar para la síntesis de película delgada de varios MOF de tipo UiO. [23]
Los métodos de alto rendimiento (HT) son parte de la química combinatoria y una herramienta para aumentar la eficiencia. Hay dos estrategias sintéticas dentro de los métodos HT: en el enfoque combinatorio, todas las reacciones tienen lugar en un recipiente, lo que conduce a mezclas de productos. En la síntesis paralela, las reacciones tienen lugar en diferentes recipientes. Además, se distingue entre películas finas y métodos basados en disolventes. [24]
La síntesis solvotérmica se puede realizar de forma convencional en un reactor de teflón en un horno de convección o en reactores de vidrio en un horno de microondas (síntesis de microondas de alto rendimiento). El uso de un horno microondas cambia, en parte dramáticamente, los parámetros de reacción.
Además de la síntesis solvotérmica, ha habido avances en el uso de fluido supercrítico como disolvente en un reactor de flujo continuo. El agua supercrítica se utilizó por primera vez en 2012 para sintetizar MOF a base de cobre y níquel en sólo unos segundos. [25] En 2020, se utilizó dióxido de carbono supercrítico en un reactor de flujo continuo a lo largo de la misma escala de tiempo que el método supercrítico a base de agua, pero el punto crítico más bajo del dióxido de carbono permitió la síntesis del MOF UiO-66 a base de circonio. . [26]
En la síntesis solvotérmica de alto rendimiento se utiliza un reactor solvotérmico con (p. ej.) 24 cavidades para reactores de teflón. Un reactor de este tipo se denomina a veces multiclav. El bloque del reactor o el inserto del reactor está fabricado de acero inoxidable y contiene 24 cámaras de reacción dispuestas en cuatro filas. Con los reactores de teflón miniaturizados se pueden utilizar volúmenes de hasta 2 ml. El bloque del reactor está sellado en un autoclave de acero inoxidable; Para ello se introducen los reactores llenos en el fondo del reactor, se sellan los reactores de teflón con dos láminas de teflón y se coloca la parte superior del reactor. A continuación se cierra el autoclave en una prensa hidráulica. A continuación se puede someter el reactor solvotérmico sellado a un programa de temperatura-tiempo. La película de teflón reutilizable sirve para resistir la tensión mecánica, mientras que la película de teflón desechable sella los recipientes de reacción. Después de la reacción, los productos se pueden aislar y lavar en paralelo en un dispositivo de filtración al vacío. Los productos se encuentran entonces por separado sobre el papel de filtro en una denominada biblioteca de muestras y posteriormente pueden caracterizarse mediante difracción de rayos X de polvo automatizada. La información obtenida se utiliza luego para planificar futuras síntesis. [27]
Los eventos de reemplazo de minerales pseudomórficos ocurren siempre que una fase mineral entra en contacto con un fluido con el que está fuera de equilibrio. El reequilibrio tenderá a tener lugar para reducir la energía libre y transformar la fase inicial en una fase más termodinámicamente estable, involucrando subprocesos de disolución y reprecipitación. [28] [29]
Inspirándose en tales procesos geológicos, las películas delgadas de MOF se pueden cultivar mediante la combinación de la deposición de capas atómicas (ALD) de óxido de aluminio sobre un sustrato adecuado (por ejemplo, FTO) y la posterior síntesis solvotérmica de microondas. La capa de óxido de aluminio sirve como agente director de la arquitectura y como fuente de metal para la columna vertebral de la estructura MOF. [30] La construcción de la estructura organometálica 3D porosa tiene lugar durante la síntesis de microondas, cuando el sustrato depositado en la capa atómica se expone a una solución del conector requerido en una mezcla DMF /H 2 O 3:1 (v/v). ) a temperatura elevada. De manera análoga, Kornienko y sus colaboradores describieron en 2015 la síntesis de un MOF de cobalto-porfirina (Al 2 (OH) 2 TCPP-Co; TCPP-H 2 =4,4 ′ ,4″,4‴-(porfirina-5,10, 15,20-tetrail)tetrabenzoato), el primer catalizador MOF construido para la conversión electrocatalítica de CO 2 acuoso en CO . [31]
Aunque en teoría la estructura tridimensional y el entorno interno de los poros pueden controlarse mediante la selección adecuada de nodos y grupos de enlace orgánicos, la síntesis directa de dichos materiales con las funcionalidades deseadas puede resultar difícil debido a la alta sensibilidad de los sistemas MOF. La sensibilidad térmica y química, así como la alta reactividad de los materiales de reacción, pueden hacer que lograr la formación de los productos deseados sea un desafío. El intercambio de moléculas invitadas y contraiones y la eliminación de disolventes permiten alguna funcionalidad adicional, pero aún se limitan a las partes integrales de la estructura. [32] El intercambio postsintético de enlazadores orgánicos e iones metálicos es un área en expansión del campo y abre posibilidades para estructuras más complejas, mayor funcionalidad y mayor control del sistema. [32] [33]
Se pueden utilizar técnicas de modificación postsintética para intercambiar un grupo conector orgánico existente en un MOF prefabricado con un nuevo conector mediante intercambio de ligando o intercambio parcial de ligando. [33] [34] Este intercambio permite que los poros y, en algunos casos, el marco general de los MOF, se adapten para propósitos específicos. Algunos de estos usos incluyen el ajuste del material para adsorción selectiva, almacenamiento de gas y catálisis. [33] [13] Para realizar el intercambio de ligandos, los cristales de MOF prefabricados se lavan con disolvente y luego se sumergen en una solución del nuevo conector. El intercambio a menudo requiere calor y se produce en una escala de tiempo de unos pocos días. [34] El intercambio de ligando post-sintético también permite la incorporación de grupos funcionales en MOF que de otro modo no sobrevivirían a la síntesis de MOF, debido a la temperatura, el pH u otras condiciones de reacción, o dificultarían la síntesis misma por competencia con grupos donantes en el ligando prestado. . [33]
También se pueden utilizar técnicas de modificación postsintética para intercambiar un ion metálico existente en un MOF prefabricado con un nuevo ion metálico mediante intercambio de iones metálicos. La metátesis metálica completa de una parte integral de la estructura se ha logrado sin alterar la estructura o la estructura de poros del MOF. De manera similar al intercambio de ligandos postsintético, el intercambio de metales postsintético se realiza lavando cristales de MOF prefabricados con solvente y luego sumergiendo el cristal en una solución del nuevo metal. [35] El intercambio de metales postsintético permite una ruta simple para la formación de MOF con la misma estructura pero con diferentes iones metálicos. [32]
Además de modificar la funcionalidad de los ligandos y los propios metales, se puede utilizar la modificación postsintética para ampliar la estructura del MOF. Usando modificación post-sintética, los MOF se pueden convertir de un material cristalino altamente ordenado a un material poroso heterogéneo. [36] Utilizando técnicas postsintéticas, es posible la instalación controlada de dominios dentro de un cristal MOF que exhiben características estructurales y funcionales únicas. Se han preparado MOF de núcleo-cubierta y otros MOF en capas donde las capas tienen una funcionalización única pero en la mayoría de los casos son cristalográficamente compatibles de una capa a otra. [37]
En algunos casos, los nodos metálicos MOF tienen un entorno insaturado y es posible modificar este entorno utilizando diferentes técnicas. Si el tamaño del ligando coincide con el tamaño de la apertura del poro, es posible instalar ligandos adicionales en la estructura MOF existente. [38] [39] A veces, los nodos metálicos tienen una buena afinidad de unión por especies inorgánicas. Por ejemplo, se demostró que los nodos metálicos pueden realizar una extensión y crear un enlace con el catión uranilo. [40]
Otro enfoque para aumentar la adsorción en MOF es alterar el sistema de tal manera que sea posible la quimisorción . Esta funcionalidad se ha introducido fabricando un material compuesto, que contiene un MOF y un complejo de platino con carbón activado . En un efecto conocido como desbordamiento de hidrógeno , el H2 puede unirse a la superficie del platino a través de un mecanismo disociativo que escinde la molécula de hidrógeno en dos átomos de hidrógeno y les permite viajar por el carbón activado hasta la superficie del MOF. Esta innovación produjo un triple aumento en la capacidad de almacenamiento a temperatura ambiente de un MOF; sin embargo, la desorción puede tardar más de 12 horas y, a veces, se observa desorción reversible durante sólo dos ciclos. [41] [42] La relación entre el desbordamiento de hidrógeno y las propiedades de almacenamiento de hidrógeno en los MOF no se comprende bien, pero puede resultar relevante para el almacenamiento de hidrógeno.

Los MOF tienen potencial como catalizadores heterogéneos , aunque no se han comercializado aplicaciones. [43] Su alta superficie, porosidad sintonizable, diversidad de metales y grupos funcionales los hacen especialmente atractivos para su uso como catalizadores. Las zeolitas son extraordinariamente útiles en catálisis. [44] Las zeolitas están limitadas por la coordinación tetraédrica fija de los puntos de conexión Si/Al y los enlaces de óxido de dos coordinaciones. Se conocen menos de 200 zeolitas. En contraste con este alcance limitado, los MOF exhiben geometrías de coordinación , conectores politópicos y ligandos auxiliares más diversos (F − , OH − , H 2 O, entre otros). También es difícil obtener zeolitas con tamaños de poro superiores a 1 nm, lo que limita las aplicaciones catalíticas de las zeolitas a moléculas orgánicas relativamente pequeñas (normalmente no mayores que los xilenos ). Además, las condiciones sintéticas suaves que normalmente se emplean para la síntesis de MOF permiten la incorporación directa de funcionalidades delicadas en las estructuras estructurales. Tal proceso no sería posible con zeolitas u otros materiales microporosos a base de óxido cristalino debido a las duras condiciones típicamente utilizadas para su síntesis (por ejemplo, calcinación a altas temperaturas para eliminar plantillas orgánicas). La estructura metal-orgánica MIL-101 es uno de los MOF más utilizados para catálisis que incorpora diferentes metales de transición como el Cr. [45] Sin embargo, la estabilidad de algunos fotocatalizadores MOF en medio acuoso y en condiciones fuertemente oxidantes es muy baja. [46] [47]
Las zeolitas todavía no se pueden obtener en forma enantiopura, lo que excluye sus aplicaciones en síntesis catalítica asimétrica , por ejemplo, para las industrias farmacéutica, agroquímica y de fragancias. Se han incorporado ligandos quirales enantiopuros o sus complejos metálicos a los MOF para producir catalizadores asimétricos eficientes. Incluso algunos materiales MOF pueden cerrar la brecha entre las zeolitas y las enzimas cuando combinan sitios polinucleares aislados, respuestas dinámicas huésped-huésped y un entorno de cavidad hidrofóbica . Los MOF podrían resultar útiles para fabricar semiconductores. Los cálculos teóricos muestran que los MOF son semiconductores o aislantes con bandas prohibidas entre 1,0 y 5,5 eV que pueden alterarse cambiando el grado de conjugación en los ligandos, lo que indica su posibilidad de ser fotocatalizadores.

Al igual que otros catalizadores heterogéneos , los MOF pueden permitir una separación y un reciclado posteriores a la reacción más fáciles que los catalizadores homogéneos . En algunos casos, también proporcionan una estabilidad del catalizador muy mejorada. Además, normalmente ofrecen selectividad por el tamaño del sustrato. Sin embargo, aunque es claramente importante para las reacciones en sistemas vivos, la selectividad basada en el tamaño del sustrato tiene un valor limitado en la catálisis abiótica, ya que generalmente se encuentran disponibles materias primas razonablemente puras.

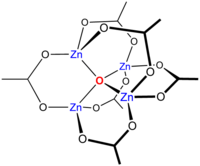
Entre los primeros informes de catálisis basada en MOF se encontraba la cianosililación de aldehídos mediante un MOF (cuadrículas cuadradas en capas) 2D de fórmula Cd(4,4 ′ -bpy) 2 (NO 3 ) 2 . [48] Esta investigación se centró principalmente en la clatración selectiva de tamaño y forma. Un segundo conjunto de ejemplos se basó en un MOF de rejilla cuadrada bidimensional que contenía iones Pd (II) individuales como nodos y 2-hidroxipirimidinolatos como puntales. [49] A pesar de la saturación coordinativa inicial , los centros de paladio en este MOF catalizan la oxidación del alcohol, la hidrogenación de olefinas y el acoplamiento Suzuki C-C. Como mínimo, estas reacciones implican necesariamente oscilaciones redox de los nodos metálicos entre los intermediarios Pd (II) y Pd (0) acompañadas de cambios drásticos en el número de coordinación, lo que ciertamente conduciría a la desestabilización y la posible destrucción de la estructura original si todo el Pd Los centros son catalíticamente activos. La observación de la selectividad de forma y tamaño del sustrato implica que las reacciones catalíticas son heterogéneas y, de hecho, ocurren dentro del MOF. Sin embargo, al menos para la hidrogenación, es difícil descartar la posibilidad de que la catálisis esté ocurriendo en la superficie de grupos/ nanopartículas de paladio encapsulados en MOF (es decir, sitios de descomposición parcial) o sitios defectuosos, en lugar de en sitios transitoriamente lábiles, pero por lo demás intactos. , nodos MOF de un solo átomo. Se ha descrito una catálisis "oportunista" basada en MOF para el compuesto cúbico MOF-5. [50] Este material comprende nodos de Zn 4 O coordinativamente saturados y puntales BDC completamente complejados (ver arriba para la abreviatura); sin embargo, aparentemente cataliza la terc-butilación de Friedel-Crafts tanto de tolueno como de bifenilo . Además, la para alquilación se ve fuertemente favorecida sobre la orto alquilación, un comportamiento que se cree que refleja la encapsulación de reactivos por el MOF.
El material de estructura porosa [Cu 3 (btc) 2 (H 2 O) 3 ] , también conocido como HKUST-1, [51] contiene grandes cavidades con ventanas de diámetro ~6 Å. Las moléculas de agua coordinadas se eliminan fácilmente, dejando sitios de Cu(II) abiertos. Kaskel y sus colaboradores demostraron que estos sitios ácidos de Lewis podrían catalizar la cianosililación de benzaldehído o acetona . La versión anhidra de HKUST-1 es un catalizador ácido. [52] En comparación con las vías catalizadas por ácido de Brønsted y Lewis , la selectividad del producto es distintiva para tres reacciones: isomerización de óxido de α-pineno, ciclación de citronelal y reordenamiento de α-bromoacetales, lo que indica que efectivamente [Cu 3 (btc) 2 ] funciona principalmente como catalizador ácido de Lewis . También se ha demostrado que la selectividad del producto y el rendimiento de las reacciones catalíticas (por ejemplo, ciclopropanación ) se ven afectados por sitios defectuosos, como Cu(I) o restos de ácido carboxílico desprotonados de forma incompleta de los conectores. [20]
MIL-101, un MOF de cavidad grande que tiene la fórmula [Cr 3 F (H 2 O) 2 O (BDC) 3 ], es un catalizador de cianosililación. [53] Las moléculas de agua coordinadas en MIL-101 se eliminan fácilmente para exponer los sitios de Cr(III). Como era de esperar, dada la mayor acidez de Lewis del Cr(III) frente al Cu(II), MIL-101 es mucho más activo que HKUST-1 como catalizador para la cianosililación de aldehídos . Además, el grupo de Kaskel observó que los sitios catalíticos de MIL-101, a diferencia de los de HKUST-1, son inmunes a la reducción no deseada por parte del benzaldehído . Long y colaboradores también han llevado a cabo la cianosililación catalizada por ácido de Lewis de aldehídos aromáticos utilizando un MOF de fórmula Mn 3 [(Mn 4 Cl) 3 BTT 8 (CH 3 OH) 10 ]. [54] Este material contiene una estructura de poros tridimensional, con un diámetro de poro igual a 10 Å. En principio, cualquiera de los dos tipos de sitios de Mn (II) podría funcionar como catalizador . Las características notables de este catalizador son los altos rendimientos de conversión (para sustratos pequeños) y una buena selectividad por tamaño de sustrato, consistente con la catálisis localizada en canales.
El enfoque de encapsulación de MOF invita a la comparación con estudios anteriores de catálisis oxidativa mediante sistemas de Fe ( porfirina ) [55] y Mn ( porfirina ) [56] encapsulados en zeolita . Los estudios de zeolita generalmente emplearon yodosilbenceno (PhIO), en lugar de TPHP como oxidante. Es probable que la diferencia sea mecánicamente significativa, lo que complica las comparaciones. Brevemente, PhIO es un donante de un solo átomo de oxígeno, mientras que TBHP es capaz de tener un comportamiento más complejo. Además, para el sistema basado en MOF, es concebible que la oxidación se produzca tanto a través de la transferencia de oxígeno desde un intermedio oxo de manganeso como a través de una vía de reacción en cadena de radicales iniciada por manganeso . Independientemente del mecanismo, el enfoque es prometedor para aislar y estabilizar así las porfirinas contra la formación de dímeros con puentes oxo y la degradación oxidativa. [57]
La mayoría de los ejemplos de catálisis basada en MOF utilizan iones o átomos metálicos como sitios activos. Entre las pocas excepciones se encuentran dos MOF que contienen níquel y dos cobre sintetizados por Rosseinsky y sus colaboradores. [58] Estos compuestos emplean aminoácidos (L- o D- aspartato ) junto con dipiridilos como puntales. La química de coordinación es tal que el grupo amino del aspartato no puede ser protonado mediante la adición de HCl , pero uno de los carboxilatos de aspartato sí puede. Por tanto, el aminoácido incorporado en la estructura puede existir en una forma que no sea accesible para el aminoácido libre . Mientras que los compuestos a base de níquel son marginalmente porosos , debido a las pequeñas dimensiones del canal, las versiones de cobre son claramente porosas. El grupo de Rosseinsky demostró que los ácidos carboxílicos se comportan como catalizadores ácidos de Brønsted, facilitando (en los casos de cobre) la metanólisis con apertura de anillo de un epóxido pequeño y accesible a la cavidad con un rendimiento de hasta el 65%. Sin embargo, existen catalizadores homogéneos superiores.
Kitagawa y colaboradores han informado sobre la síntesis de un MOF catalítico que tiene la fórmula [Cd(4-BTAPA) 2 (NO3 ) 2 ] . [59] El MOF es tridimensional y consta de un par de redes catenadas idénticas, pero aún presenta poros de dimensiones moleculares. Los nodos consisten en iones de cadmio individuales , ligados octaédricamente por nitrógenos de piridilo. Sin embargo, desde el punto de vista de la catálisis , la característica más interesante de este material es la presencia de funcionalidades amida accesibles para los huéspedes . Las amidas son capaces de catalizar con bases la condensación de Knoevenagel de benzaldehído con malononitrilo . Sin embargo, las reacciones con nitrilos más grandes se aceleran sólo marginalmente, lo que implica que la catálisis tiene lugar principalmente dentro de los canales del material y no en su exterior. Un hallazgo digno de mención es la falta de catálisis por parte del puntal libre en solución homogénea, evidentemente debido al enlace de H intermolecular entre moléculas de bptda. Por lo tanto, la arquitectura MOF provoca una actividad catalítica que de otro modo no se encontraría.
En un enfoque alternativo interesante, Férey y sus compañeros pudieron modificar el interior de MIL-101 mediante la coordinación con Cr (III) de uno de los dos átomos de nitrógeno disponibles de cada una de varias moléculas de etilendiamina . [60] Los extremos libres no coordinados de las etilendiaminas se utilizaron luego como catalizadores básicos de Brønsted, nuevamente para la condensación de Knoevenagel de benzaldehído con nitrilos .
Kim Kimoon y sus compañeros describieron un tercer enfoque . [61] Utilizando un derivado del ácido tartárico funcionalizado con piridina y una fuente de Zn (II), pudieron sintetizar un MOF 2D denominado POST-1. POST-1 posee canales 1D cuyas secciones transversales están definidas por seis grupos trinucleares de zinc y seis puntales. Mientras que tres de las seis piridinas están coordinadas por iones de zinc, las tres restantes están protonadas y dirigidas hacia el interior del canal. Cuando se neutralizan, los grupos piridilo no coordinados catalizan reacciones de transesterificación , presumiblemente facilitando la desprotonación del alcohol reactivo . La ausencia de catálisis significativa cuando se emplean alcoholes grandes sugiere fuertemente que la catálisis ocurre dentro de los canales del MOF.

Los metales en la estructura MOF a menudo actúan como ácidos de Lewis . Los metales en los MOF a menudo se coordinan con moléculas de solvente lábiles o contraiones que pueden eliminarse después de la activación de la estructura. La naturaleza ácida de Lewis de tales centros metálicos insaturados puede activar los sustratos orgánicos coordinados para transformaciones orgánicas posteriores. El uso de centros metálicos insaturados fue demostrado en la cianosililación de aldehídos e iminas por Fujita y compañeros de trabajo en 2004. [62] Informaron MOF de composición {[Cd(4,4 ′ -bpy) 2 (H 2 O) 2 ] • (NO 3 ) 2 • 4H 2 O} que se obtuvo tratando el ligando de puente lineal 4,4 ′ - bipiridina (bpy) con Cd(NO 3 ) 2 . Los centros de Cd (II) en este MOF poseen una geometría octaédrica distorsionada que tiene cuatro piridinas en las posiciones ecuatoriales y dos moléculas de agua en las posiciones axiales para formar una red infinita bidimensional. Tras la activación, se eliminaron dos moléculas de agua dejando los centros metálicos insaturados y ácidos de Lewis. El carácter ácido de Lewis del centro metálico se probó en reacciones de cianosililación de imina donde la imina se une al centro metálico ácido de Lewis, lo que da como resultado una mayor electrofilia de las iminas. Para la cianosililación de iminas, la mayoría de las reacciones se completaron en 1 h, proporcionando aminonitrilos con rendimiento cuantitativo. Kaskel y colaboradores [63] llevaron a cabo reacciones de cianosililación similares con metales coordinativamente insaturados en MOF tridimensionales (3D) como catalizadores heterogéneos. El marco 3D [Cu 3 (btc) 2 (H 2 O) 3 ] (btc: benceno-1,3,5-tricarboxilato ) ( HKUST-1 ) utilizado en este estudio fue informado por primera vez por Williams et al. [64] La estructura abierta de [Cu 3 (btc) 2 (H 2 O) 3 ] está construida a partir de unidades diméricas de tetracarboxilato cúprico (ruedas de paletas) con moléculas de agua que se coordinan con las posiciones axiales y ligandos puente btc. El armazón resultante después de la eliminación de dos moléculas de agua de sus posiciones axiales posee un canal poroso. Este MOF activado cataliza la trimetilcianosililación de benzaldehídos.con una conversión muy baja (<5% en 24 h) a 293 K. A medida que la temperatura de reacción se elevó a 313 K, se obtuvo una buena conversión del 57% con una selectividad del 89% después de 72 h. En comparación, se observó menos del 10 % de conversión para la reacción de fondo (sin MOF) en las mismas condiciones. Pero esta estrategia adolece de algunos problemas como 1) la descomposición de la estructura con aumento de la temperatura de reacción debido a la reducción de Cu(II) a Cu(I) por los aldehídos ; 2) fuerte efecto de inhibición de disolventes; los disolventes donadores de electrones, como el THF, competían con los aldehídos por la coordinación con los sitios Cu(II), y no se observó ningún producto de cianosililación en estos disolventes; 3) la inestabilidad estructural en algunos disolventes orgánicos. Varios otros grupos también han informado del uso de centros metálicos en MOF como catalizadores. [54] [65] Nuevamente, la naturaleza deficiente de electrones de algunos metales y grupos de metales hace que los MOF resultantes sean catalizadores de oxidación eficientes . Mori y compañeros de trabajo [66] informaron MOF con unidades de rueda de paletas de Cu 2 como catalizadores heterogéneos para la oxidación de alcoholes . La actividad catalítica del MOF resultante se examinó llevando a cabo oxidación de alcohol con H 2 O 2 como oxidante. También catalizó la oxidación de alcohol primario, alcohol secundario y alcoholes bencílicos con alta selectividad. Hill y cols. [67] han demostrado la sulfoxidación de tioéteres utilizando un MOF basado en unidades de construcción del grupo V 6 O 13 de vanadio-oxo .
Los enlazadores funcionales también se pueden utilizar como sitios catalíticos. A MOF 3D {[Cd(4-BTAPA) 2 (NO3 ) 2 ] • 6H2O • 2DMF} (4-BTAPA = tris [N-(4-piridil)amida] del ácido 1,3,5-bencenotricarboxílico] , DMF = N , N -dimetilformamida) construido mediante enlaces de amida tridentados y la sal de cadmio cataliza la reacción de condensación de Knoevenagel . [59] Los grupos piridina en el ligando 4-BTAPA actúan como ligandos que se unen a los centros octaédricos de cadmio, mientras que los grupos amida pueden proporcionar la funcionalidad para la interacción con los sustratos entrantes. Específicamente, el resto −NH del grupo amida puede actuar como aceptor de electrones , mientras que el grupo C=O puede actuar como donador de electrones para activar sustratos orgánicos para reacciones posteriores. Ferey et al. [68] informaron de un MOF robusto y altamente poroso [Cr 3 (μ 3 -O)F(H 2 O) 2 (BDC) 3 ] (BDC: benceno-1,4-dicarboxilato) donde en lugar de usar directamente el Cr insaturado (III) como sitios catalíticos, los autores injertaron etilendiamina (ED) en los sitios de Cr (III). Los extremos no coordinados de la DE pueden actuar como sitios catalíticos básicos. Se investigó el MOF injertado con ED para detectar reacciones de condensación de Knoevenagel. Se observó un aumento significativo en la conversión para MOF con injerto ED en comparación con la estructura no tratada (98 % frente a 36 %). Otro ejemplo de modificación del enlazador para generar un sitio catalítico son los conocidos MOF basados en Al (MIL-53 y DUT-5) y los MOF basados en Zr (UiO-66 y UiO-67) funcionalizados con yodo para la oxidación catalítica de dioles. [69] [70]
El atrapamiento de metales nobles catalíticamente activos se puede lograr injertando grupos funcionales en el sitio del metal insaturado en los MOF. Se ha demostrado que la etilendiamina (ED) se injerta en los sitios del metal Cr y puede modificarse aún más para encapsular metales nobles como el Pd. [60] El Pd atrapado tiene una actividad catalítica similar a la del Pd/C en la reacción de Heck . Las nanopartículas de rutenio tienen actividad catalítica en varias reacciones cuando quedan atrapadas en la estructura MOF-5. [71] Este MOF encapsulado en Ru cataliza la oxidación del alcohol bencílico a benzaldehído , aunque se produce degradación del MOF. El mismo catalizador se utilizó en la hidrogenación del benceno a ciclohexano . En otro ejemplo, las nanopartículas de Pd incrustadas en la estructura defectuosa de HKUST-1 permiten la generación de sitios básicos de Lewis sintonizables. [72] Por lo tanto, este compuesto multifuncional de Pd/MOF es capaz de realizar oxidación gradual de alcohol bencílico y condensación de Knoevenagel.
Los MOF podrían resultar útiles tanto para reacciones fotoquímicas como de polimerización debido a la capacidad de ajuste del tamaño y la forma de sus poros. Li y sus colaboradores sintetizaron un MOF 3D {[Co(bpdc) 3 (bpy)] • 4DMF • H2O } (bpdc: bifenildicarboxilato, bpy: 4,4 ′ -bipiridina). [73] Utilizando este MOF, se estudió ampliamente la fotoquímica de la o -metil dibencilcetona ( o -MeDBK). Se descubrió que esta molécula tiene una variedad de propiedades de reacción fotoquímica, incluida la producción de ciclopentanol . Los MOF se han utilizado para estudiar la polimerización en el espacio confinado de los canales MOF. Las reacciones de polimerización en espacios reducidos pueden tener propiedades diferentes a las de la polimerización en espacios abiertos. Kitagawa y colaboradores han estudiado el estireno , el divinilbenceno , los acetilenos sustituidos , el metacrilato de metilo y el acetato de vinilo como posibles monómeros activados para la polimerización radical . [74] [75] Debido al diferente tamaño del enlazador, el tamaño del canal MOF podría sintonizarse en el orden de aproximadamente 25 y 100 Å 2 . Se demostró que los canales estabilizan los radicales en propagación y suprimen las reacciones de terminación cuando se usan como sitios de polimerización de radicales.
Existen varias estrategias para construir MOF homoquirales . La cristalización de MOF homoquirales mediante la autorresolución de ligandos enlazadores aquirales es una de las formas de lograr tal objetivo. Sin embargo, las muestras masivas resultantes contienen enantiomorfos y son racémicas. Aoyama y compañeros de trabajo [76] obtuvieron con éxito MOF homoquirales en masa a partir de ligandos aquirales controlando cuidadosamente la nucleación en el proceso de crecimiento de los cristales . Zheng y colaboradores [77] informaron sobre la síntesis de MOF homoquirales a partir de ligandos aquirales mediante la manipulación química de la fluctuación estadística de la formación de pares de cristales enantioméricos. El cultivo de cristales de MOF bajo influencias quirales es otro enfoque para obtener MOF homoquirales utilizando ligandos enlazadores aquirales. Rosseinsky y sus compañeros de trabajo [78] [79] han introducido un coligando quiral para dirigir la formación de MOF homoquirales controlando la lateralidad de las hélices durante el crecimiento del cristal. Morris y compañeros de trabajo [80] utilizaron líquido iónico con cationes quirales como medio de reacción para sintetizar MOF y obtuvieron MOF homoquirales. Sin embargo, la estrategia más sencilla y racional para sintetizar MOF homoquirales es utilizar ligandos enlazadores quirales fácilmente disponibles para su construcción.
Lin y sus compañeros de trabajo han fabricado MOF homoquirales utilizando 2,2 ′ -bis(difenilfosfino)-1,1 ′ -binaftilo ( BINAP ) y 1,1 ′ -bi-2,2 ′ -naftol ( BINOL ) como ligandos quirales. [81] Estos ligandos pueden coordinarse con sitios metálicos catalíticamente activos para mejorar la enantioselectividad . Se pueden introducir selectivamente una variedad de grupos de enlace tales como piridina , ácido fosfónico y ácido carboxílico en las posiciones 3,3 ' , 4,4 ' y 6,6 ' del resto 1,1'-binaftilo. Además, al cambiar la longitud de los ligandos enlazadores, la porosidad y la estructura estructural del MOF se pueden ajustar selectivamente.
Lin y sus compañeros de trabajo han demostrado que la posmodificación de los MOF se puede lograr para producir MOF homoquirales enantioselectivos para su uso como catalizadores. [82] El MOF homoquiral 3D resultante {[Cd 3 (L) 3 Cl 6 ] • 4DMF • 6MeOH • 3H 2 O} (L=(R)-6,6'-dicloro-2,2'-dihidroxil-1 ,1'-binaftil-bipiridina) sintetizada por Lin demostró tener una eficiencia catalítica similar para la reacción de adición de dietilzinc en comparación con el análogo homogéneo cuando se pretrató con Ti(O i Pr) 4 para generar la especie Ti-BINOLato injertada. La actividad catalítica de los MOF puede variar según la estructura del marco. Lin y otros descubrieron que los MOF sintetizados a partir de los mismos materiales podrían tener actividades catalíticas drásticamente diferentes dependiendo de la estructura estructural presente. [83]
Otro enfoque para construir MOF homoquirales catalíticamente activos es incorporar complejos metálicos quirales que son catalizadores activos o precatalizadores directamente en las estructuras estructurales. Por ejemplo, Hupp y colaboradores [84] combinaron un ligando quiral y bpdc (bpdc: bifenildicarboxilato) con Zn(NO 3 ) 2 y obtuvieron redes 3D interpenetrantes dobles. La orientación del ligando quiral en las estructuras hace que todos los sitios de Mn(III) sean accesibles a través de los canales. Las estructuras abiertas resultantes mostraron actividad catalítica hacia reacciones asimétricas de epoxidación de olefinas. No se observó una disminución significativa de la actividad del catalizador durante la reacción y el catalizador pudo reciclarse y reutilizarse varias veces. Lin y colaboradores [85] han informado sobre sistemas Ru-BINAP derivados de fosfonato de circonio. Los materiales híbridos porosos quirales a base de fosfonato de circonio que contienen precatalizadores Ru(BINAP)(diamina)Cl 2 mostraron una excelente enantioselectividad (hasta 99,2% ee) en la hidrogenación asimétrica de cetonas aromáticas.
Algunos materiales MOF pueden parecerse a enzimas cuando combinan sitios polinucleares aislados, respuestas dinámicas huésped-huésped y un ambiente de cavidad hidrofóbica que son características de una enzima. [86] Algunos ejemplos bien conocidos de catálisis cooperativa que involucra dos iones metálicos en sistemas biológicos incluyen: los sitios de hierro en la metano monooxigenasa , dicobre en la citocromo c oxidasa y tricobre oxidasas que tienen analogía con grupos polinucleares que se encuentran en los polímeros de coordinación 0D, como como unidades binucleares de rueda de paletas de Cu 2 encontradas en MOP-1 [87] [88] y [Cu 3 (btc) 2 ] (btc=benceno-1,3,5-tricarboxilato) en HKUST-1 o unidades trinucleares como { Fe 3 O(CO 2 ) 6 } en MIL-88, [89] e IRMOP-51. [90] Por lo tanto, los MOF 0D tienen centros catalíticos biomiméticos accesibles . En los sistemas enzimáticos, las unidades proteicas muestran "reconocimiento molecular", alta afinidad por sustratos específicos. Parece que los efectos del reconocimiento molecular están limitados en las zeolitas por la estructura rígida de la zeolita. [91] Por el contrario, las características dinámicas y la respuesta en forma de huésped hacen que los MOF sean más similares a las enzimas. De hecho, muchas estructuras híbridas contienen partes orgánicas que pueden girar como resultado de estímulos, como la luz y el calor. [92] Los canales porosos en las estructuras MOF se pueden utilizar como sitios de fotocatálisis . En fotocatálisis, el uso de complejos mononucleares suele estar limitado porque solo se someten a un proceso de un solo electrón o por la necesidad de irradiación de alta energía. En este caso, los sistemas binucleares presentan una serie de características atractivas para el desarrollo de fotocatalizadores. [93] Para estructuras MOF 0D, los nodos policatiónicos pueden actuar como puntos cuánticos semiconductores que pueden activarse ante fotoestímulos con los enlazadores sirviendo como antenas de fotones. [94] Los cálculos teóricos muestran que los MOF son semiconductores o aislantes con bandas prohibidas entre 1,0 y 5,5 eV que pueden alterarse cambiando el grado de conjugación en los ligandos. [95] Los resultados experimentales muestran que la banda prohibida de muestras de tipo IRMOF se puede ajustar variando la funcionalidad del enlazador. [96] Se desarrolló una nanozima MOF integrada para la terapia antiinflamatoria. [97]
La implementación de MOF en la industria requiere una comprensión profunda de las propiedades mecánicas, ya que la mayoría de las técnicas de procesamiento (por ejemplo, extrusión y peletización) exponen los MOF a importantes tensiones de compresión mecánica. [98] La respuesta mecánica de las estructuras porosas es de interés ya que estas estructuras pueden exhibir una respuesta inusual a altas presiones. Si bien las zeolitas ( minerales de aluminosilicato microporosos ) pueden brindar algunas ideas sobre la respuesta mecánica de los MOF, la presencia de conectores orgánicos, a diferencia de las zeolitas , genera respuestas mecánicas novedosas. [99] Los MOF son estructuralmente muy diversos, lo que significa que es un desafío clasificar todas sus propiedades mecánicas. Además, la variabilidad en los MOF de un lote a otro y las condiciones experimentales extremas ( celdas de yunque de diamante ) significan que la determinación experimental de la respuesta mecánica a la carga es limitada; sin embargo, se han creado muchos modelos computacionales para determinar las relaciones estructura-propiedad. Los principales sistemas MOF que se han explorado son las estructuras de imidazolato zeolítico (ZIF), los MOF de carboxilato y los MOF basados en circonio, entre otros. [99] Generalmente, los MOF se someten a tres procesos bajo carga de compresión (lo cual es relevante en un contexto de procesamiento): amorfización, hiperllenado y/o transiciones de fase inducidas por presión. Durante la amorfización, los enlazadores se pandean y la porosidad interna dentro del MOF colapsa. Durante el hiperllenado, el MOF que se comprime hidrostáticamente en un líquido (normalmente disolvente) se expandirá en lugar de contraerse debido al llenado de los poros con el medio de carga. Finalmente, son posibles transiciones de fase inducidas por presión en las que la estructura del cristal se altera durante la carga. La respuesta del MOF depende predominantemente de la especie enlazadora y de los nodos inorgánicos.
Se han observado varios fenómenos mecánicos diferentes en estructuras de imidazolato zeolítico (ZIF), los MOF más estudiados en cuanto a propiedades mecánicas debido a sus muchas similitudes con las zeolitas. [99] Las tendencias generales para la familia ZIF son la tendencia del módulo de Young y la dureza de los ZIF a disminuir a medida que aumenta el volumen de poros accesible. [100] Los módulos de volumen de la serie ZIF-62 aumentan con el aumento de la concentración de benzoimidazolato (bim − ). ZIF-62 muestra una transición de fase continua desde la fase de poro abierto ( op ) a la fase de poro cerrado ( cp ) cuando la concentración de bim - es superior a 0,35 por unidad de fórmula. El tamaño y el volumen de poro accesibles de ZIF-62-bim 0,35 se pueden ajustar con precisión aplicando presiones adecuadas. [101] Otro estudio ha demostrado que bajo carga hidrostática en solvente el material ZIF-8 se expande en lugar de contraerse. Esto es el resultado del hiperllenado de los poros internos con disolvente. [102] Un estudio computacional demostró que los materiales ZIF-4 y ZIF-8 se someten a un mecanismo de ablandamiento por cizallamiento con amorfización (a ~ 0,34 GPa) del material bajo carga hidrostática, sin dejar de poseer un módulo de volumen del orden de 6,5 GPa. [103] [104] Además, los MOF ZIF-4 y ZIF-8 están sujetos a muchas transiciones de fase dependientes de la presión. [100] [105]
Los MOF de carboxilato se presentan en muchas formas y han sido ampliamente estudiados. En este documento, las series HKUST-1, MOF-5 y MIL se analizan como ejemplos representativos de la clase MOF de carboxilato.
HKUST-1 consta de una rueda de paletas de Cu dimérica que posee dos tipos de poros. Bajo peletización, los MOF como HKUST-1 exhiben un colapso de los poros. [106] Aunque la mayoría de los MOF de carboxilato tienen una expansión térmica negativa (se densifican durante el calentamiento), se descubrió que la dureza y los módulos de Young disminuyen inesperadamente al aumentar la temperatura debido al desorden de los enlazadores. [107] También se encontró computacionalmente que una estructura más mesoporosa tiene un módulo de volumen más bajo. Sin embargo, se observó un aumento del módulo de volumen en sistemas con unos pocos mesoporos grandes versus muchos mesoporos pequeños, aunque ambas distribuciones de tamaño de poro tenían el mismo volumen total de poro. [108] El HKUST-1 muestra un fenómeno de "hiperllenado" similar al de las estructuras ZIF bajo carga hidrostática. [109]
MOF-5 tiene nodos tetranucleares en una configuración octaédrica con una estructura cúbica general. MOF-5 tiene una compresibilidad y un módulo de Young (~14,9 GPa) comparables a los de la madera, lo que se confirmó con la teoría funcional de la densidad (DFT) y la nanoindentación . [110] [111] Si bien se demostró que el MOF-5 puede demostrar el fenómeno de hiperllenado dentro de un medio de carga de solvente, estos MOF son muy sensibles a la presión y sufren un colapso de poro inducido por amorfización/presión a una presión de 3,5 MPa cuando hay No hay líquido en los poros. [112]

Los MOF MIL-53 poseen una estructura de "botellero". Estos MOF se han explorado para determinar la anisotropía en el módulo de Young debido a la flexibilidad de la carga y el potencial de compresibilidad lineal negativa cuando se comprimen en una dirección, debido a la capacidad del botellero para abrirse durante la carga. [113] [114]

Los MOF a base de circonio, como el UiO-66, son una clase muy robusta de MOF (atribuidos a fuertes nodos metálicos hexanucleares) con mayor resistencia al calor, los disolventes y otras condiciones adversas, lo que los hace interesantes en términos de propiedades mecánicas. [115] Las determinaciones del módulo de corte y la granulación han demostrado que los MOF UiO-66 son muy robustos mecánicamente y tienen una alta tolerancia al colapso de los poros en comparación con los ZIF y los MOF de carboxilato. [106] [116] Aunque el MOF UiO-66 muestra una mayor estabilidad bajo peletización, los MOF UiO-66 se amorfizaron con bastante rapidez en condiciones de molienda de bolas debido a la destrucción de los nodos inorgánicos coordinadores del enlazador. [117]
El hidrógeno molecular tiene la energía específica más alta de todos los combustibles. Sin embargo, a menos que el gas hidrógeno se comprima, su densidad de energía volumétrica es muy baja, por lo que el transporte y almacenamiento de hidrógeno requieren procesos de compresión y licuefacción que consumen mucha energía. [118] [119] [120] Por lo tanto, el desarrollo de nuevos métodos de almacenamiento de hidrógeno que disminuyan la presión concomitante requerida para la densidad de energía volumétrica práctica es un área activa de investigación. [118] Los MOF atraen la atención como materiales para el almacenamiento de hidrógeno por adsorción debido a sus altas áreas de superficie específicas y relaciones superficie-volumen, así como sus estructuras químicamente sintonizables. [41]
En comparación con un cilindro de gas vacío , un cilindro de gas lleno de MOF puede almacenar más hidrógeno a una presión determinada porque las moléculas de hidrógeno se adsorben en la superficie de los MOF. Además, los MOF no tienen volumen muerto, por lo que casi no hay pérdida de capacidad de almacenamiento como resultado del bloqueo de espacio por un volumen no accesible. [8] Además, debido a que la absorción de hidrógeno se basa principalmente en la fisisorción , muchos MOF tienen un comportamiento de absorción y liberación totalmente reversible. No se requieren grandes barreras de activación para liberar el hidrógeno adsorbido. [8] La capacidad de almacenamiento de un MOF está limitada por la densidad del hidrógeno en fase líquida porque los beneficios proporcionados por los MOF sólo pueden obtenerse si el hidrógeno está en estado gaseoso. [8]
El grado en que un gas puede adsorberse en la superficie de un MOF depende de la temperatura y la presión del gas. En general, la adsorción aumenta al disminuir la temperatura y aumentar la presión (hasta que se alcanza un máximo, típicamente 20 a 30 bar, después del cual la capacidad de adsorción disminuye). [8] [41] [120] Sin embargo, los MOF que se utilizarán para el almacenamiento de hidrógeno en celdas de combustible de automóviles deben funcionar de manera eficiente a temperatura ambiente y presiones entre 1 y 100 bar, ya que estos son los valores que se consideran seguros para aplicaciones automotrices. [41]

El Departamento de Energía de EE. UU. (DOE) ha publicado una lista de objetivos técnicos anuales del sistema para el almacenamiento de hidrógeno a bordo de vehículos ligeros de pila de combustible que guían a los investigadores en el campo (5,5 % en peso/40 g L −1 para 2017; 7,5 % en peso/70 g L −1 último). [121] Se han diseñado y sintetizado materiales con alta porosidad y gran superficie, como los MOF, en un esfuerzo por cumplir estos objetivos. Estos materiales adsorbentes generalmente funcionan mediante adsorción física en lugar de quimisorción debido a la gran brecha HOMO-LUMO y al bajo nivel de energía HOMO del hidrógeno molecular. Un material de referencia para este fin es el MOF-177, que almacena hidrógeno al 7,5 % en peso con una capacidad volumétrica de 32 g L −1 a 77 K y 70 bar. [122] MOF-177 consta de grupos [Zn 4 O] 6+ interconectados por enlaces orgánicos de 1,3,5-bencenotribenzoato y tiene un área de superficie BET medida de 4630 m 2 g −1 . Otro material ejemplar es PCN-61 que exhibe una absorción de hidrógeno de 6,24 % en peso y 42,5 g L −1 a 35 bar y 77 K y 2,25 % en peso a presión atmosférica. [123] PCN-61 consta de [Cu 2 ] 4+ unidades de rueda de paletas conectadas a través de enlaces orgánicos 5,5 ′ ,5 ′ ′ -benceno-1,3,5-triiltris(1-etinil-2-isoftalato) y tiene una superficie BET medida de 3000 m 2 g −1 . A pesar de estos prometedores ejemplos de MOF, las clases de materiales porosos sintéticos con mayor rendimiento para el almacenamiento práctico de hidrógeno son el carbón activado y las estructuras orgánicas covalentes (COF). [124]
Las aplicaciones prácticas de los MOF para el almacenamiento de hidrógeno enfrentan varios desafíos. Para la adsorción de hidrógeno cerca de la temperatura ambiente, sería necesario aumentar considerablemente la energía de unión del hidrógeno. [41] Se han explorado varias clases de MOF, incluidos los MOF basados en carboxilato , los MOF basados en azolato heterocíclico , los MOF de cianuro metálico y las estructuras orgánicas covalentes . Los MOF basados en carboxilato han recibido, con diferencia, la mayor atención porque
Los metales de transición más comunes empleados en estructuras a base de carboxilato son Cu 2+ y Zn 2+ . También se han explorado iones metálicos más ligeros del grupo principal . Be 12 (OH) 12 (BTB) 4 , el primer MOF sintetizado y caracterizado estructuralmente con éxito que consiste en un ion metálico ligero del grupo principal, muestra una alta capacidad de almacenamiento de hidrógeno, pero es demasiado tóxico para ser empleado en la práctica. [125] Se están realizando esfuerzos considerables en el desarrollo de MOF compuestos de otros iones metálicos ligeros del grupo principal, como el magnesio en Mg 4 (BDC) 3 . [41]
La siguiente es una lista de varios MOF que se considera que tienen las mejores propiedades para el almacenamiento de hidrógeno en mayo de 2012 (en orden decreciente de capacidad de almacenamiento de hidrógeno). [41] Si bien cada MOF descrito tiene sus ventajas, ninguno de estos MOF alcanza todos los estándares establecidos por el DOE de EE. UU. Por lo tanto, aún no se sabe si los materiales con áreas superficiales altas, poros pequeños o grupos de metales di o trivalentes producen los MOF más favorables para el almacenamiento de hidrógeno. [8]
Hasta la fecha, el almacenamiento de hidrógeno en MOF a temperatura ambiente es una batalla entre maximizar la capacidad de almacenamiento y mantener tasas de desorción razonables, al tiempo que se conserva la integridad de la estructura adsorbente (por ejemplo, evacuar completamente los poros, preservar la estructura del MOF, etc.) durante muchos ciclos. Hay dos estrategias principales que rigen el diseño de MOF para el almacenamiento de hidrógeno:
La tendencia general en los MOF utilizados para el almacenamiento de hidrógeno es que cuanto mayor es la superficie, más hidrógeno puede almacenar el MOF. Los materiales de alta área superficial tienden a exhibir un mayor volumen de microporos y una densidad aparente inherentemente baja, lo que permite que se produzca una mayor adsorción de hidrógeno. [41]
También es importante una alta entalpía de adsorción de hidrógeno. Los estudios teóricos han demostrado que las interacciones de 22 a 25 kJ/mol son ideales para el almacenamiento de hidrógeno a temperatura ambiente, ya que son lo suficientemente fuertes como para adsorber H 2 , pero lo suficientemente débiles como para permitir una rápida desorción. [133] La interacción entre el hidrógeno y los enlaces orgánicos no cargados no es tan fuerte, por lo que se ha realizado una cantidad considerable de trabajo en la síntesis de MOF con sitios metálicos expuestos, en los que el hidrógeno se adsorbe con una entalpía de 5 a 10 kJ/mol. Sintéticamente, esto se puede lograr mediante el uso de ligandos cuyas geometrías impidan que el metal esté completamente coordinado, eliminando moléculas volátiles de disolvente unidas a metales durante el transcurso de la síntesis y mediante impregnación post-sintética con cationes metálicos adicionales. [13] [129] (C 5 H 5 )V(CO) 3 (H 2 ) y Mo(CO) 5 (H 2 ) son excelentes ejemplos de mayor energía de enlace debido a los sitios de coordinación metálicos abiertos; [134] sin embargo, sus altas energías de disociación del enlace metal-hidrógeno dan como resultado una tremenda liberación de calor al cargarlas con hidrógeno, lo que no es favorable para las pilas de combustible . [41] Los MOF, por lo tanto, deben evitar interacciones orbitales que conducen a enlaces metal-hidrógeno tan fuertes y emplear interacciones dipolares inducidas por carga simple , como se demuestra en Mn 3 [(Mn 4 Cl) 3 (BTT) 8 ] 2 .
Una energía de asociación de 22 a 25 kJ/mol es típica de las interacciones dipolares inducidas por carga, por lo que existe interés en el uso de conectores y metales cargados. [41] La fuerza del enlace metal-hidrógeno disminuye en los MOF, probablemente debido a la difusión de carga, por lo que se están estudiando iones metálicos 2+ y 3+ para fortalecer aún más esta interacción. Un problema con este enfoque es que los MOF con superficies metálicas expuestas tienen concentraciones más bajas de enlazadores; esto los hace difíciles de sintetizar, ya que son propensos al colapso del marco. Esto también puede disminuir su vida útil. [13] [41]
Los MOF suelen ser sensibles a la humedad del aire. En particular, IRMOF-1 se degrada en presencia de pequeñas cantidades de agua a temperatura ambiente. Los estudios sobre análogos de metales han desvelado la capacidad de metales distintos del Zn para soportar mayores concentraciones de agua a altas temperaturas. [135] [136]
Para compensar esto, se necesitan contenedores de almacenamiento especialmente construidos, lo que puede resultar costoso. Se sabe que los fuertes enlaces metal-ligando, como en las estructuras de imidazolato, triazolato y pirazolato metálico, disminuyen la sensibilidad de un MOF al aire, lo que reduce el gasto de almacenamiento. [137]
En un material microporoso donde la fisisorción y las fuerzas débiles de Van der Waals dominan la adsorción, la densidad de almacenamiento depende en gran medida del tamaño de los poros. Los cálculos de materiales homogéneos idealizados, como los carbonos grafíticos y los nanotubos de carbono , predicen que un material microporoso con poros de 7 Å de ancho exhibirá una absorción máxima de hidrógeno a temperatura ambiente. Con este ancho, exactamente dos capas de moléculas de hidrógeno se adsorben en superficies opuestas sin dejar espacio entre ellas. [41] [138] Los poros de 10 Å de ancho también tienen un tamaño ideal porque, con este ancho, pueden existir exactamente tres capas de hidrógeno sin espacio entre ellas. [41] (Una molécula de hidrógeno tiene una longitud de enlace de 0,74 Å con un radio de van der Waals de 1,17 Å para cada átomo; por lo tanto, su longitud efectiva de van der Waals es 3,08 Å.) [139]
Los defectos estructurales también juegan un papel importante en el desempeño de los MOF. La absorción de hidrógeno a temperatura ambiente a través de puentes se rige principalmente por defectos estructurales, que pueden tener dos efectos:
Los defectos estructurales también pueden dejar los nodos que contienen metal coordinados de manera incompleta. Esto mejora el rendimiento de los MOF utilizados para el almacenamiento de hidrógeno al aumentar la cantidad de centros metálicos accesibles. [141] Finalmente, los defectos estructurales pueden afectar el transporte de fonones , lo que afecta la conductividad térmica del MOF. [142]
La adsorción es el proceso de atrapar átomos o moléculas que inciden sobre una superficie; por lo tanto, la capacidad de adsorción de un material aumenta con su superficie. En tres dimensiones, la superficie máxima la obtendrá una estructura muy porosa, de modo que los átomos y moléculas puedan acceder a las superficies internas. Este simple argumento cualitativo sugiere que las estructuras organometálicas (MOF) altamente porosas deberían ser excelentes candidatos para dispositivos de almacenamiento de hidrógeno.
La adsorción se puede clasificar en términos generales en uno de dos tipos: fisisorción o quimisorción . La fisisorción se caracteriza por interacciones débiles de van der Waals y entalpías de enlace típicamente inferiores a 20 kJ/mol. La quimisorción, alternativamente, se define por enlaces covalentes e iónicos más fuertes , con entalpías de enlace entre 250 y 500 kJ/mol. En ambos casos, los átomos o moléculas de adsorbato (es decir, las partículas que se adhieren a la superficie) son atraídos hacia la superficie adsorbente (sólida) debido a la energía superficial que resulta de las ubicaciones de enlace desocupadas en la superficie. El grado de superposición orbital determina si las interacciones serán fisisortivas o quimisortivas. [143]
La adsorción de hidrógeno molecular en MOF es fisisortiva. Dado que el hidrógeno molecular solo tiene dos electrones, las fuerzas de dispersión son débiles, típicamente de 4 a 7 kJ/mol, y solo son suficientes para la adsorción a temperaturas inferiores a 298 K. [41]
Se logró una explicación completa del mecanismo de sorción de H 2 en los MOF mediante un promedio estadístico en el gran conjunto canónico, explorando una amplia gama de presiones y temperaturas. [144] [145]
Se utilizan dos métodos de medición de la absorción de hidrógeno para la caracterización de MOF como materiales de almacenamiento de hidrógeno: gravimétrico y volumétrico . Para obtener la cantidad total de hidrógeno en el MOF se debe considerar tanto la cantidad de hidrógeno absorbido en su superficie como la cantidad de hidrógeno residente en sus poros. Para calcular la cantidad absorbida absoluta ( N abs ), la cantidad en exceso de la superficie ( N ex ) se agrega al producto de la densidad aparente del hidrógeno (ρ a granel ) y el volumen de poros del MOF ( V poro ), como se muestra en la siguiente ecuación: [146]
El aumento de masa del MOF debido al hidrógeno almacenado se calcula directamente mediante una microbalanza altamente sensible. [146] Debido a la flotabilidad , la masa detectada de hidrógeno adsorbido disminuye nuevamente cuando se aplica una presión suficientemente alta al sistema porque la densidad del hidrógeno gaseoso circundante se vuelve cada vez más importante a presiones más altas. Por tanto, esta "pérdida de peso" debe corregirse utilizando el volumen de la estructura del MOF y la densidad del hidrógeno. [147]
El cambio en la cantidad de hidrógeno almacenado en el MOF se mide detectando la presión variada del hidrógeno a volumen constante. [146] El volumen de hidrógeno adsorbido en el MOF se calcula restando el volumen de hidrógeno en el espacio libre del volumen total de hidrógeno dosificado. [148]
Existen seis métodos posibles que se pueden utilizar para el almacenamiento reversible de hidrógeno con alta densidad volumétrica y gravimétrica, los cuales se resumen en la siguiente tabla (donde ρ m es la densidad gravimétrica, ρ v es la densidad volumétrica, T es la temperatura de trabajo y P es la presión de trabajo): [149]
De estos, los cilindros de gas a alta presión y el hidrógeno líquido en tanques criogénicos son las formas menos prácticas de almacenar hidrógeno como combustible debido a la presión extremadamente alta requerida para almacenar hidrógeno gaseoso o la temperatura extremadamente baja requerida para almacenar hidrógeno líquido. Los demás métodos se están estudiando y desarrollando exhaustivamente. [149]
La alta área de superficie y los sitios metálicos atómicos de los MOF los convierten en candidatos adecuados para electrocatalizadores , especialmente los relacionados con la energía. Hasta ahora, los MOF se han utilizado ampliamente como electrocatalizador para la división del agua (reacción de desprendimiento de hidrógeno y reacción de desprendimiento de oxígeno), reducción de dióxido de carbono y reacción de reducción de oxígeno. [150] Actualmente existen dos rutas: 1. Utilizar MOF como precursores para preparar electrocatalizadores con soporte de carbono. [151] 2. Utilizar MOF directamente como electrocatalizadores. [152] [153] Sin embargo, algunos resultados han demostrado que algunos MOF no son estables en un entorno electroquímico. [154] La conversión electroquímica de MOF durante la electrocatálisis puede producir materiales catalizadores reales, y los MOF son precatalizadores en tales condiciones. [155] Por lo tanto, reivindicar los MOF como electrocatalizadores requiere técnicas in situ junto con electrocatálisis.

Una aplicación potencial para los MOF es la obtención de imágenes biológicas y la detección mediante fotoluminiscencia . Un gran subconjunto de MOF luminiscentes utiliza lantánidos en los grupos metálicos. La fotoluminiscencia de los lantánidos tiene muchas propiedades únicas que los hacen ideales para aplicaciones de imágenes, como bandas de emisión característicamente nítidas y generalmente no superpuestas en las regiones visible e infrarroja cercana (NIR) del espectro, resistencia al fotoblanqueo o "parpadeo" y larga duración. Vidas de luminiscencia. [156] Sin embargo, las emisiones de lantánidos son difíciles de sensibilizar directamente porque deben someterse a transiciones ff prohibidas por LaPorte . La sensibilización indirecta de la emisión de lantánidos se puede lograr empleando el "efecto antena", donde los enlazadores orgánicos actúan como antenas y absorben la energía de excitación, transfieren la energía al estado excitado del lantánido y producen luminiscencia del lantánido tras la relajación. [157] Un excelente ejemplo del efecto antena lo demuestra MOF-76, que combina iones de lantánidos trivalentes y enlazadores de 1,3,5-bencenotricarboxilato (BTC) para formar SBU de varillas infinitas coordinadas en una red tridimensional. [158] Como lo demostraron múltiples grupos de investigación, el conector BTC puede sensibilizar eficazmente la emisión de lantánidos, lo que da como resultado un MOF con longitudes de onda de emisión variables dependiendo de la identidad de los lantánidos. [159] [160] Además, el grupo Yan ha demostrado que Eu 3+ - y Tb 3+ - MOF-76 se pueden utilizar para la detección selectiva de acetofenona de otros hidrocarburos monoaromáticos volátiles. Tras la absorción de acetofenona, el MOF muestra una disminución o extinción muy marcada de la intensidad de la luminiscencia. [161]
Sin embargo, para su uso en imágenes biológicas, se deben superar dos obstáculos principales:
Con respecto al primer punto, la síntesis de MOF (NMOF) a nanoescala se mencionó en una sección anterior. El último obstáculo aborda la limitación del efecto antena. Los enlazadores más pequeños tienden a mejorar la estabilidad de los MOF, pero tienen mayores absorciones de energía, predominantemente en las regiones ultravioleta (UV) y visibles de alta energía. Se ha logrado una estrategia de diseño para MOF con propiedades de absorción desplazadas al rojo mediante el uso de enlaces cromóforos grandes. Estos enlazadores a menudo están compuestos de especies poliaromáticas, lo que da lugar a poros de gran tamaño y, por tanto, a una menor estabilidad. Para evitar el uso de enlazadores grandes, se requieren otros métodos para desplazar al rojo la absorbancia del MOF, de modo que se puedan utilizar fuentes de excitación de menor energía. La modificación postsintética (PSM) es una estrategia prometedora. Luo y col. introdujo una nueva familia de MOF de lantánidos con conectores orgánicos funcionalizados. Los MOF, considerados MOF-1114, MOF-1115, MOF-1130 y MOF-1131, están compuestos de SBU octaédricas unidas por enlaces de dicarboxilato amino funcionalizados. Los grupos amino de los conectores sirvieron como sitios para reacciones covalentes de PSM con salicilaldehído o 3-hidroxinaftaleno-2-carboxaldehído. Ambas reacciones extienden la conjugación π del conector, provocando un corrimiento al rojo en la longitud de onda de absorbancia de 450 nm a 650 nm. Los autores también proponen que esta técnica podría adaptarse a sistemas MOF similares y, al aumentar el volumen de poros con longitudes de conector cada vez mayores, se pueden usar reactivos conjugados con pi más grandes para desplazar aún más al rojo las longitudes de onda de absorción. [164] Varios grupos, a saber, Foucault-Collet y sus colaboradores, han realizado imágenes biológicas utilizando MOF. En 2013, sintetizaron un Yb 3+ -NMOF emisor de NIR utilizando conectores de dicarboxilato de fenilenvinileno (PVDC). Observaron la captación celular tanto en células HeLa como en células NIH-3T3 mediante espectroscopía confocal, visible y NIR. [165] Aunque persisten rendimientos cuánticos bajos en agua y solución tampón de Hepes, la intensidad de la luminiscencia sigue siendo lo suficientemente fuerte como para visualizar la captación celular tanto en el régimen visible como en el NIR.

El desarrollo de nuevas vías para una administración eficiente de los desechos nucleares es esencial a raíz de la creciente preocupación pública por la contaminación radiactiva , debido a la operación de las plantas nucleares y al desmantelamiento de las armas nucleares. La síntesis de nuevos materiales capaces de secuestrar y separar selectivamente actínidos es uno de los desafíos actuales reconocidos en el sector de los residuos nucleares. Las estructuras metal-orgánicas (MOF) son una clase prometedora de materiales para abordar este desafío debido a su porosidad, modularidad, cristalinidad y capacidad de ajuste. Cada componente básico de las estructuras MOF puede incorporar actínidos. En primer lugar, se puede sintetizar un MOF a partir de sales de actínidos. En este caso los nodos metálicos son actínidos. [40] [166] Además, los nodos metálicos se pueden extender o el intercambio catiónico puede intercambiar metales por actínidos. [40] Los conectores orgánicos pueden funcionalizarse con grupos capaces de captar actínidos. [167] [168] [169] [170] [171] Por último, la porosidad de los MOF se puede utilizar para incorporar moléculas invitadas contenidas [172] [173] [174] y atraparlas en una estructura mediante la instalación de elementos adicionales o de protección. enlazadores. [40]
La síntesis, caracterización y estudios relacionados con fármacos de MOF biocompatibles y de baja toxicidad han demostrado que tienen potencial para aplicaciones médicas. Muchos grupos han sintetizado varios MOF de baja toxicidad y han estudiado sus usos en la carga y liberación de diversos fármacos terapéuticos para posibles aplicaciones médicas. Existe una variedad de métodos para inducir la liberación de fármacos, como la respuesta al pH, la respuesta magnética, la respuesta a los iones, la respuesta a la temperatura y la respuesta a la presión. [175]
En 2010, Smaldone et al., un grupo de investigación internacional, sintetizaron un MOF biocompatible denominado CD-MOF-1 a partir de productos naturales comestibles baratos. CD-MOF-1 consta de unidades básicas repetidas de 6 anillos de γ-ciclodextrina unidos por iones de potasio. La γ-ciclodextrina (γ-CD) es un oligosacárido cíclico simétrico que se produce enzimáticamente en masa a partir de almidón y consta de ocho residuos de D-glucopiranosilo asimétricos con enlaces α-1,4. [176] La estructura molecular de estos derivados de glucosa, que se aproxima a un cono, cubo o toro truncado, genera una superficie exterior hidrófila y una cavidad interior no polar. Las ciclodextrinas pueden interactuar con moléculas de fármacos de tamaño apropiado para producir un complejo de inclusión. [177] El grupo de Smaldone propuso una síntesis sencilla y barata del CD-MOF-1 a partir de productos naturales. Disolvieron azúcar (γ-ciclodextrina) y una sal alcalina (KOH, KCl, benzoato de potasio) en agua embotellada destilada y permitieron que alcohol de grano de 190 grados (Everclear) se vaporizara en la solución durante una semana. La síntesis dio como resultado un motivo repetitivo cúbico (γ-CD) 6 con un tamaño de poro de aproximadamente 1 nm. Posteriormente, en 2017 Hartlieb et al. en Northwestern realizó más investigaciones con CD-MOF-1 que involucran la encapsulación de ibuprofeno. El grupo estudió diferentes métodos para cargar el MOF con ibuprofeno, además de realizar estudios de biodisponibilidad relacionados en el MOF cargado con ibuprofeno. Investigaron dos métodos diferentes para cargar CD-MOF-1 con ibuprofeno; cristalización utilizando la sal potásica de ibuprofeno como fuente de cationes alcalinos para la producción de MOF, y absorción y desprotonación del ácido libre de ibuprofeno en el MOF. A partir de ahí, el grupo realizó estudios in vitro e in vivo para determinar la aplicabilidad de CD-MOF-1 como método de administración viable de ibuprofeno y otros AINE. Los estudios in vitro no mostraron toxicidad ni efecto sobre la viabilidad celular hasta 100 μM. Los estudios in vivo en ratones mostraron la misma rápida absorción de ibuprofeno que la muestra de control de sal potásica de ibuprofeno con una concentración plasmática máxima observada en 20 minutos, y el cocristal tiene el beneficio adicional de duplicar la vida media en muestras de plasma sanguíneo. [178] El aumento en la vida media se debe a que CD-MOF-1 aumenta la solubilidad del ibuprofeno en comparación con la forma de sal pura.
Desde estos avances, muchos grupos han realizado más investigaciones sobre la administración de medicamentos con MOF biocompatibles y solubles en agua que involucran medicamentos comunes de venta libre. [179] En marzo de 2018, Sara Rojas y su equipo publicaron su investigación sobre la incorporación y administración de fármacos con varios MOF biocompatibles distintos de CD-MOF-1 mediante administración cutánea simulada. El grupo estudió la carga y liberación de ibuprofeno (hidrófobo) y aspirina (hidrófilo) en tres MOF biocompatibles (MIL-100(Fe), UiO-66(Zr) y MIL-127(Fe)). En condiciones cutáneas simuladas (medios acuosos a 37 °C), las seis combinaciones diferentes de MOF cargados con fármaco cumplieron "los requisitos para ser utilizados como sistemas de administración tópica de fármacos , como la carga útil liberada entre 1 y 7 días" y la administración de una concentración terapéutica de el medicamento de elección sin causar efectos secundarios no deseados. [180] El grupo descubrió que la absorción del fármaco está "gobernada por el equilibrio hidrófilo/hidrófobo entre la carga y la matriz" y "la accesibilidad del fármaco a través de la estructura". La "liberación controlada en condiciones cutáneas sigue diferentes perfiles cinéticos dependiendo de: (i) la estructura de la estructura, ya sea con una liberación rápida desde la estructura muy abierta MIL-100 o una liberación más lenta del fármaco desde el estrecho sistema de poros 1D de MIL- 127 o (ii) la naturaleza hidrófoba/hidrófila de la carga, con una liberación rápida (aspirina) y lenta (ibuprofeno) de la matriz de UiO-66". Además, se utiliza una técnica simple de molienda de bolas para encapsular eficientemente los medicamentos modelo 5-fluorouracilo, cafeína, ácido paraaminobenzoico y benzocaína. Tanto los estudios computacionales como los experimentales confirman la idoneidad de [Zn 4 O(dmcapz) 3 ] para incorporar altas cargas de las moléculas bioactivas estudiadas. [181]
Investigaciones recientes que involucran a los MOF como método de administración de medicamentos incluyen algo más que la simple encapsulación de medicamentos cotidianos como el ibuprofeno y la aspirina. A principios de 2018, Chen et al. publicaron detallando su trabajo sobre el uso de MOF, ZIF-8 (estructura de imidazolato zeolítico-8) en la investigación antitumoral "para controlar la liberación de un inhibidor de la autofagia, la 3-metiladenina (3-MA), y evitar que se disipe en gran cantidad antes de alcanzar el objetivo". [182] El grupo realizó estudios in vitro y determinó que "las proteínas relacionadas con la autofagia y el flujo de autofagia en células HeLa tratadas con NP 3-MA@ZIF-8 muestran que la formación de autofagosomas está significativamente bloqueada, lo que revela que las células sensibles al pH La disociación aumenta la eficiencia de la inhibición de la autofagia en la concentración equivalente de 3-MA". Esto es prometedor para futuras investigaciones y aplicabilidad de los MOF como métodos de administración de fármacos en la lucha contra el cáncer.
En 2014, los investigadores demostraron que pueden crear películas delgadas eléctricamente conductoras de MOF (Cu 3 (BTC) 2 (también conocido como HKUST-1 ; BTC, ácido benceno-1,3,5-tricarboxílico) infiltradas con la molécula 7,7, 8,8-tetracianoquinododimetano) que podría usarse en aplicaciones que incluyen energía fotovoltaica, sensores y materiales electrónicos y un camino hacia la creación de semiconductores. El equipo demostró una conductividad eléctrica sintonizable y estable al aire con valores de hasta 7 siemens por metro, comparable al bronce. [183]
Ni
3Se demostró que el (2,3,6,7,10,11-hexaiminotrifenileno) 2 es un análogo del grafeno organometálico que tiene una banda prohibida natural , lo que lo convierte en un semiconductor y es capaz de autoensamblarse. Es un ejemplo de estructura metal-orgánica conductora . Representa una familia de compuestos similares. Debido a la simetría y geometría del 2,3,6,7,10,11-hexaiminotrifenileno (HITP), el complejo organometálico general tiene una naturaleza casi fractal que le permite autoorganizarse perfectamente. Por el contrario, el grafeno debe estar dopado para darle las propiedades de un semiconductor. Los gránulos de Ni 3 (HITP) 2 tenían una conductividad de 2 S/cm, un récord para un compuesto organometálico. [184] [185]
En 2018, los investigadores sintetizaron un MOF semiconductor bidimensional (Fe 3 (THT) 2 (NH 4 ) 3 , también conocido como THT, 2,3,6,7,10,11-trifenilenhexatiol) y mostraron una alta movilidad eléctrica a temperatura ambiente. . [186] En 2020, el mismo material se integró en un dispositivo de fotodetección, que detecta un amplio rango de longitudes de onda desde UV hasta NIR (400-1575 nm). [187] Esta fue la primera vez que se demostró el uso de un MOF semiconductor bidimensional en dispositivos optoelectrónicos. [188]
es una estructura MOF 2D y existen ejemplos limitados de materiales que son intrínsecamente conductores, porosos y cristalinos. Los MOF 2D en capas tienen una estructura cristalina porosa que muestra conductividad eléctrica. Estos materiales están construidos a partir de moléculas enlazadoras trigonales (fenileno o trifenileno) y seis grupos funcionales de –OH, - o –SH. Las moléculas enlazadoras trigonales y los iones metálicos coordinados de forma cuadrada y plana, como , , y forman capas con estructuras hexagonales que parecen grafeno a mayor escala. El apilamiento de estas capas puede construir sistemas de poros unidimensionales. Los MOF 2D similares al grafeno han mostrado conductividades decentes. Esto los convierte en una buena opción para probarlos como material de electrodos para la evolución de hidrógeno a partir del agua, reacciones de reducción de oxígeno, supercondensadores y detección de compuestos orgánicos volátiles (COV). Entre estos MOF, ha mostrado la conductividad más baja, pero también la reacción más fuerte en la detección de COV. [189] [190] [191]
Se pueden incorporar biomoléculas durante el proceso de cristalización de MOF. Biomoléculas que incluyen proteínas, ADN y anticuerpos podrían encapsularse dentro de ZIF-8. Las enzimas encapsuladas de esta manera eran estables y activas incluso después de haber sido expuestas a condiciones duras (por ejemplo, disolventes agresivos y altas temperaturas). Para el proceso de mineralización biomimética se utilizaron ZIF-8, MIL-88A, HKUST-1 y varios MOF luminiscentes que contienen metales lantánidos. [192]
Los tamaños de poro pequeños y ajustables del MOF y sus altas fracciones de huecos son prometedores como adsorbente para capturar CO 2 . [193] Los MOF podrían proporcionar una alternativa más eficiente a los métodos tradicionales basados en disolventes de aminas en la captura de CO 2 de las centrales eléctricas alimentadas con carbón. [194]
Los MOF podrían emplearse en cada una de las tres configuraciones principales de captura de carbono para centrales eléctricas alimentadas con carbón: precombustión, poscombustión y oxicombustión. [195] La configuración de poscombustión es la única que se puede adaptar a las plantas existentes, lo que genera el mayor interés e investigación. El gas de combustión se alimentaría a través de un MOF en una configuración de reactor de lecho compacto. Los gases de combustión generalmente están a una temperatura de 40 a 60 °C con una presión parcial de CO 2 de 0,13 – 0,16 bar. El CO 2 puede unirse a la superficie del MOF mediante fisisorción (mediante interacciones de Van der Waals ) o quimisorción (mediante formación de enlaces covalentes ). [196]
Una vez que el MOF está saturado, el CO 2 se extrae del MOF mediante un cambio de temperatura o un cambio de presión. Este proceso se conoce como regeneración. En una regeneración por cambio de temperatura, el MOF se calentaría hasta que se desorba el CO2 . Para lograr capacidades de trabajo comparables a las del proceso de aminas, el MOF debe calentarse a unos 200 °C. En una oscilación de presión, la presión disminuiría hasta que el CO 2 se desorbe. [197]
Otra propiedad relevante de los MOF es su baja capacidad calorífica. Las soluciones de monoetanolamina (MEA), el método de captura líder, tienen una capacidad calorífica de entre 3 y 4 J/(g⋅K), ya que son principalmente agua. Esta alta capacidad calorífica contribuye a la penalización energética en la etapa de regeneración del disolvente, es decir, cuando el CO2 adsorbido se elimina de la solución MEA. MOF-177, un MOF diseñado para la captura de CO 2 , tiene una capacidad calorífica de 0,5 J/(g⋅K) a temperatura ambiente. [195]
Los MOF adsorben el 90% del CO 2 mediante un proceso de cambio de presión al vacío. El MOF Mg(dobdc) tiene una capacidad de carga de CO2 de 21,7% en peso . Aplicado a una planta de energía a gran escala, el costo de la energía aumentaría en un 65%, mientras que un sistema de referencia NETL basado en aminas de EE. UU. causaría un aumento del 81% (la meta es el 35%). El costo de captura sería de $57/tonelada, mientras que para el sistema de aminas el costo se estima en $72/tonelada. A ese ritmo, el capital necesario para implementar dicho proyecto en una central eléctrica de 580 MW sería de 354 millones de dólares. [198]
Un MOF cargado con óxido de propileno puede actuar como catalizador , convirtiendo el CO 2 en carbonatos cíclicos (moléculas en forma de anillo con muchas aplicaciones). También pueden eliminar el carbono del biogás . Este MOF se basa en lantánidos , que proporcionan estabilidad química. Esto es especialmente importante porque los gases a los que estará expuesto el MOF son calientes, tienen mucha humedad y son ácidos. [199] Los POF y Zn/POF a base de triaminoguanidinio son nuevos materiales multifuncionales para la remediación ambiental y aplicaciones biomédicas. [200]
Las membranas MOF pueden imitar una selectividad iónica sustancial. Esto ofrece potencial para su uso en desalinización y tratamiento de agua. En 2018, la ósmosis inversa suministraba más de la mitad de la capacidad mundial de desalinización y la última etapa de la mayoría de los procesos de tratamiento de agua. La ósmosis no utiliza la deshidratación de iones ni el transporte selectivo de iones en canales biológicos y no es energéticamente eficiente. La industria minera utiliza procesos basados en membranas para reducir la contaminación del agua y recuperar metales. Los MOF podrían usarse para extraer metales como el litio del agua de mar y de flujos de desechos. [201]
Las membranas MOF, como las membranas ZIF-8 y UiO-66 con poros subnanómetros uniformes que consisten en ventanas de escala de angstrom y cavidades de escala nanométrica, mostraron un transporte selectivo ultrarrápido de iones de metales alcalinos. Las ventanas actuaron como filtros de selectividad iónica para iones de metales alcalinos, mientras que las cavidades funcionaron como poros para el transporte. Las membranas ZIF-8 [202] y UiO-66 [203] mostraron una selectividad LiCl / RbCl de ~4,6 y ~1,8, respectivamente, mucho mayor que la selectividad de 0,6 a 0,8 en las membranas tradicionales. [204] Un estudio de 2020 sugirió que un nuevo MOF llamado PSP-MIL-53 podría usarse junto con la luz solar para purificar el agua en solo media hora. [205]
También se prevé que los MOF sean medios muy eficaces para separar gases con bajo coste energético mediante el cribado computacional de alto rendimiento de sus propiedades de adsorción [206] o de penetración/difusión de gases [207] . Un ejemplo es NbOFFIVE-1-Ni, también conocido como KAUST-7, que puede separar propano y propileno mediante difusión con una selectividad de casi el 100%. [208] Las propiedades de selectividad molecular específicas proporcionadas por el crecimiento de la estructura organometálica montada en superficie de Cu-BDC (SURMOF-2) sobre una capa de alúmina encima del transistor de efecto de campo de grafeno (GFET) con puerta trasera pueden proporcionar un sensor que solo es sensible al etanol pero no al metanol ni al isopropanol. [209]
Se ha demostrado que los MOF capturan vapor de agua del aire. [210] En 2021, en condiciones húmedas, un prototipo de laboratorio de polímero-MOF produjo 17 litros (4,5 gal) de agua por kg por día sin energía adicional. [211] [212]
Los MOF también podrían usarse para aumentar la eficiencia energética en aplicaciones de refrigeración de espacios a temperatura ambiente. [213] [214]

Al enfriar el aire exterior, una unidad de enfriamiento debe lidiar tanto con el calor sensible como con el calor latente del aire . Las unidades típicas de aire acondicionado por compresión de vapor (VCAC) gestionan el calor latente en el aire a través de aletas de refrigeración mantenidas por debajo de la temperatura del punto de rocío del aire húmedo en la entrada. Estas aletas condensan el agua, deshidratando el aire y reduciendo así sustancialmente el contenido de calor del aire. El uso de energía del enfriador depende en gran medida de la temperatura del serpentín de enfriamiento y mejoraría enormemente si la temperatura de este serpentín pudiera elevarse por encima del punto de rocío . [215] Esto hace que sea deseable manejar la deshumidificación a través de medios distintos de la condensación. Uno de esos medios es adsorber el agua del aire en un desecante que recubre los intercambiadores de calor, utilizando el calor residual extraído de la unidad para desorber el agua del sorbente y así regenerar el desecante para uso repetido. Esto se logra teniendo dos unidades de condensador/evaporador a través de las cuales se puede invertir el flujo de refrigerante una vez que el desecante del condensador está saturado, convirtiendo así al condensador en el evaporador y viceversa. [213]
Las áreas superficiales y porosidades extremadamente altas de los MOF los han convertido en objeto de mucha investigación en aplicaciones de adsorción de agua. [213] [216] [217] [218] La química puede ayudar a ajustar la humedad relativa óptima para la adsorción/desorción y la intensidad de la absorción de agua. [213] [219]
Algunos MOF también exhiben polarización eléctrica espontánea, que se produce debido al ordenamiento de los dipolos eléctricos (enlazadores polares o moléculas invitadas) por debajo de una determinada temperatura de transición de fase. [220] Si este orden dipolar de largo alcance puede ser controlado por el campo eléctrico externo, un MOF se llama ferroeléctrico. [221] Algunos MOF ferroeléctricos también exhiben un orden magnético que los convierte en multiferroicos de fase estructural única. Esta propiedad del material es muy interesante para la construcción de dispositivos de memoria con alta densidad de información. El mecanismo de acoplamiento del multiferroico molecular tipo I [(CH 3 ) 2 NH 2 ][Ni(HCOO) 3 ] es un acoplamiento indirecto mediado por deformación elástica espontánea. [222]