El acetileno ( nombre sistemático : etino ) es el compuesto químico con la fórmula C 2 H 2 y estructura H−C≡C−H . Es un hidrocarburo y el alquino más simple . [7] Este gas incoloro se utiliza ampliamente como combustible y componente químico. Es inestable en su forma pura y, por tanto, normalmente se trata como una solución. [8] El acetileno puro es inodoro, pero los grados comerciales suelen tener un olor marcado debido a impurezas como el sulfuro de divinilo y la fosfina . [8] [9]
Como alquino, el acetileno está insaturado porque sus dos átomos de carbono están unidos entre sí mediante un triple enlace . El triple enlace carbono-carbono coloca los cuatro átomos en la misma línea recta, con ángulos de enlace CCH de 180°. [10]
El acetileno fue descubierto en 1836 por Edmund Davy , quien lo identificó como un "nuevo carburador de hidrógeno". [11] [12] Fue un descubrimiento accidental al intentar aislar el potasio metálico. Calentando carbonato de potasio con carbono a temperaturas muy altas, produjo un residuo de lo que ahora se conoce como carburo de potasio (K 2 C 2 ), que reaccionó con agua para liberar el nuevo gas. Fue redescubierto en 1860 por el químico francés Marcellin Berthelot , quien acuñó el nombre de acétylène . [13] La fórmula empírica de Berthelot para el acetileno (C 4 H 2 ), así como el nombre alternativo " quadricarbure d'hydrogène " (cuadricarburo de hidrógeno), eran incorrectos porque muchos químicos en ese momento usaban la masa atómica incorrecta para el carbono (6 en lugar de 12). [14] Berthelot pudo preparar este gas haciendo pasar vapores de compuestos orgánicos (metanol, etanol, etc.) a través de un tubo al rojo vivo y recogiendo el efluente . También descubrió que el acetileno se formaba provocando chispas de electricidad a través de una mezcla de gases de cianógeno e hidrógeno . Más tarde, Berthelot obtuvo acetileno directamente pasando hidrógeno entre los polos de un arco de carbono . [15] [16]
Excepto en China, la producción de acetileno está dominada por la combustión parcial de gas natural. [17]
Desde la década de 1950, el acetileno se produce principalmente mediante la combustión parcial de metano . [18] [19] [20] Es un subproducto recuperado en la producción de etileno por craqueo de hidrocarburos . En 1983 se produjeron aproximadamente 400.000 toneladas mediante este método. [18] Su presencia en el etileno suele ser indeseable debido a su carácter explosivo y su capacidad para envenenar los catalizadores de Ziegler-Natta . Se hidrogena selectivamente para obtener etileno , normalmente utilizando catalizadores de Pd - Ag . [21]
3 CH 4 + 3 O 2 → C 2 H 2 + CO + 5 H 2 O.
La combustión parcial del metano también produce acetileno:
Los alcanos más pesados del petróleo y el gas natural se descomponen en moléculas más ligeras que se deshidrogenan a alta temperatura:
Esta última reacción se implementa en el proceso de descomposición anaeróbica del metano mediante plasma de microondas. La ventaja de esta tecnología es la ausencia de emisiones de CO2 y la producción conjunta de hidrógeno como producto secundario. [22] Esto lo convierte en una producción con tecnología baja en carbono y también en un proceso electrificado. Por 32 t de metano transformado, producción de 26 t de acetileno y 6 t de hidrógeno (según estequiometría).
La producción de acetileno a partir de carburo de calcio es una ruta tradicional y sigue siendo la dominante:
Las condiciones para la producción de carburo de calcio son ambientalmente inaceptables en la mayoría de los países avanzados, excepto China. [ cita necesaria ]
Hasta la década de 1950, cuando el petróleo sustituyó al carbón como principal fuente de carbono reducido , el acetileno (y la fracción aromática del alquitrán de hulla ) era la principal fuente de productos químicos orgánicos en la industria química. Se preparaba mediante la hidrólisis del carburo de calcio , reacción descubierta por Friedrich Wöhler en 1862 [23] y aún familiar para los estudiantes:
La producción de carburo de calcio requiere altas temperaturas, ~2000 °C, lo que requiere el uso de un horno de arco eléctrico . En Estados Unidos, este proceso fue una parte importante de la revolución química de finales del siglo XIX impulsada por el enorme proyecto de energía hidroeléctrica en las Cataratas del Niágara . [24]
En uso, el carburo reacciona con agua para producir acetileno; 1 kg de carburo se combina con 562,5 g de agua para liberar 350 l de acetileno.
En términos de la teoría del enlace de valencia , en cada átomo de carbono el orbital 2s se hibrida con un orbital 2p formando así un híbrido sp. Los otros dos orbitales 2p permanecen sin hibridar. Los dos extremos de los dos orbitales híbridos sp se superponen para formar un fuerte enlace de valencia σ entre los carbonos, mientras que en cada uno de los otros dos extremos los átomos de hidrógeno se unen también mediante enlaces σ. Los dos orbitales 2p sin cambios forman un par de enlaces π más débiles . [25]
Dado que el acetileno es una molécula simétrica lineal , posee el grupo puntual D ∞h . [26]
A presión atmosférica, el acetileno no puede existir como líquido y no tiene punto de fusión. El punto triple en el diagrama de fases corresponde al punto de fusión (-80,8 °C) a la presión mínima a la que puede existir el acetileno líquido (1,27 atm). A temperaturas por debajo del punto triple, el acetileno sólido puede convertirse directamente en vapor (gas) por sublimación . El punto de sublimación a presión atmosférica es −84,0 °C. [27]
A temperatura ambiente, la solubilidad del acetileno en acetona es de 27,9 g por kg. Para la misma cantidad de dimetilformamida (DMF), la solubilidad es de 51 g. A 20,26 bar, la solubilidad aumenta a 689,0 y 628,0 g para acetona y DMF, respectivamente. Estos disolventes se utilizan en cilindros de gas a presión. [28]
Aproximadamente el 20% del acetileno lo suministra la industria de gases industriales para soldadura y corte con gas oxiacetileno debido a la alta temperatura de la llama. La combustión de acetileno con oxígeno produce una llama de más de 3600 K (3330 °C; 6020 °F), liberando 11,8 kJ /g. El oxígeno con acetileno es la mezcla de gases comunes que arde más caliente. [29] El acetileno es la tercera llama química natural más caliente después de los 5.260 K (4.990 °C; 9.010 °F) del dicianoacetileno y el cianógeno a 4.798 K (4.525 °C; 8.177 °F). La soldadura con oxiacetileno fue un proceso de soldadura popular en décadas anteriores. El desarrollo y las ventajas de los procesos de soldadura por arco han hecho que la soldadura con oxicombustible esté casi extinta para muchas aplicaciones. El uso de acetileno para soldar ha disminuido significativamente. Por otro lado, el equipo de soldadura de oxiacetileno es bastante versátil, no sólo porque se prefiere el soplete para algunos tipos de soldadura de hierro o acero (como en ciertas aplicaciones artísticas), sino también porque se presta fácilmente para soldar , calentamiento de metales (para recocido o templado, doblado o formado), aflojamiento de tuercas y pernos corroídos y otras aplicaciones. Los técnicos de reparación de cables de Bell Canada todavía utilizan kits de sopletes portátiles alimentados con acetileno como herramienta de soldadura para sellar empalmes de manguitos de plomo en bocas de acceso y en algunos lugares aéreos. La soldadura con oxiacetileno también se puede utilizar en áreas donde no se puede acceder fácilmente a la electricidad. El corte con oxiacetileno se utiliza en muchos talleres de fabricación de metales. Para su uso en soldadura y corte, las presiones de trabajo deben ser controladas por un regulador, ya que por encima de 15 psi (100 kPa), si se somete a una onda de choque (provocada, por ejemplo, por un flashback ), el acetileno se descompone explosivamente en hidrógeno y carbono . [30]

El acetileno, a pesar de su sencillez, no se utiliza en muchos procesos industriales.
Una de las principales aplicaciones químicas es la etinilación del formaldehído. [8] El acetileno se suma a los aldehídos y cetonas para formar alcoholes α-etinílicos:
La reacción da butinodiol , con alcohol propargílico como subproducto. Como catalizador se utiliza acetiluro de cobre . [31] [32]
Además de la etinilación, el acetileno reacciona con monóxido de carbono , el acetileno reacciona para dar ácido acrílico o ésteres acrílicos. Se requieren catalizadores metálicos. Estos derivados forman productos como fibras acrílicas , vidrios , pinturas , resinas y polímeros . Excepto en China, el uso de acetileno como materia prima química ha disminuido en un 70% entre 1965 y 2007 debido a consideraciones ambientales y de costos. [33]
Antes del uso generalizado de productos petroquímicos, el acetileno derivado del carbón era un componente básico de varios productos químicos industriales. Así, el acetileno se puede hidratar para dar acetaldehído , que a su vez se puede oxidar a ácido acético. También se comercializaron procesos que conducen a la obtención de acrilatos. Casi todos estos procesos quedaron obsoletos con la disponibilidad de etileno y propileno derivados del petróleo. [34]
En 1881, el químico ruso Mikhail Kucherov [35] describió la hidratación del acetileno a acetaldehído utilizando catalizadores como el bromuro de mercurio (II) . Antes de la llegada del proceso Wacker , esta reacción se llevaba a cabo a escala industrial. [36]
La polimerización de acetileno con catalizadores Ziegler-Natta produce películas de poliacetileno . El poliacetileno, una cadena de centros CH con enlaces simples y dobles alternos, fue uno de los primeros semiconductores orgánicos descubiertos . Su reacción con el yodo produce un material altamente conductor de electricidad. Aunque tales materiales no son útiles, estos descubrimientos condujeron al desarrollo de semiconductores orgánicos , como reconoció el Premio Nobel de Química en 2000 a Alan J. Heeger , Alan G MacDiarmid y Hideki Shirakawa . [8]
En la década de 1920, se utilizó experimentalmente acetileno puro como anestésico por inhalación . [37]
A veces se utiliza acetileno para la carburación (es decir, el endurecimiento) del acero cuando el objeto es demasiado grande para caber en un horno. [38]
El acetileno se utiliza para volatilizar el carbono en la datación por radiocarbono . El material carbonoso de una muestra arqueológica se trata con litio metálico en un pequeño horno de investigación especializado para formar carburo de litio (también conocido como acetiluro de litio). Luego, el carburo se puede hacer reaccionar con agua, como de costumbre, para formar gas acetileno y alimentarlo a un espectrómetro de masas para medir la relación isotópica del carbono-14 al carbono-12. [39]
La combustión de acetileno produce una luz fuerte y brillante y la ubicuidad de las lámparas de carburo impulsó gran parte de la comercialización del acetileno a principios del siglo XX. Las aplicaciones comunes incluían faros costeros , [40] farolas , [41] y faros para automóviles [42] y minería . [43] En la mayoría de estas aplicaciones, la combustión directa supone un riesgo de incendio , por lo que el acetileno ha sido sustituido, primero por iluminación incandescente y muchos años después por LED de bajo consumo y alto lumen. Sin embargo, las lámparas de acetileno siguen teniendo un uso limitado en áreas remotas o inaccesibles y en países con una red eléctrica central débil o poco confiable . [43]
La riqueza energética del triple enlace C≡C y la solubilidad bastante alta del acetileno en agua lo convierten en un sustrato adecuado para las bacterias, siempre que esté disponible una fuente adecuada. [44] Se han identificado varias bacterias que viven en acetileno. La enzima acetileno hidratasa cataliza la hidratación del acetileno para dar acetaldehído : [45]
El acetileno es una sustancia química moderadamente común en el universo, a menudo asociada con las atmósferas de los gigantes gaseosos . [46] Un curioso descubrimiento de acetileno se encuentra en Encelado , una luna de Saturno . Se cree que el acetileno natural se forma a partir de la descomposición catalítica de hidrocarburos de cadena larga a temperaturas de 1700 K (1430 °C; 2600 °F) y superiores. Dado que tales temperaturas son muy poco probables en un cuerpo distante tan pequeño, este descubrimiento sugiere potencialmente reacciones catalíticas dentro de esa luna, lo que la convierte en un sitio prometedor para buscar química prebiótica. [47] [48]
En las reacciones de vinilación , los compuestos H-X se añaden a través del triple enlace. Los alcoholes y fenoles se añaden al acetileno para dar éteres vinílicos . Los tioles dan tioéteres vinílicos. De manera similar, la vinilpirrolidona y el vinilcarbazol se producen industrialmente mediante vinilación de 2-pirrolidona y carbazol . [28] [8]
La hidratación del acetileno es una reacción de vinilación, pero el alcohol vinílico resultante se isomeriza a acetaldehído . La reacción está catalizada por sales de mercurio. Esta reacción alguna vez fue la tecnología dominante para la producción de acetaldehído, pero ha sido desplazada por el proceso Wacker , que produce acetaldehído mediante oxidación de etileno , una materia prima más barata. Una situación similar se aplica a la conversión de acetileno en el valioso cloruro de vinilo mediante hidrocloración frente a la oxicloración de etileno.
Se utiliza acetato de vinilo en lugar de acetileno para algunas vinilaciones, que se describen con mayor precisión como transvinilaciones . [49] Se han utilizado ésteres superiores de acetato de vinilo en la síntesis de formiato de vinilo .
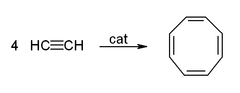
El acetileno y sus derivados (2-butino, difenilacetileno, etc.) forman complejos con metales de transición . Su unión al metal es algo similar a la de los complejos de etileno. Estos complejos son intermedios en muchas reacciones catalíticas, como la trimerización de alquinos a benceno, la tetramerización a ciclooctatetraeno , [8] y la carbonilación a hidroquinona : [50]

También son comunes los acetiluros metálicos , especies de fórmula L n M − C 2 R . El acetiluro de cobre (I) y el acetiluro de plata se pueden formar en soluciones acuosas con facilidad debido a un equilibrio de solubilidad favorable . [51]
El acetileno tiene un p K a de 25, el acetileno puede ser desprotonado por una superbase para formar un acetiluro : [51]
Varios reactivos organometálicos [52] e inorgánicos [53] son eficaces.
El acetileno se puede semihidrogenar a etileno , proporcionando una materia prima para una variedad de plásticos de polietileno . Los halógenos se suman al triple enlace.
El acetileno no es especialmente tóxico, pero cuando se genera a partir de carburo de calcio , puede contener impurezas tóxicas como trazas de fosfina y arsina , que le dan un olor distintivo parecido al del ajo . También es muy inflamable, como lo son la mayoría de los hidrocarburos ligeros, de ahí su uso en soldadura. Su peligro más singular está asociado con su inestabilidad intrínseca, especialmente cuando está presurizado: bajo ciertas condiciones, el acetileno puede reaccionar en una reacción exotérmica de tipo adición para formar una serie de productos, típicamente benceno y/o vinilacetileno , posiblemente además de carbono y hidrógeno . [ cita necesaria ] En consecuencia, el acetileno, si se inicia mediante un calor intenso o una onda de choque, puede descomponerse explosivamente si la presión absoluta del gas supera los 200 kilopascales (29 psi). La mayoría de los reguladores y manómetros de los equipos informan la presión manométrica y, por lo tanto, el límite seguro para el acetileno es 101 kPa manométricos o 15 psig. [54] [55] Por lo tanto, se suministra y almacena disuelto en acetona o dimetilformamida (DMF), [55] [56] [57] contenido en una bombona de gas con un relleno poroso ( Agamassan ), lo que lo hace seguro para su transporte y uso, siempre que se maneje adecuadamente. Los cilindros de acetileno deben usarse en posición vertical para evitar extraer acetona durante el uso. [58]
OSHA, [59] [60] Asociación de Gas Comprimido, [55] Administración de Salud y Seguridad Minera de los Estados Unidos (MSHA), [61] EIGA, [58] y otras agencias proporcionan información sobre el almacenamiento seguro de acetileno en cilindros verticales. .
El cobre cataliza la descomposición del acetileno y, como resultado, el acetileno no debe transportarse en tuberías de cobre. [62]
Los cilindros deben almacenarse en un área separada de oxidantes para evitar una reacción exacerbada en caso de incendio o fuga. [55] [60] Los cilindros de acetileno no deben almacenarse en espacios confinados, vehículos cerrados, garajes y edificios, para evitar fugas involuntarias que conduzcan a una atmósfera explosiva. [55] [60] En los EE. UU., el Código Eléctrico Nacional (NEC) requiere consideración para áreas peligrosas, incluidas aquellas donde se puede liberar acetileno durante accidentes o fugas. [63] La consideración puede incluir la clasificación eléctrica y el uso de componentes eléctricos listados en el Grupo A en EE. UU. [63] Más información sobre cómo determinar las áreas que requieren consideración especial se encuentra en NFPA 497. [64] En Europa, ATEX también requiere consideración para áreas peligrosas donde se pueden liberar gases inflamables durante accidentes o fugas. [58]
El nombre acetileno se conserva para el compuesto HC≡CH. Es el nombre preferido de la IUPAC, pero no se permite sustitución de ningún tipo; sin embargo, en la nomenclatura general se permite la sustitución, por ejemplo fluoroacetileno [fluoroetino (PIN)], pero no por grupos alquilo o cualquier otro grupo que extienda la cadena carbonada, ni por grupos característicos expresados por sufijos.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) Mantenimiento de CS1: otros ( enlace )Para el carbono se utilizaban pesos atómicos de 6 y 12.
{{cite encyclopedia}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )