

Los metabolitos secundarios , también llamados metabolitos especializados o productos secundarios , son un tipo de producto natural (compuestos orgánicos producidos por organismos vivos) generados por formas de vida (por ejemplo, bacterias , arqueas , hongos , plantas o animales ) que no están directamente involucradas en el crecimiento , desarrollo o reproducción normales del organismo. En cambio, generalmente median interacciones ecológicas , que pueden producir una ventaja selectiva para el organismo al aumentar su capacidad de supervivencia o fecundidad . Los metabolitos secundarios específicos a menudo se restringen a un conjunto estrecho de especies dentro de un grupo filogenético . Los metabolitos secundarios a menudo juegan un papel importante en la defensa de las plantas contra la herbivoría y otras defensas interespecies. Los humanos usan metabolitos secundarios como medicamentos, saborizantes, pigmentos y drogas recreativas. [2]
El término metabolito secundario fue acuñado por primera vez por Albrecht Kossel , premio Nobel de medicina y fisiología en 1910. [3] Treinta años más tarde, el botánico polaco Friedrich Czapek describió los metabolitos secundarios como productos finales del metabolismo del nitrógeno . [4]
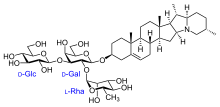
Los metabolitos secundarios comúnmente median interacciones antagónicas, como la competencia y la depredación , así como las mutualistas como la polinización y los mutualismos de recursos . Por lo general, los metabolitos secundarios se limitan a un linaje específico o incluso a una especie, [5] aunque hay evidencia considerable de que la transferencia horizontal a través de especies o géneros de vías completas juega un papel importante en la evolución bacteriana (y, probablemente, fúngica). [6] La investigación también muestra que el metabolismo secundario puede afectar a diferentes especies de diversas maneras. En el mismo bosque, cuatro especies distintas de folívoros marsupiales arbóreos reaccionaron de manera diferente a un metabolito secundario en eucaliptos. [7] Esto muestra que diferentes tipos de metabolitos secundarios pueden ser la división entre dos nichos ecológicos de herbívoros . [7] Además, ciertas especies evolucionan para resistir los metabolitos secundarios e incluso los utilizan para su propio beneficio. Por ejemplo, las mariposas monarca han evolucionado para poder comer algodoncillo ( Asclepias ) a pesar de la presencia de glucósidos cardíacos tóxicos . [8] Las mariposas no sólo son resistentes a las toxinas, sino que además pueden beneficiarse secuestrándolas activamente, lo que puede disuadir a los depredadores. [8]
Las plantas son capaces de producir y sintetizar diversos grupos de compuestos orgánicos y se dividen en dos grupos principales: metabolitos primarios y secundarios. [9] Los metabolitos secundarios son intermediarios metabólicos o productos que no son esenciales para el crecimiento y la vida de las plantas productoras, sino que son necesarios para la interacción de las plantas con su entorno y se producen en respuesta al estrés. Sus propiedades antibióticas, antifúngicas y antivirales protegen a la planta de los patógenos. Algunos metabolitos secundarios como los fenilpropanoides protegen a las plantas del daño de los rayos UV . [10] Los efectos biológicos de los metabolitos secundarios de las plantas en los humanos se conocen desde la antigüedad. La hierba Artemisia annua que contiene artemisinina , ha sido ampliamente utilizada en la medicina tradicional china hace más de dos mil años. [ cita requerida ] Los metabolitos secundarios de las plantas se clasifican por su estructura química y se pueden dividir en cuatro clases principales: terpenos , fenilpropanoides (es decir, fenólicos ), policétidos y alcaloides . [11]



Los terpenos constituyen una gran clase de productos naturales que se componen deunidades de isopreno . Los terpenos son solo hidrocarburos y los terpenoides son hidrocarburos oxigenados. La fórmula molecular general de los terpenos son múltiplos de (C 5 H 8 ) n, donde 'n' es el número de unidades de isopreno enlazadas. Por lo tanto, los terpenos también se denominan compuestos isoprenoides. La clasificación se basa en el número de unidades de isopreno presentes en su estructura. Algunos terpenoides (es decir, muchos esteroles ) son metabolitos primarios. Algunos terpenoides que pueden haberse originado como metabolitos secundarios se han reclutado posteriormente como hormonas vegetales, como las giberelinas , los brasinoesteroides y las estrigolactonas .
Ejemplos de terpenoides construidos a partir de la oligomerización de hemitepeno son:
Los fenólicos son compuestos químicos que se caracterizan por la presencia de una estructura de anillo aromático que lleva uno o más grupos hidroxilo . Los fenólicos son los metabolitos secundarios más abundantes de las plantas y van desde moléculas simples como el ácido fenólico hasta sustancias altamente polimerizadas como los taninos . Las clases de fenólicos se han caracterizado sobre la base de su esqueleto básico.
Un ejemplo de fenol vegetal es:
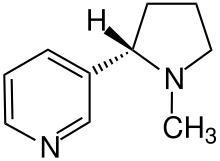
Los alcaloides son un grupo diverso de compuestos básicos que contienen nitrógeno. Por lo general, se derivan de fuentes vegetales y contienen uno o más átomos de nitrógeno. Químicamente son muy heterogéneos. Según sus estructuras químicas, se pueden clasificar en dos grandes categorías:
Ejemplos de alcaloides producidos por las plantas son:
Muchos alcaloides afectan el sistema nervioso central de los animales al unirse a los receptores de neurotransmisores .

Los glucosinolatos son metabolitos secundarios que incluyen átomos de azufre y nitrógeno , y se derivan de la glucosa , un aminoácido y el sulfato .
Un ejemplo de glucosinolato en plantas es la glucorafanina , del brócoli ( Brassica oleracea var. italica ).
Muchos medicamentos utilizados en la medicina moderna se derivan de metabolitos secundarios de plantas.

Los dos terpenoides más conocidos son la artemisinina y el paclitaxel . La artemisinina se utilizó ampliamente en la medicina tradicional china y luego fue redescubierta como un poderoso antipalúdico por la científica china Tu Youyou . Más tarde recibió el Premio Nobel por el descubrimiento en 2015. Actualmente, el parásito de la malaria , Plasmodium falciparum , se ha vuelto resistente a la artemisinina sola y la Organización Mundial de la Salud recomienda su uso con otros medicamentos antipalúdicos para una terapia exitosa. El paclitaxel, el compuesto activo que se encuentra en Taxol, es un medicamento de quimioterapia que se usa para tratar muchas formas de cáncer, incluido el cáncer de ovario , el cáncer de mama , el cáncer de pulmón , el sarcoma de Kaposi , el cáncer de cuello uterino y el cáncer de páncreas . [14] Taxol se aisló por primera vez en 1973 de las cortezas de un árbol conífero, el tejo del Pacífico . [15]
La morfina y la codeína pertenecen a la clase de alcaloides y se derivan de las amapolas del opio . La morfina fue descubierta en 1804 por un farmacéutico alemán Friedrich Sertürner t. Fue el primer alcaloide activo extraído de la adormidera . Es principalmente conocida por sus fuertes efectos analgésicos , sin embargo, la morfina también se usa para tratar la falta de aliento y el tratamiento de la adicción a opiáceos más fuertes como la heroína . [16] [17] A pesar de sus efectos positivos en los humanos, la morfina tiene efectos adversos muy fuertes, como adicción, desequilibrio hormonal o estreñimiento. [17] [18] Debido a su naturaleza altamente adictiva, la morfina es una sustancia estrictamente controlada en todo el mundo, utilizada solo en casos muy graves y algunos países la subutilizan en comparación con el promedio mundial debido al estigma social que la rodea. [19]

La codeína, también un alcaloide derivado de la adormidera, se considera la droga más utilizada en el mundo según la Organización Mundial de la Salud . Fue aislada por primera vez en 1832 por un químico francés Pierre Jean Robiquet , también conocido por el descubrimiento de la cafeína y un colorante rojo ampliamente utilizado, la alizarina . [21] La codeína se utiliza principalmente para tratar el dolor leve y aliviar la tos [22] aunque en algunos casos se utiliza para tratar la diarrea y algunas formas del síndrome del intestino irritable . [22] La codeína tiene una fuerza de 0,1-0,15 en comparación con la morfina ingerida por vía oral, [23] por lo que es mucho más seguro de usar. Aunque la codeína se puede extraer de la adormidera, el proceso no es viable económicamente debido a la baja abundancia de codeína pura en la planta. Un proceso químico de metilación de la morfina mucho más abundante es el principal método de producción. [24]
La atropina es un alcaloide que se encontró por primera vez en Atropa belladonna , un miembro de la familia de las solanáceas . Si bien la atropina se aisló por primera vez en el siglo XIX, su uso médico se remonta al menos al siglo IV a. C., donde se usaba para heridas, gota e insomnio. Actualmente, la atropina se administra por vía intravenosa para tratar la bradicardia y como antídoto para la intoxicación por organofosforados . La sobredosis de atropina puede provocar una intoxicación por atropina que produce efectos secundarios como visión borrosa , náuseas , falta de sudoración, sequedad de boca y taquicardia . [25]
El resveratrol es un compuesto fenólico de la clase de los flavonoides. Es muy abundante en uvas , arándanos , frambuesas y cacahuetes . Se toma comúnmente como suplemento dietético para prolongar la vida y reducir el riesgo de cáncer y enfermedades cardíacas, sin embargo, no hay evidencia sólida que respalde su eficacia. [26] [27] Sin embargo, en general se cree que los flavonoides tienen efectos beneficiosos para los humanos. [ cita requerida ] Ciertos estudios han demostrado que los flavonoides tienen actividad antibiótica directa. [28] Una serie de estudios in vitro y limitados in vivo han demostrado que los flavonoides como la quercetina tienen actividad sinérgica con los antibióticos y son capaces de suprimir las cargas bacterianas. [29]
La digoxina es un glucósido cardíaco derivado por primera vez por William Withering en 1785 de la planta dedalera (Digitalis) . Se utiliza típicamente para tratar afecciones cardíacas como fibrilación auricular , aleteo auricular o insuficiencia cardíaca . [30] Sin embargo, la digoxina puede tener efectos secundarios como náuseas , bradicardia , diarrea o incluso arritmia potencialmente mortal .
Las tres clases principales de metabolitos secundarios fúngicos son: policétidos , péptidos no ribosómicos y terpenos . Aunque los metabolitos secundarios fúngicos no son necesarios para el crecimiento, desempeñan un papel esencial en la supervivencia de los hongos en su nicho ecológico. [31] El metabolito secundario fúngico más conocido es la penicilina descubierta por Alexander Fleming en 1928. Más tarde, en 1945, Fleming, junto con Ernst Chain y Howard Florey , recibió un Premio Nobel por su descubrimiento, que fue fundamental para reducir el número de muertes en la Segunda Guerra Mundial en más de 100.000. [32]
Ejemplos de otros metabolitos secundarios fúngicos son:
La lovastatina fue el primer metabolito secundario aprobado por la FDA para reducir los niveles de colesterol. La lovastatina se encuentra de forma natural en bajas concentraciones en los hongos ostra , [33] el arroz de levadura roja , [34] y el Pu-erh . [35] El modo de acción de la lovastatina es la inhibición competitiva de la HMG-CoA reductasa , una enzima limitante de la velocidad responsable de convertir la HMG-CoA en mevalonato .
Los metabolitos secundarios de los hongos también pueden ser peligrosos para los humanos. Claviceps purpurea , un miembro del grupo de hongos del cornezuelo que crece típicamente en el centeno, provoca la muerte cuando se ingiere. La acumulación de alcaloides venenosos que se encuentran en C. purpurea provoca síntomas como convulsiones y espasmos , diarrea , parestesias , picazón , psicosis o gangrena . Actualmente, la eliminación de los cuerpos del cornezuelo requiere poner el centeno en una solución de salmuera con los granos sanos hundiéndose y los infectados flotando. [36]
La producción bacteriana de metabolitos secundarios comienza en la fase estacionaria como consecuencia de la falta de nutrientes o en respuesta al estrés ambiental. La síntesis de metabolitos secundarios en bacterias no es esencial para su crecimiento, sin embargo, les permiten interactuar mejor con su nicho ecológico. Las principales vías sintéticas de producción de metabolitos secundarios en bacterias son; b-lactama, oligosacárido, shikimato, policétido y vías no ribosómicas. [37] Muchos metabolitos secundarios bacterianos son tóxicos para los mamíferos . Cuando se secretan, esos compuestos venenosos se conocen como exotoxinas, mientras que los que se encuentran en la pared celular procariota son endotoxinas .
Ejemplos de metabolitos secundarios bacterianos son:
Las arqueas son capaces de producir una variedad de metabolitos secundarios, que pueden tener importantes aplicaciones biotecnológicas. [41] A pesar de saber esto, las vías biosintéticas de los metabolitos secundarios en las arqueas son menos conocidas que las de las bacterias. Cabe destacar que las arqueas a menudo carecen de algunos genes de biosíntesis comúnmente presentes en las bacterias, lo que sugiere que pueden poseer vías metabólicas únicas para sintetizar estos compuestos. [41]
Las sustancias poliméricas extracelulares pueden adsorber y degradar eficazmente sustancias químicas orgánicas peligrosas. Si bien estos compuestos son producidos por diversos organismos, las arqueas son particularmente prometedoras para el tratamiento de aguas residuales debido a su alta tolerancia a las concentraciones salinas y su capacidad de crecer anaeróbicamente. [42]
Las arqueocinas son péptidos antibióticos que se pueden dividir principalmente en dos clases: halocinas y sulfolobicinas [41] .
Las dicetopiperazinas son dipéptidos cíclicos con potencial para fines médicos e industriales [41] .

La cría selectiva se utilizó como una de las primeras técnicas biotecnológicas utilizadas para reducir los metabolitos secundarios no deseados en los alimentos, como la naringina que causa amargura en el pomelo. [43] En algunos casos, el resultado deseado es aumentar el contenido de metabolitos secundarios en una planta. Tradicionalmente, esto se hacía utilizando técnicas de cultivo de tejidos vegetales in vitro que permiten: controlar las condiciones de crecimiento, mitigar la estacionalidad de las plantas o protegerlas de parásitos y microbios dañinos. [ cita requerida ] La síntesis de metabolitos secundarios se puede mejorar aún más introduciendo elicitores en un cultivo de tejidos vegetales, como ácido jasmónico , UV-B u ozono . Estos compuestos inducen estrés en una planta, lo que conduce a una mayor producción de metabolitos secundarios.
Para aumentar aún más el rendimiento de los SM, se han desarrollado nuevos enfoques. Un enfoque novedoso utilizado por Evolva utiliza cepas de levadura recombinante S. cerevisiae para producir metabolitos secundarios que normalmente se encuentran en las plantas. El primer compuesto químico sintetizado con éxito con Evolva fue la vainillina, ampliamente utilizada en la industria de bebidas alimentarias como aromatizante. El proceso implica la inserción del gen del metabolito secundario deseado en un cromosoma artificial en la levadura recombinante, lo que conduce a la síntesis de vainillina. Actualmente, Evolva produce una amplia gama de productos químicos como la stevia , el resveratrol o la nootkatona .
Con el desarrollo de las tecnologías recombinantes, en 2010 se firmó el Protocolo de Nagoya sobre acceso a los recursos genéticos y participación justa y equitativa en los beneficios que se deriven de su utilización, del Convenio sobre la Diversidad Biológica. El protocolo regula la conservación y protección de los recursos genéticos para impedir la explotación por parte de países más pequeños y pobres. Si los recursos genéticos, proteínicos o de moléculas pequeñas procedentes de países con biodiversidad se vuelven rentables, se establece un sistema de compensación para los países de origen. [44]