Un compuesto cíclico (o compuesto de anillo ) es un término para un compuesto en el campo de la química en el que una o más series de átomos del compuesto están conectados para formar un anillo . Los anillos pueden variar en tamaño de tres a muchos átomos e incluyen ejemplos en los que todos los átomos son de carbono (es decir, son carbociclos ), ninguno de los átomos es de carbono (compuestos cíclicos inorgánicos), o donde están presentes átomos de carbono y no carbono. ( compuestos heterocíclicos con anillos que contienen carbono y no carbono). Dependiendo del tamaño del anillo, el orden de los enlaces individuales entre los átomos del anillo y su disposición dentro de los anillos, los compuestos carbocíclicos y heterocíclicos pueden ser aromáticos o no aromáticos; en el último caso, pueden variar desde estar completamente saturados hasta tener un número variable de enlaces múltiples entre los átomos del anillo. Debido a la tremenda diversidad que permiten, en combinación, las valencias de los átomos comunes y su capacidad para formar anillos, el número de estructuras cíclicas posibles, incluso las de tamaño pequeño (p. ej., < 17 átomos en total) asciende a muchos miles de millones.
Además de su complejidad y número, el cierre de átomos en anillos puede bloquear átomos particulares con distintas sustituciones (por grupos funcionales ), de modo que se produzcan estereoquímica y quiralidad del compuesto, incluidas algunas manifestaciones que son exclusivas de los anillos (p. ej., isómeros configuracionales ). Además, dependiendo del tamaño del anillo, las formas tridimensionales de estructuras cíclicas particulares (típicamente anillos de cinco átomos o más) pueden variar e interconvertirse de manera que se muestre isomería conformacional . De hecho, el desarrollo de este importante concepto químico surgió históricamente en referencia a compuestos cíclicos. Finalmente, los compuestos cíclicos, debido a las formas, reactividades, propiedades y bioactividades únicas que engendran, son la mayoría de todas las moléculas involucradas en la bioquímica, estructura y función de los organismos vivos y en las moléculas artificiales como las drogas, pesticidas, etc
Un compuesto cíclico o compuesto de anillo es un compuesto en el que al menos algunos de sus átomos están conectados para formar un anillo. [1] Los anillos varían en tamaño desde tres hasta muchas decenas o incluso cientos de átomos. Los ejemplos de compuestos de anillo incluyen fácilmente casos en los que:
Los átomos comunes pueden (como resultado de sus valencias ) formar un número variable de enlaces, y muchos átomos comunes forman fácilmente anillos. Además, dependiendo del tamaño del anillo, el orden de los enlaces individuales entre los átomos del anillo y su disposición dentro de los anillos, los compuestos cíclicos pueden ser aromáticos o no aromáticos; en el caso de compuestos cíclicos no aromáticos, pueden variar desde estar completamente saturados hasta tener un número variable de enlaces múltiples. Como consecuencia de la variabilidad constitucional que es termodinámicamente posible en las estructuras cíclicas, el número de estructuras cíclicas posibles, incluso de tamaño pequeño (por ejemplo, <17 átomos) asciende a muchos miles de millones. [3]
Además, el cierre de átomos en anillos puede bloquear un grupo funcional particular : átomos sustituidos en su lugar, lo que da como resultado que la estereoquímica y la quiralidad se asocien con el compuesto, incluidas algunas manifestaciones que son exclusivas de los anillos (p. ej., isómeros configuracionales ); [4] Además, dependiendo del tamaño del anillo, las formas tridimensionales de estructuras cíclicas particulares (generalmente anillos de cinco átomos o más) pueden variar e interconvertirse de manera que se muestre isomería conformacional . [4]
La gran mayoría de los compuestos cíclicos son orgánicos , y de ellos, una porción significativa y conceptualmente importante están compuestas por anillos formados únicamente por átomos de carbono (es decir, son carbociclos). [ cita necesaria ]
Los átomos inorgánicos también forman compuestos cíclicos. Los ejemplos incluyen azufre y nitrógeno (p. ej., heptasulfurimida S 7 NH , tricloruro de tritiazilo (NSCl) 3 , tetranitruro de tetraazufre S 4 N 4 ), silicio (p. ej., ciclopentasilano (SiH 2 ) 5 ), fósforo y nitrógeno (p. ej., hexaclorofosfaceno (NPCl 2 ) 3 ), fósforo y oxígeno (p. ej., metafosfatos (PO −3) 3 y otros derivados del ácido fosfórico cíclico), boro y oxígeno (por ejemplo, metaborato de sodio Na 3 (BO 2 ) 3 , bórax ), boro y nitrógeno (por ejemplo, borazina (BN) 3 H 6 ). [ cita necesaria ] Cuando el carbono en el benceno se "reemplaza" por otros elementos, por ejemplo, como en borabenceno , silabenceno , germanabenceno , estannabenceno y fosforina , la aromaticidad se conserva, por lo que los compuestos cíclicos inorgánicos aromáticos también se conocen y están bien caracterizados. [ cita necesaria ]
Un compuesto heterocíclico es un compuesto cíclico que tiene átomos de al menos dos elementos diferentes como miembros de su(s) anillo(s). [5] Los compuestos cíclicos que tienen átomos de carbono y no carbono presentes son compuestos de carbono heterocíclicos , y el nombre se refiere también a compuestos cíclicos inorgánicos (por ejemplo, siloxanos , que contienen solo silicio y oxígeno en los anillos, y borazinas , que contienen sólo boro y nitrógeno en los anillos). [5] La IUPAC recomienda la nomenclatura Hantzsch-Widman para nombrar heterociclos, pero muchos nombres comunes siguen utilizándose habitualmente. [ cita necesaria ]

El término macrociclo se utiliza para compuestos que tienen anillos de 8 o más átomos. [6] [7] Los macrociclos pueden ser completamente carbocíclicos (anillos que contienen sólo átomos de carbono, por ejemplo, ciclooctano ), heterocíclicos que contienen átomos de carbono y no carbono (por ejemplo, lactonas y lactamas que contienen anillos de 8 o más átomos), o sin carbono ( que contienen sólo átomos distintos de carbono en los anillos, por ejemplo, hexasulfuro de diselenio ). Los heterociclos con carbono en los anillos pueden tener átomos distintos de carbono limitados en sus anillos (p. ej., en lactonas y lactamas cuyos anillos son ricos en carbono pero tienen un número limitado de átomos distintos de carbono), o ser ricos en átomos distintos de carbono y presentar simetría significativa (por ejemplo, en el caso de macrociclos quelantes). Los macrociclos pueden acceder a una serie de conformaciones estables , con preferencia para residir en conformaciones que minimicen las interacciones transanulares no enlazadas dentro del anillo (por ejemplo, siendo la conformación silla y silla-bote más estable que la conformación barco-barco para el ciclooctano , debido a las interacciones representadas por los arcos mostrados). [ cita necesaria ] Los anillos medianos (8-11 átomos) son los más tensos, con entre 9 y 13 (kcal/mol) de energía de deformación, y el análisis de factores importantes en las conformaciones de macrociclos más grandes se puede modelar utilizando conformaciones de anillos medianos. [8] El análisis conformacional de anillos de miembros impares sugiere que tienden a residir en formas menos simétricas con diferencias de energía más pequeñas entre conformaciones estables. [9]

La nomenclatura de la IUPAC tiene reglas extensas para cubrir la denominación de estructuras cíclicas, tanto como estructuras centrales como como sustituyentes añadidos a estructuras alicíclicas . [ cita necesaria ] El término macrociclo se usa cuando un compuesto que contiene un anillo tiene un anillo de 12 o más átomos. [6] [7] El término policíclico se utiliza cuando aparece más de un anillo en una sola molécula. La naftaleno es formalmente un compuesto policíclico, pero más específicamente se denomina compuesto bicíclico. En la galería final a continuación se ofrecen varios ejemplos de estructuras macrocíclicas y policíclicas.
Los átomos que forman parte de la estructura del anillo se llaman átomos anulares. [10]
El cierre de átomos en anillos puede bloquear átomos particulares con distintas sustituciones por grupos funcionales, de modo que el resultado sea la estereoquímica y la quiralidad del compuesto, incluidas algunas manifestaciones que son exclusivas de los anillos (p. ej., isómeros configuracionales ). [4]
Dependiendo del tamaño del anillo, las formas tridimensionales de estructuras cíclicas particulares (típicamente anillos de 5 átomos y más) pueden variar e interconvertirse de modo que se muestre isomería conformacional . [4] De hecho, el desarrollo de este importante concepto químico surgió, históricamente, en referencia a los compuestos cíclicos. Por ejemplo, los ciclohexanos ( carbociclos de seis miembros sin dobles enlaces, a los que se pueden unir varios sustituyentes, ver imagen) muestran un equilibrio entre dos conformaciones, la silla y el barco, como se muestra en la imagen.
La conformación en silla es la configuración preferida, porque en esta conformación se minimizan la deformación estérica , la deformación eclipsante y la deformación angular que de otro modo serían posibles. [4] Cuál de las posibles conformaciones de silla predomina en los ciclohexanos que llevan uno o más sustituyentes depende de los sustituyentes y de dónde se encuentran en el anillo; en general, los sustituyentes "voluminosos", aquellos grupos con grandes volúmenes o grupos que de otro modo son repulsivos en sus interacciones [ cita necesaria ] , prefieren ocupar una ubicación ecuatorial. [4] Un ejemplo de interacciones dentro de una molécula que conducirían a una tensión estérica , lo que provocaría un cambio en el equilibrio del barco a la silla, es la interacción entre los dos grupos metilo en cis -1,4-dimetilciclohexano. En esta molécula, los dos grupos metilo están en posiciones opuestas del anillo (1,4-), y su estereoquímica cis proyecta a ambos grupos hacia el mismo lado del anillo. Por lo tanto, si se los fuerza a adoptar la forma de barco de mayor energía, estos grupos metilo están en contacto estérico, se repelen entre sí e impulsan el equilibrio hacia la conformación de silla. [4]
Los compuestos cíclicos pueden presentar o no aromaticidad ; el benceno es un ejemplo de compuesto cíclico aromático, mientras que el ciclohexano no es aromático. En química orgánica, el término aromaticidad se utiliza para describir una molécula plana (plana) cíclica (en forma de anillo) que exhibe una estabilidad inusual en comparación con otras disposiciones geométricas o conectivas del mismo conjunto de átomos. Debido a su estabilidad, es muy difícil provocar que las moléculas aromáticas se rompan y reaccionen con otras sustancias. Los compuestos orgánicos que no son aromáticos se clasifican como compuestos alifáticos; pueden ser cíclicos, pero sólo los anillos aromáticos tienen una estabilidad especial (baja reactividad).
Dado que uno de los sistemas de compuestos aromáticos más comunes en la química orgánica se basa en derivados del compuesto aromático prototípico benceno (un hidrocarburo aromático común en el petróleo y sus destilados), la palabra "aromático" se utiliza ocasionalmente para referirse informalmente a los derivados del benceno. , y así es como se definió por primera vez. Sin embargo, existen muchos compuestos aromáticos distintos del benceno. En los organismos vivos, por ejemplo, los anillos aromáticos más comunes son las bases de doble anillo en el ARN y el ADN. Un grupo funcional u otro sustituyente que es aromático se llama grupo arilo.
El primer uso del término "aromático" fue en un artículo de August Wilhelm Hofmann en 1855. Hofmann usó el término para una clase de compuestos de benceno, muchos de los cuales tienen olores (aromas), a diferencia de los hidrocarburos saturados puros. Hoy en día, no existe una relación general entre la aromaticidad como propiedad química y las propiedades olfativas de dichos compuestos (cómo huelen), aunque en 1855, antes de que se comprendiera la estructura del benceno o de los compuestos orgánicos, químicos como Hofmann comenzaban a comprender que los odoríferos. Las moléculas de las plantas, como los terpenos, tenían propiedades químicas que hoy reconocemos que son similares a los hidrocarburos de petróleo insaturados como el benceno.
En términos de la naturaleza electrónica de la molécula, la aromaticidad describe un sistema conjugado a menudo formado por enlaces simples y dobles alternos en un anillo. Esta configuración permite que los electrones del sistema pi de la molécula se deslocalicen alrededor del anillo, aumentando la estabilidad de la molécula. La molécula no puede representarse mediante una estructura, sino más bien como un híbrido resonante de diferentes estructuras, como ocurre con las dos estructuras resonantes del benceno. Estas moléculas no se pueden encontrar en ninguna de estas representaciones, con los enlaces simples más largos en un lugar y el doble enlace más corto en otro (consulte la teoría a continuación). Más bien, la molécula exhibe longitudes de enlace entre las de los enlaces simples y dobles. Este modelo comúnmente visto de anillos aromáticos, es decir, la idea de que el benceno se formó a partir de un anillo de carbono de seis miembros con enlaces simples y dobles alternos (ciclohexatrieno), fue desarrollado por August Kekulé (consulte la sección Historia a continuación). El modelo del benceno consta de dos formas de resonancia, que corresponden a enlaces dobles y simples que se superponen para producir seis enlaces de uno y medio. El benceno es una molécula más estable de lo que se esperaría sin tener en cuenta la deslocalización de carga. [ cita necesaria ]
Debido a las formas, reactividades, propiedades y bioactividades únicas que engendran, los compuestos cíclicos son la mayoría de todas las moléculas involucradas en la bioquímica, estructura y función de los organismos vivos y en las moléculas artificiales (p. ej., medicamentos, herbicidas, etc.) mediante los cuales el hombre intenta ejercer control sobre la naturaleza y los sistemas biológicos.
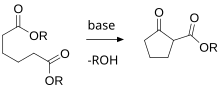
Existe una variedad de reacciones especializadas cuyo uso es únicamente la formación de anillos, y se analizarán a continuación. Además de éstas, existe una amplia variedad de reacciones orgánicas generales que históricamente han sido cruciales en el desarrollo, primero, de la comprensión de los conceptos de la química de anillos y, segundo, de procedimientos confiables para preparar estructuras de anillos con alto rendimiento y con condiciones definidas. orientación de los sustituyentes del anillo (es decir, estereoquímica definida ). Estas reacciones generales incluyen:
En química orgánica, una variedad de productos sintéticos son particularmente útiles para cerrar anillos carbocíclicos y otros; éstas se denominan reacciones de cierre de anillo . Ejemplos incluyen:
Una variedad de procedimientos sintéticos adicionales son particularmente útiles para abrir anillos carbocíclicos y otros, que generalmente contienen un doble enlace u otro grupo funcional "asa" para facilitar la química; éstas se denominan reacciones de apertura de anillo . Ejemplos incluyen:
Las reacciones de expansión y contracción del anillo son comunes en la síntesis orgánica y se encuentran con frecuencia en reacciones pericíclicas . Las expansiones y contracciones de los anillos pueden implicar la inserción de un grupo funcional, como en el caso de la oxidación de Baeyer-Villiger de cetonas cíclicas, los reordenamientos de carbociclos cíclicos como se observa en las reacciones intramoleculares de Diels-Alder , o el colapso o reordenamiento de compuestos bicíclicos , como varios ejemplos.
Los siguientes son ejemplos de carbociclos simples y aromáticos, compuestos cíclicos inorgánicos y heterociclos:
Los siguientes son ejemplos de compuestos cíclicos que exhiben sistemas de anillos y características estereoquímicas más complejos: