
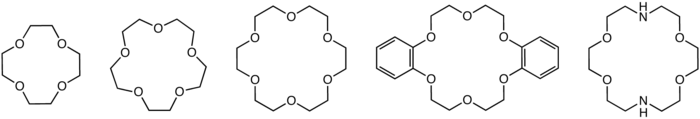
En química orgánica , los éteres corona son compuestos químicos cíclicos que constan de un anillo que contiene varios grupos éter ( R−O−R' ). Los éteres corona más comunes son oligómeros cíclicos de óxido de etileno , siendo la unidad repetitiva etilenoxi , es decir, −CH2CH2O− . Los miembros importantes de esta serie son el tetrámero ( n = 4), el pentámero ( n = 5) y el hexámero ( n = 6). El término "corona" se refiere a la semejanza entre la estructura de un éter de corona unido a un catión y una corona colocada sobre la cabeza de una persona. El primer número en el nombre de un éter corona se refiere a la cantidad de átomos en el ciclo, y el segundo número se refiere a la cantidad de esos átomos que son oxígeno . Los éteres corona son mucho más amplios que los oligómeros de óxido de etileno; un grupo importante se deriva del catecol .
Los éteres corona se unen fuertemente a ciertos cationes, formando complejos . Los átomos de oxígeno están bien situados para coordinarse con un catión ubicado en el interior del anillo, mientras que el exterior del anillo es hidrofóbico. Los cationes resultantes a menudo forman sales que son solubles en disolventes no polares y, por esta razón, los éteres corona son útiles en la catálisis de transferencia de fase . La denticidad del poliéter influye en la afinidad del éter corona por diversos cationes. Por ejemplo, 18-corona-6 tiene alta afinidad por el catión potasio, 15-corona-5 por el catión sodio y 12-corona-4 por el catión litio. La alta afinidad del 18-crown-6 por los iones de potasio contribuye a su toxicidad. El éter corona más pequeño que todavía es capaz de unir cationes es el 8-corona-4, [1] y el éter corona más grande confirmado experimentalmente es el 81-corona-27. [2] Los éteres corona no son los únicos ligandos macrocíclicos que tienen afinidad por el catión potasio. Los ionóforos como la valinomicina también muestran una marcada preferencia por el catión potasio sobre otros cationes.
Se ha demostrado que los éteres de corona se coordinan con los ácidos de Lewis a través de interacciones electrostáticas de orificio σ (ver enlace halógeno ), entre los átomos de oxígeno básicos de Lewis del éter de corona y el centro electrófilo del ácido de Lewis. [3] [4]
En 1967, Charles Pedersen , químico que trabajaba en DuPont , descubrió un método sencillo para sintetizar un éter corona cuando intentaba preparar un agente complejante para cationes divalentes. [5] [6] Su estrategia implicaba unir dos grupos catecolato a través de un hidroxilo en cada molécula. Esta unión define un ligando polidentado que podría envolver parcialmente el catión y, mediante ionización de los hidroxilos fenólicos, neutralizar el catión unido. Se sorprendió al aislar un subproducto que formaba fuertes complejos con cationes de potasio . Citando trabajos anteriores sobre la disolución de potasio en 16-corona-4, [7] [8] se dio cuenta de que los poliéteres cíclicos representaban una nueva clase de agentes complejantes que eran capaces de unirse a cationes de metales alcalinos . Procedió a informar sobre estudios sistemáticos de la síntesis y las propiedades vinculantes de los éteres corona en una serie de artículos fundamentales. Los campos de la síntesis orgánica , los catalizadores de transferencia de fase y otras disciplinas emergentes se beneficiaron del descubrimiento de los éteres corona. Pedersen popularizó especialmente los éteres corona dibenzo. [9]

Pedersen compartió el Premio Nobel de Química de 1987 por el descubrimiento de las rutas sintéticas y las propiedades de unión de los éteres corona.
Debido al efecto quelato y al efecto macrocíclico , los éteres corona muestran afinidades más fuertes por diversos cationes que sus análogos divididos o acíclicos . Por lo tanto, la selectividad catiónica para los iones de metales alcalinos depende principalmente del tamaño y la densidad de carga del ion y del tamaño de la cavidad del éter corona. [11]
Las afinidades de un éter corona determinado hacia los cationes de litio , sodio y potasio pueden cambiar en múltiples magnitudes, lo que se atribuye a las grandes diferencias en su densidad de carga. Entre los cationes de potasio, rubidio y cesio los cambios en las afinidades son menos notables, ya que su densidad de carga varía menos que la de los metales alcalinos en períodos anteriores. [11]
Además de su alta afinidad por los cationes de potasio, 18-crown-6 también puede unirse a aminas protonadas y formar complejos muy estables tanto en solución como en fase gaseosa. Algunos aminoácidos , como la lisina , contienen una amina primaria en sus cadenas laterales. Esos grupos amino protonados pueden unirse a la cavidad de 18-corona-6 y formar complejos estables en la fase gaseosa. Los enlaces de hidrógeno se forman entre los tres átomos de hidrógeno de las aminas protonadas y los tres átomos de oxígeno de la 18-corona-6. Estos enlaces de hidrógeno convierten al complejo en un aducto estable. Al incorporar sustituyentes luminiscentes en su estructura principal, estos compuestos han demostrado ser sondas de iones sensibles, ya que se pueden medir cambios en la absorción o fluorescencia de los grupos fotoactivos para concentraciones muy bajas de metal presente. [15] Algunos ejemplos atractivos incluyen macrociclos, que incorporan donantes de oxígeno y/o nitrógeno, que están unidos a especies poliaromáticas como antracenos (a través de las posiciones 9 y/o 10) [16] o naftalenos (a través de las posiciones 2 y 3). [17] Algunas modificaciones de los ionóforos de tinte mediante éteres corona exhiben coeficientes de extinción que dependen de la longitud de las cadenas de los cationes encadenados. [18]