Los metales alcalinos se componen de los elementos químicos litio (Li), sodio (Na), potasio (K), [nota 1] rubidio (Rb), cesio (Cs), [nota 2] y francio (Fr). Junto con el hidrógeno constituyen el grupo 1 , [nota 3] que se encuentra en el bloque s de la tabla periódica . Todos los metales alcalinos tienen su electrón más externo en un orbital s : esta configuración electrónica compartida da como resultado que tengan propiedades características muy similares. [nota 4] De hecho, los metales alcalinos proporcionan el mejor ejemplo de tendencias grupales en propiedades en la tabla periódica, con elementos que exhiben un comportamiento homólogo bien caracterizado . [5] Esta familia de elementos también se conoce como familia del litio por su elemento principal.
Los metales alcalinos son todos metales brillantes, blandos y altamente reactivos a temperatura y presión estándar y pierden fácilmente su electrón más externo para formar cationes con carga +1. Todos se pueden cortar fácilmente con un cuchillo debido a su suavidad, dejando al descubierto una superficie brillante que se empaña rápidamente en el aire debido a la oxidación por la humedad atmosférica y el oxígeno (y en el caso del litio, el nitrógeno ). Debido a su alta reactividad, deben almacenarse bajo aceite para evitar la reacción con el aire y se encuentran naturalmente sólo en sales y nunca como elementos libres. El cesio, el quinto metal alcalino, es el más reactivo de todos los metales. Todos los metales alcalinos reaccionan con el agua, reaccionando los metales alcalinos más pesados con más fuerza que los más ligeros.
Todos los metales alcalinos descubiertos se encuentran en la naturaleza como sus compuestos: en orden de abundancia , el sodio es el más abundante, seguido del potasio, el litio, el rubidio, el cesio y finalmente el francio, que es muy raro debido a su altísima radiactividad ; El francio se encuentra sólo en trazas diminutas en la naturaleza como paso intermedio en algunas ramas laterales oscuras de las cadenas de descomposición natural . Se han realizado experimentos para intentar la síntesis del elemento 119 , que probablemente sea el siguiente miembro del grupo; ninguno tuvo éxito. Sin embargo, es posible que el ununennio no sea un metal alcalino debido a efectos relativistas , que se prevé que tendrán una gran influencia en las propiedades químicas de los elementos superpesados ; Incluso si resulta ser un metal alcalino, se predice que tendrá algunas diferencias en propiedades físicas y químicas con respecto a sus homólogos más ligeros.
La mayoría de los metales alcalinos tienen muchas aplicaciones diferentes. Una de las aplicaciones más conocidas de los elementos puros es el uso de rubidio y cesio en relojes atómicos , de los cuales los relojes atómicos de cesio forman la base del segundo. Una aplicación común de los compuestos de sodio es la lámpara de vapor de sodio , que emite luz de manera muy eficiente. La sal de mesa , o cloruro de sodio, se utiliza desde la antigüedad. El litio se utiliza como medicamento psiquiátrico y como ánodo en baterías de litio . El sodio, el potasio y posiblemente el litio son elementos esenciales , que desempeñan importantes funciones biológicas como electrolitos , y aunque los demás metales alcalinos no son esenciales, también tienen diversos efectos sobre el organismo, tanto beneficiosos como perjudiciales.

Los compuestos de sodio se conocen desde la antigüedad; La sal ( cloruro de sodio ) ha sido un bien importante en las actividades humanas, como lo atestigua la palabra inglesa salario , en referencia al salarium , dinero pagado a los soldados romanos para la compra de sal. [6] [ se necesita una mejor fuente ] Si bien la potasa se ha utilizado desde la antigüedad, durante la mayor parte de su historia no se entendió que fuera una sustancia fundamentalmente diferente de las sales minerales de sodio. Georg Ernst Stahl obtuvo evidencia experimental que lo llevó a sugerir la diferencia fundamental entre las sales de sodio y potasio en 1702, [7] y Henri-Louis Duhamel du Monceau pudo demostrar esta diferencia en 1736. [8] La composición química exacta del potasio y los compuestos de sodio, y el estado como elemento químico del potasio y el sodio, no se conocía entonces, por lo que Antoine Lavoisier no incluyó ninguno de los álcalis en su lista de elementos químicos en 1789. [9] [10]
El potasio puro fue aislado por primera vez en 1807 en Inglaterra por Humphry Davy , quien lo derivó de la potasa cáustica (KOH, hidróxido de potasio) mediante el uso de electrólisis de la sal fundida con la recién inventada pila voltaica . Los intentos anteriores de electrólisis de la sal acuosa no tuvieron éxito debido a la extrema reactividad del potasio. [11] : 68 El potasio fue el primer metal que se aisló por electrólisis. [12] Más tarde, ese mismo año, Davy informó sobre la extracción de sodio de una sustancia similar, la soda cáustica (NaOH, lejía), mediante una técnica similar, demostrando que los elementos, y por tanto las sales, son diferentes. [9] [10] [13] [14]

La petalita ( Li Al Si 4 O 10 ) fue descubierta en 1800 por el químico brasileño José Bonifácio de Andrada en una mina de la isla de Utö, Suecia . [15] [16] [17] Sin embargo, no fue hasta 1817 que Johan August Arfwedson , entonces trabajando en el laboratorio del químico Jöns Jacob Berzelius , detectó la presencia de un nuevo elemento mientras analizaba el mineral de petalita . [18] [19] Observó que este nuevo elemento formaba compuestos similares a los del sodio y el potasio, aunque su carbonato e hidróxido eran menos solubles en agua y más alcalinos que los otros metales alcalinos. [20] Berzelius dio al material desconocido el nombre lithion / lithina , de la palabra griega λιθoς (transliterada como lithos , que significa "piedra"), para reflejar su descubrimiento en un mineral sólido, a diferencia del potasio, que se había descubierto en plantas. cenizas y sodio, conocido en parte por su gran abundancia en la sangre animal. Llamó al metal dentro del material litio . [21] [16] [19] El litio, el sodio y el potasio fueron parte del descubrimiento de la periodicidad , ya que se encuentran entre una serie de tríadas de elementos del mismo grupo que, según Johann Wolfgang Döbereiner en 1850, tenían propiedades similares. . [22]

El rubidio y el cesio fueron los primeros elementos descubiertos mediante el espectroscopio , inventado en 1859 por Robert Bunsen y Gustav Kirchhoff . [23] Al año siguiente, descubrieron cesio en el agua mineral de Bad Dürkheim , Alemania. Su descubrimiento del rubidio se produjo al año siguiente en Heidelberg , Alemania, encontrándolo en el mineral lepidolita . [24] Los nombres de rubidio y cesio provienen de las líneas más prominentes en sus espectros de emisión : una línea roja brillante para el rubidio (de la palabra latina rubidus , que significa rojo oscuro o rojo brillante), y una línea azul cielo para el cesio ( derivado de la palabra latina caesius , que significa azul cielo). [25] [26]
Alrededor de 1865, John Newlands produjo una serie de artículos en los que enumeraba los elementos en orden de peso atómico creciente y propiedades físicas y químicas similares que se repetían en intervalos de ocho; comparó esa periodicidad con las octavas de la música, donde las notas separadas por una octava tienen funciones musicales similares. [27] [28] Su versión reunió en un grupo todos los metales alcalinos entonces conocidos (de litio a cesio), así como el cobre, la plata y el talio (que muestran el estado de oxidación +1 característico de los metales alcalinos). Su mesa colocó el hidrógeno con los halógenos . [22]
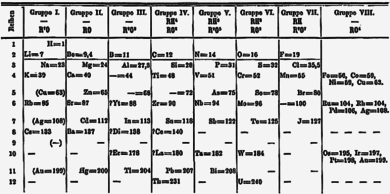
Después de 1869, Dmitri Mendeleev propuso su tabla periódica colocando al litio en la parte superior de un grupo junto con el sodio, el potasio, el rubidio, el cesio y el talio. [29] Dos años más tarde, Mendeleev revisó su tabla, colocando el hidrógeno en el grupo 1 por encima del litio, y también moviendo el talio al grupo del boro . En esta versión de 1871, el cobre, la plata y el oro se colocaron dos veces, una vez como parte del grupo IB y otra como parte de un "grupo VIII" que abarca los grupos actuales 8 a 11. [30] [nota 5] Después de la introducción de En la tabla de 18 columnas, los elementos del grupo IB se movieron a su posición actual en el bloque d , mientras que los metales alcalinos se dejaron en el grupo IA . Posteriormente, el nombre del grupo se cambió al grupo 1 en 1988. [4] El nombre trivial "metales alcalinos" proviene del hecho de que los hidróxidos de los elementos del grupo 1 son todos álcalis fuertes cuando se disuelven en agua. [5]
Hubo al menos cuatro descubrimientos erróneos e incompletos [31] [32] [33] [34] antes de que Marguerite Perey del Instituto Curie en París, Francia, descubriera el francio en 1939 purificando una muestra de actinio-227 , que se había informado que tienen una energía de desintegración de 220 keV . Sin embargo, Perey notó partículas en descomposición con un nivel de energía inferior a 80 keV. Perey pensó que esta actividad de desintegración podría haber sido causada por un producto de desintegración no identificado previamente, uno que se separó durante la purificación, pero que emergió nuevamente del actinio -227 puro. Varias pruebas eliminaron la posibilidad de que el elemento desconocido fuera torio , radio , plomo, bismuto o talio . El nuevo producto presentaba propiedades químicas de un metal alcalino (como la coprecipitación con sales de cesio), lo que llevó a Perey a creer que se trataba del elemento 87, causado por la desintegración alfa del actinio-227. [35] Perey luego intentó determinar la proporción de desintegración beta y alfa en actinio-227. Su primera prueba situó la ramificación alfa en un 0,6%, cifra que luego revisó al 1%. [36]
El siguiente elemento debajo del francio ( eka -francio) en la tabla periódica sería ununennio (Uue), elemento 119. [37] : 1729-1730 La síntesis de ununennio se intentó por primera vez en 1985 bombardeando un objetivo de einstenio -254 con calcio. -48 iones en el acelerador superHILAC del Laboratorio Nacional Lawrence Berkeley en Berkeley, California. No se identificaron átomos, lo que llevó a un rendimiento límite de 300 nb . [38] [39]
Es muy improbable [38] que esta reacción pueda crear átomos de ununennio en un futuro próximo, dada la tarea extremadamente difícil de producir cantidades suficientes de einstenio-254, que es el preferido para la producción de elementos ultrapesados debido a su gran tamaño. masa, vida media relativamente larga de 270 días y disponibilidad en cantidades significativas de varios microgramos, [40] para crear un objetivo lo suficientemente grande como para aumentar la sensibilidad del experimento al nivel requerido; El einstenio no se ha encontrado en la naturaleza y sólo se ha producido en laboratorios y en cantidades menores que las necesarias para una síntesis eficaz de elementos superpesados. Sin embargo, dado que ununennium es sólo el primer elemento del período 8 de la tabla periódica ampliada , es muy posible que se descubra en un futuro próximo mediante otras reacciones y, de hecho, actualmente se está intentando sintetizarlo en Japón. [41] Actualmente, ninguno de los elementos del período 8 ha sido descubierto todavía, y también es posible, debido a las inestabilidades del goteo , que solo los elementos del período 8 inferiores, hasta alrededor del elemento 128, sean físicamente posibles. [42] [43] No se han realizado intentos de síntesis para metales alcalinos más pesados: debido a su número atómico extremadamente alto, requerirían métodos y tecnología nuevos y más potentes para fabricarlos. [37] : 1737-1739

La regla de Oddo-Harkins sostiene que los elementos con números atómicos pares son más comunes que aquellos con números atómicos impares, a excepción del hidrógeno. Esta regla sostiene que los elementos con números atómicos impares tienen un protón desapareado y es más probable que capturen otro, aumentando así su número atómico. En elementos con números atómicos pares, los protones están emparejados, y cada miembro del par compensa el giro del otro, lo que mejora la estabilidad. [45] [46] [47] Todos los metales alcalinos tienen números atómicos impares y no son tan comunes como los elementos con números atómicos pares adyacentes a ellos (los gases nobles y los metales alcalinotérreos ) en el Sistema Solar. Los metales alcalinos más pesados también son menos abundantes que los más ligeros, ya que los metales alcalinos a partir del rubidio sólo pueden sintetizarse en supernovas y no en nucleosíntesis estelar . El litio también es mucho menos abundante que el sodio y el potasio, ya que se sintetiza mal tanto en la nucleosíntesis del Big Bang como en las estrellas: el Big Bang sólo pudo producir trazas de litio, berilio y boro debido a la ausencia de un núcleo estable con 5 u 8 Los nucleones y la nucleosíntesis estelar sólo podían superar este cuello de botella mediante el proceso triple alfa , fusionando tres núcleos de helio para formar carbono y saltándose esos tres elementos. [44]

La Tierra se formó a partir de la misma nube de materia que formó el Sol, pero los planetas adquirieron composiciones diferentes durante la formación y evolución del sistema solar . A su vez, la historia natural de la Tierra hizo que partes de este planeta tuvieran diferentes concentraciones de elementos. La masa de la Tierra es aproximadamente 5,98 × 1024 kilogramos. Está compuesto principalmente por hierro (32,1%), oxígeno (30,1%), silicio (15,1%), magnesio (13,9%), azufre (2,9%), níquel (1,8%), calcio (1,5%) y aluminio ( 1,4%); y el 1,2% restante consiste en trazas de otros elementos. Debido a la diferenciación planetaria , se cree que la región central está compuesta principalmente de hierro (88,8%), con cantidades más pequeñas de níquel (5,8%), azufre (4,5%) y menos del 1% de oligoelementos. [48]
Los metales alcalinos, debido a su alta reactividad, no se encuentran naturalmente en forma pura en la naturaleza. Son litófilos y, por lo tanto, permanecen cerca de la superficie de la Tierra porque se combinan fácilmente con el oxígeno y, por lo tanto, se asocian fuertemente con la sílice , formando minerales de densidad relativamente baja que no se hunden en el núcleo de la Tierra. El potasio, el rubidio y el cesio también son elementos incompatibles debido a sus grandes radios iónicos . [49]
El sodio y el potasio son muy abundantes en la Tierra, estando ambos entre los diez elementos más comunes en la corteza terrestre ; [50] [51] el sodio constituye aproximadamente el 2,6% de la corteza terrestre medida en peso, lo que lo convierte en el sexto elemento más abundante en general [52] y el metal alcalino más abundante. El potasio constituye aproximadamente el 1,5% de la corteza terrestre y es el séptimo elemento más abundante. [52] El sodio se encuentra en muchos minerales diferentes, de los cuales el más común es la sal común (cloruro de sodio), que se encuentra en grandes cantidades disuelta en el agua de mar. Otros depósitos sólidos incluyen halita , anfíbol , criolita , nitratina y zeolita . [52] Muchos de estos depósitos sólidos se producen como resultado de la evaporación de los mares antiguos, lo que todavía ocurre ahora en lugares como el Gran Lago Salado de Utah y el Mar Muerto . [11] : 69 A pesar de su abundancia casi igual en la corteza terrestre, el sodio es mucho más común que el potasio en el océano, porque el mayor tamaño del potasio hace que sus sales sean menos solubles y porque el potasio está unido a los silicatos del suelo y lo que el potasio se lixivia. Las plantas lo absorben mucho más fácilmente que el sodio. [11] : 69
A pesar de su similitud química, el litio normalmente no se encuentra junto con el sodio o el potasio debido a su tamaño más pequeño. [11] : 69 Debido a su reactividad relativamente baja, se puede encontrar en el agua de mar en grandes cantidades; Se estima que la concentración de litio en el agua de mar es de aproximadamente 0,14 a 0,25 partes por millón (ppm) [53] [54] o 25 micromolar . [55] Su relación diagonal con el magnesio a menudo le permite reemplazar el magnesio en los minerales de ferromagnesio, donde su concentración en la corteza es de aproximadamente 18 ppm , comparable a la del galio y el niobio . Comercialmente, el mineral de litio más importante es la espodumena , que se encuentra en grandes depósitos en todo el mundo. [11] : 69
El rubidio es aproximadamente tan abundante como el zinc y más abundante que el cobre. Se encuentra naturalmente en los minerales leucita , polucita , carnalita , zinnwaldita y lepidolita , [56] aunque ninguno de ellos contiene solo rubidio ni otros metales alcalinos. [11] : 70 El cesio es más abundante que algunos elementos comúnmente conocidos, como el antimonio , el cadmio , el estaño y el tungsteno , pero es mucho menos abundante que el rubidio. [57]
El francio-223 , el único isótopo natural del francio, [58] [59] es el producto de la desintegración alfa del actinio-227 y se puede encontrar en pequeñas cantidades en minerales de uranio . [60] En una muestra dada de uranio, se estima que hay sólo un átomo de francio por cada 10 18 átomos de uranio. [61] [62] Se ha calculado que hay como máximo 30 gramos de francio en la corteza terrestre en cualquier momento, debido a su extremadamente corta vida media de 22 minutos. [63] [64]
Las propiedades físicas y químicas de los metales alcalinos pueden explicarse fácilmente porque tienen una configuración electrónica de valencia ns 1 , lo que da lugar a enlaces metálicos débiles . De ahí que todos los metales alcalinos sean blandos y tengan bajas densidades , [5] puntos de fusión [5] y de ebullición , [5] así como calores de sublimación , vaporización y disociación . [11] : 74 Todos cristalizan en la estructura cristalina cúbica centrada en el cuerpo , [11] : 73 y tienen colores de llama distintivos porque su electrón s externo se excita muy fácilmente. [11] : 75 De hecho, estos colores de prueba de llama son la forma más común de identificarlos ya que todas sus sales con iones comunes son solubles. [11] : 75 La configuración ns 1 también da como resultado que los metales alcalinos tengan radios atómicos e iónicos muy grandes , así como una conductividad térmica y eléctrica muy alta . [11] : 75 Su química está dominada por la pérdida de su único electrón de valencia en el orbital s más externo para formar el estado de oxidación +1, debido a la facilidad de ionizar este electrón y la muy alta segunda energía de ionización. [11] : 76 La mayor parte de la química se ha observado sólo en los primeros cinco miembros del grupo. La química del francio no está bien establecida debido a su extrema radiactividad ; [5] por lo tanto, la presentación aquí de sus propiedades es limitada. Lo poco que se sabe sobre el francio muestra que su comportamiento es muy parecido al del cesio, como se esperaba. Las propiedades físicas del francio son aún más incompletas porque nunca se ha observado el elemento en masa; por lo tanto, cualquier dato que pueda encontrarse en la literatura son ciertamente extrapolaciones especulativas. [sesenta y cinco]
Los metales alcalinos son más similares entre sí que los elementos de cualquier otro grupo entre sí. [5] De hecho, la similitud es tan grande que es bastante difícil separar el potasio, el rubidio y el cesio, debido a sus radios iónicos similares ; el litio y el sodio son más distintos. Por ejemplo, al descender en la tabla, todos los metales alcalinos conocidos muestran un radio atómico creciente , [72] una electronegatividad decreciente , [72] una reactividad creciente , [5] y puntos de fusión y ebullición decrecientes [72] , así como calores de fusión y vaporización. . [11] : 75 En general, sus densidades aumentan al descender en la tabla, con la excepción de que el potasio es menos denso que el sodio. [72] Una de las pocas propiedades de los metales alcalinos que no muestra una tendencia muy suave es su potencial de reducción : el valor del litio es anómalo, siendo más negativo que los demás. [11] : 75 Esto se debe a que el ion Li + tiene una energía de hidratación muy alta en la fase gaseosa: aunque el ion litio altera significativamente la estructura del agua, provocando un mayor cambio en la entropía, esta alta energía de hidratación es suficiente para hacer que el Los potenciales de reducción lo indican como el metal alcalino más electropositivo, a pesar de la dificultad de ionizarlo en fase gaseosa. [11] : 75
Los metales alcalinos estables son todos metales de color plateado excepto el cesio, que tiene un tinte dorado pálido: [73] es uno de los tres únicos metales que están claramente coloreados (los otros dos son cobre y oro). [11] : 74 Además, los metales pesados alcalinotérreos calcio , estroncio y bario , así como los lantánidos divalentes europio e iterbio , son de color amarillo pálido, aunque el color es mucho menos prominente que el del cesio. [11] : 74 Su brillo se empaña rápidamente en el aire debido a la oxidación. [5]
Todos los metales alcalinos son altamente reactivos y nunca se encuentran en formas elementales en la naturaleza. [21] Debido a esto, generalmente se almacenan en aceite mineral o queroseno (aceite de parafina). [74] Reaccionan agresivamente con los halógenos para formar haluros de metales alcalinos , que son compuestos cristalinos iónicos blancos que son todos solubles en agua excepto el fluoruro de litio (LiF). [5] Los metales alcalinos también reaccionan con el agua para formar hidróxidos fuertemente alcalinos y, por lo tanto, deben manipularse con mucho cuidado. Los metales alcalinos más pesados reaccionan con más fuerza que los más ligeros; por ejemplo, cuando se deja caer al agua, el cesio produce una explosión mayor que el potasio si se utiliza la misma cantidad de moles de cada metal. [5] [75] [57] Los metales alcalinos tienen las primeras energías de ionización más bajas en sus respectivos períodos de la tabla periódica [65] debido a su baja carga nuclear efectiva [5] y la capacidad de alcanzar una configuración de gas noble al perder sólo un electrón . [5] Los metales alcalinos no sólo reaccionan con el agua, sino también con donantes de protones como alcoholes y fenoles , amoníaco gaseoso y alquinos , demostrando este último el fenomenal grado de su reactividad. Su gran poder como agentes reductores los hace muy útiles para liberar otros metales de sus óxidos o haluros. [11] : 76
La segunda energía de ionización de todos los metales alcalinos es muy alta [5] [65] ya que se encuentran en una capa completa que también está más cerca del núcleo; [5] por lo tanto, casi siempre pierden un solo electrón, formando cationes. [11] : 28 Los alcaluros son una excepción: son compuestos inestables que contienen metales alcalinos en un estado de oxidación -1, lo cual es muy inusual ya que antes del descubrimiento de los alcaluros, no se esperaba que los metales alcalinos pudieran formar aniones. y se pensaba que podían aparecer en las sales sólo como cationes. Los aniones alcalinos tienen subcapas s llenas , lo que les da suficiente estabilidad para existir. Se sabe que todos los metales alcalinos estables, excepto el litio, pueden formar alcalidos, [76] [77] [78] y los alcalidos tienen mucho interés teórico debido a su estequiometría inusual y sus bajos potenciales de ionización . Los alcaluros son químicamente similares a los electruros , que son sales con electrones atrapados que actúan como aniones. [79] Un ejemplo particularmente sorprendente de un álcali es el " hidruro de sodio inverso ", H + Na − (ambos iones están formando complejos ), a diferencia del hidruro de sodio habitual, Na + H − : [80] es inestable de forma aislada. debido a su alta energía resultante del desplazamiento de dos electrones del hidrógeno al sodio, aunque se predice que varios derivados serán metaestables o estables. [80] [81]
En solución acuosa, los iones de metales alcalinos forman iones acuáticos de fórmula [M(H 2 O) n ] + , donde n es el número de solvatación. Sus números y formas de coordinación concuerdan bien con los que se esperan de sus radios iónicos. En solución acuosa, se dice que las moléculas de agua directamente unidas al ion metálico pertenecen a la primera esfera de coordinación , también conocida como primera capa de solvatación o primaria. El enlace entre una molécula de agua y el ion metálico es un enlace covalente dativo , en el que el átomo de oxígeno dona ambos electrones al enlace. Cada molécula de agua coordinada puede estar unida mediante enlaces de hidrógeno a otras moléculas de agua. Se dice que estos últimos residen en la segunda esfera de coordinación. Sin embargo, para los cationes de metales alcalinos, la segunda esfera de coordinación no está bien definida ya que la carga +1 en el catión no es lo suficientemente alta como para polarizar las moléculas de agua en la capa de solvatación primaria lo suficiente como para que formen fuertes enlaces de hidrógeno con las de la capa de solvatación primaria. la segunda esfera de coordinación, produciendo una entidad más estable. [82] [83] : 25 Se ha determinado experimentalmente que el número de solvatación del Li + es 4, formando el tetraédrico [Li(H 2 O) 4 ] + : mientras que se han encontrado números de solvatación de 3 a 6 para los iones de litio y agua. , los números de solvatación inferiores a 4 pueden ser el resultado de la formación de pares de iones de contacto , y los números de solvatación más altos pueden interpretarse en términos de moléculas de agua que se aproximan a [Li(H 2 O) 4 ] + a través de una cara del tetraedro, aunque las simulaciones de dinámica molecular pueden indicar la existencia de un ion hexaaqua octaédrico . Probablemente también haya seis moléculas de agua en la esfera de solvatación primaria del ion sodio, formando el ion octaédrico [Na(H 2 O) 6 ] + . [66] [83] : 126–127 Si bien anteriormente se pensaba que los metales alcalinos más pesados también formaban iones hexaaqua octaédricos, desde entonces se ha descubierto que el potasio y el rubidio probablemente forman [K(H 2 O) 8 ] + y [ Rb(H 2 O) 8 ] + iones, que tienen la estructura antiprismática cuadrada , y que el cesio forma el ion de 12 coordenadas [Cs(H 2 O) 12 ] + . [84]
La química del litio muestra varias diferencias con la del resto del grupo, ya que el pequeño catión Li + polariza los aniones y da a sus compuestos un carácter más covalente . [5] El litio y el magnesio tienen una relación diagonal debido a sus radios atómicos similares, [5] por lo que muestran algunas similitudes. Por ejemplo, el litio forma un nitruro estable , una propiedad común entre todos los metales alcalinotérreos (grupo del magnesio) pero única entre los metales alcalinos. [85] Además, entre sus respectivos grupos, sólo el litio y el magnesio forman compuestos organometálicos con carácter covalente significativo (por ejemplo, Li Me y MgMe 2 ). [86]
El fluoruro de litio es el único haluro de metal alcalino que es poco soluble en agua, [5] y el hidróxido de litio es el único hidróxido de metal alcalino que no es delicuescente . [5] Por el contrario, el perclorato de litio y otras sales de litio con aniones grandes que no pueden polarizarse son mucho más estables que los compuestos análogos de otros metales alcalinos, probablemente porque el Li + tiene una alta energía de solvatación. [11] : 76 Este efecto también significa que la mayoría de las sales de litio simples se encuentran comúnmente en forma hidratada, porque las formas anhidras son extremadamente higroscópicas : esto permite que sales como el cloruro de litio y el bromuro de litio se utilicen en deshumidificadores y acondicionadores de aire . [11] : 76
También se predice que el francio mostrará algunas diferencias debido a su alto peso atómico , lo que hace que sus electrones viajen a fracciones considerables de la velocidad de la luz y, por lo tanto, hace que los efectos relativistas sean más prominentes. En contraste con la tendencia a la disminución de la electronegatividad y la energía de ionización de los metales alcalinos, se predice que la electronegatividad y la energía de ionización del francio serán mayores que las del cesio debido a la estabilización relativista de los electrones 7s; Además, se espera que su radio atómico sea anormalmente bajo. Por tanto, contrariamente a lo esperado, el cesio es el más reactivo de los metales alcalinos, no el francio. [68] [37] : 1729 [87] Todas las propiedades físicas conocidas del francio también se desvían de las tendencias claras que van del litio al cesio, como la primera energía de ionización, la afinidad electrónica y la polarización de los aniones, aunque debido a la escasez de conocimientos conocidos. Los datos sobre el francio muchas fuentes dan valores extrapolados, ignorando que los efectos relativistas hacen que la tendencia del litio al cesio se vuelva inaplicable en el francio. [87] Algunas de las pocas propiedades del francio que se han predicho teniendo en cuenta la relatividad son la afinidad electrónica (47,2 kJ/mol) [88] y la entalpía de disociación de la molécula de Fr 2 (42,1 kJ/mol). [89] La molécula CsFr está polarizada como Cs + Fr − , lo que muestra que la subcapa 7s del francio se ve mucho más afectada por efectos relativistas que la subcapa 6s del cesio. [87] Además, se espera que el superóxido de francio (FrO 2 ) tenga un carácter covalente significativo, a diferencia de otros superóxidos de metales alcalinos, debido a las contribuciones de enlace de los electrones 6p del francio. [87]
Todos los metales alcalinos tienen números atómicos impares; por lo tanto, sus isótopos deben ser impares-impares (tanto el número de protones como de neutrones son impares) o impares-pares ( el número de protones es impar, pero el número de neutrones es par). Los núcleos impares e impares tienen números de masa pares , mientras que los núcleos pares e impares tienen números de masa impares. Los nucleidos primordiales impares son raros porque la mayoría de los núcleos impares son altamente inestables con respecto a la desintegración beta , porque los productos de la desintegración son pares-pares y, por lo tanto, están más fuertemente unidos debido a los efectos del apareamiento nuclear . [90]
Debido a la gran rareza de los núcleos impares e impares, casi todos los isótopos primordiales de los metales alcalinos son pares o impares (las excepciones son el isótopo estable a la luz litio-6 y el radioisótopo de larga vida potasio-40). Para un número de masa impar dado, solo puede haber un único nucleido beta estable , ya que no hay una diferencia en la energía de enlace entre par-impar e impar-par comparable a la que existe entre par-par e impar-impar, dejando otros nucleidos del mismo número de masa ( isobaras ) libres de desintegración beta hacia el nucleido de menor masa. Un efecto de la inestabilidad de un número impar de cualquier tipo de nucleones es que los elementos impares, como los metales alcalinos, tienden a tener menos isótopos estables que los elementos pares. De los 26 elementos monoisotópicos que tienen un solo isótopo estable, todos menos uno tienen un número atómico impar y todos menos uno también tienen un número par de neutrones. El berilio es la única excepción a ambas reglas, debido a su bajo número atómico. [90]
Todos los metales alcalinos, excepto el litio y el cesio, tienen al menos un radioisótopo natural : el sodio-22 y el sodio-24 son trazas de radioisótopos producidos cosmogénicamente , [91] el potasio-40 y el rubidio-87 tienen vidas medias muy largas y, por tanto, se producen de forma natural. , [92] y todos los isótopos del francio son radiactivos . [92] También se pensaba que el cesio era radiactivo a principios del siglo XX, [93] [94] aunque no tiene radioisótopos naturales. [92] (El franco aún no se había descubierto en ese momento). El radioisótopo natural de larga duración del potasio, el potasio-40, constituye aproximadamente el 0,012% del potasio natural, [95] y, por lo tanto, el potasio natural es débilmente radiactivo. Esta radiactividad natural se convirtió en la base de una afirmación errónea sobre el descubrimiento del elemento 87 (el siguiente metal alcalino después del cesio) en 1925. [31] [32] El rubidio natural es igualmente ligeramente radiactivo, siendo el 27,83% el radioisótopo de larga vida rubidio. -87. [11] : 74
El cesio-137 , con una vida media de 30,17 años, es uno de los dos principales productos de fisión de vida media , junto con el estroncio-90 , responsables de la mayor parte de la radiactividad del combustible nuclear gastado tras varios años de enfriamiento, hasta hasta varios cientos de años después de su uso. Constituye la mayor parte de la radiactividad que aún queda del accidente de Chernóbil . El cesio-137 sufre una desintegración beta de alta energía y finalmente se convierte en bario-137 estable . Es un fuerte emisor de radiación gamma. El cesio-137 tiene una tasa muy baja de captura de neutrones y no es factible eliminarlo de esta manera, sino que se debe permitir que se desintegre. [96] El cesio-137 se ha utilizado como trazador en estudios hidrológicos, de forma análoga al uso del tritio . [97] Pequeñas cantidades de cesio-134 y cesio-137 fueron liberadas al medio ambiente durante casi todas las pruebas de armas nucleares y algunos accidentes nucleares , sobre todo el accidente de Goiânia y el desastre de Chernobyl . Desde 2005, el cesio-137 es la principal fuente de radiación en la zona de aislamiento alrededor de la central nuclear de Chernóbil . [98] Sus propiedades químicas como uno de los metales alcalinos lo convierten en uno de los productos de fisión de vida corta a media más problemáticos porque se mueve y propaga fácilmente en la naturaleza debido a la alta solubilidad en agua de sus sales, y es absorbido por el cuerpo, que lo confunde con sus congéneres esenciales sodio y potasio. [99] : 114
Los metales alcalinos son más similares entre sí que los elementos de cualquier otro grupo entre sí. [5] Por ejemplo, al moverse hacia abajo en la tabla, todos los metales alcalinos conocidos muestran un radio atómico creciente , [72] una electronegatividad decreciente , [72] una reactividad creciente , [5] y puntos de fusión y ebullición decrecientes [72] , así como calores de fusión y vaporización. [11] : 75 En general, sus densidades aumentan al descender en la tabla, con la excepción de que el potasio es menos denso que el sodio. [72]

Los radios atómicos de los metales alcalinos aumentan a medida que avanza el grupo. [72] Debido al efecto de protección , cuando un átomo tiene más de una capa electrónica , cada electrón siente repulsión eléctrica de los otros electrones, así como atracción eléctrica del núcleo. [100] En los metales alcalinos, el electrón más externo solo siente una carga neta de +1, ya que parte de la carga nuclear (que es igual al número atómico ) es cancelada por los electrones internos; El número de electrones internos de un metal alcalino es siempre uno menos que la carga nuclear. Por tanto, el único factor que afecta al radio atómico de los metales alcalinos es el número de capas de electrones. Dado que este número aumenta a lo largo del grupo, el radio atómico también debe aumentar a lo largo del grupo. [72]
Los radios iónicos de los metales alcalinos son mucho más pequeños que sus radios atómicos. Esto se debe a que el electrón más externo de los metales alcalinos está en una capa electrónica diferente a la de los electrones internos y, por lo tanto, cuando se elimina, el átomo resultante tiene una capa electrónica menos y es más pequeño. Además, la carga nuclear efectiva ha aumentado y, por tanto, los electrones son atraídos con más fuerza hacia el núcleo y el radio iónico disminuye. [5]

La primera energía de ionización de un elemento o molécula es la energía necesaria para mover el electrón más flojo de un mol de átomos gaseosos del elemento o molécula para formar un mol de iones gaseosos con carga eléctrica +1. Los factores que afectan la primera energía de ionización son la carga nuclear , la cantidad de blindaje de los electrones internos y la distancia desde el núcleo al electrón más suelto, que siempre es un electrón externo en los elementos del grupo principal . Los dos primeros factores cambian la carga nuclear efectiva que siente el electrón más débilmente retenido. Dado que el electrón más externo de los metales alcalinos siempre siente la misma carga nuclear efectiva (+1), el único factor que afecta la primera energía de ionización es la distancia desde el electrón más externo al núcleo. Dado que esta distancia aumenta a lo largo del grupo, el electrón más externo siente menos atracción por parte del núcleo y, por tanto, la primera energía de ionización disminuye. [72] Esta tendencia se rompe en el francio debido a la estabilización relativista y la contracción del orbital 7s, lo que acerca el electrón de valencia del francio al núcleo de lo que se esperaría a partir de cálculos no relativistas. Esto hace que el electrón más externo del francio sienta más atracción por parte del núcleo, aumentando su primera energía de ionización ligeramente más allá de la del cesio. [37] : 1729
La segunda energía de ionización de los metales alcalinos es mucho mayor que la primera, ya que el segundo electrón más suelto forma parte de una capa electrónica completamente llena y, por tanto, es difícil de eliminar. [5]
Las reactividades de los metales alcalinos aumentan a medida que avanzan en el grupo. Esto es el resultado de una combinación de dos factores: las primeras energías de ionización y las energías de atomización de los metales alcalinos. Debido a que la primera energía de ionización de los metales alcalinos disminuye en el grupo, es más fácil que el electrón más externo sea eliminado del átomo y participe en reacciones químicas , aumentando así la reactividad en el grupo. La energía de atomización mide la fuerza del enlace metálico de un elemento, que cae dentro del grupo a medida que los átomos aumentan de radio y por tanto el enlace metálico debe aumentar de longitud, alejando los electrones deslocalizados de la atracción de los núcleos del elemento más pesado. Metales alcalinos. La suma de las energías de atomización y de la primera ionización da una cantidad estrechamente relacionada (pero no igual) con la energía de activación de la reacción de un metal alcalino con otra sustancia. Esta cantidad disminuye a medida que avanza el grupo, al igual que la energía de activación; por lo tanto, las reacciones químicas pueden ocurrir más rápido y la reactividad aumenta en el grupo. [101]
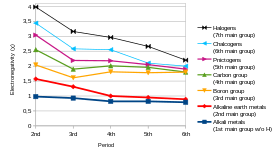
La electronegatividad es una propiedad química que describe la tendencia de un átomo o un grupo funcional a atraer electrones (o densidad electrónica ) hacia sí mismo. [102] Si el enlace entre el sodio y el cloro en el cloruro de sodio fuera covalente , el par de electrones compartidos sería atraído por el cloro porque la carga nuclear efectiva en los electrones externos es +7 en el cloro pero solo es +1 en el sodio. El par de electrones es atraído tan cerca del átomo de cloro que prácticamente se transfieren al átomo de cloro (un enlace iónico ). Sin embargo, si el átomo de sodio fue reemplazado por un átomo de litio, los electrones no serán atraídos tan cerca del átomo de cloro como antes porque el átomo de litio es más pequeño, lo que hace que el par de electrones se atraiga más fuertemente hacia la carga nuclear efectiva más cercana del litio. Por lo tanto, los átomos de metales alcalinos más grandes (más abajo en el grupo) serán menos electronegativos ya que el par de enlace se siente menos atraído hacia ellos. Como se mencionó anteriormente, se espera que el francio sea una excepción. [72]
Debido a la mayor electronegatividad del litio, algunos de sus compuestos tienen un carácter más covalente. Por ejemplo, el yoduro de litio (LiI) se disolverá en disolventes orgánicos , una propiedad de la mayoría de los compuestos covalentes. [72] El fluoruro de litio (LiF) es el único haluro alcalino que no es soluble en agua, [5] y el hidróxido de litio (LiOH) es el único hidróxido de metal alcalino que no es delicuescente . [5]
El punto de fusión de una sustancia es el punto donde cambia de estado de sólido a líquido, mientras que el punto de ebullición de una sustancia (en estado líquido) es el punto donde la presión de vapor del líquido es igual a la presión ambiental que rodea al líquido [103] [ 104] y todo el líquido cambia de estado a gas. A medida que un metal se calienta hasta su punto de fusión, los enlaces metálicos que mantienen los átomos en su lugar se debilitan para que los átomos puedan moverse y, finalmente, los enlaces metálicos se rompen por completo en el punto de ebullición del metal. [72] [105] Por lo tanto, la caída de los puntos de fusión y ebullición de los metales alcalinos indica que la fuerza de los enlaces metálicos de los metales alcalinos disminuye a lo largo del grupo. [72] Esto se debe a que los átomos metálicos se mantienen unidos por la atracción electromagnética de los iones positivos a los electrones deslocalizados. [72] [105] A medida que los átomos aumentan de tamaño al descender por el grupo (debido a que su radio atómico aumenta), los núcleos de los iones se alejan más de los electrones deslocalizados y, por lo tanto, el enlace metálico se vuelve más débil, de modo que el metal puede separarse más fácilmente. derretir y hervir, disminuyendo así los puntos de fusión y ebullición. [72] El aumento de la carga nuclear no es un factor relevante debido al efecto de blindaje. [72]
Todos los metales alcalinos tienen la misma estructura cristalina ( cúbica centrada en el cuerpo ) [11] y por lo tanto los únicos factores relevantes son el número de átomos que pueden caber en un cierto volumen y la masa de uno de los átomos, ya que la densidad se define como masa por unidad de volumen. El primer factor depende del volumen del átomo y, por tanto, del radio atómico, que aumenta a medida que avanza el grupo; por tanto, el volumen de un átomo de metal alcalino aumenta al descender por el grupo. La masa de un átomo de metal alcalino también aumenta a medida que desciende del grupo. Así, la tendencia de las densidades de los metales alcalinos depende de sus pesos atómicos y radios atómicos; Si se conocen las cifras de estos dos factores, se pueden calcular las relaciones entre las densidades de los metales alcalinos. La tendencia resultante es que las densidades de los metales alcalinos aumentan en la tabla, con excepción del potasio. Debido a que tienen el peso atómico más bajo y el radio atómico más grande de todos los elementos en sus períodos, los metales alcalinos son los metales menos densos de la tabla periódica. [72] El litio, el sodio y el potasio son los únicos tres metales de la tabla periódica que son menos densos que el agua: [5] de hecho, el litio es el sólido menos denso conocido a temperatura ambiente . [11] : 75
Los metales alcalinos forman series completas de compuestos con todos los aniones habituales, que ilustran bien las tendencias del grupo. Se puede describir que estos compuestos implican que los metales alcalinos pierdan electrones hacia especies aceptoras y formen iones monopositivos. [11] : 79 Esta descripción es más precisa para los haluros alcalinos y se vuelve cada vez menos precisa a medida que aumentan las cargas catiónicas y aniónicas, y a medida que el anión se vuelve más grande y más polarizable. Por ejemplo, el enlace iónico da paso al enlace metálico a lo largo de la serie NaCl, Na 2 O, Na 2 S, Na 3 P, Na 3 As, Na 3 Sb, Na 3 Bi, Na. [11] : 81

Todos los metales alcalinos reaccionan vigorosa o explosivamente con agua fría, produciendo una solución acuosa de un hidróxido de metal alcalino fuertemente básico y liberando gas hidrógeno. [101] Esta reacción se vuelve más vigorosa a medida que avanza el grupo: el litio reacciona de manera constante con efervescencia , pero el sodio y el potasio pueden encenderse, y el rubidio y el cesio se hunden en el agua y generan gas hidrógeno tan rápidamente que se forman ondas de choque en el agua que pueden romper el vidrio. contenedores. [5] Cuando un metal alcalino se deja caer al agua, se produce una explosión, de la cual hay dos etapas separadas. El metal reacciona primero con el agua, rompiendo los enlaces de hidrógeno en el agua y produciendo gas hidrógeno ; esto ocurre más rápido para los metales alcalinos más pesados y reactivos. En segundo lugar, el calor generado por la primera parte de la reacción a menudo enciende el gas hidrógeno, provocando que se queme explosivamente en el aire circundante. Esta explosión secundaria de gas hidrógeno produce la llama visible sobre el recipiente de agua, lago u otro cuerpo de agua, no la reacción inicial del metal con el agua (que tiende a ocurrir principalmente bajo el agua). [75] Los hidróxidos de metales alcalinos son los hidróxidos más básicos conocidos. [11] : 87
Investigaciones recientes han sugerido que el comportamiento explosivo de los metales alcalinos en el agua se debe a una explosión de Coulomb y no únicamente a la rápida generación de hidrógeno. [106] Todos los metales alcalinos se funden como parte de la reacción con el agua. Las moléculas de agua ionizan la superficie metálica desnuda del metal líquido, dejando una superficie metálica cargada positivamente e iones de agua cargados negativamente. La atracción entre el metal cargado y los iones de agua aumentará rápidamente el área de superficie, provocando un aumento exponencial de la ionización. Cuando las fuerzas repulsivas dentro de la superficie del metal líquido exceden las fuerzas de tensión superficial, explota vigorosamente. [106]
Los propios hidróxidos son los hidróxidos más básicos conocidos y reaccionan con ácidos para dar sales y con alcoholes para dar alcóxidos oligoméricos . Reaccionan fácilmente con dióxido de carbono para formar carbonatos o bicarbonatos , o con sulfuro de hidrógeno para formar sulfuros o bisulfuros , y pueden usarse para separar tioles del petróleo. Reaccionan con óxidos anfóteros: por ejemplo, los óxidos de aluminio , zinc , estaño y plomo reaccionan con los hidróxidos de metales alcalinos para dar aluminatos, zincatos, estanatos y plumbatos. El dióxido de silicio es ácido y, por tanto, los hidróxidos de metales alcalinos también pueden atacar al vidrio de silicato . [11] : 87

Los metales alcalinos forman muchos compuestos intermetálicos entre sí y con los elementos de los grupos 2 a 13 de la tabla periódica de diferentes estequiometrías, [11] : 81, como las amalgamas de sodio con mercurio , entre ellas Na 5 Hg 8 y Na 3 Hg. [107] Algunos de ellos tienen características iónicas: tomando como ejemplo las aleaciones con oro, el más electronegativo de los metales, NaAu y KAu son metálicos, pero RbAu y CsAu son semiconductores. [11] : 81 NaK es una aleación de sodio y potasio muy útil por ser líquido a temperatura ambiente, aunque hay que extremar precauciones debido a su extrema reactividad con el agua y el aire. La mezcla eutéctica se funde a -12,6 °C. [108] Una aleación de 41% de cesio, 47% de sodio y 12% de potasio tiene el punto de fusión más bajo conocido de cualquier metal o aleación, -78 °C. [23]
Los compuestos intermetálicos de los metales alcalinos con los elementos más pesados del grupo 13 (aluminio, galio , indio y talio ), como el NaTl, son malos conductores o semiconductores , a diferencia de las aleaciones normales con los elementos anteriores, lo que implica que el metal alcalino involucrado tiene perdió un electrón por los aniones Zintl involucrados. [109] Sin embargo, mientras que los elementos del grupo 14 y posteriores tienden a formar grupos aniónicos discretos, los elementos del grupo 13 tienden a formar iones poliméricos con los cationes de metales alcalinos ubicados entre la red iónica gigante. Por ejemplo, NaTl consiste en un anión polimérico (—Tl − —) n con una estructura cúbica de diamante covalente con iones Na + ubicados entre la red aniónica. Los metales alcalinos más grandes no pueden encajar de manera similar en una red aniónica y tienden a forzar a los elementos más pesados del grupo 13 a formar grupos aniónicos. [110]
El boro es un caso especial, ya que es el único no metal del grupo 13. Los boruros de metales alcalinos tienden a ser ricos en boro, implicando enlaces boro-boro apreciables que involucran estructuras deltaédricas , [11] : 147-8 y son térmicamente inestables debido al álcali. metales que tienen una presión de vapor muy alta a temperaturas elevadas. Esto hace que la síntesis directa sea problemática porque los metales alcalinos no reaccionan con el boro por debajo de 700 °C y, por lo tanto, esto debe lograrse en recipientes sellados con metal alcalino en exceso. Además, excepcionalmente en este grupo, la reactividad con el boro disminuye a lo largo del grupo: el litio reacciona completamente a 700 °C, pero el sodio a 900 °C y el potasio no hasta 1200 °C, y la reacción es instantánea para el litio pero tarda horas para el potasio. Los boruros de rubidio y de cesio ni siquiera han sido caracterizados. Se conocen varias fases, como LiB 10 , NaB 6 , NaB 15 y KB 6 . [111] [112] Bajo alta presión, el enlace boro-boro en los boruros de litio cambia de seguir las reglas de Wade a formar aniones Zintl como el resto del grupo 13. [113]
El litio y el sodio reaccionan con el carbono para formar acetiluros , Li 2 C 2 y Na 2 C 2 , que también pueden obtenerse por reacción del metal con acetileno . El potasio, el rubidio y el cesio reaccionan con el grafito ; sus átomos se intercalan entre las capas de grafito hexagonal, formando compuestos de intercalación de grafito de fórmulas MC 60 (gris oscuro, casi negro), MC 48 (gris oscuro, casi negro), MC 36 (azul), MC 24 (azul acero) y MC 8 (bronce) (M = K, Rb o Cs). Estos compuestos son más de 200 veces más conductores de electricidad que el grafito puro, lo que sugiere que el electrón de valencia del metal alcalino se transfiere a las capas de grafito (por ejemplo, M + C−8). [66] Al calentar KC 8 , la eliminación de los átomos de potasio da como resultado la conversión en secuencia a KC 24 , KC 36 , KC 48 y finalmente KC 60 . KC 8 es un agente reductor muy fuerte , es pirofórico y explota al contacto con el agua. [114] [115] Mientras que los metales alcalinos más grandes (K, Rb y Cs) inicialmente forman MC 8 , los más pequeños inicialmente forman MC 6 y, de hecho, requieren la reacción de los metales con grafito a altas temperaturas alrededor de 500 °C para forma. [116] Aparte de esto, los metales alcalinos son agentes reductores tan fuertes que pueden incluso reducir el buckminsterfullereno para producir fulleruros sólidos M n C 60 ; el sodio, el potasio, el rubidio y el cesio pueden formar fulleridas donde n = 2, 3, 4 o 6, y el rubidio y el cesio adicionalmente pueden alcanzar n = 1. [11] : 285
Cuando los metales alcalinos reaccionan con los elementos más pesados del grupo del carbono ( silicio , germanio , estaño y plomo), se forman sustancias iónicas con estructuras en forma de jaula, como los siliciuros M 4 Si 4 (M = K, Rb o Cs), que contiene M + y Si tetraédrico4-4iones. [66] La química de las germanuros de metales alcalinos , que involucra el ion germanuro Ge 4− y otros iones de grupo ( Zintl ) como Ge2-4, Ge4-9, Ge2-9, y [(Ge 9 ) 2 ] 6− , es en gran medida análogo al de los siliciuros correspondientes. [11] : 393 Los estanuros de metales alcalinos son en su mayoría iónicos, a veces con el ion estanuro ( Sn 4− ), [110] y a veces con iones Zintl más complejos como el Sn.4-9, que aparece en el nonastannuro de tetrapotasio (K 4 Sn 9 ). [117] El ion monoatómico plumbide ( Pb 4− ) es desconocido y, de hecho, se predice que su formación será energéticamente desfavorable; Los plomados de metales alcalinos tienen iones complejos de Zintl, como el Pb.4-9. Estos germanuros, estanuros y plumbiuros de metales alcalinos se pueden producir reduciendo germanio, estaño y plomo con sodio metálico en amoníaco líquido. [11] : 394

El litio, el más ligero de los metales alcalinos, es el único metal alcalino que reacciona con el nitrógeno en condiciones estándar , y su nitruro es el único nitruro de metal alcalino estable. El nitrógeno es un gas no reactivo porque romper el fuerte triple enlace de la molécula de dinitrógeno (N 2 ) requiere mucha energía. La formación de un nitruro de metal alcalino consumiría la energía de ionización del metal alcalino (formando iones M + ), la energía requerida para romper el triple enlace en N 2 y la formación de iones N 3− , y toda la energía liberada del La formación de un nitruro de metal alcalino se debe a la energía reticular del nitruro de metal alcalino. La energía reticular se maximiza con iones pequeños y altamente cargados; Los metales alcalinos no forman iones altamente cargados, solo forman iones con una carga de +1, por lo que solo el litio, el metal alcalino más pequeño, puede liberar suficiente energía reticular para hacer que la reacción con el nitrógeno sea exotérmica , formando nitruro de litio . Las reacciones de los otros metales alcalinos con nitrógeno no liberarían suficiente energía reticular y, por tanto, serían endotérmicas , por lo que no forman nitruros en condiciones estándar. [85] El nitruro de sodio (Na 3 N) y el nitruro de potasio (K 3 N), aunque existen, son extremadamente inestables, propensos a descomponerse nuevamente en sus elementos constituyentes y no pueden producirse haciendo reaccionar los elementos entre sí en condiciones estándar. . [119] [120] El impedimento estérico prohíbe la existencia de rubidio o nitruro de cesio. [11] : 417 Sin embargo, el sodio y el potasio forman sales de azida incoloras que involucran el N lineal .−3anión; debido al gran tamaño de los cationes de metales alcalinos, son lo suficientemente estables térmicamente como para poder fundirse antes de descomponerse. [11] : 417
Todos los metales alcalinos reaccionan fácilmente con fósforo y arsénico para formar fosfuros y arseniuros con la fórmula M 3 Pn (donde M representa un metal alcalino y Pn representa un pnictógeno : fósforo, arsénico, antimonio o bismuto ). Esto se debe al mayor tamaño de los iones P 3− y As 3− , por lo que es necesario liberar menos energía reticular para que se formen las sales. [66] Estos no son los únicos fosfuros y arseniuros de los metales alcalinos: por ejemplo, el potasio tiene nueve fosfuros diferentes conocidos, con fórmulas K 3 P, K 4 P 3 , K 5 P 4 , KP, K 4 P 6 , K 3 P 7 , K 3 P 11 , KP 10,3 y KP 15 . [121] Si bien la mayoría de los metales forman arseniuros, sólo los metales alcalinos y alcalinotérreos forman en su mayoría arseniuros iónicos. La estructura del Na 3 As es compleja con distancias Na-Na inusualmente cortas de 328 a 330 pm, que son más cortas que en el sodio metálico, y esto indica que incluso con estos metales electropositivos el enlace no puede ser directamente iónico. [11] Se conocen otros arseniuros de metales alcalinos que no se ajustan a la fórmula M 3 As, como el LiAs, que tiene un brillo metálico y una conductividad eléctrica que indican la presencia de algún enlace metálico . [11] Los antimonuros son inestables y reactivos ya que el ion Sb 3− es un fuerte agente reductor; Al reaccionar con ácidos se forma el gas tóxico e inestable estibina (SbH 3 ). [122] De hecho, tienen algunas propiedades metálicas, y los antimonuros de metales alcalinos de estequiometría MSb implican átomos de antimonio unidos en una estructura espiral de Zintl. [123] Los bismutos ni siquiera son completamente iónicos; son compuestos intermetálicos que contienen enlaces parcialmente metálicos y parcialmente iónicos. [124]
Todos los metales alcalinos reaccionan vigorosamente con el oxígeno en condiciones estándar. Forman varios tipos de óxidos, como óxidos simples (que contienen el ion O 2− ), peróxidos (que contienen el ion O2-2ion, donde hay un enlace simple entre los dos átomos de oxígeno), superóxidos (que contienen el O−2ion), y muchos otros. El litio se quema en el aire para formar óxido de litio , pero el sodio reacciona con el oxígeno para formar una mezcla de óxido de sodio y peróxido de sodio . El potasio forma una mezcla de peróxido de potasio y superóxido de potasio , mientras que el rubidio y el cesio forman exclusivamente el superóxido. Su reactividad aumenta a medida que avanza el grupo: mientras que el litio, el sodio y el potasio simplemente arden en el aire, el rubidio y el cesio son pirofóricos (se incendian espontáneamente en el aire). [85]
Los metales alcalinos más pequeños tienden a polarizar los aniones más grandes (peróxido y superóxido) debido a su pequeño tamaño. Esto atrae los electrones de los aniones más complejos hacia uno de sus átomos de oxígeno constituyentes, formando un ion óxido y un átomo de oxígeno. Esto hace que el litio forme óxido exclusivamente al reaccionar con oxígeno a temperatura ambiente. Este efecto se vuelve drásticamente más débil para el sodio y el potasio más grandes, lo que les permite formar peróxidos menos estables. El rubidio y el cesio, situados al final del grupo, son tan grandes que incluso los superóxidos menos estables pueden formarse. Debido a que el superóxido libera la mayor cantidad de energía cuando se forma, el superóxido se forma preferentemente para los metales alcalinos más grandes donde los aniones más complejos no están polarizados. Los óxidos y peróxidos de estos metales alcalinos existen, pero no se forman por reacción directa del metal con oxígeno en condiciones estándar. [85] Además, el pequeño tamaño de los iones Li + y O 2− contribuye a que formen una estructura reticular iónica estable. Sin embargo, en condiciones controladas, se sabe que todos los metales alcalinos, con excepción del francio, forman sus óxidos, peróxidos y superóxidos. Los peróxidos y superóxidos de metales alcalinos son potentes agentes oxidantes . El peróxido de sodio y el superóxido de potasio reaccionan con el dióxido de carbono para formar carbonato de metal alcalino y oxígeno gaseoso, lo que permite su uso en purificadores de aire submarinos ; La presencia de vapor de agua , presente naturalmente en el aliento, hace que la eliminación del dióxido de carbono por el superóxido de potasio sea aún más eficaz. [66] [125] Todos los metales alcalinos estables, excepto el litio, pueden formar ozónuros rojos (MO 3 ) mediante la reacción a baja temperatura del hidróxido anhidro en polvo con ozono : los ozónuros se pueden extraer luego utilizando amoníaco líquido . Se descomponen lentamente en condiciones estándar en superóxidos y oxígeno, y se hidrolizan inmediatamente en hidróxidos cuando entran en contacto con el agua. [11] : 85 El potasio, el rubidio y el cesio también forman sesquióxidos M 2 O 3 , que pueden considerarse mejor disuperóxidos de peróxido, [(M + ) 4 (O2-2)(O−2) 2 ] . [11] : 85
El rubidio y el cesio pueden formar una gran variedad de subóxidos con metales en estados de oxidación formales inferiores a +1. [11] : 85 El rubidio puede formar Rb 6 O y Rb 9 O 2 (de color cobrizo) tras la oxidación en el aire, mientras que el cesio forma una inmensa variedad de óxidos, como el ozonuro CsO 3 [126] [127] y varios de colores brillantes. subóxidos coloreados , [128] como Cs 7 O (bronce), Cs 4 O (rojo-violeta), Cs 11 O 3 (violeta), Cs 3 O (verde oscuro), [129] CsO, Cs 3 O 2 , [130] así como Cs 7 O 2 . [131] [132] El último de ellos se puede calentar al vacío para generar Cs 2 O. [57]
Los metales alcalinos también pueden reaccionar de manera análoga con los calcógenos más pesados ( azufre , selenio , telurio y polonio ), y todos los calcogenuros de metales alcalinos son conocidos (con excepción del francio). La reacción con un exceso de calcógeno puede dar como resultado también calcogenuros inferiores, en los que los iones de calcógeno contienen cadenas de los átomos de calcógeno en cuestión. Por ejemplo, el sodio puede reaccionar con el azufre para formar el sulfuro ( Na 2 S ) y varios polisulfuros con la fórmula Na 2 S x ( x de 2 a 6), que contienen el S2-
xiones. [66] Debido a la basicidad de los iones Se 2− y Te 2− , los seleniuros y telururos de metales alcalinos son alcalinos en solución; cuando reacciona directamente con selenio y telurio, se forman poliseleniuros y politelururos de metales alcalinos junto con los seleniuros y telururos con el Se.2-
xy te2-
xiones. [133] Pueden obtenerse directamente de los elementos en el amoníaco líquido o cuando no hay aire, y son compuestos incoloros y solubles en agua que el aire oxida rápidamente de nuevo a selenio o telurio. [11] : 766 Los polonuros de metales alcalinos son todos compuestos iónicos que contienen el ion Po 2− ; son muy estables químicamente y pueden producirse mediante reacción directa de los elementos a una temperatura de entre 300 y 400 °C. [11] : 766 [134] [135]
Los metales alcalinos se encuentran entre los elementos más electropositivos de la tabla periódica y, por tanto, tienden a unirse iónicamente a los elementos más electronegativos de la tabla periódica, los halógenos ( flúor , cloro , bromo , yodo y astato ), formando sales conocidas como sales alcalinas. halogenuros metálicos. La reacción es muy vigorosa y en ocasiones puede provocar explosiones. [11] : 76 Se conocen los veinte haluros de metales alcalinos estables; los inestables no se conocen, a excepción del astatido sódico, debido a la gran inestabilidad y rareza del astato y el francio. El más conocido de los veinte es sin duda el cloruro de sodio , también conocido como sal común. Todos los haluros de metales alcalinos estables tienen la fórmula MX donde M es un metal alcalino y X es un halógeno. Todos ellos son sólidos cristalinos iónicos blancos que tienen altos puntos de fusión. [5] [85] Todos los haluros de metales alcalinos son solubles en agua, excepto el fluoruro de litio (LiF), que es insoluble en agua debido a su muy alta entalpía de red . La alta entalpía reticular del fluoruro de litio se debe a los pequeños tamaños de los iones Li + y F − , lo que hace que las interacciones electrostáticas entre ellos sean fuertes: [5] ocurre un efecto similar para el fluoruro de magnesio , consistente con la relación diagonal entre el litio y magnesio. [11] : 76
Los metales alcalinos también reaccionan de manera similar con el hidrógeno para formar hidruros iónicos de metales alcalinos, donde el anión hidruro actúa como un pseudohaluro : estos se utilizan a menudo como agentes reductores, produciendo hidruros, hidruros metálicos complejos o gas hidrógeno. [11] : 83 [66] También se conocen otros pseudohaluros, en particular los cianuros . Estos son isoestructurales a los respectivos haluros, excepto el cianuro de litio , lo que indica que los iones de cianuro pueden girar libremente. [11] : 322 También se conocen óxidos de haluros de metales alcalinos ternarios, como Na 3 ClO, K 3 BrO (amarillo), Na 4 Br 2 O, Na 4 I 2 O y K 4 Br 2 O. [11] : 83 Los polihaluros son bastante inestables, aunque los de rubidio y cesio se estabilizan en gran medida por el débil poder polarizador de estos cationes extremadamente grandes. [11] : 835
Los cationes de metales alcalinos no suelen formar complejos de coordinación con bases de Lewis simples debido a su baja carga de sólo +1 y su tamaño relativamente grande; por lo tanto, el ion Li + forma la mayoría de los complejos y los iones de metales alcalinos más pesados forman cada vez menos (aunque se producen excepciones para los complejos débiles). [11] : 90 El litio en particular tiene una química de coordinación muy rica en la que exhibe números de coordinación del 1 al 12, aunque la hexacoordinación octaédrica es su modo preferido. [11] : 90-1 En solución acuosa , los iones de metales alcalinos existen como complejos octaédricos de hexahidrato [M(H 2 O) 6 ] + , con la excepción del ion litio, que debido a su pequeño tamaño forma complejos tetraédricos de tetrahidrato [ Li( H2O ) 4 ] + ; Los metales alcalinos forman estos complejos porque sus iones son atraídos por fuerzas electrostáticas de atracción hacia las moléculas de agua polares. Debido a esto, a menudo se utilizan como desecantes sales anhidras que contienen cationes de metales alcalinos . [66] Los metales alcalinos también forman fácilmente complejos con éteres corona (por ejemplo, 12-corona-4 para Li + , 15-corona-5 para Na + , 18-corona-6 para K + y 21-corona-7 para Rb +). ) y criptandos debido a la atracción electrostática. [66]
Los metales alcalinos se disuelven lentamente en amoníaco líquido , formando soluciones amoniacales de catión metálico solvatado M + y electrón solvatado e- , que reaccionan para formar gas hidrógeno y la amida de metal alcalino (MNH 2 , donde M representa un metal alcalino): esto fue primero observado por Humphry Davy en 1809 y redescubierto por W. Weyl en 1864. El proceso puede acelerarse mediante un catalizador . Soluciones similares se forman con los metales alcalinotérreos bivalentes pesados calcio , estroncio y bario , así como con los lantánidos bivalentes , europio e iterbio . La sal de amida es bastante insoluble y precipita fácilmente fuera de la solución, dejando soluciones de amoníaco de metales alcalinos de colores intensos. En 1907, Charles A. Kraus identificó el color como debido a la presencia de electrones solvatados , que contribuyen a la alta conductividad eléctrica de estas soluciones. En concentraciones bajas (por debajo de 3 M), la solución es azul oscuro y tiene diez veces la conductividad del cloruro de sodio acuoso ; en concentraciones más altas (por encima de 3 M), la solución es de color cobrizo y tiene aproximadamente la conductividad de los metales líquidos como el mercurio . [11] [66] [137] Además de la sal de amida de metal alcalino y electrones solvatados, estas soluciones de amoníaco también contienen el catión de metal alcalino (M + ), el átomo de metal alcalino neutro (M), moléculas diatómicas de metal alcalino (M 2 ) y aniones de metales alcalinos (M − ). Estos son inestables y eventualmente se convierten en gas hidrógeno y amida de metal alcalino termodinámicamente más estables. Los electrones solvatados son potentes agentes reductores y se utilizan a menudo en síntesis química. [66]


Al ser el metal alcalino más pequeño, el litio forma la variedad más amplia y estable de compuestos organometálicos , que están unidos de forma covalente. Los compuestos de organolitio son sólidos o líquidos volátiles no conductores de electricidad que se funden a bajas temperaturas y tienden a formar oligómeros con la estructura (RLi) x donde R es el grupo orgánico. Como la naturaleza electropositiva del litio coloca la mayor parte de la densidad de carga del enlace en el átomo de carbono, creando efectivamente un carbanión , los compuestos de organolitio son bases y nucleófilos extremadamente poderosos . Para su uso como bases, a menudo se utilizan butillitios y están disponibles comercialmente. Un ejemplo de compuesto de organolitio es el metillitio ((CH 3 Li) x ), que existe en formas tetramérica ( x = 4, tetraédrica) y hexamérica ( x = 6, octaédrica). [66] [141] Los compuestos de organolitio, especialmente n -butillitio, son reactivos útiles en la síntesis orgánica, como podría esperarse dada la relación diagonal del litio con el magnesio, que juega un papel importante en la reacción de Grignard . [11] : 102 Por ejemplo, se pueden utilizar alquillitios y arillitios para sintetizar aldehídos y cetonas mediante reacción con carbonilos metálicos . La reacción con tetracarbonilo de níquel , por ejemplo, transcurre a través de un complejo acilníquelcarbonilo inestable que luego sufre sustitución electrófila para dar el producto deseado de aldehído (usando H + como electrófilo) o cetona (usando un haluro de alquilo). [11] : 105
Los alquillitios y arillitios también pueden reaccionar con amidas N , N -disustituidas para dar aldehídos y cetonas, y cetonas simétricas al reaccionar con monóxido de carbono . Se descomponen térmicamente para eliminar un β-hidrógeno, produciendo alquenos e hidruro de litio : otra vía es la reacción de los éteres con alquil- y aril-litios que actúan como bases fuertes. [11] : 105 En disolventes no polares, los arillitios reaccionan como los carbaniones que efectivamente son, convirtiendo el dióxido de carbono en ácidos carboxílicos aromáticos (ArCO 2 H) y las arilcetonas en carbinoles terciarios (Ar' 2 C(Ar)OH). Finalmente, pueden usarse para sintetizar otros compuestos organometálicos mediante intercambio metal-halógeno. [11] : 106
A diferencia de los compuestos organolitíicos, los compuestos organometálicos de los metales alcalinos más pesados son predominantemente iónicos. La aplicación de los compuestos organosódicos en química está limitada en parte debido a la competencia de los compuestos organolitíicos , que están disponibles comercialmente y exhiben una reactividad más conveniente. El principal compuesto organosódico de importancia comercial es el ciclopentadienuro de sodio . El tetrafenilborato de sodio también se puede clasificar como un compuesto organosódico ya que en estado sólido el sodio está unido a los grupos arilo. Los compuestos organometálicos de metales alcalinos superiores son incluso más reactivos que los compuestos organosódicos y de utilidad limitada. Un reactivo notable es la base de Schlosser , una mezcla de n -butillitio y terc -butóxido de potasio . Este reactivo reacciona con propeno para formar el compuesto alilpotasio (KCH 2 CHCH 2 ). cis -2-buteno y trans -2-buteno se equilibran cuando entran en contacto con metales alcalinos. Mientras que la isomerización es rápida con el litio y el sodio, es lenta con los metales alcalinos más pesados. Los metales alcalinos más pesados también favorecen la conformación estéricamente congestionada. [142] Se han informado varias estructuras cristalinas de compuestos organopotasicos, estableciendo que, al igual que los compuestos de sodio, son poliméricos. [143] Los compuestos de organosodio, organopotasio, organorrubidio y organocesio son en su mayoría iónicos y son insolubles (o casi) en disolventes no polares. [66]
Los derivados de alquilo y arilo de sodio y potasio tienden a reaccionar con el aire. Provocan la escisión de los éteres , generando alcóxidos. A diferencia de los compuestos de alquillitio, los alquilsodios y alquilpotasios no se pueden producir haciendo reaccionar los metales con haluros de alquilo porque se produce el acoplamiento de Wurtz : [123] : 265
Como tales, deben prepararse haciendo reaccionar compuestos de alquilmercurio con sodio o potasio metálico en disolventes de hidrocarburos inertes. Mientras que el metilsodio forma tetrámeros como el metillitio, el metilpotasio es más iónico y tiene la estructura de arseniuro de níquel con aniones de metilo discretos y cationes de potasio. [123] : 265
Los metales alcalinos y sus hidruros reaccionan con hidrocarburos ácidos, por ejemplo ciclopentadienos y alquinos terminales, para formar sales. Se utilizan disolventes líquidos de amoníaco, éter o hidrocarburos, siendo el más común el tetrahidrofurano . El más importante de estos compuestos es el ciclopentadienuro de sodio , NaC 5 H 5 , un precursor importante de muchos derivados de ciclopentadienilo de metales de transición. [123] : 265 De manera similar, los metales alcalinos reaccionan con ciclooctatetraeno en tetrahidrofurano para dar ciclooctatetraenuros de metales alcalinos ; por ejemplo, el ciclooctatetraenuro dipotásico (K 2 C 8 H 8 ) es un precursor importante de muchos derivados metálicos del ciclooctatetraenilo, como el uranoceno . [123] : 266 Los cationes de metales alcalinos grandes y muy débilmente polarizantes pueden estabilizar aniones radicales grandes, aromáticos y polarizables, como el naftalenuro de sodio de color verde oscuro , Na + [C 10 H 8 •] − , un fuerte agente reductor. [123] : 266
Al reaccionar con el oxígeno, los metales alcalinos forman óxidos , peróxidos , superóxidos y subóxidos . Sin embargo, los tres primeros son más comunes. La siguiente tabla [144] muestra los tipos de compuestos formados en reacción con oxígeno. El compuesto entre paréntesis representa el producto menor de la combustión.
Los peróxidos de metales alcalinos son compuestos iónicos que son inestables en agua. El anión peróxido está débilmente unido al catión y se hidroliza formando enlaces covalentes más fuertes.
Los demás compuestos de oxígeno también son inestables en el agua.
Con el azufre forman sulfuros y polisulfuros . [146]
Debido a que los sulfuros de metales alcalinos son esencialmente sales de un ácido débil y una base fuerte, forman soluciones básicas.
El litio es el único metal que se combina directamente con el nitrógeno a temperatura ambiente.
Li 3 N puede reaccionar con agua para liberar amoníaco.
Con el hidrógeno, los metales alcalinos forman hidruros salinos que se hidrolizan en agua.
El litio es el único metal que reacciona directamente con el carbono para dar acetiluro de dilitio . Na y K pueden reaccionar con acetileno para dar acetiluros . [147]
Al reaccionar con el agua, generan iones de hidróxido y gas hidrógeno . Esta reacción es vigorosa y altamente exotérmica y el hidrógeno resultante puede encenderse en el aire o incluso explotar en el caso de Rb y Cs. [144]
Los metales alcalinos son muy buenos agentes reductores. Pueden reducir cationes metálicos que son menos electropositivos. El titanio se produce industrialmente mediante la reducción de tetracloruro de titanio con Na a 400 °C ( proceso de van Arkel-de Boer ).
Los metales alcalinos reaccionan con derivados halógenos para generar hidrocarburos mediante la reacción de Wurtz .
Los metales alcalinos se disuelven en amoníaco líquido u otros disolventes donantes como aminas alifáticas o hexametilfosforamida para dar soluciones azules. Se cree que estas soluciones contienen electrones libres. [144]
Debido a la presencia de electrones solvatados , estas soluciones son agentes reductores muy potentes utilizados en síntesis orgánica.

La reacción 1) se conoce como reducción de Birch . Otras reducciones [144] que pueden lograrse con estas soluciones son:

Aunque el francio es el metal alcalino más pesado que se ha descubierto, ha habido algunos trabajos teóricos que predicen las características físicas y químicas de hipotéticos metales alcalinos más pesados. Siendo el elemento del primer período 8 , se predice que el elemento no descubierto ununennium (elemento 119) será el siguiente metal alcalino después del francio y se comportará de manera muy similar a sus congéneres más ligeros ; sin embargo, también se prevé que difiera de los metales alcalinos más ligeros en algunas propiedades. [37] : 1729-1730 Se predice que su química será más cercana a la del potasio [42] o el rubidio [37] : 1729-1730 en lugar de cesio o francio. Esto es inusual ya que las tendencias periódicas , ignorando los efectos relativistas, predecirían que ununennium sería incluso más reactivo que el cesio y el francio. Esta reactividad reducida se debe a la estabilización relativista del electrón de valencia de ununennium, aumentando la primera energía de ionización de ununennium y disminuyendo los radios metálicos e iónicos ; [42] este efecto ya se observa en el caso del francio. [37] : 1729-1730 Esto supone que el ununennium se comportará químicamente como un metal alcalino, lo que, aunque probable, puede no ser cierto debido a efectos relativistas. [149] La estabilización relativista del orbital 8s también aumenta la afinidad electrónica del ununennium mucho más allá de la del cesio y el francio; de hecho, se espera que el ununennium tenga una afinidad electrónica mayor que la de todos los metales alcalinos más ligeros que él. Los efectos relativistas también provocan una caída muy grande en la polarizabilidad del ununennium. [37] : 1729–1730 Por otro lado, se predice que ununennium continuará la tendencia de disminución de los puntos de fusión a lo largo del grupo, y se espera que tenga un punto de fusión entre 0 °C y 30 °C. [37] : 1724

La estabilización del electrón de valencia del ununennio y, por tanto, la contracción del orbital 8s hacen que su radio atómico se reduzca a 240 pm , [37] : 1729-1730 muy cercano al del rubidio (247 pm), [5] de modo que la química del ununennio en el estado de oxidación +1 debería ser más similar a la química del rubidio que a la del francio. Por otro lado, se predice que el radio iónico del ion Uue + será mayor que el de Rb + , porque los orbitales 7p están desestabilizados y, por tanto, son más grandes que los orbitales p de las capas inferiores. Ununennium también puede mostrar los estados de oxidación +3 [37] : 1729–1730 y +5 , [150] que no se observan en ningún otro metal alcalino, [11] : 28, además del estado de oxidación +1 que es característico de los otros metales alcalinos y también es el principal estado de oxidación de todos los metales alcalinos conocidos: esto se debe a la desestabilización y expansión del espinor 7p 3/2 , lo que hace que sus electrones más externos tengan una energía de ionización menor de lo que se esperaría de otro modo. . [11] : 28 [37] : 1729–1730 De hecho, se espera que muchos compuestos ununennium tengan un gran carácter covalente , debido a la participación de los electrones 7p 3/2 en el enlace. [87]
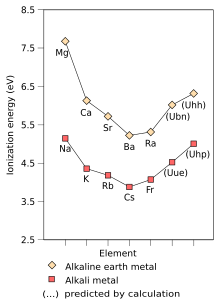
No se ha realizado tanto trabajo para predecir las propiedades de los metales alcalinos más allá del año pasado. Aunque una simple extrapolación de la tabla periódica (según el principio de Aufbau ) colocaría al elemento 169, unhexennio, debajo del ununennio, los cálculos de Dirac-Fock predicen que el siguiente elemento después del ununenio con propiedades similares a las de los metales alcalinos puede ser el elemento 165, unhexpentio, que Se predice que tendrá la configuración electrónica [Og] 5g 18 6f 14 7d 10 8s 2 8p 1/2 2 9s 1 . [37] : 1729-1730 [148] Este elemento tendría propiedades intermedias entre un metal alcalino y un elemento del grupo 11 , y si bien sus propiedades físicas y atómicas estarían más cerca del primero, su química puede estar más cerca de la del último. Otros cálculos muestran que el unhexpentium seguiría la tendencia de aumentar la energía de ionización más allá del cesio, teniendo una energía de ionización comparable a la del sodio, y que también debería continuar la tendencia de disminución de los radios atómicos más allá del cesio, teniendo un radio atómico comparable al del potasio. . [37] : 1729-1730 Sin embargo, los electrones 7d del unhexpentium también pueden participar en reacciones químicas junto con el electrón 9s, posiblemente permitiendo estados de oxidación más allá de +1, de ahí el probable comportamiento del unhexpentium como metal de transición. [37] : 1732–1733 [151] Debido a que los metales alcalinos y alcalinotérreos son elementos del bloque s , estas predicciones para las tendencias y propiedades de ununennium y unhexpentium también son en su mayoría bastante similares para los correspondientes metales alcalinotérreos unbinilium (Ubn ) y unhexhexium (Uhh). [37] : 1729-1733 Unseptrium, elemento 173, puede ser un homólogo aún mejor y más pesado de ununennium; con una configuración electrónica prevista de [Usb] 6g 1 , vuelve a la situación similar a la de un metal alcalino en la que tiene un electrón fácilmente eliminado muy por encima de una capa p cerrada en energía, y se espera que sea incluso más reactivo que el cesio. [152] [153]
Las probables propiedades de otros metales alcalinos más allá del unseptrium aún no se han explorado en 2019, y es posible que existan o no. [148] En los períodos 8 y superiores de la tabla periódica, los efectos relativistas y de estructura de capa se vuelven tan fuertes que las extrapolaciones de congéneres más ligeros se vuelven completamente inexactas. Además, los efectos relativistas y de estructura de capa (que estabilizan los orbitales s y desestabilizan y expanden los orbitales d, f y g de capas superiores) tienen efectos opuestos, causando una diferencia aún mayor entre relativistas y no relativistas. cálculos de las propiedades de elementos con números atómicos tan altos. [37] : 1732–1733 El interés en las propiedades químicas de ununennium, unhexpentium y unseptrium surge del hecho de que están ubicados cerca de las ubicaciones esperadas de las islas de estabilidad , centradas en los elementos 122 ( 306 Ubb) y 164 ( 482 Uhq). ). [154] [155] [156]
Muchas otras sustancias son similares a los metales alcalinos en su tendencia a formar cationes monopositivos. De manera análoga a los pseudohalógenos , a veces se les ha llamado "metales pseudoalcalinos". Estas sustancias incluyen algunos elementos y muchos más iones poliatómicos ; Los iones poliatómicos son especialmente similares a los metales alcalinos por su gran tamaño y su débil poder polarizador. [157]
El elemento hidrógeno , con un electrón por átomo neutro, suele situarse en la parte superior del Grupo 1 de la tabla periódica debido a su configuración electrónica. Pero normalmente no se considera que el hidrógeno sea un metal alcalino. [158] El hidrógeno metálico , que sólo existe a presiones muy altas, es conocido por sus propiedades eléctricas y magnéticas, no por sus propiedades químicas. [159] En condiciones típicas, el hidrógeno puro existe como un gas diatómico que consta de dos átomos por molécula (H 2 ); [160] sin embargo, los metales alcalinos forman moléculas diatómicas (como el dilitio , Li 2 ) sólo a altas temperaturas, cuando están en estado gaseoso. [161]
El hidrógeno, como los metales alcalinos, tiene un electrón de valencia [123] y reacciona fácilmente con los halógenos , [123] pero las similitudes en su mayoría terminan ahí debido al pequeño tamaño de un protón H + desnudo en comparación con los cationes de metales alcalinos. [123] Su ubicación por encima del litio se debe principalmente a su configuración electrónica . [158] A veces se coloca por encima del flúor debido a sus propiedades químicas similares, aunque el parecido tampoco es absoluto. [162]
La primera energía de ionización del hidrógeno (1312,0 kJ/mol ) es mucho mayor que la de los metales alcalinos. [163] [164] Como solo se requiere un electrón adicional para llenar la capa más externa del átomo de hidrógeno, el hidrógeno a menudo se comporta como un halógeno, formando el ion hidruro negativo , y muy ocasionalmente se lo considera un halógeno sobre esa base. (Los metales alcalinos también pueden formar iones negativos, conocidos como alcaluros , pero estos son poco más que curiosidades de laboratorio, ya que son inestables). [80] [81] Un argumento en contra de esta ubicación es que la formación de hidruro a partir de hidrógeno es endotérmica, a diferencia de la Formación exotérmica de haluros a partir de halógenos. El radio del anión H − tampoco se ajusta a la tendencia de aumento de tamaño que disminuye con los halógenos: de hecho, H − es muy difuso porque su único protón no puede controlar fácilmente ambos electrones. [123] : 15-6 Durante algún tiempo se esperaba que el hidrógeno líquido mostrara propiedades metálicas; [162] si bien se ha demostrado que este no es el caso, bajo presiones extremadamente altas , como las que se encuentran en los núcleos de Júpiter y Saturno , el hidrógeno se vuelve metálico y se comporta como un metal alcalino; en esta fase se le conoce como hidrógeno metálico . [165] La resistividad eléctrica del hidrógeno metálico líquido a 3000 K es aproximadamente igual a la del rubidio y cesio líquidos a 2000 K a las presiones respectivas cuando experimentan una transición de no metal a metal. [166]
La configuración electrónica 1s 1 del hidrógeno, aunque análoga a la de los metales alcalinos (ns 1 ), es única porque no existe una subcapa 1p. Por lo tanto, puede perder un electrón para formar el hidrón H + , o ganar uno para formar el ion hidruro H- . [11] : 43 En el primer caso se parece superficialmente a los metales alcalinos; en el último caso, los halógenos, pero las diferencias debidas a la falta de una subcapa 1p son lo suficientemente importantes como para que ninguno de los grupos se ajuste bien a las propiedades del hidrógeno. [11] : 43 El grupo 14 también encaja bien en términos de propiedades termodinámicas como la energía de ionización y la afinidad electrónica , pero el hidrógeno no puede ser tetravalente. Por lo tanto, ninguna de las tres ubicaciones es completamente satisfactoria, aunque el grupo 1 es la ubicación más común (si se elige una) debido a la configuración electrónica y al hecho de que el hidrón es, con mucho, la más importante de todas las especies monoatómicas de hidrógeno, siendo la base. de la química ácido-base. [162] Como ejemplo de las propiedades poco ortodoxas del hidrógeno que se derivan de su configuración electrónica inusual y su pequeño tamaño, el ion hidrógeno es muy pequeño (radio de alrededor de 150 fm en comparación con el tamaño de 50 a 220 pm de la mayoría de los otros átomos e iones) y, por lo tanto, es inexistente. en sistemas condensados que no estén asociados con otros átomos o moléculas. De hecho, la transferencia de protones entre sustancias químicas es la base de la química ácido-base . [11] : 43 También es única la capacidad del hidrógeno para formar enlaces de hidrógeno , que son un efecto de los fenómenos contribuyentes de transferencia de carga, electrostáticos y correlativos de electrones. [162] Si bien también se conocen enlaces de litio análogos, en su mayoría son electrostáticos. [162] Sin embargo, el hidrógeno puede asumir el mismo papel estructural que los metales alcalinos en algunos cristales moleculares y tiene una estrecha relación con los metales alcalinos más ligeros (especialmente el litio). [167]

El ion amonio ( NH+4) tiene propiedades muy similares a los metales alcalinos más pesados, actuando como un metal alcalino intermedio entre el potasio y el rubidio, [157] [168] [169] y a menudo se considera un pariente cercano. [170] [171] [172] Por ejemplo, la mayoría de las sales de metales alcalinos son solubles en agua, una propiedad que comparten las sales de amonio. [173] Se espera que el amonio se comporte estable como metal ( NH+4iones en un mar de electrones deslocalizados) a presiones muy altas (aunque menos que la presión típica donde ocurren las transiciones del comportamiento aislante al metálico alrededor de 100 GPa ), y posiblemente podría ocurrir dentro de los gigantes de hielo Urano y Neptuno , lo que puede tener impactos significativos. en sus campos magnéticos interiores. [171] [172] Se ha estimado que la transición de una mezcla de moléculas de amoníaco y dihidrógeno a amonio metálico puede ocurrir a presiones justo por debajo de 25 GPa. [171] En condiciones estándar, el amonio puede formar una amalgama metálica con el mercurio. [174]
Otros "metales pseudoalcalinos" incluyen los cationes alquilamonio , en los que algunos de los átomos de hidrógeno del catión amonio se reemplazan por grupos alquilo o arilo. En particular, los cationes de amonio cuaternario ( NR+4) son muy útiles ya que están cargados permanentemente y a menudo se utilizan como alternativa al costoso Cs + para estabilizar aniones muy grandes y muy fácilmente polarizables como el HI.−2. [11] : 812–9 Los hidróxidos de tetraalquilamonio, al igual que los hidróxidos de metales alcalinos, son bases muy fuertes que reaccionan con el dióxido de carbono atmosférico para formar carbonatos. [123] : 256 Además, el átomo de nitrógeno puede ser reemplazado por un átomo de fósforo, arsénico o antimonio (los pnictógenos no metálicos más pesados ), creando un fosfonio ( PH+4) o arsonio ( Ceniza+4) catión que a su vez puede sustituirse de manera similar; mientras que el estibonio ( SbH+4) en sí no se conoce, se caracterizan algunos de sus derivados orgánicos. [157]
El cobaltoceno , Co(C 5 H 5 ) 2 , es un metaloceno , el análogo del cobalto del ferroceno . Es un sólido de color púrpura oscuro. El cobaltoceno tiene 19 electrones de valencia, uno más de los que se encuentran habitualmente en los complejos de metales de organotransición, como su pariente muy estable, el ferroceno, de acuerdo con la regla de los 18 electrones . Este electrón adicional ocupa un orbital que es antienlazante con respecto a los enlaces Co-C. En consecuencia, muchas reacciones químicas del Co(C 5 H 5 ) 2 se caracterizan por su tendencia a perder este electrón "extra", produciendo un catión muy estable de 18 electrones conocido como cobaltocenio. Muchas sales de cobaltocenio coprecipitan con sales de cesio y el hidróxido de cobaltocenio es una base fuerte que absorbe el dióxido de carbono atmosférico para formar carbonato de cobaltocenio. [123] : 256 Al igual que los metales alcalinos, el cobaltoceno es un fuerte agente reductor y el decametilcobaltoceno es aún más fuerte debido al efecto inductivo combinado de los diez grupos metilo. [175] El cobalto puede sustituirse por su congénere más pesado rodio para dar rodoceno , un agente reductor aún más fuerte. [176] El iridoceno (que involucra iridio ) sería presumiblemente aún más potente, pero no está muy bien estudiado debido a su inestabilidad. [177]

El talio es el elemento estable más pesado del grupo 13 de la tabla periódica. En la parte inferior de la tabla periódica, el efecto del par inerte es bastante fuerte, debido a la estabilización relativista del orbital 6s y a la disminución de la energía del enlace a medida que los átomos aumentan de tamaño, de modo que la cantidad de energía liberada al formar dos enlaces más es No vale la pena las altas energías de ionización de los electrones 6s. [11] : 226–7 Muestra el estado de oxidación +1 [11] : 28 que muestran todos los metales alcalinos conocidos, [11] : 28 y los compuestos de talio con talio en su estado de oxidación +1 se parecen mucho al correspondiente potasio o plata. compuestos estequiométricamente debido a los radios iónicos similares de los iones Tl + (164 pm ), K + (152 pm) y Ag + (129 pm). [178] [179] A veces se lo consideraba un metal alcalino en Europa continental (pero no en Inglaterra) en los años inmediatamente posteriores a su descubrimiento, [179] : 126 y se colocó justo después del cesio como el sexto metal alcalino en Dmitri Mendeleev ' Tabla periódica de 1869 y tabla periódica de Julius Lothar Meyer de 1868. [22] La tabla periódica de Mendeleev de 1871 y la tabla periódica de Meyer de 1870 colocaron al talio en su posición actual en el grupo del boro y dejaron en blanco el espacio debajo del cesio. [22] Sin embargo, el talio también muestra el estado de oxidación +3, [11] : 28 que ningún metal alcalino conocido muestra [11] : 28 (aunque se predice que ununennium, el séptimo metal alcalino no descubierto, posiblemente muestre el estado de oxidación +3 ). [37] : 1729-1730 Actualmente se considera que el sexto metal alcalino es el francio. [180] Si bien el Tl + se estabiliza mediante el efecto del par inerte, este par inerte de electrones 6s todavía puede participar químicamente, de modo que estos electrones son estereoquímicamente activos en solución acuosa. Además, los haluros de talio (excepto el TlF ) son bastante insolubles en agua y el TlI tiene una estructura inusual debido a la presencia del par inerte estereoquímicamente activo en el talio. [181]
Los metales del grupo 11 (o metales acuñables), cobre, plata y oro, normalmente se clasifican como metales de transición dado que pueden formar iones con capas d incompletas. Físicamente, tienen puntos de fusión relativamente bajos y altos valores de electronegatividad asociados con los metales posteriores a la transición . "La subcapa d llena y el electrón s libre de Cu, Ag y Au contribuyen a su alta conductividad eléctrica y térmica. Los metales de transición a la izquierda del grupo 11 experimentan interacciones entre los electrones s y la subcapa d parcialmente llena que reduce la movilidad de los electrones". [182] Químicamente, los metales del grupo 11 se comportan como metales del grupo principal en sus estados de valencia +1 y, por lo tanto, están algo relacionados con los metales alcalinos: esta es una de las razones por las que anteriormente se los etiquetaba como "grupo IB", en paralelo con los metales alcalinos. "grupo IA" de metales. Ocasionalmente se clasifican como metales post-transición. [183] Sus espectros son análogos a los de los metales alcalinos. [30] Sus iones monopositivos son paramagnéticos y no aportan color a sus sales, como las de los metales alcalinos. [184]
En la tabla periódica de Mendeleev de 1871, el cobre, la plata y el oro aparecen dos veces, una vez en el grupo VIII (con la tríada del hierro y los metales del grupo del platino ) y otra en el grupo IB. No obstante, se puso entre paréntesis al Grupo IB para señalar que era provisional. El criterio principal de Mendeleev para la asignación de grupos era el estado de oxidación máximo de un elemento: sobre esa base, los elementos del grupo 11 no podían clasificarse en el grupo IB, debido a que en ese momento se conocía la existencia de compuestos de cobre (II) y oro (III). tiempo. [30] Sin embargo, eliminar el grupo IB convertiría al grupo I en el único grupo principal (el grupo VIII fue etiquetado como grupo de transición) que carece de una bifurcación A-B. [30] Poco después, la mayoría de los químicos optaron por clasificar estos elementos en el grupo IB y eliminarlos del grupo VIII por la simetría resultante: esta fue la clasificación predominante hasta el surgimiento de la moderna tabla periódica de 18 columnas, de longitud media y media, que Separaron los metales alcalinos y los metales del grupo 11. [30]
Los metales acuñados se consideraban tradicionalmente como una subdivisión del grupo de los metales alcalinos, debido a que comparten la configuración electrónica s 1 característica de los metales alcalinos (grupo 1: p 6 s 1 ; grupo 11: d 10 s 1 ). Sin embargo, las similitudes se limitan en gran medida a las estequiometrías de los compuestos +1 de ambos grupos, y no a sus propiedades químicas. [11] : 1177 Esto se debe a que la subcapa d llena proporciona un efecto de blindaje mucho más débil en el electrón s más externo que la subcapa p llena, de modo que los metales acuñados tienen primeras energías de ionización mucho más altas y radios iónicos más pequeños que los metales alcalinos correspondientes. . [11] : 1177 Además, tienen mayores puntos de fusión, durezas y densidades, y menores reactividades y solubilidades en amoníaco líquido , además de tener más carácter covalente en sus compuestos. [11] : 1177 Finalmente, los metales alcalinos están en la parte superior de la serie electroquímica , mientras que los metales acuñados están casi en la parte inferior. [11] : 1177 La capa d llena de los metales acuñados se rompe mucho más fácilmente que la capa p llena de los metales alcalinos, de modo que la segunda y tercera energías de ionización son más bajas, lo que permite estados de oxidación más altos que +1 y una química de coordinación más rica. dando así a los metales del grupo 11 un claro carácter de metal de transición . [11] : 1177 Particularmente digno de mención es el oro que forma compuestos iónicos con rubidio y cesio, en los que forma el ion aurido (Au − ), que también se presenta en forma solvatada en solución de amoníaco líquido: aquí el oro se comporta como un pseudohalógeno porque su 5d 10 6s La configuración 1 tiene un electrón menos que la configuración de capa casi cerrada 5d 10 6s 2 de mercurio . [11] : 1177
La producción de metales alcalinos puros es algo complicada debido a su extrema reactividad con sustancias de uso común, como el agua. [5] [66] De sus minerales de silicato , todos los metales alcalinos estables se pueden obtener de la misma manera: primero se usa ácido sulfúrico para disolver el ion de metal alcalino deseado y los iones de aluminio (III) del mineral (lixiviación), después de lo cual los metales básicos La precipitación elimina los iones de aluminio de la mezcla precipitándolos como hidróxido . A continuación se precipita selectivamente el carbonato de metal alcalino insoluble restante ; Luego, la sal se disuelve en ácido clorhídrico para producir el cloruro. A continuación se deja evaporar el resultado y se puede aislar el metal alcalino. [66] El litio y el sodio generalmente se aíslan mediante electrólisis de sus cloruros líquidos, y generalmente se agrega cloruro de calcio para reducir el punto de fusión de la mezcla. Sin embargo, los metales alcalinos más pesados se aíslan más típicamente de una manera diferente, donde se usa un agente reductor (típicamente sodio para potasio y magnesio o calcio para los metales alcalinos más pesados) para reducir el cloruro del metal alcalino. El producto líquido o gaseoso (el metal alcalino) se somete luego a una destilación fraccionada para su purificación. [66] La mayoría de las rutas hacia los metales alcalinos puros requieren el uso de electrólisis debido a su alta reactividad; uno de los pocos que no lo hace es la pirólisis de la correspondiente azida de metal alcalino , que produce el metal para sodio, potasio, rubidio y cesio y el nitruro para litio. [123] : 77
Las sales de litio deben extraerse del agua de manantiales minerales , charcas de salmuera y depósitos de salmuera. El metal se produce electrolíticamente a partir de una mezcla de cloruro de litio y cloruro de potasio fundidos . [185]
El sodio se encuentra principalmente en el agua de mar y en los fondos marinos secos , [5] pero ahora se produce mediante electrólisis del cloruro de sodio reduciendo el punto de fusión de la sustancia por debajo de 700 °C mediante el uso de una celda de Downs . [186] [187] Se puede producir sodio extremadamente puro mediante la descomposición térmica de la azida de sodio . [188] El potasio se encuentra en muchos minerales, como la silvita ( cloruro de potasio ). [5] Anteriormente, el potasio se obtenía generalmente a partir de la electrólisis del cloruro de potasio o del hidróxido de potasio , [189] que se encuentra ampliamente en lugares como Canadá, Rusia, Bielorrusia, Alemania, Israel, Estados Unidos y Jordania, en un método similar a cómo El sodio se produjo a finales del siglo XIX y principios del XX. [190] También se puede producir a partir de agua de mar . [5] Sin embargo, estos métodos son problemáticos porque el potasio metálico tiende a disolverse en su cloruro fundido y se vaporiza significativamente a las temperaturas de funcionamiento, formando potencialmente el superóxido explosivo. Como resultado, ahora se produce potasio metálico puro reduciendo el cloruro de potasio fundido con sodio metálico a 850 °C. [11] : 74
Aunque el sodio es menos reactivo que el potasio, este proceso funciona porque a temperaturas tan altas el potasio es más volátil que el sodio y puede destilarse fácilmente, de modo que el equilibrio se desplaza hacia la derecha para producir más potasio gaseoso y continúa casi hasta completarse. [11] : 74
Los metales como el sodio se obtienen por electrólisis de sales fundidas. Rb y C se obtienen principalmente como subproductos del procesamiento de Li. Para producir cesio puro, los minerales de cesio y rubidio se trituran y se calientan a 650 °C con sodio metálico, generando una aleación que luego se puede separar mediante una técnica de destilación fraccionada . Debido a que el cesio metálico es demasiado reactivo para manipularlo, normalmente se ofrece como azida de cesio (CsN3). El hidróxido de cesio se forma cuando el cesio interactúa agresivamente con el agua y el hielo (CsOH). [191]
El rubidio es el decimosexto elemento más abundante en la corteza terrestre; sin embargo, es bastante raro. Algunos minerales que se encuentran en América del Norte, Sudáfrica, Rusia y Canadá contienen rubidio. Algunos minerales potásicos ( lepidolitas , biotitas , feldespato , carnalita ) lo contienen, junto con el cesio. La polucita , la carnalita , la leucita y la lepidolita son todos minerales que contienen rubidio. Como subproducto de la extracción del litio, se obtiene comercialmente a partir de la lepidolita . El rubidio también se encuentra en rocas y salmueras de potasio , que es un suministro comercial. La mayor parte del rubidio se obtiene actualmente como subproducto del refinado del litio. El rubidio se utiliza en tubos de vacío como captador , un material que se combina con los gases traza de los tubos de vacío y los elimina. [192] [193]

Durante varios años, en las décadas de 1950 y 1960, un subproducto de la producción de potasio llamado Alkarb fue la principal fuente de rubidio. Alkarb contenía un 21% de rubidio, mientras que el resto era potasio y una pequeña fracción de cesio. [194] Hoy en día, los mayores productores de cesio, por ejemplo la mina Tanco en Manitoba, Canadá, producen rubidio como subproducto de la polucita . [195] Hoy en día, un método común para separar el rubidio del potasio y el cesio es la cristalización fraccionada de alumbre de rubidio y cesio ( Cs , Rb ) Al ( SO 4 ) 2 ·12 H 2 O , que produce alumbre de rubidio puro después de aproximadamente 30 recristalizaciones. [195] [196] Las aplicaciones limitadas y la falta de un mineral rico en rubidio limitan la producción de compuestos de rubidio a 2 a 4 toneladas por año. [195] Sin embargo, el cesio no se produce a partir de la reacción anterior. En cambio, la extracción de mineral de polucita es el método principal para obtener cesio puro, extraído del mineral principalmente mediante tres métodos: digestión ácida, descomposición alcalina y reducción directa. [195] [197] Ambos metales se producen como subproductos de la producción de litio: después de 1958, cuando el interés en las propiedades termonucleares del litio aumentó considerablemente, la producción de rubidio y cesio también aumentó en consecuencia. [11] : 71 Los metales puros de rubidio y cesio se producen reduciendo sus cloruros con calcio metálico a 750 °C y baja presión. [11] : 74
Como resultado de su extrema rareza en la naturaleza, [63] la mayor parte del francio se sintetiza en la reacción nuclear 197 Au + 18 O → 210 Fr + 5 n , produciendo francio-209 , francio-210 y francio-211 . [198] La mayor cantidad de francio jamás reunida hasta la fecha es de unos 300.000 átomos neutros, [199] que se sintetizaron mediante la reacción nuclear indicada anteriormente. [199] Cuando se requiere específicamente el único isótopo natural francio-223, se produce como hijo alfa del actinio-227, que a su vez se produce sintéticamente a partir de la irradiación de neutrones del radio natural-226, uno de los hijos del uranio natural-238. [200]
El litio, el sodio y el potasio tienen muchas aplicaciones útiles, mientras que el rubidio y el cesio son muy notables en contextos académicos pero aún no tienen muchas aplicaciones. [11] : 68 El litio es el ingrediente clave de una variedad de baterías a base de litio , y el óxido de litio puede ayudar a procesar la sílice. El estearato de litio es un espesante y puede usarse para fabricar grasas lubricantes; se produce a partir de hidróxido de litio, que también se utiliza para absorber dióxido de carbono en cápsulas espaciales y submarinos. [11] : 70 El cloruro de litio se utiliza como aleación para soldadura fuerte de piezas de aluminio. [201] En medicina, algunas sales de litio se utilizan como productos farmacéuticos estabilizadores del estado de ánimo. El litio metálico se utiliza en aleaciones con magnesio y aluminio para obtener aleaciones muy resistentes y ligeras. [11] : 70
Los compuestos de sodio tienen muchas aplicaciones, siendo la más conocida el cloruro de sodio como sal de mesa . Las sales sódicas de ácidos grasos se utilizan como jabón. [202] El metal de sodio puro también tiene muchas aplicaciones, incluido el uso en lámparas de vapor de sodio , que producen una luz muy eficiente en comparación con otros tipos de iluminación, [203] [204] y pueden ayudar a suavizar la superficie de otros metales. [205] [206] Al ser un agente reductor fuerte, a menudo se usa para reducir muchos otros metales, como el titanio y el circonio , a partir de sus cloruros. Además, es muy útil como líquido de intercambio de calor en reactores nucleares reproductores rápidos debido a su bajo punto de fusión, viscosidad y sección transversal hacia la absorción de neutrones. [11] : 74 Las baterías de iones de sodio pueden proporcionar alternativas más económicas a sus celdas equivalentes de litio. Tanto el sodio como el potasio se utilizan comúnmente como contraiones GRAS para crear formas salinas de productos farmacéuticos ácidos más solubles en agua y, por lo tanto, más biodisponibles. [207]
Los compuestos de potasio se utilizan a menudo como fertilizantes [11] : 73 [208] ya que el potasio es un elemento importante para la nutrición de las plantas. El hidróxido de potasio es una base muy fuerte y se utiliza para controlar el pH de diversas sustancias. [209] [210] El nitrato de potasio y el permanganato de potasio se utilizan a menudo como potentes agentes oxidantes. [11] : 73 El superóxido de potasio se utiliza en máscaras respiratorias, ya que reacciona con el dióxido de carbono para producir carbonato de potasio y oxígeno gaseoso. El potasio metálico puro no se utiliza con frecuencia, pero sus aleaciones con sodio pueden sustituir al sodio puro en reactores nucleares reproductores rápidos. [11] : 74
El rubidio y el cesio se utilizan a menudo en los relojes atómicos . [211] Los relojes atómicos de cesio son extraordinariamente precisos; Si se hubiera construido un reloj en la época de los dinosaurios, se habría retrasado menos de cuatro segundos (después de 80 millones de años). [57] Por esa razón, los átomos de cesio se utilizan como definición del segundo. [212] Los iones de rubidio se utilizan a menudo en fuegos artificiales de color púrpura , [213] y el cesio se utiliza a menudo en fluidos de perforación en la industria petrolera. [57] [214]
El francio no tiene aplicaciones comerciales, [61] [62] [215] pero debido a la estructura atómica relativamente simple del francio , entre otras cosas, se ha utilizado en experimentos de espectroscopia , lo que ha permitido obtener más información sobre los niveles de energía y las constantes de acoplamiento entre partículas subatómicas. . [216] Los estudios sobre la luz emitida por iones de francio-210 atrapados con láser han proporcionado datos precisos sobre las transiciones entre niveles de energía atómica, similares a los predichos por la teoría cuántica . [217]
Los metales alcalinos puros reaccionan peligrosamente con el aire y el agua y deben mantenerse alejados del calor, el fuego, agentes oxidantes, ácidos, la mayoría de los compuestos orgánicos, halocarbonos , plásticos y humedad. También reaccionan con el dióxido de carbono y el tetracloruro de carbono, por lo que los extintores normales son contraproducentes cuando se utilizan en incendios de metales alcalinos. [218] Algunos extintores de polvo seco de Clase D diseñados para incendios de metales son eficaces, ya que privan al fuego de oxígeno y enfrían el metal alcalino. [219]
Los experimentos generalmente se llevan a cabo utilizando sólo pequeñas cantidades de unos pocos gramos en una campana extractora . Se pueden eliminar pequeñas cantidades de litio mediante reacción con agua fría, pero los metales alcalinos más pesados deben disolverse en el isopropanol menos reactivo . [218] [220] Los metales alcalinos deben almacenarse bajo aceite mineral o en atmósfera inerte. La atmósfera inerte utilizada puede ser argón o nitrógeno gaseoso, excepto el litio, que reacciona con el nitrógeno. [218] El rubidio y el cesio deben mantenerse alejados del aire, incluso bajo petróleo, porque incluso una pequeña cantidad de aire difundida en el petróleo puede provocar la formación del peróxido peligrosamente explosivo; Por la misma razón, el potasio no debe almacenarse bajo aceite en una atmósfera que contenga oxígeno durante más de 6 meses. [221] [222]

Se ha revisado exhaustivamente la química bioinorgánica de los iones de metales alcalinos. [223] Se han determinado estructuras cristalinas en estado sólido para muchos complejos de iones de metales alcalinos en pequeños péptidos, constituyentes de ácidos nucleicos, carbohidratos y complejos de ionóforos. [224]
El litio naturalmente sólo se encuentra en trazas en los sistemas biológicos y no tiene ningún papel biológico conocido, pero tiene efectos en el cuerpo cuando se ingiere. [225] El carbonato de litio se utiliza como estabilizador del estado de ánimo en psiquiatría para tratar el trastorno bipolar ( maníaco-depresivo ) en dosis diarias de aproximadamente 0,5 a 2 gramos, aunque existen efectos secundarios. [225] La ingestión excesiva de litio causa somnolencia, dificultad para hablar y vómitos, entre otros síntomas, [225] y envenena el sistema nervioso central , [225] lo cual es peligroso ya que la dosis requerida de litio para tratar el trastorno bipolar es sólo ligeramente inferior a la la dosis tóxica. [225] [226] Su bioquímica, la forma en que lo maneja el cuerpo humano y los estudios con ratas y cabras sugieren que es un oligoelemento esencial , aunque la función biológica natural del litio en los humanos aún no se ha identificado. [227] [228]
El sodio y el potasio se encuentran en todos los sistemas biológicos conocidos y generalmente funcionan como electrolitos dentro y fuera de las células . [229] [230] El sodio es un nutriente esencial que regula el volumen sanguíneo, la presión arterial, el equilibrio osmótico y el pH ; El requerimiento fisiológico mínimo de sodio es de 500 miligramos por día. [231] El cloruro de sodio (también conocido como sal común) es la principal fuente de sodio en la dieta y se utiliza como condimento y conservante, por ejemplo para encurtidos y cecina ; la mayor parte proviene de alimentos procesados. [232] La ingesta dietética de referencia de sodio es de 1,5 gramos por día, [233] pero la mayoría de las personas en los Estados Unidos consumen más de 2,3 gramos por día, [234] la cantidad mínima que promueve la hipertensión; [235] esto a su vez causa 7,6 millones de muertes prematuras en todo el mundo. [236]
El potasio es el catión principal (ion positivo) dentro de las células animales , [229] mientras que el sodio es el catión principal fuera de las células animales. [229] [230] Las diferencias de concentración de estas partículas cargadas provocan una diferencia de potencial eléctrico entre el interior y el exterior de las células, conocida como potencial de membrana . El equilibrio entre potasio y sodio se mantiene mediante proteínas transportadoras de iones en la membrana celular . [237] El potencial de membrana celular creado por los iones de potasio y sodio permite que la célula genere un potencial de acción , un "pico" de descarga eléctrica. La capacidad de las células para producir descargas eléctricas es fundamental para funciones corporales como la neurotransmisión , la contracción muscular y la función cardíaca. [237] Por lo tanto, la alteración de este equilibrio puede ser fatal: por ejemplo, la ingestión de grandes cantidades de compuestos de potasio puede provocar hiperpotasemia que influye fuertemente en el sistema cardiovascular. [238] [239] El cloruro de potasio se utiliza en los Estados Unidos para ejecuciones por inyección letal . [238]

Debido a sus radios atómicos similares, el rubidio y el cesio en el cuerpo imitan al potasio y se absorben de manera similar. El rubidio no tiene ningún papel biológico conocido, pero puede ayudar a estimular el metabolismo , [240] [241] [242] y, de manera similar al cesio, [240] [243] reemplazar el potasio en el cuerpo que causa la deficiencia de potasio . [240] [242] La sustitución parcial es bastante posible y bastante no tóxica: una persona de 70 kg contiene en promedio 0,36 g de rubidio, y un aumento de este valor de 50 a 100 veces no mostró efectos negativos en las personas de prueba. [244] Las ratas pueden sobrevivir hasta un 50% de sustitución de potasio por rubidio. [242] [245] El rubidio (y en mucha menor medida el cesio) puede funcionar como cura temporal para la hipopotasemia; Si bien el rubidio puede sustituir fisiológicamente al potasio en algunos sistemas, el cesio nunca puede hacerlo. [241] Sólo hay evidencia muy limitada en forma de síntomas de deficiencia de que el rubidio sea posiblemente esencial en las cabras; Incluso si esto fuera cierto, las pequeñas cantidades que suelen estar presentes en los alimentos son más que suficientes. [246] [247]
La mayoría de las personas rara vez encuentran compuestos de cesio, pero la mayoría de los compuestos de cesio son levemente tóxicos. Al igual que el rubidio, el cesio tiende a sustituir al potasio en el cuerpo, pero es significativamente más grande y, por tanto, es un sustituto peor. [243] El exceso de cesio puede provocar hipopotasemia , arritmia y paro cardíaco agudo, [248] pero tales cantidades normalmente no se encuentran en fuentes naturales. [249] Como tal, el cesio no es un contaminante químico ambiental importante. [249] El valor medio de la dosis letal (LD 50 ) de cloruro de cesio en ratones es de 2,3 g por kilogramo, que es comparable a los valores LD 50 de cloruro de potasio y cloruro de sodio . [250] El cloruro de cesio se ha promocionado como una terapia alternativa contra el cáncer, [251] pero se ha relacionado con la muerte de más de 50 pacientes, en quienes se utilizó como parte de un tratamiento contra el cáncer científicamente no validado. [252]
Los radioisótopos de cesio requieren precauciones especiales: la manipulación inadecuada de fuentes de rayos gamma de cesio-137 puede provocar la liberación de este radioisótopo y lesiones por radiación. Quizás el caso más conocido sea el accidente de Goiânia de 1987, en el que un sistema de radioterapia mal desechado de una clínica abandonada en la ciudad de Goiânia , Brasil, fue recuperado de un depósito de chatarra y la brillante sal de cesio se vendió a curiosos. , compradores sin educación. Esto provocó cuatro muertes y lesiones graves por exposición a la radiación. Junto con el cesio-134 , el yodo-131 y el estroncio-90 , el cesio-137 se encontraba entre los isótopos distribuidos por la catástrofe de Chernóbil que constituyen el mayor riesgo para la salud. [98] Los radioisótopos de francio presumiblemente también serían peligrosos debido a su alta energía de desintegración y su corta vida media, pero ninguno se ha producido en cantidades suficientemente grandes como para representar un riesgo grave. [200]
{{cite journal}}: CS1 maint: numeric names: authors list (link)