El rodoceno es un compuesto químico con la fórmula [Rh(C 5 H 5 ) 2 ] . Cada molécula contiene un átomo de rodio unido entre dos sistemas aromáticos planos de cinco átomos de carbono conocidos como anillos de ciclopentadienilo en una disposición tipo sándwich . Es un compuesto organometálico ya que tiene enlaces covalentes rodio-carbono ( hápticos ) . [2] El radical [Rh(C 5 H 5 ) 2 ] se encuentra por encima de 150 °C (302 °F) o cuando queda atrapado enfriándolo a temperaturas de nitrógeno líquido (-196 °C [-321 °F]). A temperatura ambiente, los pares de estos radicales se unen mediante sus anillos de ciclopentadienilo para formar un dímero , un sólido amarillo. [1] [3] [4]
La historia de la química organometálica incluye los descubrimientos del siglo XIX de la sal de Zeise [5] [6] [7] y el tetracarbonilo de níquel . [2] Estos compuestos plantearon un desafío para los químicos ya que no encajaban con los modelos de enlaces químicos existentes . Otro desafío surgió con el descubrimiento del ferroceno , [8] el análogo de hierro del rodoceno y el primero de la clase de compuestos ahora conocidos como metalocenos . [9] Se descubrió que el ferroceno era inusualmente químicamente estable , [10] al igual que estructuras químicas análogas, incluido el rodocenio, el catión unipositivo del rodoceno [Nota 1] y sus homólogos de cobalto e iridio . [11] El estudio de las especies organometálicas, incluidas estas, condujo finalmente al desarrollo de nuevos modelos de enlace que explicaban su formación y estabilidad. [12] [13] El trabajo sobre compuestos sándwich, incluido el sistema rodocenio-rodoceno, le valió a Geoffrey Wilkinson y Ernst Otto Fischer el Premio Nobel de Química en 1973 . [14] [15]
Debido a su estabilidad y relativa facilidad de preparación, las sales de rodocenio son el material de partida habitual para la preparación de rodoceno y rodoceno sustituidos, todos los cuales son inestables. La síntesis original utilizó un anión ciclopentadienilo y tris (acetilacetonato) rodio (III) ; [11] Desde entonces se han informado muchos otros enfoques, incluida la transmetalación redox en fase gaseosa [16] y el uso de precursores de medio sándwich . [17] El octafenilrodoceno (un derivado con ocho grupos fenilo unidos) fue el primer rodoceno sustituido que se aisló a temperatura ambiente, aunque se descompone rápidamente en el aire. La cristalografía de rayos X confirmó que el octafenilrodoceno tiene una estructura tipo sándwich con una conformación escalonada . [18] A diferencia del cobaltoceno, que se ha convertido en un agente reductor de un electrón útil en la investigación, [19] ningún derivado del rodoceno descubierto hasta ahora es lo suficientemente estable para tales aplicaciones.
Investigadores biomédicos han examinado las aplicaciones de los compuestos de rodio y sus derivados en medicina [20] y han informado de una posible aplicación de un derivado de rodoceno como radiofármaco para tratar cánceres pequeños . [21] [22] Los derivados del rodoceno se utilizan para sintetizar metalocenos enlazados para poder estudiar las interacciones metal-metal; [23] Las posibles aplicaciones de estos derivados incluyen la electrónica molecular y la investigación de los mecanismos de catálisis . [24]

Los descubrimientos en química organometálica han dado lugar a importantes conocimientos sobre los enlaces químicos . La sal de Zeise , K[PtCl 3 (C 2 H 4 )]·H 2 O , se informó en 1831 [5] y el descubrimiento de Mond del tetracarbonilo de níquel ( Ni(CO) 4 ) ocurrió en 1888. [27] Cada uno contenía un enlace entre un centro metálico y una molécula pequeña, etileno en el caso de la sal de Zeise y monóxido de carbono en el caso del tetracarbonilo de níquel. [6] El modelo de llenado de espacio del anión de la sal de Zeise (imagen de la izquierda) [25] [26] muestra el enlace directo entre el centro del metal platino (que se muestra en azul) y los átomos de carbono (que se muestran en negro) del etileno. ligando ; Estos enlaces metal-carbono son la característica definitoria de las especies organometálicas . Los modelos de enlace no pudieron explicar la naturaleza de tales enlaces metal-alqueno hasta que se propuso el modelo de Dewar-Chatt-Duncanson en la década de 1950. [12] [7] [28] [29] La formulación original cubría solo enlaces metal-alqueno [27] pero el modelo se amplió con el tiempo para cubrir sistemas como carbonilos metálicos (incluido [Ni (CO) 4 ] ) donde π backbonding es importante. [29]
El ferroceno , [Fe(C 5 H 5 ) 2 ] , se sintetizó por primera vez en 1951 durante un intento de preparar el fuvaleno ( C
10h
8) por dimerización oxidativa del ciclopentadieno ; Se encontró que el producto resultante tenía la fórmula molecular C.
10h
10Fe y se informó que exhibía una "estabilidad notable". [10] El descubrimiento despertó un interés sustancial en el campo de la química organometálica, [8] [9] en parte porque la estructura propuesta por Pauson y Kealy era inconsistente con los modelos de enlace existentes en ese momento y no explicaba su inesperada estabilidad. En consecuencia, el desafío inicial fue determinar definitivamente la estructura del ferroceno con la esperanza de que luego se comprendieran sus enlaces y propiedades. La estructura sándwich fue deducida e informada de forma independiente por tres grupos en 1952: Robert Burns Woodward y Geoffrey Wilkinson investigaron la reactividad para determinar la estructura [30] y demostraron que el ferroceno sufre reacciones similares a las de una molécula aromática típica (como el benceno ). [31] Ernst Otto Fischer dedujo la estructura sándwich y también comenzó a sintetizar otros metalocenos , incluido el cobaltoceno ; [32] Eiland y Pepinsky proporcionaron confirmación cristalográfica por rayos X de la estructura tipo sándwich. [33] Aplicación de la teoría del enlace de valencia al ferroceno considerando un Fe2+
centro y dos aniones ciclopentadienuro (C 5 H 5 − ), que según la regla de Hückel son aromáticos y, por tanto, muy estables, permitieron una predicción correcta de la geometría de la molécula. Una vez que se aplicó con éxito la teoría de los orbitales moleculares , quedaron claras las razones de la notable estabilidad del ferroceno. [13]
Las propiedades del cobaltoceno informadas por Wilkinson y Fischer demostraron que el catión cobalticinio unipositivo [Co(C 5 H 5 ) 2 ] + exhibía una estabilidad similar a la del propio ferroceno. Esta observación no es inesperada dado que el catión cobalticinio y el ferroceno son isoelectrónicos , aunque el enlace no se entendía en ese momento. Sin embargo, la observación llevó a Wilkinson y F. Albert Cotton a intentar la síntesis de sales de rodocenio [Nota 1] y de iridocenio . [11] Informaron sobre la síntesis de numerosas sales de rodocenio, incluidas las que contienen tribromuro ( [Rh(C 5 H 5 ) 2 ]Br 3 ), perclorato ( [Rh(C 5 H 5 ) 2 ]ClO 4 ) y reineckato. ( [Rh(C 5 H 5 ) 2 ] [Cr(NCS) 4 (NH 3 ) 2 ]·H 2 O ) aniones, y encontró que la adición de dipicrilamina producía un compuesto de composición [Rh(C 5 H 5 ) 2 ] [ N ( C6H2N3O6 ) 2 ] . _ _ _ [11] En cada caso, se descubrió que el catión rodocenio poseía una alta estabilidad. Wilkinson y Fischer compartieron el Premio Nobel de Química de 1973 "por su trabajo pionero, realizado de forma independiente, sobre la química de los compuestos organometálicos, llamados compuestos sándwich ". [14] [15]
La estabilidad de los metalocenos se puede comparar directamente observando los potenciales de reducción de la reducción de un electrón del catión unipositivo. Se presentan los siguientes datos relativos al electrodo de calomelanos saturados (SCE) en acetonitrilo :
Estos datos indican claramente la estabilidad del ferroceno neutro y de los cationes cobaltocenio y rodocenio. El rodoceno es ca. 500 mV más reductor que el cobaltoceno, lo que indica que se oxida más fácilmente y, por tanto, menos estable. [1] Una investigación polarográfica anterior de perclorato de rodocenio a pH neutro mostró un pico de onda catódica a −1,53 V (frente a SCE) en el electrodo de caída de mercurio , correspondiente a la formación de rodoceno en solución, pero los investigadores no pudieron aislar el producto neutro. de la solución. En el mismo estudio, los intentos de detectar el iridoceno exponiendo sales de iridocenio a condiciones oxidantes no tuvieron éxito incluso con un pH elevado. Estos datos son consistentes con que el rodoceno es altamente inestable y pueden indicar que el iridoceno es aún más inestable. [11]
La regla de los 18 electrones es el equivalente de la regla del octeto en la química de grupos principales y proporciona una guía útil para predecir la estabilidad de compuestos organometálicos . [35] Predice que las especies organometálicas "en las que la suma de los electrones de valencia del metal más los electrones donados por los grupos ligando suman 18 probablemente sean estables". [35] Esto ayuda a explicar la estabilidad inusualmente alta observada para el ferroceno [10] y para los cationes cobalticinio y rodocenio [32] ; las tres especies tienen geometrías análogas y son estructuras isoelectrónicas de electrones de 18 valencias. La inestabilidad del rodoceno y el cobaltoceno también es comprensible en términos de la regla de los 18 electrones, ya que ambos son estructuras de 19 electrones de valencia; esto explica las primeras dificultades para aislar el rodoceno a partir de soluciones de rodocenio. [11] La química del rodoceno está dominada por el deseo de alcanzar una configuración de 18 electrones. [35]
El rodoceno existe como [Rh(C 5 H 5 ) 2 ] , un monómero radical paramagnético de 19 electrones de valencia solo a -196 °C (-320,8 °F) o por debajo ( temperaturas del nitrógeno líquido ) o por encima de 150 °C (302 °F). ) en fase gaseosa . [1] [3] [4] Es esta forma monomérica la que muestra la típica estructura sándwich de metaloceno escalonada . A temperatura ambiente (25 °C [77 °F]), la vida útil de la forma monomérica en acetonitrilo es inferior a dos segundos; [1] y el rodoceno forma [Rh(C 5 H 5 ) 2 ] 2 , una estructura dimérica ansa -metaloceno diamagnética con puente de electrones de valencia de 18 . [36] Las mediciones de resonancia de espín electrónico (ESR), resonancia magnética nuclear (NMR) y espectroscopía infrarroja (IR) apuntan a la presencia de un equilibrio que interconvierte las formas monoméricas y diméricas. [4] La evidencia de ESR confirma que el monómero posee un eje de simetría de alto orden (C n , n > 2) con un plano especular (σ) perpendicular a él como elementos de simetría ; esto demuestra experimentalmente que el monómero posee la estructura tipo sándwich típica de un metaloceno [3] [Nota 2] aunque se ha cuestionado la interpretación de los datos de ESR. [36] La vía de descomposición del monómero también se ha estudiado mediante espectrometría de masas . [37] La dimerización es un proceso redox ; el dímero es una especie de rodio (I) y el monómero tiene un centro de rodio (II). [Nota 3] El rodio normalmente ocupa estados de oxidación +I o +III en sus compuestos estables. [38]
Este proceso de dimerización tiene el efecto general de disminuir el recuento de electrones alrededor del centro de rodio de 19 a 18. Esto ocurre porque el acoplamiento oxidativo de los dos ligandos de ciclopentadienilo produce un nuevo ligando con menor hapticidad y que dona menos electrones al centro metálico. El término hapticidad se utiliza para indicar el "número de átomos de carbono (u otros) a través de los cuales [un ligando] se une ( n )" [39] a un centro metálico y se simboliza como ηn . Por ejemplo, el ligando de etileno en la sal de Zeise está unido al centro de platino a través de ambos átomos de carbono y, por lo tanto, tiene formalmente la fórmula K[PtCl 3 (η 2 -C 2 H 4 )]·H 2 O . [6] Los ligandos carbonilo en el tetracarbonilo de níquel están unidos cada uno solo a través de un átomo de carbono y, por lo tanto, se describen como ligandos monohapto, pero las notaciones η 1 generalmente se omiten en las fórmulas. Los ligandos de ciclopentadienilo en muchos compuestos de metaloceno y semisándwich son ligandos de pentahapto, de ahí la fórmula [Rh(η 5 -C 5 H 5 ) 2 ] para el monómero de rodoceno. En el dímero de rodoceno, los ligandos de ciclopentadienilo acoplados son donantes de tetrahapto de 4 electrones para cada centro metálico de rodio (I), en contraste con los donantes de pentahapto ciclopentadienilo de 6 electrones [Nota 4] . La mayor estabilidad de la especie dímera de rodio (I) de 18 electrones de valencia en comparación con el monómero de rodio (II) de 19 electrones de valencia probablemente explica por qué el monómero solo se detecta en condiciones extremas. [1] [4]
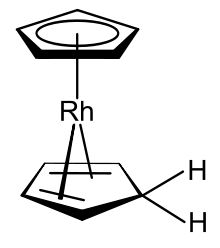
Cotton y Wilkinson demostraron [11] que el catión rodocenio rodio (III) de 18 electrones de valencia [Rh(η 5 -C 5 H 5 ) 2 ] + puede reducirse en solución acuosa a la forma monomérica; no pudieron aislar el producto neutro ya que no solo puede dimerizarse, sino que el monómero radical rodio (II) también puede formar espontáneamente la especie de rodio (I) estable de hapticidad mixta [(η 5 -C 5 H 5 )Rh(η 4 -C5H6 ) ] . _ _ [3] Las diferencias entre el rodoceno y este derivado se encuentran en dos áreas:
Estos dos cambios convierten a la derivada en una especie de electrones de valencia 18. Fischer y sus colegas plantearon la hipótesis de que la formación de este derivado del rodoceno podría ocurrir en pasos separados de protonación y reducción, pero no publicaron evidencia que respalde esta sugerencia. [3] (η 4 -Ciclopentadieno)(η 5 -ciclopentadienil)rodio(I), el compuesto resultante, es un complejo organometálico inusual porque tiene un anión ciclopentadienilo y el propio ciclopentadieno como ligandos. Se ha demostrado que este compuesto también puede prepararse mediante reducción con borohidruro de sodio de una solución de rodocenio en etanol acuoso ; Los investigadores que hicieron este descubrimiento caracterizaron el producto como hidruro de bisciclopentadienilrodio. [40]
Fischer y sus colaboradores también estudiaron la química del iridoceno, la tercera serie de transición análoga del rodoceno y el cobaltoceno, y descubrieron que la química del rodoceno y el iridoceno son generalmente similares. Se ha descrito la síntesis de numerosas sales de iridocenio, incluidos el tribromuro y el hexafluorofosfato . [4] Al igual que el rodoceno, el iridoceno se dimeriza a temperatura ambiente, pero se puede detectar una forma monómera a bajas temperaturas y en fase gaseosa, y las mediciones de IR, RMN y ESR indican que hay un equilibrio químico presente y confirman la estructura tipo sándwich del monómero de iridoceno. . [3] [4] El complejo [(η 5 -C 5 H 5 )Ir(η 4 -C 5 H 6 )] , el análogo del derivado de rodoceno informado por Fischer, [3] también ha sido estudiado y demuestra propiedades consistentes con un mayor grado de enlace π en los sistemas de iridio (I) que el que se encuentra en los casos análogos de cobalto (I) o rodio (I). [41]
Las sales de rodoceno se informaron por primera vez [11] dos años después del descubrimiento del ferroceno. [10] Estas sales se prepararon haciendo reaccionar el carbanión reactivo de Grignard bromuro de ciclopentadienilmagnesio ( C
5h
5MgBr ) con tris(acetilacetonato)rodio(III) (Rh(acac) 3 ). Más recientemente, los cationes de rodocenio en fase gaseosa se han generado mediante una reacción de transmetalación redox de iones de rodio (I) con ferroceno o níqueloceno . [dieciséis]
También se han informado métodos modernos de síntesis por microondas. [42] El hexafluorofosfato de rodocenio se forma después de la reacción de ciclopentadieno y cloruro de rodio (III) hidrato en metanol después del procesamiento con hexafluorofosfato de amonio metanólico ; el rendimiento de la reacción supera el 60% con sólo 30 segundos de exposición a la radiación de microondas . [43]
El propio rodoceno se forma entonces mediante la reducción de sales de rodocenio con sodio fundido . [3] Si una masa fundida que contiene rodocenio se trata con metales de sodio o potasio y luego se sublima en un dedo frío enfriado con nitrógeno líquido, se obtiene un material policristalino negro. [36] Calentar este material a temperatura ambiente produce un sólido amarillo que se ha confirmado que es el dímero de rodoceno. Se puede utilizar un método similar para preparar el dímero de iridoceno. [36]
Se han desarrollado nuevos enfoques para sintetizar complejos de ciclopentadienilo sustituidos utilizando materiales de partida de vinilciclopropeno sustituidos. [44] [45] [46] Las reacciones de reordenamiento de vinilciclopropano con agrandamiento de anillo para producir ciclopentenos son bien conocidas [47] y sirven como precedente para el reordenamiento de vinilciclopropenos en ciclopentadienos. El catión [(η 5 -C 5 t Bu 3 H 2 )Rh(η 5 -C 5 H 5 )] + se ha generado mediante una secuencia de reacción que comienza con la adición del dímero de clorobisetilenorodio(I), [(η 2 - C 2 H 4 ) 2 Rh(μ-Cl)] 2 , a 1,2,3-tri - terc -butil-3-vinil-1-ciclopropeno seguido de reacción con ciclopentadienuro de talio : [44] [45]
La especie pentadienodiilo rodio(III) de 18 electrones de valencia generada por esta reacción demuestra nuevamente la inestabilidad de la fracción rodoceno, ya que puede refluir en tolueno durante meses sin que se forme 1,2,3-tri- terc -butilrodoceno, pero sí se oxida. condiciones, el catión 1,2,3-tri- terc -butilrodocenio se forma rápidamente. [44] La voltamperometría cíclica se ha utilizado para investigar este y otros procesos similares en detalle. [44] [45] Se ha demostrado que el mecanismo de la reacción implica una pérdida de un electrón del ligando pentadiendiilo seguida de un rápido reordenamiento (con pérdida de un átomo de hidrógeno) para formar el 1,2,3-tri- tert . -catión butilrodocenio. [45] Tanto las sales de tetrafluoroborato como de hexafluorofosfato de este catión se han caracterizado estructuralmente mediante cristalografía de rayos X. [45]
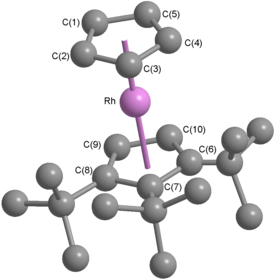
[(η 5 -C 5 t Bu 3 H 2 )Rh(η 5 -C 5 H 5 )]BF 4 forma un cristal monoclínico centrosimétrico incoloro perteneciente al grupo espacial P 2 1 /c , y con una densidad de 1,486 g cm -3 . [45] Al observar el diagrama ORTEP de la estructura del catión (a la derecha), es evidente que posee la geometría típica que se espera de un catión de rodoceno o rodocenio. Los dos anillos de ciclopentadienilo son casi paralelos (el ángulo centroide -Rh-centroide es de 177,2°) y el centro de rodio está ligeramente más cerca del anillo de ciclopentadienilo sustituido (las distancias Rh-centroide son 1,819 Å y 1,795 Å), una observación atribuida a la mayor efecto inductivo de los grupos terc -butilo sobre el ligando sustituido. [45] El diagrama ORTEP muestra que el catión adopta una conformación eclipsada en estado sólido. La estructura cristalina de la sal de hexafluorofosfato muestra tres cationes cristalográficamente independientes, uno eclipsado, otro escalonado y otro rotacionalmente desordenado. [45] Esto sugiere que la conformación adoptada depende del anión presente y también que la barrera de energía a la rotación es baja: en el ferroceno, se sabe que la barrera de energía a la rotación es ~5 kJ mol −1 tanto en solución como en fase gaseosa. [13]

El diagrama de arriba muestra las distancias de enlace rodio-carbono ( en rojo, dentro de los pentágonos a la izquierda) y carbono-carbono ( en azul, fuera de los pentágonos a la izquierda) para ambos ligandos, junto con los ángulos de enlace ( en verde, dentro de los pentágonos a la izquierda). la derecha) dentro de cada anillo de ciclopentadienilo. Las etiquetas de los átomos utilizadas son las mismas que se muestran en la estructura cristalina anterior. Dentro del ligando ciclopentadienilo no sustituido, las longitudes de los enlaces carbono-carbono varían entre 1,35 Å y 1,40 Å y los ángulos de enlace internos varían entre 107 ° y 109 °. A modo de comparación, el ángulo interno en cada vértice de un pentágono regular es 108°. Las longitudes de los enlaces rodio-carbono varían entre 2,16 Å y 2,18 Å. [45] Estos resultados son consistentes con la coordinación η 5 del ligando con el centro metálico. En el caso del ligando ciclopentadienilo sustituido, hay una variación algo mayor: las longitudes de los enlaces carbono-carbono varían entre 1,39 Å y 1,48 Å, los ángulos de enlace internos varían entre 106° y 111°, y las longitudes de los enlaces rodio-carbono varían entre 2,14 Å y 2,20 Å. La mayor variación en el ligando sustituido se atribuye a las distorsiones necesarias para aliviar la tensión estérica impuesta por los sustituyentes terc -butilo vecinos; a pesar de estas variaciones, los datos demuestran que el ciclopentadienilo sustituido también está coordinado en η5 . [45]
La estabilidad de los metalocenos cambia con la sustitución del anillo. La comparación de los potenciales de reducción de los cationes cobaltocenio y decametilcobaltocenio muestra que la especie decametilo es ca. 600 mV más reductor que su metaloceno original, [19] una situación que también se observa en los sistemas de ferroceno [48] y rodoceno. [49] Los siguientes datos se presentan en relación con la pareja redox ferrocenio/ferroceno : [50]
Las diferencias en los potenciales de reducción se atribuyen en el sistema de cobaltocenio al efecto inductivo de los grupos alquilo, [19] que estabilizan aún más las especies de electrones de 18 valencia. Se observa un efecto similar en los datos de rodocenio mostrados arriba, nuevamente consistente con efectos inductivos. [45] En el sistema de iridocenio sustituido, las investigaciones de voltamperometría cíclica muestran reducciones irreversibles a temperaturas tan bajas como -60 °C; [51] en comparación, la reducción de los rodocenos correspondientes es casi reversible a temperatura ambiente y completamente reversible a -35 °C. [49] La irreversibilidad de las reducciones del iridocenio sustituido se atribuye a la dimerización extremadamente rápida de las especies de electrones de valencia 19 resultantes, lo que ilustra aún más que los iridocenos son menos estables que sus correspondientes rodocenos. [51]
El conjunto de conocimientos sobre compuestos con ligandos de ciclopentadienilo pentasustituidos es extenso, siendo bien conocidos los complejos organometálicos de los ligandos de pentametilciclopentadienilo y pentafenilciclopentadienilo. [52] Las sustituciones en los anillos de ciclopentadienilo de rodocenos y sales de rodocenio producen compuestos de mayor estabilidad ya que permiten una mayor deslocalización de la carga positiva o la densidad electrónica y también proporcionan un impedimento estérico contra otras especies que se acercan al centro metálico. [37] Se conocen varias especies de rodocenio mono y disustituidas, pero no se logra una estabilización sustancial sin mayores sustituciones. [37] Las sales de rodocenio altamente sustituidas conocidas incluyen hexafluorofosfato de decametilrodocenio [(η 5 -C 5 Me 5 ) 2 Rh]PF 6 , [53] hexafluorofosfato de decaisopropilrodocenio [(η 5 -C 5 i Pr 5 ) 2 Rh]PF 6 , [ 54] y hexafluorofosfato de octafenilrodocenio [ ( η5 - C5 Ph4H ) 2Rh ] PF6 . [18] [Nota 5] El tetrafluoroborato de decametilrodocenio se puede sintetizar a partir del complejo tris(acetona) [(η 5 -C 5 Me 5 )Rh(Me 2 CO) 3 ](BF 4 ) 2 mediante reacción con pentametilciclopentadieno , y el análogo También se conoce la síntesis de iridio. [55] El hexafluorofosfato de decaisopropilrodicnio se sintetizó en 1,2-dimetoxietano ( disolvente ) en una síntesis inusual en un solo recipiente que implica la formación de 20 enlaces carbono-carbono : [54]
En una reacción similar, el hexafluorofosfato de pentaisopropilrodocenio [(η 5 -C 5 i Pr 5 )Rh(η 5 -C 5 H 5 )]PF 6 se puede sintetizar a partir de hexafluorofosfato de pentametilrodocenio [(η 5 -C 5 Me 5 )Rh(η 5 - C5H5 )]PF6 con un rendimiento del 80%. [54] Estas reacciones demuestran que la acidez de los hidrógenos metílicos en un complejo de pentametilciclopentadienilo puede aumentar considerablemente por la presencia del centro metálico. Mecánicamente, la reacción continúa con el hidróxido de potasio desprotonando un grupo metilo y el carbanión resultante experimenta una sustitución nucleofílica con yoduro de metilo para formar un nuevo enlace carbono-carbono. [54]
Los compuestos tetrafluoroborato de pentafenilrodocenio [(η 5 -C 5 Ph 5 )Rh(η 5 -C 5 H 5 )]BF 4 , y tetrafluoroborato de pentametilpentafenilrodocenio [(η 5 -C 5 Ph 5 )Rh(η 5 -C 5 Me 5 )] También se han reportado BF 4 . Demuestran que se pueden preparar compuestos sándwich de rodio a partir de precursores de medio sándwich. Por ejemplo, en un enfoque muy similar a la síntesis de tris(acetona) del tetrafluoroborato de decametilrodocenio, [55] se ha sintetizado tetrafluoroborato de pentafenilrodocenio a partir de la sal de tris( acetonitrilo ) [(η 5 -C 5 Ph 5 )Rh(CH 3 CN) 3 ](BF 4 ) 2 por reacción con ciclopentadienuro de sodio : [17]

El octafenilrodoceno, [(η 5 -C 5 Ph 4 H) 2 Rh], es el primer derivado de rodoceno que se aísla a temperatura ambiente. Sus cristales de color verde oliva se descomponen rápidamente en solución y en cuestión de minutos en el aire, lo que demuestra una sensibilidad al aire dramáticamente mayor que el complejo de cobalto análogo , aunque es significativamente más estable que el propio rodoceno. Esta diferencia se atribuye a la estabilidad relativamente menor del estado de rodio (II) en comparación con el estado de cobalto (II). [18] [38] El potencial de reducción para el catión [(η 5 -C 5 Ph 4 H) 2 Rh] + (medido en dimetilformamida en relación con el par ferrocenio/ferroceno) es −1,44 V, consistente con la mayor estabilización termodinámica de el rodoceno por el ligando C 5 HPh 4 en comparación con los ligandos C 5 H 5 o C 5 Me 5 . [18] El cobaltoceno es un agente reductor de un electrón útil en el laboratorio de investigación, ya que es soluble en solventes orgánicos no polares , [19] y su par redox se comporta lo suficientemente bien como para usarse como estándar interno en voltamperometría cíclica. . [56] Ningún rodoceno sustituido preparado todavía ha demostrado suficiente estabilidad para ser utilizado de manera similar.
La síntesis de octafenilrodoceno se produce en tres pasos, con un reflujo de diglima seguido de un tratamiento con ácido hexafluorofosfórico y luego una reducción de amalgama de sodio en tetrahidrofurano : [18]
La estructura cristalina del octafenilrodoceno muestra una conformación escalonada [18] (similar a la del ferroceno y en contraste con la conformación eclipsada del rutenoceno ). [13] La distancia rodio-centroide es 1,904 Å y las longitudes promedio de los enlaces rodio-carbono son 2,26 Å; las longitudes promedio de los enlaces carbono-carbono son 1,44 Å. [18] Todas estas distancias son similares a las encontradas en el catión 1,2,3-tri- terc -butilrodocenio descrito anteriormente, con la única diferencia de que el tamaño efectivo del centro de rodio parece mayor, una observación consistente con la distancia iónica expandida. Radio del rodio (II) en comparación con el rodio (III). [45]
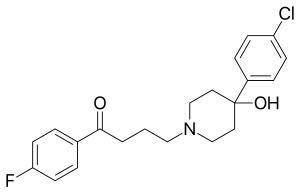
Se han realizado extensas investigaciones sobre metalofármacos , [57] [58] , incluida la discusión sobre los compuestos de rodio en medicina. [20] Un importante conjunto de investigaciones ha examinado el uso de derivados metaloceno de rutenio [59] y hierro [60] como metalofármacos. Un área de dicha investigación ha utilizado metalocenos en lugar del grupo fluorofenilo en el haloperidol , [21] que es un fármaco clasificado como antipsicótico típico . El compuesto de ferrocenil-haloperidol investigado tiene estructura (C 5 H 5 )Fe(C 5 H 4 )–C(=O)–(CH 2 ) 3 –N(CH 2 CH 2 ) 2 C(OH)–C 6 H 4 Cl y se puede convertir en el análogo de rutenio mediante una reacción de transmetalación. El uso del isótopo radiactivo 103 Ru produce un radiofármaco rutenocenil-haloperidol con una alta afinidad por el tejido pulmonar pero no cerebral en ratones y ratas . [21] La desintegración beta de 103 Ru produce el isótopo metaestable 103 m Rh en un compuesto de rodocenil-haloperidol. Este compuesto, al igual que otros derivados del rodoceno, tiene una configuración electrónica inestable de 19 valencias y se oxida rápidamente a las especies catiónicas esperadas de rodocenio-haloperidol. [21] Se ha estudiado la separación de las especies rutenocenil-haloperidol y rodocenio-haloperidol y la distribución de cada una entre los órganos del cuerpo. [22] 103 m Rh tiene una vida media de 56 min y emite un rayo gamma de energía 39,8 keV , por lo que la desintegración gamma del isótopo de rodio debería seguir poco después de la desintegración beta del isótopo de rutenio. Los radionucleidos emisores beta y gamma utilizados en medicina incluyen 131 I , 59 Fe y 47 Ca , y se ha propuesto el uso de 103 m Rh en radioterapia para tumores pequeños. [20]
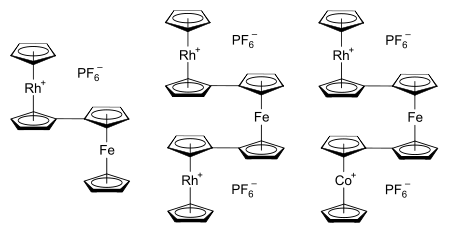
La motivación original para las investigaciones del sistema rodoceno fue comprender la naturaleza y los enlaces dentro de la clase de compuestos metaloceno. En tiempos más recientes, el interés se ha reavivado por el deseo de explorar y aplicar las interacciones metal-metal que ocurren cuando se vinculan sistemas de metaloceno. [23] Las aplicaciones potenciales para tales sistemas incluyen la electrónica molecular , [24] polímeros de metaloceno semiconductores (y posiblemente ferromagnéticos ) (un ejemplo de un cable molecular ), [23] y la exploración del umbral entre catálisis heterogénea y homogénea . [24] Ejemplos de bimetalocenos y termetalocenos conocidos que poseen el resto rodocenilo incluyen las sales de hexafluorofosfato de rodocenilferroceno, 1,1'-dirhodocenilferroceno y 1-cobaltocenil-1'-rodocenilferroceno, [61] cada uno de los cuales se muestra a la derecha. Los metalocenos unidos también se pueden formar introduciendo varios sustituyentes metalocenilo en un único ligando ciclopentadienilo. [24]
Los estudios estructurales de los sistemas de termmetaloceno han demostrado que normalmente adoptan una geometría de "cigüeñal" de "doble transoide eclipsada". [62] Tomando como ejemplo el catión 1-cobaltocenil-1'-rodocenilferroceno que se muestra arriba, esto significa que los restos cobaltocenilo y rodocenilo están eclipsados y, por lo tanto, los átomos de carbono 1 y 1' en el núcleo central del ferroceno están lo más cerca posible de alineados verticalmente. como es posible dada la conformación escalonada de los anillos de ciclopentadienilo dentro de cada unidad de metaloceno. Vistos de lado, esto significa que los termmetalocenos se parecen al patrón de abajo-arriba-abajo de un cigüeñal . [62] La síntesis de este termetaloceno implica la combinación de soluciones de rodocenio y cobaltocenio con 1,1'-dilitioferroceno . Esto produce un intermedio no cargado con ligandos ciclopentadienil-ciclopentadieno unidos cuya unión se asemeja a la que se encuentra en el dímero de rodoceno. Estos ligandos luego reaccionan con el carbocatión trifenilmetilo para generar la sal de termetaloceno, [(η 5 -C 5 H 5 )Rh(μ-η 5 :η 5 -C 5 H 4 –C 5 H 4 )Fe(μ-η 5 :η 5 -C 5 H 4 –C 5 H 4 )Co(η 5 -C 5 H 5 )](PF 6 ) 2 . Esta vía sintética se ilustra a continuación: [61] [62]
Los primeros polímeros de cadena lateral que contienen rodocenio se prepararon mediante técnicas de polimerización controlada, como la polimerización por transferencia de cadena por adición-fragmentación reversible (RAFT) y la polimerización por metátesis con apertura de anillo (ROMP). [63]
Una aplicación industrial de la química organometálica de los metales de transición apareció ya en la década de 1880, cuando Ludwig Mond demostró que el níquel se puede purificar utilizando CO para recoger el níquel en forma de Ni(CO) 4 gaseoso que puede separarse fácilmente de las impurezas sólidas y Posteriormente se descompondrá térmicamente para dar níquel puro.... Trabajos recientes han demostrado la existencia de una clase creciente de metaloenzimas que tienen entornos de ligandos organometálicos, considerados como la química de los iones metálicos que tienen ligandos donantes de C como el CO o el grupo metilo.
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )Ambos metales exhiben una química extensa, principalmente en el estado de oxidación +3, siendo también importante +1, y existiendo una química significativa de iridio +4. Se conocen pocos compuestos en el estado +2, en contraste con la situación del cobalto, su homólogo más ligero (los factores responsables incluyen la mayor estabilidad del estado +3 como consecuencia de la mayor estabilización del bajo espín d 6 a medida que aumenta 10 Dq). " (pág. 78)