La transposición de vinilciclopropano o transposición de vinilciclopropano-ciclopenteno es una reacción de expansión del anillo , que convierte un anillo de ciclopropano sustituido con vinilo en un anillo de ciclopenteno . [1] [2] [3]
Los grupos ciclopropilo adyacentes a los grupos vinilo pueden sufrir reacciones de expansión del anillo . Esta reactividad se puede aprovechar para generar compuestos cíclicos inusuales, como ciclobutenos , [4] o especies bicíclicas como el ciclohepteno que se muestra a continuación. [5]

Las investigaciones experimentales y computacionales muestran que, desde el punto de vista mecánico, el reordenamiento del vinilciclopropano puede considerarse como un proceso pericíclico de dos pasos mediado por dirradicales y/o controlado por simetría orbital. La cantidad de funcionamiento de cada uno de los dos mecanismos depende en gran medida del sustrato.
Debido a su capacidad para formar anillos de ciclopenteno, la transposición de vinilciclopropano ha servido varias veces como reacción clave en la síntesis de productos naturales complejos.
En 1959, un joven químico investigador de Humble Oil and Refining ( Esso , ahora Exxon ) llamado Norman P. Neureiter recibió instrucciones de encontrar nuevos usos para el exceso de butadieno producido en uno de los procesos de la refinería. Las conversaciones sobre la química del carbeno con uno de los consultores más respetables de la empresa en ese momento, William von Eggers Doering , entonces profesor en Yale , llevaron al joven Ph.D. Graduado de la Universidad Northwestern para seguir un procedimiento reciente que combina carbenos y butadieno. [6] En particular, el procedimiento describía la reacción del 1,3-butadieno con carbenos generados a partir de la acción de una base sobre cloroformo o bromoformo , que había sido estudiado previamente por Doering. [7] Neureiter luego tomó el 1,1-dicloro-2,2-dimetilciclopropano resultante y en condiciones de pirólisis (por encima de 400 °C) descubrió una transposición a 4,4-diclorociclopenteno que hoy se considera el primer vinilciclopropano-ciclopenteno térmico. reordenamiento en la historia. [8]

La correspondiente versión totalmente de carbono de la reacción fue informada de forma independiente por Emanuel Vogel [9] y Overberger & Borchert apenas un año después de que apareciera la publicación de Neureiter. [10] [11] Doering, aunque interactuaba con Humble Oil and Refining - y por lo tanto también con Neureiter - como consultor, en una publicación de 1963 afirmó lo siguiente: "El crédito por el descubrimiento de que el vinilciclopropano se reorganiza en ciclopenteno se debe a Overberger y Borchert, y Vogel et al., quienes parecen haber desarrollado varios ejemplos de reordenamiento de forma independiente". [12] El desarrollo de nuevas variantes de reordenamiento del vinilciclopropano no tomó mucho tiempo, como lo demostraron Atkinson & Rees en 1967, [13] Lwowski en 1968. [14] y Paladini & Chuche en 1971. [15]
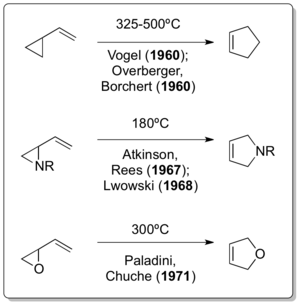
El reordenamiento clásico de vinilciclopropano se descubrió mucho después de que ya se hubieran informado dos de sus variantes de heteroátomos. Aunque se cree que el reordenamiento del vinilciclopropano debe haber ocurrido durante la preparación del vinilciclopropano por parte de Nikolay Demyanov mediante eliminación de Hofmann a temperaturas elevadas en 1922, [16] el reordenamiento ciclopropilimina-pirrolina realizado por Cloke en 1929 [17] y el ciclopropilcarbaldehído-2,3 de Wilson -El reordenamiento de dihidrofurano en 1947 [18] son realmente los únicos ejemplos de reordenamientos similares al vinilciclopropano.

Este último tipo de reacción también se conoce como reordenamiento de Cloke-Wilson [19].
La discusión mecanicista sobre si el reordenamiento del vinilciclopropano se produce a través de un mecanismo de dos pasos mediado por dirradicales o un mecanismo totalmente concertado controlado por simetría orbital se ha prolongado durante más de medio siglo. Los datos cinéticos junto con los efectos isotópicos cinéticos secundarios observados en el extremo vinílico del vinilciclopropano sugieren un mecanismo concertado, mientras que la distribución del producto indica un mecanismo dirradical escalonado. [20] En la década de 1960, poco después de que se descubriera el reordenamiento, se estableció que la energía de activación para el reordenamiento del vinilciclopropano es de alrededor de 50 kcal/mol. [21] Los datos cinéticos obtenidos para este reordenamiento fueron consistentes con un mecanismo concertado donde la escisión del enlace ciclopropilo carbono-carbono fue limitante de la velocidad. Aunque parecía probable un mecanismo concertado, pronto se reconoció que la energía de activación para romper el enlace carbono-carbono en el ciclopropano no sustituido era de 63 kcal/mol [22], exactamente 13 kcal/mol más alta que la energía de activación original, una diferencia notablemente similar a la energía de resonancia del radical alilo. [23] Inmediatamente la gente comenzó a apreciar la posibilidad de que surgiera un intermediario diradical de la escisión homolítica del enlace débil C1-C2-ciclopropano en condiciones térmicas.

La discusión sobre si el reordenamiento del vinilciclopropano se produce a través de un mecanismo totalmente concertado o de dos pasos, no concertado, recibió una consideración más cuidadosa cuando Woodward y Hoffmann utilizaron el reordenamiento del vinilciclopropano para ejemplificar los cambios de alquilo concertados [1,3]-sigmatrópicos en 1969. [24] Plantearon la hipótesis de que si un mecanismo concertado estuviera operativo, las consecuencias de los factores controlados por la simetría orbital solo permitirían la formación de ciertos productos. Según su análisis de un vinilciclopropano sustituido con tres grupos R, el desplazamiento antarafacial [1,3] del enlace 1,2 a C-5, con retención en C-2, conduce al ar ciclopenteno y al suprafacial [1,3]. ]-desplazamiento del enlace 1,2 a C-5, con inversión en C-2, lo que lleva a ciclopenteno si es simetría permitida, mientras que el desplazamiento suprafacial [1,3] del enlace 1,2 a C-5, con retención en C-2, que conduce a ciclopenteno sr y el desplazamiento antarafacial [1,3] del enlace 1,2 a C-5, con inversión en C-2, que conduce a ai ciclopenteno, están prohibidos por simetría. Es importante señalar que Woodward y Hoffmann basaron su análisis únicamente en los principios de la teoría de la conservación de la simetría orbital sin hacer ninguna predicción mecanicista o estereoquímica.

La atención dirigida hacia el reordenamiento del vinilciclopropano por Woodward y Hoffmann como un ejemplo representativo de los cambios de carbono [1,3] aumentó claramente el interés en esta reacción. Además, su análisis reveló posibles experimentos que permitirían distinguir entre un mecanismo concertado o escalonado. Las consecuencias estereoquímicas de una vía de reacción concertada sobre el resultado de la reacción sugirieron un experimento en el que se correlacionaría la estereoquímica de la reacción obtenida con la estereoquímica de la reacción predicha para un sustrato modelo. La observación de la formación de productos de ai - y sr -ciclopenteno respaldaría la idea de que está operativo un mecanismo gradual y no concertado, mientras que su ausencia apuntaría hacia un mecanismo totalmente concertado. Al final resultó que, encontrar un sustrato modelo sustituido apropiado para estudiar el resultado estereoquímico del reordenamiento del vinilciclopropano fue mucho más desafiante de lo que se pensaba inicialmente, ya que reacciones secundarias como los cambios de homodienil [1,5]-hidrógeno y, más aún, las estereomutaciones térmicas tienden a mezclar la estereoquímica. Las distinciones mucho más rápidas que los reordenamientos conducen a los productos de ciclopenteno.

Aunque la deconvolución de los complejos escenarios cinéticos subyacentes a estos reordenamientos fue difícil, se han informado varios estudios en los que fue posible realizar deconvoluciones exactas y explícitas de datos brutos cinéticos y estereoquímicos para tener en cuenta las contribuciones estereoquímicas que surgen de las estereomutaciones competitivas. [20] [25] [26] [27]
De este modo se pudieron determinar las constantes de velocidad para las cuatro vías estereoquímicamente distintas del reordenamiento del vinilciclopropano.

Los datos indicaron claramente que las preferencias mecanicistas de los reordenamientos dependen del sistema. Mientras que los trans -vinilciclopropanos tienden a formar más de los ar - y si -ciclopentenos con simetría permitida que apoyan un mecanismo concertado, los cis -vinilciclopropanos producen preferentemente los productos ai - y sr - con simetría prohibida, lo que sugiere un mecanismo diradical más escalonado. La influencia de los efectos de los sustituyentes en la estereoquímica de la reacción también resulta evidente a partir de los datos. Los sustituyentes con mayor capacidad estabilizadora de radicales no solo reducen la energía de activación de los reordenamientos, sino que también el recierre de las especies diradicales formadas inicialmente se vuelve más lento en relación con la velocidad de formación de ciclopenteno, lo que resulta en un mecanismo general más concertado con menos estereomutación (por ejemplo, entradas 6 y 7). En todos los casos, sin embargo, se formaron los cuatro productos, lo que indica que tanto los mecanismos pericíclicos controlados por simetría orbital como los mecanismos de dos pasos mediados por dirradicales están operativos en cualquier sentido. Los datos son consistentes con la formación de especies birradicales en una superficie de energía potencial relativamente plana, lo que permite una flexibilidad conformacional restringida antes de que se formen los productos. La cantidad de flexibilidad conformacional y, por lo tanto, evolución conformacional accesible a las especies dirradicales antes de formar el producto depende de la constitución de la superficie de energía potencial. Esta noción también está respaldada por el trabajo computacional. [28] Se encontró un estado de transición con un alto carácter diradicaloide. Siguiendo la superficie de energía potencial de la ruta de menor energía de la reacción, se encontró que un régimen muy superficial permite que las especies dirradicales experimenten cambios conformacionales y reacciones de estereoisomerización con consecuencias energéticas menores. Además, se demostró que los sustituyentes pueden favorecer vías estereoselectivas al desestabilizar especies que permiten la codificación estereoquímica.
Podría decirse que el mayor inconveniente de la transposición del vinilciclopropano como método sintético es su barrera de activación intrínsecamente alta que da como resultado temperaturas de reacción muy altas (500-600 °C). Estas altas temperaturas no solo permiten que se produzcan reacciones secundarias con energías de activación similares, como cambios de homodienil-[1,5]-hidrógeno, sino que también limitan significativamente los grupos funcionales tolerados en los sustratos. La comunidad química reconoció claramente que para que esta reacción se convirtiera en un método sintético útil, con suerte aplicable en entornos complejos de productos naturales en algún momento, era necesario desarrollar alguna reacción. Se descubrió que la temperatura de reacción podía reducirse drásticamente cuando el anillo de ciclopropano contenía un grupo ditiano . Aunque los sustratos de vinilciclopropano sustituidos con ditiano requirieron dos pasos de síntesis a partir de los 1,3-dienos correspondientes, el método demostró ser exitoso para la síntesis de una variedad de ciclopentenos sustituidos. Los productos de transposición inmediata podrían convertirse fácilmente en las ciclopentenonas correspondientes. [29]

Los vinilciclopropanos metoxi sustituidos muestran velocidades de reacción significativamente más rápidas, lo que permite que la transposición tenga lugar a 220 °C. [30]

Se descubrió que los siloxivinilciclopropanos [31] , así como los sulfinilvinilciclopropanos análogos [32], podrían usarse como sustratos para construir estructuras anuladas de ciclopenteno . Aunque estas reacciones todavía requerían temperaturas de reacción superiores a 300 °C, pudieron producir productos útiles que surgieron de la anulación del ciclopenteno a un sistema de anillos actual.

Los reordenamientos de vinilciclopropano también pueden mediarse fotoquímicamente. [33] [34] En un ejemplo particularmente intrigante, pudo demostrar que los vinilciclopropanos incrustados dentro de un núcleo de ciclooctano se pueden convertir en los correspondientes sistemas de anillos fusionados [5-5].

Los reordenamientos de vinilciclopropano son susceptibles a los catalizadores de metales de transición . El acetato de dirodio cataliza los reordenamientos desde temperatura ambiente hasta 80 °Cy [35] [36]

De manera análoga a la aceleración de la velocidad observada en el reordenamiento aniónico-oxi-Cope, Danheiser informó un efecto muy similar para sustratos de vinilciclopropano que llevan sustituyentes [alcoxi]. [37]

Larsen informó otro resultado intrigante en 1988. [38] Pudo promover reordenamientos de vinilciclopropano con sustratos como el que se muestra en la siguiente reacción a temperaturas tan bajas como -78 °C. Los sustratos se generaron in situ mediante la contracción del anillo de aductos de tiocarbonilo Diels-Alder en condiciones básicas. Esta metodología permitió la formación de numerosos ciclopentenos altamente funcionalizados de forma estereoselectiva .

La metodología permite la formación de varios andamios de [5-5] y [5-6] carbonos. [39]

Los anillos de carbono de cinco miembros son motivos estructurales omnipresentes en los productos naturales. A diferencia de la estructura de ciclohexano más grande y totalmente "consonante" , los ciclopentanos y sus derivados son " disonantes " según el modelo de Lapworth-Evans de polaridades alternas. La disonancia en la polaridad limita claramente las formas en que se pueden desconectar los ciclopentanos, lo que se hace evidente en la disminución del número de métodos generales disponibles para fabricar anillos de cinco miembros en comparación con los correspondientes anillos de seis miembros. Especialmente el hecho de que no exista un equivalente de Diels-Alder para la síntesis de anillos de cinco miembros preocupa desde hace muchas décadas a los químicos sintéticos. En consecuencia, después de que se descubrió el reordenamiento del vinilciclopropano alrededor de 1960, la comunidad sintética no tardó mucho en darse cuenta del potencial inherente para formar ciclopentenos mediante el reordenamiento del vinilciclopropano. A medida que el reordenamiento del vinilciclopropano avanzó como metodología y las condiciones de reacción mejoraron durante la década de 1970, las primeras síntesis totales que utilizaban el reordenamiento del vinilciclopropano comenzaron a aparecer alrededor de 1980. Las figuras clave para aplicar esta reacción en la síntesis total fueron Barry M. Trost , Elias J. Corey , Thomas Hudlicky, Leo A. Paquette ,
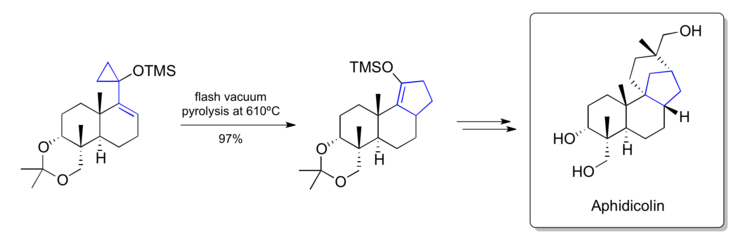
Una síntesis de la metodología de uso de Aphidicolin en torno al reordenamiento de vinilciclopropano desarrollada en su propio laboratorio. [40] Un paso clave convierte un siloxivinilciclopropano de última etapa en un ciclopenteno que contenía el esqueleto de carbono fusionado [6-6-5] que se encuentra dentro del producto natural. El producto se transforma en producto natural mediante manipulaciones adicionales.
La síntesis de zizaeno es otro ejemplo temprano de la aplicación de un reordenamiento de vinilciclopropano como desconexión clave. [41]

La metodología también se ha aplicado a la síntesis de hirsuteno [42] e isocomeno [43].

La transposición de cinilciclopropano se utilizó para construir el producto natural espirocíclico alfa-vetispireno en 1982. [44]

El anteridiogeno -An se preparó utilizando un reordenamiento de vinilciclopropano de etapa tardía mediado por ácido de Lewis. [45]

Se utilizó un reordenamiento de heteroátomo-vinilciclopropano catalizado por cobre para formar el núcleo de tetrahidrotiofeno de la biotina y la unidad de tiofeno de Plavix , respectivamente. [46]

Se utilizó una transposición de vinilciclopropano mediada por ácido para sintetizar el producto natural salviasperanol. [47]
