Los virus del herpes simple 1 y 2 ( HSV-1 y HSV-2 ), también conocidos por sus nombres taxonómicos Alfaherpesvirus humano 1 y Alfaherpesvirus humano 2 , son dos miembros de la familia Herpesviridae humana , un conjunto de virus que producen infecciones virales en su mayoría. de los humanos . [1] [2] Tanto el HSV-1 como el HSV-2 son muy comunes y contagiosos . Pueden transmitirse cuando una persona infectada comienza a eliminar el virus .
En 2016, alrededor del 67% de la población mundial menor de 50 años tenía HSV-1. [3] En los Estados Unidos, se estima que alrededor del 47,8 % y el 11,9 % tienen HSV-1 y HSV-2, respectivamente, aunque la prevalencia real puede ser mucho mayor. [4] Debido a que puede transmitirse a través de cualquier contacto íntimo, es una de las infecciones de transmisión sexual más comunes . [5]
Muchos de los infectados nunca desarrollan síntomas. [6] Los síntomas, cuando ocurren, pueden incluir ampollas acuosas en la piel de cualquier parte del cuerpo, o en las membranas mucosas de la boca, labios, nariz, genitales, [1] u ojos ( queratitis por herpes simple ). [7] Las lesiones curan con una costra característica de la enfermedad herpética. A veces, los virus causan síntomas leves o atípicos durante los brotes. Sin embargo, también pueden causar formas más problemáticas de herpes simple . Como virus neurotrópicos y neuroinvasivos , HSV-1 y -2 persisten en el cuerpo ocultándose del sistema inmunológico en los cuerpos celulares de las neuronas , particularmente en los ganglios sensoriales. Después de la infección inicial o primaria, algunas personas infectadas experimentan episodios esporádicos de reactivación o brotes virales. En un brote, el virus en una célula nerviosa se activa y se transporta a través del axón de la neurona a la piel, donde se produce la replicación y eliminación del virus y puede causar nuevas llagas. [8]
HSV-1 y HSV-2 se transmiten por contacto con una persona infectada que tiene reactivaciones del virus. HSV 1 y HSV-2 se eliminan periódicamente, con mayor frecuencia de forma asintomática. [ cita necesaria ]
En un estudio de personas con un primer episodio de infección genital por HSV-1 de 2022, la excreción genital de HSV-1 se detectó en el 12 % de los días a los 2 meses y disminuyó significativamente al 7 % de los días a los 11 meses. La mayor parte de la muda genital fue asintomática; las lesiones genitales y orales y la excreción oral fueron raras. [9]
La mayoría de las transmisiones sexuales del HSV-2 ocurren durante períodos de eliminación asintomática . [10] La reactivación asintomática significa que el virus causa síntomas atípicos, sutiles o difíciles de notar que no se identifican como una infección activa por herpes, por lo que es posible contraer el virus incluso si no hay ampollas o llagas activas por HSV. En un estudio, las muestras diarias de hisopos genitales detectaron HSV-2 en una mediana de 12 a 28 % de los días entre aquellos que tuvieron un brote y 10 % de los días entre aquellos con infección asintomática (sin brotes previos), siendo muchos de estos episodios que ocurre sin brote visible ("excreción subclínica"). [11]
En otro estudio, 73 sujetos fueron aleatorizados para recibir valaciclovir 1 g diario o placebo durante 60 días cada uno en un diseño cruzado de dos vías . Se recogió un hisopo diario del área genital para la detección del HSV-2 mediante reacción en cadena de la polimerasa, para comparar el efecto de valaciclovir versus placebo sobre la diseminación viral asintomática en sujetos inmunocompetentes seropositivos para el HSV-2 sin antecedentes de infección sintomática por herpes genital. El estudio encontró que valaciclovir redujo significativamente la eliminación durante los días subclínicos en comparación con el placebo, mostrando una reducción del 71 %; El 84% de los sujetos no tuvo pérdida de secreción mientras recibían valaciclovir frente al 54% de los sujetos que recibían placebo. Alrededor del 88% de los pacientes tratados con valaciclovir no tuvieron signos o síntomas reconocidos frente al 77% de los tratados con placebo. [12]
En el caso del HSV-2, la diseminación subclínica puede representar la mayor parte de la transmisión. [11] Los estudios sobre parejas discordantes (una infectada con HSV-2, otra no) muestran que la tasa de transmisión es aproximadamente de 5 a 8,9 por cada 10.000 contactos sexuales, y el uso de condones reduce en gran medida el riesgo de adquisición. [13] Los síntomas atípicos a menudo se atribuyen a otras causas, como una candidiasis . [14] [15] El HSV-1 a menudo se adquiere por vía oral durante la infancia. También puede transmitirse sexualmente, incluido el contacto con la saliva, como los besos y el sexo oral . [16] Históricamente, el VHS-2 era principalmente una infección de transmisión sexual, pero las tasas de infecciones genitales por VHS-1 han aumentado durante las últimas décadas. [14]
Ambos virus también pueden transmitirse verticalmente durante el parto. [17] [18] Sin embargo, el riesgo de transmisión es mínimo si la madre no presenta síntomas ni ampollas expuestas durante el parto. El riesgo es considerable cuando la madre se infecta con el virus por primera vez al final del embarazo, lo que refleja una alta carga viral. [19] Si bien la mayoría de las ETS virales no se pueden transmitir a través de objetos ya que el virus muere rápidamente fuera del cuerpo, el VHS puede sobrevivir hasta 4,5 horas en las superficies y puede transmitirse mediante el uso de toallas, cepillos de dientes, tazas, cubiertos, etc. [20] [21] [22] [23]
Los virus del herpes simple pueden afectar áreas de la piel expuestas al contacto con una persona infectada. Un ejemplo de esto es el panadizo herpético , que es una infección por herpes en los dedos; se encontraba comúnmente en las manos del cirujano dental antes del uso rutinario de guantes al tratar a los pacientes. Darle la mano a una persona infectada no transmite esta enfermedad. [24] La infección genital por HSV-2 aumenta el riesgo de contraer VIH . [25]
El HSV ha sido un virus modelo para muchos estudios en biología molecular. Por ejemplo, uno de los primeros promotores funcionales en eucariotas se descubrió en el HSV (del gen de la timidina quinasa ) y la proteína del virión VP16 es uno de los activadores transcripcionales más estudiados . [26]
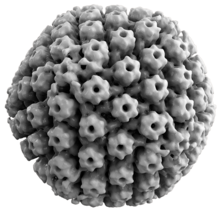

Todos los virus del herpes animal comparten algunas propiedades comunes. La estructura de los virus del herpes consiste en un genoma de ADN lineal, bicatenario y relativamente grande encerrado dentro de una jaula de proteínas icosaédrica llamada cápside , que está envuelta en una bicapa lipídica llamada envoltura . La envoltura está unida a la cápside mediante un tegumento . Esta partícula completa se conoce como virión . [27] HSV-1 y HSV-2 contienen cada uno al menos 74 genes (o marcos de lectura abiertos , ORF) dentro de sus genomas, [28] aunque la especulación sobre el hacinamiento de genes permite hasta 84 genes codificantes de proteínas únicos mediante 94 ORF putativos. [29] Estos genes codifican una variedad de proteínas involucradas en la formación de la cápside, el tegumento y la envoltura del virus, así como en el control de la replicación y la infectividad del virus. Estos genes y sus funciones se resumen en la siguiente tabla. [ cita necesaria ]
Los genomas de HSV-1 y HSV-2 son complejos y contienen dos regiones únicas llamadas región única larga (UL ) y región única corta (U S ). De los 74 ORF conocidos, UL contiene 56 genes virales, mientras que U S contiene sólo 12. [28] La transcripción de genes HSV está catalizada por la ARN polimerasa II del huésped infectado. [28] Los genes tempranos inmediatos , que codifican proteínas, por ejemplo, ICP22 [30] que regulan la expresión de genes virales tempranos y tardíos, son los primeros en expresarse después de la infección. Sigue la expresión genética temprana , para permitir la síntesis de enzimas involucradas en la replicación del ADN y la producción de ciertas glicoproteínas de la envoltura . La expresión de genes tardíos ocurre al final; Este grupo de genes codifica predominantemente proteínas que forman la partícula del virión. [28]
Cinco proteínas de (UL ) forman la cápside viral: UL6 , UL18, UL35, UL38 y la proteína principal de la cápside UL19. [27]
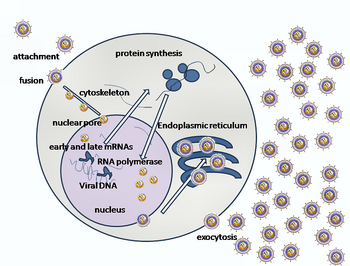
La entrada del HSV en una célula huésped implica que varias glicoproteínas en la superficie del virus envuelto se unen a sus receptores transmembrana en la superficie celular. Luego, la célula atrae muchos de estos receptores hacia adentro, lo que se cree que abre un anillo de tres heterodímeros gHgL que estabilizan una conformación compacta de la glicoproteína gB, de modo que salta y perfora la membrana celular. [31] La envoltura que cubre la partícula viral luego se fusiona con la membrana celular, creando un poro a través del cual el contenido de la envoltura viral ingresa a la célula huésped. [ cita necesaria ]
Las etapas secuenciales de entrada del HSV son análogas a las de otros virus . Al principio, los receptores complementarios del virus y la superficie celular acercan las membranas viral y celular. Las interacciones de estas moléculas forman entonces un poro de entrada estable a través del cual el contenido de la envoltura viral se introduce en la célula huésped. El virus también puede ser endocitosado después de unirse a los receptores, y la fusión podría ocurrir en el endosoma . En micrografías electrónicas, se han visto fusionadas las valvas externas de las bicapas lipídicas viral y celular; [32] esta hemifusión puede estar en el camino habitual de entrada o, por lo general, puede ser un estado detenido con mayor probabilidad de ser capturado que un mecanismo de entrada transitorio. [ cita necesaria ]
En el caso de un virus del herpes, las interacciones iniciales ocurren cuando dos glicoproteínas de la envoltura viral llamadas glicoproteína C (gC) y glicoproteína B (gB) se unen a un polisacárido de la superficie celular llamado heparán sulfato . A continuación, la principal proteína de unión al receptor, la glicoproteína D (gD), se une específicamente a al menos uno de los tres receptores de entrada conocidos. [33] Estos receptores celulares incluyen el mediador de entrada del herpesvirus ( HVEM ), nectina -1 y heparán sulfato sulfatado 3-O. Los receptores de nectina suelen producir adhesión célula-célula, para proporcionar un fuerte punto de unión del virus a la célula huésped. [31] Estas interacciones acercan las superficies de las membranas y permiten que otras glicoproteínas incrustadas en la envoltura viral interactúen con otras moléculas de la superficie celular. Una vez unida a HVEM, gD cambia su conformación e interactúa con las glicoproteínas virales H (gH) y L (gL), que forman un complejo. La interacción de estas proteínas de membrana puede dar lugar a un estado de hemifusión. La interacción de gB con el complejo gH/gL crea un poro de entrada para la cápside viral. [32] gB interactúa con los glucosaminoglicanos en la superficie de la célula huésped. [ cita necesaria ]
Después de que la cápside viral ingresa al citoplasma celular , comienza a expresar la proteína viral ICP27. ICP27 es una proteína reguladora que altera la síntesis de proteínas del huésped y la utiliza para la replicación viral. ICP27 se une a una enzima celular Serina-Arginina Proteína Quinasa 1, SRPK1 . La formación de este complejo hace que SRPK1 se desplace del citoplasma al núcleo y el genoma viral se transporta al núcleo celular . [34] Una vez unida al núcleo en un poro de entrada nuclear, la cápside expulsa su contenido de ADN a través del portal de la cápside. El portal de la cápsida está formado por 12 copias de la proteína portal, UL6, dispuestas en forma de anillo; Las proteínas contienen una secuencia de aminoácidos en cremallera de leucina , que les permite adherirse entre sí. [35] Cada cápside icosaédrica contiene un único portal, ubicado en un vértice . [36] [37] El ADN sale de la cápside en un único segmento lineal. [38]
El VHS evade el sistema inmunológico a través de la interferencia con la presentación del antígeno MHC clase I en la superficie celular, al bloquear el transportador asociado con el procesamiento de antígenos (TAP) inducido por la secreción de ICP-47 por el VHS. En la célula huésped, TAP transporta péptidos de epítopos de antígenos virales digeridos desde el citosol al retículo endoplásmico, lo que permite que estos epítopos se combinen con moléculas de MHC de clase I y se presenten en la superficie de la célula. La presentación de epítopos virales con MHC clase I es un requisito para la activación de los linfocitos T citotóxicos (CTL), los principales efectores de la respuesta inmune mediada por células contra las células infectadas por virus. ICP-47 previene el inicio de una respuesta CTL contra HSV, lo que permite que el virus sobreviva durante un período prolongado en el huésped. [39] El VHS generalmente produce un efecto citopático (CPE) dentro de las 24 a 72 horas posteriores a la infección en líneas celulares permisivas, que se observa mediante la formación de placa clásica. Sin embargo, también se han informado aislados clínicos de HSV-1 que no mostraron ningún CPE en cultivos de células Vero y A549 en varios pases con un nivel bajo de expresión de proteínas virales. Probablemente estos aislados de HSV-1 estén evolucionando hacia una forma más "críptica" para establecer una infección crónica, desentrañando así otra estrategia más para evadir el sistema inmunológico del huésped, además de la latencia neuronal. [40]

Después de la infección de una célula, se produce una cascada de proteínas del virus del herpes, denominadas inmediata-temprana, temprana y tardía. La investigación que utiliza citometría de flujo en otro miembro de la familia de los virus del herpes, el herpesvirus asociado al sarcoma de Kaposi , indica la posibilidad de una etapa lítica adicional , tardía. [41] Estas etapas de la infección lítica, particularmente la lítica tardía, son distintas de la etapa de latencia. En el caso del HSV-1, no se detectan productos proteicos durante la latencia, mientras que sí se detectan durante el ciclo lítico. [ cita necesaria ]
Las primeras proteínas transcritas se utilizan en la regulación de la replicación genética del virus. "Al ingresar a la célula, una proteína α-TIF se une a la partícula viral y ayuda en la transcripción inmediata-temprana ". La proteína de cierre del huésped del virión (VHS o UL41) es muy importante para la replicación viral. [42] Esta enzima interrumpe la síntesis de proteínas en el huésped, degrada el ARNm del huésped , ayuda en la replicación viral y regula la expresión genética de las proteínas virales. El genoma viral viaja inmediatamente al núcleo, pero la proteína VHS permanece en el citoplasma. [43] [44]
Las proteínas tardías forman la cápside y los receptores en la superficie del virus. El empaquetado de las partículas virales, incluidos el genoma , el núcleo y la cápside, se produce en el núcleo de la célula. Aquí, los concatémeros del genoma viral se separan mediante escisión y se colocan en cápsides formadas. HSV-1 sufre un proceso de envolvimiento primario y secundario. La envoltura primaria se adquiere por gemación en la membrana nuclear interna de la célula. Luego se fusiona con la membrana nuclear externa. El virus adquiere su envoltura final mediante la gemación en vesículas citoplasmáticas . [45]
Los VHS pueden persistir en una forma inactiva pero persistente conocida como infección latente, especialmente en los ganglios neurales . [1] El ADN circular del genoma del HSV reside en el núcleo celular como un episoma . [46] HSV-1 tiende a residir en los ganglios trigéminos , mientras que HSV-2 tiende a residir en los ganglios sacros , pero estas son tendencias históricas únicamente. Durante la infección latente de una célula, los HSV expresan ARN de transcripción asociada a latencia (LAT) . LAT regula el genoma de la célula huésped e interfiere con los mecanismos naturales de muerte celular. Al mantener las células huésped, la expresión de LAT preserva un reservorio del virus, lo que permite recurrencias periódicas o "brotes" posteriores, generalmente sintomáticos, característicos de la no latencia. Independientemente de que las recurrencias sean sintomáticas o no, la diseminación viral ocurre para infectar a un nuevo huésped. [ cita necesaria ]
Una proteína que se encuentra en las neuronas puede unirse al ADN del virus del herpes y regular la latencia . El ADN del virus del herpes contiene un gen para una proteína llamada ICP4, que es un importante transactivador de genes asociados con la infección lítica en HSV-1. [47] Los elementos que rodean el gen de ICP4 se unen a una proteína conocida como factor de silenciamiento restrictivo neuronal de proteína neuronal humana (NRSF) o factor de transcripción silenciador de elemento represor humano (REST) . Cuando se une a los elementos del ADN viral, se produce la desacetilación de histonas encima de la secuencia del gen ICP4 para evitar el inicio de la transcripción a partir de este gen, evitando así la transcripción de otros genes virales implicados en el ciclo lítico. [47] [48] Otra proteína del HSV revierte la inhibición de la síntesis de la proteína ICP4. ICP0 disocia NRSF del gen ICP4 y así previene el silenciamiento del ADN viral. [49]
El genoma del HSV abarca aproximadamente 150.000 pb y consta de dos segmentos únicos, denominados único largo (UL) y único corto (US), así como repeticiones terminales invertidas que se encuentran en los dos extremos de ellos denominadas repetición larga (RL) y repetición corta ( RS). También hay elementos menores de "redundancia terminal" (α) que se encuentran en los extremos más alejados de RS. La disposición general es RL-UL-RL-α-RS-US-RS-α y cada par de repeticiones se invierten entre sí. Luego, toda la secuencia se encapsula en una repetición directa terminal. Las partes larga y corta tienen cada una sus propios orígenes de replicación , con OriL ubicado entre UL28 y UL30 y OriS ubicado en un par cerca de RS. [50] Como los segmentos L y S se pueden ensamblar en cualquier dirección, se pueden invertir libremente entre sí, formando varios isómeros lineales. [51]
Los genes del HSV se expresan en 3 clases temporales: genes tempranos inmediatos (IE o α), tempranos (E o ß) y tardíos (γ). Sin embargo, la progresión de la expresión de genes virales es más bien gradual que en etapas claramente distintas. Los genes tempranos inmediatos se transcriben inmediatamente después de la infección y sus productos genéticos activan la transcripción de los genes tempranos. Los primeros productos genéticos ayudan a replicar el ADN viral. La replicación del ADN viral , a su vez, estimula la expresión de los genes tardíos que codifican las proteínas estructurales. [26]
La transcripción de los genes tempranos inmediatos (IE) comienza inmediatamente después de que el ADN del virus ingresa al núcleo. Todos los genes del virus son transcritos por la ARN polimerasa II del huésped . Aunque las proteínas del huésped son suficientes para la transcripción del virus, las proteínas virales son necesarias para la transcripción de ciertos genes. [26] Por ejemplo, VP16 desempeña un papel importante en la transcripción de IE y la partícula del virus aparentemente lo introduce en la célula huésped, por lo que no es necesario producirlo primero. De manera similar, las proteínas IE RS1 (ICP4), UL54 (ICP27) e ICP0 promueven la transcripción de los genes tempranos (E). Al igual que los genes IE, los promotores de genes tempranos contienen sitios de unión para factores de transcripción celular. Una proteína temprana, ICP8, es necesaria tanto para la transcripción de genes tardíos como para la replicación del ADN. [26]
Más adelante en el ciclo de vida del HSV, se cierra la expresión de genes tempranos e inmediatos. Esto está mediado por proteínas virales específicas, por ejemplo, ICP4, que se reprime uniéndose a elementos de su propio promotor. Como consecuencia, la regulación negativa de los niveles de ICP4 conduce a una reducción de la expresión genética temprana y tardía, ya que ICP4 es importante para ambos. [26]
Es importante destacar que el VHS desactiva la síntesis de ARN, ADN y proteínas de la célula huésped para dirigir los recursos celulares a la producción de virus. En primer lugar, la proteína del virus vhs induce la degradación de los ARNm existentes en las primeras etapas de la infección. Otros genes virales impiden la transcripción y traducción celular. Por ejemplo, ICP27 inhibe el empalme del ARN , de modo que los ARNm del virus (que normalmente no están empalmados) obtienen una ventaja sobre los ARNm del huésped. Finalmente, las proteínas del virus desestabilizan ciertas proteínas celulares implicadas en el ciclo de la célula huésped , de modo que tanto la división celular como la replicación del ADN de la célula huésped se perturban a favor de la replicación del virus. [26]
Los genomas del herpes simple 1 se pueden clasificar en seis clados . [57] Cuatro de ellos ocurren en África Oriental , uno en Asia Oriental y otro en Europa y América del Norte . Esto sugiere que el virus pudo haberse originado en África Oriental. El ancestro común más reciente de las cepas euroasiáticas parece haber evolucionado hace unos 60.000 años. [58] Los aislamientos de HSV-1 de Asia Oriental tienen un patrón inusual que actualmente se explica mejor por las dos oleadas de migración responsables del poblamiento de Japón . [58]
Los genomas del herpes simplex 2 se pueden dividir en dos grupos: uno está distribuido globalmente y el otro se limita principalmente al África subsahariana . [59] El genotipo distribuido globalmente ha experimentado cuatro recombinaciones antiguas con herpes simple 1. También se ha informado que HSV-1 y HSV-2 pueden tener eventos de recombinación contemporáneos y estables en huéspedes infectados simultáneamente con ambos patógenos. En todos los casos, el VHS-2 adquiere partes del genoma del VHS-1, y a veces cambia partes de su epítopo antigénico en el proceso. [60]
Se ha estimado que la tasa de mutación es ~1,38×10 −7 sustituciones/sitio/año. [57] En el ámbito clínico, las mutaciones en el gen de la timidina quinasa o en el gen de la ADN polimerasa han causado resistencia al aciclovir . Sin embargo, la mayoría de las mutaciones ocurren en el gen de la timidina quinasa y no en el gen de la ADN polimerasa. [61]
Otro análisis ha estimado que la tasa de mutación en el genoma del herpes simple 1 es de 1,82 × 10 −8 sustitución de nucleótidos por sitio por año. Este análisis sitúa al ancestro común más reciente de este virus hace unos 710.000 años. [62]
Herpes simplex 1 y 2 divergieron hace unos 6 millones de años . [60]
Al igual que otros herpesviridae , los virus del herpes simple establecen una infección latente de por vida y, por lo tanto, no pueden erradicarse del cuerpo con los tratamientos actuales. [63]
El tratamiento suele incluir medicamentos antivirales de uso general que interfieren con la replicación viral, reducen la gravedad física de las lesiones asociadas a los brotes y reducen las posibilidades de transmisión a otras personas. Los estudios de poblaciones de pacientes vulnerables han indicado que el uso diario de antivirales como aciclovir [64] y valaciclovir puede reducir las tasas de reactivación. [15] El uso extensivo de medicamentos antiherpéticos ha llevado al desarrollo de cierta resistencia a los medicamentos , [ cita necesaria ] que a su vez puede conducir al fracaso del tratamiento. Por lo tanto, se investigan ampliamente nuevas fuentes de medicamentos para abordar el problema. En enero de 2020, se publicó un artículo de revisión completo que demostró la eficacia de los productos naturales como fármacos prometedores contra el VHS. [65] La piritiona , un ionóforo de zinc , ha demostrado actividad antiviral contra el herpes simple. [66]
En 1979, se informó que existe un posible vínculo entre el HSV-1 y la enfermedad de Alzheimer , en personas con el alelo épsilon4 del gen APOE . [67] HSV-1 parece ser particularmente dañino para el sistema nervioso y aumenta el riesgo de desarrollar la enfermedad de Alzheimer. El virus interactúa con los componentes y receptores de las lipoproteínas , lo que puede conducir al desarrollo de la enfermedad de Alzheimer. [68] Esta investigación identifica los VHS como el patógeno más claramente relacionado con el establecimiento de la enfermedad de Alzheimer. [69] Según un estudio realizado en 1997, sin la presencia del alelo genético , HSV-1 no parece causar ningún daño neurológico ni aumentar el riesgo de Alzheimer. [70] Sin embargo, un estudio prospectivo más reciente publicado en 2008 con una cohorte de 591 personas mostró una diferencia estadísticamente significativa entre los pacientes con anticuerpos que indicaban una reactivación reciente del VHS y aquellos sin estos anticuerpos en la incidencia de la enfermedad de Alzheimer, sin correlación directa con la Alelo APOE-épsilon4. [71]
El ensayo contó con una pequeña muestra de pacientes que no tenían el anticuerpo al inicio del estudio, por lo que los resultados deben considerarse muy inciertos . En 2011, científicos de la Universidad de Manchester demostraron que el tratamiento de células infectadas por HSV1 con agentes antivirales disminuía la acumulación de proteína β-amiloide y tau y también disminuía la replicación de HSV-1. [72]
Un estudio retrospectivo realizado en Taiwán en 2018 sobre 33.000 pacientes encontró que estar infectado con el virus del herpes simple aumentaba el riesgo de demencia 2,56 veces (IC 95%: 2,3-2,8) en pacientes que no recibían medicamentos antiherpéticos (2,6 veces para infecciones por HSV-1 y 2,0 veces para infecciones por HSV-2). Sin embargo, los pacientes infectados por HSV que estaban recibiendo medicamentos antiherpéticos (p. ej., aciclovir , famciclovir , ganciclovir , idoxuridina , penciclovir , tromantadina , valaciclovir o valganciclovir ) no mostraron un riesgo elevado de demencia en comparación con los pacientes no infectados por HSV. [73]
La reactivación de multiplicidad (MR) es el proceso mediante el cual los genomas virales que contienen daño inactivante interactúan dentro de una célula infectada para formar un genoma viral viable. La RM se descubrió originalmente con el bacteriófago T4 del virus bacteriano, pero posteriormente también se encontró con virus patógenos, incluidos el virus de la influenza, el VIH-1, el virus del adenovirus simio 40, el virus vaccinia, el reovirus, el poliovirus y el virus del herpes simple. [74]
Cuando las partículas de HSV se exponen a dosis de un agente que daña el ADN que sería letal en infecciones únicas, pero luego se les permite sufrir infecciones múltiples (es decir, dos o más virus por célula huésped), se observa RM. La supervivencia mejorada del HSV-1 debido a la RM ocurre tras la exposición a diferentes agentes que dañan el ADN, incluido el metanosulfonato de metilo , [75] trimetilpsoraleno (que causa enlaces cruzados entre cadenas de ADN), [76] [77] y luz ultravioleta. [78] Después del tratamiento del HSV genéticamente marcado con trimetilpsoraleno, la recombinación entre los virus marcados aumenta, lo que sugiere que el daño del trimetilpsoraleno estimula la recombinación. [76] La RM del VHS parece depender parcialmente de la maquinaria de reparación recombinante de la célula huésped, ya que las células de fibroblastos de la piel defectuosas en un componente de esta maquinaria (es decir, células de pacientes con síndrome de Bloom) son deficientes en la RM. [78]
Estas observaciones sugieren que la RM en las infecciones por HSV implica una recombinación genética entre genomas virales dañados que da como resultado la producción de una progenie de virus viables. HSV-1, al infectar las células huésped, induce inflamación y estrés oxidativo. [79] Por lo tanto, parece que el genoma del HSV puede estar sujeto a daño oxidativo del ADN durante la infección, y que la RM puede mejorar la supervivencia y la virulencia viral en estas condiciones. [ cita necesaria ]
El virus del herpes simple modificado se considera una terapia potencial para el cáncer y ha sido ampliamente probado clínicamente para evaluar su capacidad oncolítica (eliminar el cáncer). [80] Los datos provisionales de supervivencia general del ensayo de fase 3 de Amgen de un virus del herpes genéticamente atenuado sugieren eficacia contra el melanoma . [81]
El virus del herpes simple también se utiliza como trazador transneuronal que define conexiones entre neuronas en virtud de atravesar sinapsis. [82]
HSV-2 es la causa más común de meningitis de Mollaret . [83] El VHS-1 puede provocar casos potencialmente mortales de encefalitis por herpes simple . [84] Los virus del herpes simple también se han estudiado en los trastornos del sistema nervioso central como la esclerosis múltiple , pero las investigaciones han sido contradictorias y no concluyentes. [85]
Tras un diagnóstico de infección por herpes simple genital, los pacientes pueden desarrollar un episodio de depresión profunda . Además de ofrecer medicamentos antivirales para aliviar los síntomas y acortar su duración, los médicos también deben abordar el impacto de un nuevo diagnóstico en la salud mental. Proporcionar información sobre la altísima prevalencia de estas infecciones, sus tratamientos efectivos y futuras terapias en desarrollo puede brindar esperanza a pacientes que de otro modo estarían desmoralizados. [ cita necesaria ]
Existen vacunas de uso común para algunos herpesvirus, como la vacuna veterinaria HVT/LT (vacuna contra la laringotraqueítis vectorial del herpesvirus de Turquía). Sin embargo, previene la aterosclerosis (que histológicamente refleja la aterosclerosis en humanos) en los animales vacunados. [86] [87] Las únicas vacunas humanas disponibles para los herpesvirus son las del virus Varicella zoster , que se administran a niños alrededor de su primer cumpleaños para prevenir la varicela (varicela) o a adultos para prevenir un brote de culebrilla (herpes zoster). Sin embargo, no existe ninguna vacuna humana contra los virus del herpes simple. A partir de 2022, se están realizando estudios clínicos y preclínicos activos sobre el herpes simple en humanos; Se están desarrollando vacunas tanto para el tratamiento como para la prevención. [ cita necesaria ]