
Staphylococcus aureus resistente a la meticilina ( MRSA ) es un grupo de bacterias grampositivas que son genéticamente distintas de otras cepas de Staphylococcus aureus . MRSA es responsable de varias infecciones difíciles de tratar en humanos. Causó más de 100.000 muertes en todo el mundo atribuibles a la resistencia a los antimicrobianos en 2019.
MRSA es cualquier cepa de S. aureus que ha desarrollado (mediante selección natural ) o adquirido (mediante transferencia horizontal de genes ) una resistencia múltiple a los antibióticos betalactámicos . Los antibióticos betalactámicos (β-lactámicos) son un grupo de amplio espectro que incluye algunos penams ( derivados de la penicilina como la meticilina y la oxacilina ) y cefemas como las cefalosporinas . [1] Las cepas que no pueden resistir estos antibióticos se clasifican como S. aureus sensible a la meticilina o MSSA.
La infección por MRSA es común en hospitales, prisiones y residencias de ancianos, donde las personas con heridas abiertas , dispositivos invasivos como catéteres y sistemas inmunitarios debilitados corren un mayor riesgo de sufrir infecciones asociadas a la atención sanitaria . MRSA comenzó como una infección adquirida en hospitales, pero ahora se adquiere en la comunidad y en el ganado. Los términos HA-MRSA (MRSA asociado a la atención médica o adquirido en un hospital), CA-MRSA (MRSA asociado a la comunidad) y LA-MRSA (MRSA asociado al ganado) reflejan esto. [ cita necesaria ]

En los seres humanos, Staphylococcus aureus forma parte de la microbiota normal presente en el tracto respiratorio superior [2] , en la piel y en la mucosa intestinal. [3] Sin embargo, junto con especies bacterianas similares que pueden colonizar y actuar simbióticamente, pueden causar enfermedades si comienzan a apoderarse de los tejidos que han colonizado o invaden otros tejidos; la infección resultante se ha denominado "patobionte". [2]
Después de 72 horas, MRSA puede arraigarse en los tejidos humanos y eventualmente volverse resistente al tratamiento. La presentación inicial de MRSA son pequeñas protuberancias rojas que se asemejan a granos, picaduras de araña o forúnculos; pueden ir acompañados de fiebre y, ocasionalmente, erupciones cutáneas. Al cabo de unos días, los bultos se vuelven más grandes y dolorosos; eventualmente se abren en forúnculos profundos llenos de pus. Alrededor del 75 por ciento de las infecciones por CA-MRSA se localizan en la piel y los tejidos blandos y, por lo general, pueden tratarse de forma eficaz. [4]
Algunas de las poblaciones en riesgo incluyen:
Hasta el 22% de las personas infectadas con MRSA no tienen ningún factor de riesgo discernible. [21] : 637
Las personas hospitalizadas, incluidos los ancianos, suelen estar inmunocomprometidas y son susceptibles a infecciones de todo tipo, incluido MRSA; Una infección por MRSA se llama S. aureus resistente a la meticilina asociada a la atención médica o adquirida en el hospital (HA-MRSA). [1] [5] [22] [23] Generalmente, las personas infectadas por MRSA permanecen infectadas por poco menos de 10 días, si son tratadas por un médico, aunque los efectos pueden variar de persona a persona. [24]
Tanto las heridas quirúrgicas como las no quirúrgicas pueden infectarse con HA-MRSA. [1] [5] [22] Las infecciones del sitio quirúrgico ocurren en la superficie de la piel, pero pueden extenderse a los órganos internos y a la sangre y causar sepsis . [1] La transmisión puede ocurrir entre proveedores de atención médica y pacientes porque algunos proveedores pueden descuidar el lavado de manos preventivo entre exámenes. [12] [25]
Las personas en hogares de ancianos corren riesgo por todas las razones mencionadas anteriormente, complicadas aún más por sus sistemas inmunológicos generalmente más débiles. [13] [26]
Las prisiones y los cuarteles militares [19] pueden estar abarrotados y confinados, y pueden proliferar malas condiciones de higiene, lo que pone a los habitantes en mayor riesgo de contraer MRSA. [18] Los casos de MRSA en dichas poblaciones se informaron por primera vez en los Estados Unidos y luego en Canadá. Los primeros informes fueron realizados por los Centros para el Control y la Prevención de Enfermedades en las prisiones estatales de Estados Unidos. En los medios de comunicación aparecieron cientos de informes sobre brotes de MRSA en prisiones entre 2000 y 2008. Por ejemplo, en febrero de 2008, la cárcel del condado de Tulsa en Oklahoma comenzó a tratar un promedio de 12 casos de S. aureus por mes. [27]
El uso de antibióticos en el ganado aumenta el riesgo de que se desarrolle MRSA entre el ganado y otros animales que puedan residir cerca de ellos; Las cepas MRSA ST398 y CC398 son transmisibles a los humanos. [19] [28] Generalmente, los animales son asintomáticos. [1]
Las mascotas domésticas son susceptibles a la infección por MRSA por transmisión de sus dueños; por el contrario, las mascotas infectadas con MRSA también pueden transmitir MRSA a los humanos. [29]
Los vestuarios , gimnasios e instalaciones deportivas relacionadas ofrecen sitios potenciales para la contaminación e infección por MRSA. [30] Los atletas han sido identificados como un grupo de alto riesgo. [19] Un estudio vinculó el MRSA con las abrasiones causadas por el césped artificial . [31] Tres estudios realizados por el Departamento de Salud del Estado de Texas encontraron que la tasa de infección entre los jugadores de fútbol era 16 veces el promedio nacional. En octubre de 2006, un jugador de fútbol de la escuela secundaria quedó temporalmente paralizado por quemaduras en el césped infectadas con MRSA. Su infección volvió en enero de 2007 y requirió tres cirugías para extirpar el tejido infectado y tres semanas de estancia en el hospital. [32]
En 2013, Lawrence Tynes , Carl Nicks y Johnthan Banks de los Tampa Bay Buccaneers fueron diagnosticados con MRSA. Tynes y Nicks aparentemente no contrajeron la infección el uno del otro, pero se desconoce si Banks la contrajo de alguno de los individuos. [33] En 2015, el jugador de cuadro de los Dodgers de Los Ángeles, Justin Turner, se infectó mientras el equipo visitaba a los Mets de Nueva York . [34] En octubre de 2015, el ala cerrada de los New York Giants, Daniel Fells, fue hospitalizado con una infección grave por MRSA. [35]
MRSA se está convirtiendo en un problema crítico en los niños; [36] Los estudios encontraron que el 4,6% de los pacientes en centros de atención médica de EE. UU., (presumiblemente) incluidas las guarderías de los hospitales, [37] estaban infectados o colonizados con MRSA. [38] Los niños y adultos que entran en contacto con guarderías, [19] parques infantiles, vestuarios, campamentos, dormitorios, aulas y otros entornos escolares, gimnasios e instalaciones para hacer ejercicio tienen un mayor riesgo de contraer MRSA. Los padres deben tener especial cuidado con los niños que participan en actividades en las que se comparte equipo deportivo, como cascos y uniformes de fútbol. [39]
Los medicamentos que requieren agujas han provocado un aumento de MRSA, [40] y el uso de drogas inyectables (UDI) representa el 24,1% (1.839 personas) del sistema de alta del Hospital de Tennessee. Los métodos de inyección insalubres crean un punto de acceso para que el MRSA ingrese al torrente sanguíneo y comience a infectar al huésped. Además, con la alta tasa de contagio de MRSA, [11] un factor de riesgo común son las personas que están en contacto constante con alguien que se ha inyectado drogas durante el último año.
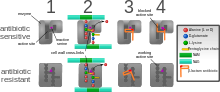
La resistencia a los antimicrobianos tiene una base genética; la resistencia está mediada por la adquisición de elementos genéticos extracromosómicos que contienen genes que confieren resistencia a ciertos antibióticos. Ejemplos de tales elementos incluyen plásmidos , elementos genéticos transponibles e islas genómicas , que pueden transferirse entre bacterias mediante transferencia horizontal de genes . [41] Una característica definitoria de MRSA es su capacidad para prosperar en presencia de antibióticos similares a la penicilina , que normalmente previenen el crecimiento bacteriano al inhibir la síntesis del material de la pared celular . Esto se debe a un gen de resistencia, mecA , que impide que los antibióticos β-lactámicos inactiven las enzimas (transpeptidasas) críticas para la síntesis de la pared celular. [42]
El cromosoma mec del casete estafilocócico ( SCC mec ) es una isla genómica de origen desconocido que contiene el gen de resistencia a los antibióticos mecA . [43] [44] SCC mec contiene genes adicionales además de mecA , incluido el gen de citolisina psm-mec , que puede suprimir la virulencia en cepas de MRSA adquiridas por HA. [45] Además, este locus codifica ARN reguladores de genes dependientes de cepa conocidos como ARN psm-mec . [46] SCC mec también contiene ccrA y ccrB ; ambos genes codifican recombinasas que median la integración específica del sitio y la escisión del elemento mec SCC del cromosoma S. aureus . [43] [44] Actualmente, se han identificado seis tipos únicos de mec de SCC que varían en tamaño de 21 a 67 kb; [43] se denominan tipos I a VI y se distinguen por la variación en los complejos de genes mec y ccr . [41] Debido al tamaño del elemento mec del SCC y a las limitaciones de la transferencia horizontal de genes, se cree que un mínimo de cinco clones son responsables de la propagación de las infecciones por MRSA, siendo el complejo clonal (CC) 8 el más prevalente. [43] [47] Se cree que SCC mec se originó en la especie estrechamente relacionada Staphylococcus sciuri y se transfirió horizontalmente a S. aureus. [48]
Los diferentes genotipos de SCC mec confieren diferentes características microbiológicas, como diferentes tasas de resistencia a los antimicrobianos. [49] Los diferentes genotipos también se asocian con diferentes tipos de infecciones. Los tipos I-III SCC mec son elementos grandes que normalmente contienen genes de resistencia adicionales y se aíslan característicamente de cepas HA-MRSA. [44] [49] Por el contrario, CA-MRSA se asocia con los tipos IV y V, que son más pequeños y carecen de genes de resistencia distintos de mecA . [44] [49]
Estas distinciones fueron investigadas a fondo por Collins et al. en 2001, y puede explicarse por las diferencias de aptitud asociadas con el transporte de un plásmido mec SCC grande o pequeño . El transporte de plásmidos grandes, como SCC mec I-III, es costoso para las bacterias, lo que resulta en una disminución compensatoria en la expresión de virulencia . [50] MRSA puede prosperar en entornos hospitalarios con mayor resistencia a los antibióticos pero menor virulencia: HA-MRSA se dirige a huéspedes hospitalizados inmunocomprometidos, por lo que una disminución de la virulencia no es una mala adaptación. [50] Por el contrario, CA-MRSA tiende a tener elementos mec SCC de menor costo de aptitud física para compensar el aumento de virulencia y expresión de toxicidad necesarios para infectar huéspedes sanos. [50]
mecA es un gen biomarcador responsable de la resistencia a la meticilina y otros antibióticos β-lactámicos. Después de la adquisición de mecA , el gen debe integrarse y localizarse en el cromosoma de S. aureus . [43] mecA codifica la proteína transportadora de penicilina 2a (PBP2a), que se diferencia de otras proteínas transportadoras de penicilina en que su sitio activo no se une a meticilina ni a otros antibióticos β-lactámicos. [43] Como tal, PBP2a puede continuar catalizando la reacción de transpeptidación requerida para elentrecruzamiento de peptidoglicanos , lo que permite la síntesis de la pared celular incluso en presencia de antibióticos. Como consecuencia de la incapacidad de PBP2a para interactuar con restos de β-lactámicos, la adquisición de mecA confiere resistencia a todos los antibióticos β-lactámicos además de la meticilina. [43] [51]
mecA está bajo el control de dos genes reguladores , mecI y mecR1 . MecI suele estar unido al promotor mecA y funciona como represor . [41] [44] En presencia de un antibiótico β-lactámico, MecR1 inicia una cascada de transducción de señales que conduce a la activación transcripcional de mecA . [41] [44] Esto se logra mediante la escisión de MecI mediada por MecR1, que alivia la represión de MecI. [41] mecA está controlado además por dos correpresores, blaI y blaR1 . blaI y blaR1 son homólogos de mecI y mecR1 , respectivamente, y normalmente funcionan como reguladores de blaZ , que es responsable de la resistencia a la penicilina. [43] [52] Las secuencias de ADN unidas por mecI y blaI son idénticas; [43] por lo tanto, blaI también puede unirse al operador mecA para reprimir la transcripción de mecA . [52]
El elemento móvil catabólico de arginina (ACME) es un factor de virulencia presente en muchas cepas de MRSA pero no prevalente en MSSA. [53] ACME SpeG positivo compensa la hipersensibilidad a las poliaminas de S. aureus y facilita la colonización estable de la piel, la infección de heridas y la transmisión de persona a persona. [54]
La adquisición de SCC mec en S. aureus sensible a meticilina (MSSA) da lugar a varios linajes de MRSA genéticamente diferentes. Estas variaciones genéticas dentro de diferentes cepas de MRSA posiblemente expliquen la variabilidad en la virulencia y las infecciones por MRSA asociadas. [55] La primera cepa de MRSA, ST250 MRSA-1, se originó a partir de la integración de SCC mec y ST250-MSSA. [55] Históricamente, los principales clones de MRSA ST2470-MRSA-I, ST239-MRSA-III, ST5-MRSA-II y ST5-MRSA-IV fueron responsables de causar infecciones por MRSA adquirida en el hospital (HA-MRSA). [55] ST239-MRSA-III, conocido como clon brasileño, era altamente transmisible en comparación con otros y se distribuía en Argentina, República Checa y Portugal. [55]
En el Reino Unido, las cepas más comunes de MRSA son EMRSA15 y EMRSA16. [56] Se ha descubierto que EMRSA16 es idéntica a la cepa ST 36:USA200, que circula en los Estados Unidos, y que porta los genes SCC mec tipo II, enterotoxina A y toxina 1 del síndrome de shock tóxico . [57] Según el nuevo sistema de tipificación internacional, esta cepa ahora se llama MRSA252. También se descubre que EMRSA 15 es una de las cepas de MRSA comunes en Asia. Otras cepas comunes incluyen ST5:USA100 y EMRSA 1. [58] Estas cepas son características genéticas de HA-MRSA. [59]
Las cepas de MRSA adquiridas en la comunidad (CA-MRSA) surgieron entre finales de 1990 y 2000 e infectaron a personas sanas que no habían estado en contacto con centros de atención médica. [59] Los investigadores sugieren que CA-MRSA no evolucionó a partir de HA-MRSA. [59] Esto se demuestra aún más mediante la tipificación molecular de las cepas de CA-MRSA [60] y la comparación del genoma entre CA-MRSA y HA-MRSA, que indican que las nuevas cepas de MRSA integraron SCC mec en MSSA por separado. [59] A mediados de 2000, CA-MRSA se introdujo en los sistemas de atención médica y distinguir CA-MRSA de HA-MRSA se convirtió en un proceso difícil. [59] El MRSA adquirido en la comunidad se trata más fácilmente y es más virulento que el MRSA adquirido en el hospital (HA-MRSA). [59] El mecanismo genético para la mayor virulencia en CA-MRSA sigue siendo un área activa de investigación. Los genes de leucocidina Panton-Valentine (PVL) son de particular interés porque son una característica única de CA-MRSA. [55]
En los Estados Unidos, la mayoría de los casos de CA-MRSA son causados por una cepa CC8 denominada ST8:USA300 , que porta SCC mec tipo IV, leucocidina Panton-Valentine , PSM-alfa y enterotoxinas Q y K, [57] y ST1:USA400. . [61] La cepa ST8:USA300 produce infecciones de la piel, fascitis necrotizante y síndrome de shock tóxico, mientras que la cepa ST1:USA400 produce neumonía necrotizante y sepsis pulmonar. [55] Otras cepas de MRSA adquiridas en la comunidad son ST8:USA500 y ST59:USA1000. En muchos países del mundo, las cepas de MRSA con diferentes tipos de antecedentes genéticos han llegado a predominar entre las cepas de CA-MRSA; USA300 encabeza fácilmente la lista en los EE. UU. y se está volviendo más común en Canadá después de su primera aparición allí en 2004. Por ejemplo, en Australia, las cepas ST93 son comunes, mientras que en Europa continental predominan las cepas ST80, que portan SCC mec tipo IV. [62] [63] En Taiwán, las cepas ST59, algunas de las cuales son resistentes a muchos antibióticos no betalactámicos, han surgido como causas comunes de infecciones de la piel y los tejidos blandos en la comunidad. En una región remota de Alaska, a diferencia de la mayor parte de los EE. UU. continentales, USA300 se encontró raramente en un estudio de cepas de MRSA de brotes de 1996 y 2000, así como en la vigilancia de 2004 a 2006. [64]
Una cepa de MRSA, CC398 , se encuentra en animales de producción criados intensivamente (principalmente cerdos, pero también ganado vacuno y aves de corral), donde puede transmitirse a los humanos como LA-MRSA (MRSA asociado al ganado). [58] [65] [66]


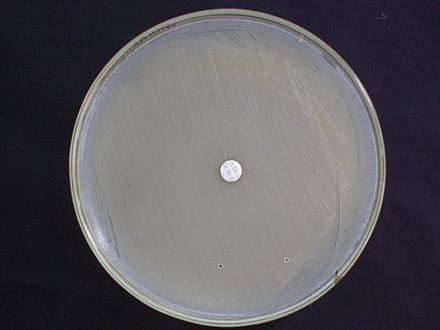
Los laboratorios de microbiología de diagnóstico y los laboratorios de referencia son clave para identificar brotes de MRSA. Normalmente, una bacteria debe cultivarse a partir de muestras de sangre, orina, esputo u otros fluidos corporales, y en cantidades suficientes para realizar pruebas de confirmación desde el principio. Aún así, debido a que no existe un método rápido y fácil para diagnosticar MRSA, el tratamiento inicial de la infección a menudo se basa en "fuertes sospechas" y técnicas del médico tratante; estos incluyen procedimientos de PCR cuantitativa , que se emplean en laboratorios clínicos para detectar e identificar rápidamente cepas de MRSA. [67] [68]
Otra prueba de laboratorio común es una prueba rápida de aglutinación en látex que detecta la proteína PBP2a. PBP2a es una variante de la proteína fijadora de penicilina que confiere a S. aureus la capacidad de ser resistente a la oxacilina. [69]
Como todos los S. aureus (a veces también abreviado SA), el S. aureus resistente a la meticilina es una bacteria grampositiva esférica ( coco ) de aproximadamente 1 micrón de diámetro . No forma esporas y no es móvil . Se encuentra frecuentemente en racimos o cadenas similares a uvas. [70] : 390 A diferencia de S. aureus susceptible a la meticilina (MSSA), MRSA crece lentamente en una variedad de medios y se ha descubierto que existe en colonias mixtas de MSSA. El gen mecA , que confiere resistencia a varios antibióticos, siempre está presente en el MRSA y generalmente está ausente en el MSSA; sin embargo, en algunos casos, el gen mecA está presente en MSSA pero no se expresa . La prueba de reacción en cadena de la polimerasa (PCR) es el método más preciso para identificar cepas de MRSA. Se han desarrollado medios de cultivo especializados para diferenciar mejor entre MSSA y MRSA y, en algunos casos, dichos medios se pueden utilizar para identificar cepas específicas que son resistentes a diferentes antibióticos. [70] : 402
Han surgido otras cepas de S. aureus que son resistentes a la oxacilina , la clindamicina, la teicoplanina y la eritromicina . Estas cepas resistentes pueden poseer o no el gen mecA . S. aureus también ha desarrollado resistencia a la vancomicina (VRSA). Una cepa es sólo parcialmente susceptible a la vancomicina y se llama S. aureus intermedio con vancomicina (VISA). GISA, una cepa de S. aureus resistente , es un S. aureus intermedio en glicopéptido y es menos susceptible a la vancomicina y la teicoplanina. La resistencia a los antibióticos en S. aureus se puede cuantificar determinando la cantidad de antibiótico que se debe utilizar para inhibir el crecimiento. Si S. aureus se inhibe con una concentración de vancomicina menor o igual a 4 μg/ml, se dice que es susceptible. Si es necesaria una concentración superior a 32 μg/ml para inhibir el crecimiento, se dice que es resistente. [21] : 637
En entornos de atención médica, aislar a las personas con MRSA de las que no tienen la infección es un método para prevenir la transmisión. Las pruebas rápidas de cultivo y sensibilidad y las pruebas moleculares identifican a los portadores y reducen las tasas de infección. [71] Es especialmente importante realizar pruebas a los pacientes en estos entornos, ya que el 2% de las personas son portadoras de MRSA, aunque en muchos de estos casos la bacteria reside en la fosa nasal y el paciente no presentará ningún síntoma. [72]
El MRSA se puede identificar limpiando las fosas nasales y aislando las bacterias que se encuentran allí. Combinado con medidas sanitarias adicionales para quienes están en contacto con personas infectadas, se ha descubierto que el examen con hisopo de las personas ingresadas en hospitales es eficaz para minimizar la propagación de MRSA en hospitales de Estados Unidos, Dinamarca , Finlandia y Países Bajos . [73]
Los Centros para el Control y la Prevención de Enfermedades ofrecen sugerencias para prevenir la contracción y propagación de la infección por MRSA que son aplicables a quienes se encuentran en entornos comunitarios, incluidas las poblaciones encarceladas, los empleados de guarderías y los atletas. Para prevenir la propagación de MRSA, las recomendaciones son lavarse las manos minuciosa y regularmente con agua y jabón o un desinfectante a base de alcohol. Las recomendaciones adicionales son mantener las heridas limpias y cubiertas, evitar el contacto con las heridas de otras personas, evitar compartir artículos personales como navajas o toallas, ducharse después de hacer ejercicio en instalaciones deportivas y ducharse antes de usar piscinas o jacuzzis. [74]
Excluyendo las instalaciones médicas , las directrices actuales de EE. UU. no exigen que los trabajadores con infecciones por MRSA sean excluidos rutinariamente del lugar de trabajo general. [75] Los Institutos Nacionales de Salud recomiendan que aquellos con drenaje de heridas que no se pueden cubrir y contener con un vendaje limpio y seco y aquellos que no pueden mantener buenas prácticas de higiene sean reasignados, [75] y los pacientes con drenaje de heridas también deben ser colocados automáticamente en " Precaución de contacto ", independientemente de si tienen o no una infección conocida. [76] Los trabajadores con infecciones activas están excluidos de actividades en las que es probable que se produzca contacto piel a piel. [77] Para prevenir la propagación de estafilococos o MRSA en el lugar de trabajo, se alienta a los empleadores a poner a disposición instalaciones adecuadas que respalden una buena higiene. Además, la desinfección de superficies y equipos debe cumplir con los desinfectantes registrados por la Agencia de Protección Ambiental . [75] En entornos hospitalarios, el aislamiento de contacto se puede suspender después de que uno a tres cultivos resulten negativos. [78] Antes de que se libere al paciente del aislamiento, se recomienda que exista un equipo de atención al paciente exclusivo o de un solo uso para ese paciente en particular. Si esto no es posible, el equipo deberá desinfectarse adecuadamente antes de utilizarlo con otro paciente. [76]
Para prevenir la propagación de MRSA en el hogar, los departamentos de salud recomiendan lavar los materiales que han estado en contacto con personas infectadas por separado y con una solución diluida de lejía; reducir la carga bacteriana en la nariz y la piel; y limpiar y desinfectar aquellas cosas de la casa que la gente toca habitualmente, como fregaderos, bañeras, encimeras de cocina, teléfonos móviles, interruptores de luz, pomos de puertas, teléfonos, inodoros y teclados de computadora. [79]
Los glicopéptidos , las cefalosporinas y, en particular, las quinolonas se asocian con un mayor riesgo de colonización por MRSA. En las directrices actuales se recomienda reducir el uso de clases de antibióticos que promueven la colonización por MRSA, especialmente fluoroquinolonas. [12] [25]
Los modelos matemáticos describen una forma en que puede ocurrir una pérdida del control de la infección después de que las medidas de detección y aislamiento parecen ser efectivas durante años, como sucedió en el Reino Unido. En la estrategia de "buscar y destruir" que emplearon todos los hospitales del Reino Unido hasta mediados de la década de 1990, todas las personas hospitalizadas con MRSA fueron aisladas inmediatamente, y todo el personal fue examinado para detectar MRSA y se les impidió trabajar hasta que hubieran completado un ciclo de erradicación. terapia que se ha demostrado que funciona. La pérdida de control se produce porque las personas colonizadas son devueltas a la comunidad y luego readmitidas; cuando el número de personas colonizadas en la comunidad alcanza un cierto umbral, la estrategia de "buscar y destruir" se ve abrumada. [80] Uno de los pocos países que no se ha visto abrumado por MRSA es los Países Bajos: una parte importante del éxito de la estrategia holandesa puede haber sido intentar la erradicación del portador tras el alta hospitalaria. [81]
Hasta 2013, no se habían realizado ensayos clínicos aleatorios para comprender cómo tratar las heridas no quirúrgicas que habían sido colonizadas, pero no infectadas, con MRSA, [22] y no se habían realizado estudios suficientes para comprender cómo tratar las heridas quirúrgicas que habían sido colonizadas. con SARM. [1] A partir de 2013, no se sabía si las estrategias para erradicar la colonización por MRSA de personas en hogares de ancianos reducían las tasas de infección. [26]
Se debe tener cuidado al intentar drenar los forúnculos, ya que la alteración del tejido circundante puede provocar infecciones mayores, incluida la infección del torrente sanguíneo . [82] La pomada de mupirocina al 2% puede ser eficaz para reducir el tamaño de las lesiones. Se prefiere una cobertura secundaria de ropa. [79] Como se muestra en un estudio en animales con ratones diabéticos, la aplicación tópica de una mezcla de azúcar (70%) y pasta de povidona yodada al 3% es un agente eficaz para el tratamiento de las úlceras diabéticas con infección por MRSA. [83]
Mantener la limpieza necesaria puede resultar difícil para las personas si no tienen acceso a instalaciones como baños públicos con instalaciones para lavarse las manos. En el Reino Unido, el Reglamento sobre el lugar de trabajo (salud, seguridad y bienestar) de 1992 [84] exige que las empresas proporcionen retretes a sus empleados, además de instalaciones de lavado que incluyan jabón u otros medios de limpieza adecuados. En el Código de prácticas y orientación L24 aprobado en el lugar de trabajo (salud, seguridad y bienestar), disponible en Health and Safety Executive Books, se proporciona orientación sobre cuántos inodoros proporcionar y qué tipo de instalaciones de lavado se deben proporcionar junto a ellos, pero no hay obligaciones legales. existen sobre las autoridades locales en el Reino Unido para proporcionar baños públicos , y aunque en 2008, el Comité de Comunidades y Gobiernos Locales de la Cámara de los Comunes pidió a las autoridades locales el deber de desarrollar una estrategia de baños públicos, [85] esto fue rechazado por el Gobierno. . [86]
La Organización Mundial de la Salud aboga por regulaciones sobre el uso de antibióticos en la alimentación animal para prevenir la aparición de cepas de MRSA resistentes a los medicamentos. [28] MRSA está establecido en animales y aves. [19]
El tratamiento de la infección por MRSA es urgente y los retrasos pueden ser fatales. [20] : 328 La ubicación y la historia relacionada con la infección determinan el tratamiento. La vía de administración de un antibiótico varía. Los antibióticos eficaces contra MRSA se pueden administrar por vía intravenosa, oral o una combinación de ambos, y dependen de las circunstancias específicas y las características del paciente. [4] El uso de tratamiento concomitante con vancomicina u otros agentes betalactámicos puede tener un efecto sinérgico. [21] : 637
Tanto CA-MRSA como HA-MRSA son resistentes a los antibióticos betalactámicos antiestafilocócicos tradicionales , como la cefalexina . CA-MRSA tiene un mayor espectro de susceptibilidad antimicrobiana a las sulfonamidas (como cotrimoxazol ( trimetoprim/sulfametoxazol ), tetraciclinas (como doxiciclina y minociclina ) y clindamicina (para la osteomielitis ). [4] MRSA se puede erradicar con un régimen de linezolid , [87] aunque los protocolos de tratamiento varían y los niveles séricos de antibióticos varían ampliamente de persona a persona y pueden afectar los resultados [88] El tratamiento efectivo de MRSA con linezolid ha sido exitoso [87] en el 87% de las personas. en infecciones de tejidos blandos que la vancomicina [89] [1] Esto se compara con la erradicación de la infección en personas con MRSA tratadas con vancomicina. El tratamiento con vancomicina tiene éxito en aproximadamente el 49% de las personas [1] Linezolid pertenece a la clase más nueva de oxazolidinona. de antibióticos que ha demostrado ser eficaz contra CA-MRSA y HA-MRSA. La Sociedad de Enfermedades Infecciosas de América recomienda vancomicina, linezolid o clindamicina (si son susceptibles) para tratar a las personas con neumonía por MRSA. [4] La ceftarolina , una cefalosporina de quinta generación, es el primer antibiótico betalactámico aprobado en los EE. UU. para tratar las infecciones por MRSA en la piel y los tejidos blandos o la neumonía adquirida en la comunidad. [90]
La vancomicina y la teicoplanina son antibióticos glicopéptidos que se usan para tratar las infecciones por MRSA. [91] La teicoplanina es un congénere estructural de la vancomicina que tiene un espectro de actividad similar pero una vida media más larga . [92] Debido a que la absorción oral de vancomicina y teicoplanina es muy baja, estos agentes se pueden administrar por vía intravenosa para controlar las infecciones sistémicas. [93] El tratamiento de la infección por MRSA con vancomicina puede ser complicado debido a su incómoda vía de administración. Además, la eficacia de la vancomicina contra MRSA es inferior a la de los antibióticos betalactámicos antiestafilocócicos contra S. aureus sensible a meticilina (MSSA). [94] [95]
Varias cepas de MRSA recientemente descubiertas muestran resistencia a los antibióticos incluso a la vancomicina y la teicoplanina. Cepas con niveles intermedios de resistencia (4–8 μg/ml), denominadas S. aureus intermedio con glicopéptido (GISA) o S. aureus intermedio con vancomicina (VISA) , [96] [97] comenzaron a aparecer a finales de los años 1990. El primer caso identificado se produjo en Japón en 1996 y desde entonces se han encontrado cepas en hospitales de Inglaterra, Francia y Estados Unidos. La primera cepa documentada con resistencia completa (>16 μg/ml) a la vancomicina, denominada S. aureus resistente a la vancomicina (VRSA) , apareció en los Estados Unidos en 2002. [98] En 2011, se probó una variante de vancomicina que se une a la variación del lactato y también se une bien al objetivo original, restableciendo así una potente actividad antimicrobiana. [99] Linezolid , quinupristina/dalfopristina , daptomicina , ceftarolina y tigeciclina se usan para tratar infecciones más graves que no responden a glicopéptidos como la vancomicina. [100] Las pautas actuales recomiendan daptomicina para las infecciones del torrente sanguíneo y la endocarditis VISA. [4]
Las oxazolidinonas como el linezolid estuvieron disponibles en la década de 1990 y son comparables a la vancomicina en eficacia contra MRSA. La resistencia al linezolid en S. aureus se informó en 2001, [101] pero las tasas de infección se han mantenido en niveles consistentemente bajos. En el Reino Unido e Irlanda, no se encontró resistencia al linezolid en estafilococos recolectados de casos de bacteriemia entre 2001 y 2006. [102]
En los abscesos cutáneos, el tratamiento principal recomendado es la eliminación del tejido muerto, la incisión y el drenaje. Se necesita más información para determinar la eficacia de la terapia con antibióticos específicos en las infecciones del sitio quirúrgico (ISQ). [4] Ejemplos de infecciones de tejidos blandos por MRSA incluyen úlceras, impétigo , abscesos e ISQ. [89] En heridas quirúrgicas, la evidencia es débil (alto riesgo de sesgo ) de que linezolid puede ser mejor que vancomicina para erradicar las ISQ por MRSA. [1]
La colonización por MRSA también se encuentra en heridas no quirúrgicas, como heridas traumáticas, quemaduras y úlceras crónicas (es decir, úlcera diabética , úlcera por presión , úlcera por insuficiencia arterial , úlcera venosa ). No se ha encontrado evidencia concluyente sobre cuál es el mejor régimen de antibióticos para tratar la colonización por MRSA. [22]
En infecciones de la piel y sitios de infección secundaria, la mupirocina tópica se usa con éxito. Para bacteriemia y endocarditis se considera vancomicina o daptomicina. Para los niños con huesos o articulaciones infectados por MRSA, el tratamiento es individualizado y a largo plazo. Los recién nacidos pueden desarrollar pustulosis neonatal como resultado de una infección tópica con MRSA. [4] La clindamicina no está aprobada para el tratamiento de la infección por MRSA, pero todavía se usa en niños para infecciones de tejidos blandos. [4]
Se considera evaluación para el reemplazo de una prótesis valvular. Se puede administrar una terapia antibiótica adecuada durante un máximo de seis semanas. A menudo se recomienda un tratamiento con antibióticos de cuatro a seis semanas, y depende del grado de infección por MRSA. [4]
CA-MRSA en pacientes hospitalizados el tratamiento de la neumonía comienza antes de los resultados del cultivo. Una vez realizada la susceptibilidad a los antibióticos, la infección se puede tratar con vancomicina o linezolid por hasta 21 días. Si la neumonía se complica por la acumulación de pus en la cavidad pleural que rodea los pulmones, se puede realizar un drenaje junto con una terapia con antibióticos. [4] Las personas con fibrosis quística pueden desarrollar complicaciones respiratorias relacionadas con la infección por MRSA. La incidencia de MRSA en personas con fibrosis quística aumentó cinco veces entre 2000 y 2015. La mayoría de estas infecciones fueron HA-MRSA. MRSA representa el 26% de las infecciones pulmonares en personas con fibrosis quística. [103]
No hay evidencia suficiente para respaldar el uso de antibióticos tópicos o sistemáticos para la infección nasal o extranasal por MRSA. [104]
Limpiar la herida del tejido muerto y drenar los abscesos es la primera acción para tratar la infección por MRSA. La administración de antibióticos no está estandarizada y se adapta caso por caso. La terapia con antibióticos puede durar hasta 3 meses y, a veces, incluso más. [4]
La infección por MRSA puede ocurrir asociada con implantes y reemplazos de articulaciones. Las recomendaciones sobre el tratamiento se basan en el tiempo que el implante ha estado colocado. En casos de colocación reciente de un implante quirúrgico o articulación artificial, el dispositivo podrá conservarse mientras continúa la terapia con antibióticos. Si la colocación del dispositivo se produjo hace más de 3 semanas, se podrá retirar el dispositivo. La terapia con antibióticos se utiliza en cada caso, a veces a largo plazo. [4]
MRSA puede infectar el sistema nervioso central y formar absceso cerebral, empiema subdural y absceso epidural espinal. La escisión y el drenaje se pueden realizar junto con el tratamiento con antibióticos. La trombosis séptica del seno venoso cavernoso o dural a veces puede ser una complicación. [4]
El tratamiento no está estandarizado para otros casos de infección por MRSA en una amplia gama de tejidos. El tratamiento varía para las infecciones por MRSA relacionadas con: abscesos subperiósticos, neumonía necrotizante, celulitis, piomiositis, fascitis necrotizante, mediastinitis, abscesos miocárdicos, perinéfricos, hepáticos y esplénicos, tromboflebitis séptica e infecciones oculares graves, incluida la endoftalmitis. [4] Las mascotas pueden ser reservorios y transmitir MRSA a las personas. En algunos casos, la infección puede ser sintomática y la mascota puede desarrollar una infección por MRSA. Los departamentos de salud recomiendan que la mascota sea llevada al veterinario si continúan ocurriendo infecciones por MRSA en las personas que tienen contacto con la mascota. [79]
En todo el mundo, se estima que 2 mil millones de personas son portadoras de alguna forma de S. aureus ; de estos, se cree que hasta 53 millones (2,7% de los portadores) son portadores de MRSA. [105] S. aureus fue identificado como uno de los seis patógenos principales en muertes asociadas con la resistencia en 2019 y 100 000 muertes causadas por MRSA fueron atribuibles a la resistencia a los antimicrobianos. [106]
En un estudio de cohorte estadounidense de 1.300 niños sanos, el 2,4% portaba MRSA en la nariz. [107] La sepsis bacteriana ocurre en la mayoría (75%) de los casos de infección invasiva por MRSA. [4] En 2009, se estima que hubo 463.017 hospitalizaciones debido a MRSA, o una tasa de 11,74 por 1.000 hospitalizaciones. [108] Muchas de estas infecciones son menos graves, pero los Centros para el Control y la Prevención de Enfermedades (CDC) estiman que hay 80.461 infecciones invasivas por MRSA y 11.285 muertes debido a MRSA anualmente. [109] En 2003, el costo de una hospitalización debido a una infección por MRSA fue de 92.363 dólares estadounidenses; una estadía en el hospital por MSSA fue de $52,791. [89]
La infección después de la cirugía es relativamente poco común, pero ocurre hasta en un 33% en tipos específicos de cirugías. Las infecciones de los sitios quirúrgicos oscilan entre el 1% y el 33%. La sepsis por MRSA que ocurre dentro de los 30 días posteriores a una infección quirúrgica tiene una tasa de mortalidad de 15 a 38%; La sepsis por MRSA que ocurre dentro de un año tiene una tasa de mortalidad de alrededor del 55%. Puede haber una mayor mortalidad asociada con la cirugía cardíaca. Hay una tasa del 12,9% en aquellos infectados con MRSA, mientras que solo el 3% está infectado con otros organismos. Las ISQ infectadas con MRSA tuvieron estancias hospitalarias más largas que las que no lo hicieron. [1]
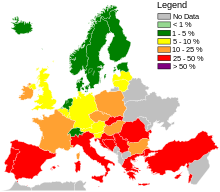
A nivel mundial, las tasas de infección por MRSA son dinámicas y varían de año en año. [110] Según el informe del Programa de Vigilancia Antimicrobiana SENTRY de 2006, la incidencia de infecciones del torrente sanguíneo por SARM fue del 35,9% en América del Norte. Las infecciones sanguíneas por MRSA en América Latina fueron del 29%. La incidencia europea fue del 22,8%. La tasa de todas las infecciones por MRSA en Europa osciló entre el 50% en Portugal y el 0,8% en Suecia. Las tasas generales de infección por MRSA variaron en América Latina: Colombia y Venezuela combinadas tuvieron el 3%, México el 50%, Chile el 38%, Brasil el 29% y Argentina el 28%. [89]
Los Centros para el Control y la Prevención de Enfermedades (CDC) estimaron que en 2002 se produjeron en Estados Unidos alrededor de 1,7 millones de infecciones nosocomiales, con 99.000 muertes asociadas. [111] La incidencia estimada es de 4,5 infecciones nosocomiales por cada 100 admisiones, con costos directos (a precios de 2004) que oscilan entre 10.500 dólares (£5.300, €8.000 a precios de 2006) por caso (para infecciones del torrente sanguíneo, del tracto urinario o respiratorias en personas inmunocompetentes). ) a 111.000 dólares (57.000 libras esterlinas, 85.000 euros) por caso para infecciones resistentes a los antibióticos en el torrente sanguíneo en personas trasplantadas. Con estas cifras, las estimaciones conservadoras de los costos directos totales de las infecciones nosocomiales superan los 17 mil millones de dólares. La reducción de este tipo de infecciones constituye un componente importante de los esfuerzos por mejorar la seguridad de la atención sanitaria. (BMJ 2007) [ cita necesaria ] MRSA solo se asoció con el 8% de las infecciones nosocomiales reportadas a la Red Nacional de Seguridad de la Atención Médica de los CDC desde enero de 2006 hasta octubre de 2007. [112]
La Oficina Nacional de Auditoría británica estimó que la incidencia de infecciones nosocomiales en Europa oscila entre el 4% y el 10% de todos los ingresos hospitalarios. A principios de 2005, varias fuentes estimaron que el número de muertes en el Reino Unido atribuidas a MRSA rondaba las 3.000 por año. [113]
En Estados Unidos, se estima que 95 millones de personas portan S. aureus en la nariz; de ellos, 2,5 millones (2,6% de los transportistas) son portadores de MRSA. [114] Una revisión de la población realizada en tres comunidades de EE. UU. mostró que la incidencia anual de CA-MRSA durante 2001-2002 fue de 18 a 25,7/100.000; la mayoría de los aislados de CA-MRSA se asociaron con infecciones clínicamente relevantes y el 23% de las personas requirieron hospitalización. [115]
En un estudio de cohorte estadounidense de 1.300 niños sanos, el 2,4% portaba MRSA en la nariz. [107] Existe la preocupación de que la presencia de MRSA en el medio ambiente pueda permitir que la resistencia se transfiera a otras bacterias a través de fagos (virus que infectan bacterias). La fuente de MRSA podría provenir de desechos hospitalarios, aguas residuales agrícolas u otras aguas residuales. [4]
En 2004, se aisló por primera vez MRSA en una granja de cerdos holandesa, lo que dio lugar a más investigaciones sobre MRSA asociado al ganado (LA-MRSA). [116] Se ha observado MRSA asociado al ganado (LA-MRSA) en Corea, Brasil, Suiza, Malasia, India, Gran Bretaña, Dinamarca y China. [19]
En 1961, los primeros aislados conocidos de MRSA se informaron en un estudio británico, y de 1961 a 1967, se produjeron brotes hospitalarios poco frecuentes en Europa occidental y Australia, [17] y luego se autorizó la meticilina en Inglaterra para tratar infecciones resistentes. Otros informes de MRSA comenzaron a describirse en la década de 1970. [1] Se documentó resistencia a otros antibióticos en algunas cepas de S. aureus . En 1996 se informó en Japón de resistencia a la vancomicina. [21] : 637 En muchos países, se informó que los brotes de infección por MRSA se transmitían entre hospitales. [70] : 402 La tasa había aumentado al 22% en 1995, y en 1997 el nivel de infecciones hospitalarias por S. aureus atribuibles a MRSA había alcanzado el 50%.
El primer informe de MRSA asociado a la comunidad (CA-MRSA) se produjo en 1981, y en 1982, se produjo un gran brote de CA-MRSA entre usuarios de drogas intravenosas en Detroit, Michigan. [17] Se informaron brotes adicionales de CA-MRSA durante las décadas de 1980 y 1990, incluidos brotes entre poblaciones aborígenes australianas que nunca habían estado expuestas a hospitales. A mediados de la década de 1990, se hicieron informes dispersos sobre brotes de CA-MRSA entre niños estadounidenses. Mientras que las tasas de HA-MRSA se estabilizaron entre 1998 y 2008, las tasas de CA-MRSA continuaron aumentando. Un informe publicado por el Hospital Infantil de la Universidad de Chicago que compara dos períodos (1993–1995 y 1995–1997) encontró un aumento de 25 veces en la tasa de hospitalizaciones por MRSA entre niños en los Estados Unidos. [117] En 1999, la Universidad de Chicago informó las primeras muertes por MRSA invasivo entre niños por lo demás sanos en los Estados Unidos. [17] En 2004, se describió el genoma de varias cepas de MRSA. [118]
Podría decirse que el aumento de la mortalidad observado entre las personas infectadas por MRSA puede ser el resultado del aumento de la morbilidad subyacente de estas personas. Sin embargo, varios estudios, incluido uno de Blot y colegas, que se han ajustado según la enfermedad subyacente, todavía encontraron que la bacteriemia por MRSA tiene una mortalidad atribuible más alta que la bacteriemia por S. aureus susceptible a la meticilina (MSSA). [119]
Un estudio poblacional sobre la incidencia de infecciones por MRSA en San Francisco durante 2004-05 demostró que casi uno de cada 300 residentes tuvo dicha infección en el transcurso de un año y que más del 85% de estas infecciones ocurrieron fuera del entorno de atención médica. . [120] Un estudio de 2004 demostró que las personas en los Estados Unidos con infección por S. aureus tuvieron, en promedio, tres veces más duración de la estancia hospitalaria (14,3 frente a 4,5 días), e incurrieron en tres veces el costo total ($48,824 frente a $14,141). , y experimentaron cinco veces más riesgo de muerte hospitalaria (11,2% frente a 2,3%) que las personas sin esta infección. [121] En un metanálisis de 31 estudios, Cosgrove et al. , [122] concluyeron que la bacteriemia por SAMR se asocia con una mayor mortalidad en comparación con la bacteriemia por SAMS (odds ratio = 1,93; IC del 95 % = 1,93 ± 0,39 ). [123] Además, Wyllie et al. informan una tasa de mortalidad del 34 % en 30 días entre las personas infectadas con MRSA, una tasa similar a la tasa de mortalidad del 27 % observada entre las personas infectadas con MSSA. [124]
En Estados Unidos, los CDC publicaron directrices el 19 de octubre de 2006, citando la necesidad de realizar investigaciones adicionales, pero se negaron a recomendar dicha detección. [125] Según los CDC, las estimaciones más recientes de la incidencia de infecciones asociadas a la atención médica atribuibles a MRSA en los Estados Unidos indican una disminución en dichas tasas de infección. La incidencia de infecciones del torrente sanguíneo asociadas a vías centrales de MRSA, según lo informado por cientos de unidades de cuidados intensivos, disminuyó entre un 50% y un 70% entre 2001 y 2007. [126] Un sistema separado que rastrea todas las infecciones del torrente sanguíneo por MRSA hospitalarias encontró una disminución general del 34% entre 2005 y 2008. [126] En 2010, la vancomicina fue el fármaco de elección. [4]
En toda Europa, basándose principalmente en datos de 2013, siete países (Islandia, Noruega, Suecia, Países Bajos, Dinamarca, Finlandia y Estonia, de menor a mayor) tenían niveles bajos de infecciones por MRSA adquiridas en hospitales en comparación con los demás [127 ] : 92–93 y entre los países con niveles más altos, sólo se habían logrado mejoras significativas en Bulgaria, Polonia y las Islas Británicas. [127] : 40
Se descubrió que una receta de ungüento para los ojos de hace 1.000 años encontrada en el libro medieval Bald's Leech de la Biblioteca Británica , uno de los primeros libros de texto médicos conocidos, tiene actividad contra MRSA in vitro y en heridas de la piel en ratones. [128] [129] [130]
El MRSA suele ser un tema mediático, especialmente si personalidades conocidas han anunciado que tienen o han tenido la infección. [131] [132] [133] Regularmente aparecen noticias sobre brotes de infección en periódicos y programas de noticias de televisión. Un informe sobre infecciones de la piel y tejidos blandos en la cárcel del condado de Cook en Chicago en 2004-05 demostró que MRSA era la causa más común de estas infecciones entre los encarcelados allí. [134] Las demandas presentadas contra aquellos acusados de infectar a otros con MRSA también son historias populares en los medios. [135] [136]
MRSA es el tema de programas de radio, [137] programas de televisión, [138] [139] [140] libros, [141] y películas. [142]
Se han investigado varios extractos químicos antibacterianos de varias especies del árbol del liquidámbar (género Liquidambar ) por su actividad para inhibir el MRSA. En concreto, estos son: ácido cinámico , cinamato de cinamilo, cinamato de etilo , cinamato de bencilo , estireno , vainillina , alcohol cinamilo , alcohol 2-fenilpropílico y cinamato de 3-fenilpropilo. [143]
Se está desarrollando la administración de antibióticos inhalados junto con la administración sistemática para tratar MRSA. Esto puede mejorar los resultados de las personas con fibrosis quística y otras infecciones respiratorias. [103] La terapia con fagos se ha utilizado durante años en MRSA en los países orientales y se están realizando estudios en los países occidentales. [144] [145] Se están estudiando terapias dirigidas al huésped , incluidos inhibidores de la quinasa del huésped, así como péptidos antimicrobianos, como tratamiento complementario o alternativo para el SARM. [146] [147] [148]
Una revisión sistemática Cochrane de 2015 tuvo como objetivo evaluar la efectividad del uso de guantes, batas y máscaras para ayudar a detener la propagación de MRSA en los hospitales; sin embargo, no se identificaron estudios elegibles para su inclusión. Los autores de la revisión concluyeron que es necesario realizar ensayos controlados aleatorios para ayudar a determinar si el uso de guantes, batas y mascarillas reduce la transmisión de MRSA en los hospitales. [149]
{{cite journal}}: Mantenimiento CS1: DOI inactivo a partir de enero de 2024 ( enlace ){{cite web}}: Mantenimiento CS1: bot: estado de la URL original desconocido ( enlace )