_(6982162417).jpg/440px-Inspecting_a_Drug_Manufacturer_(FDA034)_(6982162417).jpg)
La industria farmacéutica es una industria de la medicina que descubre, desarrolla, produce y comercializa fármacos para su uso como medicamentos para ser administrados a los pacientes (o autoadministrados), con el objetivo de curar y prevenir enfermedades, o aliviar los síntomas . [1] [2] Las empresas farmacéuticas pueden comercializar medicamentos y dispositivos médicos genéricos o de marca . Están sujetos a una variedad de leyes y regulaciones que rigen las patentes , las pruebas, la seguridad, la eficacia mediante pruebas de drogas y la comercialización de medicamentos . El mercado farmacéutico mundial produjo tratamientos por valor de 1.228,45 mil millones de dólares en 2020 y mostró una tasa de crecimiento anual compuesta (CAGR) del 1,8%. [3]
La era moderna de la industria farmacéutica comenzó con los boticarios locales que ampliaron su función tradicional de distribuir medicamentos botánicos como la morfina y la quinina a la fabricación al por mayor a mediados del siglo XIX, y a partir de descubrimientos resultantes de la investigación aplicada. El descubrimiento intencional de fármacos a partir de plantas comenzó con el aislamiento entre 1803 y 1805 de la morfina (un agente analgésico e inductor del sueño) del opio por parte del asistente del boticario alemán Friedrich Sertürner , quien nombró a este compuesto en honor al dios griego de los sueños, Morfeo . [4] A finales de la década de 1880, los fabricantes de tintes alemanes habían perfeccionado la purificación de compuestos orgánicos individuales a partir de alquitrán y otras fuentes minerales y también habían establecido métodos rudimentarios en la síntesis química orgánica . [5] El desarrollo de métodos químicos sintéticos permitió a los científicos variar sistemáticamente la estructura de las sustancias químicas, y el crecimiento de la ciencia emergente de la farmacología amplió su capacidad para evaluar los efectos biológicos de estos cambios estructurales.
En la década de 1890, se descubrió el profundo efecto de los extractos suprarrenales en muchos tipos diferentes de tejidos, lo que desencadenó una búsqueda tanto del mecanismo de señalización química como de esfuerzos por explotar estas observaciones para el desarrollo de nuevos fármacos. Los efectos vasoconstrictores y de aumento de la presión arterial de los extractos suprarrenales eran de particular interés para los cirujanos como agentes hemostáticos y como tratamiento para el shock, y varias empresas desarrollaron productos basados en extractos suprarrenales que contenían purezas variables del principio activo. En 1897, John Abel, de la Universidad Johns Hopkins , identificó el principio activo como epinefrina , que aisló en estado impuro como sal sulfato. El químico industrial Jōkichi Takamine desarrolló más tarde un método para obtener epinefrina en estado puro y otorgó la licencia de la tecnología a Parke-Davis . Parke-Davis comercializó epinefrina bajo el nombre comercial Adrenalin . La epinefrina inyectada demostró ser especialmente eficaz para el tratamiento agudo de los ataques de asma , y hasta 2011 se vendió en Estados Unidos una versión inhalada ( Primatene Mist ). [6] [7] En 1929, la epinefrina se había formulado en un inhalador para su uso en el tratamiento de la congestión nasal.
Si bien era muy eficaz, la necesidad de inyección limitó el uso de epinefrina [ se necesita aclaración ] y se buscaron derivados activos por vía oral. Un compuesto estructuralmente similar, la efedrina , fue identificado por químicos japoneses en la planta de Ma Huang y comercializado por Eli Lilly como tratamiento oral para el asma. Siguiendo el trabajo de Henry Dale y George Barger en Burroughs-Wellcome , el químico académico Gordon Alles sintetizó anfetamina y la probó en pacientes con asma en 1929. La droga demostró tener sólo efectos modestos contra el asma, pero produjo sensaciones de euforia y palpitaciones. La anfetamina fue desarrollada por Smith, Kline y French como descongestionante nasal bajo el nombre comercial Benzedrine Inhaler. La anfetamina finalmente se desarrolló para el tratamiento de la narcolepsia , el parkinsonismo postencefalítico y la elevación del estado de ánimo en la depresión y otras indicaciones psiquiátricas. Recibió la aprobación como remedio nuevo y no oficial de la Asociación Médica Estadounidense para estos usos en 1937, [8] y siguió siendo de uso común para la depresión hasta el desarrollo de los antidepresivos tricíclicos en la década de 1960. [7]

En 1903, Hermann Emil Fischer y Joseph von Mering descubrieron que el ácido dietilbarbitúrico, formado a partir de la reacción del ácido dietilmalónico, el oxicloruro de fósforo y la urea, induce el sueño en los perros. El descubrimiento fue patentado y autorizado por Bayer Pharmaceuticals , que comercializó el compuesto con el nombre comercial Veronal como ayuda para dormir a partir de 1904. Las investigaciones sistemáticas del efecto de los cambios estructurales sobre la potencia y la duración de la acción llevaron al descubrimiento del fenobarbital en Bayer en 1911 y el descubrimiento de su potente actividad antiepiléptica en 1912. El fenobarbital estuvo entre los medicamentos más utilizados para el tratamiento de la epilepsia durante la década de 1970 y, a partir de 2014, permanece en la lista de medicamentos esenciales de la Organización Mundial de la Salud. [9] [10] Las décadas de 1950 y 1960 vieron una mayor conciencia de las propiedades adictivas y el potencial de abuso de los barbitúricos y las anfetaminas y llevaron a restricciones cada vez mayores sobre su uso y a una creciente supervisión gubernamental de los prescriptores. Hoy en día, el uso de anfetamina está restringido en gran medida al tratamiento del trastorno por déficit de atención y el fenobarbital en el tratamiento de la epilepsia . [11] [12]
En 1958, Leo Sternbach descubrió la primera benzodiazepina , el clordiazepóxido (Librium). Se han desarrollado y se utilizan docenas de otras benzodiazepinas, siendo algunos de los fármacos más populares el diazepam (Valium), el alprazolam (Xanax), el clonazepam (Klonopin) y el lorazepam (Ativan). Debido a su seguridad y propiedades terapéuticas muy superiores, las benzodiacepinas han reemplazado en gran medida el uso de barbitúricos en medicina, excepto en ciertos casos especiales. Cuando más tarde se descubrió que las benzodiazepinas, al igual que los barbitúricos, pierden significativamente su eficacia y pueden tener efectos secundarios graves cuando se toman a largo plazo, Heather Ashton investigó la dependencia de las benzodiazepinas y desarrolló un protocolo para suspender su uso.
Una serie de experimentos realizados desde finales del siglo XIX hasta principios del XX revelaron que la diabetes es causada por la ausencia de una sustancia normalmente producida por el páncreas. En 1869, Oskar Minkowski y Joseph von Mering descubrieron que se podía inducir diabetes en perros mediante la extirpación quirúrgica del páncreas. En 1921, el profesor canadiense Frederick Banting y su alumno Charles Best repitieron este estudio y descubrieron que las inyecciones de extracto pancreático revertían los síntomas producidos por la extirpación del páncreas. Pronto se demostró que el extracto funciona en humanos, pero el desarrollo de la terapia con insulina como procedimiento médico de rutina se retrasó por las dificultades para producir el material en cantidad suficiente y con una pureza reproducible. Los investigadores buscaron ayuda de colaboradores industriales de Eli Lilly and Co. basándose en la experiencia de la empresa en la purificación a gran escala de materiales biológicos. El químico George B. Walden de Eli Lilly and Company descubrió que un ajuste cuidadoso del pH del extracto permitía producir un grado relativamente puro de insulina. Bajo la presión de la Universidad de Toronto y una posible impugnación de patente por parte de científicos académicos que habían desarrollado de forma independiente un método de purificación similar, se llegó a un acuerdo para la producción no exclusiva de insulina por parte de varias empresas. Antes del descubrimiento y la disponibilidad generalizada de la terapia con insulina, la esperanza de vida de los diabéticos era sólo de unos pocos meses. [13]
El desarrollo de medicamentos para el tratamiento de enfermedades infecciosas fue un foco importante de los primeros esfuerzos de investigación y desarrollo; En 1900, la neumonía, la tuberculosis y la diarrea eran las tres principales causas de muerte en Estados Unidos y la mortalidad en el primer año de vida superaba el 10%. [14] [15] [ verificación fallida ]
En 1911 , Paul Ehrlich y el químico Alfred Bertheim del Instituto de Terapia Experimental de Berlín desarrollaron la arsfenamina , el primer fármaco antiinfeccioso sintético . El medicamento recibió el nombre comercial de Salvarsan. [16] Ehrlich, al observar tanto la toxicidad general del arsénico como la absorción selectiva de ciertos tintes por parte de las bacterias, planteó la hipótesis de que un tinte que contenga arsénico con propiedades de absorción selectiva similares podría usarse para tratar infecciones bacterianas. La arsfenamina se preparó como parte de una campaña para sintetizar una serie de dichos compuestos y se descubrió que exhibía una toxicidad parcialmente selectiva. La arsfenamina demostró ser el primer tratamiento eficaz contra la sífilis , una enfermedad hasta entonces incurable y que conducía inexorablemente a graves ulceraciones cutáneas, daños neurológicos y la muerte. [17]
El enfoque de Ehrlich de variar sistemáticamente la estructura química de los compuestos sintéticos y medir los efectos de estos cambios en la actividad biológica fue ampliamente seguido por científicos industriales, incluidos los científicos de Bayer Josef Klarer, Fritz Mietzsch y Gerhard Domagk . Este trabajo, basado también en las pruebas de compuestos disponibles en la industria de tintes alemana, condujo al desarrollo de Prontosil , el primer representante de la clase de antibióticos de las sulfonamidas . En comparación con la arsfenamina, las sulfonamidas tenían un espectro de actividad más amplio y eran mucho menos tóxicas, lo que las hacía útiles para infecciones causadas por patógenos como los estreptococos . [18] En 1939, Domagk recibió el Premio Nobel de Medicina por este descubrimiento. [19] [20] No obstante, la espectacular disminución de las muertes por enfermedades infecciosas que se produjo antes de la Segunda Guerra Mundial fue principalmente el resultado de mejores medidas de salud pública, como agua potable y viviendas menos hacinadas, y el impacto de los medicamentos antiinfecciosos y vacunas fue significativo principalmente después de la Segunda Guerra Mundial. [21] [22]
En 1928, Alexander Fleming descubrió los efectos antibacterianos de la penicilina , pero su explotación para el tratamiento de enfermedades humanas esperaba el desarrollo de métodos para su producción y purificación a gran escala. Estos fueron desarrollados por un consorcio de compañías farmacéuticas liderado por los gobiernos de Estados Unidos y Gran Bretaña durante la guerra mundial. [23]
A lo largo de este período hubo avances tempranos hacia el desarrollo de vacunas, principalmente en forma de investigación básica académica y financiada por el gobierno dirigida a la identificación de los patógenos responsables de enfermedades transmisibles comunes. En 1885, Louis Pasteur y Pierre Paul Émile Roux crearon la primera vacuna contra la rabia . Las primeras vacunas contra la difteria se produjeron en 1914 a partir de una mezcla de toxina y antitoxina diftérica (producida a partir del suero de un animal inoculado), pero la seguridad de la inoculación era marginal y no se utilizó ampliamente. Estados Unidos registró 206.000 casos de difteria en 1921, lo que provocó 15.520 muertes. En 1923, los esfuerzos paralelos de Gaston Ramon en el Instituto Pasteur y Alexander Glenny en los Laboratorios de Investigación Wellcome (posteriormente parte de GlaxoSmithKline ) llevaron al descubrimiento de que se podía producir una vacuna más segura tratando la toxina diftérica con formaldehído . [24] En 1944, Maurice Hilleman de Squibb Pharmaceuticals desarrolló la primera vacuna contra la encefalitis japonesa . [25] Hilleman se trasladó más tarde a Merck , donde desempeñó un papel clave en el desarrollo de vacunas contra el sarampión , las paperas , la varicela , la rubéola , la hepatitis A , la hepatitis B y la meningitis .

Antes del siglo XX, los medicamentos eran generalmente producidos por fabricantes de pequeña escala con poco control regulatorio sobre la fabricación o afirmaciones de seguridad y eficacia. En la medida en que tales leyes existieron, su aplicación fue laxa. En Estados Unidos, la mayor regulación de las vacunas y otros medicamentos biológicos fue impulsada por brotes de tétanos y muertes causadas por la distribución de vacuna contra la viruela y antitoxina diftérica contaminadas. [26] La Ley de Control de Productos Biológicos de 1902 exigía que el gobierno federal otorgara aprobación previa a la comercialización de cada medicamento biológico y del proceso y las instalaciones que producían dichos medicamentos. A esto le siguió en 1906 la Ley de Alimentos y Medicamentos Puros , que prohibía la distribución interestatal de alimentos y medicamentos adulterados o mal etiquetados. Se consideraba que una droga estaba mal etiquetada si contenía alcohol, morfina, opio, cocaína o cualquiera de otras drogas potencialmente peligrosas o adictivas, y si su etiqueta no indicaba la cantidad o proporción de dichas drogas. Los intentos del gobierno de utilizar la ley para procesar a los fabricantes por hacer afirmaciones de eficacia sin fundamento se vieron socavados por un fallo de la Corte Suprema que restringió los poderes de aplicación del gobierno federal a casos de especificación incorrecta de los ingredientes del medicamento. [27]
En 1937, más de 100 personas murieron después de ingerir el " Elixir Sulfanilamida " fabricado por SE Massengill Company de Tennessee. El producto fue formulado en dietilenglicol , un solvente altamente tóxico que ahora se usa ampliamente como anticongelante. [28] Según las leyes vigentes en ese momento, el procesamiento del fabricante sólo era posible bajo el tecnicismo de que el producto había sido llamado "elixir", lo que literalmente implicaba una solución en etanol. En respuesta a este episodio, el Congreso de los Estados Unidos aprobó la Ley Federal de Alimentos, Medicamentos y Cosméticos de 1938 , que por primera vez exigía una demostración de seguridad previa a la comercialización antes de que un medicamento pudiera venderse, y prohibía explícitamente las afirmaciones terapéuticas falsas. [29]
Las secuelas de la Segunda Guerra Mundial vieron una explosión en el descubrimiento de nuevas clases de fármacos antibacterianos [30] , incluidas las cefalosporinas (desarrolladas por Eli Lilly basándose en el trabajo fundamental de Giuseppe Brotzu y Edward Abraham ), [31] [32] estreptomicina ( descubiertas durante un programa de investigación financiado por Merck en el laboratorio de Selman Waksman [33] ), las tetraciclinas [34] (descubiertas en los Laboratorios Lederle, ahora parte de Pfizer ), la eritromicina (descubierta en Eli Lilly and Co.) [35] y sus extensión a una gama cada vez más amplia de patógenos bacterianos. La estreptomicina, descubierta durante un programa de investigación financiado por Merck en el laboratorio de Selman Waksman en Rutgers en 1943, se convirtió en el primer tratamiento eficaz para la tuberculosis. En el momento de su descubrimiento, los sanatorios para el aislamiento de personas infectadas por tuberculosis eran una característica omnipresente en las ciudades de los países desarrollados, y el 50% moría dentro de los cinco años posteriores a la admisión. [33] [36]
Un informe de la Comisión Federal de Comercio publicado en 1958 intentó cuantificar el efecto del desarrollo de antibióticos en la salud pública estadounidense. El informe encontró que durante el período 1946-1955, hubo una caída del 42% en la incidencia de enfermedades para las cuales los antibióticos eran efectivos y sólo una caída del 20% en aquellas para las cuales los antibióticos no eran efectivos. El informe concluye que "parece que el uso de antibióticos, el diagnóstico precoz y otros factores han limitado la propagación de la epidemia y, por tanto, el número de estas enfermedades que se han producido". El estudio examinó además las tasas de mortalidad de ocho enfermedades comunes para las cuales los antibióticos ofrecían una terapia eficaz (sífilis, tuberculosis, disentería, escarlatina, tos ferina, infecciones meningocócicas y neumonía) y encontró una disminución del 56% durante el mismo período. [37] Entre ellos destaca una disminución del 75% en las muertes por tuberculosis. [38]
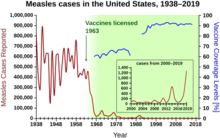

Durante los años 1940-1955, la tasa de disminución de la tasa de mortalidad en Estados Unidos se aceleró del 2% anual al 8% anual, y luego volvió a la tasa histórica del 2% anual. La dramática disminución en los años inmediatos a la posguerra se ha atribuido al rápido desarrollo de nuevos tratamientos y vacunas para enfermedades infecciosas que se produjo durante esos años. [40] [22] El desarrollo de vacunas continuó acelerándose, siendo el logro más notable del período el desarrollo de la vacuna contra la polio por parte de Jonas Salk en 1954 con la financiación de la Fundación Nacional para la Parálisis Infantil, una organización sin fines de lucro . El proceso de la vacuna nunca fue patentado, sino que se entregó a compañías farmacéuticas para que lo fabricaran como un genérico de bajo costo . En 1960, Maurice Hilleman de Merck Sharp & Dohme identificó el virus SV40 , que más tarde se demostró que causa tumores en muchas especies de mamíferos. Más tarde se determinó que SV40 estaba presente como contaminante en lotes de vacunas contra la polio que se habían administrado al 90% de los niños en los Estados Unidos. [41] [42] La contaminación parece haberse originado tanto en el stock celular original como en el tejido de mono utilizado para la producción. En 2004, el Instituto Nacional del Cáncer anunció que había llegado a la conclusión de que el SV40 no está asociado con el cáncer en las personas. [43]
Otras vacunas nuevas notables de la época incluyen las del sarampión (1962, John Franklin Enders del Children's Medical Center Boston, posteriormente refinada por Maurice Hilleman en Merck), la rubéola (1969, Hilleman, Merck) y las paperas (1967, Hilleman, Merck) [ 44] Las incidencias de rubéola, síndrome de rubéola congénita, sarampión y paperas en Estados Unidos disminuyeron >95% inmediatamente después de la vacunación generalizada. [45] Los primeros 20 años de vacunación autorizada contra el sarampión en los EE. UU. evitaron aproximadamente 52 millones de casos de la enfermedad, 17.400 casos de retraso mental y 5.200 muertes. [46]
La hipertensión es un factor de riesgo de aterosclerosis, [47] insuficiencia cardíaca , [48] enfermedad de las arterias coronarias , [49] [50] accidente cerebrovascular , [51] enfermedad renal , [52] [53] y enfermedad arterial periférica , [54] [ 55] y es el factor de riesgo más importante de morbilidad y mortalidad cardiovascular en los países industrializados . [56] Antes de 1940, aproximadamente el 23% de todas las muertes entre personas mayores de 50 años se atribuían a la hipertensión. Los casos graves de hipertensión se trataban mediante cirugía. [57]
Los primeros avances en el campo del tratamiento de la hipertensión incluyeron agentes bloqueantes del sistema nervioso simpático de iones de amonio cuaternario, pero estos compuestos nunca se utilizaron ampliamente debido a sus graves efectos secundarios, porque aún no se habían establecido las consecuencias a largo plazo de la presión arterial para la salud, y porque debían administrarse mediante inyección.
En 1952, investigadores de Ciba descubrieron el primer vasodilatador disponible por vía oral, la hidralazina . [58] Una deficiencia importante de la monoterapia con hidralazina fue que perdió su eficacia con el tiempo ( taquifilaxia ). A mediados de la década de 1950, Karl H. Beyer, James M. Sprague, John E. Baer y Frederick C. Novello de Merck and Co. descubrieron y desarrollaron la clorotiazida , que sigue siendo el fármaco antihipertensivo más utilizado en la actualidad. [59] Este desarrollo se asoció con una disminución sustancial en la tasa de mortalidad entre las personas con hipertensión. [60] Los inventores fueron reconocidos con el Premio Lasker de Salud Pública en 1975 por "salvar incontables miles de vidas y aliviar el sufrimiento de millones de víctimas de hipertensión". [61]
Una revisión Cochrane de 2009 concluyó que los fármacos antihipertensivos tiazídicos reducen el riesgo de muerte ( RR 0,89), accidente cerebrovascular (RR 0,63), enfermedad coronaria (RR 0,84) y eventos cardiovasculares (RR 0,70) en personas con presión arterial alta. [62] En los años siguientes se desarrollaron otras clases de fármacos antihipertensivos que encontraron amplia aceptación en la terapia combinada, incluidos los diuréticos de asa (Lasix/ furosemida , Hoechst Pharmaceuticals , 1963), [63] los betabloqueantes ( ICI Pharmaceuticals , 1964) [64] Inhibidores de la ECA y bloqueadores de los receptores de angiotensina . Los inhibidores de la ECA reducen el riesgo de nueva aparición de enfermedad renal [RR 0,71] y de muerte [RR 0,84] en pacientes diabéticos, independientemente de si tienen hipertensión. [sesenta y cinco]
Antes de la Segunda Guerra Mundial, el control de la natalidad estaba prohibido en muchos países, y en los Estados Unidos incluso la discusión sobre métodos anticonceptivos a veces llevaba a un proceso judicial bajo las leyes de Comstock . Por lo tanto, la historia del desarrollo de los anticonceptivos orales está estrechamente ligada al movimiento de control de la natalidad y a los esfuerzos de las activistas Margaret Sanger , Mary Dennett y Emma Goldman . Basado en investigaciones fundamentales realizadas por Gregory Pincus y métodos sintéticos para la progesterona desarrollados por Carl Djerassi en Syntex y Frank Colton en GD Searle & Co. , el primer anticonceptivo oral, Enovid , fue desarrollado por GD Searle & Co. y aprobado por la FDA. en 1960. La formulación original incorporaba dosis muy excesivas de hormonas y provocaba graves efectos secundarios. No obstante, en 1962, 1,2 millones de mujeres estadounidenses tomaban la píldora y en 1965 el número había aumentado a 6,5 millones. [66] [67] [68] [69] La disponibilidad de una forma conveniente de anticonceptivo temporal condujo a cambios dramáticos en las costumbres sociales, incluida la ampliación de la gama de opciones de estilo de vida disponibles para las mujeres, la reducción de la dependencia de las mujeres de los hombres para la práctica anticonceptiva, fomentar el retraso del matrimonio y aumentar la convivencia prematrimonial. [70]

En Estados Unidos, de las audiencias en el Congreso dirigidas por el senador Estes Kefauver de Tennessee en 1959 surgió una presión para que se revisara la Ley FD&C. Las audiencias cubrieron una amplia gama de cuestiones políticas, incluidos los abusos publicitarios, la eficacia cuestionable de las drogas y la necesidad de una mayor regulación de la industria. Si bien el impulso para una nueva legislación decayó temporalmente tras un prolongado debate, surgió una nueva tragedia que subrayó la necesidad de una regulación más integral y proporcionó la fuerza impulsora para la aprobación de nuevas leyes.
El 12 de septiembre de 1960, un licenciatario estadounidense, la William S. Merrell Company de Cincinnati, presentó una nueva solicitud de fármaco para Kevadon ( talidomida ), un sedante que se comercializaba en Europa desde 1956. El médico de la FDA encargado de revisar el compuesto Frances Kelsey creía que los datos que respaldaban la seguridad de la talidomida estaban incompletos. La firma continuó presionando a Kelsey y a la FDA para que aprobaran la solicitud hasta noviembre de 1961, cuando el medicamento fue retirado del mercado alemán debido a su asociación con graves anomalías congénitas. Varios miles de recién nacidos en Europa y otros lugares sufrieron los efectos teratogénicos de la talidomida. Sin la aprobación de la FDA, la empresa distribuyó Kevadon a más de 1.000 médicos bajo el pretexto de un uso en investigación. Más de 20.000 estadounidenses recibieron talidomida en este "estudio", incluidas 624 pacientes embarazadas, y alrededor de 17 recién nacidos conocidos sufrieron los efectos de la droga. [ cita necesaria ]
La tragedia de la talidomida resucitó el proyecto de ley de Kefauver para mejorar la regulación de los medicamentos que se había estancado en el Congreso, y la Enmienda Kefauver-Harris se convirtió en ley el 10 de octubre de 1962. A partir de entonces, los fabricantes tuvieron que demostrar a la FDA que sus medicamentos eran eficaces y seguros antes de poder seguir adelante. el mercado estadounidense. La FDA recibió autoridad para regular la publicidad de medicamentos recetados y establecer buenas prácticas de fabricación . La ley exigía que todos los medicamentos introducidos entre 1938 y 1962 fueran eficaces. Un estudio colaborativo de la FDA y la Academia Nacional de Ciencias mostró que casi el 40 por ciento de estos productos no eran efectivos. Diez años después se inició un estudio igualmente exhaustivo sobre productos de venta libre. [71]
En 1971, Akira Endo , un bioquímico japonés que trabajaba para la compañía farmacéutica Sankyo, identificó la mevastatina (ML-236B), una molécula producida por el hongo Penicillium citrinum , como un inhibidor de la HMG-CoA reductasa, una enzima crítica utilizada por el cuerpo para producir colesterol. Los ensayos en animales mostraron un efecto inhibidor muy bueno al igual que en los ensayos clínicos , sin embargo, un estudio a largo plazo en perros encontró efectos tóxicos en dosis más altas y, como resultado, se creyó que la mevastatina era demasiado tóxica para el uso humano. La mevastatina nunca se comercializó debido a sus efectos adversos de tumores, deterioro muscular y, a veces, muerte en perros de laboratorio.
P. Roy Vagelos , científico jefe y más tarde director general de Merck & Co , se interesó y realizó varios viajes a Japón a partir de 1975. En 1978, Merck había aislado la lovastatina (mevinolina, MK803) del hongo Aspergillus terreus , comercializado por primera vez en 1987. como Mevacor. [72] [73] [74]
En abril de 1994, se anunciaron los resultados de un estudio patrocinado por Merck, el Scandinavian Simvastatin Survival Study . Los investigadores probaron la simvastatina , posteriormente vendida por Merck como Zocor, en 4.444 pacientes con colesterol alto y enfermedades cardíacas. Después de cinco años, el estudio concluyó que los pacientes vieron una reducción del 35% en su colesterol y sus posibilidades de morir de un ataque cardíaco se redujeron en un 42%. [75] En 1995, Zocor y Mevacor ganaron a Merck más de mil millones de dólares. Endo recibió el Premio Japón 2006 y el Premio de Investigación Médica Clínica Lasker-DeBakey en 2008. Por su "investigación pionera en una nueva clase de moléculas" para "reducir el colesterol", [ fragmento de oración ] [76] [77]
Desde hace varias décadas, los productos biológicos han ido ganando importancia en comparación con los tratamientos con moléculas pequeñas. El subsector biotecnológico , la salud animal y el sector farmacéutico chino también han crecido sustancialmente. En el aspecto organizativo, las grandes corporaciones farmacéuticas internacionales han experimentado una disminución sustancial de su participación en el valor. Además, el sector genérico básico (sustituciones de marcas sin patente) se ha devaluado debido a la competencia. [78]
Torreya estimó que la industria farmacéutica tendrá una valoración de mercado de 7,03 billones de dólares en febrero de 2021, de los cuales 6,1 billones de dólares son el valor de las empresas que cotizan en bolsa. La modalidad de Moléculas Pequeñas tuvo un 58,2% de la cuota de valoración, frente al 84,6% en 2003. Los productos biológicos subieron al 30,5% desde el 14,5%. La cuota de valoración de Chinese Pharma creció de 2003 a 2021 del 1% al 12%, superando a Suiza, que ahora ocupa el puesto número 3 con un 7,7%. Estados Unidos seguía siendo, con diferencia, la industria farmacéutica más valorada, con el 40% de la valoración mundial. [79] 2023 fue un año de despidos para al menos 10.000 personas en 129 empresas públicas de biotecnología en todo el mundo, aunque la mayoría eran empresas pequeñas; Este fue un aumento significativo de las reducciones en comparación con 2022 y se debió en parte al empeoramiento de las condiciones financieras globales y a una reducción de la inversión por parte de "inversores generalistas". [80] Las empresas privadas también experimentaron una reducción significativa en la inversión de capital de riesgo en 2023, continuando una tendencia a la baja iniciada en 2021, que también condujo a una reducción en las ofertas públicas iniciales . [80]
Un artículo de 2022 articuló esta noción de manera sucinta al decir: "En el negocio del desarrollo de medicamentos, los acuerdos pueden ser tan importantes como los avances científicos", lo que generalmente se conoce como fusiones y adquisiciones farmacéuticas (para fusiones y adquisiciones). [81] Destacó que algunas de las soluciones más impactantes de principios del siglo XXI solo fueron posibles gracias a actividades de fusiones y adquisiciones, destacando específicamente a Keytruda y Humira . [81]
El descubrimiento de fármacos es el proceso mediante el cual se descubren o diseñan fármacos potenciales . En el pasado, la mayoría de los medicamentos se descubrieron aislando el ingrediente activo de remedios tradicionales o mediante un descubrimiento fortuito . La biotecnología moderna a menudo se centra en comprender las vías metabólicas relacionadas con una enfermedad o patógeno , y en manipular estas vías mediante la biología molecular o la bioquímica . Tradicionalmente, gran parte del descubrimiento de fármacos en sus primeras etapas ha sido realizado por universidades e instituciones de investigación.
El desarrollo de fármacos se refiere a las actividades realizadas después de que un compuesto se identifica como fármaco potencial para establecer su idoneidad como medicamento. Los objetivos del desarrollo de fármacos son determinar la formulación y dosificación apropiadas , así como establecer la seguridad . La investigación en estas áreas generalmente incluye una combinación de estudios in vitro , estudios in vivo y ensayos clínicos . El costo del desarrollo en la última etapa ha significado que generalmente lo realicen las compañías farmacéuticas más grandes. [82] La industria farmacéutica y biotecnológica destina más del 15 por ciento de sus ventas netas a investigación y desarrollo, lo que supone, con diferencia, la proporción más alta en comparación con otras industrias. [83]
A menudo, las grandes corporaciones multinacionales exhiben integración vertical , participando en una amplia gama de descubrimiento y desarrollo de fármacos, fabricación y control de calidad, marketing, ventas y distribución. Las organizaciones más pequeñas, por otro lado, suelen centrarse en un aspecto específico, como descubrir candidatos a fármacos o desarrollar formulaciones. A menudo, se forman acuerdos de colaboración entre organizaciones de investigación y grandes empresas farmacéuticas para explorar el potencial de nuevas sustancias farmacológicas. Más recientemente, las multinacionales dependen cada vez más de organizaciones de investigación por contrato para gestionar el desarrollo de fármacos. [84]
El descubrimiento y desarrollo de fármacos son muy costosos; De todos los compuestos investigados para su uso en humanos, sólo una pequeña fracción es finalmente aprobada en la mayoría de los países por instituciones o juntas médicas designadas por el gobierno, que tienen que aprobar nuevos medicamentos antes de que puedan comercializarse en esos países. En 2010, la FDA aprobó 18 NME (Nuevas Entidades Moleculares) y tres productos biológicos , o 21 en total, frente a 26 en 2009 y 24 en 2008. Por otro lado, solo hubo 18 aprobaciones en total en 2007 y 22 en 2006. Desde 2001, el Centro de Evaluación e Investigación de Medicamentos ha promediado 22,9 aprobaciones al año. [85] Esta aprobación se produce sólo después de una gran inversión en desarrollo preclínico y ensayos clínicos , así como un compromiso con el monitoreo continuo de la seguridad . Los medicamentos que fallan a mitad de este proceso a menudo generan grandes costos y no generan ingresos a cambio. Si se tiene en cuenta el coste de estos fármacos fallidos, el coste de desarrollar un nuevo fármaco exitoso ( nueva entidad química o NCE) se ha estimado en 1.300 millones de dólares [86] (sin incluir los gastos de marketing ). Sin embargo, los profesores Light y Lexchin informaron en 2012 que la tasa de aprobación de nuevos medicamentos ha sido una tasa promedio relativamente estable de 15 a 25 durante décadas. [87]
La investigación y la inversión en toda la industria alcanzaron un récord de 65.3 mil millones de dólares en 2009. [88] Si bien el costo de la investigación en los EE. UU. fue de alrededor de 34.2 mil millones de dólares entre 1995 y 2010, los ingresos aumentaron más rápidamente (los ingresos aumentaron en 200.4 mil millones de dólares en ese tiempo). [87]
Un estudio realizado por la consultora Bain & Company informó que el costo de descubrir, desarrollar y lanzar (que incluye el marketing y otros gastos comerciales) de un nuevo medicamento (junto con los posibles medicamentos que fallan) aumentó en un período de cinco años a casi 1.700 millones de dólares en 2003. [89] Según Forbes, en 2010 los costos de desarrollo oscilaban entre 4.000 y 11.000 millones de dólares por fármaco. [90]
Algunas de estas estimaciones también tienen en cuenta el costo de oportunidad de invertir capital muchos años antes de que se obtengan ingresos (consulte Valor del dinero en el tiempo ). Debido al largo tiempo necesario para el descubrimiento, desarrollo y aprobación de productos farmacéuticos, estos costos pueden acumularse hasta casi la mitad del gasto total. Una consecuencia directa dentro de la cadena de valor de la industria farmacéutica es que las principales multinacionales farmacéuticas tienden a subcontratar cada vez más los riesgos relacionados con la investigación fundamental, lo que en cierto modo remodela el ecosistema industrial en el que las empresas de biotecnología desempeñan un papel cada vez más importante y las estrategias generales se redefinen en consecuencia. [91] Algunos medicamentos aprobados, como los que se basan en la reformulación de un ingrediente activo existente (también conocidos como extensiones de línea), son mucho menos costosos de desarrollar.
En los Estados Unidos, los nuevos productos farmacéuticos deben ser aprobados por la Administración de Alimentos y Medicamentos (FDA) por ser seguros y eficaces. Este proceso generalmente implica la presentación de una solicitud de nuevo fármaco en investigación con suficientes datos preclínicos para respaldar el proceso de ensayos en humanos. Tras la aprobación del IND, se podrán realizar tres fases de ensayos clínicos en humanos cada vez más amplios. La fase I generalmente estudia la toxicidad utilizando voluntarios sanos. La Fase II puede incluir farmacocinética y dosificación en pacientes, y la Fase III es un estudio muy amplio de eficacia en la población de pacientes prevista. Tras la finalización exitosa de las pruebas de la fase III, se envía una Solicitud de Nuevo Medicamento a la FDA. La FDA revisa los datos y si se considera que el producto tiene una evaluación de riesgo-beneficio positiva, se otorga la aprobación para comercializar el producto en los EE. UU. [92]
A menudo también se requiere una cuarta fase de vigilancia posterior a la aprobación debido al hecho de que incluso los ensayos clínicos más grandes no pueden predecir de manera efectiva la prevalencia de efectos secundarios raros. La vigilancia poscomercialización garantiza que después de la comercialización se vigile de cerca la seguridad de un medicamento. En ciertos casos, puede ser necesario limitar su indicación a grupos concretos de pacientes, y en otros, la sustancia se retira completamente del mercado.
La FDA proporciona información sobre medicamentos aprobados en el sitio del Libro Naranja. [93]
En el Reino Unido, la Agencia Reguladora de Medicamentos y Productos Sanitarios aprueba y evalúa el uso de los medicamentos. Normalmente, la aprobación en el Reino Unido y otros países europeos llega más tarde que en los EE. UU. Luego es el Instituto Nacional para la Excelencia en la Salud y la Atención (NICE), para Inglaterra y Gales, quien decide si el Servicio Nacional de Salud (NHS) permitirá (en el sentido de pagar por) su uso y cómo. El Formulario Nacional Británico es la guía básica para farmacéuticos y médicos.
En muchos países occidentales no estadounidenses, se ha desarrollado un "cuarto obstáculo" de análisis de rentabilidad antes de que se puedan proporcionar nuevas tecnologías. Esto se centra en el 'precio de la eficacia' (en términos de, por ejemplo, el coste por AVAC ) de las tecnologías en cuestión. En Inglaterra y Gales, el NICE decide si el NHS pondrá a disposición medicamentos y tecnologías y en qué circunstancias, mientras que existen acuerdos similares con el Consorcio Escocés de Medicamentos en Escocia y el Comité Asesor de Beneficios Farmacéuticos en Australia. Un producto debe superar el umbral de rentabilidad para ser aprobado. Los tratamientos deben representar una "valoración del dinero" y un beneficio neto para la sociedad.
Existen normas especiales para determinadas enfermedades raras ("enfermedades huérfanas") en varios de los principales territorios reguladores de medicamentos. Por ejemplo, las enfermedades que afectan a menos de 200.000 pacientes en los Estados Unidos, o a poblaciones más grandes en determinadas circunstancias, están sujetas a la Ley de Medicamentos Huérfanos. [94] Debido a que la investigación médica y el desarrollo de medicamentos para tratar tales enfermedades son financieramente desventajosos, las empresas que lo hacen son recompensadas con reducciones de impuestos, exenciones de tarifas y exclusividad en el mercado de ese medicamento por un tiempo limitado (siete años), independientemente de si el El medicamento está protegido por patentes.
En 2011, el gasto mundial en medicamentos recetados superó los 954 mil millones de dólares, incluso cuando el crecimiento se desaceleró un poco en Europa y América del Norte. Estados Unidos representa más de un tercio del mercado farmacéutico mundial, con 340 mil millones de dólares en ventas anuales, seguido por la UE y Japón. [96] Los mercados emergentes como China, Rusia, Corea del Sur y México superaron a ese mercado, creciendo un enorme 81 por ciento. [97] [98]
Los diez medicamentos más vendidos en 2013 totalizaron 75.600 millones de dólares en ventas, siendo el fármaco antiinflamatorio Humira el fármaco más vendido en todo el mundo con 10.700 millones de dólares en ventas. Los segundos y terceros más vendidos fueron Enbrel y Remicade, respectivamente. [99] Los tres medicamentos más vendidos en los Estados Unidos en 2013 fueron Abilify ($6,3 mil millones), Nexium ($6 mil millones) y Humira ($5,4 mil millones). [100] El fármaco más vendido de todos los tiempos, Lipitor , promedió 13 mil millones de dólares al año y obtuvo un total de 141 mil millones de dólares durante su vida útil antes de que expirara la patente de Pfizer en noviembre de 2011.
IMS Health publica un análisis de las tendencias esperadas en la industria farmacéutica en 2007, incluido el aumento de las ganancias en la mayoría de los sectores a pesar de la pérdida de algunas patentes, y nuevos medicamentos de gran éxito en el horizonte. [101]
Dependiendo de una serie de consideraciones, una empresa puede solicitar y obtener una patente para el medicamento, o el proceso de producción del medicamento, otorgando derechos de exclusividad generalmente durante unos 20 años. [102] Sin embargo, sólo después de estudios y pruebas rigurosos, que demoran entre 10 y 15 años en promedio, las autoridades gubernamentales otorgarán permiso a la empresa para comercializar y vender el medicamento. [103] La protección de una patente permite al titular de la patente recuperar los costos de investigación y desarrollo mediante altos márgenes de ganancia para el medicamento de marca . Cuando expira la protección de la patente del medicamento, una empresa competidora generalmente desarrolla y vende un medicamento genérico . El desarrollo y aprobación de genéricos es menos costoso, lo que permite venderlos a un precio más bajo. A menudo, el propietario del medicamento de marca introduce una versión genérica antes de que expire la patente para tener una ventaja en el mercado de genéricos. [104] Por lo tanto, la reestructuración se ha convertido en una rutina, impulsada por la expiración de las patentes de los productos lanzados durante la "era dorada" de la industria en la década de 1990 y la incapacidad de las empresas para desarrollar suficientes nuevos productos exitosos para reemplazar los ingresos perdidos. [105]
En Estados Unidos, el valor de las recetas aumentó durante el período de 1995 a 2005 en 3.400 millones anuales, un aumento del 61 por ciento. Las ventas minoristas de medicamentos recetados aumentaron un 250 por ciento, de 72 mil millones de dólares a 250 mil millones de dólares, mientras que el precio promedio de las recetas se duplicó con creces, de 30 a 68 dólares. [106]
La publicidad es común en las revistas de salud, así como a través de los medios de comunicación más convencionales. En algunos países, especialmente en Estados Unidos, se les permite hacer publicidad directamente al público en general. Las compañías farmacéuticas generalmente emplean vendedores (a menudo llamados "representantes de medicamentos" o, un término más antiguo, "hombres de detalle") para promocionar directa y personalmente a los médicos y otros proveedores de atención médica. En algunos países, especialmente en Estados Unidos, las empresas farmacéuticas también emplean cabilderos para influir en los políticos. La comercialización de medicamentos recetados en los EE. UU. está regulada por la Ley federal de comercialización de medicamentos recetados de 1987 . El plan de marketing farmacéutico incorpora los planes de gasto, canales e ideas que harán avanzar a la asociación farmacéutica, y sus productos y administraciones, en el escenario actual.
El libro Bad Pharma también analiza la influencia de los representantes farmacéuticos, cómo las compañías farmacéuticas emplean escritores fantasmas para escribir artículos para que los publiquen los académicos, cuán independientes son realmente las revistas académicas, cómo las compañías farmacéuticas financian la educación continua de los médicos y cómo los pacientes Los grupos suelen estar financiados por la industria. [107]
Desde la década de 1980, han adquirido importancia nuevos métodos de comercialización de medicamentos recetados para los consumidores. La publicidad en medios directa al consumidor fue legalizada en la Guía de la FDA para la industria sobre anuncios de radiodifusión dirigidos al consumidor.
Ha habido una creciente controversia en torno al marketing y la influencia farmacéutica. Ha habido acusaciones y hallazgos de influencia sobre médicos y otros profesionales de la salud a través de representantes farmacéuticos, incluido el suministro constante de "obsequios" de marketing e información sesgada a los profesionales de la salud; [108] publicidad muy frecuente en revistas y congresos; financiar organizaciones sanitarias independientes y campañas de promoción de la salud; ejercer presión sobre médicos y políticos (más que cualquier otra industria en Estados Unidos [109] ); patrocinio de escuelas de medicina o formación de enfermeras; patrocinio de eventos de educación continua, con influencia en el currículo; [110] y contratación de médicos como consultores remunerados en juntas asesoras médicas.
Algunos grupos de defensa, como No Free Lunch y AllTrials , han criticado el efecto de la comercialización de medicamentos a los médicos porque dicen que los predispone a recetar los medicamentos comercializados incluso cuando otros podrían ser más baratos o mejores para el paciente. [111]
Ha habido acusaciones relacionadas de tráfico de enfermedades [112] (medicalización excesiva) para expandir el mercado de medicamentos. En 2006 se celebró en Australia una conferencia inaugural sobre ese tema. [113] En 2009, el Servicio Nacional de Prescripción, financiado por el Gobierno, lanzó el programa "Finding Evidence - Recognizing Hype", destinado a educar a los médicos de cabecera sobre métodos para el análisis independiente de medicamentos. [114]
Los metanálisis han demostrado que los estudios psiquiátricos patrocinados por compañías farmacéuticas tienen muchas más probabilidades de arrojar resultados positivos, y si participa un empleado de una compañía farmacéutica, el efecto es aún mayor. [115] [116] [117] La influencia también se ha extendido a la formación de médicos y enfermeras en las facultades de medicina, contra lo que se está combatiendo.
Se ha argumentado que el diseño del Manual Diagnóstico y Estadístico de los Trastornos Mentales y la ampliación de los criterios representan una medicalización creciente de la naturaleza humana, o " traficante de enfermedades ", impulsada por la influencia de las compañías farmacéuticas en la psiquiatría. [118] Se ha planteado el potencial de conflicto de intereses directo, en parte porque aproximadamente la mitad de los autores que seleccionaron y definieron los trastornos psiquiátricos del DSM-IV tenían o habían tenido anteriormente relaciones financieras con la industria farmacéutica. [119]
En los EE. UU., a partir de 2013, según los Informes de transparencia financiera de los médicos (parte de la Ley Sunshine), los Centros de servicios de Medicare y Medicaid deben recopilar información de los fabricantes correspondientes y de las organizaciones de compras grupales para poder reportar información sobre sus relaciones financieras con médicos y hospitales. Los datos se hacen públicos en el sitio web de los Centros de Servicios de Medicare y Medicaid. La expectativa es que la relación entre los médicos y la industria farmacéutica sea completamente transparente. [120]
En un informe realizado por OpenSecrets , había más de 1.100 cabilderos trabajando de alguna manera para el negocio farmacéutico en 2017. En el primer trimestre de 2017, la industria farmacéutica y de productos sanitarios gastó 78 millones de dólares en cabildeo ante miembros del Congreso de los Estados Unidos. [121]
El precio de los productos farmacéuticos se está convirtiendo en un desafío importante para los sistemas de salud. [122] Un estudio de noviembre de 2020 realizado por el West Health Policy Center afirmó que se espera que más de 1,1 millones de personas mayores en el programa Medicare de EE. UU . mueran prematuramente durante la próxima década porque no podrán pagar sus medicamentos recetados, lo que requerirá $17,7 adicionales. miles de millones que se gastarán anualmente en costos médicos evitables debido a complicaciones de salud. [123]
Ben Goldacre ha argumentado que los reguladores –como la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) en el Reino Unido, o la Administración de Alimentos y Medicamentos (FDA) en los Estados Unidos– promueven los intereses de las compañías farmacéuticas en lugar de los intereses de las empresas farmacéuticas. público debido al intercambio de puertas giratorias de empleados entre el regulador y las empresas y al desarrollo de amistades entre el regulador y los empleados de la empresa. [124] Sostiene que los reguladores no exigen que los nuevos medicamentos ofrezcan una mejora con respecto a los que ya están disponibles, ni siquiera que sean particularmente efectivos. [124]
Otros han argumentado que una regulación excesiva suprime la innovación terapéutica y que el costo actual de los ensayos clínicos requeridos por los reguladores impide la plena explotación de nuevos conocimientos genéticos y biológicos para el tratamiento de enfermedades humanas. Un informe de 2012 del Consejo Presidencial de Asesores en Ciencia y Tecnología hizo varias recomendaciones clave para reducir las cargas regulatorias para el desarrollo de nuevos medicamentos, incluyendo 1) ampliar el uso de procesos de aprobación acelerados por parte de la FDA, 2) crear una vía de aprobación acelerada para los medicamentos destinados a su uso. en poblaciones estrictamente definidas, y 3) emprender proyectos piloto diseñados para evaluar la viabilidad de un nuevo proceso de aprobación de medicamentos adaptativo. [125]
El fraude farmacéutico implica engaños que aportan beneficios económicos a una empresa farmacéutica. Afecta a particulares y a aseguradoras públicas y privadas. Hay varios esquemas diferentes [126] utilizados para defraudar al sistema de atención médica que son específicos de la industria farmacéutica. Estos incluyen: violaciones de las buenas prácticas de fabricación (GMP), marketing no autorizado, fraude al mejor precio, fraude CME, informes de precios de Medicaid y medicamentos compuestos fabricados. [127] De esta cantidad, 2.500 millones de dólares se recuperaron a través de casos de la Ley de Reclamaciones Falsas en el año fiscal 2010. Ejemplos de casos de fraude incluyen el acuerdo de 3.000 millones de dólares de GlaxoSmithKline , el acuerdo de 2.300 millones de dólares de Pfizer y el acuerdo de 650 millones de dólares de Merck & Co. Los daños por fraude se pueden recuperar mediante el uso de la Ley de Reclamaciones Falsas , más comúnmente bajo las disposiciones qui tam que recompensan a un individuo por ser un " denunciante " o relator (ley) . [128]
Todas las grandes empresas que venden antipsicóticos atípicos ( Bristol-Myers Squibb , Eli Lilly and Company , Pfizer , AstraZeneca y Johnson & Johnson ) han llegado a acuerdos recientes en casos gubernamentales, en virtud de la Ley de Reclamaciones Falsas, por cientos de millones de dólares o están actualmente bajo investigación por posible fraude en la atención médica. Tras acusaciones de marketing ilegal, dos de los acuerdos establecieron récords en 2009 por las multas penales más grandes jamás impuestas a corporaciones. Uno involucró el antipsicótico Zyprexa de Eli Lilly , y el otro involucró Bextra , un medicamento antiinflamatorio utilizado para la artritis. En el caso Bextra, el gobierno también acusó a Pfizer de comercializar ilegalmente otro antipsicótico, Geodon ; Pfizer resolvió esa parte de la demanda por 301 millones de dólares, sin admitir ninguna irregularidad. [129]
El 2 de julio de 2012, GlaxoSmithKline se declaró culpable de cargos penales y acordó un acuerdo de 3.000 millones de dólares en el mayor caso de fraude sanitario en Estados Unidos y el mayor pago realizado por una empresa farmacéutica. [130] El acuerdo está relacionado con la promoción ilegal de medicamentos recetados por parte de la empresa, su omisión de informar datos de seguridad, [131] el soborno a médicos y la promoción de medicamentos para usos para los que no estaban autorizados. Los medicamentos involucrados fueron Paxil , Wellbutrin , Advair , Lamictal y Zofran para usos no autorizados y no cubiertos. Estos y los medicamentos Imitrex , Lotronex , Flovent y Valtrex estuvieron involucrados en el plan de sobornos . [132] [133] [134]
La siguiente es una lista de los cuatro acuerdos más importantes alcanzados con compañías farmacéuticas entre 1991 y 2012, ordenados por el tamaño del acuerdo total. Los reclamos legales contra la industria farmacéutica han variado ampliamente en las últimas dos décadas, incluido el fraude a Medicare y Medicaid , la promoción no autorizada y las prácticas de fabricación inadecuadas. [135] [136]
En mayo de 2015, el New England Journal of Medicine enfatizó la importancia de las interacciones entre la industria farmacéutica y los médicos para el desarrollo de nuevos tratamientos, y argumentó que la indignación moral por las malas conductas de la industria había llevado injustificadamente a muchos a enfatizar demasiado los problemas creados por los conflictos de intereses financieros. El artículo señalaba que las principales organizaciones sanitarias, como el Centro Nacional para el Avance de las Ciencias Traslacionales de los Institutos Nacionales de Salud, el Consejo Presidencial de Asesores en Ciencia y Tecnología, el Foro Económico Mundial, la Fundación Gates, el Wellcome Trust y el Food and La Administración de Medicamentos había fomentado mayores interacciones entre los médicos y la industria para mejorar los beneficios para los pacientes. [141] [142]
En noviembre de 2020, varias empresas farmacéuticas anunciaron ensayos exitosos de vacunas contra la COVID-19, con una eficacia del 90 al 95 % en la prevención de la infección. Según los anuncios de la empresa y los datos revisados por analistas externos, estas vacunas tienen un precio de entre 3 y 37 dólares por dosis. [143] El Wall Street Journal publicó un editorial pidiendo que este logro fuera reconocido con el Premio Nobel de la Paz. [144]
Médicos Sin Fronteras advirtió que los altos precios y los monopolios sobre medicamentos, pruebas y vacunas prolongarían la pandemia y costarían vidas. Instaron a los gobiernos a evitar la especulación, utilizando licencias obligatorias según sea necesario, como ya lo habían hecho Canadá, Chile, Ecuador, Alemania e Israel. [145]
El 20 de febrero, 46 legisladores estadounidenses pidieron al gobierno estadounidense que no otorgara derechos de monopolio al otorgar dinero de los contribuyentes para el desarrollo de vacunas y tratamientos contra el coronavirus, para evitar otorgar el control exclusivo de los precios y la disponibilidad a los fabricantes privados. [146]
En Estados Unidos, el gobierno firmó acuerdos en los que se subvencionaba la investigación y el desarrollo y/o la construcción de plantas de fabricación de posibles terapias contra el COVID-19. Normalmente, el acuerdo implicaba que el gobierno se hiciera cargo de una determinada cantidad de dosis del producto sin pago adicional. Por ejemplo, bajo los auspicios de la Operación Warp Speed en Estados Unidos, el gobierno subvencionó investigaciones relacionadas con las vacunas y terapias contra la COVID-19 en Regeneron, [147] Johnson and Johnson, Moderna, AstraZeneca, Novavax, Pfizer y GSK. Los términos típicos implicaban subsidios para investigación de entre 400 y 2 mil millones de dólares, e incluían la propiedad gubernamental de los primeros 100 millones de dosis de cualquier vacuna contra el COVID-19 desarrollada con éxito. [148]
La empresa farmacéutica estadounidense Gilead solicitó y obtuvo el estatus de medicamento huérfano para remdesivir de la Administración de Medicamentos y Alimentos de los EE. UU . (FDA) el 23 de marzo de 2020. Esta disposición tiene como objetivo fomentar el desarrollo de medicamentos que afectan a menos de 200.000 estadounidenses mediante la concesión de derechos de monopolio legales reforzados y ampliados. al fabricante, junto con exenciones de impuestos y tasas gubernamentales. [149] [150] Remdesivir es un candidato para tratar COVID-19; en el momento en que se concedió el estatus, menos de 200.000 estadounidenses tenían COVID-19, pero las cifras aumentaron rápidamente a medida que la pandemia de COVID-19 llegó a los EE. UU., y pronto se consideró inevitable cruzar el umbral. [149] [150] Remdesivir fue desarrollado por Gilead con más de $79 millones en financiación del gobierno de EE. UU. [150] En mayo de 2020, Gilead anunció que proporcionaría las primeras 940.000 dosis de remdesivir al gobierno federal de forma gratuita. [151] Después de enfrentar fuertes reacciones públicas, Gilead renunció al estatus de "medicamento huérfano" para remdesivir el 25 de marzo. [152] Gilead conserva patentes de remdesivir por 20 años en más de 70 países. [145] En mayo de 2020, la compañía anunció además que estaba en conversaciones con varias compañías de genéricos para otorgar derechos para producir remdesivir para los países en desarrollo, y con Medicines Patent Pool para brindar un acceso genérico más amplio. [153]
Las patentes han sido criticadas en el mundo en desarrollo, ya que se cree que [ ¿ quién? ] para reducir el acceso a los medicamentos existentes. [154] Conciliar las patentes y el acceso universal a los medicamentos requeriría una política internacional eficiente de discriminación de precios . Además, según el acuerdo ADPIC de la Organización Mundial del Comercio , los países deben permitir que se patenten productos farmacéuticos. En 2001, la OMC adoptó la Declaración de Doha , que indica que el acuerdo ADPIC debe leerse teniendo en cuenta los objetivos de salud pública y permite algunos métodos para eludir los monopolios farmacéuticos: mediante licencias obligatorias o importaciones paralelas , incluso antes de que expiren las patentes. [155]
En marzo de 2001, 40 compañías farmacéuticas multinacionales entablaron un litigio contra Sudáfrica por su Ley de Medicamentos , que permitía la producción genérica de medicamentos antirretrovirales (ARV) para el tratamiento del VIH, a pesar de que estos medicamentos estaban protegidos por patentes. [156] El VIH era y es una epidemia en Sudáfrica, y los ARV en ese momento costaban entre 10.000 y 15.000 dólares por paciente al año. Esto era inasequible para la mayoría de los ciudadanos sudafricanos, por lo que el gobierno sudafricano se comprometió a proporcionar ARV a precios más cercanos a lo que la gente podía pagar. Para hacerlo, tendrían que ignorar las patentes de los medicamentos y producir genéricos dentro del país (mediante una licencia obligatoria), o importarlos del extranjero. Después de las protestas internacionales a favor de los derechos de salud pública (incluida la recolección de 250.000 firmas por parte de Médicos Sin Fronteras ), los gobiernos de varios países desarrollados (incluidos los Países Bajos, Alemania, Francia y más tarde Estados Unidos) respaldaron al gobierno sudafricano, y el El caso fue abandonado en abril de ese año. [157]
En 2016, GlaxoSmithKline (la sexta compañía farmacéutica más grande del mundo) anunció que eliminaría sus patentes en los países pobres para permitir que compañías independientes fabriquen y vendan versiones de sus medicamentos en esas áreas, ampliando así el acceso público a ellos. [158] GlaxoSmithKline publicó una lista de 50 países en los que ya no tendrían patentes, lo que afecta a mil millones de personas en todo el mundo.
En 2011, cuatro de las 20 principales donaciones caritativas corporativas y ocho de las 30 principales donaciones caritativas corporativas provinieron de fabricantes farmacéuticos. La mayor parte de las donaciones caritativas corporativas (69% a partir de 2012) provienen de donaciones caritativas no monetarias, la mayoría de las cuales nuevamente fueron donaciones aportadas por compañías farmacéuticas. [159]
Los programas benéficos y los esfuerzos de descubrimiento y desarrollo de fármacos por parte de compañías farmacéuticas incluyen:
La misión principal de la industria farmacéutica es fabricar productos para pacientes para curarlos, vacunarlos o aliviar un síntoma, a menudo mediante la fabricación de un líquido inyectable o un sólido oral, entre otras terapias.
Los funcionarios de la Administración de Alimentos y Medicamentos, conscientes de la gravedad del problema, estiman que aproximadamente la mitad de los 9.000.000.000 de cápsulas y tabletas de barbitúricos y anfetaminas que se fabrican anualmente en este país se desvían para uso ilegal.
Los beneficios que se obtienen con la venta ilegal de estas drogas han demostrado ser un atractivo para el crimen organizado, ya que la anfetamina se puede comprar al por mayor por menos de 1 dólar por 1.000 cápsulas, pero cuando se vende en el mercado ilegal, cuesta entre 30 y 50 dólares por 1.000. y cuando se vende al por menor a un comprador individual, una tableta puede costar entre 10 y 25 centavos.
Los barbitúricos, introducidos en la medicina por E. Fischer y J. von Mering en 1903, se encuentran sin duda entre las drogas más utilizadas y de las que más se abusa en medicina.
Cada año se fabrican aproximadamente 400 toneladas de estos agentes;
esto es suficiente para hacer dormir aproximadamente a 9.000.000 de personas cada noche durante ese período si a cada una se le administrara 0,1 g.
dosis
{{cite web}}: Mantenimiento CS1: copia archivada como título ( enlace )