Las lactonas son ésteres carboxílicos cíclicos , son ésteres intramoleculares derivados de ácidos hidroxicarboxílicos. Pueden ser saturados o insaturados. Algunos contienen heteroátomos que reemplazan uno o más átomos de carbono del anillo. [1]
Las lactonas se forman mediante esterificación intramolecular de los correspondientes ácidos hidroxicarboxílicos, que se produce de forma espontánea cuando el anillo formado tiene cinco o seis miembros. Las lactonas con anillos de tres o cuatro miembros (α-lactonas y β-lactonas) son muy reactivas, lo que dificulta su aislamiento. Normalmente se requieren métodos especiales para la síntesis en laboratorio de lactonas de anillos pequeños, así como de aquellas que contienen anillos de más de seis miembros. [2]
Los prefijos griegos en orden alfabético indican el tamaño del anillo.
Las lactonas suelen denominarse según la molécula de ácido precursora ( aceto = 2 átomos de carbono, propio = 3, butiro = 4, valero = 5, capro = 6, etc.), con un sufijo -lactona y un prefijo de letra griega que especifica la número de átomos de carbono en el heterociclo, es decir, la distancia entre los grupos -OH y -COOH relevantes a lo largo de dicha cadena principal. El primer átomo de carbono después del carbono del grupo -COOH en el compuesto original se marcará con α, el segundo se marcará con β, y así sucesivamente. Por lo tanto, los prefijos también indican el tamaño del anillo de lactona: α-lactona = anillo de 3 miembros, β-lactona = 4 miembros, γ-lactona = 5 miembros, δ-lactona = 6 miembros, etc.Las lactonas macrocíclicas se conocen como macrolactonas . [3]
El otro sufijo utilizado para indicar una lactona es -olido , utilizado en nombres de clases de sustancias como butenólido , macrólido , cardenólido o bufadienólido .
Para obtener los nombres IUPAC preferidos , las lactonas se denominan pseudocetonas heterocíclicas añadiendo el sufijo 'uno', 'diona', 'tiona', etc. y los prefijos multiplicativos apropiados al nombre del hidruro original heterocíclico. [4]
El nombre lactona deriva del compuesto del anillo llamado lactida , que se forma a partir de la deshidratación del ácido 2-hidroxipropanoico ( ácido láctico ) CH3 - CH(OH)-COOH. El ácido láctico, a su vez, deriva su nombre de su aislamiento original de la leche agria (latín: lac, lactis). El nombre fue acuñado en 1844 por el químico francés Théophile-Jules Pelouze , quien lo obtuvo por primera vez como un derivado del ácido láctico. [5] Una reacción de deshidratación interna dentro de la misma molécula de ácido láctico habría producido alfa-propiolactona , una lactona con un anillo de 3 miembros.
En 1880, el químico alemán Wilhelm Rudolph Fittig amplió el nombre de "lactona" a todos los ésteres carboxílicos intramoleculares. [6]
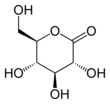
Las lactonas más estables son las γ-lactonas de 5 miembros y las δ-lactonas de 6 miembros porque, como en la mayoría de los ciclos orgánicos, los anillos de 5 y 6 miembros minimizan la tensión de los ángulos de enlace . Las β-lactonas no se pueden aislar, sino que sólo se pueden producir mediante métodos especiales. Las α-lactonas pueden detectarse como especies transitorias en experimentos de espectrometría de masas . [7] Las reacciones de las lactonas son similares a las de los ésteres.
Muchas lactonas naturales son γ y δ-lactonas, tanto saturadas como insaturadas. Contribuyen al aroma de frutas, mantequilla, queso y otros alimentos.
Las lactonas macrocíclicas también son productos naturales importantes. La ciclopentadecanolida es responsable del olor almizclado del aceite de raíz de angélica . De las lactonas bicíclicas naturales, las ftalidas son responsables de los olores del apio y los aceites de apio , y la cumarina de la aspa . [8] Las lactonas están presentes en la madera de roble y contribuyen al perfil de sabor de las cervezas envejecidas en barrica . [9]
Los anillos de lactona se encuentran ampliamente como componentes básicos en la naturaleza, como en el ácido ascórbico , kavain , nepetalactona , gluconolactona , hormonas ( espironolactona , mevalonolactona), enzimas ( lactonasa ), neurotransmisores ( butirolactona , avermectinas ), antibióticos ( macrólidos como la eritromicina ; anfotericina B ) . , medicamentos contra el cáncer ( vernolepina , epotilonas ), fitoestrógenos ( lactonas del ácido resorcílico , glucósidos cardíacos ).

Muchos métodos de síntesis de ésteres también se pueden aplicar a la síntesis de lactonas. La lactonización compite con la polimerización por hidroxiácidos más largos. Las γ-lactonas, por otro lado, son tan estables que los 4-hidroxiácidos (R-CH(OH)-(CH 2 ) 2 -CO 2 H) se ciclan espontáneamente a lactona.
En una síntesis industrial de oxandrolona, el paso clave para la formación de lactonas es una reacción orgánica : la esterificación . [10] [11]

En la halolactonización , un alqueno es atacado por un halógeno mediante adición electrófila y el intermedio catiónico es capturado intramolecularmente por un ácido carboxílico adyacente . [12]
Los métodos específicos incluyen la esterificación de Yamaguchi , la macrolactonización de Shiina , la macrolactonización de Corey-Nicolaou , la oxidación de Baeyer-Villiger y la abstracción nucleofílica .

Las γ-lactonas γ-octalactona , γ-nonalactona , γ-decalactona , γ-undecalactona se pueden preparar con buen rendimiento en un proceso de un solo paso mediante la adición radicalaria de alcoholes grasos primarios al ácido acrílico , usando peróxido de di-terc-butilo como un catalizador. [8]
Una reacción radical alternativa que produce γ-lactonas es el acoplamiento mediado por manganeso .
Las lactonas exhiben las reacciones características de los ésteres.
Calentar una lactona con una base ( hidróxido de sodio ) hidrolizará la lactona a su compuesto original, el compuesto bifuncional de cadena lineal. Al igual que los ésteres de cadena lineal, la reacción de hidrólisis-condensación de las lactonas es una reacción reversible , con equilibrio . Sin embargo, la constante de equilibrio de la reacción de hidrólisis de la lactona es menor que la del éster de cadena lineal, es decir, los productos (hidroxiácidos) son menos favorecidos en el caso de las lactonas. Esto se debe a que, aunque las entalpías de la hidrólisis de ésteres y lactonas son aproximadamente las mismas, la entropía de la hidrólisis de las lactonas es menor que la entropía de los ésteres de cadena lineal. Los ésteres de cadena lineal dan dos productos tras la hidrólisis, lo que hace que el cambio de entropía sea más favorable que en el caso de las lactonas, que dan un solo producto.
Las lactonas también reaccionan para dar alcohol y amida de anillo abierto.
Las lactonas se pueden reducir a dioles utilizando hidruro de litio y aluminio . Por ejemplo, las gamma-lactonas se reducen a butano-1,4-diol, (CH 2 (OH)-(CH 2 ) 2 -CH 2 (OH).
Las lactonas forman fácilmente poliésteres según la fórmula y se ha demostrado que también se oligomerizan sin catalizador: [13] [14]
La doble lactona llamada lactida se polimeriza formando ácido poliláctico (polilactida). Los materiales resultantes, el ácido poliláctico, tienen muchas propiedades atractivas. [15] [16]
Las lactonas contribuyen significativamente al sabor de la fruta y de los productos lácteos fermentados y no fermentados [17] y, por lo tanto, se utilizan como sabores y fragancias. [8] Algunos ejemplos son la γ-decalactona (4-decanolida), que tiene un sabor característico a melocotón; [17] δ-decalactona (5-decanolida), que tiene un sabor cremoso a coco/melocotón; γ-dodecalactona (4-dodecanolida), que también tiene sabor a coco/afrutado, [17] descripción que también encaja con la γ-octalactona (4-octanolida), [18] aunque también tiene un carácter herbáceo; [17] γ-nonalactona , que tiene un intenso sabor a coco de esta serie, a pesar de no encontrarse en el coco, [19] y γ-undecalactona.
Las lactonas macrocíclicas ( ciclopentadecanolida , 15-pentadec-11/12-enolida) tienen olores similares a las cetonas macrocíclicas de origen animal ( muscona , civetona ), pero se pueden preparar más fácilmente, por ejemplo, mediante despolimerización de los correspondientes poliésteres lineales . La sustitución de una unidad de metileno por oxígeno apenas afecta el olor de estos compuestos, y además de la ciclopentadecanolida (p. ej., 12-oxa-16-hexadecanolida) se producen oxalactonas con anillos de 15 a 17 miembros. [8]
Se ha demostrado que las lactonas prebióticamente plausibles, como la ε-caprolactona y la δ-valerolactona, se oligomerizan sin el uso de catalizadores formando oligómeros que pueden haber sido relevantes durante el origen de la vida . [20]
La policaprolactona es un plástico importante.