Buckminsterfullereno
El buckminsterfullereno, buckybola o futboleno es una molécula de fullereno esférico con la fórmula empírica C60.
Fue preparado intencionalmente por primera vez en 1985 por Harold Kroto, James R. Heath, Sean O'Brien, Robert Curl y Richard Smalley en la Universidad Rice.
El nombre es un homenaje a Buckminster Fuller, el ingeniero inventor de la cúpula geodésica, que tiene una enorme semejanza con esta molécula.
El nombre buckminsterfullerene deriva del notorio inventor y futurista Buckminster Fuller.
En los años 1980, Richard Smalley y Bob Curl de la Universidad Rice desarrollaron una técnica para aislar estas sustancias.
Kroto utilizó la misma técnica, empleando un blanco de grafito como objetivo para el láser.
Kroto mencionó su similitud con las cúpulas geodésicas del notable ingeniero, arquitecto, inventor y futurólogo Buckminster Fuller, eso condujo finalmente al nombre de buckminsterfullereno.
[11] En 1989, los miembros del grupo Heidelberg/Tuscon, liderado por los físicos Wolfgang Krätschmer y Donald Huffman, observaron una absorción óptica inusual en láminas delgadas de carbono generadas por arco eléctrico entre barras de grafito.
Los fullerenos son extraídos del hollín usando un procedimiento de múltiples etapas.
Este paso lleva a una disolución que contiene más del 75% de C60, así como otros fullerenos.
[13] La molécula C60 es extremadamente estable, siendo capaz de resistir altas temperaturas y presiones.
El C60 puede sufrir seis reducciones monoelectrónicas reversibles hasta C606-, mientras que la oxidación es irreversible.
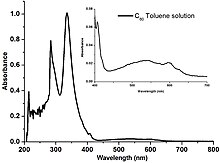
[15] Los fulerenos son un poco solubles en muchos disolventes aromáticos como el tolueno y también en otros apolares, como el disulfuro de carbono, pero no en agua.
Esto permite que una disolución donde las moléculas no se encuentran formando agregados pueda transmitir un poco de luz azul y roja lo que resulta en un color púrpura de la misma.
Al evaporar el disolvente, las interacciones moleculares provocan la superposición y ensanchamiento de las bandas energéticas, eliminando así la transmisión de la luz azul y haciendo que el color púrpura vire hacia el marrón.
A temperaturas por encima de la máxima solubilidad, el solvato no es estable, ni siquiera sumergido en la solución saturada, y funde para formar C60 cF.
El C60 forma un sólido amarronado con una barrera de absorción óptica a aproximadamente 1,6 eV.
Estos huecos son lo suficientemente grandes como para acomodar átomos de diferentes tipos.
Recientemente, la superconductividad a 38 K ha sido reportada en Cs3C60 en gran cantidad,[33] pero solo bajo la aplicación de presión.
Por lo tanto, ha habido muchos esfuerzos en incrementar la separación dentro del fullereno, en particular, intercalando moléculas neutras dentro de la red A3C60 para incrementar el espaciado interfullereno mientras que la valencia del C60 se mantiene inalterada.
[35] Una banda estrecha o un sistema electrónico fuertemente correlacionado y estados basales degenerados son puntos importantes para entender la superconductividad en fullerenos sólidos.
[44] Algunos experimentos sugieren que el C60 al cual se le han añadido metales alcalinos posee propiedades catalíticas similares a las del platino.
[45] Desde entonces, diversos aceites con C60 son comercializados como antioxidantes para consumo humano, pero un experimento posterior mostró que la exposición a la luz degradaba a esos aceites, volviéndolos tóxicos y haciendo que incrementasen 'masivamente' el riesgo de contraer cáncer (tumores).
[46][47] Para evitar ese riesgo, los aceites con C60 deberían ser producidos en ambientes muy oscuros, embotellados en recipientes de la mayor opacidad posible, y guardados en la oscuridad, siendo además conveniente el consumirlos en lugares poco luminosos y el advertir mediante etiquetas de los peligros que tiene la luz para esos productos.
[46][48] Algunas empresas han conseguido disolver C60 en agua para evitar posibles problemas con el aceite, pero en principio eso no protege al C60 de la luz, por lo que habría que tomar las mismas precauciones.