La aspirina , también conocida como ácido acetilsalicílico ( AAS ), es un fármaco antiinflamatorio no esteroide (AINE) que se utiliza para reducir el dolor , la fiebre y/o la inflamación , y como antitrombótico . [10] Las afecciones inflamatorias específicas para las que se utiliza la aspirina incluyen la enfermedad de Kawasaki , la pericarditis y la fiebre reumática . [10]
La aspirina también se usa a largo plazo para ayudar a prevenir futuros ataques cardíacos , accidentes cerebrovasculares isquémicos y coágulos sanguíneos en personas con alto riesgo. [10] En el caso del dolor o la fiebre, los efectos suelen comenzar en 30 minutos. [10] La aspirina funciona de manera similar a otros AINE, pero también suprime el funcionamiento normal de las plaquetas . [10]
Un efecto adverso común es el malestar estomacal . [10] Los efectos secundarios más significativos incluyen úlceras de estómago , sangrado estomacal y empeoramiento del asma . [10] El riesgo de sangrado es mayor entre las personas mayores, que beben alcohol , toman otros AINE o están tomando otros anticoagulantes . [10] La aspirina no se recomienda en la última parte del embarazo . [10] Generalmente no se recomienda en niños con infecciones debido al riesgo de síndrome de Reye . [10] Las dosis altas pueden provocar zumbidos en los oídos . [10]
Un precursor de la aspirina que se encuentra en la corteza del sauce (género Salix ) se ha utilizado por sus efectos sobre la salud durante al menos 2400 años. [11] [12] En 1853, el químico Charles Frédéric Gerhardt trató el medicamento salicilato de sodio con cloruro de acetilo para producir ácido acetilsalicílico por primera vez. [13] Durante los siguientes 50 años, otros químicos, principalmente de la empresa alemana Bayer , establecieron la estructura química e idearon métodos de producción más eficientes. [13] : 69–75
La aspirina está disponible sin receta médica como medicamento patentado o genérico [10] en la mayoría de las jurisdicciones. Es uno de los medicamentos más utilizados a nivel mundial, con un consumo estimado de 40.000 toneladas (44.000 toneladas) (50 a 120 mil millones de pastillas ) cada año, [11] [14] y está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [15] En 2022, fue el 36.º medicamento más recetado en los Estados Unidos, con más de 16 millones de recetas. [16] [17]
En 1897, los científicos de la empresa Bayer comenzaron a estudiar el ácido acetilsalicílico como un medicamento de reemplazo menos irritante para los medicamentos comunes a base de salicilato. [13] : 69–75 [18] En 1899, Bayer lo había llamado "Aspirina" y lo vendía en todo el mundo. [19]
La popularidad de la aspirina creció durante la primera mitad del siglo XX, lo que llevó a la competencia entre muchas marcas y fórmulas. [20] La palabra Aspirina era el nombre comercial de Bayer; sin embargo, sus derechos sobre la marca registrada se perdieron o se vendieron en muchos países . [20] El nombre es en última instancia una mezcla del prefijo a (cetil) + spir Spiraea , el género de plantas reina de los prados del que originalmente se derivó el ácido acetilsalicílico en Bayer + -in , el sufijo químico común. [ cita requerida ]
La aspirina se descompone rápidamente en soluciones de acetato de amonio o de acetatos , carbonatos , citratos o hidróxidos de metales alcalinos . Es estable en aire seco, pero se hidroliza gradualmente en contacto con la humedad para formar ácidos acético y salicílico . En solución con álcalis, la hidrólisis se produce rápidamente y las soluciones transparentes formadas pueden consistir enteramente en acetato y salicilato. [21]
Al igual que los molinos de harina , las fábricas que producen tabletas de aspirina deben controlar la cantidad de polvo que se transporta por el aire dentro del edificio, porque la mezcla de polvo y aire puede ser explosiva . El Instituto Nacional para la Seguridad y Salud Ocupacional (NIOSH) ha establecido un límite de exposición recomendado en los Estados Unidos de 5 mg/m 3 (promedio ponderado en el tiempo). [22] En 1989, la Administración de Seguridad y Salud Ocupacional (OSHA) estableció un límite de exposición legal permisible para la aspirina de 5 mg/m 3 , pero esto fue anulado por la decisión AFL-CIO v. OSHA en 1993. [23]
La síntesis de aspirina se clasifica como una reacción de esterificación . El ácido salicílico se trata con anhídrido acético , un derivado del ácido, lo que provoca una reacción química que convierte el grupo hidroxilo del ácido salicílico en un grupo éster (R-OH → R-OCOCH 3 ). Este proceso produce aspirina y ácido acético , que se considera un subproducto de esta reacción. Casi siempre se utilizan pequeñas cantidades de ácido sulfúrico (y ocasionalmente ácido fosfórico ) como catalizador . Este método se demuestra comúnmente en los laboratorios de enseñanza de pregrado. [24]
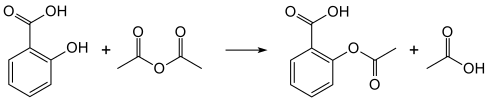
La reacción entre el ácido acético y el ácido salicílico también puede formar aspirina, pero esta reacción de esterificación es reversible y la presencia de agua puede provocar la hidrólisis de la aspirina, por lo que se prefiere un reactivo anhidro. [25]
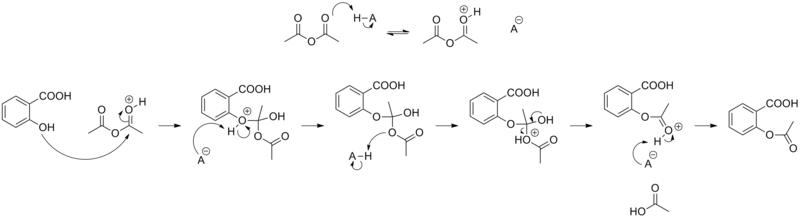
Las formulaciones que contienen altas concentraciones de aspirina a menudo huelen a vinagre [26] porque la aspirina puede descomponerse por hidrólisis en condiciones húmedas, produciendo ácidos salicílico y acético. [27]
La aspirina, un derivado acetilado del ácido salicílico, es una sustancia blanca, cristalina y débilmente ácida que se funde a 136 °C (277 °F), [9] y se descompone alrededor de 140 °C (284 °F). [28] Su constante de disociación ácida (p K a ) es 3,5 a 25 °C (77 °F). [29]
El polimorfismo , o la capacidad de una sustancia de formar más de una estructura cristalina , es importante en el desarrollo de ingredientes farmacéuticos. Muchos medicamentos reciben aprobación regulatoria solo para una única forma cristalina o polimorfo.
Sólo se ha demostrado la existencia de un polimorfo , la forma I de la aspirina, aunque desde los años 1960 se ha debatido la existencia de otro polimorfo, y un informe de 1981 informó que, cuando se cristaliza en presencia de anhídrido de aspirina , el difractograma de la aspirina presenta picos adicionales débiles. Aunque en su momento se descartó como una mera impureza, en retrospectiva se trataba de la forma II de la aspirina. [30]
La Forma II se informó en 2005, [31] [32] encontrada después del intento de cocristalización de aspirina y levetiracetam a partir de acetonitrilo caliente .
En la forma I, los pares de moléculas de aspirina forman dímeros centrosimétricos a través de los grupos acetilo con el protón metilo (ácido) uniendo los enlaces de hidrógeno con el grupo carbonilo . En la forma II, cada molécula de aspirina forma los mismos enlaces de hidrógeno, pero con dos moléculas vecinas en lugar de una. Con respecto a los enlaces de hidrógeno formados por los grupos de ácido carboxílico , ambos polimorfos forman estructuras diméricas idénticas. Los polimorfos de aspirina contienen secciones bidimensionales idénticas y, por lo tanto, se describen con mayor precisión como politipos. [33]
La aspirina de forma II pura se puede preparar sembrando el lote con anhidrato de aspirina al 15 % en peso. [30]
En 1971, el farmacólogo británico John Robert Vane , entonces empleado por el Real Colegio de Cirujanos de Londres, demostró que la aspirina suprimía la producción de prostaglandinas y tromboxanos . [34] [35] Por este descubrimiento fue galardonado con el Premio Nobel de Fisiología o Medicina de 1982 , junto con Sune Bergström y Bengt Ingemar Samuelsson . [36]
La capacidad de la aspirina para suprimir la producción de prostaglandinas y tromboxanos se debe a su inactivación irreversible de la enzima ciclooxigenasa (COX; oficialmente conocida como prostaglandina-endoperóxido sintasa, PTGS), necesaria para la síntesis de prostaglandinas y tromboxanos. La aspirina actúa como un agente acetilante donde un grupo acetilo se une covalentemente a un residuo de serina en el sitio activo de la enzima COX ( inhibición suicida ). Esto hace que la aspirina sea diferente de otros AINE (como el diclofenaco y el ibuprofeno ), que son inhibidores reversibles.
El uso de aspirina en dosis bajas bloquea irreversiblemente la formación de tromboxano A2 en las plaquetas, produciendo un efecto inhibidor sobre la agregación plaquetaria durante la vida de la plaqueta afectada (8-9 días). Esta propiedad antitrombótica hace que la aspirina sea útil para reducir la incidencia de ataques cardíacos en personas que han tenido un ataque cardíaco, angina inestable, accidente cerebrovascular isquémico o accidente isquémico transitorio. [37] 40 mg de aspirina al día son capaces de inhibir una gran proporción de la liberación máxima de tromboxano A2 provocada de forma aguda, y la síntesis de prostaglandina I2 se ve poco afectada; sin embargo, se requieren dosis más altas de aspirina para lograr una mayor inhibición. [38]
Las prostaglandinas, hormonas locales producidas en el cuerpo, tienen diversos efectos, entre ellos la transmisión de información sobre el dolor al cerebro, la modulación del termostato hipotalámico y la inflamación. Los tromboxanos son responsables de la agregación de plaquetas que forman coágulos sanguíneos . Los ataques cardíacos son causados principalmente por coágulos sanguíneos, y las dosis bajas de aspirina se consideran una intervención médica eficaz para prevenir un segundo infarto agudo de miocardio. [39]
La aspirina actúa sobre al menos dos tipos diferentes de ciclooxigenasas , COX-1 y COX-2 . La aspirina inhibe irreversiblemente la COX-1 y modifica la actividad enzimática de la COX-2. La COX-2 normalmente produce prostanoides , la mayoría de los cuales son proinflamatorios. La COX-2 modificada por aspirina (también conocida como prostaglandina-endoperóxido sintasa 2 o PTGS2) produce lipoxinas, la mayoría de las cuales son antiinflamatorias. [40] [ verificación necesaria ] Se han desarrollado fármacos AINE más nuevos, inhibidores de la COX-2 (coxibs), para inhibir solo la COX-2, con la intención de reducir la incidencia de efectos secundarios gastrointestinales. [14]
Varios inhibidores de la COX-2, como el rofecoxib (Vioxx), han sido retirados del mercado, después de que surgiera evidencia de que los inhibidores de la COX-2 aumentan el riesgo de ataque cardíaco y accidente cerebrovascular. [41] [42] Se propone que las células endoteliales que recubren la microvasculatura en el cuerpo expresen COX-2 y, al inhibir selectivamente la COX-2, la producción de prostaglandinas (específicamente, PGI 2 ; prostaciclina) se regula a la baja con respecto a los niveles de tromboxano, ya que la COX-1 en las plaquetas no se ve afectada. Por lo tanto, se elimina el efecto anticoagulante protector de la PGI 2 , lo que aumenta el riesgo de trombo y ataques cardíacos asociados y otros problemas circulatorios. Dado que las plaquetas no tienen ADN, no pueden sintetizar nueva COX una vez que la aspirina ha inhibido irreversiblemente la enzima, una diferencia importante en comparación con los inhibidores reversibles.
Además, la aspirina, al tiempo que inhibe la capacidad de la COX-2 para formar productos proinflamatorios como las prostaglandinas , convierte la actividad de esta enzima de una ciclooxigenasa formadora de prostaglandinas a una enzima similar a la lipoxigenasa : la COX-2 tratada con aspirina metaboliza una variedad de ácidos grasos poliinsaturados a productos hidroperoxi que luego se metabolizan a mediadores prorresolutivos especializados como las lipoxinas activadas por aspirina , las resolvinas activadas por aspirina y las maresinas activadas por aspirina . Estos mediadores poseen una potente actividad antiinflamatoria. Se propone que esta transición de la COX-2 activada por aspirina de la actividad de ciclooxigenasa a lipoxigenasa y la consiguiente formación de mediadores prorresolutivos especializados contribuye a los efectos antiinflamatorios de la aspirina. [43] [44] [45]
Se ha demostrado que la aspirina tiene al menos tres modos de acción adicionales. Desacopla la fosforilación oxidativa en las mitocondrias cartilaginosas (y hepáticas), al difundirse desde el espacio de la membrana interna como transportador de protones de regreso a la matriz mitocondrial, donde se ioniza una vez más para liberar protones. [46] La aspirina amortigua y transporta los protones. Cuando se administran dosis altas, en realidad puede causar fiebre, debido al calor liberado de la cadena de transporte de electrones, a diferencia de la acción antipirética de la aspirina observada con dosis más bajas. Además, la aspirina induce la formación de radicales NO en el cuerpo, que se ha demostrado en ratones que tienen un mecanismo independiente de reducción de la inflamación. Esta adhesión leucocitaria reducida es un paso importante en la respuesta inmune a la infección; sin embargo, la evidencia es insuficiente para demostrar que la aspirina ayuda a combatir la infección. [47] Datos más recientes también sugieren que el ácido salicílico y sus derivados modulan la señalización a través de NF-κB . [48] NF-κB, un complejo de factores de transcripción , desempeña un papel central en muchos procesos biológicos, incluida la inflamación. [49] [50] [51]
La aspirina se descompone fácilmente en el cuerpo en ácido salicílico, que tiene efectos antiinflamatorios, antipiréticos y analgésicos. En 2012, se descubrió que el ácido salicílico activa la proteína quinasa activada por AMP , lo que se ha sugerido como una posible explicación de algunos de los efectos tanto del ácido salicílico como de la aspirina. [52] [53] La porción acetilada de la molécula de aspirina tiene sus propios objetivos. La acetilación de proteínas celulares es un fenómeno bien establecido en la regulación de la función proteica a nivel postraduccional. La aspirina es capaz de acetilar varios otros objetivos además de las isoenzimas COX. [54] [55] Estas reacciones de acetilación pueden explicar muchos efectos hasta ahora inexplicados de la aspirina. [56]
La aspirina se produce en muchas formulaciones, con algunas diferencias en sus efectos. En particular, la aspirina puede causar sangrado gastrointestinal, y se buscan formulaciones que brinden los beneficios de la aspirina y al mismo tiempo mitiguen el sangrado dañino. Las formulaciones pueden combinarse (por ejemplo, tamponadas + vitamina C).
El ácido acetilsalicílico es un ácido débil y muy poco de él se ioniza en el estómago después de la administración oral. El ácido acetilsalicílico se absorbe rápidamente a través de la membrana celular en las condiciones ácidas del estómago. El aumento del pH y la mayor superficie del intestino delgado hacen que la aspirina se absorba más lentamente allí, ya que está más ionizada. Debido a la formación de concreciones, la aspirina se absorbe mucho más lentamente durante la sobredosis y las concentraciones plasmáticas pueden seguir aumentando hasta 24 horas después de la ingestión. [58] [59] [60]
Entre el 50 y el 80 % del salicilato en la sangre se une a la albúmina sérica humana , mientras que el resto permanece en estado activo, ionizado; la unión a proteínas depende de la concentración. La saturación de los sitios de unión conduce a una mayor cantidad de salicilato libre y a un aumento de la toxicidad. El volumen de distribución es de 0,1 a 0,2 l/kg. La acidosis aumenta el volumen de distribución debido a la mejora de la penetración tisular de los salicilatos. [60]
Hasta el 80% de las dosis terapéuticas de ácido salicílico se metaboliza en el hígado . La conjugación con glicina forma ácido salicilúrico y con ácido glucurónico para formar dos ésteres de glucurónido diferentes. El conjugado con el grupo acetilo intacto se conoce como acil glucurónido ; el conjugado desacetilado es el glucurónido fenólico . Estas vías metabólicas tienen solo una capacidad limitada. Pequeñas cantidades de ácido salicílico también se hidroxilan a ácido gentísico . Con grandes dosis de salicilato, la cinética cambia de primer orden a orden cero, a medida que las vías metabólicas se saturan y la excreción renal se vuelve cada vez más importante. [60]
Los salicilatos se excretan principalmente por los riñones como ácido salicilúrico (75%), ácido salicílico libre (10%), fenol salicílico (10%) y glucurónidos de acilo (5%), ácido gentísico (< 1%) y ácido 2,3-dihidroxibenzoico . [61] Cuando se ingieren dosis pequeñas (menos de 250 mg en un adulto), todas las vías proceden por cinética de primer orden, con una vida media de eliminación de aproximadamente 2,0 h a 4,5 h. [62] [63] Cuando se ingieren dosis más altas de salicilato (más de 4 g), la vida media se vuelve mucho más larga (15 h a 30 h), [64] porque las vías de biotransformación relacionadas con la formación de ácido salicilúrico y glucurónido fenólico salicílico se saturan. [65] La excreción renal de ácido salicílico se vuelve cada vez más importante a medida que las vías metabólicas se saturan, porque es extremadamente sensible a los cambios en el pH urinario . Se produce un aumento de 10 a 20 veces en el aclaramiento renal cuando el pH de la orina aumenta de 5 a 8. El uso de la alcalinización urinaria explota este aspecto particular de la eliminación de salicilato. [66] Se encontró que el uso de aspirina a corto plazo en dosis terapéuticas podría precipitar una lesión renal aguda reversible cuando el paciente estaba enfermo de glomerulonefritis o cirrosis . [67] La aspirina para algunos pacientes con enfermedad renal crónica y algunos niños con insuficiencia cardíaca congestiva estaba contraindicada. [67]

Los medicamentos elaborados a partir de sauce y otras plantas ricas en salicilatos aparecen en tablillas de arcilla de la antigua Sumeria, así como en el Papiro de Ebers del antiguo Egipto. [13] : 8–13 [20] Hipócrates se refirió al uso del té salicílico para reducir la fiebre alrededor del 400 a. C., y las preparaciones de corteza de sauce formaban parte de la farmacopea de la medicina occidental en la antigüedad clásica y la Edad Media . [20] El extracto de corteza de sauce se hizo reconocido por sus efectos específicos sobre la fiebre, el dolor y la inflamación a mediados del siglo XVIII. [68] En el siglo XIX, los farmacéuticos estaban experimentando y prescribiendo una variedad de productos químicos relacionados con el ácido salicílico , el componente activo del extracto de sauce. [13] : 46–55

En 1853, el químico Charles Frédéric Gerhardt trató el salicilato de sodio con cloruro de acetilo para producir ácido acetilsalicílico por primera vez; [13] : 46–48 en la segunda mitad del siglo XIX, otros químicos académicos establecieron la estructura química del compuesto e idearon métodos de síntesis más eficientes. En 1897, los científicos de la empresa de medicamentos y tintes Bayer comenzaron a investigar el ácido acetilsalicílico como un reemplazo menos irritante para los medicamentos salicilatos comunes estándar, e identificaron una nueva forma de sintetizarlo. [13] : 69–75 En 1899, Bayer había bautizado este medicamento como Aspirina y lo vendía a nivel mundial. [19] : 27 La palabra Aspirina era la marca de Bayer, en lugar del nombre genérico del medicamento; sin embargo, los derechos de Bayer sobre la marca registrada se perdieron o se vendieron en muchos países. La popularidad de la aspirina creció durante la primera mitad del siglo XX, lo que dio lugar a una feroz competencia con la proliferación de marcas y productos de aspirina. [20]
La popularidad de la aspirina disminuyó después del desarrollo del paracetamol en 1956 y del ibuprofeno en 1962. En los años 1960 y 1970, John Vane y otros descubrieron el mecanismo básico de los efectos de la aspirina, [13] : 226–231 mientras que los ensayos clínicos y otros estudios de los años 1960 a los años 1980 establecieron la eficacia de la aspirina como un agente anticoagulante que reduce el riesgo de enfermedades de coagulación. [13] : 247–257 Los grandes estudios iniciales sobre el uso de aspirina en dosis bajas para prevenir ataques cardíacos que se publicaron en los años 1970 y 1980 ayudaron a impulsar la reforma en la ética de la investigación clínica y las pautas para la investigación con sujetos humanos y la ley federal de los EE. UU., y a menudo se citan como ejemplos de ensayos clínicos que incluyeron solo hombres, pero de los cuales las personas sacaron conclusiones generales que no eran válidas para las mujeres. [69] [70] [71]
Las ventas de aspirina se recuperaron considerablemente en las últimas décadas del siglo XX y siguen siendo fuertes en el siglo XXI con un uso generalizado como tratamiento preventivo para ataques cardíacos y accidentes cerebrovasculares . [13] : 267–269
Bayer perdió su marca registrada para Aspirina en los Estados Unidos y algunos otros países en acciones tomadas entre 1918 y 1921 porque no había usado el nombre para su propio producto correctamente y había permitido durante años el uso de "Aspirina" por otros fabricantes sin defender los derechos de propiedad intelectual. [72] Hoy, la aspirina es una marca registrada genérica en muchos países. [73] [74] Aspirina, con "A" mayúscula, sigue siendo una marca registrada de Bayer en Alemania, Canadá, México y en más de 80 países más, para el ácido acetilsalicílico en todos los mercados, pero utilizando diferentes empaques y aspectos físicos para cada uno. [75] [76]
La aspirina se utiliza en el tratamiento de una serie de afecciones, entre ellas fiebre, dolor, fiebre reumática y afecciones inflamatorias, como artritis reumatoide , pericarditis y enfermedad de Kawasaki . [10] También se ha demostrado que dosis más bajas de aspirina reducen el riesgo de muerte por ataque cardíaco o el riesgo de accidente cerebrovascular en personas con alto riesgo o que tienen enfermedad cardiovascular, pero no en personas mayores que por lo demás están sanas. [79] [80] [81] [82] [83] Hay evidencia de que la aspirina es eficaz para prevenir el cáncer colorrectal , aunque los mecanismos de este efecto no están claros. [84]
La aspirina es un analgésico eficaz para el dolor agudo, aunque generalmente se considera inferior al ibuprofeno porque la aspirina tiene más probabilidades de causar sangrado gastrointestinal . [85] La aspirina generalmente es ineficaz para aquellos dolores causados por calambres musculares , hinchazón , distensión gástrica o irritación aguda de la piel. [86] Al igual que con otros AINE, las combinaciones de aspirina y cafeína proporcionan un alivio del dolor ligeramente mayor que la aspirina sola. [87] Las formulaciones efervescentes de aspirina alivian el dolor más rápido que la aspirina en tabletas, [88] lo que las hace útiles para el tratamiento de las migrañas . [89] La aspirina tópica puede ser eficaz para tratar algunos tipos de dolor neuropático . [90]
La aspirina, ya sea sola o en una formulación combinada, trata eficazmente ciertos tipos de dolor de cabeza , pero su eficacia puede ser cuestionable para otros. Los dolores de cabeza secundarios, es decir, los causados por otro trastorno o trauma, deben ser tratados rápidamente por un proveedor médico. Entre los dolores de cabeza primarios, la Clasificación Internacional de Trastornos de Cefalea distingue entre dolor de cabeza tensional (el más común), migraña y dolor de cabeza en racimos . La aspirina u otros analgésicos de venta libre son ampliamente reconocidos como efectivos para el tratamiento de los dolores de cabeza tensionales. [91] La aspirina, especialmente como un componente de una combinación de aspirina/paracetamol/cafeína , se considera una terapia de primera línea en el tratamiento de la migraña, y comparable a dosis más bajas de sumatriptán . Es más eficaz para detener las migrañas cuando comienzan. [92]
Al igual que su capacidad para controlar el dolor, la capacidad de la aspirina para controlar la fiebre se debe a su acción sobre el sistema de prostaglandinas a través de su inhibición irreversible de la COX . [93] Aunque el uso de la aspirina como antipirético en adultos está bien establecido, muchas sociedades médicas y agencias reguladoras, incluidas la Academia Estadounidense de Médicos de Familia , la Academia Estadounidense de Pediatría y la Administración de Alimentos y Medicamentos , desaconsejan enfáticamente el uso de aspirina para el tratamiento de la fiebre en niños debido al riesgo de síndrome de Reye , una enfermedad rara pero a menudo fatal asociada con el uso de aspirina u otros salicilatos en niños durante episodios de infección viral o bacteriana. [94] [95] [96] Debido al riesgo de síndrome de Reye en niños, en 1986, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) requirió el etiquetado de todos los medicamentos que contienen aspirina desaconsejando su uso en niños y adolescentes. [97]
La aspirina se utiliza como agente antiinflamatorio tanto para la inflamación aguda como para la inflamación a largo plazo , [98] así como para el tratamiento de enfermedades inflamatorias, como la artritis reumatoide . [10]
La aspirina es una parte importante del tratamiento de quienes han tenido un ataque cardíaco . [99] Por lo general, no se recomienda su uso rutinario en personas sin otros problemas de salud, incluidas aquellas mayores de 70 años. [100]
El estudio Antithrombotic Trialists' Collaboration de 2009 publicado en Lancet evaluó la eficacia y seguridad de la aspirina en dosis bajas en la prevención secundaria. En aquellos con accidente cerebrovascular isquémico previo o infarto agudo de miocardio, la aspirina en dosis bajas diaria se asoció con una reducción del riesgo relativo del 19% de eventos cardiovasculares graves (infarto de miocardio no fatal, accidente cerebrovascular no fatal o muerte vascular). Esto se produjo a expensas de un aumento del riesgo absoluto del 0,19% en el sangrado gastrointestinal; sin embargo, los beneficios superan el riesgo de peligro en este caso. [ cita requerida ] Los datos de ensayos previos han sugerido que la dosificación basada en el peso de la aspirina tiene mayores beneficios en la prevención primaria de los resultados cardiovasculares. [101] Sin embargo, ensayos más recientes no pudieron replicar resultados similares utilizando aspirina en dosis bajas en bajo peso corporal (<70 kg) en un subconjunto específico de la población estudiada, es decir, población de edad avanzada y diabética, y se requiere más evidencia para estudiar el efecto de la aspirina en dosis altas en peso corporal alto (≥70 kg). [102] [103] [104]
Después de intervenciones coronarias percutáneas (ICP), como la colocación de un stent en la arteria coronaria , una guía de la Agencia para la Investigación y la Calidad de la Atención Médica de EE. UU. recomienda que se tome aspirina de forma indefinida. [105] Con frecuencia, la aspirina se combina con un inhibidor del receptor de ADP , como clopidogrel , prasugrel o ticagrelor para prevenir los coágulos de sangre . Esto se llama terapia antiplaquetaria dual (TAPD). La duración de la TAPD se recomendó en las guías de los Estados Unidos y la Unión Europea después de los estudios CURE [106] y PRODIGY [107] . En 2020, la revisión sistemática y el metanálisis en red de Khan et al. [108] mostraron beneficios prometedores de la TAPD a corto plazo (<6 meses) seguida de inhibidores de P2Y12 en pacientes seleccionados, así como los beneficios de la TAPD a largo plazo (>12 meses) en pacientes de alto riesgo. En conclusión, la duración óptima de la terapia antiplaquetaria doble después de una intervención coronaria percutánea debe personalizarse después de sopesar los riesgos de eventos isquémicos y de eventos hemorrágicos de cada paciente, teniendo en cuenta múltiples factores relacionados con el paciente y con el procedimiento. Además, la aspirina debe continuarse indefinidamente después de completar la terapia antiplaquetaria doble. [109] [110] [111]
El estado del uso de aspirina para la prevención primaria en la enfermedad cardiovascular es conflictivo e inconsistente, con cambios recientes desde que se la recomendaba ampliamente hace décadas, y algunos ensayos más nuevos a los que se hace referencia en las pautas clínicas muestran menos beneficios de agregar aspirina junto con otras terapias antihipertensivas y reductoras del colesterol. [100] [112] El estudio ASCEND demostró que en diabéticos con alto riesgo de sangrado sin enfermedad cardiovascular previa, no hay un beneficio clínico general (disminución del 12% en el riesgo de eventos isquémicos frente al aumento del 29% en el sangrado gastrointestinal) de la aspirina en dosis bajas para prevenir los eventos vasculares graves durante un período de 7,4 años. De manera similar, los resultados del estudio ARRIVE tampoco mostraron ningún beneficio de la misma dosis de aspirina para reducir el tiempo hasta el primer resultado cardiovascular en pacientes con riesgo moderado de enfermedad cardiovascular durante un período de cinco años. También se ha sugerido la aspirina como un componente de una polipíldora para la prevención de la enfermedad cardiovascular. [113] [114] Lo que complica el uso de aspirina para la prevención es el fenómeno de la resistencia a la aspirina. [115] [116] En las personas resistentes, la eficacia de la aspirina se reduce. [117] Algunos autores han sugerido regímenes de pruebas para identificar a las personas resistentes a la aspirina. [118]
A partir de abril de 2022 [update], el Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF) determinó que había un "pequeño beneficio neto" para los pacientes de 40 a 59 años con un riesgo de enfermedad cardiovascular (ECV) a 10 años del 10 % o más, y "ningún beneficio neto" para los pacientes mayores de 60 años. [119] [120] [121] La determinación del beneficio neto se basó en equilibrar la reducción del riesgo de tomar aspirina para ataques cardíacos y accidentes cerebrovasculares isquémicos, con el aumento del riesgo de hemorragia gastrointestinal , hemorragia intracraneal y accidentes cerebrovasculares hemorrágicos . Sus recomendaciones establecen que la edad cambia el riesgo del medicamento, y que la magnitud del beneficio de la aspirina proviene de comenzar a una edad más temprana, mientras que el riesgo de sangrado, aunque pequeño, aumenta con la edad, en particular para los adultos mayores de 60 años, y puede verse agravado por otros factores de riesgo como la diabetes y antecedentes de sangrado gastrointestinal. Como resultado, el USPSTF sugiere que "las personas de 40 a 59 años que tienen un mayor riesgo de ECV deben decidir con su médico si comienzan a tomar aspirina; las personas de 60 años o más no deben comenzar a tomar aspirina para prevenir un primer ataque cardíaco o accidente cerebrovascular". Las pautas de prevención primaria de septiembre de 2019 [update]realizadas por el Colegio Estadounidense de Cardiología y la Asociación Estadounidense del Corazón establecen que podrían considerar la aspirina para pacientes de 40 a 69 años con un mayor riesgo de ECV aterosclerótica, sin un mayor riesgo de sangrado, al tiempo que afirman que no recomendarían aspirina para pacientes mayores de 70 años o adultos de cualquier edad con un mayor riesgo de sangrado. [100] Afirman que se debe realizar una estimación del riesgo de ECV y una discusión del riesgo antes de comenzar a tomar aspirina, al tiempo que afirman que la aspirina debe usarse "con poca frecuencia en la prevención primaria de rutina de (ECV aterosclerótica) debido a la falta de beneficio neto". A partir de agosto de 2021 [update], la Sociedad Europea de Cardiología hizo recomendaciones similares; Considerando la aspirina específicamente para pacientes menores de 70 años con riesgo alto o muy alto de ECV, sin contraindicaciones claras, caso por caso considerando tanto el riesgo isquémico como el riesgo de sangrado. [112]
La aspirina puede reducir el riesgo general de contraer cáncer y de morir por cáncer. [122] Hay evidencia sustancial de que reduce el riesgo de cáncer colorrectal (CCR), [84] [123] [124] [125] pero la aspirina debe tomarse durante al menos 10 a 20 años para ver este beneficio. [126] También puede reducir levemente el riesgo de cáncer de endometrio [127] y cáncer de próstata . [128]
Algunos concluyen que los beneficios son mayores que los riesgos debido al sangrado en aquellos con riesgo promedio. [122] Otros no tienen claro si los beneficios son mayores que el riesgo. [129] [130] Dada esta incertidumbre, las directrices de 2007 del Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF) sobre este tema recomendaron no usar aspirina para la prevención del CCR en personas con riesgo promedio. [131] Sin embargo, nueve años después, el USPSTF emitió una recomendación de grado B para el uso de aspirina en dosis bajas (75 a 100 mg/día) "para la prevención primaria de la ECV [enfermedad cardiovascular] y el CCR en adultos de 50 a 59 años de edad que tienen un riesgo de ECV de 10% o más a 10 años, no tienen mayor riesgo de sangrado, tienen una expectativa de vida de al menos 10 años y están dispuestos a tomar aspirina en dosis bajas diariamente durante al menos 10 años". [132]
Un metanálisis realizado en 2019 indicó que había una asociación entre tomar aspirina y un menor riesgo de cáncer de colon y recto, esófago y estómago. [133]
En 2021, el Grupo de Trabajo de Servicios Preventivos de Estados Unidos planteó preguntas sobre el uso de aspirina en la prevención del cáncer. Señala los resultados del ensayo ASPREE (Aspirin in Reducing Events in the Elderly) de 2018, en el que el riesgo de muerte relacionada con el cáncer fue mayor en el grupo tratado con aspirina que en el grupo placebo. [134]
La aspirina, junto con varios otros agentes con propiedades antiinflamatorias, se ha reutilizado como tratamiento complementario para episodios depresivos en sujetos con trastorno bipolar a la luz del posible papel de la inflamación en la patogénesis de trastornos mentales graves. [135] Una revisión sistemática de 2022 concluyó que la exposición a la aspirina redujo el riesgo de depresión en una cohorte agrupada de tres estudios (HR 0,624, IC del 95 %: 0,0503, 1,198, P = 0,033). Sin embargo, se necesitan más ensayos controlados aleatorios (ECA) de alta calidad y mayor duración para determinar si la aspirina es un tratamiento complementario eficaz para la depresión bipolar. [136] [137] [138] Por lo tanto, a pesar de la lógica biológica, las perspectivas clínicas de la aspirina y los agentes antiinflamatorios en el tratamiento de la depresión bipolar siguen siendo inciertas. [135]
Aunque los estudios de cohorte y longitudinales han demostrado que la aspirina en dosis bajas tiene una mayor probabilidad de reducir la incidencia de demencia, numerosos ensayos controlados aleatorios no han validado esto. [139] [140]
Algunos investigadores han especulado que los efectos antiinflamatorios de la aspirina pueden ser beneficiosos para la esquizofrenia. Se han realizado pequeños ensayos, pero aún faltan pruebas. [141] [142]
La aspirina es un tratamiento de primera línea para los síntomas de fiebre y dolor articular de la fiebre reumática aguda . El tratamiento suele durar una o dos semanas y rara vez se indica por períodos más prolongados. Una vez que la fiebre y el dolor han remitido, la aspirina ya no es necesaria, ya que no disminuye la incidencia de complicaciones cardíacas y cardiopatía reumática residual. [143] [144] Se ha demostrado que el naproxeno es tan eficaz como la aspirina y menos tóxico, pero debido a la limitada experiencia clínica, el naproxeno se recomienda solo como tratamiento de segunda línea. [143] [145]
Junto con la fiebre reumática, la enfermedad de Kawasaki sigue siendo una de las pocas indicaciones para el uso de aspirina en niños [146] a pesar de la falta de evidencia de alta calidad sobre su eficacia. [147]
La suplementación con aspirina en dosis bajas tiene beneficios moderados cuando se utiliza para la prevención de la preeclampsia . [148] [149] Este beneficio es mayor cuando se inicia al comienzo del embarazo. [150]
La aspirina también ha demostrado efectos antitumorales , a través de la inhibición del gen PTTG1 , que a menudo se sobreexpresa en los tumores. [151]
En algunas personas, la aspirina no tiene un efecto tan fuerte sobre las plaquetas como en otras, un efecto conocido como resistencia o insensibilidad a la aspirina. Un estudio ha sugerido que las mujeres tienen más probabilidades de ser resistentes que los hombres, [152] y un estudio agregado diferente de 2.930 personas encontró que el 28% eran resistentes. [153] Un estudio en 100 personas italianas encontró que, del aparente 31% de sujetos resistentes a la aspirina, solo el 5% eran verdaderamente resistentes, y los demás no cumplían con el tratamiento . [154] Otro estudio de 400 voluntarios sanos no encontró sujetos que fueran verdaderamente resistentes, pero algunos tenían "pseudoresistencia, lo que refleja una absorción retardada y reducida del fármaco". [155]
Los metaanálisis y las revisiones sistemáticas han concluido que la resistencia a la aspirina confirmada en laboratorio confiere mayores tasas de peores resultados en enfermedades cardiovasculares y neurovasculares. [156] [153] [157] [158] [159] [160] Aunque la mayoría de las investigaciones realizadas han girado en torno a enfermedades cardiovasculares y neurovasculares, hay investigaciones emergentes sobre el riesgo de resistencia a la aspirina después de la cirugía ortopédica donde se utiliza aspirina para la profilaxis de la tromboembolia venosa. [161] La resistencia a la aspirina en la cirugía ortopédica, específicamente después de artroplastias totales de cadera y rodilla, es de interés ya que los factores de riesgo para la resistencia a la aspirina también son factores de riesgo para las tromboembolias venosas y la osteoartritis; las secuelas de requerir una artroplastia total de cadera o rodilla. Algunos de estos factores de riesgo incluyen la obesidad, la edad avanzada, la diabetes mellitus, la dislipidemia y las enfermedades inflamatorias. [161]
Los comprimidos de aspirina para adultos se producen en tamaños estandarizados, que varían ligeramente de un país a otro, por ejemplo, 300 mg en Gran Bretaña y 325 mg en los Estados Unidos. Las dosis más pequeñas se basan en estos estándares, por ejemplo , comprimidos de 75 mg y 81 mg. Los comprimidos de 81 mg se denominan comúnmente "aspirina infantil" o "aspirina para bebés", porque originalmente, pero ya no , estaban destinados a ser administrados a bebés y niños. [162] No se produce ninguna importancia médica debido a la ligera diferencia en la dosis entre los comprimidos de 75 mg y los de 81 mg. La dosis necesaria para obtener un beneficio parece depender del peso de la persona. [101] Para aquellos que pesan menos de 70 kilogramos (154 libras), una dosis baja es eficaz para prevenir la enfermedad cardiovascular; para los pacientes por encima de este peso, se requieren dosis más altas. [101]
En general, para los adultos, las dosis se toman cuatro veces al día para la fiebre o la artritis, [163] con dosis cercanas a la dosis diaria máxima utilizada históricamente para el tratamiento de la fiebre reumática . [164] Para la prevención del infarto de miocardio (IM) en alguien con enfermedad de la arteria coronaria documentada o sospechada , se toman dosis mucho más bajas una vez al día. [163]
Las recomendaciones de marzo de 2009 del USPSTF sobre el uso de aspirina para la prevención primaria de la enfermedad cardíaca coronaria alientan a los hombres de 45 a 79 años y a las mujeres de 55 a 79 años a usar aspirina cuando el beneficio potencial de una reducción en el infarto de miocardio para los hombres o el accidente cerebrovascular para las mujeres supera el daño potencial de un aumento en la hemorragia gastrointestinal . [165] [166] [ necesita actualización ] El estudio WHI de mujeres posmenopáusicas encontró que la aspirina resultó en un riesgo 25% menor de muerte por enfermedad cardiovascular y un riesgo 14% menor de muerte por cualquier causa, aunque no hubo una diferencia significativa entre las dosis de aspirina de 81 mg y 325 mg. [167] El estudio ADAPTABLE de 2021 tampoco mostró una diferencia significativa en eventos cardiovasculares o sangrado mayor entre dosis de aspirina de 81 mg y 325 mg en pacientes (tanto hombres como mujeres) con enfermedad cardiovascular establecida. [168]
El uso de aspirina en dosis bajas también se asoció con una tendencia hacia un menor riesgo de eventos cardiovasculares, y dosis más bajas de aspirina (75 u 81 mg/día) pueden optimizar la eficacia y la seguridad para las personas que requieren aspirina para la prevención a largo plazo. [166]
En los niños con enfermedad de Kawasaki, se toma aspirina en dosis basadas en el peso corporal, inicialmente cuatro veces al día durante hasta dos semanas y luego en una dosis más baja una vez al día durante otras seis a ocho semanas. [169]
En octubre de 2020, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) exigió que se actualizara la etiqueta del medicamento para todos los medicamentos antiinflamatorios no esteroides para describir el riesgo de problemas renales en los fetos que resultan en un bajo nivel de líquido amniótico. [170] [171] Recomiendan evitar los AINE en mujeres embarazadas a las 20 semanas o más tarde en el embarazo. [170] [171] Una excepción a la recomendación es el uso de aspirina en dosis bajas de 81 mg en cualquier momento del embarazo bajo la dirección de un profesional de la salud. [171]
La aspirina no debe ser tomada por personas alérgicas al ibuprofeno o naproxeno , [172] [173] o que tienen intolerancia a los salicilatos [174] [175] o una intolerancia a medicamentos más generalizada a los AINE, y se debe tener precaución en aquellos con asma o broncoespasmo precipitado por AINE . Debido a su efecto sobre el revestimiento del estómago, los fabricantes recomiendan que las personas con úlceras pépticas , diabetes leve o gastritis consulten al médico antes de usar aspirina. [172] [176] Incluso si ninguna de estas condiciones está presente, el riesgo de sangrado estomacal aún aumenta cuando la aspirina se toma con alcohol o warfarina . [172] [173] Las personas con hemofilia u otras tendencias hemorrágicas no deben tomar aspirina u otros salicilatos. [172] [176] Se sabe que la aspirina causa anemia hemolítica en personas que tienen la enfermedad genética deficiencia de glucosa-6-fosfato deshidrogenasa , particularmente en grandes dosis y dependiendo de la gravedad de la enfermedad. [177] No se recomienda el uso de aspirina durante la fiebre del dengue debido a una mayor tendencia al sangrado. [178] La aspirina tomada en dosis de ≤325 mg y ≤100 mg por día durante ≥2 días puede aumentar las probabilidades de sufrir un ataque de gota en un 81% y 91% respectivamente. Este efecto puede empeorar potencialmente con dietas ricas en purinas, diuréticos y enfermedad renal, pero se elimina con el fármaco reductor de uratos alopurinol. [179] La aspirina diaria en dosis bajas no parece empeorar la función renal. [180] La aspirina puede reducir el riesgo cardiovascular en aquellos sin enfermedad cardiovascular establecida en personas con ERC moderada, sin aumentar significativamente el riesgo de sangrado. [181] No se debe administrar aspirina a niños o adolescentes menores de 16 años para controlar los síntomas del resfriado o la gripe, ya que esto se ha relacionado con el síndrome de Reye . [182]
La aspirina aumenta el riesgo de sangrado gastrointestinal superior . [183] El recubrimiento entérico en la aspirina se puede utilizar en la fabricación para prevenir la liberación de aspirina en el estómago para reducir el daño gástrico, pero el recubrimiento entérico no reduce el riesgo de sangrado gastrointestinal. [183] [184] La aspirina con recubrimiento entérico puede no ser tan eficaz para reducir el riesgo de coágulos sanguíneos. [185] [186] Se ha demostrado que la combinación de aspirina con otros AINE aumenta aún más el riesgo de sangrado gastrointestinal. [183] El uso de aspirina en combinación con clopidogrel o warfarina también aumenta el riesgo de sangrado gastrointestinal superior. [187]
El bloqueo de la COX-1 por la aspirina aparentemente da como resultado la regulación positiva de la COX-2 como parte de una defensa gástrica. [188] No hay evidencia clara de que el uso simultáneo de un inhibidor de la COX-2 con aspirina pueda aumentar el riesgo de lesión gastrointestinal. [189]
El " buffering " es un método adicional utilizado con la intención de mitigar el sangrado gastrointestinal, por ejemplo, evitando que la aspirina se concentre en las paredes del estómago, aunque los beneficios de la aspirina tamponada son discutidos. [190] Se puede utilizar casi cualquier agente tampón utilizado en antiácidos; Bufferin, por ejemplo, utiliza óxido de magnesio . Otras preparaciones utilizan carbonato de calcio . [191] Los agentes formadores de gas en formulaciones de comprimidos y polvos efervescentes también pueden funcionar como agentes tampón, un ejemplo es el bicarbonato de sodio , utilizado en Alka-Seltzer . [192]
Se ha investigado la posibilidad de tomar vitamina C junto con aspirina como método para proteger el revestimiento del estómago. En los ensayos, se descubrió que la aspirina que libera vitamina C (ASA-VitC) o una formulación de aspirina tamponada que contiene vitamina C causa menos daño estomacal que la aspirina sola. [193] [194]
Es una costumbre muy extendida entre los oftalmólogos recetar aspirina como medicación complementaria a los pacientes con oclusión de la vena retiniana (OVR), como la oclusión de la vena central de la retina (OVCR) y la oclusión de las ramas venosas de la retina (OVR). La razón de este uso tan extendido es la evidencia de su eficacia demostrada en los principales trastornos trombóticos venosos sistémicos , y se ha asumido que puede ser igualmente beneficiosa en varios tipos de oclusión de la vena retiniana.
Sin embargo, una investigación a gran escala basada en datos de casi 700 pacientes mostró "que la aspirina u otros agentes antiagregantes plaquetarios o anticoagulantes influyen negativamente en el resultado visual en pacientes con OVCR y hemi-OVCR, sin ninguna evidencia de efecto protector o beneficioso". [195] Varios grupos de expertos, incluido el Royal College of Ophthalmologists , recomendaron no utilizar fármacos antitrombóticos (incluida la aspirina) en pacientes con OVR. [196]
Grandes dosis de salicilato , un metabolito de la aspirina, causan tinnitus temporal (zumbido en los oídos) según experimentos en ratas, a través de la acción en cascada sobre el ácido araquidónico y los receptores NMDA . [197]
El síndrome de Reye, una enfermedad rara pero grave caracterizada por encefalopatía aguda e hígado graso , puede ocurrir cuando a los niños o adolescentes se les da aspirina para la fiebre u otra enfermedad o infección. De 1981 a 1997, se informaron 1207 casos de síndrome de Reye en personas menores de 18 años a los Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. De estos, el 93% informó haber estado enfermo en las tres semanas anteriores al inicio del síndrome de Reye, más comúnmente con una infección respiratoria , varicela o diarrea . Los salicilatos fueron detectables en el 81,9% de los niños para quienes se informaron los resultados de las pruebas. [198] Después de que se informó la asociación entre el síndrome de Reye y la aspirina, y se implementaron medidas de seguridad para prevenirlo (incluida una advertencia del Cirujano General y cambios en el etiquetado de los medicamentos que contienen aspirina), la aspirina tomada por niños disminuyó considerablemente en los Estados Unidos, al igual que el número de casos informados de síndrome de Reye; Se encontró una disminución similar en el Reino Unido después de que se emitieran advertencias contra el uso de aspirina pediátrica. [198] La Administración de Alimentos y Medicamentos de los EE. UU. recomienda que no se administre aspirina (o productos que contengan aspirina) a ninguna persona menor de 12 años que tenga fiebre, [182] y el Servicio Nacional de Salud del Reino Unido recomienda que los niños menores de 16 años no tomen aspirina, a menos que sea por consejo de un médico. [199]
Para una pequeña cantidad de personas, tomar aspirina puede provocar síntomas que incluyen urticaria , hinchazón y dolor de cabeza. [200] La aspirina puede exacerbar los síntomas entre quienes padecen urticaria crónica o crear síntomas agudos de urticaria. [201] Estas respuestas pueden deberse a reacciones alérgicas a la aspirina o, más a menudo, a su efecto inhibidor de la enzima COX-1. [201] [202] Las reacciones cutáneas también pueden estar relacionadas con contraindicaciones sistémicas, como las observadas en el broncoespasmo precipitado por AINE , [201] [202] o en aquellos con atopia . [203]
La aspirina y otros AINE, como el ibuprofeno, pueden retrasar la cicatrización de las heridas de la piel. [204] Hallazgos anteriores de dos ensayos pequeños y de baja calidad sugirieron un beneficio con la aspirina (junto con la terapia de compresión) en el tiempo de cicatrización de las úlceras venosas de las piernas y el tamaño de las úlceras de las piernas, [205] [206] [207] sin embargo, estudios más grandes, más recientes y de mayor calidad no han podido corroborar estos resultados. [208] [209] Como tal, se requieren más investigaciones para aclarar el papel de la aspirina en este contexto.
La aspirina puede provocar hinchazón de los tejidos de la piel en algunas personas. En un estudio, en algunas personas, el angioedema apareció entre una y seis horas después de ingerir aspirina. Sin embargo, cuando la aspirina se tomó sola, no provocó angioedema en estas personas; la aspirina se había tomado en combinación con otro fármaco inducido por AINE cuando apareció el angioedema. [210]
La aspirina aumenta el riesgo de microhemorragias cerebrales, que aparecen en las exploraciones por resonancia magnética como parches hipointensos (agujeros oscuros) de 5 a 10 mm o menos. [211] [212]
Un estudio de un grupo con una dosis media de aspirina de 270 mg por día estimó un aumento absoluto promedio del riesgo de hemorragia intracerebral (HIC) de 12 eventos por cada 10.000 personas. [213] En comparación, la reducción absoluta estimada del riesgo de infarto de miocardio fue de 137 eventos por cada 10.000 personas, y una reducción de 39 eventos por cada 10.000 personas en accidente cerebrovascular isquémico. [213] En los casos en los que ya se ha producido una HIC, el uso de aspirina produce una mayor mortalidad, con una dosis de aproximadamente 250 mg por día que resulta en un riesgo relativo de muerte dentro de los tres meses posteriores a la HIC de alrededor de 2,5 ( intervalo de confianza del 95%: 1,3 a 4,6). [214]
La aspirina y otros AINE pueden causar niveles anormalmente altos de potasio en sangre al inducir un estado de hipoaldosteronismo hiporreninémico mediante la inhibición de la síntesis de prostaglandinas; sin embargo, estos agentes no suelen causar hipercalemia por sí mismos en el contexto de una función renal normal y un estado euvolémico. [215]
El uso de aspirina en dosis bajas antes de un procedimiento quirúrgico se ha asociado con un mayor riesgo de eventos hemorrágicos en algunos pacientes; sin embargo, la suspensión de la aspirina antes de la cirugía también se ha asociado con un aumento de eventos cardíacos adversos importantes. Un análisis de múltiples estudios encontró un aumento de tres veces en eventos adversos como infarto de miocardio en pacientes que suspendieron la aspirina antes de la cirugía. El análisis encontró que el riesgo depende del tipo de cirugía que se realiza y la indicación del paciente para el uso de aspirina. [216]
El 9 de julio de 2015, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) endureció las advertencias sobre el aumento del riesgo de ataque cardíaco y accidente cerebrovascular asociado con los medicamentos antiinflamatorios no esteroides (AINE). [217] La aspirina es un AINE, pero no se ve afectada por las nuevas advertencias. [217]
La sobredosis de aspirina puede ser aguda o crónica. En la intoxicación aguda, se toma una sola dosis grande; en la intoxicación crónica, se toman dosis más altas de lo normal durante un período de tiempo. La sobredosis aguda tiene una tasa de mortalidad del 2%. La sobredosis crónica es más comúnmente letal, con una tasa de mortalidad del 25%; [218] la sobredosis crónica puede ser especialmente grave en niños. [219] La toxicidad se maneja con una serie de tratamientos potenciales, que incluyen carbón activado , dextrosa intravenosa y solución salina normal, bicarbonato de sodio y diálisis . [220] El diagnóstico de intoxicación generalmente implica la medición del salicilato plasmático, el metabolito activo de la aspirina, mediante métodos espectrofotométricos automatizados. Los niveles de salicilato plasmático en general varían de 30 a 100 mg/L después de las dosis terapéuticas habituales, 50-300 mg/L en personas que toman dosis altas y 700-1400 mg/L después de una sobredosis aguda. El salicilato también se produce como resultado de la exposición al subsalicilato de bismuto , al salicilato de metilo y al salicilato de sodio . [221] [222]
Se sabe que la aspirina interactúa con otros fármacos. Por ejemplo, se sabe que la acetazolamida y el cloruro de amonio mejoran el efecto intoxicante de los salicilatos, y el alcohol también aumenta el sangrado gastrointestinal asociado con estos tipos de fármacos. [172] [173] Se sabe que la aspirina desplaza una serie de fármacos de los sitios de unión a proteínas en la sangre, incluidos los fármacos antidiabéticos tolbutamida y clorpropamida , warfarina , metotrexato , fenitoína , probenecid , ácido valproico (además de interferir con la beta oxidación , una parte importante del metabolismo del valproato) y otros AINE. Los corticosteroides también pueden reducir la concentración de aspirina. Otros AINE, como el ibuprofeno y el naproxeno, pueden reducir el efecto antiplaquetario de la aspirina. [223] [224] Aunque la evidencia limitada sugiere que esto puede no resultar en un efecto cardioprotector reducido de la aspirina. [223] Las dosis analgésicas de aspirina disminuyen la pérdida de sodio inducida por la espironolactona en la orina, sin embargo esto no reduce los efectos antihipertensivos de la espironolactona. [225] Además, las dosis antiplaquetarias de aspirina se consideran demasiado pequeñas para producir una interacción con la espironolactona. [226] Se sabe que la aspirina compite con la penicilina G por la secreción tubular renal. [227] La aspirina también puede inhibir la absorción de vitamina C. [228] [229] [ ¿ Fuente médica poco confiable? ] [230]
El ensayo ISIS-2 demostró que la aspirina en dosis de 160 mg diarios durante un mes, redujo la mortalidad en un 21% de los participantes con sospecha de infarto de miocardio en las primeras cinco semanas. [231] Una dosis diaria única de 324 mg de aspirina durante 12 semanas tiene un efecto altamente protector contra el infarto agudo de miocardio y la muerte en hombres con angina inestable. [232]
La aspirina se ha reutilizado como tratamiento complementario para episodios depresivos en sujetos con trastorno bipolar . [135] Sin embargo, la evidencia metaanalítica se basa en muy pocos estudios y no sugiere ninguna eficacia de la aspirina en el tratamiento de la depresión bipolar. [135] Por lo tanto, a pesar de la lógica biológica, las perspectivas clínicas de la aspirina y los agentes antiinflamatorios en el tratamiento de la depresión bipolar siguen siendo inciertas. [135]
Varios estudios investigaron las propiedades antiinfecciosas de la aspirina en infecciones bacterianas, virales y parasitarias. Se demostró que la aspirina limita la activación plaquetaria inducida por Staphylococcus aureus y Enterococcus faecalis y reduce la adhesión de los estreptococos a las válvulas cardíacas. En pacientes con meningitis tuberculosa, la adición de aspirina redujo el riesgo de un nuevo infarto cerebral [RR = 0,52 (0,29-0,92)]. La creciente evidencia también respalda el papel de la aspirina en el biofilm bacteriano y fúngico. [233]
La evidencia de los estudios observacionales fue contradictoria sobre el efecto de la aspirina en la prevención del cáncer de mama, [234] un ensayo controlado aleatorio mostró que la aspirina no tuvo un efecto significativo en la reducción del cáncer de mama [235] por lo tanto, se necesitan más estudios para aclarar el efecto de la aspirina en la prevención del cáncer.
Hay muchos informes anecdóticos de que la aspirina puede mejorar el crecimiento y la resistencia de las plantas [236] [237], aunque la mayoría de las investigaciones involucraron ácido salicílico en lugar de aspirina. [238]
La aspirina se utiliza a veces en medicina veterinaria como anticoagulante o para aliviar el dolor asociado con la inflamación musculoesquelética o la osteoartritis . La aspirina debe administrarse a los animales solo bajo la supervisión directa de un veterinario , ya que los efectos adversos, incluidos los problemas gastrointestinales, son comunes. Una sobredosis de aspirina en cualquier especie puede provocar intoxicación por salicilato , caracterizada por hemorragias, convulsiones, coma e incluso la muerte. [239]
Los perros toleran mejor la aspirina que los gatos. [240] Los gatos metabolizan la aspirina lentamente porque carecen de los conjugados glucurónidos que ayudan a la excreción de la aspirina, lo que la hace potencialmente tóxica si la dosis no se espacia adecuadamente. [239] [241] No se produjeron signos clínicos de toxicosis cuando se administró a los gatos 25 mg/kg de aspirina cada 48 horas durante 4 semanas, [240] pero la dosis recomendada para aliviar el dolor y la fiebre y para tratar enfermedades de coagulación sanguínea en gatos es de 10 mg/kg cada 48 horas para permitir la metabolización. [239] [242]
...there was postprandial reduction on the plasma concentration of IL-6 and IkBα preservation, followed by the lower activation of NFκB, considered the main transcription factor capable of inducing inflammatory response by stimulating the expression of proinflammatory cytokines, chemokines, and adhesion molecules.
El presente metanálisis integral respalda y cuantifica aún más la asociación inversa entre el uso regular de aspirina y el riesgo de cáncer colorrectal y otros cánceres del tracto digestivo, incluidos algunos raros. El efecto favorable de la aspirina aumenta con una mayor duración del uso y, en el caso del cáncer colorrectal, con el aumento de la dosis.