El cáncer de vejiga es uno de los diversos tipos de cáncer que surgen de los tejidos de la vejiga urinaria . [1] Los síntomas incluyen sangre en la orina , dolor al orinar y dolor lumbar. [1] Se produce cuando las células epiteliales que recubren la vejiga se vuelven malignas. [4]
Los factores de riesgo para el cáncer de vejiga incluyen el tabaquismo , los antecedentes familiares, la radioterapia previa, las infecciones frecuentes de la vejiga y la exposición a ciertas sustancias químicas. [1] El tipo más común es el carcinoma de células transicionales . [1] Otros tipos incluyen el carcinoma de células escamosas y el adenocarcinoma . [1] El diagnóstico se realiza típicamente mediante cistoscopia con biopsias de tejido . [5] La estadificación del cáncer se determina mediante resección transuretral e imágenes médicas . [1] [6] [7]
El tratamiento depende del estadio del cáncer . [1] Puede incluir alguna combinación de cirugía, radioterapia, quimioterapia o inmunoterapia . [1] Las opciones quirúrgicas pueden incluir resección transuretral, extirpación parcial o completa de la vejiga o derivación urinaria . [1] Las tasas típicas de supervivencia a cinco años en los Estados Unidos son del 77 %, en Canadá del 75 % y en Europa del 68 %. [2] [8] [9]
El cáncer de vejiga, en 2018, afectó a alrededor de 1,6 millones de personas en todo el mundo, con 549 000 casos nuevos y 200 000 muertes. [3] La edad de aparición es más frecuente entre los 65 y los 84 años. [2] Los hombres se ven afectados con mayor frecuencia que las mujeres. [2] En 2018, la tasa más alta de cáncer de vejiga se produjo en el sur y el oeste de Europa, seguida de América del Norte, con tasas de 15, 13 y 12 casos por cada 100 000 personas. [3] Las tasas más altas de muertes por cáncer de vejiga se observaron en el norte de África y el oeste de Asia, seguidas del sur de Europa. [3]

El síntoma más común del cáncer de vejiga es la presencia de sangre visible en la orina (hematuria) a pesar de que la micción no produce dolor. Esto afecta a alrededor del 75% de las personas a las que finalmente se les diagnostica la enfermedad. [10] Algunas personas, en cambio, presentan "hematuria microscópica" (pequeñas cantidades de sangre en la orina que solo se pueden ver con un microscopio durante un análisis de orina ), dolor al orinar o ningún síntoma en absoluto (sus tumores se detectan durante un estudio de imágenes no relacionado ). [10] [11] Con menor frecuencia, un tumor puede bloquear el flujo de orina hacia la vejiga, lo que provoca dolor a lo largo del flanco del cuerpo (entre las costillas y las caderas). [12] La mayoría de las personas con sangre en la orina no tienen cáncer de vejiga; hasta el 22% de las personas con hematuria visible y el 5% con hematuria microscópica son diagnosticadas con la enfermedad. [10] Las mujeres con cáncer de vejiga y hematuria a menudo reciben un diagnóstico erróneo de infecciones del tracto urinario , lo que retrasa el diagnóstico y el tratamiento adecuados. [11]
Las personas con enfermedad avanzada pueden tener dolor pélvico o óseo, hinchazón de las extremidades inferiores o dolor en el flanco . [13]


Las personas con sospecha de cáncer de vejiga pueden someterse a varias pruebas para evaluar la presencia y extensión de cualquier tumor. Primero, muchos se someten a un examen físico que puede incluir un examen rectal digital y un examen pélvico , donde un médico palpa el área pélvica en busca de masas inusuales que podrían ser tumores. [14] Los tumores de vejiga graves a menudo arrojan células en la orina; estas pueden detectarse mediante citología de orina , donde se recogen células de una muestra de orina y se observan bajo un microscopio . [14] [15] La citología puede detectar alrededor de dos tercios de los tumores de alto grado , pero detecta solo 1 de cada 8 tumores de bajo grado. [16] Se pueden utilizar pruebas de orina adicionales para detectar moléculas asociadas con el cáncer de vejiga. Algunas detectan las proteínas antígeno tumoral de vejiga o NMP22 que tienden a estar elevadas en la orina de las personas con cáncer de vejiga; algunas detectan el ARNm de los genes asociados al tumor; algunas usan microscopía de fluorescencia para detectar células cancerosas con mayor sensibilidad que la citología regular. [16]
Muchos también se someten a una cistoscopia , en la que se introduce una cámara flexible por la uretra hasta la vejiga para inspeccionar visualmente si hay tejido canceroso. [14] La cistoscopia es más sensible a los tumores papilares (tumores con forma de dedo que crecen en la parte de la vejiga que contiene la orina); es menos sensible a los carcinomas in situ (CIS) pequeños y de baja localización. [17] La detección del CIS se mejora con la cistoscopia con luz azul , en la que se inyecta en la vejiga un tinte ( hexaminolevulinato ) que se acumula en las células cancerosas durante la cistoscopia. El tinte emite fluorescencia cuando el cistoscopio lo ilumina con luz azul, lo que permite una detección más sensible de tumores pequeños. [14] [17]
También se toman imágenes del tracto urinario superior ( uréteres y riñones ) para detectar tumores que podrían causar sangre en la orina. Esto se hace típicamente inyectando un tinte en la sangre que los riñones filtrarán hacia el tracto urinario y luego se toman imágenes mediante una tomografía computarizada . En cambio, a aquellos cuyos riñones no funcionan lo suficientemente bien como para filtrar el tinte se les puede realizar una exploración mediante una resonancia magnética . [12]
Los tumores sospechosos se extirpan introduciendo un dispositivo por la uretra en un proceso denominado "resección transuretral de tumor de vejiga" (RTUT). Se extirpan todos los tumores, así como una parte del músculo de la vejiga subyacente. Un patólogo examina el tejido extirpado para determinar si es canceroso. [14] [18]
_pT1.JPG/440px-Bladder_urothelial_carcinoma_(1)_pT1.JPG)
Los tumores de vejiga se clasifican por su apariencia bajo el microscopio y por su tipo de célula de origen. Más del 90% de los tumores de vejiga surgen de las células que forman el revestimiento interno de la vejiga, llamadas células uroteliales o células de transición; el tumor se clasifica entonces como cáncer urotelial o cáncer de células de transición . [19] [20] Alrededor del 5% de los casos son cáncer de células escamosas (de una célula más rara en el revestimiento de la vejiga), particularmente común en lugares con esquistosomiasis . [20] Hasta el 2% de los casos son adenocarcinoma (de células de glándulas productoras de moco ). [20] Los casos restantes son sarcomas (del músculo de la vejiga) o cáncer de células pequeñas (de células neuroendocrinas ), ambos relativamente raros. [20]
El patólogo también clasifica la muestra tumoral en función de la diferencia entre las células cancerosas y las células sanas. El cáncer de vejiga se divide en cáncer de bajo grado (más similar a las células sanas) o cáncer de alto grado (menos similar). El cáncer de alto grado se subdivide a su vez en "cáncer de vejiga no músculo-invasivo" (NMIBC, por sus siglas en inglés) o "cáncer de vejiga músculo-invasivo" (MIBC, por sus siglas en inglés), más agresivo, en función de si el tumor ha crecido hacia el músculo circundante de la vejiga. [19]
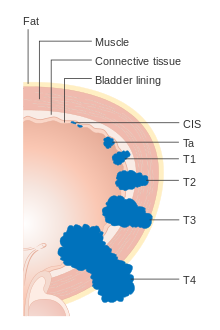




A cada caso de cáncer de vejiga se le asigna un estadio basado en el sistema TNM definido por el Comité Conjunto Estadounidense sobre Cáncer . [19] A un tumor se le asignan tres puntuaciones basadas en la extensión del tumor primario (T), su propagación a los ganglios linfáticos cercanos (N) y la metástasis a sitios distantes (M). [21] La puntuación T representa la extensión del tumor original: Ta o Tis para tumores que están confinados a la capa más interna de la vejiga; T1 para tumores que se extienden al tejido conectivo de la vejiga; T2 para la extensión al músculo; T3 para la extensión a través del músculo al tejido graso circundante; y T4 para la extensión completamente fuera de la vejiga. [21] La puntuación N representa la propagación a los ganglios linfáticos cercanos: N0 para ninguna propagación; N1 para propagación a un solo ganglio linfático cercano; N2 para propagación a varios ganglios linfáticos cercanos; N3 para propagación a ganglios linfáticos más distantes fuera de la pelvis. [21] La puntuación M designa la propagación a órganos más distantes: M0 para un tumor que no se ha propagado; M1 para uno que sí lo ha hecho. [21]
Las puntuaciones TNM se combinan para determinar el estadio del caso de cáncer en una escala de 0 a 4, donde un estadio más alto representa un cáncer más extenso con un peor pronóstico. [22]
Las personas con cáncer de vejiga no músculo invasivo (NMIBC) se estratifican según el riesgo en función de factores clínicos y patológicos para que sean tratadas adecuadamente según su probabilidad de progresión y/o recurrencia. [24] Las personas con tumores no músculo invasivos se clasifican en riesgo bajo, riesgo intermedio y riesgo alto o se les proporciona una puntuación numérica de riesgo. El marco de estratificación del riesgo lo proporciona la Asociación Estadounidense de Urología/Sociedad de Oncología Urológica (estratificación AUA/SUO), las directrices de la Asociación Europea de Urología (EAU), las tablas de riesgo de la Organización Europea para la Investigación y el Tratamiento del Cáncer (EORTC) y el modelo de puntuación del Club Urológico Español de Tratamiento Oncológico (CUETO). [25] [26] [27]

El tratamiento del cáncer de vejiga depende de la profundidad con la que el tumor invade la pared de la vejiga. El primer paso es la cirugía, la resección transuretral del tumor de vejiga (RTUT), que es tanto un procedimiento de diagnóstico como el paso inicial del tratamiento. [28]
Las estrategias de tratamiento para el cáncer de vejiga incluyen: [29] [30]
El NMIBC se trata principalmente mediante la extirpación quirúrgica de todos los tumores mediante TURBT en el mismo procedimiento utilizado para recolectar tejido de biopsia para el diagnóstico. [31] [32] Para aquellos con un riesgo relativamente bajo de recurrencia de tumores, una dosis única de quimioterapia ( mitomicina C , epirubicina o gemcitabina ) inyectada en la vejiga después de la TURBT reduce el riesgo de aparición de tumores alrededor del 12%. [31] En cambio, aquellos con mayor riesgo son tratados con inyecciones en la vejiga de la vacuna BCG (una vacuna bacteriana viva, generalmente utilizada para la tuberculosis ), administrada semanalmente durante seis semanas. Esto casi reduce a la mitad la tasa de recurrencia del tumor. [31] El riesgo de recurrencia se reduce aún más con una serie de inyecciones de BCG de "mantenimiento", administradas regularmente durante al menos un año. [31] [33] Aquellos cuyos tumores recurren pueden recibir una segunda ronda de inyecciones de BCG. [31] Los tumores que no responden a la BCG pueden tratarse con estimulantes inmunitarios alternativos nadofaragene firadenovec (comercializado como "Adstiladrin", una terapia génica que hace que las células de la vejiga produzcan una proteína inmunoestimulante ), nogapendekin alfa inbakicept ("Anktiva", una combinación de proteínas inmunoestimulantes) o pembrolizumab ("Keytruda", un inhibidor de puntos de control inmunitario ). [34]
Las personas cuyos tumores continúan creciendo a menudo son tratadas con cirugía para extirpar la vejiga y los órganos circundantes, llamada cistectomía radical . [35] Se extirpan la vejiga, varios ganglios linfáticos adyacentes , los uréteres inferiores y los órganos genitales cercanos (en los hombres, la próstata y las vesículas seminales ; en las mujeres, el útero y parte de la pared vaginal ). [35] Los cirujanos también construyen una nueva forma para que la orina salga del cuerpo. El método más común es mediante un conducto ileal , donde se extrae un trozo del íleon (parte del intestino delgado) y se utiliza para transportar la orina desde los uréteres hasta una nueva abertura quirúrgica ( estoma ) en el abdomen. La orina drena pasivamente en una bolsa de ostomía que se usa fuera del cuerpo, que el usuario puede vaciar regularmente. [36] Alternativamente, se puede realizar una derivación urinaria continente, donde los uréteres se unen a un trozo de íleon que incluye la válvula entre el intestino delgado y grueso; Esta válvula se cierra de forma natural, lo que permite retener la orina en el cuerpo en lugar de en una bolsa de ostomía. La persona afectada vacía el nuevo depósito de orina varias veces al día mediante autocateterismo, pasando un tubo estrecho a través del estoma. [37] [38] En cambio, algunas personas pueden tener el trozo de íleon conectado directamente a la uretra, lo que permite a la persona afectada orinar a través de la uretra como lo haría antes de la cirugía, aunque sin los nervios originales de la vejiga, ya no tendrá la necesidad de orinar cuando el depósito de orina esté lleno. [39]
Las personas que no están lo suficientemente bien o no están dispuestas a someterse a una cistectomía radical pueden beneficiarse de más inyecciones de quimioterapia en la vejiga (mitomicina C, gemcitabina, docetaxel o valrubicina ) o de una inyección intravenosa de pembrolizumab. [31] Alrededor de 1 de cada 5 personas con NMIBC eventualmente progresará a MIBC. [40]
Los efectos secundarios de la terapia con BCG incluyen cistitis , prostatitis , epididimoorquitis , balanitis , obstrucción ureteral , contracción de la vejiga, osteomielitis micobacteriana , artritis reactiva , neumonía micobacteriana, hepatitis granulomatosa , nefritis granulomatosa, nefritis intersticial , vasculitis infecciosa e infección diseminada. [41] [42]
La infección local (es decir, prostatitis , epididimoorquitis , balanitis ) debido a BCG debe tratarse con terapia triple tuberculosa, siendo uno de los medicamentos una fluoroquinolona durante 3 a 6 meses. En personas con infecciones sistémicas, se debe suspender la terapia con BCG y se debe iniciar un tratamiento antituberculoso con múltiples medicamentos durante al menos 6 meses. Los medicamentos que se pueden utilizar para este tratamiento son INH , rifampicina , etambutol , fluoroquinolonas , claritromicina , aminoglucósidos y doxiciclina . Las cepas de BCG no son sensibles a la pirazinamida , por lo tanto, no debe ser parte del tratamiento antituberculoso. [43]

La mayoría de las personas con cáncer de vejiga invasivo muscular son tratadas con cistectomía radical, que cura a aproximadamente la mitad de los afectados. [38] El tratamiento con quimioterapia antes de la cirugía (llamada " terapia neoadyuvante ") utilizando una combinación de medicamentos que contiene cisplatino (gemcitabina más cisplatino; o metotrexato , vinblastina, doxorrubicina y cisplatino) mejora la supervivencia entre un 5 y un 10 % más. [38] [45]
La cistectomía radical tiene una morbilidad significativa asociada. Alrededor del 50-65% de las personas experimentan complicaciones dentro de los 90 días posteriores a la cirugía. [46] [47] Las tasas de mortalidad fueron del 7% dentro de los 90 días posteriores a la cirugía. Los centros de alto volumen tienen mejores resultados que los centros de bajo volumen. [48] Algunos centros están implementando las recomendaciones de la sociedad Enhanced Recovery After Surgery (ERAS) para disminuir la morbilidad después de la cistectomía radical. Sin embargo, debido a la falta de evidencia específica en cirugía urológica, el protocolo ERAS no se ha incorporado ampliamente en la atención clínica urológica. [49]
Las personas con ciertos tipos de enfermedades de menor riesgo pueden recibir en cambio una terapia de conservación de la vejiga. Las personas con un solo tumor en la parte posterior de la vejiga pueden someterse a una cistectomía parcial , en la que se extirpan el tumor y la zona circundante y se repara la vejiga. [38] Las personas sin CIS ni obstrucción urinaria pueden someterse a una TURBT para extirpar los tumores visibles, seguida de quimioterapia y radiación; alrededor de dos tercios de estas personas se curan de forma permanente, mientras que aquellas cuyos tumores reaparecen se tratan con una cistectomía radical. [38]
La radioterapia se realiza mediante radioterapia externa con radiación ( EBRT ) con una dosis curativa objetivo de 64-66 Gy. [50] La vigilancia de la progresión o recurrencia debe realizarse con la ayuda de tomografías computarizadas , cistoscopias y citología de orina. [51] Los efectos secundarios de la quimiorradiación incluyen náuseas , vómitos , pérdida de apetito , pérdida de cabello , llagas en la boca , diarrea , estreñimiento , mayor riesgo de infecciones y sangrado y fatiga. [52]
Incluso después de la extirpación quirúrgica de la vejiga, el 50% de las personas con enfermedad invasiva muscular (T2-T4) desarrollan enfermedad metastásica dentro de los dos años debido a micrometástasis . [53]
La quimioterapia combinada con cisplatino es el tratamiento estándar para el tratamiento de la vejiga metastásica. [54] La aptitud para recibir quimioterapia basada en cisplatino se evalúa antes del tratamiento. Se considera que una persona no es apta si se cumple alguna de las siguientes condiciones: [55]
Las personas que se consideran aptas reciben regímenes basados en platino; metotrexato , vinblastina , doxorrubicina , con cisplatino (MVAC) o gemcitabina con cisplatino (GC). Los regímenes alternativos incluyen paclitaxel con gemcitabina y cisplatino (PCG, terapia triple) y cisplatino, metotrexato y vinblastina (CMV). La tasa de respuesta para la combinación basada en cisplatino varía del 39 al 65% y se observa una respuesta completa en el 12-35% de las personas. [56] MVAC se tolera mejor si se combina con factor estimulante de colonias de granulocitos y el régimen se conoce como régimen MVAC de dosis densa (DDMVAC). Esta combinación ha demostrado disminuir la mortalidad por todas las causas. [57] El régimen MVAC es agresivo. La neutropenia febril (fiebre debido a la disminución de los glóbulos blancos) ocurre en el 10 al 14% y la muerte debido a toxicidad en aproximadamente el 3-4%. Los efectos secundarios comunes de MVAC incluyen supresión de la médula ósea , fiebre debido a la disminución de los glóbulos blancos, sepsis , mucositis y náuseas y vómitos . [56] Por el contrario, el régimen GC ha mostrado tasas más bajas de sepsis neutropénica y mucositis de grado 3/4 en comparación con MVAC. [58] Se han realizado esfuerzos para aumentar la tolerancia del régimen basado en cisplatino reemplazándolo con quimioterapia basada en carboplatino . Sin embargo, la terapia basada en cisplatino es superior a la quimioterapia basada en carboplatino para lograr una respuesta general y completa. [59] Sin embargo, casi la mitad de las personas con enfermedad metastásica son "no aptas" para la terapia basada en cisplatino. En tales personas, se puede utilizar una combinación de carboplatino y gemcitabina (GemCarbo) como quimioterapia de primera línea . [60] En personas que no son elegibles para ninguna quimioterapia basada en platino y tienen expresión de PD-L1 , se puede utilizar atezolizumab y pembrolizumab . [ cita requerida ]
Las personas con metástasis ósea deben recibir bifosfonatos o denosumab para prevenir eventos relacionados con el esqueleto (por ejemplo, fracturas , compresión de la médula espinal , dolor óseo). [61]
El cáncer de vejiga que es refractario o muestra progresión después de la quimioterapia basada en platino se puede tratar con quimioterapia de segunda línea o inmunoterapia. [ cita requerida ]
La quimioterapia de segunda línea más comúnmente utilizada son los regímenes de agente único de taxanos ( paclitaxel , nab-paclitaxel y docetaxel ). Otros regímenes de agente único incluyen vinflunina , un alcaloide de la vinca de tercera generación (aprobado en Europa), gemcitabina , pemetrexed , oxaliplatino e ifosfamida . [63] [64] [65] Los efectos secundarios de la vinflunina incluyen neutropenia , estreñimiento , fatiga y anemia y han limitado su uso como agente de segunda línea. La respuesta a la quimioterapia de segunda línea ocurre en el 5%–20% de las personas. La mediana de supervivencia libre de progresión con quimioterapia de segunda línea es de 3–4 meses. [66]
En pacientes con mutaciones en los receptores del factor de crecimiento de fibroblastos ( FGFR ) que no responden a la quimioterapia convencional basada en platino, se puede utilizar erdafitinib . Erdafitinib ha demostrado una tasa de respuesta del 40 % en estos pacientes. [67]
En los EE. UU. se han aprobado cinco agentes de inmunoterapia para su uso en el cáncer de vejiga metastásico. Actúan inhibiendo la proteína de muerte celular programada 1 (PD-1) o el ligando de muerte celular programada 1 (PD-L1) . Pembrolizumab y nivolumab son inhibidores del ligando de muerte celular programada 1 (PD-1) . Avelumab , atezolizumab y durvalumab son inhibidores de PD-L1 . [68] [69]
El pembrolizumab probablemente mejora un poco la supervivencia general y puede mejorar levemente la calidad de vida de las personas con cáncer urotelial que ha empeorado después del tratamiento inicial en comparación con la quimioterapia continua. [70] Sin embargo, el pembrolizumab puede tener solo efectos mínimos en la tasa de muerte resultante del tratamiento o la velocidad a la que avanza el cáncer. [70] El pembrolizumab puede causar efectos secundarios menos graves que la quimioterapia. [70]
La tomografía computarizada con contraste se utiliza para controlar las metástasis pulmonares, hepáticas y de los ganglios linfáticos. La gammagrafía ósea se utiliza para detectar y controlar la metástasis ósea. [71] La respuesta al tratamiento se mide utilizando los criterios de evaluación de la respuesta en tumores sólidos ( RECIST ) en uno de los siguientes grupos: respuesta (completa o parcial), enfermedad estable y enfermedad progresiva. [72]
El cáncer de vejiga es causado por un daño genético en el ADN de las células de la vejiga. Estos cambios pueden ser aleatorios o pueden ser inducidos por la exposición de la vejiga a sustancias tóxicas, como las que se producen al consumir tabaco. La acumulación de este daño genético altera el funcionamiento normal de las células de la vejiga, lo que hace que crezcan sin control y formen un tumor. [73]
El tabaquismo es el principal factor conocido que contribuye al cáncer de vejiga urinaria; en la mayoría de las poblaciones, el tabaquismo se asocia con más de la mitad de los casos de cáncer de vejiga en hombres y un tercio de los casos entre mujeres, [74] sin embargo, estas proporciones se han reducido en los últimos años debido a que hay menos fumadores en Europa y América del Norte. [75] Existe una relación casi lineal entre la duración del tabaquismo (en años), los paquetes-año y el riesgo de cáncer de vejiga. Se puede observar una meseta de riesgo al fumar alrededor de 15 cigarrillos al día (lo que significa que quienes fuman 15 cigarrillos al día tienen aproximadamente el mismo riesgo que quienes fuman 30 cigarrillos al día). Fumar en cualquier forma (puros, cigarrillos, pipas, pipas de agua egipcias y tabaco sin humo) aumenta el riesgo de cáncer de vejiga. [76] Dejar de fumar reduce el riesgo. El riesgo de cáncer de vejiga disminuye en un 30% en 1 a 4 años y continúa disminuyendo en un 60% a los 25 años después de dejar de fumar. [77] Sin embargo, los ex fumadores probablemente siempre tendrán un mayor riesgo de cáncer de vejiga en comparación con las personas que nunca han fumado. [75] El tabaquismo pasivo también parece ser un riesgo. [78] [79]
El consumo de opio triplica el riesgo de cáncer de vejiga, mientras que el consumo concomitante de opio y tabaco quintuplica el riesgo de cáncer de vejiga en comparación con la población general. [80]
El treinta por ciento de los tumores de vejiga probablemente son resultado de la exposición ocupacional en el lugar de trabajo a carcinógenos. La exposición ocupacional o circunstancial a las siguientes sustancias se ha implicado como causa de cáncer de vejiga: bencidina (fabricación de tintes), 4-aminobifenilo (industria del caucho), 2-naftilamina (fabricación de tintes azoicos, humos de fundición, industria del caucho, humo de cigarrillos e investigación del cáncer), fenacetina (analgésico), arsénico e hidrocarburos alifáticos clorados en el agua potable, auramina (fabricación de tintes), magenta (fabricación de tintes), orto-toluidina (fabricación de tintes), agentes endurecedores de resina epoxi y poliuretano (industria del plástico), clornafazina , brea de hulla . [81] [82] [83] [84] [85] Las ocupaciones en riesgo son los conductores de autobús, los trabajadores del caucho, los pintores, los mecánicos de motores, los trabajadores del cuero (incluido el calzado), los herreros, los ajustadores de máquinas y los mecánicos. [86] [87] Se cree que los peluqueros también corren riesgo debido a su frecuente exposición a tintes permanentes para el cabello. [88]
La infección por Schistosoma haematobium (bilharzia o esquistosomiasis ) puede causar cáncer de vejiga, particularmente del tipo de células escamosas. [89] Los huevos de Schistosoma inducen un estado inflamatorio crónico en la pared de la vejiga que resulta en fibrosis tisular. [90] Se han detectado niveles más altos de compuestos N-nitrosos en muestras de orina de personas con esquistosomiasis. [91] Los compuestos N-nitrosos se han implicado en la patogénesis del cáncer de vejiga relacionado con la esquistosomiasis. Causan daño al ADN por alquilación, especialmente mutaciones de transición de guanina a adenina en el gen supresor de tumores HRAS y p53 . [92] Se detectan mutaciones de p53 en el 73% de los tumores, las mutaciones BCL-2 representan el 32% y la combinación de los dos representa el 13%. [93] Otras causas de carcinoma de células escamosas de la vejiga incluyen cateterizaciones crónicas en personas con lesión de la médula espinal y antecedentes de tratamiento con ciclofosfamida. [94] [95]
El Instituto Americano para la Investigación del Cáncer ha declarado que existen pruebas sólidas de que beber agua que contiene arsénico aumenta el riesgo de cáncer de vejiga. [96]
El consumo elevado de grasas animales y colesterol en la dieta aumenta el riesgo de cáncer de vejiga en los hombres. [97]
Se ha demostrado que la ingestión de ácido aristolóquico presente en muchos medicamentos herbales chinos causa carcinoma urotelial e insuficiencia renal . [98] El ácido aristolóquico activa la peroxidasa en el urotelio y causa una mutación de transversión en el gen supresor de tumores TP53 . [ cita requerida ]
Las personas que se someten a radioterapia de haz externo (EBRT) para el cáncer de próstata tienen un mayor riesgo de desarrollar cáncer de vejiga invasivo. [99]
Además de estos factores de riesgo importantes, también hay muchos otros factores modificables que están menos fuertemente asociados (es decir, un aumento del riesgo del 10 al 20 %) con el cáncer de vejiga, por ejemplo, la obesidad . [100] Aunque estos podrían considerarse efectos menores, la reducción del riesgo en la población general aún podría lograrse reduciendo la prevalencia de una serie de factores de riesgo más pequeños en conjunto. [101]
Las mutaciones en los genes FGFR3 , TP53 , PIK3CA , KDM6A , ARID1A , KMT2D , HRAS , TERT , KRAS , CREBBP , RB1 y TSC1 pueden estar asociadas con algunos casos de cáncer de vejiga. [102] [103] [104] Las deleciones de partes o de la totalidad del cromosoma 9 son comunes en el cáncer de vejiga. [105] Se sabe que el cáncer de bajo grado alberga mutaciones en la vía RAS y en el gen del receptor 3 del factor de crecimiento de fibroblastos (FGFR3), los cuales desempeñan un papel en la vía MAPK/ERK . Las mutaciones de los genes p53 y RB están implicadas en tumores invasivos de músculo de alto grado. [106] El ochenta y nueve por ciento de los cánceres invasivos de músculo tienen mutaciones en los genes de remodelación de cromatina y modificación de histonas. [107] La deleción de ambas copias del gen GSTM1 tiene un aumento modesto en el riesgo de cáncer de vejiga. El producto del gen GSTM1, glutatión S-transferasa M1 (GSTM1), participa en el proceso de desintoxicación de carcinógenos como los hidrocarburos aromáticos policíclicos que se encuentran en el humo del cigarrillo. [108] De manera similar, las mutaciones en NAT2 ( N-acetiltransferasa ) se asocian con un mayor riesgo de cáncer de vejiga. La N-acetiltransferasa ayuda en la desintoxicación de carcinógenos como las aminas aromáticas (también presentes en el humo del cigarrillo). [109] Se ha demostrado que varios polimorfismos de un solo nucleótido en el gen PSCA presente en el cromosoma 8 aumentan el riesgo de cáncer de vejiga. La región promotora del gen PSCA tiene una región de respuesta a los andrógenos . Se plantea la hipótesis de que la pérdida de reactividad de esta región a los andrógenos es una causa de tumores más agresivos en las mujeres (a diferencia de los hombres que tienen una mayor cantidad de andrógenos). [110]
El cáncer de vejiga con invasión muscular es heterogéneo por naturaleza. En general, se puede clasificar genéticamente en subtipos basal y luminal. El subtipo basal muestra alteraciones que involucran RB y NFE2L2 y el tipo luminal muestra cambios en los genes FGFR3 y KDM6A. [111] El subtipo basal se subdivide en el grupo basal y el de tipo bajo en claudina y es agresivo y muestra metástasis en la presentación, sin embargo responde a la quimioterapia basada en platino. El subtipo luminal se puede subdividir en tumores similares a p53 y luminal. Los tumores similares a p53 del subtipo luminal, aunque no son tan agresivos como los del tipo basal, muestran resistencia a la quimioterapia [112]
Los sitios más comunes de metástasis de cáncer de vejiga son los ganglios linfáticos, los huesos, los pulmones, el hígado y el peritoneo . [113] Los ganglios linfáticos centinela más comunes que drenan el cáncer de vejiga son los ganglios linfáticos obturadores e ilíacos internos . La ubicación de la propagación linfática depende de la ubicación de los tumores. Los tumores en la pared superolateral de la vejiga se propagan a los ganglios linfáticos ilíacos externos . Los tumores en el cuello, la pared anterior y el fondo se propagan comúnmente a los ganglios linfáticos ilíacos internos. [114] Desde los ganglios linfáticos regionales (es decir, los ganglios linfáticos obturadores, internos y externos), el cáncer se propaga a sitios distantes como los ganglios linfáticos ilíacos comunes y los ganglios linfáticos paraaórticos . [115] Las lesiones de ganglios linfáticos salteados no se ven en el cáncer de vejiga. [114]
A partir de 2019, existe evidencia limitada de alto nivel que sugiere que comer frutas y verduras disminuye el riesgo de cáncer de vejiga. [109] Se ha identificado que las frutas y las verduras de color amarillo anaranjado , en particular las zanahorias y las que contienen selenio , las frutas cítricas y las verduras crucíferas tienen un posible efecto protector.
Si bien se sugiere que los compuestos polifenólicos del té pueden tener un efecto inhibidor sobre la formación y el crecimiento de tumores de vejiga, existe evidencia limitada que sugiere que beber té disminuye el riesgo de cáncer de vejiga. [109] Una revisión de 2022 encontró que una dieta mediterránea tiene un efecto protector sobre el riesgo de cáncer de vejiga. [116] Un mayor consumo de grasas monoinsaturadas y aceites vegetales disminuye el riesgo de cáncer de vejiga en las mujeres. [97] Un mayor consumo de fibra dietética total y cereales integrales se asocia con un menor riesgo de cáncer de vejiga. [117]
Hasta el año 2019 no hay evidencia suficiente para determinar si la detección del cáncer de vejiga en personas asintomáticas es eficaz o no. [118]
Las personas con tumores no invasivos de músculo tienen un pronóstico favorable (la supervivencia a 5 años es del 95% frente al 69% del cáncer de vejiga invasivo de músculo). [119] [120] Sin embargo, el 70% de ellos tendrá una recurrencia después del tratamiento inicial y el 30% de ellos presentará una enfermedad invasiva de músculo. [121] La recurrencia y la progresión a un estadio más avanzado de la enfermedad tienen un pronóstico menos favorable. [122]
La supervivencia después de una cistectomía radical y disección de ganglios linfáticos pélvicos depende del estadio patológico. Si la enfermedad no se ha propagado a los ganglios linfáticos y se limita a la vejiga (T1 o T2, N0), la supervivencia a los 5 años es del 78%. Si se ha propagado localmente alrededor de la región de la vejiga sin ganglios linfáticos afectados (T3, N0), la supervivencia a los 5 años se reduce al 47%. En la enfermedad con propagación a los ganglios linfáticos (N+, independientemente del estadio T), la supervivencia a los 5 años es del 31%. La enfermedad localmente avanzada y metastásica disminuye drásticamente la supervivencia, con una supervivencia media de 3 a 6 meses sin quimioterapia. La quimioterapia basada en cisplatino ha aumentado la supervivencia media a 15 meses. Sin embargo, la supervivencia a los 5 años sigue siendo del 15%. [123]
Existen varios factores pronósticos que determinan la supervivencia específica del cáncer después de una cistectomía radical. Los factores con efecto perjudicial sobre la supervivencia específica del cáncer son la edad avanzada, un mayor grado tumoral y estadio patológico, metástasis en los ganglios linfáticos , presencia de invasión linfovascular y margen positivo de tejido blando. [124] La densidad de los ganglios linfáticos (ganglios linfáticos positivos/ ganglios linfáticos totales observados en la muestra de la cirugía) es un predictor de supervivencia en la enfermedad con ganglios linfáticos positivos. Cuanto mayor sea la densidad, menor será la supervivencia. [125]
Después de una cistectomía radical, la función urinaria y sexual siguen siendo inferiores a las de la población general. Las personas que tienen una neovejiga tienen una mejor función emocional y una mejor imagen corporal en comparación con las que tienen una derivación cutánea (que necesitan llevar una bolsa para recoger la orina sobre el abdomen). [126] Los factores sociales como la familia, las relaciones, la salud y las finanzas contribuyen significativamente a determinar una buena calidad de vida en las personas a las que se les ha diagnosticado cáncer de vejiga. [127]
Un alto porcentaje de personas con cáncer de vejiga padecen ansiedad y depresión . [128] Las personas jóvenes, solteras y con enfermedad clínica avanzada tienen un alto riesgo de que se les diagnostique una enfermedad psiquiátrica después del tratamiento. Las personas con enfermedad psiquiátrica después del tratamiento parecen tener peor supervivencia general y específica del cáncer. [129] [130]

Cada año se diagnostica cáncer de vejiga a unas 500.000 personas y 200.000 mueren a causa de esta enfermedad. [134] Esto convierte al cáncer de vejiga en el décimo cáncer más diagnosticado y la decimotercera causa de muerte por cáncer. [135] El cáncer de vejiga es más común en las regiones más ricas del mundo, donde la exposición a ciertos carcinógenos es mayor. También es común en lugares donde la infección por esquistosomas es común, como el norte de África. [135]
El cáncer de vejiga es mucho más común en hombres que en mujeres; alrededor del 1,1% de los hombres y el 0,27% de las mujeres desarrollan cáncer de vejiga. [11] Esto hace que el cáncer de vejiga sea el sexto cáncer más común en hombres y el decimoséptimo en mujeres. [136] Cuando a las mujeres se les diagnostica cáncer de vejiga, tienden a tener una enfermedad más avanzada y, en consecuencia, un peor pronóstico. [136] Esta diferencia en los resultados se atribuye a numerosos factores como la diferencia en la exposición a carcinógenos, la genética , la atención social y la calidad. [110] Uno de los signos comunes del cáncer de vejiga es la hematuria y, con bastante frecuencia, se diagnostica erróneamente como infección del tracto urinario en mujeres, lo que lleva a un retraso en el diagnóstico. [110] Fumar solo puede explicar parcialmente estas tasas más altas en los hombres en el hemisferio occidental. [137] En África , los hombres son más propensos a realizar trabajo de campo y están expuestos a la infección por Schistosoma , esto puede explicar hasta cierto punto la brecha en la incidencia de cánceres de células escamosas en áreas donde el cáncer de vejiga es endémico. [137]
Al igual que la mayoría de los cánceres, el cáncer de vejiga es más común en personas mayores; la persona promedio con cáncer de vejiga es diagnosticada a los 73 años. [138]
{{cite book}}: CS1 maint: falta la ubicación del editor ( enlace ) CS1 maint: otros ( enlace ){{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ){{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ){{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ){{cite journal}}: CS1 maint: DOI inactivo a partir de abril de 2024 ( enlace )