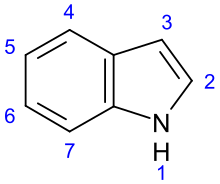
Los alcaloides indólicos son una clase de alcaloides que contienen una fracción estructural de indol ; muchos alcaloides indólicos también incluyen grupos isopreno y, por lo tanto, se denominan alcaloides de triptamina secologanina o indol terpénicos. Con más de 4100 compuestos diferentes conocidos, es una de las clases más grandes de alcaloides. [1] Muchos de ellos poseen una actividad fisiológica significativa y algunos de ellos se utilizan en medicina. El aminoácido triptófano es el precursor bioquímico de los alcaloides indólicos. [2]

La acción de algunos alcaloides indólicos se conoce desde hace siglos. Los aztecas utilizaban los hongos psilocibios que contienen los alcaloides psilocibina y psilocina . La planta con flores Rauvolfia serpentina , que contiene reserpina, era una medicina común en la India alrededor del año 1000 a. C. Los africanos utilizaban las raíces del arbusto perenne de la selva tropical Iboga , que contiene ibogaína , como estimulante. En Nigeria se administraba una infusión de semillas de frijol de Calabar a las personas acusadas de un delito : su rechazo por el estómago se consideraba un signo de inocencia; de lo contrario, la persona era asesinada por la acción de la fisostigmina , que está presente en la planta y que causa parálisis del corazón y los pulmones. [3]
El consumo de centeno y cereales relacionados contaminados con el hongo Claviceps purpurea provoca intoxicación por cornezuelo y ergotismo en humanos y otros mamíferos. La relación entre el cornezuelo y el ergotismo se estableció recién en 1717, y el alcaloide ergotamina , uno de los principales ingredientes activos del cornezuelo, fue aislado en 1918. [4]
El primer alcaloide indólico, la estricnina , fue aislado por Pierre Joseph Pelletier y Joseph Bienaimé Caventou en 1818 a partir de plantas del género Strychnos . La fórmula estructural correcta de la estricnina se determinó recién en 1947, aunque la presencia del núcleo indólico en la estructura de la estricnina se estableció algo antes. [5] [6] El propio indol fue obtenido por primera vez por Adolf von Baeyer en 1866 mientras descomponía índigo . [7]
Los alcaloides indólicos se distinguen según su biosíntesis. Los dos tipos de alcaloides indólicos son los isoprenoides y los no isoprenoides. Estos últimos incluyen elementos estructurales terpenoides , sintetizados por organismos vivos a partir de pirofosfato de dimetilalilo (DMAPP) y/o pirofosfato de isopentenilo (IPP): [8]
También existen clasificaciones puramente estructurales basadas en la presencia de carbazol , β-carbolina u otras unidades en el esqueleto carbonado de la molécula del alcaloide. [9] Se conocen unos 200 alcaloides indólicos diméricos con dos grupos indólicos. [10]
El número de alcaloides indólicos no isoprenoides conocidos es pequeño en comparación con el número de alcaloides indólicos. [2]
Uno de los derivados indólicos más simples y aún así extendidos son las aminas biógenas triptamina y 5-hidroxitriptamina ( serotonina ). [11] Aunque su asignación al alcaloide no es universalmente aceptada, [12] ambos se encuentran en plantas y animales. [13] El esqueleto de triptamina es parte de la gran mayoría de alcaloides indólicos. [14] Por ejemplo, la N , N - dimetiltriptamina (DMT), la psilocina y su psilocibina fosforilada son los derivados más simples de la triptamina. [13] Algunos alcaloides indólicos simples no contienen triptamina, como la gramina y la glicozolina (esta última es un derivado del carbazol ). [15] La camalexina es un alcaloide indólico simple producido por la planta Arabidopsis thaliana , a menudo utilizada como modelo para la biología vegetal. [16]
La prevalencia de alcaloides de β-carbolina está asociada con la facilidad de formación del núcleo de β-carbolina a partir de triptamina en la reacción intramolecular de Mannich . Los derivados de β-carbolina simples (no isoprenoides) incluyen harmina , harmalina , harmano [17] y una estructura ligeramente más compleja de cantinona. [18] La harmalina fue aislada por primera vez en 1838 por Göbel [19] y la harmina en 1848 por Fritzche. [20] [21] [22]
Los alcaloides pirolo-indólicos forman un grupo relativamente pequeño de derivados de la triptamina. Se producen por metilación del núcleo indólico en la posición 3 y la posterior adición nucleofílica en el átomo de carbono en la posición 2 con el cierre del grupo etilamino en un anillo. Un representante típico de este grupo es la fisostigmina [23] , que fue aislada por Jobst y Hesse en 1864. [24] [25]

Los alcaloides indólicos isoprenoides incluyen residuos de triptófano o triptamina y bloques de construcción isoprenoides derivados del pirofosfato de dimetilalilo y el pirofosfato de isopentenilo . [2]
Los alcaloides del cornezuelo son una clase de alcaloides indólicos hemiterpenoides relacionados con el ácido lisérgico , que, a su vez, se forma en reacciones de múltiples etapas que involucran triptófano y DMAPP. Muchos alcaloides del cornezuelo son amidas del ácido lisérgico. La amida más simple de estas es la ergina , y las más complejas se pueden distinguir en los siguientes grupos: [26] [27]
Posteriormente se demostró que la ergotinina, descubierta en 1875, y la ergotoxina (1906) eran una mezcla de varios alcaloides. En forma pura, los primeros alcaloides del cornezuelo, la ergotamina y su isómero ergotaminamina, fueron aislados por Arthur Stoll en 1918. [27]
La mayoría de los alcaloides monoterpenoides incluyen un fragmento de 9 o 10 carbonos (en negrita en la imagen) (que se origina a partir de la secologanina ), y la configuración permite agruparlos en las clases Corynanthe , Iboga y Aspidosperma . La parte monoterpenoide de sus esqueletos carbonados se ilustra a continuación con el ejemplo de los alcaloides ajmalicina y catarantina. Los átomos de carbono en círculo faltan en los alcaloides que contienen el fragmento C 9 en lugar de C 10. [14]
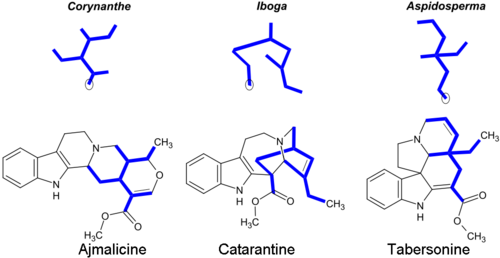
Los alcaloides de Corynanthe incluyen el esqueleto inalterado de secologanina, que está modificado en los alcaloides de Iboga y Aspidosperma . [28] Algunos alcaloides indólicos monoterpenoides representativos: [5] [29] [30]
También hay un pequeño grupo de alcaloides presentes en la planta Aristotelia – alrededor de 30 compuestos, el más importante de los cuales es la peduncularina – que contienen una parte monoterpenoide C 10 que no se origina a partir de la secologanina. [31]
Dímeros de derivados de estrictósidina, llamados de manera general bisindoles, pero más complejos que eso. Se conocen más de 200 alcaloides indólicos diméricos. Se producen en organismos vivos a través de la dimerización de bases indólicas monoméricas, en las siguientes reacciones: [32]
Además de los alcaloides bisindólicos, existen alcaloides diméricos que se forman mediante la dimerización del monómero indólico con otro tipo de alcaloide. Un ejemplo es la tubulosina, que consiste en fragmentos de indol e isoquinolina . [33]
Las plantas que son ricas en alcaloides indólicos no isoprenoides incluyen harmal ( Peganum harmala ), que contiene harmano, harmina y harmalina, y frijol de Calabar ( Physostigma venenosum ) que contiene fisostigmina . [34] Algunos miembros de la familia Convolvulaceae , en particular Ipomoea violacea y Turbina corymbosa , contienen ergolinas y lisergamidas . [35] A pesar de la considerable diversidad estructural, la mayoría de los alcaloides indólicos monoterpenoides se localizan en tres familias de plantas dicotiledóneas : Apocynaceae (géneros Alstonia , Aspidosperma , Rauvolfia y Catharanthus ), Rubiaceae ( Corynanthe ) y Loganiaceae ( Strychnos ). [36] [37]
Los alcaloides indólicos también están presentes en los hongos. Por ejemplo, los hongos psilocibios contienen derivados de la triptamina y el Claviceps contiene derivados del ácido lisérgico. [34] La piel de muchas especies de sapos del género Bufo contiene un derivado de la triptamina, la bufotenina , y la piel y el veneno de la especie Bufo alvarius ( sapo del río Colorado ) contiene 5-MeO-DMT . [38] La serotonina , que es un neurotransmisor importante en los mamíferos, también se puede atribuir a alcaloides indólicos simples. [39]
El precursor biogenético de todos los alcaloides indólicos es el aminoácido triptófano . Para la mayoría de ellos, el primer paso de síntesis es la descarboxilación del triptófano para formar triptamina . La dimetiltriptamina (DMT) se forma a partir de la triptamina por metilación con la participación de la coenzima de S-adenosil metionina (SAM). La psilocina se produce por desfosforilación espontánea de la psilocibina . [41]
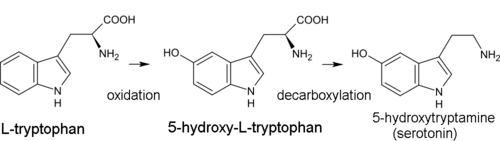
En la biosíntesis de la serotonina, el producto intermedio no es la triptamina sino el 5-hidroxitriptófano, que a su vez se descarboxila para formar 5-hidroxitriptamina (serotonina). [13]
La biosíntesis de los alcaloides β-carbolínicos se produce mediante la formación de la base de Schiff a partir de triptamina y aldehído (o ácido ceto ) y la posterior reacción intramolecular de Mannich , donde el átomo de carbono C(2) del indol actúa como nucleófilo. Luego, la aromaticidad se restaura mediante la pérdida de un protón en el átomo C(2). El esqueleto tetrahidro-β-carbolínico resultante se oxida gradualmente a dihidro-β-carbolínico y β-carbolínico. En la formación de alcaloides β-carbolínicos simples, como la harmina y la harmalina, el ácido pirúvico actúa como cetoácido. En la síntesis de alcaloides indólicos monoterpenoides, la secologanina desempeña el papel del aldehído. Los alcaloides pirroloindólicos se sintetizan en organismos vivos de forma similar. [42]

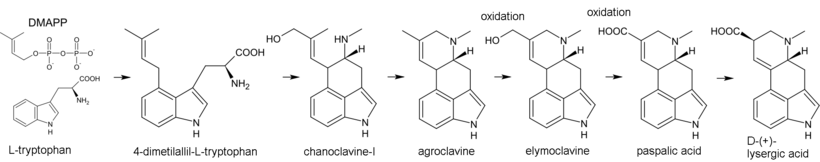
La biosíntesis de los alcaloides del cornezuelo comienza con la alquilación del triptófano por el pirofosfato de dimetilalilo (DMAPP), donde el átomo de carbono C(4) en el núcleo indólico desempeña el papel de nucleófilo. El 4-dimetilalil-L-triptófano resultante sufre N-metilación. Otros productos de la biosíntesis son la canoclavina-I y la agroclavina; esta última se hidroxila a elimoclavina, que a su vez se oxida a ácido paspálico. En el proceso de reordenamiento alílico, el ácido paspálico se convierte en ácido lisérgico. [43]
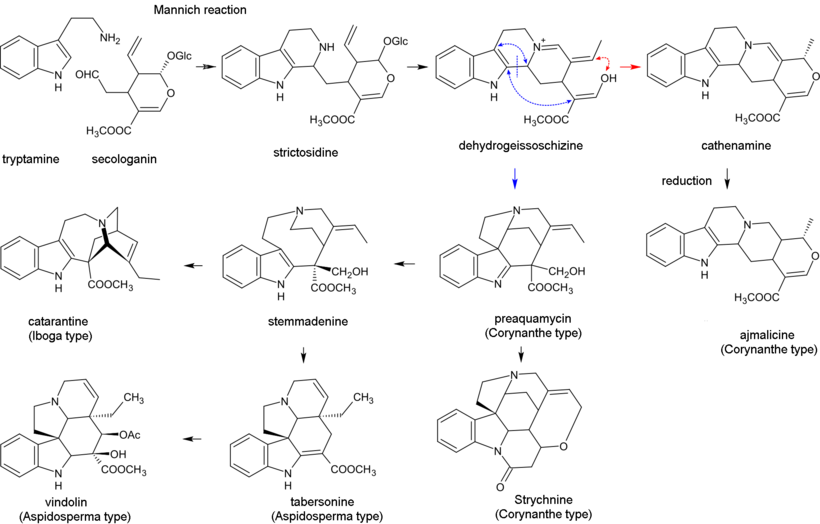
La biosíntesis de los alcaloides indólicos monoterpenoides comienza con la reacción de Mannich de la triptamina y la secologanina; produce estrictósidina que se convierte en 4,21-deshidrogeissoschizina. Luego, la biosíntesis de la mayoría de los alcaloides que contienen la parte monoterpenoide no perturbada ( tipo Corynanthe ) procede a través de la ciclización con la formación de catenamina y posterior reducción a ajmalicina en presencia de nicotinamida adenina dinucleótido fosfato (NADPH). En la biosíntesis de otros alcaloides, la 4,21-deshidrogeissoschizina primero se convierte en preakuammicina (un alcaloide del subtipo strychnos, tipo Corynanthe ) que da lugar a otros alcaloides del subtipo strychnos y de los tipos Iboga y Aspidosperma . Los alcaloides bisindólicos vinblastina y vincristina se producen en la reacción que involucra a la catarantina (alcaloide del tipo Iboga ) y la vindolina (del tipo Aspidosperma ). [29] [44]

Los alcaloides indólicos actúan sobre el sistema nervioso central y periférico . Además, los alcaloides bisindólicos vinblastina y vincristina muestran un efecto antineoplásico . [45]
Debido a las similitudes estructurales con la serotonina, muchas triptaminas pueden interactuar con los receptores de serotonina 5-HT . [46] El principal efecto de los psicodélicos serotoninérgicos como el LSD , la DMT y la psilocibina está relacionado con su condición de agonistas de los receptores 5-HT 2A . [47] [48] Por el contrario, la gramina es un antagonista del receptor 5-HT 2A . [49]
Las ergolinas , como el ácido lisérgico , incluyen elementos estructurales tanto de la triptamina como de la feniletilamina y, por lo tanto, actúan sobre todo el grupo de receptores 5-HT, adrenoceptores (principalmente de tipo α) y receptores de dopamina (principalmente de tipo D 2 ). [50] [51] Por lo tanto, la ergotamina es un agonista parcial de los receptores α-adrenérgicos y 5-HT 2 , y por lo tanto estrecha los vasos sanguíneos y estimula la constricción del útero . La dihidroergotamina es más selectiva para los receptores α-adrenérgicos y tiene un efecto más débil sobre los receptores de serotonina. La ergometrina es un agonista de los receptores α-adrenérgicos, 5-HT 2 y parcialmente D 2 . [51] [52] En comparación con otros alcaloides del cornezuelo, la ergometrina tiene una mayor selectividad para estimular el útero. [52] El LSD , una ergolina psicodélica semisintética, es un agonista de los receptores 5-HT 2A , 5-HT 1A y en menor medida D 2 y tiene un potente efecto psicodélico. [53] [54]
Algunos alcaloides indólicos monoterpenoides también interactúan con los adrenoceptores. Por ejemplo, la ajmalicina es un antagonista selectivo de los receptores α1 - adrenérgicos y, por lo tanto, tiene una acción antihipertensiva . [55] [56] La yohimbina es más selectiva con respecto a los adrenoceptores α2 ; [ 56] al bloquear los adrenoceptores α2 presinápticos , aumenta la liberación de noradrenalina , lo que eleva la presión arterial. La yohimbina se utilizó para el tratamiento de la disfunción eréctil en hombres hasta la aparición de fármacos más eficaces. [57]
Algunos alcaloides afectan indirectamente el recambio de monoaminas. Así, la harmina y la harmalina son inhibidores selectivos reversibles de la monoaminooxidasa-A . [58] La reserpina reduce la concentración de monoaminas en las neuronas presinápticas y sinápticas , induciendo así efectos antihipertensivos y antipsicóticos. [55]
Algunos alcaloides indólicos interactúan con otros tipos de receptores. La mitragynina es un agonista del receptor opioide μ . [30] Los alcaloides harmales son antagonistas del receptor GABA A , [59] y la ibogaína , de los receptores NMDA . [60] La fisostigmina es un inhibidor reversible de la acetilcolinesterasa . [61]

Las plantas y los hongos que contienen alcaloides indólicos tienen una larga historia de uso en la medicina tradicional . La Rauvolfia serpentina , que contiene reserpina como principio activo, se utilizó durante más de 3000 años en la India para tratar las mordeduras de serpiente y la locura . [62] En la Europa medieval, los extractos de cornezuelo se utilizaban en el aborto médico . [63]
Más tarde, a las plantas se les unieron preparaciones puras de alcaloides indólicos. La reserpina fue el segundo fármaco antipsicótico (después de la clorpromazina ) ; sin embargo, mostró una acción relativamente débil y fuertes efectos secundarios, y ya no se utiliza con este fin. [64] En cambio, se prescribe como un fármaco antihipertensivo , a menudo en combinación con otras sustancias. [65]
Otros fármacos que afectan al sistema cardiovascular incluyen ajmalina , que es un agente antiarrítmico de clase I, [66] y ajmalicina, que se utiliza en Europa como un fármaco antihipertensivo. [55] La fisostigmina, un inhibidor de la acetilcolinesterasa, y sus análogos sintéticos se utilizan en el tratamiento del glaucoma , la enfermedad de Alzheimer ( rivastigmina ) y la miastenia ( neostigmina , piridostigmina , distigmina ). [67] Los alcaloides del cornezuelo ergometrina (ergobazina, ergonovina), ergotamina y sus derivados sintéticos ( metilergometrina ) se aplican contra el sangrado uterino, [68] y los alcaloides bisindólicos vinblastina y vincristina son agentes antitumorales. [69]
Los estudios realizados en animales han demostrado que la ibogaína tiene potencial para tratar las adicciones a la heroína , la cocaína y el alcohol , lo que está asociado con el antagonismo de la ibogaína con los receptores NMDA . El uso médico de la ibogaína se ve obstaculizado por su estatus legal, ya que está prohibida en muchos países por considerarse una potente droga psicodélica con peligrosas implicaciones de sobredosis. Sin embargo, la red ilegal en Europa y Estados Unidos proporciona ibogaína para tratar la adicción a las drogas. [70] [71]

Desde la antigüedad, las plantas que contienen alcaloides indólicos se han utilizado como drogas psicodélicas . Los aztecas usaban y los mazatecos continúan usando hongos psilocibios y semillas psicoactivas de especies de gloria de la mañana como Ipomoea tricolor . [72] Las tribus amazónicas usan la infusión psicodélica, ayahuasca , hecha de Psychotria viridis y Banisteriopsis caapi . [73] Psychotria viridis contiene la droga psicodélica DMT , mientras que Banisteriopsis caapi contiene alcaloides harmala , que actúan como inhibidores de la monoaminooxidasa . Se cree que la función principal de los alcaloides harmala en la ayahuasca es prevenir la metabolización de DMT en el tracto digestivo y el hígado , por lo que puede cruzar la barrera hematoencefálica , mientras que el efecto directo de los alcaloides harmala en el sistema nervioso central es mínimo. [74] El veneno del sapo del río Colorado , Bufo alvarius , puede haber sido utilizado como droga psicodélica, siendo sus componentes activos 5-MeO-DMT y bufotenina . [75] Una de las drogas psicodélicas recreativas más comunes , el LSD , es una ergolina semisintética (que contiene la fracción indol). [76]
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ).