El estaño es un elemento químico ; tiene símbolo Sn (del latín stannum ) y número atómico 50. El estaño, un metal de color plateado, es lo suficientemente blando como para cortarlo con poca fuerza, [9] y una barra de estaño se puede doblar a mano con poco esfuerzo. Cuando se dobla, se puede escuchar el llamado " grito del estaño " debido al maclamiento de los cristales de estaño; [10] este rasgo es compartido por el indio , el cadmio , el zinc y el mercurio en su estado sólido.
El estaño puro después de solidificarse presenta una apariencia de espejo similar a la mayoría de los metales. En la mayoría de las aleaciones de estaño (p. ej., peltre ), el metal se solidifica con un color gris apagado.
El estaño es un metal de post-transición en el grupo 14 de la tabla periódica de elementos. Se obtiene principalmente del mineral casiterita , que contiene óxido estánnico , SnO .
2. El estaño muestra una similitud química con sus dos vecinos del grupo 14, el germanio y el plomo , y tiene dos estados de oxidación principales , +2 y el ligeramente más estable +4. El estaño es el elemento número 49 más abundante en la Tierra y tiene, con 10 isótopos estables, el mayor número de isótopos estables de la tabla periódica, debido a su número mágico de protones.
Tiene dos alótropos principales: a temperatura ambiente, el alótropo estable es el β-estaño, un metal maleable de color blanco plateado ; a bajas temperaturas es el α-estaño gris menos denso, que tiene la estructura cúbica de diamante . El estaño metálico no se oxida fácilmente en el aire y el agua.
La primera aleación de estaño utilizada a gran escala fue el bronce, fabricado con 1⁄8 de estaño y 7⁄8 de cobre ( 12,5 % y 87,5 % respectivamente ) , ya en el año 3000 a.C. Después del 600 a. C. se produjo estaño metálico puro. El peltre , que es una aleación de 85 a 90% de estaño y el resto comúnmente consiste en cobre , antimonio , bismuto y, a veces, plomo y plata, se ha utilizado para cubiertos desde la Edad del Bronce . En los tiempos modernos, el estaño se utiliza en muchas aleaciones, en particular en soldaduras blandas de estaño y plomo , que suelen tener un 60% o más de estaño, y en la fabricación de películas transparentes y eléctricamente conductoras de óxido de indio y estaño en aplicaciones optoelectrónicas . Otra gran aplicación es el estañado de acero resistente a la corrosión . Debido a la baja toxicidad del estaño inorgánico, el acero estañado se utiliza ampliamente para el envasado de alimentos como " latas ". Algunos compuestos organoestánnicos pueden ser extremadamente tóxicos.

El estaño es un metal de color blanco plateado blando, maleable , dúctil y muy cristalino . Cuando se dobla una barra de estaño , se puede escuchar un crujido conocido como " grito de estaño " debido al entrelazamiento de los cristales. [10] El estaño se funde a aproximadamente 232 °C (450 °F), el más bajo del grupo 14. El punto de fusión se reduce aún más a 177,3 °C (351,1 °F) para partículas de 11 nm. [11] [12]
El β-estaño, también llamado estaño blanco , es el alótropo (forma estructural) del estaño elemental que es estable a temperatura ambiente y por encima de ella. Es metálico y maleable, y tiene una estructura cristalina tetragonal centrada en el cuerpo . El α-estaño, o estaño gris , es la forma no metálica. Es estable por debajo de 13,2 °C (55,8 °F) y es quebradizo . El α-estaño tiene una estructura cristalina cúbica de diamante , al igual que el diamante y el silicio . El α-estaño no tiene propiedades metálicas porque sus átomos forman una estructura covalente en la que los electrones no pueden moverse libremente. El α-estaño es un material en polvo de color gris opaco que no tiene usos comunes aparte de las aplicaciones de semiconductores especializadas . [10] El γ-estaño y el σ-estaño existen a temperaturas superiores a 161 °C (322 °F) y presiones superiores a varios GPa . [13]
En condiciones de frío, el β-estaño tiende a transformarse espontáneamente en α-estaño, fenómeno conocido como " plaga del estaño " o "enfermedad del estaño". [14] Algunas fuentes no verificables también dicen que, durante la campaña rusa de Napoleón de 1812, las temperaturas llegaron a ser tan frías que los botones de hojalata de los uniformes de los soldados se desintegraron con el tiempo, contribuyendo a la derrota de la Grande Armée , [15] a leyenda persistente. [16] [17] [18]
La temperatura de transformación α-β es de 13,2 °C (55,8 °F), pero las impurezas (por ejemplo, Al, Zn, etc.) la reducen muy por debajo de 0 °C (32 °F). Con la adición de antimonio o bismuto es posible que la transformación no se produzca en absoluto, lo que aumenta la durabilidad. [19]
Los grados comerciales de estaño (99,8% de contenido de estaño) resisten la transformación debido al efecto inhibidor de pequeñas cantidades de bismuto, antimonio, plomo y plata presentes como impurezas. Los elementos de aleación como el cobre, el antimonio, el bismuto, el cadmio y la plata aumentan la dureza del estaño. [20] El estaño forma fácilmente fases intermetálicas duras y quebradizas que normalmente son indeseables. No se mezcla en una solución con la mayoría de los metales y elementos, por lo que el estaño no tiene mucha solubilidad sólida. El estaño se mezcla bien con bismuto , galio , plomo , talio y zinc , formando sistemas eutécticos simples . [19]
El estaño se convierte en superconductor por debajo de 3,72 K [21] y fue uno de los primeros superconductores en ser estudiados. [22] El efecto Meissner , uno de los rasgos característicos de los superconductores, se descubrió por primera vez en cristales de estaño superconductores. [22]
El estaño resiste la corrosión del agua , pero puede sufrir corrosión con ácidos y álcalis . El estaño se puede pulir mucho y se utiliza como capa protectora para otros metales, [10] una capa protectora de óxido ( pasivación ) evita una mayor oxidación. [23] El estaño actúa como catalizador desencadenando una reacción química de una solución que contiene oxígeno y ayuda a aumentar la velocidad de la reacción química resultante. [24]
El estaño tiene diez isótopos estables , el mayor número de cualquier elemento. Sus números de masa son: 112, 114, 115, 116, 117, 118, 119, 120, 122 y 124, aunque el Sn-112, el Sn-122 y el Sn-124 son teóricamente inestables y pueden sufrir una doble desintegración beta . El estaño 120 constituye casi un tercio de todo el estaño. También son comunes el estaño-118 y el estaño-116. El estaño-115 es el isótopo estable menos común. Los isótopos con número de masa par no tienen espín nuclear , mientras que los de número de masa impar tienen espín nuclear de 1/2. Se cree que el estaño tiene una gran multitud de isótopos estables debido a que su número atómico es 50, que es un " número mágico " en física nuclear.
El estaño es uno de los elementos más fáciles de detectar y analizar mediante espectroscopía de RMN , que se basa en el peso molecular y sus cambios químicos se comparan con el tetrametilestaño ( SnMe) .
4). [notas 1] [25]
De los isótopos estables, el estaño-115 tiene una sección transversal de captura alta para energías de neutrones rápidos, de 30 graneros . El estaño-117 ocupa el primer lugar, con una sección transversal de 2,3 graneros, mientras que el estaño-119 tiene una sección transversal ligeramente más pequeña de 2,2 graneros. [26] Antes de que estas secciones transversales fueran bien conocidas, se propuso utilizar soldadura de estaño y plomo como refrigerante para reactores rápidos debido a su bajo punto de fusión. Los estudios actuales son para refrigerantes de reactores de plomo o plomo-bismuto porque ambos metales pesados son casi transparentes a los neutrones rápidos, con secciones transversales de captura muy bajas. [27] Para utilizar un refrigerante de estaño o estaño-plomo, el estaño primero tendría que pasar por una separación de isótopos para eliminar los isótopos de estaño 115, 117 y 119. Combinados, estos tres isótopos constituyen aproximadamente el 17% del estaño natural, pero representan casi toda la sección transversal de captura. De los siete isótopos restantes, el estaño-112 tiene una sección transversal de captura de 1 granero. Los otros seis isótopos que forman el 82,7% del estaño natural tienen secciones transversales de captura de 0,3 graneros o menos, lo que los hace efectivamente transparentes a los neutrones, como lo son el plomo y el bismuto.
El estaño tiene 31 isótopos inestables, cuyo número de masa oscila entre 99 y 139. Los isótopos de estaño inestables tienen vidas medias de menos de un año, excepto el estaño-126 , que tiene una vida media de unos 230.000 años. El estaño-100 y el estaño-132 son dos de los pocos nucleidos con un núcleo " doblemente mágico " que, a pesar de ser inestables, ya que tienen relaciones neutrones-protones muy desiguales , son los puntos finales más allá de los cuales los isótopos del estaño son más ligeros que el estaño-100 y más pesados. que el estaño-132 son mucho menos estables. [28] Se han identificado otros 30 isómeros metaestables para los isótopos de estaño entre 111 y 131, siendo el más estable el estaño-121m, con una vida media de 43,9 años. [29]
Las diferencias relativas en el número de isótopos estables del estaño pueden explicarse por cómo se forman durante la nucleosíntesis estelar . El estaño-116 al estaño-120 se forman en el proceso s (captura lenta de neutrones) en la mayoría de las estrellas , lo que los convierte en los isótopos de estaño más comunes, mientras que el estaño-122 y el estaño-124 solo se forman en el proceso r ( captura rápida de neutrones) en supernovas y son menos comunes. Los isótopos de estaño 117 a 120 también se producen en el proceso r . [ cita necesaria ] . Los isótopos de estaño 112, 114 y 115 no se pueden producir en cantidades significativas en los procesos s o r y se encuentran entre los núcleos p cuyos orígenes no se comprenden bien. Algunas teorías sobre su formación incluyen la captura de protones y la fotodesintegración . El estaño-115 podría producirse parcialmente en el proceso s , tanto directamente como como hijo del indio-115 de larga duración . [30]
La palabra estaño se comparte entre las lenguas germánicas y se remonta al protogermánico * tin-om reconstruido ; los cognados incluyen el Zinn alemán , el tenn sueco y el estaño holandés . No se encuentra en otras ramas del indoeuropeo , excepto tomando prestado del germánico (por ejemplo, el irlandés tinne del inglés). [31] [32]
El nombre latino del estaño, stannum , originalmente significaba una aleación de plata y plomo, y pasó a significar "estaño" en el siglo IV [33] ; la palabra latina anterior era plumbum candidum , o "plomo blanco". Stannum aparentemente proviene de un stāgnum anterior (que significa la misma sustancia), [31] el origen de los términos romances y celtas para el estaño , como el francés étain , el español estaño , el italiano stagno y el irlandés stán . [31] [34] Se desconoce el origen de stannum / stāgnum ; puede ser preindoeuropeo . [35]
Las Meyers Konversations-Lexikon sugieren, en cambio, que el estannum procedía del steen de Cornualles , y es una prueba de que Cornualles en los primeros siglos d.C. era la principal fuente de estaño. [ cita necesaria ]
.jpg/440px-Sword_bronze_age_(2nd_version).jpg)
La extracción y el uso del estaño se remontan a principios de la Edad del Bronce, alrededor del año 3000 a. C., cuando se observó que los objetos de cobre formados por minerales polimetálicos con diferentes contenidos de metal tenían diferentes propiedades físicas. [36] Los primeros objetos de bronce tenían un contenido de estaño o arsénico de menos del 2% y se cree que son el resultado de una aleación no intencionada debido al contenido de trazas de metal en el mineral de cobre. [37] La adición de un segundo metal al cobre aumenta su dureza, reduce la temperatura de fusión y mejora el proceso de fundición al producir una masa fundida más fluida que se enfría hasta convertirse en un metal más denso y menos esponjoso. [37] Esta fue una innovación importante que permitió formas mucho más complejas fundidas en moldes cerrados de la Edad del Bronce. Los objetos de bronce con arsénico aparecen por primera vez en el Cercano Oriente, donde el arsénico se encuentra comúnmente con el mineral de cobre, pero los riesgos para la salud se dieron cuenta rápidamente y la búsqueda de fuentes de minerales de estaño, mucho menos peligrosos, comenzó a principios de la Edad del Bronce. [38] Esto creó la demanda de estaño metal raro y formó una red comercial que vinculaba las fuentes distantes de estaño con los mercados de las culturas de la Edad del Bronce. [ cita necesaria ]
Casiterita ( SnO
2), la forma de óxido de estaño, fue probablemente la fuente original de estaño. Otros minerales de estaño son sulfuros menos comunes , como la estannita , que requieren un proceso de fundición más complicado . La casiterita a menudo se acumula en canales aluviales como depósitos de placer porque es más dura, pesada y químicamente más resistente que el granito que la acompaña . [37] La casiterita suele ser de color negro u oscuro, y estos depósitos se pueden ver fácilmente en las orillas de los ríos . Es posible que, incidentalmente, los depósitos aluviales ( placeres ) hayan sido recolectados y separados mediante métodos similares a los del lavado de oro . [39]
En la gran mayoría de sus compuestos, el estaño tiene el estado de oxidación II o IV. Los compuestos que contienen estaño bivalente se denominan '"`UNIQ--templatestyles-0000005F-QINU`"' estañosos, mientras que los que contienen estaño tetravalente se denominan estánnicos .
Los compuestos de halogenuros son conocidos por ambos estados de oxidación. Para el Sn(IV), los cuatro haluros son bien conocidos: SnF 4 , SnCl 4 , SnBr 4 y SnI 4 . Los tres miembros más pesados son compuestos moleculares volátiles, mientras que el tetrafluoruro es polimérico. Los cuatro haluros son conocidos por Sn(II) también: SnF 2 , SnCl
2, SnBr 2 y SnI 2 . Todos son sólidos poliméricos. De estos ocho compuestos, sólo los yoduros están coloreados. [40]
El cloruro de estaño (II) (también conocido como cloruro estannoso) es el haluro de estaño comercial más importante. Para ilustrar las rutas hacia tales compuestos, el cloro reacciona con el estaño metálico para dar SnCl 4 , mientras que la reacción del ácido clorhídrico y el estaño produce SnCl.
2y gas hidrógeno. Alternativamente, el SnCl 4 y el Sn se combinan para formar cloruro estannoso mediante un proceso llamado comproporcionación : [41]
El estaño puede formar muchos óxidos, sulfuros y otros derivados de calcogenuros . El dióxido SnO
2(casiterita) se forma cuando el estaño se calienta en presencia de aire . [40] SnO
2Es anfótero , lo que significa que se disuelve tanto en soluciones ácidas como básicas. [42] Estanantos con la estructura [ Sn(OH)
6] 2− , como K
2[ Sn(OH)
6], también son conocidos, aunque el ácido estánnico libre H
2[ Sn(OH)
6] es desconocido.
Los sulfuros de estaño existen en los estados de oxidación +2 y +4: sulfuro de estaño (II) y sulfuro de estaño (IV) ( oro mosaico ).

Estanano ( SnH
4), con estaño en estado de oxidación +4, es inestable. Sin embargo, los hidruros de organoestaño son bien conocidos, por ejemplo el hidruro de tributilestaño (Sn(C4H9 ) 3H ) . [10] Estos compuestos liberan radicales tributil estaño transitorios , que son ejemplos raros de compuestos de estaño (III). [44]
Los compuestos organoestaño , a veces llamados estannanos, son compuestos químicos con enlaces estaño-carbono. [45] De los compuestos de estaño, los derivados orgánicos son comercialmente los más útiles. [46] Algunos compuestos organoestánnicos son altamente tóxicos y se han utilizado como biocidas . El primer compuesto organoestaño que se informó fue el diyoduro de dietilestaño ((C 2 H 5 ) 2 SnI 2 ), informado por Edward Frankland en 1849. [47]
La mayoría de los compuestos organoestaño son líquidos o sólidos incoloros que son estables al aire y al agua. Adoptan geometría tetraédrica. Los compuestos de tetraalquil y tetraarilestaño se pueden preparar utilizando reactivos de Grignard : [46]
Los haluros-alquilo mixtos, que son más comunes y más importantes comercialmente que los derivados tetraorgánicos, se preparan mediante reacciones de redistribución :
Los compuestos de organoestaño divalentes son poco comunes, aunque más comunes que los compuestos de organogermanio y organosilicio divalentes relacionados . La mayor estabilización de la que disfruta el Sn(II) se atribuye al " efecto par inerte ". Los compuestos organoestaño(II) incluyen tanto estanilenos (fórmula: R 2 Sn, como se ve para los carbenos singletes ) como distanilenos (R 4 Sn 2 ), que son aproximadamente equivalentes a los alquenos . Ambas clases exhiben reacciones inusuales. [48]

El estaño se genera mediante el largo proceso s en estrellas de masa baja a media (con masas de 0,6 a 10 veces la del Sol ) y, finalmente, mediante la desintegración beta de los isótopos pesados del indio . [49]
El estaño es el 49º elemento más abundante en la corteza terrestre , representando 2 ppm frente a 75 ppm del zinc, 50 ppm del cobre y 14 ppm del plomo. [50]
El estaño no se encuentra como elemento nativo, sino que debe extraerse de varios minerales. Casiterita ( SnO
2) es la única fuente comercialmente importante de estaño, aunque se recuperan pequeñas cantidades de estaño a partir de sulfuros complejos como estanita , cilindrita , francqueita , canfieldita y teallita . Los minerales con estaño casi siempre están asociados con rocas de granito , generalmente en un nivel de contenido de óxido de estaño del 1%. [51]
Debido a la mayor gravedad específica del dióxido de estaño, aproximadamente el 80% del estaño extraído proviene de depósitos secundarios que se encuentran aguas abajo de las vetas primarias. El estaño a menudo se recupera de gránulos arrastrados río abajo en el pasado y depositados en valles o en el mar. Las formas más económicas de extraer estaño son mediante dragado , hidráulica o a cielo abierto . La mayor parte del estaño del mundo se produce a partir de depósitos de placer , que pueden contener tan solo un 0,015% de estaño. [52]
En 2011 se extrajeron unas 253.000 toneladas de estaño, principalmente en China (110.000 t), Indonesia (51.000 t), Perú (34.600 t), Bolivia (20.700 t) y Brasil (12.000 t). [53] Históricamente, las estimaciones de la producción de estaño han variado según el mercado y la tecnología minera. Se estima que, con las actuales tasas de consumo y tecnologías, la Tierra se quedará sin estaño explotable en 40 años. [54] En 2006 , Lester Brown sugirió que el estaño podría agotarse en 20 años basándose en estimaciones conservadoras de un crecimiento anual del 2%. [55]
La chatarra de estaño es una fuente importante de metal. La recuperación de estaño mediante el reciclaje está aumentando rápidamente. [ ¿ cuando? ] [ cita necesaria ] Si bien Estados Unidos no ha extraído (desde 1993) ni fundido (desde 1989) estaño, fue el mayor productor secundario, reciclando casi 14.000 toneladas en 2006. [53]
Se reportan nuevos depósitos en Mongolia , [56] y en 2009 se descubrieron nuevos depósitos de estaño en Colombia. [57]
El estaño se produce por reducción carbotérmica del mineral de óxido con carbono o coque. Se pueden utilizar tanto hornos de reverbero como hornos eléctricos : [58] [59] [60]
Las diez mayores empresas produjeron la mayor parte del estaño del mundo en 2007.
La mayor parte del estaño del mundo se comercializa en la LME, procedente de 8 países, bajo 17 marcas. [61]
El Consejo Internacional del Estaño se creó en 1947 para controlar el precio del estaño. Se derrumbó en 1985. En 1984, se creó la Asociación de Países Productores de Estaño , con Australia, Bolivia, Indonesia, Malasia, Nigeria, Tailandia y Zaire como miembros. [64]
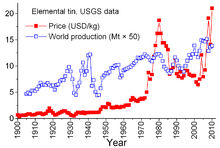
El estaño es único entre los productos minerales debido a los complejos acuerdos entre los países productores y los países consumidores que se remontan a 1921. Los acuerdos anteriores tendían a ser algo informales y condujeron al "Primer Acuerdo Internacional del Estaño" en 1956, el primero de una serie que efectivamente colapsó. en 1985. A través de estos acuerdos, el Consejo Internacional del Estaño (ITC) tuvo un efecto considerable sobre los precios del estaño. El ITC apoyó el precio del estaño durante los períodos de precios bajos comprando estaño para su reserva de reserva y pudo limitar el precio durante los períodos de precios altos vendiendo de la reserva. Se trataba de un enfoque contrario al libre mercado, diseñado para asegurar un flujo suficiente de estaño a los países consumidores y beneficios para los países productores. Sin embargo, la reserva de reserva no era lo suficientemente grande, y durante la mayor parte de esos 29 años los precios del estaño aumentaron, a veces bruscamente, especialmente entre 1973 y 1980, cuando una inflación galopante azotó a muchas economías mundiales. [sesenta y cinco]
A finales de los años 1970 y principios de los 1980, Estados Unidos redujo sus reservas estratégicas de estaño, en parte para aprovechar los precios históricamente altos del estaño. La recesión de 1981-82 dañó la industria del estaño. El consumo de estaño disminuyó drásticamente. El ITC pudo evitar caídas realmente pronunciadas mediante compras aceleradas de su reserva de reserva; esta actividad requirió un gran endeudamiento. El ITC siguió tomando préstamos hasta finales de 1985, cuando alcanzó su límite de crédito. Inmediatamente, se produjo una importante "crisis del estaño": el estaño fue excluido de la cotización en la Bolsa de Metales de Londres durante unos tres años. El ITC se disolvió poco después y el precio del estaño, ahora en un entorno de libre mercado, cayó a 4 dólares por libra y se mantuvo en ese nivel durante los años noventa. [65] El precio volvió a aumentar en 2010 con un repunte del consumo tras la crisis económica de 2007-2008 , que acompañó a la reposición de existencias y al crecimiento continuo del consumo. [53]

La Bolsa de Metales de Londres (LME) es el principal sitio de negociación del estaño. [53] Otros mercados de contratos de estaño son el Mercado del Estaño de Kuala Lumpur (KLTM) y la Bolsa del Estaño de Indonesia (INATIN). [66]
Debido a factores involucrados en la crisis de la cadena de suministro global de 2021 , los precios del estaño casi se duplicaron durante 2020-21 y han tenido su mayor aumento anual en más de 30 años. La Asociación Internacional del Estaño estimó que el consumo mundial de estaño refinado crecerá un 7,2 por ciento en 2021, después de perder un 1,6 por ciento en 2020 cuando la pandemia de COVID-19 trastornó las industrias manufactureras mundiales. [67]

En 2018, poco menos de la mitad de todo el estaño producido se utilizó para soldadura. El resto se dividió entre estañado, productos químicos de estaño, latón y aleaciones de bronce, y usos especializados. [68]
El estaño se ha utilizado durante mucho tiempo en aleaciones con plomo como soldadura , en cantidades del 5 al 70% p/p. El estaño con plomo forma una mezcla eutéctica en una proporción en peso de 61,9% de estaño y 38,1% de plomo (la proporción atómica: 73,9% de estaño y 26,1% de plomo), con una temperatura de fusión de 183 °C (361,4 °F). Estas soldaduras se utilizan principalmente para unir tuberías o circuitos eléctricos . Desde que la Directiva sobre residuos de aparatos eléctricos y electrónicos (Directiva RAEE) y la Directiva sobre restricción de sustancias peligrosas de la Unión Europea entraron en vigor el 1 de julio de 2006, el contenido de plomo en dichas aleaciones ha disminuido. Si bien la exposición al plomo se asocia con problemas de salud graves , la soldadura sin plomo no está exenta de desafíos, incluido un punto de fusión más alto y la formación de bigotes de estaño que causan problemas eléctricos. La plaga del estaño puede ocurrir en soldaduras sin plomo, provocando la pérdida de la unión soldada. Se están encontrando aleaciones de reemplazo, pero persisten los problemas de integridad de las uniones. [69] Una aleación común sin plomo es 99% estaño, 0,7% cobre y 0,3% plata. [70]

El estaño se adhiere fácilmente al hierro y se utiliza para recubrir plomo , zinc y acero para evitar la corrosión. Los recipientes de acero estañado (o estañado) se utilizan ampliamente para la conservación de alimentos , y esto constituye una gran parte del mercado del estaño metálico. Un bote de hojalata para conservar alimentos se fabricó por primera vez en Londres en 1812. [71] Los hablantes de inglés británico llaman a estos recipientes "tins", mientras que los hablantes de inglés estadounidense los llaman " cans " o "tin cans". Una derivación de tal uso es el término del argot " tinnie " o "tinny", que significa "lata de cerveza" en Australia. El silbato de hojalata se llama así porque primero se produjo en masa en acero estañado. [72] [73]
Los recipientes para cocinar de cobre, como cacerolas y sartenes, se recubren frecuentemente con una fina capa de estaño, mediante galvanoplastia o mediante métodos químicos tradicionales , ya que el uso de utensilios de cocina de cobre con alimentos ácidos puede ser tóxico.


El estaño en combinación con otros elementos forma una amplia variedad de aleaciones útiles. El estaño suele estar aleado con cobre. El peltre tiene entre 85% y 99% de estaño; [74] El metal que contiene también tiene un alto porcentaje de estaño. [75] [76] El bronce es principalmente cobre con un 12% de estaño, mientras que la adición de fósforo produce bronce fosforado . El metal de campana también es una aleación de cobre y estaño que contiene un 22% de estaño. En ocasiones se ha utilizado estaño en la acuñación; alguna vez formó un porcentaje de un solo dígito (generalmente cinco por ciento o menos) de centavos estadounidenses [77] y canadienses [78] . Debido a que el cobre es a menudo el metal principal en tales monedas, incluido a veces el zinc, podrían llamarse bronce o aleaciones de latón.
El compuesto de niobio y estaño Nb 3 Sn se utiliza comercialmente en bobinas de imanes superconductores por su alta temperatura crítica (18 K) y campo magnético crítico (25 T ). Un imán superconductor que pesa tan solo dos kilogramos es capaz de producir el campo magnético de un electroimán convencional que pesa toneladas. [79]
Se añade un pequeño porcentaje de estaño a las aleaciones de circonio para el revestimiento del combustible nuclear. [80]
La mayoría de los tubos metálicos de un órgano de tubos son de una aleación de estaño y plomo, siendo la composición más común 50/50. La proporción de estaño en la pipa define el tono de la pipa, ya que el estaño tiene una resonancia tonal deseable. Cuando una aleación de estaño/plomo se enfría, la fase de plomo se solidifica primero, luego, cuando se alcanza la temperatura eutéctica, el líquido restante forma la estructura eutéctica en capas de estaño/plomo, que es brillante; El contraste con la fase principal produce un efecto moteado o moteado. Esta aleación de metal se conoce como metal manchado. Las principales ventajas del uso de estaño para tuberías incluyen su apariencia, trabajabilidad y resistencia a la corrosión. [81] [82]
Los óxidos de indio y estaño son conductores de electricidad y transparentes, y se utilizan para fabricar películas transparentes conductoras de electricidad con aplicaciones en dispositivos optoelectrónicos como pantallas de cristal líquido . [83]

El acero estañado perforado, también llamado estaño perforado, es una técnica artesanal originaria del centro de Europa para la creación de artículos para el hogar funcionales y decorativos. Los diseños de piercings decorativos existen en una amplia variedad, basados en la tradición local y el artesano. Los faroles de hojalata troquelada son la aplicación más habitual de esta técnica artesanal. La luz de una vela que brilla a través del diseño perforado crea un patrón de luz decorativo en la habitación donde se encuentra. Las linternas y otros artículos de hojalata perforada se crearon en el Nuevo Mundo desde los primeros asentamientos europeos. Un ejemplo muy conocido es la linterna Revere, que lleva el nombre de Paul Revere . [84]
Antes de la era moderna, en algunas zonas de los Alpes , se afilaba un cuerno de cabra o de oveja y se perforaba un panel de hojalata utilizando el alfabeto y los números del uno al nueve. Esta herramienta de aprendizaje se conocía apropiadamente como "cuerno de hojalata". Las reproducciones modernas están decoradas con motivos como corazones y tulipanes.
En Estados Unidos, las cajas fuertes para pasteles y alimentos se utilizaban en los días anteriores a la refrigeración. Se trataba de armarios de madera de varios estilos y tamaños, ya fueran de suelo o colgantes, destinados a disuadir a las alimañas e insectos y a mantener el polvo de los alimentos perecederos. Estos gabinetes tenían inserciones de hojalata en las puertas y, a veces, en los costados, perforadas por el propietario, el ebanista o el hojalatero en diferentes diseños para permitir la circulación del aire y excluir las moscas. Las reproducciones modernas de estos artículos siguen siendo populares en América del Norte. [85]
El vidrio para ventanas se fabrica con mayor frecuencia flotando vidrio fundido sobre estaño fundido ( vidrio flotado ), lo que da como resultado una superficie plana e impecable. A esto también se le llama " proceso Pilkington ". [86]
El estaño se utiliza como electrodo negativo en baterías avanzadas de iones de litio . Su aplicación está algo limitada por el hecho de que algunas superficies de estaño [ ¿cuáles? ] catalizan la descomposición de electrolitos a base de carbonatos utilizados en baterías de iones de litio. [87]
El fluoruro de estaño (II) se añade a algunos productos para el cuidado dental [88] como fluoruro estannoso (SnF 2 ). El fluoruro de estaño (II) se puede mezclar con abrasivos de calcio , mientras que el fluoruro de sodio, más común , se vuelve biológicamente inactivo gradualmente en presencia de compuestos de calcio. [89] También se ha demostrado que es más eficaz que el fluoruro de sodio para controlar la gingivitis . [90]
El estaño se utiliza como objetivo para crear plasmas inducidos por láser que actúan como fuente de luz para la litografía ultravioleta extrema .
Los compuestos organoestánnicos son los más utilizados. La producción industrial mundial probablemente supere las 50.000 toneladas . [91]
La principal aplicación comercial de los compuestos organoestaño es la estabilización de plásticos de PVC . En ausencia de tales estabilizadores, el PVC se degradaría rápidamente con el calor, la luz y el oxígeno atmosférico, dando como resultado productos descoloridos y quebradizos. El estaño elimina los iones de cloruro lábiles (Cl − ), que de otro modo eliminarían el HCl del material plástico. [92] Los compuestos de estaño típicos son derivados de ácido carboxílico del dicloruro de dibutilestaño, como el dilaurato . [93]
Algunos compuestos organoestánnicos son relativamente tóxicos, con ventajas y problemas. Se utilizan por sus propiedades biocidas como fungicidas , pesticidas , alguicidas , conservantes de la madera y agentes antiincrustantes . [92] El óxido de tributilestaño se utiliza como conservante de la madera . [94] El tributilestaño también se utiliza para diversos fines industriales, como el control de lodos en fábricas de papel y la desinfección de aguas de refrigeración industriales en circulación. [95] El tributilestaño se usaba como aditivo en la pintura de barcos para prevenir el crecimiento de organismos contaminantes en los barcos, y su uso disminuyó después de que los compuestos organoestaño fueron reconocidos como contaminantes orgánicos persistentes con alta toxicidad para algunos organismos marinos (el buccino , por ejemplo). [96] La UE prohibió el uso de compuestos organoestánnicos en 2003, [97] mientras preocupaba la toxicidad de estos compuestos para la vida marina y el daño a la reproducción y el crecimiento de algunas especies marinas [92] (algunos informes describen efectos biológicos en la vida marina). vida en una concentración de 1 nanogramo por litro) han llevado a una prohibición mundial por parte de la Organización Marítima Internacional . [98] Muchas naciones ahora restringen el uso de compuestos organoestánnicos a embarcaciones de más de 25 m (82 pies) de largo. [92] La persistencia del tributilestaño en el medio acuático depende de la naturaleza del ecosistema. [99] Debido a esta persistencia y su uso como aditivo en la pintura de barcos, se han encontrado altas concentraciones de tributilestaño en sedimentos marinos ubicados cerca de muelles navales. [100] El tributilestaño se ha utilizado como biomarcador de imponex en neogasterópodos , con al menos 82 especies conocidas. [101] Con los altos niveles de TBT en las zonas costeras locales, debido a las actividades marítimas, los mariscos tuvieron un efecto adverso. [99] Imposex es la imposición de características sexuales masculinas a especímenes femeninos donde les crece un pene y un conducto deferente palial . [101] [102] Un nivel alto de TBT puede dañar las glándulas endocrinas , el sistema nervioso central y reproductivo de los mamíferos , la estructura ósea y el tracto gastrointestinal . [102] El tributilestaño no solo afecta a los mamíferos, sino que también afecta a las nutrias marinas, las ballenas, los delfines y los humanos. [102]
Algunos reactivos de estaño son útiles en química orgánica . En la aplicación más amplia, el cloruro estannoso es un agente reductor común para la conversión de grupos nitro y oxima en aminas . La reacción de Stille acopla compuestos organoestaño con haluros o pseudohaluros orgánicos . [103]
El estaño forma varias fases intermetálicas con el litio metálico, lo que lo convierte en un material potencialmente atractivo para aplicaciones de baterías. La gran expansión volumétrica del estaño al alearse con litio y la inestabilidad de la interfaz estaño-electrolito orgánico a potenciales electroquímicos bajos son los mayores desafíos para el empleo en celdas comerciales. [104] Sony implementó el compuesto intermetálico de estaño con cobalto y carbono en sus celdas Nexelion lanzadas a finales de la década de 2000. La composición del material activo es aproximadamente Sn 0,3 Co 0,4 C 0,3 . La investigación demostró que sólo algunas facetas cristalinas del Sn tetragonal (beta) son responsables de una actividad electroquímica indeseable. [105]
Son casi desconocidos los casos de intoxicación por estaño metálico, sus óxidos y sus sales. Por otro lado, ciertos compuestos orgánicos de estaño son casi tan tóxicos como el cianuro . [46]
La exposición al estaño en el lugar de trabajo puede ocurrir por inhalación, contacto con la piel y contacto con los ojos. La Administración de Salud y Seguridad Ocupacional de EE. UU. (OSHA) estableció el límite de exposición permisible para la exposición al estaño en el lugar de trabajo en 2 mg/m 3 durante una jornada laboral de 8 horas. El Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) determinó un límite de exposición recomendado (REL) de 2 mg/m 3 durante una jornada laboral de 8 horas. En niveles de 100 mg/m 3 , el estaño es inmediatamente peligroso para la vida y la salud . [106]
Sólo los oficiales tenían botones de metal, y éstos estaban hechos de latón.
{{cite book}}: |journal=ignorado ( ayuda )