El receptor de células T ( TCR ) es un complejo proteico que se encuentra en la superficie de las células T , o linfocitos T, [1] y que es responsable de reconocer fragmentos de antígeno como péptidos unidos a moléculas del complejo mayor de histocompatibilidad (MHC). La unión entre el TCR y los péptidos antigénicos es de afinidad relativamente baja y es degenerada : es decir, muchos TCR reconocen el mismo péptido antigénico y muchos péptidos antigénicos son reconocidos por el mismo TCR. [2]
El TCR está compuesto por dos cadenas proteicas diferentes (es decir, es un heterodímero ). En humanos, en el 95% de las células T el TCR consta de una cadena alfa (α) y una cadena beta (β) (codificadas por TRA y TRB , respectivamente), mientras que en el 5% de las células T el TCR consta de gamma y delta. (γ/δ) cadenas (codificadas por TRG y TRD , respectivamente). Esta proporción cambia durante la ontogenia y en estados patológicos (como la leucemia ). También difiere entre especies. Se han cartografiado ortólogos de los 4 loci en varias especies. [3] [4] Cada locus puede producir una variedad de polipéptidos con regiones constantes y variables. [3]
Cuando el TCR se relaciona con el péptido antigénico y el MHC (péptido/MHC), el linfocito T se activa mediante transducción de señales , es decir, una serie de eventos bioquímicos mediados por enzimas asociadas, correceptores, moléculas adaptadoras especializadas y transcripción activada o liberada. factores . Según el mecanismo de activación inicial del receptor, el TCR pertenece a la familia de receptores fosforilados en tirosina (NTR) no catalíticos . [5]
En 1982, el premio Nobel James P. Allison descubrió por primera vez un epítopo de superficie de células T expresado clonalmente en el linfoma T murino. [6] En 1983, Ellis Reinherz definió por primera vez la estructura del receptor de células T humanas utilizando anticuerpos monoclonales antiidiotípicos contra clones de células T, complementados con estudios en ratones realizados por Philippa Marrack y John Kappler . [7] [8] Luego, Tak Wah Mak [9] y Mark M. Davis [10] identificaron los clones de ADNc que codifican el TCR humano y de ratón respectivamente en 1984. Estos hallazgos permitieron determinar la entidad y estructura del elusivo TCR, conocido antes. como el "Santo Grial de la Inmunología", por revelar. Esto permitió a científicos de todo el mundo realizar estudios sobre el TCR, lo que dio lugar a importantes estudios en los campos de CAR-T , inmunoterapia contra el cáncer e inhibición de puntos de control .
El TCR es una proteína heterodimérica anclada a una membrana con enlaces disulfuro que normalmente consta de cadenas alfa (α) y beta (β) altamente variables expresadas como parte de un complejo con las moléculas de cadena CD3 invariantes . Las células T que expresan este receptor se denominan células T α:β (o αβ), aunque una minoría de células T expresan un receptor alternativo, formado por cadenas variables gamma (γ) y delta (δ), denominadas células T γδ . [11]
Cada cadena está compuesta por dos dominios extracelulares: una región variable (V) y una región constante (C), ambas de dominio de la superfamilia de inmunoglobulinas (IgSF) que forman láminas β antiparalelas . La región constante está proximal a la membrana celular, seguida de una región transmembrana y una cola citoplasmática corta, mientras que la región variable se une al complejo péptido/MHC.
El dominio variable tanto de la cadena α como de la cadena β de TCR tiene cada uno tres regiones hipervariables o determinantes de la complementariedad (CDR). También hay un área adicional de hipervariabilidad en la cadena β (HV4) que normalmente no entra en contacto con el antígeno y, por lo tanto, no se considera una CDR. [ cita necesaria ]
Los residuos en estos dominios variables se encuentran en dos regiones del TCR, en la interfaz de las cadenas α y β y en la región estructural de la cadena β que se cree que está próxima al complejo de transducción de señales CD3. [12] La CDR3 es la principal CDR responsable de reconocer el antígeno procesado , aunque también se ha demostrado que la CDR1 de la cadena alfa interactúa con la parte N-terminal del péptido antigénico, mientras que la CDR1 de la cadena β interactúa con la parte C-terminal. parte del péptido.
Se cree que CDR2 reconoce el MHC. No se cree que el HV4 de la cadena β participe en el reconocimiento de antígenos como en las CDR clásicas, pero se ha demostrado que interactúa con superantígenos . [13]
El dominio constante del TCR consta de secuencias de conexión cortas en las que un residuo de cisteína forma enlaces disulfuro, que forman un vínculo entre las dos cadenas.
El TCR es un miembro de la superfamilia de las inmunoglobulinas, un gran grupo de proteínas implicadas en la unión, el reconocimiento y la adhesión; la familia lleva el nombre de anticuerpos (también llamados inmunoglobulinas). El TCR es similar a un medio anticuerpo que consta de una única cadena pesada y una única cadena ligera, excepto que la cadena pesada no tiene su fracción cristalizable (Fc). Las dos subunidades principales del TCR (cadenas α y β) están entrelazadas. Se requieren las subunidades CD3 y zeta para llevar a cabo la transducción de señales. La interacción MHC-TCR-CD3 para las células T es funcionalmente similar a la interacción antígeno (Ag) -inmunoglobulina (Ig) -FcR para los leucocitos mieloides y a la interacción Ag-Ig-CD79 para las células B.
La generación de diversidad de TCR es similar a la de los anticuerpos y los receptores de antígenos de células B. Surge principalmente de la recombinación genética de los segmentos codificados por ADN en células T somáticas individuales mediante recombinación somática V(D)J utilizando recombinasas RAG1 y RAG2 . Sin embargo, a diferencia de las inmunoglobulinas , los genes TCR no sufren hipermutación somática y las células T no expresan citidina desaminasa inducida por activación (AID). El proceso de recombinación que crea diversidad en BCR ( anticuerpos ) y TCR es exclusivo de los linfocitos (células T y B) durante las primeras etapas de su desarrollo en los órganos linfoides primarios ( timo para las células T, médula ósea para las células B).
Cada TCR recombinado posee una especificidad antigénica única , determinada por la estructura del sitio de unión al antígeno formado por las cadenas α y β en el caso de las células T αβ o las cadenas γ y δ en el caso de las células T γδ. [14]
La intersección de estas regiones específicas (V y J para la cadena alfa o gamma; V, D y J para la cadena beta o delta) corresponde a la región CDR3 que es importante para el reconocimiento de péptido/MHC (ver arriba).
Es la combinación única de los segmentos en esta región, junto con adiciones palindrómicas y aleatorias de nucleótidos (denominadas respectivamente "P-" y "N-"), lo que explica la diversidad aún mayor de la especificidad del receptor de células T por los péptidos antigénicos procesados. .
Más adelante durante el desarrollo, los bucles CDR individuales de TCR se pueden reeditar en la periferia fuera del timo mediante la reactivación de recombinasas utilizando un proceso denominado revisión (edición) de TCR y cambiar su especificidad antigénica.
En la membrana plasmática, las cadenas α y β del receptor TCR se asocian con seis proteínas adaptadoras adicionales para formar un complejo octamérico. El complejo contiene cadenas α y β, que forman el sitio de unión del ligando, y los módulos de señalización CD3 δ, CD3γ, CD3ε y CD3ζ en la estequiometría TCR α β - CD3εγ - CD3εδ - CD3ζζ. Los residuos cargados en el dominio transmembrana de cada subunidad forman interacciones polares permitiendo un ensamblaje correcto y estable del complejo. [15] La cola citoplasmática del TCR es muy corta, por lo que las proteínas adaptadoras CD3 que contienen los motivos de señalización son necesarias para propagar la señal desde el TCR activado hacia la célula.
Los motivos de señalización implicados en la señalización de TCR son residuos de tirosina en la cola citoplasmática de estas proteínas adaptadoras que pueden fosforilarse en caso de unión de TCR-pMHC. Los residuos de tirosina residen en una secuencia de aminoácidos específica de la firma Yxx(L/I)x6-8Yxx(L/I), donde Y, L, I indican residuos de tirosina, leucina e isoleucina, x denota cualquier aminoácido, el subíndice 6-8 indica una secuencia de 6 a 8 aminoácidos de longitud. Este motivo es muy común en los receptores activadores de la familia de receptores fosforilados de tirosina (NTR) no catalíticos y se denomina motivo de activación basado en tirosina de inmunorreceptores (ITAM). [5] CD3δ, CD3γ y CD3ε contienen cada uno un único ITAM, mientras que CD3ζ contiene tres ITAM. En total el complejo TCR contiene 10 ITAM. [15] Los ITAM fosforilados actúan como sitio de unión para los dominios SH2 de proteínas reclutadas adicionalmente.

Cada célula T expresa TCR clonales que reconocen un péptido específico cargado en una molécula de MHC (pMHC), ya sea en el MHC de clase II en la superficie de las células presentadoras de antígenos o en el MHC de clase I en cualquier otro tipo de célula. [16] Una característica única de las células T es su capacidad para discriminar entre péptidos derivados de células endógenas sanas y péptidos de células extrañas o anormales (por ejemplo, infectadas o cancerosas) en el cuerpo. [17] Las células presentadoras de antígenos no discriminan entre péptidos propios y extraños y típicamente expresan una gran cantidad de pMHC propios en su superficie celular y solo unas pocas copias de cualquier pMHC extraño. Por ejemplo, las células infectadas con VIH tienen sólo entre 8 y 46 pMHC específicos del VIH, en comparación con un total de 100.000 pMHC por célula. [18] [19]
Debido a que las células T se someten a una selección positiva en el timo, existe una afinidad no despreciable entre el propio pMHC y el TCR. Sin embargo, la señalización del receptor de células T no debe ser activada por el propio pMHC, de modo que las células T endógenas y sanas sean ignoradas. Sin embargo, cuando estas mismas células contienen incluso cantidades mínimas de pMHC derivado de patógenos, las células T deben activarse e iniciar respuestas inmunes. La capacidad de las células T de ignorar las células sanas pero responder cuando estas mismas células expresan una pequeña cantidad de pMHC extraños se conoce como discriminación de antígenos. [20] [21]
Para ello, las células T tienen un grado muy alto de especificidad antigénica, a pesar de que la afinidad por el ligando péptido/MHC es bastante baja en comparación con otros tipos de receptores. [22] La afinidad, dada como la constante de disociación ( K d ), entre un TCR y un pMHC se determinó mediante resonancia de plasmón superficial (SPR) en el rango de 1 a 100 μM, con una tasa de asociación ( k on ) de 1000 -10000 M −1 s −1 y una tasa de disociación ( k off ) de 0,01 -0,1 s −1 . [23] En comparación, las citocinas tienen una afinidad de KD = 10–600 pM por su receptor. [24] Se ha demostrado que incluso un solo cambio de aminoácido en el péptido presentado que afecte la afinidad del pMHC por el TCR reduce la respuesta de las células T y no puede compensarse con una concentración más alta de pMHC. [25] Se ha observado una correlación negativa entre la tasa de disociación del complejo pMHC-TCR y la fuerza de la respuesta de las células T. [26] Eso significa que el pMHC que se une al TCR durante más tiempo inicia una activación más fuerte de la célula T. Además, las células T son muy sensibles; la interacción con un solo pMHC es suficiente para desencadenar la activación. [27] Las células T pasan rápidamente de los antígenos que no desencadenan respuestas, escaneando rápidamente el pMHC en una célula presentadora de antígeno (APC) para aumentar las posibilidades de encontrar un pMHC específico. En promedio, una célula T encuentra 20 APC por hora. [28]
Se han propuesto diferentes modelos de los mecanismos moleculares que subyacen a este proceso altamente específico y sensible de discriminación de antígenos. El modelo ocupacional simplemente sugiere que la respuesta del TCR es proporcional al número de pMHC unidos al receptor. Dado este modelo, una vida útil más corta de un péptido puede compensarse con una concentración más alta, de modo que la respuesta máxima de la célula T siga siendo la misma. Sin embargo, esto no se puede comprobar en los experimentos y el modelo ha sido ampliamente rechazado. [26] La opinión más aceptada es que el TCR se dedica a la corrección cinética. El modelo de corrección cinética propone que no se produce una señal directamente tras la vinculación, sino que una serie de pasos intermedios garantizan un retraso de tiempo entre la vinculación y la salida de la señal. Estos pasos intermedios de "corrección" pueden consistir en múltiples rondas de fosforilación de tirosina. Estos pasos requieren energía y, por lo tanto, no ocurren espontáneamente, sólo cuando el receptor está unido a su ligando. De esta manera, sólo los ligandos con alta afinidad que se unen al TCR durante un tiempo suficientemente largo pueden iniciar una señal. Todos los pasos intermedios son reversibles, de modo que tras la disociación del ligando, el receptor vuelve a su estado original no fosforilado antes de que se una un nuevo ligando. [29] Este modelo predice que la respuesta máxima de las células T disminuye para el pMHC con una vida útil más corta. Los experimentos han confirmado este modelo. [26] Sin embargo, el modelo básico de corrección cinética tiene un equilibrio entre sensibilidad y especificidad. Aumentar el número de pasos de revisión aumenta la especificidad pero reduce la sensibilidad del receptor. Por tanto, el modelo no es suficiente para explicar la alta sensibilidad y especificidad de los TCR que se han observado. (Altan Bonnet2005) Se han propuesto múltiples modelos que amplían el modelo de corrección cinética, pero la evidencia de los modelos aún es controvertida. [17] [30] [31]
La sensibilidad al antígeno es mayor en las células T experimentadas con antígenos que en las células T vírgenes. Las células T vírgenes pasan por el proceso de maduración por avidez funcional sin cambios en la afinidad. Se basa en el hecho de que las células T efectoras y de memoria (experimentadas con antígenos) dependen menos de señales coestimuladoras y tienen una mayor concentración de antígeno que las células T vírgenes. [32]
La función esencial del complejo TCR es identificar un antígeno unido específico derivado de un patógeno potencialmente dañino y provocar una respuesta distinta y crítica. Al mismo tiempo, debe ignorar cualquier autoantígeno y tolerar antígenos inofensivos, como los antígenos alimentarios. El mecanismo de transducción de señales mediante el cual una célula T provoca esta respuesta al entrar en contacto con su antígeno único se denomina activación de células T. Al unirse al pMHC, el TCR inicia una cascada de señalización que implica la activación del factor de transcripción y la remodelación del citoesqueleto que da como resultado la activación de las células T. Las células T activas secretan citoquinas, experimentan una rápida proliferación, tienen actividad citotóxica y se diferencian en células efectoras y de memoria. Cuando se activa el TCR, las células T forman una sinapsis inmunológica que les permite permanecer en contacto con la célula presentadora del antígeno durante varias horas. [33] A nivel poblacional, la activación de las células T depende de la fuerza de la estimulación del TCR; la curva dosis-respuesta del ligando a la producción de citoquinas es sigmoidea. Sin embargo, la activación de las células T a nivel de una sola célula se puede caracterizar por una respuesta similar a un interruptor digital, lo que significa que la célula T se activa completamente si el estímulo es superior a un umbral determinado; de lo contrario, la célula T permanece en su estado no activado. No existe un estado de activación intermedio. La curva dosis-respuesta sigmoidea robusta a nivel de población se debe a que las células T individuales tienen umbrales ligeramente diferentes. [25]
Las células T necesitan tres señales para activarse por completo. La señal 1 la proporciona el receptor de células T cuando reconoce un antígeno específico en una molécula de MHC. La señal 2 proviene de receptores coestimuladores de las células T, como CD28 , y se activa mediante ligandos presentados en la superficie de otras células inmunitarias, como CD80 y CD86. Estos receptores coestimuladores se expresan sólo cuando el sistema inmunológico innato detecta una infección o un estímulo inflamatorio, lo que se conoce como "señal de peligro". Este sistema de dos señales garantiza que las células T sólo respondan a estímulos dañinos (es decir, patógenos o lesiones) y no a autoantígenos. Una tercera señal adicional la proporcionan las citocinas , que regulan la diferenciación de las células T en diferentes subconjuntos de células T efectoras. [33] Hay una gran cantidad de moléculas involucradas en el complejo proceso bioquímico (llamado señalización transmembrana ) mediante el cual se produce la activación de las células T. A continuación se describe detalladamente la cascada de señalización.
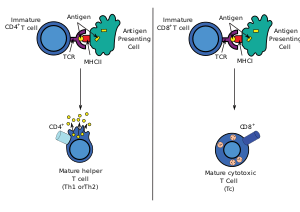
La activación inicial sigue el mecanismo común a todos los miembros de la familia de receptores NTR . Una vez que el TCR se une a un pMHC específico, los residuos de tirosina de los motivos de activación basados en tirosina del inmunorreceptor (ITAM) en sus proteínas adaptadoras CD3 se fosforilan. Los residuos sirven como sitios de acoplamiento para moléculas de señalización posteriores, que pueden propagar la señal. [34] [35] La fosforilación de ITAM está mediada por la Src quinasa Lck . Lck se ancla a la membrana plasmática asociándose con el correceptor CD4 o CD8 , según el subtipo de célula T. CD4 se expresa en células T colaboradoras y células T reguladoras , y es específico para MHC clase II . El CD8, en cambio, específico del MHC de clase I , se expresa en las células T citotóxicas . La unión del correceptor al MHC acerca a Lck a los ITAM CD3. Se ha demostrado que el 40% de la Lck está activa incluso antes de que el TCR se una al pMHC y, por tanto, tiene la capacidad de fosforilar constantemente el TCR. [36] La señalización tónica de TCR se evita mediante la presencia de fosfatasa CD45 que elimina la fosforilación de los residuos de tirosina e inhibe el inicio de la señal. Al unirse, el equilibrio de la actividad quinasa con la actividad fosfatasa se altera, lo que lleva a un exceso de fosforilación y al inicio de la señal. Aún se debate cómo se logra tal perturbación mediante la unión de TCR. Se han sugerido mecanismos que implican cambio conformacional de TCR, agregación de TCR y segregación cinética . [34] La tirosina quinasa Fyn podría estar involucrada en la fosforilación de ITAM, pero no es esencial para la señalización de TCR. [37] [38]
Los ITAM fosforilados en las colas citoplasmáticas de CD3 reclutan la proteína tirosina quinasa Zap70 que puede unirse a los residuos de tirosina fosforilados con su dominio SH2 . Esto acerca a Zap70 a Lck, lo que da como resultado su fosforilación y activación por Lck. [39] Lck fosforila varias proteínas diferentes en la vía TCR. [40] Una vez activado, Zap70 es capaz de fosforilar múltiples residuos de tirosina de la proteína transmembrana LAT . LAT es una proteína de andamio asociada con la membrana. En sí mismo no tiene ninguna actividad catalítica, pero proporciona sitios de unión para moléculas de señalización a través de residuos de tirosina fosforilados. LAT se asocia con otra proteína de andamiaje Slp-76 a través de la proteína adaptadora Grap2 , que proporciona sitios de unión adicionales. Juntos, LAT y Slp-76 proporcionan una plataforma para el reclutamiento de muchas moléculas de señalización posteriores. Al acercar estas moléculas de señalización, pueden ser activadas por Lck, Zap70 y otras quinasas. Por tanto, el complejo LAT/Slp76 actúa como un signalosoma altamente cooperativo. [39]
Las moléculas que se unen al complejo LAT/Slp76 incluyen: fosfolipasa C γ1 (PLCγ1), SOS mediante un adaptador Grb2 , Itk , Vav , Nck1 y Fyb . [39]
PLCγ es una enzima muy importante en la vía ya que genera moléculas de segundo mensajero . Es activado por la tirosina quinasa Itk, que se recluta en la membrana celular uniéndose al fosfatidilinositol (3,4,5)-trifosfato (PIP3). PIP3 se produce por la acción de la fosfoinositida 3-quinasa (PI-3K), que fosforila el fosfatidilinositol 4,5-bisfosfato (PIP2) para producir PIP3. No se sabe que PI-3K sea activado por el propio receptor de células T, pero hay evidencia de que CD28, un receptor coestimulador que proporciona la segunda señal, es capaz de activar PI-3K. La interacción entre PLCγ, Itk y PI-3K podría ser el punto del camino donde se integran la primera y la segunda señal. Sólo si ambas señales están presentes se activa PLCγ. [33] Una vez que PLCγ se activa por fosforilación. Hidroliza PIP2 en dos moléculas mensajeras secundarias , a saber, el diacilglicerol (DAG) unido a la membrana y el inositol 1,4,5-trifosfato soluble (IP3). [41]
Estas moléculas de segundo mensajero amplifican la señal de TCR y distribuyen la activación localizada previa a toda la célula y activan cascadas de proteínas que finalmente conducen a la activación de factores de transcripción . Los factores de transcripción implicados en la vía de señalización de las células T son NFAT , NF-κB y AP1 , un heterodímero de las proteínas Fos y Jun . Los tres factores de transcripción son necesarios para activar la transcripción del gen de la interleucina-2 (IL2). [33]
La activación de NFAT depende de la señalización del calcio . El IP3 producido por PLC-γ ya no está unido a la membrana y se difunde rápidamente en la célula. La unión de IP3 a los receptores de los canales de calcio en el retículo endoplásmico (RE) induce la liberación de calcio (Ca 2+ ) en el citosol. La baja concentración de Ca 2+ resultante en el ER provoca la agrupación de STIM1 en la membrana del ER, lo que a su vez conduce a la activación de los canales CRAC de la membrana celular que permiten que fluya calcio adicional hacia el citosol desde el espacio extracelular. Por lo tanto, los niveles de Ca 2+ aumentan considerablemente en las células T. Este calcio citosólico se une a la calmodulina , induciendo un cambio conformacional de la proteína de modo que luego puede unirse y activar la calcineurina . La calcineurina, a su vez, desfosforila el NFAT. En su estado desactivado, NFAT no puede ingresar al núcleo ya que los transportadores nucleares no pueden reconocer su secuencia de localización nuclear (NLS) debido a la fosforilación por GSK-3 . Cuando se desfosforila con calcineurina, es posible la translocación de NFAT al núcleo. [33] Además, existe evidencia de que PI-3K a través de moléculas señal recluta la proteína quinasa AKT a la membrana celular. AKT es capaz de desactivar GSK3 y así inhibir la fosforilación de NFAT, lo que podría contribuir a la activación de NFAT. [39]
La activación de NF-κB es iniciada por DAG, el segundo producto unido a la membrana de la hidrolización de PLCγ de PIP2. DAG se une y recluta la proteína quinasa C θ (PKCθ) a la membrana, donde puede activar la proteína de andamio CARMA1 unida a la membrana . CARMA1 luego sufre un cambio conformacional que le permite oligomerizarse y unirse a las proteínas adaptadoras BCL10 , el dominio CARD y MALT1 . Este complejo de múltiples subunidades se une a la ubiquitina ligasa TRAF6 . La ubiquitinación de TRAF6 sirve como andamio para reclutar NEMO , IκB quinasa (IKK) y TAK1 . [33] TAK 1 fosforila IKK, que a su vez fosforila el inhibidor de NF-κB I-κB , lo que lleva a la ubiquitinación y posterior degradación de I-κB. I-κB bloquea el NLS de NF-κB impidiendo así su translocación al núcleo. Una vez que I-κB se degrada, no puede unirse a NF-κB y el NLS de NF-κB se vuelve accesible para la translocación nuclear. [33]
La activación de AP1 implica tres vías de señalización MAPK . Estas vías utilizan una cascada de fosforilación de tres proteínas quinasas de acción sucesiva para transmitir una señal. Las tres vías MAPK en las células T involucran quinasas de diferentes especificidades que pertenecen a cada una de las familias MAP3K , MAP2K y MAPK . La activación inicial la realiza la GTPasa Ras o Rac que fosforilan el MAP3K. [33] Una cascada que involucra las enzimas Raf , MEK1 , ERK da como resultado la fosforilación de Jun, el cambio conformacional permite que Jun se una a Fos y, por lo tanto, se forme AP-1. AP-1 actúa entonces como factor de transcripción. Raf se activa a través del segundo mensajero DAG, SOS y Ras. DAG recluta, entre otras proteínas, la proteína liberadora de nucleótidos de guanilo RAS ( RasGRP ), un factor de intercambio de nucleótidos de guanina (GEF), a la membrana. RasGRP activa la pequeña GTPasa Ras mediante el intercambio de guanosina difosfato (GDP) unido a Ras por guanosina trifosfato (GTP). Ras también puede ser activado por el factor de intercambio de nucleótidos de guanina SOS que se une al señalosoma LAT. Luego, Ras inicia la cascada MAPK. [39] La segunda cascada MAPK con MEKK1 , JNKK, JNK induce la expresión de proteínas de Jun. Otra cascada, que también involucra a MEKK1 como MAPK3, pero luego activa MKK3 /6 y p38 induce la transcripción de Fos. La activación de MEKK1, además de ser activada por Ras, implica que Slp-76 reclute GEF Vav en el signalosoma LAT, que luego activa la GTPasa Rac. Rac y Ras activan MEKK1 y así inician la cascada MAPK. [39]