
Las enzimas ( / ˈɛ n z aɪ m z / ) son proteínas que actúan como catalizadores biológicos acelerando reacciones químicas . Las moléculas sobre las que pueden actuar las enzimas se denominan sustratos , y la enzima convierte los sustratos en diferentes moléculas conocidas como productos . Casi todos los procesos metabólicos en la célula necesitan catálisis enzimática para ocurrir a un ritmo lo suficientemente rápido como para sustentar la vida. [1] : 8.1 Las vías metabólicas dependen de enzimas para catalizar pasos individuales. El estudio de las enzimas se llama enzimología y el campo del análisis de pseudoenzimas reconoce que durante la evolución, algunas enzimas han perdido la capacidad de llevar a cabo catálisis biológica, lo que a menudo se refleja en sus secuencias de aminoácidos y sus inusuales propiedades "pseudocatalíticas". [2] [3]
Se sabe que las enzimas catalizan más de 5.000 tipos de reacciones bioquímicas. [4]
Otros biocatalizadores son moléculas catalíticas de ARN , también llamadas ribozimas . A veces se describen como un tipo de enzima en lugar de ser como una enzima, pero incluso en las décadas transcurridas desde el descubrimiento de las ribozimas en 1980-1982, la palabra enzima por sí sola a menudo significa específicamente el tipo de proteína (como se usa en este artículo).
La especificidad de una enzima proviene de su estructura tridimensional única .
Como todos los catalizadores, las enzimas aumentan la velocidad de reacción al reducir su energía de activación . Algunas enzimas pueden hacer que la conversión de sustrato en producto ocurra millones de veces más rápido. Un ejemplo extremo es la orotidina 5'-fosfato descarboxilasa , que permite que se produzca en milisegundos una reacción que de otro modo tardaría millones de años. [5] [6] Químicamente, las enzimas son como cualquier catalizador y no se consumen en reacciones químicas, ni alteran el equilibrio de una reacción. Las enzimas se diferencian de la mayoría de los demás catalizadores por ser mucho más específicas. La actividad enzimática puede verse afectada por otras moléculas: los inhibidores son moléculas que disminuyen la actividad enzimática y los activadores son moléculas que aumentan la actividad. Muchos fármacos terapéuticos y venenos son inhibidores de enzimas. La actividad de una enzima disminuye notablemente fuera de su temperatura y pH óptimos , y muchas enzimas se desnaturalizan (permanentemente) cuando se exponen a un calor excesivo, perdiendo su estructura y propiedades catalíticas.
Algunas enzimas se utilizan comercialmente, por ejemplo, en la síntesis de antibióticos . Algunos productos domésticos utilizan enzimas para acelerar las reacciones químicas: las enzimas de los detergentes biológicos descomponen las proteínas, el almidón o las manchas de grasa de la ropa, y las enzimas de los ablandadores de carne descomponen las proteínas en moléculas más pequeñas, lo que hace que la carne sea más fácil de masticar.

A finales del siglo XVII y principios del XVIII, se conocía la digestión de la carne mediante secreciones estomacales [7] y la conversión de almidón en azúcares mediante extractos de plantas y saliva , pero no se habían identificado los mecanismos por los cuales ocurrían. [8]
El químico francés Anselme Payen fue el primero en descubrir una enzima, la diastasa , en 1833. [9] Unas décadas más tarde, al estudiar la fermentación del azúcar a alcohol por la levadura , Louis Pasteur concluyó que esta fermentación era causada por una fuerza vital contenida dentro las células de levadura llamadas "fermentos", que se pensaba que funcionaban sólo dentro de organismos vivos. Escribió que "la fermentación alcohólica es un acto correlacionado con la vida y organización de las células de levadura, no con la muerte o putrefacción de las células". [10]
En 1877, el fisiólogo alemán Wilhelm Kühne (1837-1900) utilizó por primera vez el término enzima , que proviene del griego antiguo ἔνζυμον (énzymon) ' levadura , en levadura', para describir este proceso. [11] La palabra enzima se usó más tarde para referirse a sustancias no vivas como la pepsina , y la palabra fermento se usó para referirse a la actividad química producida por organismos vivos. [12]
Eduard Buchner presentó su primer artículo sobre el estudio de extractos de levadura en 1897. En una serie de experimentos en la Universidad de Berlín , descubrió que el azúcar era fermentado por extractos de levadura incluso cuando no había células de levadura vivas en la mezcla. [13] Llamó a la enzima que provocaba la fermentación de la sacarosa " zimasa ". [14] En 1907, recibió el Premio Nobel de Química por "su descubrimiento de la fermentación libre de células". Siguiendo el ejemplo de Buchner, las enzimas suelen denominarse según la reacción que realizan: el sufijo -asa se combina con el nombre del sustrato ( p. ej., la lactasa es la enzima que escinde la lactosa ) o con el tipo de reacción (p. ej., ADN polimerasa forma polímeros de ADN). [15]
La identidad bioquímica de las enzimas aún era desconocida a principios del siglo XX. Muchos científicos observaron que la actividad enzimática estaba asociada con las proteínas, pero otros (como el premio Nobel Richard Willstätter ) argumentaron que las proteínas eran meros portadores de las verdaderas enzimas y que las proteínas per se eran incapaces de catálisis. [16] En 1926, James B. Sumner demostró que la enzima ureasa era una proteína pura y la cristalizó; hizo lo mismo con la enzima catalasa en 1937. La conclusión de que las proteínas puras pueden ser enzimas fue demostrada definitivamente por John Howard Northrop y Wendell Meredith Stanley , quienes trabajaron con las enzimas digestivas pepsina (1930), tripsina y quimotripsina . Estos tres científicos recibieron el Premio Nobel de Química en 1946. [17]
El descubrimiento de que las enzimas podían cristalizarse permitió finalmente resolver sus estructuras mediante cristalografía de rayos X. Esto se hizo por primera vez con la lisozima , una enzima que se encuentra en las lágrimas, la saliva y las claras de huevo y que digiere la capa de algunas bacterias; la estructura fue resuelta por un grupo dirigido por David Chilton Phillips y publicada en 1965. [18] Esta estructura de alta resolución de la lisozima marcó el comienzo del campo de la biología estructural y el esfuerzo por comprender cómo funcionan las enzimas a un nivel atómico de detalle. . [19]
Las enzimas se pueden clasificar según dos criterios principales: similitud de secuencia de aminoácidos (y, por tanto, relación evolutiva) o actividad enzimática.
Actividad enzimática . El nombre de una enzima a menudo se deriva de su sustrato o de la reacción química que cataliza, y la palabra termina en -ase . [1] : 8.1.3 Ejemplos son lactasa , alcohol deshidrogenasa y ADN polimerasa . Las diferentes enzimas que catalizan una misma reacción química se denominan isozimas . [1] : 10,3
La Unión Internacional de Bioquímica y Biología Molecular ha desarrollado una nomenclatura para las enzimas, los números CE (para "Comisión de Enzimas") . Cada enzima se describe mediante "EC" seguida de una secuencia de cuatro números que representan la jerarquía de actividad enzimática (de muy general a muy específica). Es decir, el primer número clasifica ampliamente la enzima según su mecanismo, mientras que los otros dígitos añaden cada vez más especificidad. [20]
La clasificación de nivel superior es:
Estas secciones se subdividen por otras características como el sustrato, los productos y el mecanismo químico . Una enzima se especifica completamente mediante cuatro designaciones numéricas. Por ejemplo, la hexoquinasa (EC 2.7.1.1) es una transferasa (EC 2) que agrega un grupo fosfato (EC 2.7) a un azúcar hexosa, una molécula que contiene un grupo alcohol (EC 2.7.1). [21]
Similitud de secuencia . Las categorías CE no reflejan similitud de secuencia. Por ejemplo, dos ligasas del mismo número de EC que catalizan exactamente la misma reacción pueden tener secuencias completamente diferentes. Independientemente de su función, las enzimas, como cualquier otra proteína, se han clasificado según su similitud de secuencia en numerosas familias. Estas familias han sido documentadas en docenas de bases de datos de proteínas y familias de proteínas diferentes, como Pfam . [22]
Enzimas isofuncionales no homólogas . Las enzimas no relacionadas que tienen la misma actividad enzimática han sido denominadas enzimas isofuncionales no homólogas . [23] La transferencia horizontal de genes puede propagar estos genes a especies no relacionadas, especialmente bacterias, donde pueden reemplazar genes endógenos de la misma función, lo que lleva al desplazamiento de genes homólogos.

Las enzimas son generalmente proteínas globulares que actúan solas o en complejos más grandes . La secuencia de aminoácidos especifica la estructura que a su vez determina la actividad catalítica de la enzima. [24] Aunque la estructura determina la función, todavía no se puede predecir una nueva actividad enzimática a partir de la estructura únicamente. [25] Las estructuras enzimáticas se desarrollan ( desnaturalizan ) cuando se calientan o se exponen a desnaturalizantes químicos y esta alteración de la estructura normalmente provoca una pérdida de actividad. [26] La desnaturalización de la enzima normalmente está relacionada con temperaturas superiores al nivel normal de una especie; Como resultado, los usuarios industriales valoran las enzimas de las bacterias que viven en entornos volcánicos, como las aguas termales, por su capacidad para funcionar a altas temperaturas, lo que permite que las reacciones catalizadas por enzimas funcionen a un ritmo muy alto.
Las enzimas suelen ser mucho más grandes que sus sustratos. Los tamaños varían desde sólo 62 residuos de aminoácidos, para el monómero de la 4-oxalocrotonato tautomerasa , [27] hasta más de 2500 residuos en la ácido graso sintasa animal . [28] Sólo una pequeña porción de su estructura (alrededor de 2 a 4 aminoácidos) está directamente involucrada en la catálisis: el sitio catalítico. [29] Este sitio catalítico está ubicado junto a uno o más sitios de unión donde los residuos orientan los sustratos. El sitio catalítico y el sitio de unión juntos componen el sitio activo de la enzima . La mayoría restante de la estructura enzimática sirve para mantener la orientación y dinámica precisas del sitio activo. [30]
En algunas enzimas, ningún aminoácido participa directamente en la catálisis; en cambio, la enzima contiene sitios para unirse y orientar cofactores catalíticos . [30] Las estructuras enzimáticas también pueden contener sitios alostéricos donde la unión de una molécula pequeña provoca un cambio conformacional que aumenta o disminuye la actividad. [31]
Existe una pequeña cantidad de catalizadores biológicos basados en ARN llamados ribozimas , que a su vez pueden actuar solos o en complejo con proteínas. El más común de ellos es el ribosoma , que es un complejo de proteínas y componentes catalíticos de ARN. [1] : 2.2
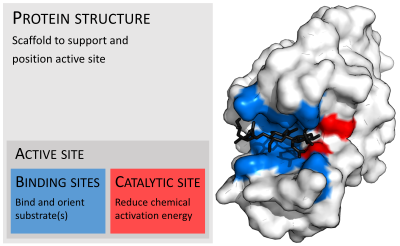
Las enzimas deben unirse a sus sustratos antes de poder catalizar cualquier reacción química. Las enzimas suelen ser muy específicas en cuanto a los sustratos a los que se unen y luego catalizan la reacción química. La especificidad se logra uniendo bolsas con forma, carga y características hidrófilas / hidrófobas complementarias a los sustratos. Por lo tanto, las enzimas pueden distinguir entre moléculas de sustrato muy similares para ser quimioselectivas , regioselectivas y estereoespecíficas . [32]
Algunas de las enzimas que muestran la mayor especificidad y precisión están involucradas en la copia y expresión del genoma . Algunas de estas enzimas tienen mecanismos de " corrección de pruebas ". En este caso, una enzima como la ADN polimerasa cataliza una reacción en un primer paso y luego comprueba que el producto sea correcto en un segundo paso. [33] Este proceso de dos pasos da como resultado tasas de error promedio de menos de 1 error en 100 millones de reacciones en polimerasas de mamíferos de alta fidelidad. [1] : 5.3.1 También se encuentran mecanismos de corrección similares en la ARN polimerasa , [34] aminoacil tRNA sintetasas [35] y los ribosomas . [36]
Por el contrario, algunas enzimas muestran promiscuidad enzimática , tienen una amplia especificidad y actúan sobre una variedad de diferentes sustratos fisiológicamente relevantes. Muchas enzimas poseen pequeñas actividades secundarias que surgieron de forma fortuita (es decir, de forma neutra ), que pueden ser el punto de partida para la selección evolutiva de una nueva función. [37] [38]
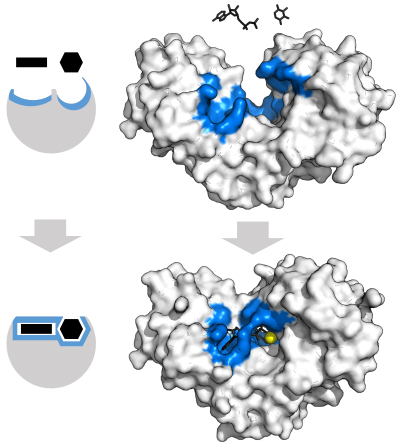
Para explicar la especificidad observada de las enzimas, en 1894 Emil Fischer propuso que tanto la enzima como el sustrato poseen formas geométricas complementarias específicas que encajan exactamente entre sí. [39] Esto a menudo se conoce como el modelo de "cerradura y llave". [1] : 8.3.2 Este modelo inicial explica la especificidad de la enzima, pero no explica la estabilización del estado de transición que alcanzan las enzimas. [40]
En 1958, Daniel Koshland sugirió una modificación al modelo de cerradura y llave: dado que las enzimas son estructuras bastante flexibles, el sitio activo se remodela continuamente mediante interacciones con el sustrato a medida que el sustrato interactúa con la enzima. [41] Como resultado, el sustrato no se une simplemente a un sitio activo rígido; las cadenas laterales de aminoácidos que forman el sitio activo se moldean en las posiciones precisas que permiten a la enzima realizar su función catalítica. En algunos casos, como en el caso de las glicosidasas , la molécula sustrato también cambia ligeramente de forma al entrar en el sitio activo. [42] El sitio activo continúa cambiando hasta que el sustrato está completamente unido, momento en el cual se determina la forma final y la distribución de carga. [43] El ajuste inducido puede mejorar la fidelidad del reconocimiento molecular en presencia de competencia y ruido a través del mecanismo de corrección conformacional . [44]
Las enzimas pueden acelerar las reacciones de varias maneras, todas las cuales reducen la energía de activación (ΔG ‡ , energía libre de Gibbs ) [45]
Las enzimas pueden utilizar varios de estos mecanismos simultáneamente. Por ejemplo, las proteasas como la tripsina realizan catálisis covalente usando una tríada catalítica , estabilizan la acumulación de carga en los estados de transición usando un agujero de oxianión y completan la hidrólisis usando un sustrato de agua orientado. [51]
Las enzimas no son estructuras rígidas y estáticas; en cambio, tienen movimientos dinámicos internos complejos, es decir, movimientos de partes de la estructura de la enzima, como residuos de aminoácidos individuales, grupos de residuos que forman un bucle proteico o una unidad de estructura secundaria , o incluso un dominio proteico completo . Estos movimientos dan lugar a un conjunto conformacional de estructuras ligeramente diferentes que se interconvierten entre sí en equilibrio . Diferentes estados dentro de este conjunto pueden estar asociados con diferentes aspectos de la función de una enzima. Por ejemplo, diferentes conformaciones de la enzima dihidrofolato reductasa están asociadas con los pasos de unión del sustrato, catálisis, liberación de cofactor y liberación de producto del ciclo catalítico, [52] de acuerdo con la teoría de la resonancia catalítica .
La presentación de sustrato es un proceso en el que la enzima se secuestra de su sustrato. Las enzimas pueden ser secuestradas en la membrana plasmática lejos de un sustrato en el núcleo o el citosol. O dentro de la membrana, una enzima puede ser secuestrada en balsas de lípidos lejos de su sustrato en la región desordenada. Cuando se libera la enzima, se mezcla con su sustrato. Alternativamente, la enzima puede secuestrarse cerca de su sustrato para activarla. Por ejemplo, la enzima puede ser soluble y tras la activación unirse a un lípido en la membrana plasmática y luego actuar sobre las moléculas en la membrana plasmática.
Los sitios alostéricos son bolsas de la enzima, distintas del sitio activo, que se unen a moléculas en el entorno celular. Luego, estas moléculas provocan un cambio en la conformación o dinámica de la enzima que se transduce al sitio activo y, por lo tanto, afecta la velocidad de reacción de la enzima. [53] De esta manera, las interacciones alostéricas pueden inhibir o activar enzimas. Las interacciones alostéricas con metabolitos aguas arriba o aguas abajo en la vía metabólica de una enzima provocan una regulación por retroalimentación , alterando la actividad de la enzima de acuerdo con el flujo a través del resto de la vía. [54]

Algunas enzimas no necesitan componentes adicionales para mostrar actividad completa. Otros requieren que moléculas no proteicas llamadas cofactores se unan para activarse. [55] Los cofactores pueden ser compuestos inorgánicos (p. ej., iones metálicos y grupos hierro-azufre ) o orgánicos (p. ej., flavina y hemo ). Estos cofactores sirven para muchos propósitos; por ejemplo, los iones metálicos pueden ayudar a estabilizar especies nucleofílicas dentro del sitio activo. [56] Los cofactores orgánicos pueden ser coenzimas , que se liberan del sitio activo de la enzima durante la reacción, o grupos protésicos , que están estrechamente unidos a una enzima. Los grupos protésicos orgánicos pueden unirse covalentemente (p. ej., biotina en enzimas como la piruvato carboxilasa ). [57]
Un ejemplo de enzima que contiene un cofactor es la anhidrasa carbónica , que utiliza un cofactor de zinc unido como parte de su sitio activo. [58] Estos iones o moléculas estrechamente unidos generalmente se encuentran en el sitio activo y participan en la catálisis. [1] : 8.1.1 Por ejemplo, los cofactores flavina y hemo a menudo participan en reacciones redox . [1] : 17
Las enzimas que requieren un cofactor pero no tienen uno unido se llaman apoenzimas o apoproteínas . Una enzima junto con los cofactores necesarios para la actividad se denomina holoenzima (o haloenzima). El término holoenzima también se puede aplicar a enzimas que contienen múltiples subunidades proteicas, como las ADN polimerasas ; aquí la holoenzima es el complejo completo que contiene todas las subunidades necesarias para la actividad. [1] : 8.1.1
Las coenzimas son pequeñas moléculas orgánicas que pueden estar unidas débil o firmemente a una enzima. Las coenzimas transportan grupos químicos de una enzima a otra. [59] Los ejemplos incluyen NADH , NADPH y trifosfato de adenosina (ATP). Algunas coenzimas, como el mononucleótido de flavina (FMN), el dinucleótido de flavina y adenina (FAD), el pirofosfato de tiamina (TPP) y el tetrahidrofolato (THF), se derivan de vitaminas . Estas coenzimas no pueden ser sintetizadas por el cuerpo de novo y los compuestos estrechamente relacionados (vitaminas) deben adquirirse de la dieta. Los grupos químicos transportados incluyen:
Dado que las coenzimas cambian químicamente como consecuencia de la acción enzimática, es útil considerarlas como una clase especial de sustratos, o segundos sustratos, que son comunes a muchas enzimas diferentes. Por ejemplo, se sabe que alrededor de 1000 enzimas utilizan la coenzima NADH. [60]
Las coenzimas suelen regenerarse continuamente y sus concentraciones se mantienen a un nivel constante dentro de la célula. Por ejemplo, el NADPH se regenera a través de la vía de las pentosas fosfato y la S -adenosilmetionina por la metionina adenosiltransferasa . Esta regeneración continua permite utilizar pequeñas cantidades de coenzimas de forma muy intensiva. Por ejemplo, el cuerpo humano transforma su propio peso en ATP cada día. [61]
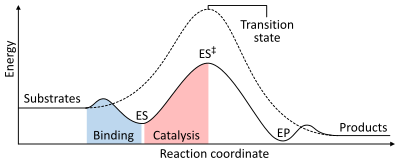
Como ocurre con todos los catalizadores, las enzimas no alteran la posición del equilibrio químico de la reacción. En presencia de una enzima, la reacción transcurre en la misma dirección que sin la enzima, sólo que más rápidamente. [1] : 8.2.3 Por ejemplo, la anhidrasa carbónica cataliza su reacción en cualquier dirección dependiendo de la concentración de sus reactivos: [62]
La velocidad de una reacción depende de la energía de activación necesaria para formar el estado de transición que luego se descompone en productos. Las enzimas aumentan la velocidad de reacción al reducir la energía del estado de transición. Primero, la unión forma un complejo enzima-sustrato (ES) de baja energía. En segundo lugar, la enzima estabiliza el estado de transición de modo que requiere menos energía para lograrlo en comparación con la reacción no catalizada (ES ‡ ). Finalmente, el complejo enzima-producto (EP) se disocia para liberar los productos. [1] : 8,3
Las enzimas pueden acoplar dos o más reacciones, de modo que una reacción termodinámicamente favorable puede usarse para "impulsar" una termodinámicamente desfavorable de modo que la energía combinada de los productos sea menor que la de los sustratos. Por ejemplo, la hidrólisis del ATP se utiliza a menudo para impulsar otras reacciones químicas. [63]
La cinética enzimática es la investigación de cómo las enzimas se unen a los sustratos y los convierten en productos. [64] Los datos de velocidad utilizados en los análisis cinéticos se obtienen comúnmente a partir de ensayos enzimáticos . En 1913, Leonor Michaelis y Maud Leonora Menten propusieron una teoría cuantitativa de la cinética enzimática, conocida como cinética de Michaelis-Menten . [65] La principal contribución de Michaelis y Menten fue pensar en reacciones enzimáticas en dos etapas. En el primero, el sustrato se une reversiblemente a la enzima, formando el complejo enzima-sustrato. A esto a veces se le llama complejo Michaelis-Menten en su honor. Luego, la enzima cataliza el paso químico de la reacción y libera el producto. Este trabajo fue desarrollado aún más por G. E. Briggs y J. B. S. Haldane , quienes derivaron ecuaciones cinéticas que todavía se utilizan ampliamente en la actualidad. [66]
Las tasas de enzimas dependen de las condiciones de la solución y de la concentración del sustrato . Para encontrar la velocidad máxima de una reacción enzimática, se aumenta la concentración del sustrato hasta que se observe una velocidad constante de formación de producto. Esto se muestra en la curva de saturación de la derecha. La saturación ocurre porque, a medida que aumenta la concentración del sustrato, una mayor cantidad de enzima libre se convierte en el complejo ES unido al sustrato. A la velocidad de reacción máxima ( Vmax ) de la enzima, todos los sitios activos de la enzima están unidos al sustrato y la cantidad de complejo ES es la misma que la cantidad total de enzima. [1] : 8,4
Vmax es sólo uno de varios parámetros cinéticos importantes. También es importante la cantidad de sustrato necesaria para lograr una velocidad de reacción determinada. Esto viene dado por la constante de Michaelis-Menten ( Km ), que es la concentración de sustrato necesaria para que una enzima alcance la mitad de su velocidad de reacción máxima ; generalmente, cada enzima tiene un KM característico para un sustrato determinado. Otra constante útil es kcat , también llamada número de recambio , que es el número de moléculas de sustrato manejadas por un sitio activo por segundo. [1] : 8,4
La eficiencia de una enzima se puede expresar en términos de k cat / K m . Esto también se llama constante de especificidad e incorpora las constantes de velocidad para todos los pasos de la reacción hasta el primer paso irreversible inclusive. Debido a que la constante de especificidad refleja tanto la afinidad como la capacidad catalítica, es útil para comparar diferentes enzimas entre sí, o la misma enzima con diferentes sustratos. El máximo teórico para la constante de especificidad se llama límite de difusión y es aproximadamente de 10 8 a 10 9 (M −1 s −1 ). En este punto, cada colisión de la enzima con su sustrato dará como resultado una catálisis, y la velocidad de formación del producto no está limitada por la velocidad de reacción sino por la velocidad de difusión. Las enzimas con esta propiedad se denominan catalíticamente perfectas o cinéticamente perfectas . Ejemplos de tales enzimas son triosa-fosfato isomerasa , anhidrasa carbónica , acetilcolinesterasa , catalasa , fumarasa , β-lactamasa y superóxido dismutasa . [1] : 8.4.2 El recambio de dichas enzimas puede alcanzar varios millones de reacciones por segundo. [1] : 9.2 Pero la mayoría de las enzimas están lejos de ser perfectas: los valores promedio de y son aproximadamente y , respectivamente. [67]
La cinética de Michaelis-Menten se basa en la ley de acción de masas , que se deriva de los supuestos de difusión libre y colisión aleatoria impulsada termodinámicamente. Muchos procesos bioquímicos o celulares se desvían significativamente de estas condiciones debido al hacinamiento macromolecular y al movimiento molecular restringido. [68] Extensiones más recientes y complejas del modelo intentan corregir estos efectos. [69]
Las velocidades de reacción enzimática pueden reducirse mediante varios tipos de inhibidores enzimáticos. [70] : 73–74
Un inhibidor competitivo y un sustrato no pueden unirse a la enzima al mismo tiempo. [71] A menudo, los inhibidores competitivos se parecen mucho al sustrato real de la enzima. Por ejemplo, el fármaco metotrexato es un inhibidor competitivo de la enzima dihidrofolato reductasa , que cataliza la reducción del dihidrofolato a tetrahidrofolato. [72] La similitud entre las estructuras del dihidrofolato y este fármaco se muestra en la figura adjunta. Este tipo de inhibición se puede superar con una alta concentración de sustrato. En algunos casos, el inhibidor puede unirse a un sitio distinto del sitio de unión del sustrato habitual y ejercer un efecto alostérico para cambiar la forma del sitio de unión habitual. [73]
Un inhibidor no competitivo se une a un sitio distinto al que se une el sustrato. El sustrato todavía se une con su afinidad habitual y por tanto K m sigue siendo el mismo. Sin embargo, el inhibidor reduce la eficacia catalítica de la enzima, de modo que se reduce la Vmax . A diferencia de la inhibición competitiva, la inhibición no competitiva no se puede superar con una alta concentración de sustrato. [70] : 76–78
Un inhibidor no competitivo no puede unirse a la enzima libre, sólo al complejo enzima-sustrato; por lo tanto, estos tipos de inhibidores son más eficaces en concentraciones altas de sustrato. En presencia del inhibidor, el complejo enzima-sustrato está inactivo. [70] : 78 Este tipo de inhibición es poco común. [74]
Un inhibidor mixto se une a un sitio alostérico y la unión del sustrato y el inhibidor se afectan entre sí. La función de la enzima se reduce pero no se elimina cuando se une al inhibidor. Este tipo de inhibidor no sigue la ecuación de Michaelis-Menten. [70] : 76–78
Un inhibidor irreversible inactiva permanentemente la enzima, generalmente formando un enlace covalente con la proteína. [75] La penicilina [76] y la aspirina [77] son fármacos comunes que actúan de esta manera.
En muchos organismos, los inhibidores pueden actuar como parte de un mecanismo de retroalimentación . Si una enzima produce demasiada cantidad de una sustancia en el organismo, esa sustancia puede actuar como un inhibidor de la enzima al comienzo de la vía que la produce, lo que hace que la producción de la sustancia se ralentice o se detenga cuando hay una cantidad suficiente. Esta es una forma de retroalimentación negativa . Las principales vías metabólicas, como el ciclo del ácido cítrico, utilizan este mecanismo. [1] : 17.2.2
Dado que los inhibidores modulan la función de las enzimas, a menudo se utilizan como fármacos. Muchos de estos fármacos son inhibidores competitivos reversibles que se asemejan al sustrato nativo de la enzima, similar al metotrexato mencionado anteriormente; Otros ejemplos bien conocidos incluyen las estatinas utilizadas para tratar el colesterol alto [78] y los inhibidores de proteasa utilizados para tratar infecciones retrovirales como el VIH . [79] Un ejemplo común de un inhibidor irreversible que se utiliza como fármaco es la aspirina , que inhibe las enzimas COX-1 y COX-2 que producen la prostaglandina, mensajera de la inflamación . [77] Otros inhibidores de enzimas son venenos. Por ejemplo, el veneno cianuro es un inhibidor enzimático irreversible que se combina con el cobre y el hierro en el sitio activo de la enzima citocromo c oxidasa y bloquea la respiración celular . [80]
Como las enzimas están formadas por proteínas, sus acciones son sensibles a cambios en muchos factores fisicoquímicos como el pH, la temperatura, la concentración de sustrato, etc.
La siguiente tabla muestra el pH óptimo para varias enzimas. [81]
Las enzimas cumplen una amplia variedad de funciones dentro de los organismos vivos. Son indispensables para la transducción de señales y la regulación celular, a menudo mediante quinasas y fosfatasas . [82] También generan movimiento, ya que la miosina hidroliza el trifosfato de adenosina (ATP) para generar contracción muscular y también transporta carga alrededor de la célula como parte del citoesqueleto . [83] Otras ATPasas en la membrana celular son bombas de iones involucradas en el transporte activo . Las enzimas también participan en funciones más exóticas, como la luciferasa que genera luz en las luciérnagas . [84] Los virus también pueden contener enzimas para infectar células, como la integrasa y la transcriptasa inversa del VIH , o para la liberación viral de las células, como la neuraminidasa del virus de la influenza . [85]
Una función importante de las enzimas es en el sistema digestivo de los animales. Enzimas como las amilasas y proteasas descomponen moléculas grandes ( almidón o proteínas , respectivamente) en otras más pequeñas, para que puedan ser absorbidas por los intestinos. Las moléculas de almidón, por ejemplo, son demasiado grandes para ser absorbidas en el intestino, pero las enzimas hidrolizan las cadenas de almidón en moléculas más pequeñas, como maltosa y, finalmente, glucosa , que luego pueden absorberse. Diferentes enzimas digieren diferentes sustancias alimenticias. En los rumiantes , que tienen dietas herbívoras , los microorganismos del intestino producen otra enzima, la celulasa , para descomponer las paredes celulares de celulosa de la fibra vegetal. [86]
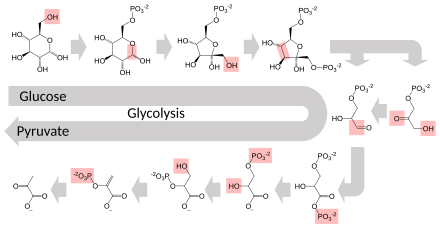
Varias enzimas pueden trabajar juntas en un orden específico, creando vías metabólicas . [1] : 30.1 En una vía metabólica, una enzima toma el producto de otra enzima como sustrato. Después de la reacción catalítica, el producto pasa a otra enzima. A veces, más de una enzima puede catalizar la misma reacción en paralelo; esto puede permitir una regulación más compleja: con, por ejemplo, una actividad constante baja proporcionada por una enzima pero una actividad alta inducible por una segunda enzima. [87]
Las enzimas determinan qué pasos ocurren en estas vías. Sin enzimas, el metabolismo no seguiría los mismos pasos y no podría regularse para satisfacer las necesidades de la célula. La mayoría de las vías metabólicas centrales están reguladas en unos pocos pasos clave, típicamente a través de enzimas cuya actividad implica la hidrólisis de ATP. Debido a que esta reacción libera tanta energía, otras reacciones que son termodinámicamente desfavorables pueden acoplarse a la hidrólisis del ATP, impulsando la serie general de reacciones metabólicas vinculadas. [1] : 30,1
Hay cinco formas principales en que se controla la actividad enzimática en la célula. [1] : 30.1.1
Las enzimas pueden ser activadas o inhibidas por otras moléculas. Por ejemplo, los productos finales de una vía metabólica suelen ser inhibidores de una de las primeras enzimas de la vía (normalmente el primer paso irreversible, llamado paso comprometido), regulando así la cantidad de producto final elaborado por las vías. Este mecanismo regulador se denomina mecanismo de retroalimentación negativa , porque la cantidad de producto final producido está regulada por su propia concentración. [88] : 141–48 El mecanismo de retroalimentación negativa puede ajustar eficazmente la tasa de síntesis de metabolitos intermedios de acuerdo con las demandas de las células. Esto ayuda a la asignación eficaz de materiales y a la economía energética, y evita la fabricación excesiva de productos finales. Al igual que otros dispositivos homeostáticos , el control de la acción enzimática ayuda a mantener un ambiente interno estable en los organismos vivos. [88] : 141
Ejemplos de modificación postraduccional incluyen fosforilación , miristoilación y glicosilación . [88] : 149–69 Por ejemplo, en la respuesta a la insulina , la fosforilación de múltiples enzimas, incluida la glucógeno sintasa , ayuda a controlar la síntesis o degradación del glucógeno y permite que la célula responda a los cambios en el azúcar en sangre . [89] Otro ejemplo de modificación postraduccional es la escisión de la cadena polipeptídica. La quimotripsina , una proteasa digestiva, se produce en forma inactiva como quimotripsinógeno en el páncreas y se transporta de esta forma al estómago , donde se activa. Esto impide que la enzima digiera el páncreas u otros tejidos antes de ingresar al intestino. Este tipo de precursor inactivo de una enzima se conoce como zimógeno [88] : 149-53 o proenzima.
La producción de enzimas ( transcripción y traducción de genes enzimáticos) puede ser potenciada o disminuida por una célula en respuesta a cambios en el entorno celular. Esta forma de regulación genética se llama inducción enzimática . Por ejemplo, las bacterias pueden volverse resistentes a antibióticos como la penicilina porque se inducen enzimas llamadas beta-lactamasas que hidrolizan el crucial anillo beta-lactámico dentro de la molécula de penicilina. [90] Otro ejemplo proviene de las enzimas del hígado llamadas citocromo P450 oxidasas , que son importantes en el metabolismo de los fármacos . La inducción o inhibición de estas enzimas puede provocar interacciones farmacológicas . [91] Los niveles de enzimas también se pueden regular cambiando la tasa de degradación de las enzimas . [1] : 30.1.1 Lo opuesto a la inducción enzimática es la represión enzimática .
Las enzimas pueden estar compartimentadas, con diferentes vías metabólicas que ocurren en diferentes compartimentos celulares . Por ejemplo, los ácidos grasos son sintetizados por un conjunto de enzimas en el citosol , el retículo endoplasmático y Golgi y utilizados por un conjunto diferente de enzimas como fuente de energía en la mitocondria , a través de la β-oxidación . [92] Además, el tráfico de la enzima a diferentes compartimentos puede cambiar el grado de protonación (p. ej., el citoplasma neutro y el lisosoma ácido ) o el estado oxidativo (p. ej., periplasma oxidante o citoplasma reductor ), lo que a su vez afecta la actividad enzimática. [93] A diferencia de la partición en orgánulos unidos a membranas, la localización subcelular de enzimas también puede alterarse mediante la polimerización de enzimas en filamentos citoplasmáticos macromoleculares. [94] [95]
En los eucariotas multicelulares , las células de diferentes órganos y tejidos tienen diferentes patrones de expresión genética y, por lo tanto, tienen diferentes conjuntos de enzimas (conocidas como isozimas ) disponibles para reacciones metabólicas. Esto proporciona un mecanismo para regular el metabolismo general del organismo. Por ejemplo, la hexoquinasa , la primera enzima en la vía de la glucólisis , tiene una forma especializada llamada glucocinasa expresada en el hígado y el páncreas que tiene una menor afinidad por la glucosa pero es más sensible a la concentración de glucosa. [96] Esta enzima participa en la detección del azúcar en sangre y en la regulación de la producción de insulina. [97]


Dado que el control estricto de la actividad enzimática es esencial para la homeostasis , cualquier mal funcionamiento (mutación, sobreproducción, subproducción o deleción) de una única enzima crítica puede conducir a una enfermedad genética. El mal funcionamiento de un solo tipo de enzima entre los miles de tipos presentes en el cuerpo humano puede ser fatal. Un ejemplo de enfermedad genética mortal debida a insuficiencia enzimática es la enfermedad de Tay-Sachs , en la que los pacientes carecen de la enzima hexosaminidasa . [98] [99]
Un ejemplo de deficiencia enzimática es el tipo más común de fenilcetonuria . Muchas mutaciones diferentes de aminoácidos individuales en la enzima fenilalanina hidroxilasa , que cataliza el primer paso en la degradación de la fenilalanina , dan como resultado la acumulación de fenilalanina y productos relacionados. Algunas mutaciones se encuentran en el sitio activo, lo que interrumpe directamente la unión y la catálisis, pero muchas están lejos del sitio activo y reducen la actividad al desestabilizar la estructura de la proteína o afectar la oligomerización correcta. [100] [101] Esto puede provocar discapacidad intelectual si la enfermedad no se trata. [102] Otro ejemplo es la deficiencia de pseudocolinesterasa , en la que se altera la capacidad del cuerpo para descomponer los fármacos éster de colina. [103] La administración oral de enzimas se puede utilizar para tratar algunas deficiencias de enzimas funcionales, como la insuficiencia pancreática [104] y la intolerancia a la lactosa . [105]
Otra forma en que el mal funcionamiento de las enzimas puede causar enfermedades proviene de mutaciones de la línea germinal en genes que codifican las enzimas reparadoras del ADN . Los defectos en estas enzimas causan cáncer porque las células son menos capaces de reparar mutaciones en sus genomas . Esto provoca una lenta acumulación de mutaciones y da como resultado el desarrollo de cánceres . Un ejemplo de este síndrome de cáncer hereditario es el xeroderma pigmentoso , que provoca el desarrollo de cánceres de piel en respuesta incluso a una exposición mínima a la luz ultravioleta . [106] [107]
Al igual que cualquier otra proteína, las enzimas cambian con el tiempo mediante mutaciones y divergencia de secuencias. Dado su papel central en el metabolismo , la evolución de las enzimas desempeña un papel crítico en la adaptación . Por lo tanto, una pregunta clave es si las enzimas pueden cambiar sus actividades enzimáticas y cómo hacerlo. Generalmente se acepta que muchas actividades enzimáticas nuevas han evolucionado a través de la duplicación de genes y la mutación de las copias duplicadas, aunque la evolución también puede ocurrir sin duplicación. Un ejemplo de una enzima que ha cambiado su actividad es el antepasado de la metionil aminopeptidasa (MAP) y la creatina amidinohidrolasa ( creatinasa ), que son claramente homólogas pero catalizan reacciones muy diferentes (MAP elimina la metionina amino terminal en nuevas proteínas, mientras que la creatinasa hidroliza la creatina para sarcosina y urea ). Además, la MAP depende de los iones metálicos, mientras que la creatinasa no, por lo que esta propiedad también se perdió con el tiempo. [108] Pequeños cambios de actividad enzimática son extremadamente comunes entre las enzimas. En particular, la especificidad de unión al sustrato (ver arriba) puede cambiar fácil y rápidamente con cambios de un solo aminoácido en sus bolsas de unión al sustrato. Esto se observa frecuentemente en las principales clases de enzimas, como las quinasas . [109]
La evolución artificial (in vitro) ahora se usa comúnmente para modificar la actividad o especificidad de las enzimas para aplicaciones industriales (ver más abajo).
Las enzimas se utilizan en la industria química y otras aplicaciones industriales cuando se requieren catalizadores extremadamente específicos. Las enzimas en general están limitadas en el número de reacciones que han evolucionado para catalizar y también por su falta de estabilidad en disolventes orgánicos y a altas temperaturas. Como consecuencia, la ingeniería de proteínas es un área activa de investigación e implica intentos de crear nuevas enzimas con propiedades novedosas, ya sea mediante diseño racional o evolución in vitro . [110] [111] Estos esfuerzos han comenzado a tener éxito y ahora se han diseñado algunas enzimas "desde cero" para catalizar reacciones que no ocurren en la naturaleza. [112]