
La biología sintética ( SynBio ) es un campo multidisciplinario de la ciencia que se centra en sistemas y organismos vivos, y aplica principios de ingeniería para desarrollar nuevas partes, dispositivos y sistemas biológicos o para rediseñar sistemas existentes que se encuentran en la naturaleza. [1]
Es una rama de la ciencia que abarca una amplia gama de metodologías de diversas disciplinas, como bioquímica , biotecnología , biomateriales , ciencia/ingeniería de materiales , ingeniería genética , biología molecular , ingeniería molecular , biología de sistemas , ciencia de membranas , biofísica , química y biológica. ingeniería , ingeniería eléctrica e informática , ingeniería de control y biología evolutiva .
Incluye el diseño y la construcción de módulos biológicos , sistemas biológicos y máquinas biológicas , o el rediseño de sistemas biológicos existentes para fines útiles. [2]
Además, es la rama de la ciencia que se centra en las nuevas capacidades de la ingeniería en organismos existentes para rediseñarlos con fines útiles. [3]
Para producir sistemas predecibles y robustos con funcionalidades novedosas que aún no existen en la naturaleza, también es necesario aplicar el paradigma de ingeniería del diseño de sistemas a los sistemas biológicos. Según la Comisión Europea , se trata posiblemente de un ensamblador molecular basado en sistemas biomoleculares como el ribosoma . [4]
1910: Primer uso identificable del término biología sintética en la publicación de Stéphane Leduc Théorie physico-chimique de la vie et générations spontanées . [5] También señaló este término en otra publicación, La Biologie Synthétique en 1912. [6]
1944 : el científico canadiense-estadounidense Oswald Avery demuestra que el ADN es el material del que están hechos los genes y los cromosomas . Esto se convierte en la base sobre la que se construye toda la investigación genética posterior. [7]
1953 : Francis Crick y James Watson publican la estructura del ADN en Nature .
1961 : Jacob y Monod postulan la regulación celular mediante redes moleculares a partir de su estudio del operón lac en E. coli e imaginaron la capacidad de ensamblar nuevos sistemas a partir de componentes moleculares. [8]
1973 : Cohen, Boyer et al. publican la primera clonación molecular y amplificación de ADN en un plásmido en PNAS . constituyendo el amanecer de la biología sintética. [9]
1978 : Arber , Nathans y Smith ganan el Premio Nobel de Fisiología o Medicina por el descubrimiento de las enzimas de restricción , lo que llevó a Szybalski a ofrecer un comentario editorial en la revista Gene :
El trabajo sobre las nucleasas de restricción no sólo nos permite construir fácilmente moléculas de ADN recombinantes y analizar genes individuales, sino que también nos ha llevado a la nueva era de la biología sintética, donde no sólo se describen y analizan genes existentes sino que también se pueden construir nuevas disposiciones genéticas. y evaluado. [10]
1988 : Mullis et al. publican en Science la primera amplificación de ADN mediante la reacción en cadena de la polimerasa (PCR) utilizando una ADN polimerasa termoestable. [11] Esto evitó la adición de nueva ADN polimerasa después de cada ciclo de PCR, lo que simplificó enormemente la mutagénesis y el ensamblaje del ADN.
2000 : Dos artículos en Nature informan sobre circuitos biológicos sintéticos , un interruptor de palanca genético y un reloj biológico, mediante la combinación de genes dentro de las células de E. coli . [12] [13]
2003 : Tom Knight inventa las piezas de ADN estandarizadas más utilizadas, los plásmidos BioBrick . [14] Estas piezas serán fundamentales para la competencia internacional de máquinas de ingeniería genética (iGEM) fundada en el MIT el año siguiente.
2003 : Los investigadores diseñan una vía precursora de la artemisinina en E. coli . [15]
2004 : Se celebra en el MIT la primera conferencia internacional de biología sintética, Synthetic Biology 1.0 (SB1.0).
2005 : Investigadores desarrollan un circuito sensor de luz en E. coli . [16] Otro grupo diseña circuitos capaces de formar patrones multicelulares. [17]
2006 : Los investigadores diseñan un circuito sintético que promueve la invasión bacteriana de las células tumorales. [18]
2010 : Investigadores publican en Science el primer genoma bacteriano sintético, denominado M. mycoides JCVI-syn1.0. [19] [20] El genoma se elabora a partir de ADN sintetizado químicamente mediante recombinación de levaduras.
2011 : Se diseñan brazos cromosómicos sintéticos funcionales en levadura. [21]
2012 : Los laboratorios Charpentier y Doudna publican en Science la programación de la inmunidad bacteriana CRISPR-Cas9 para atacar la escisión del ADN. [22] Esta tecnología simplificó y amplió enormemente la edición de genes eucariotas.
2019 : Científicos de ETH Zurich informan de la creación del primer genoma bacteriano , llamado Caulobacter ethensis-2.0 , elaborado íntegramente por computadora, aunque aún no existe una forma viable relacionada de C. ethensis-2.0 . [23] [24]
2019 : Los investigadores informan sobre la producción de una nueva forma sintética (posiblemente artificial ) de vida viable , una variante de la bacteria Escherichia coli , reduciendo el número natural de 64 codones en el genoma bacteriano a 59 codones, para codificar 20 aminoácidos. ácidos . [25] [26]
2020 : Los científicos crean el primer xenobot , un organismo sintético programable derivado de células de rana y diseñado por IA. [27]
2021 : Los científicos informaron que los xenobots pueden autorreplicarse reuniendo células sueltas en el medio ambiente y luego formando nuevos xenobots. [28]
Es un campo cuyo alcance se está ampliando en términos de integración de sistemas, organismos diseñados y hallazgos prácticos. [1]
Los ingenieros ven la biología como tecnología (en otras palabras, un sistema determinado incluye la biotecnología o su ingeniería biológica ). [29] La biología sintética incluye la amplia redefinición y expansión de la biotecnología, con el objetivo final de poder diseñar y construir sistemas biológicos vivos diseñados que procesen información, manipulen productos químicos, fabriquen materiales y estructuras, produzcan energía, proporcionen alimentos y mantengan y mejorar la salud humana, así como avanzar en el conocimiento fundamental de los sistemas biológicos y nuestro medio ambiente. [30]
Los investigadores y las empresas que trabajan en biología sintética están utilizando el poder de la naturaleza para resolver problemas en la agricultura, la manufactura y la medicina. [3]
Debido a capacidades de ingeniería genética más poderosas y menores costos de síntesis y secuenciación de ADN , el campo de la biología sintética está creciendo rápidamente. En 2016, más de 350 empresas en 40 países participaron activamente en aplicaciones de biología sintética; Todas estas empresas tenían un patrimonio neto estimado de 3.900 millones de dólares en el mercado global. [31] La biología sintética actualmente no tiene una definición generalmente aceptada. A continuación se muestran algunos ejemplos:
Es la ciencia de la ingeniería genética y física emergente para producir formas de vida nuevas (y, por tanto, sintéticas). Para desarrollar organismos con características nuevas o mejoradas, este campo de estudio emergente combina conocimientos y técnicas de biología, ingeniería y disciplinas relacionadas para diseñar ADN sintetizado químicamente. [32] [33]
La ingeniería biomolecular incluye enfoques que tienen como objetivo crear un conjunto de herramientas de unidades funcionales que pueden introducirse para presentar nuevas funciones tecnológicas en células vivas. La ingeniería genética incluye enfoques para construir cromosomas sintéticos u organismos mínimos como Mycoplasma laboratorium .
El diseño biomolecular se refiere a la idea general de diseño de novo y combinación aditiva de componentes biomoleculares. Cada uno de estos enfoques comparte una tarea similar: desarrollar una entidad más sintética en un nivel más alto de complejidad manipulando inventivamente una parte más simple en el nivel anterior. [34] [35] La optimización de estas vías exógenas en sistemas no naturales requiere un ajuste iterativo de los componentes biomoleculares individuales para seleccionar las concentraciones más altas del producto deseado. [36]
Por otro lado, los "reescritores" son biólogos sintéticos interesados en probar la irreductibilidad de los sistemas biológicos. Debido a la complejidad de los sistemas biológicos naturales, sería más sencillo reconstruir los sistemas naturales de interés desde cero; proporcionar sustitutos diseñados que sean más fáciles de comprender, controlar y manipular. [37] Los reescritores se inspiran en la refactorización , un proceso que a veces se utiliza para mejorar el software informático.
La bioingeniería, la genómica sintética, la biología sintética de protocélulas, la biología molecular no convencional y las técnicas in silico son las cinco categorías de la biología sintética. [38]
Es necesario revisar las distinciones y analogías entre las categorías de la biología sintética para su valoración social y ética, para distinguir entre cuestiones que afectan a todo el campo y particulares a uno específico. [38]
El subcampo de la bioingeniería se concentra en la creación de nuevas vías metabólicas y regulatorias, y actualmente es el que probablemente atrae la atención de la mayoría de los investigadores y la financiación. Está motivado principalmente por el deseo de establecer la biotecnología como una disciplina de ingeniería legítima. Cuando se hace referencia a esta área de la biología sintética, la palabra "bioingeniería" no debe confundirse con "ingeniería genética tradicional", que implica la introducción de un único transgén en el organismo previsto. Los bioingenieros adaptaron la biología sintética para proporcionar una perspectiva sustancialmente más integrada sobre cómo alterar organismos o sistemas metabólicos. [38]
Un ejemplo típico de ingeniería genética de un solo gen es la inserción del gen de la insulina humana en bacterias para crear proteínas transgénicas. La creación de vías de señalización completamente nuevas, que contienen numerosos genes y componentes reguladores (como un circuito oscilador para iniciar la producción periódica de proteína verde fluorescente (GFP) en células de mamíferos), se conoce como bioingeniería como parte de la biología sintética. [38]
Al utilizar módulos metabólicos y regulatorios simplificados y abstractos, así como otras partes estandarizadas que pueden combinarse libremente para crear nuevas vías o criaturas, la bioingeniería tiene como objetivo crear sistemas biológicos innovadores. Además de crear infinitas oportunidades para aplicaciones novedosas, se prevé que esta estrategia hará que la bioingeniería sea más predecible y controlable que la biotecnología tradicional. [38]
La formación de animales con un genoma (mínimo) fabricado químicamente es otra faceta de la biología sintética que destaca la genómica sintética. Esta área de la biología sintética ha sido posible gracias a los avances continuos en la tecnología de síntesis de ADN, que ahora hace posible producir moléculas de ADN con miles de pares de bases a un costo razonable. El objetivo es combinar estas moléculas en genomas completos y trasplantarlos a células vivas, reemplazando el genoma de la célula huésped y reprogramando su metabolismo para realizar diferentes funciones. [38]
Los científicos han demostrado previamente el potencial de este enfoque al crear virus infecciosos mediante la síntesis de los genomas de múltiples virus. Estos importantes avances en ciencia y tecnología desencadenaron las preocupaciones iniciales del público sobre los riesgos asociados con esta tecnología. [38]
Un genoma simple también podría funcionar como un "genoma chasis" que podría ampliarse rápidamente mediante la inclusión de genes creados para tareas particulares. Estas "criaturas de chasis" serían más adecuadas para la inserción de nuevas funciones que los organismos salvajes, ya que tendrían menos vías biológicas que potencialmente podrían entrar en conflicto con las nuevas funcionalidades, además de tener sitios de inserción específicos. La genómica sintética se esfuerza por crear criaturas con "arquitecturas" novedosas, muy parecidas al método de la bioingeniería. Adopta una perspectiva integradora u holística del organismo. En este caso, el objetivo es la creación de genomas chasis basados en genes necesarios y otras secuencias de ADN requeridas en lugar del diseño de vías metabólicas o regulatorias basadas en criterios abstractos. [38]
La generación in vitro de células sintéticas es la rama de protocélulas de la biología sintética. Para crear estas células artificiales se pueden utilizar vesículas lipídicas, que cuentan con todos los componentes necesarios para funcionar como un sistema completo. Al final, estas células sintéticas deberían cumplir los requisitos para ser consideradas vivas, es decir, la capacidad de autorreplicación, automantenimiento y evolución. La técnica de las protocélulas tiene este como objetivo final, sin embargo, hay otros pasos intermedios que no cumplen todos los criterios para una célula viva. Para llevar a cabo una función específica, estas vesículas lipídicas contienen extractos celulares o conjuntos más específicos de macromoléculas biológicas y estructuras complejas, como enzimas, ácidos nucleicos o ribosomas. Por ejemplo, los liposomas pueden llevar a cabo reacciones en cadena de la polimerasa particulares o sintetizar una proteína particular. [38]
La biología sintética de protocélulas acerca la vida artificial un paso más a la realidad al sintetizar no sólo el genoma sino también todos los componentes de la célula in vitro, a diferencia del enfoque de la genómica sintética, que se basa en obligar a una célula natural a llevar a cabo las instrucciones codificadas por el genoma sintético introducido. Los biólogos sintéticos en este campo ven su trabajo como un estudio básico de las condiciones necesarias para que exista la vida y su origen más que en cualquier otra técnica. Sin embargo, la técnica de la protocélula también se presta bien a sus aplicaciones; Al igual que otros subproductos de la biología sintética, las protocélulas podrían emplearse para la fabricación de biopolímeros y medicamentos. [38]
El objetivo de la estrategia de "biología molecular antinatural" es crear nuevas variedades de vida basadas en un tipo diferente de biología molecular, como nuevos tipos de ácidos nucleicos o un nuevo código genético. La creación de nuevos tipos de nucleótidos que puedan integrarse en ácidos nucleicos únicos podría lograrse cambiando ciertos componentes del ADN o del ARN, como las bases o los azúcares del esqueleto. [38]
El código genético normal se está alterando insertando codones cuádruples o cambiando algunos codones para codificar nuevos aminoácidos, lo que permitiría posteriormente el uso de aminoácidos no naturales con características únicas en la producción de proteínas. Es un problema científico y tecnológico ajustar la maquinaria enzimática de la célula para ambos enfoques. [38]
Un nuevo tipo de vida estaría formado por organismos con un genoma construido sobre ácidos nucleicos sintéticos o sobre un sistema de codificación totalmente nuevo para aminoácidos sintéticos. Este nuevo estilo de vida tendría algunos beneficios pero también algunos nuevos peligros. Al liberarse en el medio ambiente, no habría transferencia horizontal de genes ni cruce de genes con especies naturales. Además, este tipo de organismos sintéticos podrían crearse para requerir materiales no naturales para la síntesis de proteínas o ácidos nucleicos, lo que los haría incapaces de prosperar en la naturaleza si escaparan accidentalmente. [38]
Por otro lado, si estos organismos finalmente pudieran sobrevivir fuera del espacio controlado, podrían tener un beneficio particular sobre los organismos naturales porque serían resistentes a organismos vivos depredadores o virus naturales, lo que podría conducir a una propagación incontrolada del virus sintético. organismos. [38]
La biología sintética in silico y las diversas estrategias están interconectadas. El desarrollo de diseños complejos, ya sean vías metabólicas, procesos celulares fundamentales o genomas de chasis, es una de las principales dificultades que enfrentan los cuatro métodos de biología sintética descritos anteriormente. Debido a esto, la biología sintética tiene una rama in silico robusta, similar a la biología de sistemas, que tiene como objetivo crear modelos computacionales para el diseño de componentes biológicos comunes o circuitos sintéticos, que son esencialmente simulaciones de organismos sintéticos. [38]
La aplicación práctica de simulaciones y modelos mediante bioingeniería u otros campos de la biología sintética es el objetivo a largo plazo de la biología sintética in silico. Muchas de las simulaciones computacionales de organismos sintéticos hasta ahora poseen poca o ninguna analogía directa con los seres vivos. Debido a esto, la biología sintética in silico se considera un grupo separado en este artículo. [38]
Es sensato integrar las cinco áreas bajo el paraguas de la biología sintética como un área de estudio unificada. Aunque se centran en varias facetas de la vida, como la regulación metabólica, los elementos esenciales o la composición bioquímica, estas cinco estrategias apuntan al mismo fin: crear nuevos tipos de organismos vivos. Además, las variadas metodologías comienzan con numerosos enfoques metodológicos, lo que conduce a la diversidad de enfoques de biología sintética. [38]
La biología sintética es un campo interdisciplinario que se basa y se inspira en muchas disciplinas científicas diferentes, no en un solo campo o técnica. Todos los biólogos sintéticos tienen el mismo objetivo subyacente de diseñar y producir nuevas formas de vida, a pesar de que pueden emplear diversas metodologías, técnicas e instrumentos de investigación. Cualquier evaluación de la biología sintética, ya sea que examine consideraciones éticas, legales o de seguridad, debe tener en cuenta el hecho de que, si bien algunas preguntas, riesgos y cuestiones son únicos para cada técnica, en otras circunstancias, se debe considerar la biología sintética en su conjunto. en consideración. [38]
La biología sintética se ha dividido tradicionalmente en cuatro enfoques de ingeniería diferentes: de arriba hacia abajo, paralelo, ortogonal y de abajo hacia arriba. [39]
Para replicar comportamientos emergentes de la biología natural y construir vida artificial, se utilizan productos químicos no naturales. El otro busca componentes intercambiables de sistemas biológicos para juntarlos y crear sistemas que no funcionan de forma natural. En cualquier caso, un objetivo sintético obliga a los investigadores a aventurarse en nuevas áreas para abordar y resolver cuestiones que no pueden resolverse fácilmente mediante el análisis. Debido a esto, nuevos paradigmas se ven obligados a surgir en formas que el análisis no puede lograr fácilmente. Además de equipos que oscilan, se arrastran y juegan al tres en raya, la biología sintética ha producido instrumentos de diagnóstico que mejoran el tratamiento de pacientes con enfermedades infecciosas. [40]
Implica el uso de técnicas de ingeniería genética y metabólica para impartir nuevas funciones a las células vivas. [41] Al comparar genes universales y eliminar los no esenciales para crear un genoma básico, este método busca disminuir la complejidad de las células existentes. Estas iniciativas se basan en la hipótesis de una génesis única de la vida celular, el llamado Último Ancestro Común Universal , que sustenta la presencia de un genoma mínimo universal que dio origen a todos los seres vivos. Sin embargo, estudios recientes plantean la posibilidad de que las células eucariotas y procarióticas que componen el árbol de la vida hayan evolucionado a partir de un grupo de células primordiales en lugar de una sola célula. Como resultado, aunque la búsqueda del "genoma mínimo" se ha vuelto difícil de alcanzar, eliminar una serie de funciones no esenciales perjudica la aptitud de un organismo y conduce a genomas "frágiles". [39]
Este enfoque implica la creación de nuevos sistemas biológicos in vitro reuniendo componentes biomoleculares "no vivos", [42] a menudo con el objetivo de construir una célula artificial .
La reproducción, la replicación y el ensamblaje son tres principios autoorganizativos cruciales que se tienen en cuenta para lograrlo. Las células, que están formadas por un contenedor y un metabolismo, se consideran "hardware" en la definición de reproducción, mientras que la replicación se produce cuando un sistema duplica una copia perfecta de sí mismo, como en el caso del ADN, que se considera "software". " Cuando las vesículas o contenedores (como los coacervados de Oparin) se forman a partir de pequeñas gotas de moléculas que son orgánicas como lípidos o liposomas, se producen estructuras similares a membranas que comprenden fosfolípidos, agregados y ensamblajes. [39]
El estudio de las protocélulas existe junto con otras iniciativas de biología sintética in vitro que buscan producir un mínimo de células, vías metabólicas o "proteínas que nunca nacen", así como imitar funciones fisiológicas que incluyen la división y el crecimiento celular. La mejora in vitro de las vías sintéticas tiene el potencial de tener un efecto en otros sectores de la biología sintética, incluida la ingeniería metabólica, a pesar de que ya no se clasifica como investigación de biología sintética. Esta investigación, que es ante todo esencial, merece el debido reconocimiento como investigación en biología sintética. [39]
La ingeniería paralela también se conoce como bioingeniería. El código genético básico es la base para la investigación de ingeniería paralela, que utiliza biomoléculas convencionales como los ácidos nucleicos y los 20 aminoácidos para construir sistemas biológicos. Para una variedad de aplicaciones en biocomputación, bioenergía, biocombustibles, biorremediación, optogenética y medicina, implica la estandarización de componentes de ADN, ingeniería de interruptores, biosensores, circuitos genéticos, puertas lógicas y operadores de comunicación celular. Para dirigir la expresión de dos o más genes y/o proteínas, la mayoría de estas aplicaciones a menudo se basan en el uso de uno o más vectores (o plásmidos). Pequeñas unidades de ADN circulares de doble hebra conocidas como plásmidos, que se encuentran principalmente en células procarióticas pero que ocasionalmente también pueden detectarse en células eucariotas, pueden replicarse de forma autónoma del ADN cromosómico. [39]
También se la conoce como ingeniería perpendicular. Esta estrategia, también conocida como "biología química sintética", busca principalmente alterar o ampliar los códigos genéticos de los sistemas vivos utilizando bases de ADN y/o aminoácidos artificiales. Este subcampo también está relacionado con la xenobiología , un campo recientemente desarrollado que combina la química de sistemas, la biología sintética, la exobiología y la investigación sobre los orígenes de la vida. En las últimas décadas, los investigadores han creado compuestos que son estructuralmente similares a las bases canónicas del ADN para ver si esas moléculas "alienígenas" o xeno (XNA) pueden emplearse como portadores de información genética. De manera similar, restos no canónicos han reemplazado el azúcar del ADN ( desoxirribosa ). [39] Para expresar información distinta de los 20 aminoácidos convencionales de las proteínas, el código genético se puede alterar o ampliar. Un método implica incorporar un aminoácido xeno, no canónico o no natural (XAA) específico en una o más proteínas en uno o más lugares precisos utilizando enzimas ortogonales y un adaptador de ARN de transferencia de otro organismo. Mediante el uso de "evolución dirigida", que implica ciclos repetidos de mutagénesis genética (producción de diversidad genotípica), detección o selección (de un rasgo fenotípico específico) y amplificación de una mejor variante para la siguiente ronda iterativa, se producen enzimas ortogonales. Numerosos XAA tienen Se ha incorporado eficazmente a proteínas de criaturas más complejas como gusanos y moscas, así como a bacterias, levaduras y líneas celulares humanas. Como resultado de los cambios canónicos en la secuencia del ADN, la evolución dirigida también permite el desarrollo de ribosomas ortogonales, que facilitan la incorporación de XAA en proteínas o la creación de "vida espejo", o sistemas biológicos que contienen biomoléculas formadas por enantiómeros con diferentes orientaciones quirales. [39]
Varias tecnologías habilitadoras novedosas fueron fundamentales para el éxito de la biología sintética. Los conceptos incluyen la estandarización de partes biológicas y la abstracción jerárquica para permitir el uso de esas partes en sistemas sintéticos. [43] El ADN sirve como guía sobre cómo deberían funcionar los procesos biológicos, como la partitura de una compleja sinfonía de la vida. Nuestra capacidad para comprender y diseñar sistemas biológicos ha sufrido modificaciones significativas como resultado de los avances ocurridos en las últimas décadas en la lectura (secuenciación) y la escritura (síntesis) de secuencias de ADN. Estos avances han producido técnicas innovadoras para diseñar, ensamblar y modificar genes, materiales, circuitos y vías metabólicas codificados por el ADN, lo que permite un control cada vez mayor sobre sistemas biológicos e incluso organismos completos. [44]
Las tecnologías básicas incluyen lectura y escritura de ADN (secuenciación y fabricación). Se necesitan mediciones en múltiples condiciones para lograr un modelado y un diseño asistido por computadora (CAD) precisos.
Impulsado por las dramáticas reducciones en los costos de la síntesis de oligonucleótidos ("oligos") y la llegada de la PCR, los tamaños de las construcciones de ADN a partir de oligos han aumentado hasta el nivel genómico. [45] En 2000, los investigadores informaron sobre la síntesis del genoma del virus de la hepatitis C de 9,6 kpb (kilo pb) a partir de 60 a 80 unidades sintetizadas químicamente. [46] En 2002, investigadores de la Universidad de Stony Brook lograron sintetizar el genoma del poliovirus de 7741 pb a partir de su secuencia publicada, produciendo el segundo genoma sintético, que abarcó dos años. [47] En 2003, el genoma de 5386 pb del bacteriófago Phi X 174 se ensambló en aproximadamente dos semanas. [48] En 2006, el mismo equipo, en el Instituto J. Craig Venter , construyó y patentó un genoma sintético de una nueva bacteria mínima, Mycoplasma laboratorium , y estaban trabajando para lograr que funcionara en una célula viva. [49] [50] [51]
En 2007, se informó que varias empresas ofrecían síntesis de secuencias genéticas de hasta 2.000 pares de bases (pb) de largo, por un precio de alrededor de 1 dólar por pb y un tiempo de respuesta de menos de dos semanas. [52] Los oligonucleótidos recolectados de un chip de ADN fabricado mediante fotolitografía o inyección de tinta combinados con PCR y corrección de errores de coincidencia de ADN permiten cambios económicos a gran escala de codones en sistemas genéticos para mejorar la expresión génica o incorporar nuevos aminoácidos (ver George M. Proyectos de células sintéticas de Church y Anthony Forster [53] [54] ) . Esto favorece un enfoque de síntesis desde cero.
Además, el sistema CRISPR/Cas se ha convertido en una técnica prometedora para la edición de genes. Fue descrita como "la innovación más importante en el espacio de la biología sintética en casi 30 años". [55] Mientras que otros métodos tardan meses o años en editar secuencias genéticas, CRISPR acelera ese tiempo hasta semanas. [55] Sin embargo, debido a su facilidad de uso y accesibilidad, ha generado preocupaciones éticas, especialmente en torno a su uso en biohacking . [56] [57] [58]
La secuenciación del ADN determina el orden de las bases de nucleótidos en una molécula de ADN. Los biólogos sintéticos utilizan la secuenciación del ADN en su trabajo de varias maneras. En primer lugar, los esfuerzos de secuenciación del genoma a gran escala continúan proporcionando información sobre organismos naturales. Esta información proporciona un rico sustrato a partir del cual los biólogos sintéticos pueden construir piezas y dispositivos. En segundo lugar, la secuenciación puede verificar que el sistema fabricado sea el previsto. En tercer lugar, la secuenciación rápida, económica y fiable puede facilitar la detección e identificación rápidas de sistemas y organismos sintéticos. [59]
Esta es la capacidad de un sistema o componente para operar sin referencia a su contexto. [60]
Las partes de ADN estandarizadas más utilizadas [61] : 22–23 son los plásmidos BioBrick , inventados por Tom Knight en 2003. [14] Los biobricks se almacenan en el Registro de Piezas Biológicas Estándar en Cambridge, Massachusetts. El estándar BioBrick ha sido utilizado por decenas de miles de estudiantes en todo el mundo en la competencia internacional de Máquinas de Ingeniería Genética (iGEM). BioBrick Assembly Standard 10 promueve la modularidad al permitir que las secuencias codificantes de BioBrick se corten e intercambien utilizando las enzimas de restricción EcoRI o XbaI (prefijo de BioBrick) y SpeI y PstI (sufijo de BioBrick). [61] : 22-23
La superposición de secuencias entre dos elementos genéticos ( genes o secuencias codificantes ), denominadas genes superpuestos , puede impedir su manipulación individual. [62] Para aumentar la modularidad del genoma, la práctica de refactorizar el genoma o mejorar "la estructura interna de un sistema existente para uso futuro, manteniendo simultáneamente la función del sistema externo" [63] se ha adoptado en todas las disciplinas de la biología sintética. [62] Algunos ejemplos notables de refactorización incluyen el grupo de fijación de nitrógeno [64] y el sistema de secreción tipo III [65] junto con los bacteriófagos T7 [63] y ΦX174. [66]
Si bien el ADN es más importante para el almacenamiento de información, una gran fracción de las actividades de la célula las llevan a cabo las proteínas. Las herramientas pueden enviar proteínas a regiones específicas de la célula y unir diferentes proteínas. La intensidad de la interacción entre las proteínas asociadas debe poder ajustarse entre una vida útil de segundos (deseable para eventos de señalización dinámica) hasta una interacción irreversible (deseable para la estabilidad del dispositivo o resistente a condiciones adversas). Interacciones como bobinas enrolladas , [67] unión de péptidos al dominio SH3 [68] o SpyTag/SpyCatcher [69] ofrecen dicho control. Además, es necesario regular las interacciones proteína-proteína en las células, como con la luz (utilizando dominios de detección de voltaje de luz-oxígeno ) o moléculas pequeñas permeables a las células mediante dimerización inducida químicamente . [70]
En una célula viva, los motivos moleculares están incrustados en una red más grande con componentes ascendentes y descendentes. Estos componentes pueden alterar la capacidad de señalización del módulo de modelado. En el caso de módulos ultrasensibles, la contribución de sensibilidad de un módulo puede diferir de la sensibilidad que el módulo mantiene de forma aislada. [71] [72]
Los modelos informan el diseño de sistemas biológicos diseñados al predecir mejor el comportamiento del sistema antes de la fabricación. La biología sintética se beneficia de mejores modelos sobre cómo las moléculas biológicas se unen a sustratos y catalizan reacciones, cómo el ADN codifica la información necesaria para especificar la célula y cómo se comportan los sistemas integrados de múltiples componentes. Los modelos multiescala de redes reguladoras de genes se centran en aplicaciones de biología sintética. Las simulaciones pueden modelar todas las interacciones biomoleculares en la transcripción , traducción , regulación e inducción de redes reguladoras de genes. [73] [74] [75] [76]
Sólo un modelado exhaustivo puede permitir la exploración de la expresión genética dinámica en una forma adecuada para la investigación y el diseño debido a las numerosas especies involucradas y la complejidad de sus relaciones. Las simulaciones dinámicas de toda la interconexión biomolecular involucrada en la regulación, el transporte, la transcripción, la inducción y la traducción permiten detallar los diseños a nivel molecular. A diferencia del modelado de redes artificiales a posteriori, esto contrasta. [77]
La microfluídica , en particular la microfluídica de gotas, es una herramienta emergente que se utiliza para construir nuevos componentes, analizarlos y caracterizarlos. [78] [79] Se emplea ampliamente en ensayos de detección. [80]
Los estudios han considerado los componentes del mecanismo de transcripción del ADN . Uno de los deseos de los científicos que crean circuitos biológicos sintéticos es poder controlar la transcripción del ADN sintético en organismos unicelulares ( procariotas ) y en organismos multicelulares ( eucariotas ). Un estudio probó la capacidad de ajuste de los factores de transcripción sintéticos (sTF) en áreas de producción de transcripción y capacidad cooperativa entre múltiples complejos de factores de transcripción. [81] Los investigadores pudieron mutar regiones funcionales llamadas dedos de zinc , el componente específico del ADN de los sTF, para disminuir su afinidad por sitios de secuencia de ADN operadores específicos y, por lo tanto, disminuir la actividad asociada específica del sitio del sTF (generalmente regulación transcripcional). Además, utilizaron los dedos de zinc como componentes de los STF formadores de complejos, que son los mecanismos de traducción eucariotas . [81]
Las iniciativas de biología sintética con frecuencia apuntan a rediseñar organismos para que puedan crear un material, como un medicamento o un combustible, o adquirir una nueva función, como la capacidad de sentir algo en el medio ambiente. Ejemplos de lo que los investigadores están creando utilizando la biología sintética incluyen:
Un biosensor se refiere a un organismo diseñado, generalmente una bacteria, que es capaz de informar algún fenómeno ambiental como la presencia de metales pesados o toxinas. Uno de esos sistemas es el operón Lux de Aliivibrio fischeri , [83] que codifica la enzima que es la fuente de la bioluminiscencia bacteriana y puede colocarse después de un promotor respondiente para expresar los genes de luminiscencia en respuesta a un estímulo ambiental específico. [84] Uno de esos sensores creados consistía en un recubrimiento bacteriano bioluminiscente en un chip de computadora fotosensible para detectar ciertos contaminantes del petróleo . Cuando las bacterias detectan el contaminante, se iluminan. [85] Otro ejemplo de un mecanismo similar es la detección de minas terrestres mediante una cepa indicadora de E. coli diseñada capaz de detectar TNT y su principal producto de degradación DNT y, en consecuencia, producir una proteína verde fluorescente ( GFP ). [86]
Los organismos modificados pueden detectar señales ambientales y enviar señales de salida que pueden detectarse y servir con fines de diagnóstico. Se han utilizado cohortes de microbios. [87]
Los biosensores también podrían usarse para detectar firmas patógenas, como las del SARS-CoV-2 , y pueden ser portátiles . [88] [89]
Con el fin de detectar y reaccionar ante factores ambientales diversos y temporales, las células han desarrollado una amplia gama de circuitos reguladores, que van desde transcripcionales hasta postraduccionales. Estos circuitos están formados por módulos transductores que filtran las señales y activan una respuesta biológica, así como por secciones sensibles cuidadosamente diseñadas que conectan analitos y regulan los umbrales de detección de señales. La modularidad y la selectividad están programadas en circuitos biosensores en los niveles transcripcional, traslacional y postraduccional, para lograr el delicado equilibrio de los dos módulos de detección básicos. [90]
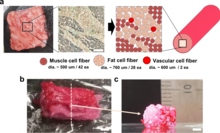
Sin embargo, no todos los productos nutricionales sintéticos son productos alimenticios para animales; por ejemplo, a partir de 2021, también hay productos de café sintético que, según se informa, están cerca de su comercialización. [98] [99] [100] Campos similares de investigación y producción basados en biología sintética que pueden usarse para la producción de alimentos y bebidas son:
Las células microbianas fotosintéticas se han utilizado como paso para la producción sintética de seda de araña . [105] [106]
Una computadora biológica se refiere a un sistema biológico diseñado que puede realizar operaciones similares a las de una computadora, que es un paradigma dominante en la biología sintética. Los investigadores construyeron y caracterizaron una variedad de puertas lógicas en varios organismos [107] y demostraron computación tanto analógica como digital en células vivas. Demostraron que se pueden diseñar bacterias para realizar cálculos tanto analógicos como digitales. [108] [109] En 2007, en células humanas, la investigación demostró un evaluador lógico universal que opera en células de mamíferos. [110] Posteriormente, los investigadores utilizaron este paradigma para demostrar una terapia de prueba de concepto que utiliza computación digital biológica para detectar y matar células cancerosas humanas en 2011. [111] En 2016, otro grupo de investigadores demostró que los principios de la ingeniería informática pueden utilizarse para automatizar el diseño de circuitos digitales en células bacterianas. [112] En 2017, los investigadores demostraron el sistema de 'lógica booleana y aritmética mediante escisión de ADN' (BLADE) para diseñar computación digital en células humanas. [113] En 2019, los investigadores implementaron un perceptrón en sistemas biológicos abriendo el camino para el aprendizaje automático en estos sistemas. [114]
Las células utilizan genes y proteínas que interactúan, llamados circuitos genéticos, para implementar diversas funciones, como responder a señales ambientales, tomar decisiones y comunicarse. Están involucrados tres componentes clave: ADN, ARN y circuitos genéticos diseñados por biólogos sintéticos que pueden controlar la expresión genética desde varios niveles, incluidos los niveles transcripcional, postranscripcional y traduccional.
La ingeniería metabólica tradicional se ha visto reforzada por la introducción de combinaciones de genes extraños y la optimización mediante evolución dirigida. Esto incluye la ingeniería de E. coli y levadura para la producción comercial de un precursor del fármaco antipalúdico , la artemisinina . [115]
Aún no se han creado organismos enteros desde cero, aunque las células vivas se pueden transformar con ADN nuevo. Varias formas permiten construir componentes sintéticos del ADN e incluso genomas sintéticos completos , pero una vez que se obtiene el código genético deseado, se integra en una célula viva que se espera que manifieste las nuevas capacidades o fenotipos deseados mientras crece y prospera. [116] La transformación celular se utiliza para crear circuitos biológicos , que pueden manipularse para producir los resultados deseados. [12] [13]
Al integrar la biología sintética con la ciencia de los materiales , sería posible utilizar células como fundiciones moleculares microscópicas para producir materiales cuyas propiedades estuvieran codificadas genéticamente. La reingeniería ha producido fibras de Curli, el componente amiloide del material extracelular de las biopelículas , como plataforma para nanomateriales programables . Estas nanofibras se construyeron genéticamente para funciones específicas, incluida la adhesión a sustratos, la creación de plantillas de nanopartículas y la inmovilización de proteínas. [117]
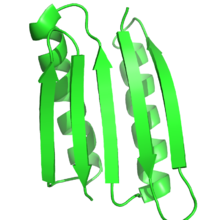
Las proteínas naturales se pueden diseñar, por ejemplo, mediante evolución dirigida , se pueden producir nuevas estructuras proteicas que coincidan o mejoren la funcionalidad de las proteínas existentes. Un grupo generó un haz de hélice que era capaz de unir oxígeno con propiedades similares a las de la hemoglobina , pero no unía monóxido de carbono . [119] Se generó una estructura proteica similar para respaldar una variedad de actividades oxidorreductasa [120] mientras que otra formó una ATPasa estructural y secuencialmente nueva . [121] Otro grupo generó una familia de receptores acoplados a proteína G que podrían ser activados por la pequeña molécula inerte N-óxido de clozapina pero insensibles al ligando nativo , la acetilcolina ; Estos receptores se conocen como DREADD . [122] También se pueden diseñar nuevas funcionalidades o especificidad de proteínas utilizando enfoques computacionales. Un estudio pudo utilizar dos métodos computacionales diferentes: un método de bioinformática y modelado molecular para extraer bases de datos de secuencias, y un método computacional de diseño de enzimas para reprogramar la especificidad de las enzimas. Ambos métodos dieron como resultado enzimas diseñadas con una especificidad superior a 100 veces para la producción de alcoholes de cadena más larga a partir de azúcar. [123]
Otra investigación común es la expansión del conjunto natural de 20 aminoácidos . Excluyendo los codones de terminación , se han identificado 61 codones , pero generalmente sólo 20 aminoácidos están codificados en todos los organismos. Ciertos codones están diseñados para codificar aminoácidos alternativos, incluidos: aminoácidos no estándar como O-metil tirosina ; o aminoácidos exógenos tales como 4-fluorofenilalanina. Por lo general, estos proyectos utilizan pares de ARNt supresor sin sentido recodificados y aminoacil ARNt sintetasa de otros organismos, aunque en la mayoría de los casos se requiere una ingeniería sustancial. [124]
Otros investigadores investigaron la estructura y función de las proteínas reduciendo el conjunto normal de 20 aminoácidos. Las bibliotecas de secuencias de proteínas limitadas se crean generando proteínas en las que los grupos de aminoácidos pueden reemplazarse por un solo aminoácido. [125] Por ejemplo, varios aminoácidos no polares dentro de una proteína se pueden reemplazar con un solo aminoácido no polar. [126] Un proyecto demostró que una versión modificada de la corismato mutasa todavía tenía actividad catalítica cuando solo se usaban nueve aminoácidos. [127]
Investigadores y empresas practican la biología sintética para sintetizar enzimas industriales con alta actividad, rendimientos óptimos y eficacia. Estas enzimas sintetizadas tienen como objetivo mejorar productos como los detergentes y los productos lácteos sin lactosa, además de hacerlos más rentables. [128] Las mejoras de la ingeniería metabólica mediante la biología sintética son un ejemplo de una técnica biotecnológica utilizada en la industria para descubrir productos farmacéuticos y químicos fermentativos. La biología sintética puede investigar sistemas de vías modulares en la producción bioquímica y aumentar el rendimiento de la producción metabólica. La actividad enzimática artificial y los efectos posteriores sobre las velocidades y rendimientos de las reacciones metabólicas pueden desarrollar "nuevas estrategias eficientes para mejorar las propiedades celulares... para la producción bioquímica de importancia industrial". [129]
Los científicos pueden codificar información digital en una sola hebra de ADN sintético . En 2012, George M. Church codificó uno de sus libros sobre biología sintética en ADN. Los 5,3 Mb de datos eran más de 1.000 veces mayores que la mayor cantidad de información almacenada anteriormente en ADN sintetizado. [130] Un proyecto similar codificó los sonetos completos de William Shakespeare en ADN. [131] De manera más general, algoritmos como NUPACK, [132] ViennaRNA, [133] Calculadora del sitio de unión de ribosomas, [134] Cello, [135] y Calculadora de partes no repetitivas [136] permiten el diseño de nuevos sistemas genéticos.
Se han desarrollado muchas tecnologías para incorporar nucleótidos y aminoácidos no naturales en ácidos nucleicos y proteínas, tanto in vitro como in vivo. Por ejemplo, en mayo de 2014, los investigadores anunciaron que habían introducido con éxito dos nuevos nucleótidos artificiales en el ADN bacteriano. Al incluir nucleótidos artificiales individuales en los medios de cultivo, pudieron intercambiar las bacterias 24 veces; no generaron ARNm ni proteínas capaces de utilizar los nucleótidos artificiales. [137] [138] [139]
La biología sintética despertó el interés de la NASA porque podría ayudar a producir recursos para los astronautas a partir de una cartera restringida de compuestos enviados desde la Tierra. [140] [141] [142] En Marte, en particular, la biología sintética podría conducir a procesos de producción basados en recursos locales, convirtiéndola en una poderosa herramienta en el desarrollo de puestos de avanzada ocupados con menos dependencia de la Tierra. [140] Se ha trabajado en el desarrollo de cepas de plantas que sean capaces de hacer frente al duro entorno marciano, utilizando técnicas similares a las empleadas para aumentar la resistencia a ciertos factores ambientales en los cultivos agrícolas. [143]
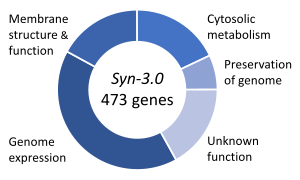
Un tema importante en biología sintética es la vida sintética , que se ocupa de organismos hipotéticos creados in vitro a partir de biomoléculas y/o análogos químicos de las mismas . Los experimentos de vida sintética intentan investigar los orígenes de la vida , estudiar algunas de las propiedades de la vida o, de manera más ambiciosa, recrear la vida a partir de componentes no vivos ( abióticos ). La biología biológica sintética intenta crear organismos vivos capaces de llevar a cabo funciones importantes, desde fabricar productos farmacéuticos hasta desintoxicar tierras y aguas contaminadas. [145] En medicina, ofrece perspectivas de utilizar piezas biológicas de diseño como punto de partida para nuevas clases de terapias y herramientas de diagnóstico. [145]
Una "célula artificial" viva ha sido definida como una célula completamente sintética que puede captar energía , mantener gradientes iónicos , contener macromoléculas además de almacenar información y tener la capacidad de mutar . [146] Nadie ha podido crear una célula así. [146]
En 2010, Craig Venter produjo un cromosoma bacteriano completamente sintético y su equipo lo introdujo en células huésped bacterianas genómicamente vaciadas. [19] Las células huésped pudieron crecer y replicarse. [147] [148] El laboratorio de Mycoplasma es el único organismo vivo con un genoma completamente diseñado.
En 2014 se presentó el primer organismo vivo con código de ADN expandido 'artificial'; El equipo utilizó E. coli a cuyo genoma se le extrajo y se reemplazó con un cromosoma con un código genético ampliado. Los nucleósidos añadidos son d5SICS y dNaM . [139]
En mayo de 2019, en un esfuerzo histórico, los investigadores informaron de la creación de una nueva forma sintética (posiblemente artificial ) de vida viable , una variante de la bacteria Escherichia coli , al reducir el número natural de 64 codones en el genoma bacteriano a 59 codones. , para codificar 20 aminoácidos . [25] [26]
En 2017, se inició la colaboración internacional de investigación de código abierto a gran escala Build-a-Cell para la construcción de células vivas sintéticas, [149] seguida de organizaciones nacionales de células sintéticas en varios países, incluidas FabriCell, [150] MaxSynBio [151 ] y BaSyC. [152] Los esfuerzos europeos sobre células sintéticas se unificaron en 2019 como iniciativa SynCellEU. [153]
En 2023, los investigadores pudieron crear los primeros embriones humanos obtenidos sintéticamente derivados de células madre. [154]
En terapéutica, la biología sintética ha logrado avances significativos al alterar y simplificar el alcance terapéutico en un período de tiempo relativamente corto. De hecho, nuevas plataformas terapéuticas, desde el descubrimiento de mecanismos de enfermedades y dianas farmacológicas hasta la fabricación y transporte de moléculas pequeñas, son posibles gracias a la construcción de diseños de componentes biológicos lógicos y guiados por modelos. [60]
Los dispositivos de biología sintética han sido diseñados para actuar como terapias en el tratamiento terapéutico. Es posible controlar virus y organismos creados completos para atacar patógenos particulares y vías enfermas. Así, en dos estudios independientes 91,92, los investigadores utilizaron bacteriófagos genéticamente modificados para combatir las bacterias resistentes a los antibióticos, dándoles características genéticas que atacan específicamente y obstaculizan las defensas bacterianas contra la actividad de los antibióticos. [155]
En la terapia del cáncer , dado que los medicamentos convencionales con frecuencia se dirigen indiscriminadamente a tumores y tejidos normales, pueden ser útiles virus y organismos creados artificialmente que puedan identificar y conectar su acción terapéutica con señales patológicas. Por ejemplo, la actividad de la vía p53 en células humanas se introdujo en adenovirus para controlar cómo se replicaban. [155]
Las bacterias se han utilizado durante mucho tiempo en el tratamiento del cáncer. Bifidobacterium y Clostridium colonizan selectivamente los tumores y reducen su tamaño. [156] Recientemente, los biólogos sintéticos reprogramaron bacterias para detectar y responder a un estado de cáncer particular. La mayoría de las veces se utilizan bacterias para administrar una molécula terapéutica directamente al tumor para minimizar los efectos no deseados. Para atacar las células tumorales, se expresaron péptidos que pueden reconocer específicamente un tumor en las superficies de las bacterias. Los péptidos utilizados incluyen una molécula aficuerpo que se dirige específicamente al receptor 2 del factor de crecimiento epidérmico humano [157] y una adhesina sintética . [158] La otra forma es permitir que las bacterias detecten el microambiente del tumor , por ejemplo, la hipoxia, mediante la construcción de una puerta lógica AND en las bacterias. [159] Luego, las bacterias solo liberan moléculas terapéuticas objetivo al tumor a través de la lisis [160] o del sistema de secreción bacteriana . [161] La lisis tiene la ventaja de que puede estimular el sistema inmunológico y controlar el crecimiento. Se pueden utilizar múltiples tipos de sistemas de secreción y también otras estrategias. El sistema es inducible por señales externas. Los inductores incluyen ondas químicas, electromagnéticas o de luz.
En estas terapéuticas se aplican múltiples especies y cepas. Las bacterias más utilizadas son Salmonella typhimurium , Escherichia coli , Bifidobacteria , Streptococcus , Lactobacillus , Listeria y Bacillus subtilis . Cada una de estas especies tiene sus propias propiedades y son exclusivas de la terapia contra el cáncer en términos de colonización de tejidos, interacción con el sistema inmunológico y facilidad de aplicación.
Plataforma diseñada a base de levadura
Los biólogos sintéticos están desarrollando levadura viva modificada genéticamente que puede administrar medicamentos biológicos terapéuticos. Cuando se administran por vía oral, estas levaduras vivas actúan como microfábricas y producirán moléculas terapéuticas directamente en el tracto gastrointestinal. Dado que las levaduras son eucariotas, un beneficio clave es que pueden administrarse junto con antibióticos. La levadura probiótica que expresa el receptor purinérgico P2Y2 humano suprimió la inflamación intestinal en modelos de ratón de enfermedad inflamatoria intestinal. [162] Se ha desarrollado una levadura S. boulardii viva que libera una antitoxina tetraespecífica que neutraliza potentemente las toxinas A y B de Clostridioides difficile. Esta antitoxina terapéutica es una fusión de cuatro anticuerpos de dominio único ( nanocuerpos ) que neutralizan potente y ampliamente los dos principales factores de virulencia de C. difficile en el sitio de la infección en modelos preclínicos. [163] El primer ensayo clínico en humanos de levadura viva diseñada para el tratamiento de la infección por Clostridium difficile se prevé para 2024 y será patrocinado por el desarrollador Fzata, Inc.
El sistema inmunológico desempeña un papel importante en el cáncer y puede aprovecharse para atacar las células cancerosas. Las terapias basadas en células se centran en inmunoterapias , principalmente mediante la ingeniería de células T.
"Los receptores de células T fueron diseñados y "entrenados" para detectar epítopos del cáncer . Los receptores de antígenos quiméricos (CAR) están compuestos por un fragmento de un anticuerpo fusionado a dominios de señalización de células T intracelulares que pueden activar y desencadenar la proliferación de la célula. La FDA ha aprobado múltiples terapias basadas en CAR de segunda generación. [164]
Los interruptores genéticos se diseñaron para mejorar la seguridad del tratamiento. Los interruptores de apagado se desarrollaron para interrumpir la terapia si el paciente presenta efectos secundarios graves. [165] Los mecanismos pueden controlar más finamente el sistema y detenerlo y reactivarlo. [166] [167] Dado que la cantidad de células T es importante para la persistencia y la gravedad de la terapia, el crecimiento de las células T también se controla para marcar la efectividad y seguridad de la terapia. [168]
Aunque varios mecanismos pueden mejorar la seguridad y el control, las limitaciones incluyen la dificultad de inducir grandes circuitos de ADN en las células y los riesgos asociados con la introducción de componentes extraños, especialmente proteínas, en las células.
El biocombustible más popular es el etanol producido a partir de maíz o caña de azúcar, pero este método de producción de biocombustibles es problemático y limitado debido al alto costo agrícola y las características inadecuadas del combustible del etanol. Un sustituto y una fuente potencial de energía renovable son los microbios cuyas rutas metabólicas han sido alteradas para ser más eficientes en la conversión de biomasa en biocombustibles. Sólo si se logra que sus costos de producción igualen o incluso superen los de la producción actual de combustible se podrá esperar que estas técnicas tengan éxito. En relación con esto, existen varios medicamentos cuyos costosos procedimientos de fabricación les impiden tener un rango terapéutico mayor. La creación de nuevos materiales y la fabricación microbiológica de biomateriales se beneficiarían sustancialmente de las nuevas herramientas de biología artificial. [155]
El sistema de repeticiones palindrómicas cortas agrupadas frecuentemente interespaciadas (CRISPR)/asociado a CRISPR (Cas) es un método poderoso de ingeniería genómica en una variedad de organismos debido a su simplicidad, modularidad y escalabilidad. En esta técnica, un ARN guía (ARNg) atrae la nucleasa CRISPR Cas9 a un punto particular del genoma, provocando una rotura de la doble cadena. Se pueden utilizar varios procesos de reparación del ADN, incluida la recombinación dirigida por homología y la unión de extremos sin homología, para lograr el cambio genómico deseado (es decir, eliminación o inserción de genes). Además, dCas9 (Cas9 muerta o Cas9 deficiente en nucleasa), un doble mutante de Cas9 (H840A, D10A), se ha utilizado para controlar la expresión genética en bacterias o cuando se vincula a una estimulación del sitio de supresión en levadura. [169]
Para construir y desarrollar sistemas biológicos, los componentes reguladores, incluidos los reguladores, los sitios de unión a ribosomas (RBS) y los terminadores, son cruciales. A pesar de años de estudio, existen muchas variedades y números de promotores y terminadores para Escherichia coli, pero también para el organismo modelo Saccharomyces cerevisiae, bien investigado, así como para otros organismos de interés, estas herramientas son bastante escasas. Se han inventado numerosas técnicas para encontrar e identificar promotores y terminadores con el fin de superar esta limitación, incluida la minería del genoma, la mutagénesis aleatoria, la ingeniería híbrida, el modelado biofísico, el diseño combinatorio y el diseño racional. [169]
La biología sintética se ha utilizado para los organoides , que son órganos cultivados en laboratorio con aplicación a la investigación médica y los trasplantes. [170]
La bioimpresión 3D se puede utilizar para reconstruir tejido de diversas regiones del cuerpo. El precursor de la adopción de la impresión 3D en la atención sanitaria fue una serie de ensayos realizados por investigadores del Boston Children's Hospital. El equipo construyó a mano vejigas urinarias de reemplazo para siete pacientes mediante la construcción de andamios, luego los colocó en capas con células de los pacientes y les permitió crecer. Los ensayos fueron un éxito ya que los pacientes mantuvieron su buena salud 7 años después de la implantación, lo que llevó a un investigador llamado Anthony Atala, MD, a buscar formas de automatizar el proceso. [171] Los pacientes con enfermedad de la vejiga en etapa terminal ahora pueden ser tratados utilizando tejidos de vejiga creados mediante bioingeniería para reconstruir el órgano dañado. [172] Esta tecnología también se puede aplicar potencialmente a huesos, piel, cartílagos y tejidos musculares. [173] Aunque un objetivo a largo plazo de la tecnología de bioimpresión 3D es reconstruir un órgano completo y minimizar el problema de la falta de órganos para trasplante. [174] Ha habido poco éxito en la bioimpresión de órganos completamente funcionales, por ejemplo, hígado, piel, menisco o páncreas. [175] [176] [177] A diferencia de los stents implantables, los órganos tienen formas complejas y son significativamente más difíciles de bioimprimir. Un corazón bioimpreso, por ejemplo, no sólo debe cumplir requisitos estructurales, sino también de vascularización, carga mecánica y propagación de señales eléctricas. [178] En 2022, se informó del primer éxito de un ensayo clínico para un trasplante bioimpreso en 3D que se elabora a partir de las propias células del paciente, un oído externo para tratar la microtia , [179] . [180]
La bioimpresión 3D contribuye a avances significativos en el campo médico de la ingeniería de tejidos al permitir la investigación de materiales innovadores llamados biomateriales . Algunas de las sustancias más notables obtenidas mediante bioingeniería suelen ser más fuertes que los materiales corporales promedio, incluidos los tejidos blandos y los huesos. Estos componentes pueden actuar como futuros sustitutos, e incluso mejoras, de los materiales originales de la carrocería. Además, la Agencia de Reducción de Amenazas de Defensa pretende imprimir miniórganos como corazones, hígados y pulmones como potencial para probar nuevos medicamentos con mayor precisión y tal vez eliminar la necesidad de realizar pruebas en animales. [181]
Se están realizando investigaciones y desarrollo de métodos basados en la biología sintética para inducir la regeneración en humanos [ ¿relevante? ] así como la creación de órganos artificiales trasplantables .
La biología sintética se puede utilizar para crear nanopartículas que se pueden utilizar para la administración de fármacos y para otros fines. [182] Como complemento a la investigación y el desarrollo se busca y se ha creado células sintéticas que imitan funciones de las células biológicas. Las aplicaciones incluyen medicamentos como las nanopartículas de diseño que hacen que las células sanguíneas devoren, de adentro hacia afuera, porciones de la placa aterosclerótica que causa ataques cardíacos. [183] [184] [185] Microgotas sintéticas para células de algas o reactores microbianos esferoides multicelulares sinérgicos de algas y bacterias , por ejemplo, podrían usarse para producir hidrógeno como biotecnología de economía de hidrógeno . [186] [187]
Las células de diseño de mamíferos son diseñadas por humanos para comportarse de una manera específica, como una célula inmune que expresa un receptor sintético diseñado para combatir una enfermedad específica. [188] [189] La electrogenética es una aplicación de la biología sintética que implica la utilización de campos eléctricos para estimular una respuesta en células diseñadas. [190] El control de las células de diseño se puede realizar con relativa facilidad mediante el uso de dispositivos electrónicos comunes, como los teléfonos inteligentes. Además, la electrogenética permite la posibilidad de crear dispositivos mucho más pequeños y compactos que los dispositivos que utilizan otros estímulos mediante el uso de electrodos microscópicos. [190] Un ejemplo de cómo se utiliza la electrogenética para beneficiar la salud pública es mediante la estimulación de células de diseño que son capaces de producir o administrar terapias. [191] Esto se implementó en celdas Electro HEK, celdas que contienen canales de calcio dependientes de voltaje que son electrosensibles, lo que significa que el canal iónico puede controlarse mediante conducción eléctrica entre los electrodos y las celdas Electro HEK. [190] Se demostró que los niveles de expresión del gen artificial que contenían estas células Electro HEK podían controlarse cambiando el voltaje o la longitud del pulso eléctrico. Se han ampliado más estudios sobre este robusto sistema, uno de los cuales es un sistema de línea de células beta diseñado para controlar la liberación de insulina basándose en señales eléctricas. [192]
La creación de nueva vida y la manipulación de la vida existente han planteado preocupaciones éticas en el campo de la biología sintética y se están discutiendo activamente. [193] [194]
Las preguntas éticas comunes incluyen:
Los aspectos éticos de la biología sintética tienen tres características principales: bioseguridad , bioprotección y creación de nuevas formas de vida. [196] Otras cuestiones éticas mencionadas incluyen la regulación de nuevas creaciones, la gestión de patentes de nuevas creaciones, la distribución de beneficios y la integridad de la investigación. [197] [193]
Han surgido cuestiones éticas en relación con las tecnologías de ADN recombinante y de organismos genéticamente modificados (OGM), y en muchas jurisdicciones existían amplias regulaciones sobre ingeniería genética e investigación de patógenos. Amy Gutmann , ex jefa de la Comisión Presidencial de Bioética, argumentó que deberíamos evitar la tentación de regular excesivamente la biología sintética en general y la ingeniería genética en particular. Según Gutmann, "la parsimonia regulatoria es especialmente importante en las tecnologías emergentes... donde la tentación de reprimir la innovación basándose en la incertidumbre y el miedo a lo desconocido es particularmente grande. Los instrumentos contundentes de restricción legal y regulatoria pueden no sólo inhibir la distribución de nuevos beneficios, pero puede ser contraproducente para la seguridad y la protección al impedir que los investigadores desarrollen salvaguardias efectivas". [198]
Una cuestión ética es si es aceptable o no crear nuevas formas de vida, lo que a veces se conoce como "jugar a ser Dios". Actualmente, la creación de nuevas formas de vida que no están presentes en la naturaleza se realiza a pequeña escala, los posibles beneficios y peligros siguen siendo desconocidos y la mayoría de los estudios están garantizados por una cuidadosa consideración y supervisión. [193] Muchos defensores expresan el gran valor potencial (para la agricultura, la medicina y el conocimiento académico, entre otros campos) de la creación de formas de vida artificiales. La creación de nuevas entidades podría ampliar el conocimiento científico mucho más allá de lo que se sabe actualmente a partir del estudio de los fenómenos naturales. Sin embargo, existe la preocupación de que las formas de vida artificiales puedan reducir la "pureza" de la naturaleza (es decir, la naturaleza podría corromperse de alguna manera por la intervención y manipulación humana) y potencialmente influir en la adopción de principios más parecidos a la ingeniería en lugar de ideales centrados en la biodiversidad y la naturaleza. A algunos también les preocupa que si se liberara una forma de vida artificial en la naturaleza, podría obstaculizar la biodiversidad al desplazar a las especies naturales en busca de recursos (de manera similar a como la proliferación de algas mata a las especies marinas). Otra preocupación tiene que ver con el tratamiento ético de entidades recién creadas si sienten dolor , sensibilidad y autopercepción. Existe un debate en curso sobre si a estas formas de vida se les deben otorgar derechos morales o legales, aunque no existe consenso sobre cómo se administrarían o harían cumplir estos derechos.
Los fundamentos éticos y morales que respaldan ciertas aplicaciones de la biología sintética incluyen su potencial mitigación de importantes problemas globales de impactos ambientales perjudiciales de la agricultura convencional (incluida la producción de carne ), el bienestar animal , la seguridad alimentaria y la salud humana , [199] [200] [201 ] [202] así como la posible reducción de las necesidades de trabajo humano y, a través de terapias de enfermedades, la reducción del sufrimiento humano y la prolongación de la vida.
¿Qué es éticamente más apropiado al considerar medidas de bioseguridad? ¿Cómo se puede evitar la introducción accidental de vida sintética en el entorno natural? Se ha dado mucha consideración ética y pensamiento crítico a estas cuestiones. La bioseguridad no sólo se refiere a la contención biológica; también se refiere a los pasos dados para proteger al público de agentes biológicos potencialmente peligrosos. Aunque estas preocupaciones son importantes y siguen sin respuesta, no todos los productos de biología sintética presentan preocupaciones por la seguridad biológica o consecuencias negativas para el medio ambiente. Se argumenta que la mayoría de las tecnologías sintéticas son benignas y son incapaces de prosperar en el mundo exterior debido a sus características "antinaturales", ya que todavía no hay un ejemplo de un microbio transgénico al que se le confiera una ventaja de aptitud física en la naturaleza.
En general, los controles de peligros existentes , las metodologías de evaluación de riesgos y las regulaciones desarrolladas para los organismos genéticamente modificados (OGM) tradicionales se consideran suficientes para los organismos sintéticos. Los métodos de biocontención "extrínsecos" en el contexto de un laboratorio incluyen la contención física mediante gabinetes y cajas de guantes de bioseguridad , así como equipos de protección personal . En un contexto agrícola, incluyen distancias de aislamiento y barreras de polen , similares a los métodos de biocontención de OGM . Los organismos sintéticos pueden ofrecer un mayor control de peligros porque pueden diseñarse con métodos de biocontención "intrínsecos" que limitan su crecimiento en un entorno no contenido o evitan la transferencia horizontal de genes a organismos naturales. Ejemplos de biocontención intrínseca incluyen auxotrofia , interruptores de muerte biológica , incapacidad del organismo para replicarse o transmitir genes modificados o sintéticos a la descendencia y el uso de organismos xenobiológicos que utilizan bioquímica alternativa, por ejemplo, el uso de ácidos xenonucleicos artificiales (XNA) en lugar de ADN. . [203] [204] En cuanto a la auxotrofia, se pueden diseñar bacterias y levaduras para que no puedan producir histidina , un aminoácido importante para toda la vida. Por lo tanto, estos organismos sólo pueden cultivarse en medios ricos en histidina en condiciones de laboratorio, anulando los temores de que puedan propagarse a áreas indeseables.
Algunas cuestiones éticas se relacionan con la bioseguridad, donde las tecnologías biosintéticas podrían usarse deliberadamente para causar daño a la sociedad y/o al medio ambiente. Dado que la biología sintética plantea cuestiones éticas y de bioseguridad, la humanidad debe considerar y planificar cómo lidiar con creaciones potencialmente dañinas y qué tipo de medidas éticas podrían emplearse para disuadir las nefastas tecnologías biosintéticas. Sin embargo , con la excepción de la regulación de las empresas de biología sintética y biotecnología, [205] [206] , las cuestiones no se consideran nuevas porque surgieron durante los debates anteriores sobre el ADN recombinante y los organismos genéticamente modificados (OGM), y las extensas regulaciones de la ingeniería genética. y la investigación de patógenos ya está en marcha en muchas jurisdicciones. [207]
Además, el desarrollo de herramientas de biología sintética ha facilitado que las personas con menos educación, capacitación y acceso a equipos modifiquen y utilicen organismos patógenos como armas biológicas. Esto aumenta la amenaza del bioterrorismo , especialmente a medida que los grupos terroristas toman conciencia de los importantes trastornos sociales, económicos y políticos causados por pandemias como la COVID-19 . A medida que se desarrollen nuevas técnicas en el campo de la biología sintética, es probable que el riesgo de bioterrorismo siga aumentando. [208] Juan Zárate, quien se desempeñó como Asesor Adjunto de Seguridad Nacional para la Lucha contra el Terrorismo de 2005 a 2009, señaló que "la gravedad y la perturbación extrema de un nuevo coronavirus probablemente estimularán la imaginación de los grupos e individuos más creativos y peligrosos para reconsiderar la posibilidad de actuar como bioterroristas". ataques." [209]
El proyecto SYNBIOSAFE [210] , financiado por la Unión Europea, ha publicado informes sobre cómo gestionar la biología sintética. Un documento de 2007 identificó cuestiones clave en seguridad, protección, ética y la interfaz ciencia-sociedad, que el proyecto definió como educación pública y diálogo continuo entre científicos, empresas, gobiernos y especialistas en ética. [211] [212] Los problemas de seguridad clave que SYNBIOSAFE identificó involucraron la participación de empresas que venden ADN sintético y la comunidad de biohacking de biólogos aficionados. Las cuestiones éticas clave se referían a la creación de nuevas formas de vida.
Un informe posterior se centró en la bioseguridad, especialmente el llamado desafío del doble uso . Por ejemplo, si bien la biología sintética puede conducir a una producción más eficiente de tratamientos médicos, también puede conducir a la síntesis o modificación de patógenos dañinos (por ejemplo, la viruela ). [213] La comunidad de biohacking sigue siendo una fuente de especial preocupación, ya que la naturaleza distribuida y difusa de la biotecnología de código abierto dificulta el seguimiento, la regulación o la mitigación de posibles preocupaciones sobre la bioseguridad y la bioprotección. [214]
COSY, otra iniciativa europea, se centra en la percepción y la comunicación públicas. [215] [216] [217] Para comunicar mejor la biología sintética y sus ramificaciones sociales a un público más amplio, COZY y SYNBIOSAFE publicaron SYNBIOSAFE , un documental de 38 minutos, en octubre de 2009. [210]
La Asociación Internacional de Biología Sintética ha propuesto la autorregulación. [218] En este se proponen medidas específicas que la industria de la biología sintética, especialmente las empresas de síntesis de ADN, deberían implementar. En 2007, un grupo dirigido por científicos de empresas líderes en síntesis de ADN publicó un "plan práctico para desarrollar un marco de supervisión eficaz para la industria de la síntesis de ADN". [205]
En enero de 2009, la Fundación Alfred P. Sloan financió el Centro Woodrow Wilson , el Centro Hastings y el Instituto J. Craig Venter para examinar la percepción pública, la ética y las implicaciones políticas de la biología sintética. [219]
Los días 9 y 10 de julio de 2009, el Comité de Ciencia, Tecnología y Derecho de las Academias Nacionales convocó un simposio sobre "Oportunidades y desafíos en el campo emergente de la biología sintética". [220]
Después de la publicación del primer genoma sintético y la consiguiente cobertura mediática sobre la creación de "vida", el presidente Barack Obama estableció la Comisión Presidencial para el Estudio de Cuestiones Bioéticas para estudiar la biología sintética. [221] La comisión convocó una serie de reuniones y publicó un informe en diciembre de 2010 titulado "Nuevas direcciones: la ética de la biología sintética y las tecnologías emergentes". La comisión afirmó que "si bien el logro de Venter marcó un avance técnico significativo al demostrar que un genoma relativamente grande podía sintetizarse con precisión y sustituirse por otro, no equivalía a la" creación de vida ". [222] Señaló que la biología sintética es un campo emergente, que crea riesgos y recompensas potenciales. La comisión no recomendó cambios de política o supervisión y pidió una financiación continua de la investigación y nuevos fondos para el seguimiento, el estudio de las cuestiones éticas emergentes y la educación pública [207] .
La biología sintética, como herramienta importante para los avances biológicos, genera "el potencial para desarrollar armas biológicas, posibles impactos negativos imprevistos sobre la salud humana... y cualquier posible impacto ambiental". [223] La proliferación de dicha tecnología también podría hacer que la producción de armas biológicas y químicas esté disponible para una gama más amplia de actores estatales y no estatales . [224] Estos problemas de seguridad pueden evitarse regulando los usos industriales de la biotecnología a través de legislación política. Las directrices federales sobre manipulación genética están siendo propuestas por "la Comisión de Bioética del Presidente... en respuesta a la creación anunciada de una célula autorreplicante a partir de un genoma sintetizado químicamente, presentó 18 recomendaciones no sólo para regular la ciencia... para educar el público". [223]
El 13 de marzo de 2012, más de 100 grupos ambientalistas y de la sociedad civil, incluidos Amigos de la Tierra , el Centro Internacional de Evaluación de Tecnología y el Grupo ETC , emitieron el manifiesto Los Principios para la Supervisión de la Biología Sintética . Este manifiesto pide una moratoria mundial sobre la liberación y el uso comercial de organismos sintéticos hasta que se establezcan regulaciones más sólidas y medidas de bioseguridad rigurosas. Los grupos piden específicamente una prohibición total del uso de biología sintética en el genoma humano o el microbioma humano . [225] [226] Richard Lewontin escribió que algunos de los principios de seguridad para la supervisión discutidos en Los Principios para la Supervisión de la Biología Sintética son razonables, pero que el principal problema con las recomendaciones del manifiesto es que "el público en general carece de la capacidad de hacer cumplir cualquier aplicación significativa de esas recomendaciones". [227]
Los peligros de la biología sintética incluyen peligros de bioseguridad para los trabajadores y el público, peligros de bioseguridad derivados de la ingeniería deliberada de organismos para causar daño y peligros ambientales. Los riesgos de bioseguridad son similares a los de los campos existentes de la biotecnología, principalmente la exposición a patógenos y sustancias químicas tóxicas, aunque los nuevos organismos sintéticos pueden tener riesgos novedosos. [203] En cuanto a la bioseguridad, existe la preocupación de que los organismos sintéticos o rediseñados puedan teóricamente utilizarse para el bioterrorismo . Los riesgos potenciales incluyen recrear patógenos conocidos desde cero, diseñar patógenos existentes para que sean más peligrosos y diseñar microbios para que produzcan bioquímicos dañinos. [228] Por último, los peligros ambientales incluyen efectos adversos sobre la biodiversidad y los servicios de los ecosistemas , incluidos posibles cambios en el uso de la tierra como resultado del uso agrícola de organismos sintéticos. [229] [230] La biología sintética es un ejemplo de una tecnología de doble uso con el potencial de usarse de maneras que podrían dañar intencionalmente o no a los humanos y/o dañar el medio ambiente. A menudo "los científicos, sus instituciones anfitrionas y organismos de financiación" consideran si la investigación planificada podría ser mal utilizada y, en ocasiones, implementan medidas para reducir la probabilidad de mal uso. [231]
Los sistemas existentes de análisis de riesgos para los OGM generalmente se consideran suficientes para los organismos sintéticos, aunque puede haber dificultades para un organismo construido "de abajo hacia arriba" a partir de secuencias genéticas individuales. [204] [232] La biología sintética generalmente se rige por las regulaciones existentes para los OGM y la biotecnología en general, y cualquier regulación que exista para productos comerciales posteriores, aunque generalmente no existen regulaciones en ninguna jurisdicción que sean específicas de la biología sintética. [233] [234]
{{cite journal}}: Parámetro desconocido |agency=ignorado ( ayuda ){{cite news}}: |last2=tiene nombre genérico ( ayuda ){{cite web}}: Falta o está vacío |title=( ayuda ){{cite book}}: |website=ignorado ( ayuda ){{cite book}}: |website=ignorado ( ayuda )