Como medicamento , la insulina es cualquier preparación farmacéutica de la hormona proteica insulina que se utiliza para tratar la hiperglucemia . [6] Dichas afecciones incluyen diabetes tipo 1 , diabetes tipo 2 , diabetes gestacional y complicaciones de la diabetes como cetoacidosis diabética y estados hiperglucémicos hiperosmolares . [6] La insulina también se usa junto con la glucosa para tratar la hipercalemia (niveles altos de potasio en sangre). [7] Por lo general, se administra mediante inyección debajo de la piel , pero algunas formas también se pueden usar mediante inyección en una vena o músculo . [6] Existen varios tipos de insulina, adecuados para varios períodos de tiempo. A menudo, todos los tipos se denominan insulina en un sentido amplio , aunque en un sentido más preciso, la insulina es idéntica a la molécula natural, mientras que los análogos de insulina tienen moléculas ligeramente diferentes que permiten un tiempo de acción modificado. Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [8] En 2021, fue el medicamento número 179 más recetado en los Estados Unidos, con más de 2 millones de recetas. [9] [10]
La insulina se puede fabricar a partir del páncreas de cerdos o vacas. [11] Las versiones humanas se pueden fabricar modificando versiones de cerdos o mediante tecnología recombinante [11] utilizando principalmente E. coli o Saccharomyces cerevisiae . [12] Viene en tres tipos principales: de acción corta (como la insulina regular ), de acción intermedia (como la insulina protamina neutra Hagedorn (NPH)) y de acción más prolongada (como la insulina glargina ). [11]
La insulina fue utilizada por primera vez como medicamento en Canadá por Charles Best y Frederick Banting en 1922. [13] [14]
Esta es una cronología de los hitos clave en la historia del uso médico de la insulina. Para obtener más detalles sobre el descubrimiento, la extracción, la purificación, el uso clínico y la síntesis de la insulina, consulte Insulina



La insulina se utiliza para tratar diversas enfermedades, entre ellas la diabetes y sus complicaciones agudas, como la cetoacidosis diabética y los estados hiperglucémicos hiperosmolares . También se utiliza junto con la glucosa para tratar los niveles elevados de potasio en sangre . Su uso durante el embarazo es relativamente seguro para el bebé. [6] La insulina se utilizaba anteriormente en un tratamiento psiquiátrico llamado terapia de choque insulínico . [22]
Algunos efectos secundarios son hipoglucemia (bajo nivel de azúcar en sangre), hipocalemia (bajo nivel de potasio en sangre) y reacciones alérgicas . [6] La alergia a la insulina afecta a alrededor del 2% de las personas, de las cuales la mayoría de las reacciones no se deben a la insulina en sí, sino a conservantes añadidos a la insulina, como zinc, protamina y metacresol . La mayoría de las reacciones son reacciones de hipersensibilidad de tipo I y rara vez causan anafilaxia . Una alergia sospechada a la insulina puede confirmarse mediante pruebas de punción cutánea , pruebas de parche y, ocasionalmente, biopsia de piel . La terapia de primera línea contra las reacciones de hipersensibilidad a la insulina incluye terapia sintomática con antihistamínicos. Luego, las personas afectadas cambian a una preparación que no contiene el agente específico al que están reaccionando o se someten a una desensibilización . [23]
Efectos adversos cutáneos
Otros efectos secundarios pueden incluir dolor o cambios en la piel en los lugares de inyección. La inyección subcutánea repetida sin rotación del lugar puede provocar lipohipertrofia y amiloidomas, que se manifiestan como nódulos firmes palpables debajo de la piel. [24]
El inicio temprano de la terapia con insulina para el manejo a largo plazo de enfermedades como la diabetes tipo 2 sugeriría que el uso de insulina tiene beneficios únicos; sin embargo, con la terapia con insulina, existe la necesidad de aumentar gradualmente la dosis y la complejidad del régimen, así como la probabilidad de desarrollar hipoglucemia grave, por lo que muchas personas y sus médicos dudan en comenzar la terapia con insulina en la etapa temprana del manejo de la enfermedad. [25] Muchos obstáculos asociados con los comportamientos de salud también impiden que las personas con diabetes mellitus tipo 2 comiencen o intensifiquen su tratamiento con insulina, incluida la falta de motivación, la falta de familiaridad o experiencia con los tratamientos y las restricciones de tiempo que hacen que las personas tengan cargas glucémicas altas durante períodos prolongados de tiempo antes de comenzar la terapia con insulina. Es por eso que el manejo de los efectos secundarios asociados con el uso sistemático temprano a largo plazo de insulina para la diabetes mellitus tipo 2 puede resultar un desafío terapéutico y conductual. [26]
La insulina es una hormona endógena producida por el páncreas . [29] La proteína insulina se ha conservado en gran medida a lo largo del tiempo evolutivo y está presente tanto en mamíferos como en invertebrados . La vía de señalización de la insulina/ factor de crecimiento similar a la insulina (IIS) se ha estudiado ampliamente en especies que incluyen gusanos nematodos (p. ej., C. elegans ), moscas ( Drosophila melanogaster ) y ratones ( Mus musculus ). Sus mecanismos de acción son muy similares en todas las especies. [30]
Tanto la diabetes tipo 1 como la diabetes tipo 2 se caracterizan por una pérdida de la función pancreática, aunque en distintos grados. [29] Las personas afectadas por diabetes se denominan diabéticos. Muchos diabéticos necesitan una fuente exógena de insulina para mantener sus niveles de azúcar en sangre dentro de un rango objetivo seguro. [31] [32] [33]
En 1916, Nicolae C. Paulescu (1869-1931) logró desarrollar un extracto pancreático acuoso que normalizó a un perro diabético. En 1921, publicó 4 artículos en la Sociedad de Biología de París centrados en los efectos exitosos del extracto pancreático en perros diabéticos. La investigación sobre el papel del páncreas en la asimilación de alimentos de Paulescu se publicó en agosto de 1921 en los Archives Internationales de Physiologie, Lieja, Bélgica. Inicialmente, la única forma de obtener insulina para uso clínico era extraerla del páncreas de otra criatura. Las glándulas animales se podían obtener como un producto de desecho de la industria empacadora de carne. La insulina se derivaba principalmente de vacas ( Eli Lilly and Company ) y cerdos ( Nordisk Insulinlaboratorium ). La fabricación de ocho onzas de insulina purificada podría requerir hasta dos toneladas de partes de cerdo. [34] [35] [36] La insulina de estas fuentes es eficaz en humanos, ya que es muy similar a la insulina humana (diferencia de tres aminoácidos en la insulina bovina, diferencia de un aminoácido en la porcina). [36] Inicialmente, la menor pureza de la preparación resultó en reacciones alérgicas a la presencia de sustancias no insulínicas. La pureza ha mejorado de manera constante desde la década de 1920, alcanzando finalmente una pureza del 99% a mediados de la década de 1970 gracias a los métodos de cromatografía líquida de alta presión (HPLC). Aún ocurren ocasionalmente reacciones alérgicas menores, incluso a las variedades de insulina "humana" sintética. [36]
Desde 1982, se fabrica insulina "humana" biosintética para uso clínico mediante técnicas de ingeniería genética que utilizan tecnología de ADN recombinante . Genentech desarrolló la técnica utilizada para producir la primera insulina de este tipo, Humulin, pero no comercializó el producto. Eli Lilly comercializó Humulin en 1982. [37] Humulin fue el primer medicamento producido mediante técnicas de ingeniería genética modernas en las que se inserta ADN humano real en una célula huésped ( E. coli en este caso). A continuación, se permite que las células huésped crezcan y se reproduzcan normalmente y, debido al ADN humano insertado, producen una versión sintética de la insulina humana. Los fabricantes afirman que esto reduce la presencia de muchas impurezas. Sin embargo, las preparaciones clínicas preparadas a partir de estas insulinas difieren de la insulina humana endógena en varios aspectos importantes; un ejemplo es la ausencia de péptido C , que en los últimos años ha demostrado tener efectos sistémicos. Novo Nordisk también ha desarrollado una insulina genéticamente modificada de forma independiente utilizando un proceso de levadura. [38] [39]
Según una encuesta que la Federación Internacional de Diabetes realizó en 2002 sobre el acceso y la disponibilidad de insulina en sus países miembros, aproximadamente el 70% de la insulina que se vende actualmente en el mundo es insulina "humana" biosintética recombinante. [40] La mayoría de la insulina que se utiliza clínicamente hoy en día se produce de esta manera, aunque la experiencia clínica ha proporcionado evidencia contradictoria sobre si estas insulinas tienen menos probabilidades de producir una reacción alérgica. Se han reportado reacciones adversas; estas incluyen pérdida de señales de advertencia de que los pacientes pueden caer en coma por hipoglucemia , convulsiones, pérdida de memoria y pérdida de concentración. [41] Sin embargo, la declaración de posición de la Federación Internacional de Diabetes de 2005 es muy clara al afirmar que "NO hay evidencia abrumadora para preferir una especie de insulina sobre otra" y "las insulinas animales [modernas, altamente purificadas] siguen siendo una alternativa perfectamente aceptable". [42]
Desde enero de 2006, todas las insulinas distribuidas en los EE. UU. y en algunos otros países son insulinas "humanas" sintéticas o sus análogos. Se requiere un proceso especial de importación de la FDA para obtener insulina de origen bovino o porcino para su uso en los EE. UU. [43] , aunque puede haber algunas existencias restantes de insulina porcina fabricada por Lilly en 2005 o antes, y la insulina porcina lenticular también se vende y comercializa bajo la marca Vetsulina (SM) en los EE. UU. para uso veterinario en el tratamiento de animales de compañía con diabetes. [44]
En la diabetes tipo 1, la producción de insulina es extremadamente baja y, por lo tanto, el cuerpo requiere insulina exógena . Algunas personas con diabetes tipo 2, en particular aquellas con valores muy altos de hemoglobina A1c , también pueden requerir una tasa basal de insulina, ya que su cuerpo está desensibilizado al nivel de insulina que se produce. La insulina basal regula la glucosa en sangre del cuerpo entre las comidas, así como durante la noche. Esta tasa basal de acción de la insulina generalmente se logra mediante el uso de una insulina de acción intermedia (como NPH) o un análogo de insulina de acción prolongada. En los diabéticos tipo 1, también se puede lograr mediante la infusión continua de insulina de acción rápida utilizando una bomba de insulina . Aproximadamente la mitad del requerimiento diario de insulina de una persona se administra como insulina basal, generalmente administrada una vez al día por la noche. [45]
Cuando una persona ingiere alimentos que contienen carbohidratos y glucosa, la insulina ayuda a regular el metabolismo de los alimentos en el cuerpo. La insulina prandial, también llamada insulina de la hora de la comida o insulina en bolo, está diseñada como una dosis de insulina en bolo antes de una comida para regular el pico de glucosa en sangre que se produce después de una comida. La dosis de insulina prandial puede ser estática o puede ser calculada por el paciente utilizando su nivel actual de azúcar en sangre, la ingesta planificada de carbohidratos o ambos. Este cálculo también puede realizarse mediante una bomba de insulina en pacientes que utilizan una bomba. Los regímenes de insulina que consisten en dosis calculadas de esta manera se consideran regímenes de insulina intensivos . [46] La insulina prandial generalmente se administra no más de 15 a 30 minutos antes de una comida utilizando una insulina de acción rápida o una insulina regular. En algunos pacientes, se puede utilizar una insulina combinada que contiene tanto insulina NPH (de acción prolongada) como una insulina rápida/regular para proporcionar tanto una insulina basal como una insulina prandial. [45]
El uso de insulina como tratamiento clínico para la diabetes implica varios desafíos: [47]
Las preparaciones médicas de insulina nunca son simplemente insulina en agua (sin nada más). Las insulinas clínicas son mezclas de insulina más otras sustancias, incluidos conservantes. Estos evitan que la proteína se estropee o desnaturalice demasiado rápido, retrasan la absorción de la insulina, ajustan el pH de la solución para reducir las reacciones en el lugar de la inyección, etc. [48]
Las ligeras variaciones de la molécula de insulina humana se denominan análogos de insulina (técnicamente, " ligandos del receptor de insulina "), así llamados porque técnicamente no son insulina, sino más bien análogos que conservan la funcionalidad de gestión de la glucosa de la hormona. Tienen características de absorción y actividad que actualmente no son posibles con la insulina inyectada por vía subcutánea. Se absorben rápidamente en un intento de imitar la insulina de las células beta reales (como ocurre con la insulina lispro , la insulina aspart y la insulina glulisina ), o se absorben de forma constante después de la inyección en lugar de tener un "pico" seguido de una disminución más o menos rápida de la acción de la insulina (como ocurre con la insulina detemir y la insulina glargina ), todo ello mientras se conserva la acción reductora de la glucosa de la insulina en el cuerpo humano. Sin embargo, una serie de metanálisis , incluidos los realizados por la Colaboración Cochrane en 2005, [49] el Instituto para la Calidad y la Rentabilidad en el Sector de la Atención Sanitaria [IQWiG] de Alemania publicado en 2007, [50] y la Agencia Canadiense de Medicamentos y Tecnología en Salud (CADTH) [51] también publicado en 2007 no han demostrado ventajas inequívocas en el uso clínico de análogos de insulina sobre tipos de insulina más convencionales. [50] [51]
Los tipos de insulina comúnmente utilizados son los siguientes. [29]
Incluye los análogos de insulina aspart , lispro y glulisina . Estos comienzan a funcionar en 5 a 15 minutos y están activos durante 3 a 4 horas. La mayoría de las insulinas forman hexámeros , que retrasan la entrada a la sangre en forma activa; estas insulinas análogas no lo hacen, pero tienen una actividad insulínica normal. Las variedades más nuevas están ahora pendientes de aprobación regulatoria en los EE. UU., que están diseñadas para funcionar rápidamente, pero conservan la misma estructura genética que la insulina humana regular . [52] [53]
Incluye la insulina regular , que comienza a actuar en 30 minutos y permanece activa durante aproximadamente 5 a 8 horas. [54]
Incluye la insulina NPH , que comienza a actuar en 1 a 3 horas y está activa durante 16 a 24 horas. [55]
Incluye los análogos glargina U100 y detemir , cada uno de los cuales comienza a actuar en 1 a 2 horas y continúa activo, sin picos ni caídas importantes, durante aproximadamente 24 horas, aunque esto varía en muchos individuos. [56] [57]
Incluye los análogos de insulina glargina U300 y degludec , que comienzan a actuar entre 30 y 90 minutos después y continúan activos durante más de 24 horas. [28]
Incluye una combinación de insulina de acción rápida o de acción corta con una insulina de acción más prolongada, típicamente una insulina NPH . Los productos combinados comienzan a funcionar con la insulina de acción más corta (5 a 15 minutos para la insulina de acción rápida y 30 minutos para la insulina de acción corta) y permanecen activos durante 16 a 24 horas. Existen varias variaciones con diferentes proporciones de las insulinas mixtas (por ejemplo, Novolog Mix 70/30 contiene 70 % de aspart protamina [similar a la NPH] y 30 % de aspart). [58]

A diferencia de muchos medicamentos, la insulina no puede administrarse por vía oral en la actualidad. Como casi todas las demás proteínas que se introducen en el tracto gastrointestinal , se reduce a fragmentos (componentes de un solo aminoácido), con lo que se pierde toda actividad. Se han realizado algunas investigaciones para encontrar formas de proteger la insulina del tracto digestivo, de modo que pueda administrarse en forma de píldora. Hasta ahora, esto es completamente experimental. [59]
La insulina se administra generalmente en forma de inyecciones subcutáneas mediante jeringas de un solo uso con agujas , una bomba de insulina o mediante lapiceras de insulina de uso repetido con agujas. Las personas que desean reducir la punción cutánea repetida de las inyecciones de insulina a menudo utilizan un puerto de inyección junto con las jeringas. [60]
El uso de inyecciones subcutáneas de insulina está diseñado para imitar el ciclo fisiológico natural de secreción de insulina, teniendo en cuenta las diversas propiedades de las formulaciones utilizadas, como la vida media, el inicio de la acción y la duración de la acción. En muchas personas, se utiliza un producto de insulina de acción rápida o corta, así como un producto de acción intermedia o prolongada para disminuir la cantidad de inyecciones por día. En algunos casos, las inyecciones de insulina se pueden combinar con otra terapia de inyección, como los agonistas del receptor de GLP-1 . Se requiere la limpieza del lugar de la inyección y la técnica de inyección para garantizar una terapia de insulina eficaz. [45]
Las bombas de insulina son una solución razonable para algunas personas. Las ventajas para la persona son un mejor control de la dosis de insulina basal , dosis de bolo calculadas en fracciones de una unidad y calculadoras en la bomba que pueden ayudar a determinar las dosis de infusión de bolo . Las limitaciones son el costo, la posibilidad de episodios de hipoglucemia e hiperglucemia, problemas con el catéter y la falta de un medio de "circuito cerrado" para controlar la administración de insulina en función de los niveles actuales de glucosa en sangre. [ cita requerida ]
Las bombas de insulina pueden ser como "inyectores eléctricos" conectados a un catéter o cánula implantados temporalmente . Algunas personas que no pueden lograr un control adecuado de la glucosa mediante una inyección convencional (o a chorro) pueden hacerlo con la bomba adecuada. [61]
Los catéteres permanentes presentan riesgo de infección y ulceración, y algunas personas también pueden desarrollar lipodistrofia debido a los equipos de infusión. Estos riesgos a menudo se pueden minimizar manteniendo limpios los sitios de infusión. Las bombas de insulina requieren cuidado y esfuerzo para su uso correcto. [61]
Una unidad internacional de insulina (1 UI) se define como el "equivalente biológico" de 34,7 μg de insulina cristalina pura. [ cita requerida ]
La primera definición de una unidad de insulina fue la cantidad necesaria para inducir hipoglucemia en un conejo. Esta fue establecida por James Collip en la Universidad de Toronto en 1922. Por supuesto, esto dependía del tamaño y la dieta de los conejos. La unidad de insulina fue establecida por el comité de insulina de la Universidad de Toronto. [62] La unidad evolucionó eventualmente a la antigua unidad de insulina USP , donde una unidad (U) de insulina se estableció igual a la cantidad de insulina requerida para reducir la concentración de glucosa en sangre en un conejo en ayunas a 45 mg / d L (2,5 m mol / L ). Una vez que se conoció la estructura química y la masa de la insulina, la unidad de insulina se definió por la masa de insulina cristalina pura requerida para obtener la unidad USP. [ cita requerida ]
La unidad de medida utilizada en la terapia con insulina no forma parte del Sistema Internacional de Unidades (SI), que es la forma moderna del sistema métrico . En cambio, la unidad farmacológica internacional (UI) está definida por el Comité de Expertos en Normalización Biológica de la OMS . [63]
El problema central para quienes necesitan insulina externa es elegir la dosis correcta de insulina y el momento adecuado.
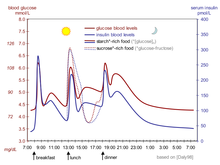
La regulación fisiológica de la glucemia, como en el caso de los no diabéticos, sería la mejor opción. El aumento de los niveles de glucemia después de una comida es un estímulo para la liberación rápida de insulina del páncreas. El aumento del nivel de insulina provoca la absorción y el almacenamiento de glucosa en las células, reduce la conversión de glucógeno en glucosa, lo que reduce los niveles de glucemia y, por lo tanto, la liberación de insulina. El resultado es que el nivel de glucemia aumenta un poco después de comer y, en una hora aproximadamente, vuelve al nivel normal de "ayuno". Incluso el mejor tratamiento para la diabetes con insulina humana sintética o incluso análogos de insulina, independientemente de cómo se administren, está muy lejos de lograr un control normal de la glucemia en los no diabéticos. [64]
Para complicar las cosas, la composición de los alimentos ingeridos (véase el índice glucémico ) afecta a las tasas de absorción intestinal. La glucosa de algunos alimentos se absorbe más (o menos) rápidamente que la misma cantidad de glucosa en otros alimentos. Además, las grasas y las proteínas provocan retrasos en la absorción de la glucosa de los carbohidratos ingeridos al mismo tiempo. Asimismo, el ejercicio reduce la necesidad de insulina incluso cuando todos los demás factores permanecen invariables, ya que el músculo que trabaja tiene cierta capacidad para absorber la glucosa sin la ayuda de la insulina. [65]
Debido a la complejidad de los factores que interactúan entre sí, en principio es imposible saber con certeza cuánta insulina (y de qué tipo) se necesita para "cubrir" una comida en particular y alcanzar un nivel de glucosa en sangre razonable en una o dos horas después de comer. Las células beta de los no diabéticos gestionan esto de forma rutinaria y automática mediante el control continuo del nivel de glucosa y la liberación de insulina. Todas estas decisiones de un diabético deben basarse en la experiencia y la formación (es decir, bajo la dirección de un médico, un asistente personal o, en algunos lugares, un educador especializado en diabetes) y, además, deben basarse específicamente en la experiencia individual de la persona. Pero no es algo sencillo y nunca debe hacerse por hábito o rutina. Sin embargo, con cierto cuidado, se puede hacer razonablemente bien en la práctica clínica. Por ejemplo, algunas personas con diabetes necesitan más insulina después de beber leche desnatada que después de tomar una cantidad equivalente de grasa, proteínas, carbohidratos y líquidos en alguna otra forma. Su reacción particular a la leche desnatada es diferente a la de otras personas con diabetes, pero es probable que la misma cantidad de leche entera provoque una reacción todavía diferente incluso en esa persona. La leche entera contiene una cantidad considerable de grasa, mientras que la leche desnatada tiene mucha menos. Es un acto de equilibrio continuo para todas las personas con diabetes, especialmente para quienes toman insulina. [ cita requerida ]
Las personas con diabetes dependiente de la insulina suelen necesitar un nivel básico de insulina (insulina basal), así como insulina de acción corta para cubrir las comidas (también conocida como insulina en bolo o insulina prandial ). Mantener la tasa basal y la tasa en bolo es un acto de equilibrio continuo que las personas con diabetes dependiente de la insulina deben controlar todos los días. Esto normalmente se logra mediante análisis de sangre regulares, aunque ahora se están poniendo a disposición equipos de medición continua de azúcar en sangre ( monitores continuos de glucosa o CGM) que podrían ayudar a refinar este acto de equilibrio una vez que se generalice su uso. [ cita requerida ]
Se utiliza una insulina de acción prolongada para aproximarse a la secreción basal de insulina por el páncreas, que varía a lo largo del día. [66] Para este fin se pueden utilizar NPH/isófana, lente, ultralente, glargina y detemir. La ventaja de la NPH es su bajo coste, el hecho de que se puede mezclar con formas de insulina de acción corta, minimizando así el número de inyecciones que se deben administrar, y que la actividad de la NPH alcanzará su pico entre 4 y 6 horas después de la administración, lo que permite una dosis antes de acostarse para equilibrar la tendencia de la glucosa a aumentar con el amanecer , junto con una dosis matutina más pequeña para equilibrar la menor necesidad basal de la tarde y posiblemente una dosis vespertina para cubrir la necesidad nocturna. Una desventaja de la NPH antes de acostarse es que si no se toma lo suficientemente tarde (cerca de la medianoche) para que su pico se produzca poco antes del amanecer, tiene el potencial de causar hipoglucemia. Una ventaja teórica de la glargina y el detemir es que sólo es necesario administrarlos una vez al día, aunque en la práctica muchas personas descubren que ninguno dura 24 horas completas. También pueden administrarse en cualquier momento del día, siempre que se administren a la misma hora todos los días. Otra ventaja de las insulinas de acción prolongada es que el componente basal de un régimen de insulina (que proporciona un nivel mínimo de insulina a lo largo del día) se puede desacoplar del componente prandial o de bolo (que proporciona cobertura durante las comidas mediante insulinas de acción ultracorta), mientras que los regímenes que utilizan insulina NPH e insulina regular tienen la desventaja de que cualquier ajuste de dosis afecta tanto a la cobertura basal como a la prandial. La glargina y la detemir son significativamente más caras que la NPH, la lenta y la ultralenta, y no se pueden mezclar con otras formas de insulina. [ cita requerida ]
Se utiliza una insulina de acción corta para simular el pico endógeno de insulina que se produce antes de comer. Para ello se pueden utilizar insulina regular, lispro, aspart y glulisina. La insulina regular debe administrarse con unos 30 minutos de antelación a la comida para que sea lo más eficaz posible y para minimizar la posibilidad de hipoglucemia. La lispro, la aspart y la glulisina están aprobadas para su dosificación con el primer bocado de la comida, e incluso pueden ser eficaces si se administran después de terminar la comida. La insulina de acción corta también se utiliza para corregir la hiperglucemia. [67]
Descrita por primera vez en 1934, [68] lo que los médicos suelen denominar insulina de escala móvil (SSI) es insulina de acción rápida únicamente, administrada por vía subcutánea, normalmente a la hora de las comidas y, a veces, antes de acostarse, [69] pero solo cuando la glucosa en sangre está por encima de un umbral (p. ej., 10 mmol/L, 180 mg/dL). [70] El método denominado "de escala móvil" se enseña ampliamente, aunque ha sido muy criticado. [71] [72] [73] [74] La insulina de escala móvil (SSI) no es una forma eficaz de controlar la diabetes a largo plazo en personas que residen en hogares de ancianos. [69] [75] La insulina de escala móvil provoca un mayor malestar y un aumento del tiempo de enfermería. [75]
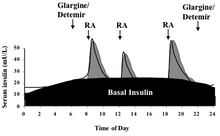
Ejemplo de régimen con insulina glargina e insulina lispro:
Durante el embarazo, puede desarrollarse hiperglucemia espontánea y conducir a diabetes mellitus gestacional (DMG) , una complicación frecuente del embarazo. Con una prevalencia del 6-20% entre las mujeres embarazadas a nivel mundial, la diabetes mellitus gestacional (DMG) se define como cualquier grado de intolerancia a la glucosa que se desarrolla o se reconoce inicialmente durante el embarazo. [76] La insulina protamina neutra Hagedorn (NPH) ha sido la piedra angular de la terapia con insulina durante el embarazo, administrada de dos a cuatro veces al día. Las mujeres con DMG y las mujeres embarazadas con diabetes mellitus tipo I que controlan con frecuencia sus niveles de glucosa en sangre y utilizan equipos de monitoreo de glucosa para hacerlo, utilizan una infusión continua de insulina de un análogo de insulina de acción rápida, como lispro y aspart. Sin embargo, hay una serie de consideraciones a la hora de elegir un régimen para administrar insulina a las pacientes. Al manejar la DMG en mujeres embarazadas, estas pautas son cruciales y pueden variar dependiendo de ciertas condiciones fisiológicas y, curiosamente, también del entorno sociocultural. Las guías perinatales actuales recomiendan una dosis baja diaria de insulina y tienen en cuenta las características fisiológicas de la mujer y la frecuencia de autocontrol. Se destaca la importancia de utilizar una planificación especializada de la terapia con insulina basada en parámetros como los mencionados anteriormente en lugar de un enfoque amplio. [77]
Las mujeres con diabetes preexistente tienen los niveles más altos de sensibilidad a la insulina al comienzo del embarazo. Se requiere un control estricto de la glucosa para prevenir la hipoglucemia, que puede provocar alteración de la conciencia, convulsiones y daño materno. [78] Los recién nacidos con bajo peso al nacer también pueden ser el resultado de la hipoglucemia, especialmente en pacientes con diabetes tipo 1, porque con frecuencia son más sensibles a la insulina que las personas con diabetes tipo 2 y es más probable que no sean conscientes de su estado de hipoglucemia. El control estricto de la glucosa es esencial porque después de las 16 semanas de embarazo, las mujeres con diabetes preexistente se vuelven más resistentes a la insulina y sus demandas de insulina pueden fluctuar semanalmente. La necesidad de insulina puede aumentar de un embarazo al siguiente. Por lo tanto, es realista esperar mayores necesidades de control de la glucosa en los embarazos posteriores en mujeres multíparas. [78]
La posibilidad de utilizar insulina para intentar mejorar el rendimiento atlético se sugirió ya en los Juegos Olímpicos de Invierno de 1998 en Nagano, Japón , como informó Peter Sönksen en la edición de julio de 2001 del Journal of Endocrinology . Un oficial médico ruso planteó la cuestión de si los atletas no diabéticos podían utilizar insulina legalmente. [79] [80] No está claro si la insulina realmente mejoraría el rendimiento atlético, pero las preocupaciones sobre su uso llevaron al Comité Olímpico Internacional a prohibir el uso de la hormona por parte de atletas no diabéticos en 1998. [81]
El libro Game of Shadows (2001), de los periodistas Mark Fainaru-Wada y Lance Williams, incluyó acusaciones de que el jugador de béisbol Barry Bonds usó insulina (así como otras drogas) en la aparente creencia de que aumentaría la efectividad de la hormona de crecimiento que supuestamente estaba tomando. [82] Bonds finalmente testificó frente a un gran jurado federal como parte de una investigación gubernamental de BALCO . [83]
Se afirma que los culturistas en particular utilizan insulina exógena y otros fármacos con la creencia de que aumentarán su masa muscular. Se ha descrito a los culturistas inyectándose hasta 10 UI de insulina sintética regular antes de ingerir comidas azucaradas. [81] Un informe de 2008 sugirió que la insulina a veces se utiliza en combinación con esteroides anabólicos y hormona del crecimiento (GH), y que "los atletas se están exponiendo a posibles daños al autoadministrarse grandes dosis de GH, IGF-I e insulina". [84] [85] El abuso de insulina se ha mencionado como un posible factor en las muertes de los culturistas Ghent Wakefield y Rich Piana . [86]
La insulina, la hormona de crecimiento humana (HGH) y el factor de crecimiento similar a la insulina 1 (IGF-1) son autoadministrados por aquellos que buscan aumentar la masa muscular más allá del alcance ofrecido por los esteroides anabólicos solos. Su fundamento es que, dado que la insulina y la HGH actúan sinérgicamente para promover el crecimiento, y dado que el IGF-1 es un mediador primario del crecimiento musculoesquelético, la "acumulación" de insulina, HGH e IGF-1 debería ofrecer un efecto de crecimiento sinérgico en el músculo esquelético. Esta teoría ha sido apoyada en los últimos años por los culturistas de alto nivel cuyo peso de competencia supera las 50 libras (23 kg) de músculo, mayor que el de los competidores en el pasado, y con niveles aún más bajos de grasa corporal. [ cita requerida ]
La insulina exógena aumenta significativamente la tasa de metabolismo de la glucosa en atletas de entrenamiento junto con un aumento sustancial en el VO2 máximo . [87] Se cree que la insulina mejora el rendimiento al aumentar la síntesis de proteínas, reducir el catabolismo proteico y facilitar la transferencia de ciertos aminoácidos en el músculo esquelético humano. Se percibe que los atletas tratados con insulina tienen masa corporal magra porque la hiperinsulinemia fisiológica en el músculo esquelético humano mejora la actividad del transporte de aminoácidos, lo que a su vez promueve la síntesis de proteínas. [87] La insulina estimula el transporte de aminoácidos a las células y también controla el metabolismo de la glucosa. Disminuye la lipólisis y aumenta la lipogénesis, por lo que los culturistas y los atletas usan rhGH junto con ella para compensar este efecto negativo al tiempo que maximizan la síntesis de proteínas. Los atletas extrapolaron la fisiología del paciente diabético en el ámbito deportivo porque están interesados en la supresión de la proteólisis. Se ha descubierto que la administración de insulina es anabólica proteica en el estado resistente a la insulina de la insuficiencia renal crónica. [88] Inhibe la proteólisis y, cuando se administra junto con aminoácidos, mejora la síntesis neta de proteínas. La inyección de insulina exógena crea una pinza hiperinsulinémica in vivo, lo que aumenta el glucógeno muscular antes y durante las fases de recuperación del ejercicio intenso. Se espera que la potencia, la fuerza y la resistencia aumenten como resultado, y también podría acelerar el proceso de curación después de una actividad física intensa. En segundo lugar, se espera que la insulina aumente la masa muscular al prevenir la descomposición de la proteína muscular cuando se consume junto con una dieta alta en carbohidratos y proteínas. Aunque un número limitado de estudios sugiere que la medicación con insulina puede ser objeto de abuso como tratamiento farmacológico para aumentar la fuerza y el rendimiento en personas o atletas jóvenes y saludables, una evaluación reciente de la investigación sostiene que esto solo es aplicable a un pequeño grupo de personas "sin experiencia en el uso de fármacos". [87]
El abuso de insulina exógena conlleva un riesgo asociado de coma hipoglucémico y muerte cuando la cantidad utilizada es superior a la necesaria para manejar los carbohidratos ingeridos. Los riesgos agudos incluyen daño cerebral , parálisis y muerte . Los síntomas pueden incluir mareos, debilidad, temblores, palpitaciones , convulsiones, confusión, dolor de cabeza, somnolencia, coma, diaforesis y náuseas . Todas las personas con sobredosis deben ser derivadas para evaluación y tratamiento médico, que puede durar horas o días. [89]
Los datos del Sistema Nacional de Datos de Envenenamiento de los Estados Unidos (2013) indican que el 89,3% de los casos de insulina notificados a los centros de intoxicaciones no son intencionados, como resultado de un error terapéutico. Otro 10% de los casos son intencionados y pueden reflejar intentos de suicidio, abuso, intención delictiva, ganancia secundaria u otras razones desconocidas. [89] La hipoglucemia inducida por insulina exógena se puede detectar químicamente examinando la relación entre insulina y péptido C en la circulación periférica. [90] Se ha sugerido que este tipo de enfoque podría utilizarse para detectar el abuso de insulina exógena por parte de los deportistas. [91]
La insulina se mide a menudo en suero, plasma o sangre para controlar la terapia en personas diabéticas, confirmar un diagnóstico de envenenamiento en personas hospitalizadas o ayudar en una investigación médico-legal de muerte sospechosa. La interpretación de las concentraciones de insulina resultantes es compleja, dados los numerosos tipos de insulina disponibles, las diversas vías de administración, la presencia de anticuerpos antiinsulina en diabéticos dependientes de insulina y la inestabilidad ex vivo del fármaco. Otros factores de confusión potenciales incluyen la amplia reactividad cruzada de los inmunoensayos comerciales de insulina para los análogos biosintéticos de insulina, el uso de insulina intravenosa en dosis altas como antídoto para la sobredosis de fármacos antihipertensivos y la redistribución post mortem de la insulina dentro del cuerpo. El uso de una técnica cromatográfica para el ensayo de insulina puede ser preferible al inmunoensayo en algunas circunstancias, para evitar el problema de la reactividad cruzada que afecta el resultado cuantitativo y también para ayudar a identificar el tipo específico de insulina en la muestra. [92]
Una terapia combinada de insulina y otros fármacos antidiabéticos parece ser más beneficiosa en personas diabéticas que aún tienen capacidad secretora de insulina residual. [93] Una combinación de terapia con insulina y sulfonilurea es más eficaz que la insulina sola en el tratamiento de personas con diabetes tipo 2 después de un fracaso secundario a los fármacos orales, lo que conduce a mejores perfiles de glucosa y/o menores necesidades de insulina. [93]
En los Estados Unidos, el precio unitario de la insulina ha aumentado de manera constante desde 1991 hasta 2019. [94] [95] Se triplicó entre 2002 y 2013. [96] Los costos pueden llegar a ser de hasta 900 dólares estadounidenses por mes. [96] En 2016 se plantearon preocupaciones sobre la colaboración de las empresas farmacéuticas para aumentar los precios. [96] En enero de 2019, los legisladores de la Cámara de Representantes de los Estados Unidos enviaron cartas a los fabricantes de insulina Eli Lilly and Company , Sanofi y Novo Nordisk pidiendo explicaciones por el rápido aumento de los precios de la insulina. El costo anual de la insulina para las personas con diabetes tipo 1 en los EE. UU. casi se duplicó de $ 2900 a $ 5700 durante el período de 2012 a 2016. [97]
En 2019, se estimó que los estadounidenses pagan entre dos y seis veces más que el resto del mundo por medicamentos de marca recetados, según la Federación Internacional de Planes de Salud. [98]
California, en julio de 2022, aprobó un presupuesto que asigna 100 millones de dólares para que el estado cree su propia insulina a un precio cercano al costo. [99]
Canadá, al igual que muchos otros países industrializados, tiene controles de precios sobre el costo de los medicamentos. La Junta de Revisión de Precios de Medicamentos Patentados garantiza que el precio de los medicamentos patentados vendidos en Canadá "no sea excesivo" y se mantenga "comparable con los precios en otros países". [98]
Los Servicios Nacionales de Salud de los países del Reino Unido suministran gratuitamente insulina y todos los demás medicamentos a las personas que los utilizan para controlar su diabetes . [100]
En marzo de 2020, la FDA cambió la vía regulatoria para la aprobación de nuevos productos de insulina. [101] La insulina está regulada como un producto biológico en lugar de como un fármaco. [101] El cambio de estatus le da a la FDA más flexibilidad para la aprobación y el etiquetado. [102] En julio de 2021, la FDA aprobó la insulina glargina-yfgn (Semglee), un producto biosimilar que contiene la insulina glargina análoga de acción prolongada. [103] La insulina glargina-yfgn es intercambiable y menos costosa que el producto de referencia, la insulina glargina (Lantus), que había sido aprobada en 2000. [104] La FDA requiere que los nuevos productos de insulina no sean inferiores a los productos de insulina existentes con respecto a la reducción de la hemoglobina A1c. [105]
En 2006, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó el uso de Exubera , la primera insulina inhalable . [106] Fue retirada del mercado por su fabricante a partir del tercer trimestre de 2007 debido a la falta de aceptación. [ cita requerida ]
Se afirmó que la insulina inhalada tenía una eficacia similar a la insulina inyectada, tanto en términos de control de los niveles de glucosa como de vida media en sangre. Actualmente, la insulina inhalada es de acción corta y se administra típicamente antes de las comidas; a menudo sigue siendo necesaria una inyección de insulina de acción prolongada por la noche. [107] Cuando se cambió a las personas de insulina inyectada a insulina inhalada, no se observó ninguna diferencia significativa en los niveles de Hb A1c a lo largo de tres meses. La dosificación precisa fue un problema particular, aunque las personas no mostraron un aumento de peso significativo ni una disminución de la función pulmonar a lo largo del ensayo en comparación con el valor inicial. [108]
Tras su lanzamiento comercial en 2005 en el Reino Unido, hasta julio de 2006 el Instituto Nacional de Salud y Excelencia Clínica no lo recomendó para uso rutinario, excepto en casos en que exista "fobia a las inyecciones comprobada y diagnosticada por un psiquiatra o psicólogo". [107]
En enero de 2008, el mayor fabricante de insulina del mundo, Novo Nordisk , también anunció que la compañía estaba descontinuando todo desarrollo adicional de la versión propia de la compañía de insulina inhalable, conocida como el sistema de insulina inhalada AERx iDMS. [109] De manera similar, Eli Lilly and Company terminó sus esfuerzos para desarrollar su insulina inhalada Air en marzo de 2008. [110] Afrezza , desarrollado por Mannkind , fue autorizado por la FDA en junio de 2014 para su uso en adultos con diabetes tipo 1 y tipo 2, con una restricción de etiqueta que limita su uso solo a aquellos que también tienen asma , cáncer de pulmón activo o enfermedad pulmonar obstructiva crónica (EPOC). [111] La insulina inhalada de acción rápida es un componente de la solución combinada de medicamento y dispositivo que se usa al comienzo de cada comida. Emplea la tecnología de tecnosferas, que parece tener un método de administración más práctico y más flexibilidad de dosificación, y una nueva formulación de insulina inhalada (2,5 m). Se utiliza un inhalador del tamaño de un pulgar con una flexibilidad de dosificación mejorada para administrar insulina inhalable. Incluye insulina humana recombinante disuelta en polvo (fumaril dicetopiperazina). La insulina de tecnosferas se absorbe rápidamente por la superficie pulmonar después de la inhalación. Dentro de las 12 horas posteriores a la inhalación, ambas sustancias, insulina y polvo (fumaril dicetopiperazina), se eliminan prácticamente de los pulmones de las personas sanas. En comparación con Exubera (8-9%), solo el 0,3% de la insulina inhalada todavía estaba presente en los pulmones después de 12 horas. Sin embargo, dado que se ha informado que los niveles de anticuerpos séricos aumentan sin cambios clínicos sustanciales, se ha informado de broncoespasmo agudo en pacientes asmáticos y con EPOC junto con una reducción significativa en la capacidad de difusión pulmonar de monóxido de carbono, en comparación con la insulina subcutánea, con su uso, Afrezza recibió la aprobación de la FDA con una advertencia (Estrategia de evaluación y mitigación de riesgos). [112] [111]
Existen varios métodos para la administración transdérmica de insulina. La insulina pulsátil utiliza microchorros para impulsar la insulina hacia la persona, imitando las secreciones fisiológicas de insulina del páncreas. [113] La inyección a chorro tuvo diferentes picos y duraciones de administración de insulina en comparación con la inyección con aguja. Algunos diabéticos pueden preferir los inyectores a chorro a la inyección hipodérmica. [114] Se ha descubierto que tanto la electricidad mediante ionoforesis [115] como los ultrasonidos hacen que la piel sea temporalmente porosa. El aspecto de la administración de insulina sigue siendo experimental, pero el aspecto de prueba de glucosa en sangre de los "dispositivos de muñeca" está disponible comercialmente. Los investigadores han producido un dispositivo similar a un reloj que prueba los niveles de glucosa en sangre a través de la piel y administra dosis correctivas de insulina a través de los poros de la piel. En 2015, se estaba probando en animales un dispositivo similar, pero que se basaba en "microagujas" que penetraban la piel. [116] En los últimos años, el uso de potenciadores químicos, dispositivos eléctricos y dispositivos de microagujas ha demostrado ser muy prometedor para mejorar la penetración de la insulina en comparación con el transporte pasivo a través de la piel. La administración transdérmica de insulina muestra un enfoque más amigable para el paciente y mínimamente invasivo para el cuidado diario de la diabetes que la inyección hipodérmica convencional; sin embargo, se necesitan investigaciones adicionales para abordar cuestiones como el uso a largo plazo, la eficiencia y la confiabilidad de la administración, así como los efectos secundarios que involucran inflamación e irritación. [117]
La insulina puede administrarse al sistema nervioso central por vía intranasal (IN) con poca o ninguna captación sistémica o efectos secundarios periféricos asociados. Se ha demostrado que la insulina administrada por vía intranasal se acumula rápidamente en el líquido cefalorraquídeo, lo que indica un transporte eficaz al cerebro. Se cree que esta acumulación se produce a lo largo de las vías olfativas y cercanas. Aunque numerosos estudios han publicado resultados alentadores, aún se están realizando más estudios para comprender sus impactos a largo plazo con el fin de comenzar la aplicación clínica exitosa. [118]
El atractivo básico de los agentes hipoglucemiantes por vía oral es que la mayoría de las personas prefieren una pastilla o un líquido oral a una inyección. Sin embargo, la insulina es una hormona peptídica que se digiere en el estómago y el intestino y, para que sea eficaz en el control del azúcar en sangre, no se puede tomar por vía oral en su forma actual. [ cita requerida ]
Se supone que el mercado potencial para una forma oral de insulina es enorme, por lo que muchos laboratorios han intentado idear formas de trasladar suficiente insulina intacta desde el intestino a la vena porta para tener un efecto mensurable sobre el azúcar en sangre. [119]
Actualmente se están llevando a cabo varias estrategias de derivatización y formulación en un intento de desarrollar una insulina disponible por vía oral. [120] Muchos de estos enfoques emplean sistemas de administración de nanopartículas [121] [122] [123] y varios se están probando en ensayos clínicos . [124] [125] [126]
Otra mejora sería un trasplante de páncreas o de células beta para evitar la administración periódica de insulina. Esto daría como resultado una fuente de insulina autorregulada. El trasplante de un páncreas entero (como órgano individual ) es difícil y relativamente poco común. A menudo se realiza junto con el trasplante de hígado o riñón , aunque puede hacerse por sí solo. También es posible hacer un trasplante de solo las células beta pancreáticas. Sin embargo, los trasplantes de islotes habían sido altamente experimentales durante muchos años, pero algunos investigadores en Alberta, Canadá , han desarrollado técnicas con una alta tasa de éxito inicial (alrededor del 90% en un grupo). Casi la mitad de los que recibieron un trasplante de células de islotes estaban libres de insulina un año después de la operación; al final del segundo año, ese número se reduce a aproximadamente uno de cada siete. Sin embargo, los investigadores de la Universidad de Illinois en Chicago (UIC) han modificado ligeramente el procedimiento del Protocolo de Edmonton para el trasplante de células de islotes y han logrado la independencia de la insulina en personas diabéticas, con menos células de islotes pancreáticos pero que funcionan mejor. [127]
El trasplante de células beta podría resultar práctico en un futuro próximo. Además, algunos investigadores han explorado la posibilidad de trasplantar células no beta modificadas genéticamente para que secreten insulina. [128]
{{cite journal}}: Mantenimiento de CS1: configuración anulada ( enlace )Si usa insulina o medicamentos para controlar su diabetes, ... no paga por ningún artículo que le receten.