La ingeniería genética , también llamada modificación genética o manipulación genética , es la modificación y manipulación de los genes de un organismo mediante tecnología . Es un conjunto de tecnologías utilizadas para cambiar la composición genética de las células, incluida la transferencia de genes dentro y a través de los límites de las especies para producir organismos nuevos o mejorados .
El ADN nuevo se obtiene aislando y copiando el material genético de interés utilizando métodos de ADN recombinante o sintetizando artificialmente el ADN. Por lo general, se crea y utiliza una construcción para insertar este ADN en el organismo huésped. La primera molécula de ADN recombinante fue creada por Paul Berg en 1972 combinando ADN del virus del mono SV40 con el virus lambda .
Además de insertar genes , el proceso se puede utilizar para eliminar o " eliminar " genes. El nuevo ADN puede insertarse aleatoriamente o dirigirse a una parte específica del genoma . [1]
Un organismo que se genera mediante ingeniería genética se considera genéticamente modificado (GM) y la entidad resultante es un organismo genéticamente modificado (OGM). El primer OGM fue una bacteria generada por Herbert Boyer y Stanley Cohen en 1973. Rudolf Jaenisch creó el primer animal transgénico cuando insertó ADN extraño en un ratón en 1974. La primera empresa que se centró en la ingeniería genética, Genentech , se fundó en 1976 y Comenzó la producción de proteínas humanas. La insulina humana genéticamente modificada se produjo en 1978 y las bacterias productoras de insulina se comercializaron en 1982. Los alimentos genéticamente modificados se venden desde 1994, con el lanzamiento del tomate Flavr Savr . El Flavr Savr fue diseñado para tener una vida útil más larga, pero la mayoría de los cultivos transgénicos actuales se modifican para aumentar la resistencia a insectos y herbicidas. GloFish , el primer OGM diseñado como mascota, se vendió en Estados Unidos en diciembre de 2003. En 2016 se vendió salmón modificado con una hormona de crecimiento.
La ingeniería genética se ha aplicado en numerosos campos, incluidos la investigación, la medicina, la biotecnología industrial y la agricultura. En la investigación, los OGM se utilizan para estudiar la función y expresión de los genes mediante experimentos de pérdida y ganancia de función y de seguimiento y expresión. Eliminando genes responsables de determinadas enfermedades es posible crear organismos animales modelo de enfermedades humanas. Además de producir hormonas, vacunas y otros medicamentos, la ingeniería genética tiene el potencial de curar enfermedades genéticas mediante la terapia génica . Las células de ovario de hámster chino (CHO) se utilizan en ingeniería genética industrial. Además, las vacunas de ARNm se fabrican mediante ingeniería genética para tratar virus como el COVID-19 . Las mismas técnicas que se utilizan para producir medicamentos también pueden tener aplicaciones industriales, como la producción de enzimas para detergentes, quesos y otros productos.
El auge de los cultivos genéticamente modificados comercializados ha proporcionado beneficios económicos a los agricultores de muchos países diferentes, pero también ha sido la fuente de la mayor parte de la controversia en torno a esta tecnología. Esto ha estado presente desde sus inicios; Las primeras pruebas de campo fueron destruidas por activistas anti-GM. Aunque existe un consenso científico de que los alimentos actualmente disponibles derivados de cultivos transgénicos no representan un riesgo mayor para la salud humana que los alimentos convencionales, los críticos consideran que la seguridad de los alimentos transgénicos es una de las principales preocupaciones. También se han planteado como posibles problemas el flujo genético , el impacto en organismos no objetivo, el control del suministro de alimentos y los derechos de propiedad intelectual . Estas preocupaciones han llevado al desarrollo de un marco regulatorio, que comenzó en 1975. Ha llevado a un tratado internacional, el Protocolo de Cartagena sobre Seguridad de la Biotecnología , que fue adoptado en 2000. Los países individuales han desarrollado sus propios sistemas regulatorios con respecto a los OGM, con la Las diferencias más marcadas se dan entre Estados Unidos y Europa .
Ingeniería genética : Proceso de insertar nueva información genética en células existentes con el fin de modificar un organismo específico con el fin de cambiar sus características.
Nota : Adaptado de la ref. [2] [3]
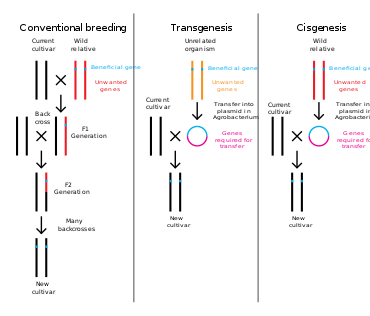
La ingeniería genética es un proceso que altera la estructura genética de un organismo, ya sea eliminando o introduciendo ADN , o modificando el material genético existente in situ. A diferencia del mejoramiento tradicional de animales y plantas , que implica realizar múltiples cruces y luego seleccionar el organismo con el fenotipo deseado , la ingeniería genética toma el gen directamente de un organismo y lo entrega al otro. Esto es mucho más rápido, se puede utilizar para insertar cualquier gen de cualquier organismo (incluso de diferentes dominios ) y evita que también se agreguen otros genes indeseables. [4]
La ingeniería genética podría potencialmente solucionar trastornos genéticos graves en humanos reemplazando el gen defectuoso por uno que funcione. [5] Es una herramienta importante en la investigación que permite estudiar la función de genes específicos. [6] Se han obtenido medicamentos, vacunas y otros productos a partir de organismos diseñados para producirlos. [7] Se han desarrollado cultivos que ayudan a la seguridad alimentaria al aumentar el rendimiento, el valor nutricional y la tolerancia al estrés ambiental. [8]
El ADN puede introducirse directamente en el organismo huésped o en una célula que luego se fusiona o hibrida con el huésped. [9] Esto se basa en técnicas de ácido nucleico recombinante para formar nuevas combinaciones de material genético hereditario seguidas de la incorporación de ese material ya sea indirectamente a través de un sistema de vectores o directamente mediante microinyección , macroinyección o microencapsulación .
La ingeniería genética normalmente no incluye técnicas de reproducción tradicional, fertilización in vitro , inducción de poliploidía , mutagénesis y fusión celular que no utilizan ácidos nucleicos recombinantes ni un organismo genéticamente modificado en el proceso. [9] Sin embargo, algunas definiciones amplias de ingeniería genética incluyen la cría selectiva . [10] La clonación y la investigación con células madre , aunque no se consideran ingeniería genética, [11] están estrechamente relacionadas y la ingeniería genética se puede utilizar dentro de ellas. [12] La biología sintética es una disciplina emergente que lleva la ingeniería genética un paso más allá al introducir material sintetizado artificialmente en un organismo. [13]
Las plantas, animales o microorganismos que han sido modificados mediante ingeniería genética se denominan organismos genéticamente modificados u OGM. [14] Si se añade material genético de otra especie al huésped, el organismo resultante se llama transgénico . Si se utiliza material genético de la misma especie o de una especie que puede reproducirse naturalmente con el huésped, el organismo resultante se llama cisgénico . [15] Si se utiliza la ingeniería genética para eliminar material genético del organismo objetivo, el organismo resultante se denomina organismo knockout . [16] En Europa, la modificación genética es sinónimo de ingeniería genética, mientras que en los Estados Unidos de América y Canadá la modificación genética también se puede utilizar para referirse a métodos de reproducción más convencionales. [17] [18] [19]
Los humanos han alterado los genomas de las especies durante miles de años mediante reproducción selectiva o selección artificial [20] : 1 [21] : 1 en contraste con la selección natural . Más recientemente, la reproducción por mutaciones ha utilizado la exposición a sustancias químicas o radiación para producir una alta frecuencia de mutaciones aleatorias, con fines de reproducción selectiva. La ingeniería genética como manipulación directa del ADN por parte de los seres humanos al margen de la reproducción y las mutaciones sólo existe desde la década de 1970. El término "ingeniería genética" fue acuñado por el genetista ruso Nikolay Timofeev-Ressovsky en su artículo de 1934 "La producción experimental de mutaciones", publicado en la revista británica Biological Reviews. [22] Jack Williamson utilizó el término en su novela de ciencia ficción Dragon's Island, publicada en 1951 [23] , un año antes de que Alfred Hershey y Martha Chase confirmaran el papel del ADN en la herencia , [24] y dos años antes de que James Watson y Francis Crick demostró que la molécula de ADN tiene una estructura de doble hélice, aunque el concepto general de manipulación genética directa se exploró de forma rudimentaria en la historia de ciencia ficción de Stanley G. Weinbaum de 1936 , Proteus Island . [25] [26]

En 1972, Paul Berg creó las primeras moléculas de ADN recombinante combinando el ADN del virus del mono SV40 con el del virus lambda . [27] En 1973, Herbert Boyer y Stanley Cohen crearon el primer organismo transgénico insertando genes de resistencia a los antibióticos en el plásmido de una bacteria Escherichia coli . [28] [29] Un año después, Rudolf Jaenisch creó un ratón transgénico introduciendo ADN extraño en su embrión, convirtiéndolo en el primer animal transgénico del mundo . [30] Estos logros generaron preocupaciones en la comunidad científica sobre los riesgos potenciales de la ingeniería genética, que se discutieron en profundidad por primera vez en la Conferencia de Asilomar en 1975. Una de las principales recomendaciones de esta reunión fue que se debería establecer una supervisión gubernamental de la investigación del ADN recombinante hasta que la tecnología se considerara segura. [31] [32]
En 1976, Herbert Boyer y Robert Swanson fundaron Genentech, la primera empresa de ingeniería genética, y un año después la empresa produjo una proteína humana ( somatostatina ) en E. coli . Genentech anunció la producción de insulina humana genéticamente modificada en 1978. [33] En 1980, la Corte Suprema de Estados Unidos en el caso Diamond v. Chakrabarty dictaminó que la vida genéticamente alterada podía patentarse. [34] La insulina producida por bacterias fue aprobada para su liberación por la Administración de Alimentos y Medicamentos (FDA) en 1982. [35]
En 1983, una empresa de biotecnología, Advanced Genetic Sciences (AGS), solicitó autorización del gobierno de EE. UU. para realizar pruebas de campo con la cepa sin hielo de Pseudomonas syringae para proteger los cultivos de las heladas, pero grupos ambientalistas y manifestantes retrasaron las pruebas de campo durante cuatro años con desafíos legales. [36] En 1987, la cepa sin hielo de P. syringae se convirtió en el primer organismo genéticamente modificado (OGM) que se liberó al medio ambiente [37] cuando se rociaron con ella un campo de fresas y un campo de patatas en California. [38] Ambos campos de pruebas fueron atacados por grupos de activistas la noche anterior a las pruebas: "El primer sitio de pruebas del mundo atrajo al primer destructor de campos del mundo". [37]
Las primeras pruebas de campo de plantas genéticamente modificadas se produjeron en Francia y Estados Unidos en 1986; las plantas de tabaco fueron diseñadas para ser resistentes a los herbicidas . [39] La República Popular China fue el primer país en comercializar plantas transgénicas, introduciendo un tabaco resistente a los virus en 1992. [40] En 1994, Calgene obtuvo la aprobación para lanzar comercialmente el primer alimento genéticamente modificado , el Flavr Savr , un tomate diseñado para tener una vida útil más larga. [41] En 1994, la Unión Europea aprobó el tabaco diseñado para ser resistente al herbicida bromoxinil , convirtiéndolo en el primer cultivo genéticamente modificado comercializado en Europa. [42] En 1995, la papa Bt fue aprobada como segura por la Agencia de Protección Ambiental , después de haber sido aprobada por la FDA, convirtiéndola en el primer cultivo productor de pesticidas aprobado en los EE. UU. [43] En 2009, se cultivaron comercialmente 11 cultivos transgénicos en 25 países, los mayores de los cuales por área cultivada fueron Estados Unidos, Brasil, Argentina, India, Canadá, China, Paraguay y Sudáfrica. [44]
En 2010, los científicos del Instituto J. Craig Venter crearon el primer genoma sintético y lo insertaron en una célula bacteriana vacía. La bacteria resultante, denominada Mycoplasma laboratorium , podría replicarse y producir proteínas. [45] [46] Cuatro años más tarde, esto se dio un paso más cuando se desarrolló una bacteria que replicaba un plásmido que contenía un par de bases único , creando el primer organismo diseñado para utilizar un alfabeto genético expandido. [47] [48] En 2012, Jennifer Doudna y Emmanuelle Charpentier colaboraron para desarrollar el sistema CRISPR/Cas9 , [49] [50] una técnica que se puede utilizar para alterar fácil y específicamente el genoma de casi cualquier organismo. [51]

La creación de un OGM es un proceso de varios pasos. Los ingenieros genéticos primero deben elegir qué gen desean insertar en el organismo. Esto está impulsado por el objetivo del organismo resultante y se basa en investigaciones anteriores. Se pueden realizar exámenes genéticos para determinar genes potenciales y luego utilizar pruebas adicionales para identificar a los mejores candidatos. El desarrollo de microarrays , transcriptómica y secuenciación del genoma ha hecho que sea mucho más fácil encontrar genes adecuados. [52] La suerte también juega su papel; El gen Roundup Ready se descubrió después de que los científicos notaron que una bacteria prosperaba en presencia del herbicida. [53]
El siguiente paso es aislar el gen candidato. Se abre la célula que contiene el gen y se purifica el ADN. [54] El gen se separa mediante el uso de enzimas de restricción para cortar el ADN en fragmentos [55] o la reacción en cadena de la polimerasa (PCR) para amplificar el segmento del gen. [56] Estos segmentos luego se pueden extraer mediante electroforesis en gel . Si el gen elegido o el genoma del organismo donante ha sido bien estudiado, es posible que ya sea accesible desde una biblioteca genética . Si se conoce la secuencia del ADN , pero no hay copias disponibles del gen, también se puede sintetizar artificialmente . [57] Una vez aislado, el gen se liga a un plásmido que luego se inserta en una bacteria. El plásmido se replica cuando las bacterias se dividen, lo que garantiza que haya copias ilimitadas del gen disponibles. [58] El plásmido RK2 se destaca por su capacidad de replicarse en una amplia variedad de organismos unicelulares , lo que lo hace adecuado como herramienta de ingeniería genética. [59]
Antes de insertar el gen en el organismo objetivo, debe combinarse con otros elementos genéticos. Estos incluyen una región promotora y terminadora , que inician y finalizan la transcripción . Se añade un gen marcador seleccionable , que en la mayoría de los casos confiere resistencia a los antibióticos , por lo que los investigadores pueden determinar fácilmente qué células se han transformado con éxito. El gen también se puede modificar en esta etapa para una mejor expresión o efectividad. Estas manipulaciones se llevan a cabo utilizando técnicas de ADN recombinante , como digestiones de restricción , ligaciones y clonación molecular. [60]

Existen varias técnicas que se utilizan para insertar material genético en el genoma del huésped. Algunas bacterias pueden captar naturalmente ADN extraño . Esta capacidad puede inducirse en otras bacterias mediante estrés (p. ej., descarga térmica o eléctrica), que aumenta la permeabilidad de la membrana celular al ADN; El ADN absorbido puede integrarse con el genoma o existir como ADN extracromosómico . El ADN generalmente se inserta en células animales mediante microinyección , donde se puede inyectar a través de la envoltura nuclear de la célula directamente en el núcleo , o mediante el uso de vectores virales . [61]
Los genomas de las plantas se pueden diseñar mediante métodos físicos o mediante el uso de Agrobacterium para la entrega de secuencias alojadas en vectores binarios de ADN-T . En las plantas, el ADN a menudo se inserta mediante transformación mediada por Agrobacterium , [62] aprovechando la secuencia de ADN T de Agrobacterium que permite la inserción natural de material genético en las células vegetales. [63] Otros métodos incluyen la biolística , donde partículas de oro o tungsteno se recubren con ADN y luego se inyectan en células de plantas jóvenes, [64] y la electroporación , que implica el uso de una descarga eléctrica para hacer que la membrana celular sea permeable al ADN plasmídico.
Como sólo una célula se transforma con material genético, el organismo debe regenerarse a partir de esa única célula. En las plantas esto se logra mediante el uso de cultivo de tejidos . [65] [66] En los animales es necesario garantizar que el ADN insertado esté presente en las células madre embrionarias . [67] Las bacterias constan de una sola célula y se reproducen clonalmente, por lo que no es necesaria la regeneración. Se utilizan marcadores seleccionables para diferenciar fácilmente las células transformadas de las no transformadas. Estos marcadores suelen estar presentes en el organismo transgénico, aunque se han desarrollado varias estrategias que pueden eliminar el marcador seleccionable de la planta transgénica madura. [68]

Se realizan pruebas adicionales mediante PCR, hibridación Southern y secuenciación de ADN para confirmar que un organismo contiene el nuevo gen. [69] Estas pruebas también pueden confirmar la ubicación cromosómica y el número de copias del gen insertado. La presencia del gen no garantiza que se exprese en niveles apropiados en el tejido objetivo, por lo que también se utilizan métodos que buscan y miden los productos del gen (ARN y proteínas). Estos incluyen hibridación Northern , RT-PCR cuantitativa , Western blot , inmunofluorescencia , ELISA y análisis fenotípico. [70]
El nuevo material genético puede insertarse aleatoriamente dentro del genoma del huésped o dirigirse a una ubicación específica. La técnica de selección genética utiliza recombinación homóloga para realizar los cambios deseados en un gen endógeno específico . Esto tiende a ocurrir con una frecuencia relativamente baja en plantas y animales y generalmente requiere el uso de marcadores seleccionables . La frecuencia de la selección de genes puede mejorarse enormemente mediante la edición del genoma . La edición del genoma utiliza nucleasas diseñadas artificialmente que crean roturas bicatenarias específicas en ubicaciones deseadas del genoma y utilizan los mecanismos endógenos de la célula para reparar la rotura inducida por los procesos naturales de recombinación homóloga y unión de extremos no homólogos . Hay cuatro familias de nucleasas diseñadas: meganucleasas , [71] [72] nucleasas con dedos de zinc , [73] [74] nucleasas efectoras similares a activadores de la transcripción (TALEN), [75] [76] y el sistema Cas9-guideRNA (adaptado de CRISPR ). [77] [78] TALEN y CRISPR son los dos más utilizados y cada uno tiene sus propias ventajas. [79] Los TALEN tienen una mayor especificidad de objetivo, mientras que CRISPR es más fácil de diseñar y más eficiente. [79] Además de mejorar la selección de genes, se pueden utilizar nucleasas diseñadas para introducir mutaciones en genes endógenos que generan una desactivación genética . [80] [81]
La ingeniería genética tiene aplicaciones en medicina, investigación, industria y agricultura y puede utilizarse en una amplia gama de plantas, animales y microorganismos. A las bacterias , los primeros organismos modificados genéticamente, se les puede insertar ADN plasmídico que contiene nuevos genes que codifican medicamentos o enzimas que procesan alimentos y otros sustratos . [82] [83] Las plantas han sido modificadas para protección contra insectos, resistencia a herbicidas , resistencia a virus, nutrición mejorada, tolerancia a presiones ambientales y la producción de vacunas comestibles . [84] La mayoría de los OGM comercializados son plantas de cultivo resistentes a los insectos o tolerantes a los herbicidas. [85] Se han utilizado animales genéticamente modificados para investigación, animales modelo y la producción de productos agrícolas o farmacéuticos. Los animales genéticamente modificados incluyen animales con genes desactivados , mayor susceptibilidad a las enfermedades , hormonas para un crecimiento adicional y la capacidad de expresar proteínas en la leche. [86]
La ingeniería genética tiene muchas aplicaciones en la medicina que incluyen la fabricación de medicamentos, la creación de animales modelo que imitan las condiciones humanas y la terapia genética . Uno de los primeros usos de la ingeniería genética fue producir en masa insulina humana en bacterias. [33] Esta aplicación ahora se ha aplicado a las hormonas de crecimiento humanas , las hormonas estimulantes del folículo (para el tratamiento de la infertilidad), la albúmina humana , los anticuerpos monoclonales , los factores antihemofílicos , las vacunas y muchos otros medicamentos. [87] [88] Los hibridomas de ratón , células fusionadas para crear anticuerpos monoclonales , se han adaptado mediante ingeniería genética para crear anticuerpos monoclonales humanos. [89] Se están desarrollando virus genéticamente modificados que aún pueden conferir inmunidad, pero carecen de secuencias infecciosas . [90]
La ingeniería genética también se utiliza para crear modelos animales de enfermedades humanas. Los ratones modificados genéticamente son el modelo animal modificado genéticamente más común. [91] Se han utilizado para estudiar y modelar el cáncer (el oncomotón ), la obesidad, las enfermedades cardíacas, la diabetes, la artritis, el abuso de sustancias, la ansiedad, el envejecimiento y la enfermedad de Parkinson. [92] Se pueden probar posibles curas en estos modelos de ratón.
La terapia génica es la ingeniería genética de los seres humanos , generalmente mediante la sustitución de genes defectuosos por otros eficaces. Se han realizado investigaciones clínicas utilizando terapia génica somática con varias enfermedades, incluida la SCID ligada al cromosoma X , [93] la leucemia linfocítica crónica (LLC), [94] [95] y la enfermedad de Parkinson . [96] En 2012, Alipogene tiparvovec se convirtió en el primer tratamiento de terapia génica aprobado para uso clínico. [97] [98] En 2015, se utilizó un virus para insertar un gen sano en las células de la piel de un niño que padecía una enfermedad rara de la piel, epidermólisis ampollosa , para crecer y luego injertar piel sana en el 80 por ciento de la piel del niño. organismo afectado por la enfermedad. [99]
La terapia genética de la línea germinal haría que cualquier cambio fuera heredable, lo que ha generado preocupación en la comunidad científica. [100] [101] En 2015, CRISPR se utilizó para editar el ADN de embriones humanos no viables , [102] [103] lo que llevó a los científicos de las principales academias del mundo a pedir una moratoria sobre las ediciones heredables del genoma humano. [104] También existe la preocupación de que la tecnología pueda usarse no sólo para el tratamiento, sino también para mejorar, modificar o alterar la apariencia, adaptabilidad, inteligencia, carácter o comportamiento de un ser humano. [105] La distinción entre curación y mejora también puede ser difícil de establecer. [106] En noviembre de 2018, He Jiankui anunció que había editado los genomas de dos embriones humanos para intentar desactivar el gen CCR5 , que codifica un receptor que el VIH utiliza para ingresar a las células. El trabajo fue ampliamente condenado por ser poco ético, peligroso y prematuro. [107] Actualmente, la modificación de la línea germinal está prohibida en 40 países. Los científicos que realizan este tipo de investigación a menudo dejan que los embriones crezcan durante unos días sin permitir que se conviertan en un bebé. [108]
Los investigadores están alterando el genoma de los cerdos para inducir el crecimiento de órganos humanos, con el objetivo de aumentar el éxito del trasplante de órganos de cerdo a humano . [109] Los científicos están creando "impulsores genéticos", cambiando los genomas de los mosquitos para hacerlos inmunes a la malaria y luego buscando propagar los mosquitos genéticamente alterados entre la población de mosquitos con la esperanza de eliminar la enfermedad. [110]
La ingeniería genética es una herramienta importante para los científicos naturales , siendo la creación de organismos transgénicos una de las herramientas más importantes para el análisis de la función genética. [111] Los genes y otra información genética de una amplia gama de organismos se pueden insertar en bacterias para su almacenamiento y modificación, creando bacterias genéticamente modificadas en el proceso. Las bacterias son baratas, fáciles de cultivar, clonales , se multiplican rápidamente, relativamente fáciles de transformar y pueden almacenarse a -80 °C casi indefinidamente. Una vez que se aísla un gen, se puede almacenar dentro de la bacteria, proporcionando un suministro ilimitado para la investigación. [112]
Los organismos están diseñados genéticamente para descubrir las funciones de ciertos genes. Este podría ser el efecto sobre el fenotipo del organismo, dónde se expresa el gen o con qué otros genes interactúa. Estos experimentos generalmente implican pérdida de función, ganancia de función, seguimiento y expresión.
Los organismos pueden transformar sus células con un gen que codifique una proteína útil, como una enzima, de modo que sobreexpresen la proteína deseada. Luego se pueden fabricar cantidades masivas de proteína haciendo crecer el organismo transformado en un equipo de biorreactor mediante fermentación industrial y luego purificando la proteína. [116] Algunos genes no funcionan bien en bacterias, por lo que también se pueden utilizar células de levadura, insectos o células de mamíferos. [117] Estas técnicas se utilizan para producir medicamentos como la insulina , la hormona del crecimiento humano y vacunas , suplementos como el triptófano , ayudas en la producción de alimentos ( quimosina en la elaboración de queso) y combustibles. [118] Otras aplicaciones con bacterias genéticamente modificadas podrían implicar hacerlas realizar tareas fuera de su ciclo natural, como producir biocombustibles , [119] limpiar derrames de petróleo, carbono y otros desechos tóxicos [120] y detectar arsénico en el agua potable. [121] Ciertos microbios genéticamente modificados también pueden usarse en biominería y biorremediación , debido a su capacidad para extraer metales pesados de su entorno e incorporarlos en compuestos que son más fácilmente recuperables. [122]
En ciencia de materiales , se ha utilizado un virus genéticamente modificado en un laboratorio de investigación como armazón para ensamblar una batería de iones de litio más respetuosa con el medio ambiente . [123] [124] También se han diseñado bacterias para que funcionen como sensores expresando una proteína fluorescente en determinadas condiciones ambientales. [125]

Una de las aplicaciones más conocidas y controvertidas de la ingeniería genética es la creación y uso de cultivos genéticamente modificados o ganado genéticamente modificado para producir alimentos genéticamente modificados . Se han desarrollado cultivos para aumentar la producción, aumentar la tolerancia al estrés abiótico , alterar la composición de los alimentos o producir nuevos productos. [127]
Los primeros cultivos que se comercializaron a gran escala ofrecieron protección contra plagas de insectos o tolerancia a los herbicidas . También se han desarrollado o están en desarrollo cultivos resistentes a hongos y virus. [128] [129] Esto facilita el manejo de insectos y malezas de los cultivos y puede aumentar indirectamente el rendimiento de los cultivos. [130] [131] También se están desarrollando cultivos transgénicos que mejoran directamente el rendimiento acelerando el crecimiento o haciendo que la planta sea más resistente (mejorando la tolerancia a la sal, el frío o la sequía). [132] En 2016, el salmón fue modificado genéticamente con hormonas de crecimiento para alcanzar el tamaño adulto normal mucho más rápido. [133]
Se han desarrollado OGM que modifican la calidad de los productos aumentando el valor nutricional o proporcionando cualidades o cantidades más útiles industrialmente. [132] La papa Amflora produce una mezcla de almidones más útil industrialmente. La soja y la canola han sido modificadas genéticamente para producir aceites más saludables. [134] [135] El primer alimento transgénico comercializado fue un tomate que había retrasado la maduración, aumentando su vida útil . [136]
Las plantas y los animales han sido diseñados para producir materiales que normalmente no fabrican. El Pharming utiliza cultivos y animales como biorreactores para producir vacunas, fármacos intermedios o los propios fármacos; el producto útil se purifica a partir de la cosecha y luego se utiliza en el proceso de producción farmacéutica estándar. [137] Las vacas y las cabras han sido diseñadas para expresar medicamentos y otras proteínas en su leche, y en 2009 la FDA aprobó un medicamento producido en leche de cabra. [138] [139]
La ingeniería genética tiene aplicaciones potenciales en la conservación y el manejo de áreas naturales. La transferencia de genes a través de vectores virales se ha propuesto como un medio para controlar especies invasoras, así como para vacunar a la fauna amenazada contra enfermedades. [140] Se han sugerido árboles transgénicos como una forma de conferir resistencia a los patógenos en poblaciones silvestres. [141] Con los crecientes riesgos de mala adaptación en los organismos como resultado del cambio climático y otras perturbaciones, la adaptación facilitada mediante ajustes genéticos podría ser una solución para reducir los riesgos de extinción. [142] Las aplicaciones de la ingeniería genética en la conservación son hasta ahora en su mayoría teóricas y aún no se han puesto en práctica.
La ingeniería genética también se utiliza para crear arte microbiano . [143] Algunas bacterias han sido modificadas genéticamente para crear fotografías en blanco y negro. [144] Artículos novedosos como claveles de color lavanda , [145] rosas azules , [146] y peces brillantes [147] [148] también se han producido mediante ingeniería genética.
La regulación de la ingeniería genética se refiere a los enfoques adoptados por los gobiernos para evaluar y gestionar los riesgos asociados con el desarrollo y la liberación de OGM. El desarrollo de un marco regulatorio comenzó en 1975, en Asilomar , California. [149] La reunión de Asilomar recomendó un conjunto de directrices voluntarias sobre el uso de tecnología recombinante. [31] A medida que la tecnología mejoró, EE. UU. estableció un comité en la Oficina de Ciencia y Tecnología , [150] que asignó la aprobación regulatoria de alimentos transgénicos al USDA, la FDA y la EPA. [151] El Protocolo de Cartagena sobre Seguridad de la Biotecnología , un tratado internacional que rige la transferencia, manipulación y uso de OGM, [152] fue adoptado el 29 de enero de 2000. [153] Ciento cincuenta y siete países son miembros del Protocolo, y muchos lo utilizan como punto de referencia para sus propias regulaciones. [154]
El estatus legal y regulatorio de los alimentos transgénicos varía según el país: algunas naciones los prohíben o restringen, y otras los permiten con grados de regulación muy diferentes. [155] [156] [157] [158] Algunos países permiten la importación de alimentos genéticamente modificados con autorización, pero no permiten su cultivo (Rusia, Noruega, Israel) o tienen disposiciones para el cultivo aunque todavía no se produzcan productos genéticamente modificados. (Japón, Corea del Sur). La mayoría de los países que no permiten el cultivo de OGM sí permiten la investigación. [159] Algunas de las diferencias más marcadas ocurren entre Estados Unidos y Europa. La política estadounidense se centra en el producto (no en el proceso), sólo mira riesgos científicos verificables y utiliza el concepto de equivalencia sustancial . [160] La Unión Europea, por el contrario, tiene posiblemente las regulaciones sobre OGM más estrictas del mundo. [161] Todos los OGM, junto con los alimentos irradiados , se consideran "alimentos nuevos" y están sujetos a una evaluación exhaustiva de los alimentos, caso por caso, con base científica por parte de la Autoridad Europea de Seguridad Alimentaria . Los criterios de autorización se dividen en cuatro grandes categorías: "seguridad", "libertad de elección", "etiquetado" y "trazabilidad". [162] El nivel de regulación en otros países que cultivan OGM se encuentra entre Europa y Estados Unidos.
Una de las cuestiones clave que preocupan a los reguladores es si los productos genéticamente modificados deben etiquetarse. La Comisión Europea afirma que el etiquetado y la trazabilidad obligatorios son necesarios para permitir una elección informada, evitar posibles publicidades engañosas [173] y facilitar la retirada de productos si se descubren efectos adversos para la salud o el medio ambiente. [174] La Asociación Médica Estadounidense [175] y la Asociación Estadounidense para el Avance de la Ciencia [176] dicen que, en ausencia de evidencia científica de daño, incluso el etiquetado voluntario es engañoso y alarmará falsamente a los consumidores. En 64 países se exige el etiquetado de los productos transgénicos en el mercado. [177] El etiquetado puede ser obligatorio hasta un nivel umbral de contenido de transgénicos (que varía según el país) o voluntario. En Canadá y Estados Unidos el etiquetado de alimentos genéticamente modificados es voluntario, [178] mientras que en Europa todos los alimentos (incluidos los procesados ) o piensos que contengan más del 0,9% de OGM aprobados deben estar etiquetados. [161]
Los críticos se han opuesto al uso de la ingeniería genética por varios motivos, incluidas preocupaciones éticas, ecológicas y económicas. Muchas de estas preocupaciones tienen que ver con los cultivos transgénicos y si los alimentos producidos a partir de ellos son seguros y qué impacto tendrá su cultivo en el medio ambiente. Estas controversias han dado lugar a litigios, disputas comerciales internacionales y protestas, y a una regulación restrictiva de los productos comerciales en algunos países. [179]
Desde el principio se han atribuido a esta tecnología acusaciones de que los científicos " juegan a ser Dios " y otras cuestiones religiosas . [180] Otras cuestiones éticas planteadas incluyen el patentamiento de la vida , [181] el uso de los derechos de propiedad intelectual , [182] el nivel de etiquetado de los productos, [183] [184] el control del suministro de alimentos [185] y la objetividad del proceso regulatorio. [186] Aunque se han planteado dudas, [187] económicamente la mayoría de los estudios han encontrado que el cultivo de cultivos transgénicos es beneficioso para los agricultores. [188] [189] [190]
El flujo genético entre cultivos transgénicos y plantas compatibles, junto con un mayor uso de herbicidas selectivos , puede aumentar el riesgo de que se desarrollen " supermalezas ". [191] Otras preocupaciones ambientales implican impactos potenciales en organismos no objetivo, incluidos los microbios del suelo , [192] y un aumento de plagas de insectos secundarias y resistentes. [193] [194] Muchos de los impactos ambientales relacionados con los cultivos transgénicos pueden tardar muchos años en comprenderse y también son evidentes en las prácticas agrícolas convencionales. [192] [195] Con la comercialización de peces genéticamente modificados existen preocupaciones sobre cuáles serán las consecuencias ambientales si escapan. [196]
Hay tres preocupaciones principales sobre la seguridad de los alimentos genéticamente modificados: si pueden provocar una reacción alérgica ; si los genes podrían transferirse de los alimentos a las células humanas; y si los genes no aprobados para el consumo humano podrían cruzarse con otros cultivos. [197] Existe un consenso científico [198] [199] [200] [201] de que los alimentos actualmente disponibles derivados de cultivos transgénicos no representan un riesgo mayor para la salud humana que los alimentos convencionales, [202] [203] [204] [205 ] [206] pero que cada alimento genéticamente modificado debe analizarse caso por caso antes de su introducción. [207] [208] [209] No obstante, los miembros del público tienen menos probabilidades que los científicos de percibir los alimentos transgénicos como seguros. [210] [211] [212] [213]
La ingeniería genética aparece en muchas historias de ciencia ficción . [214] La novela de Frank Herbert La peste blanca describe el uso deliberado de la ingeniería genética para crear un patógeno que mata específicamente a las mujeres. [214] Otra de las creaciones de Herbert, la serie de novelas Dune , utiliza la ingeniería genética para crear al poderoso Tleilaxu . [215] Pocas películas han informado al público sobre la ingeniería genética, con la excepción de The Boys from Brazil de 1978 y Jurassic Park de 1993 , las cuales utilizan una lección, una demostración y un fragmento de una película científica. [216] [217] Los métodos de ingeniería genética están débilmente representados en el cine; Michael Clark, que escribe para Wellcome Trust , califica la representación de la ingeniería genética y la biotecnología como "gravemente distorsionada" [217] en películas como The 6th Day . En opinión de Clark, a la biotecnología normalmente se le "dan formas fantásticas pero visualmente llamativas", mientras que la ciencia es relegada a un segundo plano o ficcionalizada para adaptarse a una audiencia joven. [217]
Ingeniería genética: manipulación de la dotación genética de un organismo mediante la introducción o eliminación de genes específicos mediante técnicas modernas de biología molecular. Una definición amplia de ingeniería genética también incluye la cría selectiva y otros medios de selección artificial.
{{cite web}}: CS1 maint: bot: original URL status unknown (link){{cite journal}}: |author1=tiene nombre genérico ( ayuda )El etiquetado debe incluir información objetiva en el sentido de que un alimento o pienso está compuesto, contiene o se ha producido a partir de OGM. Un etiquetado claro, independientemente de la detectabilidad del ADN o de las proteínas resultantes de la modificación genética en el producto final, responde a las exigencias expresadas en numerosas encuestas por una gran mayoría de consumidores, facilita la elección informada y evita posibles engaños a los consumidores en cuanto a los métodos de fabricación o producción.
(3) Los requisitos de trazabilidad de los OMG deben facilitar tanto la retirada de productos cuando se establezcan efectos adversos imprevistos para la salud humana, la salud animal o el medio ambiente, incluidos los ecosistemas, como la orientación del seguimiento para examinar los posibles efectos, en particular, sobre el medio ambiente. . La trazabilidad también debería facilitar la implementación de medidas de gestión de riesgos de acuerdo con el principio de precaución. (4) Deben establecerse requisitos de trazabilidad para los alimentos y piensos producidos a partir de OMG para facilitar un etiquetado preciso de dichos productos.
Hemos revisado la literatura científica sobre la seguridad de los cultivos transgénicos durante los últimos 10 años que capta el consenso científico madurado desde que las plantas transgénicas se cultivaron ampliamente en todo el mundo, y podemos concluir que la investigación científica realizada hasta ahora no ha detectado ninguna peligro significativo directamente relacionado con el uso de cultivos transgénicos. La literatura sobre la biodiversidad y el consumo de alimentos y piensos genéticamente modificados ha dado lugar en ocasiones a un animado debate sobre la idoneidad de los diseños experimentales, la elección de los métodos estadísticos o la accesibilidad pública de los datos. Dicho debate, aunque sea positivo y forme parte del proceso natural de revisión por parte de la comunidad científica, con frecuencia ha sido distorsionado por los medios de comunicación y a menudo utilizado políticamente e inapropiadamente en campañas contra los cultivos transgénicos.
Los cultivos transgénicos actualmente disponibles y los alimentos derivados de ellos se han considerado seguros para el consumo y los métodos utilizados para probar su seguridad se han considerado apropiados. Estas conclusiones representan el consenso de la evidencia científica analizada por el ICSU (2003) y son consistentes con las opiniones de la Organización Mundial de la Salud (OMS, 2002). Varias autoridades reguladoras nacionales (entre otras, la Argentina, el Brasil, el Canadá, China, el Reino Unido y los Estados Unidos) han evaluado la existencia de mayores riesgos para la salud humana de estos alimentos utilizando sus procedimientos nacionales de inocuidad de los alimentos (ICSU). Hasta la fecha, no se han descubierto en ningún lugar del mundo efectos adversos, tóxicos o nutricionalmente nocivos verificables resultantes del consumo de alimentos derivados de cultivos genéticamente modificados (GM Science Review Panel). Muchos millones de personas han consumido alimentos derivados de plantas transgénicas (principalmente maíz, soja y colza) sin que se hayan observado efectos adversos (ICSU).
Existe un amplio consenso científico en que los cultivos genéticamente modificados que se encuentran actualmente en el mercado son seguros para el consumo. Después de 14 años de cultivo y un total acumulado de 2 mil millones de acres plantados, no se han producido efectos adversos para la salud o el medio ambiente debido a la comercialización de cultivos genéticamente modificados (Junta de Agricultura y Recursos Naturales, Comité de Impactos Ambientales Asociados con la Comercialización de Plantas Transgénicas, National Research Consejo y División de Estudios de la Tierra y la Vida 2002). Tanto el Consejo Nacional de Investigación de EE.UU. como el Centro Común de Investigación (el laboratorio de investigación científica y técnica de la Unión Europea y parte integral de la Comisión Europea) han llegado a la conclusión de que existe un cuerpo integral de conocimientos que aborda adecuadamente la cuestión de la seguridad alimentaria de los cultivos genéticamente modificados. (Comité para la identificación y evaluación de efectos no deseados de alimentos genéticamente modificados en la salud humana y Consejo Nacional de Investigación 2004; Centro Conjunto de Investigación de la Comisión Europea 2008). Estos y otros informes recientes concluyen que los procesos de ingeniería genética y mejoramiento convencional no son diferentes en términos de consecuencias no deseadas para la salud humana y el medio ambiente (Dirección General de Investigación e Innovación de la Comisión Europea, 2010).
A pesar de ello, el número de estudios centrados específicamente en la evaluación de la seguridad de plantas transgénicas es todavía limitado. Sin embargo, es importante señalar que por primera vez se ha logrado un cierto equilibrio en el número de grupos de investigación que sugieren, basándose en sus estudios, que varias variedades de productos genéticamente modificados (principalmente maíz y soja) son tan seguros y nutritivos como así como las respectivas plantas convencionales no modificadas genéticamente, y aquellas que todavía plantean serias preocupaciones. Además, cabe mencionar que la mayoría de los estudios que demuestran que los alimentos transgénicos son tan nutricionales y seguros como los obtenidos mediante mejoramiento convencional, han sido realizados por empresas biotecnológicas o asociadas, que también se encargan de comercializar estas plantas transgénicas. De todos modos, esto representa un avance notable en comparación con la falta de estudios publicados en los últimos años en revistas científicas por esas empresas.Krimsky S (2015). "Un consenso ilusorio detrás de la evaluación de la salud de los OGM" (PDF) . Ciencia, tecnología y valores humanos . 40 (6): 883–914. doi :10.1177/0162243915598381. S2CID 40855100. Archivado desde el original (PDF) el 7 de febrero de 2016 . Consultado el 30 de octubre de 2016 .
Comencé este artículo con testimonios de científicos respetados de que literalmente no existe controversia científica sobre los efectos de los OGM en la salud. Mi investigación de la literatura científica cuenta otra historia.Y contraste: Panchin AY, Tuzhikov AI (marzo de 2017). "Los estudios publicados sobre OGM no encuentran evidencia de daño cuando se corrigen para comparaciones múltiples". Reseñas críticas en biotecnología . 37 (2): 213–217. doi :10.3109/07388551.2015.1130684. PMID 26767435. S2CID 11786594.
Aquí, mostramos que una serie de artículos, algunos de los cuales han influido fuerte y negativamente en la opinión pública sobre los cultivos transgénicos e incluso han provocado acciones políticas, como el embargo de transgénicos, comparten fallas comunes en la evaluación estadística de los datos. . Habiendo tenido en cuenta estos defectos, concluimos que los datos presentados en estos artículos no proporcionan ninguna evidencia sustancial del daño de los OGM. Los artículos presentados que sugieren posibles daños de los OGM recibieron gran atención pública. Sin embargo, a pesar de sus afirmaciones, en realidad debilitan la evidencia del daño y la falta de equivalencia sustancial de los OGM estudiados. Destacamos que con más de 1783 artículos publicados sobre OGM en los últimos 10 años, se espera que algunos de ellos hayan informado diferencias no deseadas entre los OGM y los cultivos convencionales, incluso si tales diferencias no existen en la realidad.y Yang YT, Chen B (abril de 2016). "Gobierno de los OGM en los EE. UU.: ciencia, derecho y salud pública". Revista de Ciencias de la Alimentación y la Agricultura . 96 (6): 1851–5. Código Bib : 2016JSFA...96.1851Y. doi :10.1002/jsfa.7523. PMID 26536836.
Por lo tanto, no sorprende que los esfuerzos para exigir el etiquetado y prohibir los OGM hayan sido una cuestión política creciente en los EE. UU.
(citando a Domingo y Bordonaba, 2011)
. En general, un amplio consenso científico sostiene que los alimentos genéticamente modificados actualmente comercializados no presentan mayores riesgos que los alimentos convencionales... Las principales asociaciones científicas y médicas nacionales e internacionales han declarado que no se han informado ni comprobado efectos adversos para la salud humana relacionados con los alimentos genéticamente modificados en estudios de pares. literatura revisada hasta la fecha. A pesar de diversas preocupaciones, hoy en día, la Asociación Estadounidense para el Avance de la Ciencia, la Organización Mundial de la Salud y muchas organizaciones científicas internacionales independientes coinciden en que los OGM son tan seguros como otros alimentos. En comparación con las técnicas de mejoramiento convencionales, la ingeniería genética es mucho más precisa y, en la mayoría de los casos, es menos probable que genere un resultado inesperado.
La UE, por ejemplo, ha invertido más de 300 millones de euros en investigación sobre la bioseguridad de los OGM. Su reciente informe afirma: "La principal conclusión que se desprende de los esfuerzos de más de 130 proyectos de investigación, que abarcan un período de más de 25 años de investigación y en los que participan más de 500 grupos de investigación independientes, es que la biotecnología, y en particular los OGM, no son per se más riesgosas que, por ejemplo, las tecnologías convencionales de fitomejoramiento". La Organización Mundial de la Salud, la Asociación Médica Estadounidense, la Academia Nacional de Ciencias de los Estados Unidos, la Sociedad Real Británica y todas las demás organizaciones respetadas que han examinado la evidencia han llegado a la misma conclusión: consumir alimentos que contienen ingredientes derivados de cultivos transgénicos no es más riesgoso. que consumir los mismos alimentos que contienen ingredientes de plantas cultivadas modificadas mediante técnicas convencionales de mejora de plantas.Pinholster G (25 de octubre de 2012). "Junta directiva de la AAAS: Exigir legalmente etiquetas de alimentos transgénicos podría" engañar y alarmar falsamente a los consumidores"". Asociación Estadounidense para el Avance de la Ciencia . Consultado el 8 de febrero de 2016 .
Un informe emitido por el consejo científico de la Asociación Médica Americana (AMA) afirma que no se han detectado efectos a largo plazo en la salud por el uso de cultivos transgénicos y alimentos genéticamente modificados, y que estos alimentos son sustancialmente equivalentes a sus homólogos convencionales.
(del resumen en línea preparado por
ISAAA
)
" "Los cultivos y alimentos producidos utilizando técnicas de ADN recombinante han estado disponibles durante menos de 10 años y hasta la fecha no se han detectado efectos a largo plazo. Estos alimentos son sustancialmente equivalentes a sus homólogos convencionales.
"Informe 2 del Consejo de Ciencia y Salud Pública (A-12): Etiquetado de alimentos de bioingeniería" (PDF) . Asociación Médica Estadounidense. 2012. Archivado desde el original el 7 de septiembre de 2012 . Consultado el 19 de marzo de 2016 .
Los alimentos elaborados mediante bioingeniería se han consumido durante casi 20 años y, durante ese tiempo, no se han informado ni fundamentado consecuencias manifiestas para la salud humana en la literatura revisada por pares.
{{cite web}}: CS1 maint: bot: original URL status unknown (link)Varias organizaciones científicas en los EE. UU. han publicado estudios o declaraciones sobre la seguridad de los OGM indicando que no hay evidencia de que los OGM presenten riesgos de seguridad únicos en comparación con los productos obtenidos convencionalmente. Estos incluyen el Consejo Nacional de Investigación, la Asociación Estadounidense para el Avance de la Ciencia y la Asociación Médica Estadounidense. Los grupos en Estados Unidos que se oponen a los OGM incluyen algunas organizaciones ambientalistas, organizaciones de agricultura orgánica y organizaciones de consumidores. Un número sustancial de académicos del derecho ha criticado el enfoque de Estados Unidos para regular los OGM.
Hallazgo general sobre los supuestos efectos adversos en la salud humana de los alimentos derivados de cultivos transgénicos: sobre la base de un examen detallado de las comparaciones de alimentos transgénicos actualmente comercializados con alimentos no transgénicos en análisis de composición, pruebas de toxicidad aguda y crónica en animales, datos a largo plazo sobre la salud. de ganado alimentado con alimentos transgénicos y datos epidemiológicos humanos, el comité no encontró diferencias que impliquen un mayor riesgo para la salud humana de los alimentos transgénicos que de sus contrapartes no transgénicos.
Los diferentes organismos genéticamente modificados incluyen diferentes genes insertados de diferentes maneras. Esto significa que los alimentos transgénicos individuales y su seguridad deben evaluarse caso por caso y que no es posible hacer declaraciones generales sobre la seguridad de todos los alimentos transgénicos. Los alimentos transgénicos actualmente disponibles en el mercado internacional han pasado evaluaciones de seguridad y no es probable que presenten riesgos para la salud humana. Además, no se han demostrado efectos sobre la salud humana como resultado del consumo de dichos alimentos por parte de la población general en los países donde han sido aprobados. La aplicación continua de evaluaciones de seguridad basadas en los principios del Codex Alimentarius y, cuando corresponda, un seguimiento adecuado posterior a la comercialización, debería constituir la base para garantizar la seguridad de los alimentos genéticamente modificados.
Estos principios dictan una evaluación previa a la comercialización caso por caso que incluye una evaluación de los efectos directos e involuntarios.
En nuestra opinión, el potencial de los alimentos transgénicos para causar efectos nocivos para la salud es muy pequeño y muchas de las preocupaciones expresadas se aplican con igual vigor a los alimentos derivados convencionalmente. Sin embargo, hasta el momento no se pueden descartar por completo los problemas de seguridad basándose en la información actualmente disponible. Cuando se busca optimizar el equilibrio entre beneficios y riesgos, es prudente pecar de cauteloso y, sobre todo, aprender acumulando conocimientos y experiencia. Cualquier tecnología nueva, como la modificación genética, debe examinarse en busca de posibles beneficios y riesgos para la salud humana y el medio ambiente. Como ocurre con todos los nuevos alimentos, las evaluaciones de seguridad en relación con los alimentos genéticamente modificados deben realizarse caso por caso. Los miembros del jurado del proyecto GM fueron informados sobre diversos aspectos de la modificación genética por un grupo diverso de reconocidos expertos en los temas relevantes. El jurado de transgénicos llegó a la conclusión de que se debe detener la venta de alimentos transgénicos actualmente disponibles y que se debe continuar con la moratoria sobre el crecimiento comercial de cultivos transgénicos. Estas conclusiones se basaron en el principio de precaución y la falta de evidencia de algún beneficio. El jurado expresó su preocupación por el impacto de los cultivos transgénicos en la agricultura, el medio ambiente, la seguridad alimentaria y otros posibles efectos sobre la salud. La revisión de la Royal Society (2002) concluyó que los riesgos para la salud humana asociados con el uso de secuencias de ADN viral específicas en plantas transgénicas son insignificantes y, si bien pidió precaución en la introducción de posibles alérgenos en cultivos alimentarios, destacó la ausencia de evidencia de que Los alimentos transgénicos disponibles comercialmente causan manifestaciones clínicas alérgicas. La BMA comparte la opinión de que no existe evidencia sólida que demuestre que los alimentos transgénicos no sean seguros, pero respaldamos el llamado a realizar más investigaciones y vigilancia para proporcionar evidencia convincente de seguridad y beneficio.
Las mayores diferencias entre el público y los científicos de la AAAS se encuentran en las creencias sobre la seguridad de comer alimentos genéticamente modificados (GM). Casi nueve de cada diez científicos (88%) dicen que, en general, es seguro comer alimentos transgénicos en comparación con el 37% del público en general, una diferencia de 51 puntos porcentuales.