El músculo esquelético (comúnmente denominado músculo ) es uno de los tres tipos de tejido muscular de los vertebrados , siendo el otro el músculo cardíaco y el músculo liso . Son parte del sistema muscular voluntario [1] y normalmente están unidos mediante tendones a los huesos del esqueleto . [2] [3] Las células del músculo esquelético son mucho más largas que en los otros tipos de tejido muscular y también se conocen como fibras musculares . [4] El tejido de un músculo esquelético es estriado y tiene una apariencia rayada debido a la disposición de los sarcómeros .
Un músculo esquelético contiene múltiples fascículos (haces de fibras musculares). Cada fibra individual y cada músculo están rodeados por un tipo de capa de tejido conectivo de fascia . Las fibras musculares se forman a partir de la fusión de mioblastos en desarrollo en un proceso conocido como miogénesis que da como resultado células largas multinucleadas . En estas células, los núcleos , denominados mionúcleos , están situados a lo largo del interior de la membrana celular . Las fibras musculares también tienen múltiples mitocondrias para satisfacer las necesidades energéticas.
Las fibras musculares están compuestas a su vez por miofibrillas . Las miofibrillas están compuestas de filamentos de actina y miosina llamados miofilamentos , repetidos en unidades llamadas sarcómeros, que son las unidades contráctiles funcionales básicas de la fibra muscular necesarias para la contracción muscular . [5] Los músculos funcionan predominantemente mediante la oxidación de grasas y carbohidratos , pero también se utilizan reacciones químicas anaeróbicas , particularmente mediante fibras de contracción rápida. Estas reacciones químicas producen moléculas de trifosfato de adenosina (ATP) que se utilizan para impulsar el movimiento de las cabezas de miosina . [6]
El músculo esquelético constituye aproximadamente el 35% del peso del cuerpo humano. [7] Las funciones del músculo esquelético incluyen producir movimiento, mantener la postura corporal, controlar la temperatura corporal y estabilizar las articulaciones. [8] El músculo esquelético también es un órgano endocrino . [9] [10] [11] En diferentes condiciones fisiológicas, en el secretoma de los músculos esqueléticos se encuentran subconjuntos de 654 proteínas diferentes, así como lípidos, aminoácidos, metabolitos y pequeños ARN . [12]
Los músculos esqueléticos están compuestos sustancialmente de fibras musculares contráctiles multinucleadas (miocitos). Sin embargo, en los músculos esqueléticos también hay un número considerable de células mononucleares residentes e infiltrantes. [13] En términos de volumen, los miocitos constituyen la gran mayoría del músculo esquelético. Los miocitos del músculo esquelético suelen ser muy grandes, midiendo entre 2 y 3 cm de largo y 100 μm de diámetro. [14] En comparación, las células mononucleares de los músculos son mucho más pequeñas. Algunas de las células mononucleares de los músculos [15] son células endoteliales (que miden aproximadamente 50 a 70 μm de largo, 10 a 30 μm de ancho y 0,1 a 10 μm de espesor), [16] macrófagos (21 μm de diámetro) y neutrófilos (12). -15 μm de diámetro). [17] Sin embargo, en términos de núcleos presentes en el músculo esquelético, los núcleos de miocitos pueden ser sólo la mitad de los núcleos presentes, mientras que los núcleos de células mononucleares residentes e infiltrantes constituyen la otra mitad. [13]
Una considerable investigación sobre el músculo esquelético se centra en las células de las fibras musculares, los miocitos, como se analiza en detalle en las primeras secciones a continuación. Sin embargo, recientemente, el interés también se ha centrado en los diferentes tipos de células mononucleares del músculo esquelético, así como en las funciones endocrinas del músculo, que se describen más adelante.
Hay más de 600 músculos esqueléticos en el cuerpo humano, que representan alrededor del 40% del peso corporal en adultos jóvenes sanos. [18] [19] [20] En las poblaciones occidentales, los hombres tienen en promedio alrededor de un 61% más de músculo esquelético que las mujeres. [21] La mayoría de los músculos se presentan en pares colocados bilateralmente para servir a ambos lados del cuerpo. Los músculos suelen clasificarse como grupos de músculos que trabajan juntos para realizar una acción. En el torso hay varios grupos de músculos principales, incluidos los músculos pectorales y abdominales ; Los músculos intrínsecos y extrínsecos son subdivisiones de grupos de músculos de la mano , el pie , la lengua y los músculos extraoculares del ojo . Los músculos también se agrupan en compartimentos que incluyen cuatro grupos en el brazo y cuatro grupos en la pierna .
Además de la parte contráctil de un músculo que consta de sus fibras, un músculo contiene una parte no contráctil de tejido conectivo fibroso denso que forma el tendón en cada extremo. Los tendones unen los músculos a los huesos para dar movimiento esquelético. La longitud de un músculo incluye los tendones. El tejido conectivo está presente en todos los músculos como fascia profunda . La fascia profunda se especializa dentro de los músculos para encerrar cada fibra muscular como endomisio ; cada fascículo muscular como perimisio , y cada músculo individual como epimisio . En conjunto estas capas se denominan misia . La fascia profunda también separa los grupos de músculos en compartimentos musculares.
Dos tipos de receptores sensoriales que se encuentran en los músculos son los husos musculares y los órganos tendinosos de Golgi . Los husos musculares son receptores de estiramiento ubicados en el vientre del músculo. Los órganos tendinosos de Golgi son propioceptores ubicados en la unión miotendinosa que informan de la tensión de un músculo .
Las células del músculo esquelético son las células contráctiles individuales dentro de un músculo y, a menudo, se denominan fibras musculares . [3] Un solo músculo, como el bíceps en un hombre adulto joven, contiene alrededor de 253.000 fibras musculares. [22]
Las fibras del músculo esquelético son multinucleadas y los núcleos a menudo se denominan mionúcleos . Esto ocurre durante la miogénesis con la fusión de mioblastos, cada uno de los cuales aporta un núcleo. [23] La fusión depende de proteínas específicas de los músculos conocidas como fusógenos llamadas myomaker y myomerger . [24]
La célula del músculo esquelético necesita muchos núcleos para producir grandes cantidades de proteínas y enzimas necesarias para el funcionamiento normal de la célula. Una sola fibra muscular puede contener desde cientos hasta miles de núcleos. [25] Una fibra muscular, por ejemplo en el bíceps humano, con una longitud de 10 cm puede tener hasta 3.000 núcleos. [25] A diferencia de una célula no muscular donde el núcleo está ubicado centralmente, el mionúcleo es alargado y está ubicado cerca del sarcolema . Los mionúcleos están dispuestos de manera bastante uniforme a lo largo de la fibra y cada núcleo tiene su propio dominio mionuclear donde es responsable de soportar el volumen de citoplasma en esa sección particular de la miofibra. [24] [25]
Un grupo de células madre musculares conocidas como células miosatélites , también células satélite, se encuentran entre la membrana basal y el sarcolema de las fibras musculares. Estas células normalmente están inactivas, pero pueden activarse mediante ejercicio o patología para proporcionar mionúcleos adicionales para el crecimiento o la reparación muscular. [26]
Los músculos se unen a los tendones en una región de interfaz compleja conocida como unión musculotendinosa, también conocida como unión miotendinosa , un área especializada para la transmisión primaria de fuerza. [27] En la interfaz músculo-tendón, la fuerza se transmite desde los sarcómeros de las células musculares al tendón. [5] Los músculos y tendones se desarrollan en estrecha asociación, y después de unirse en la unión miotendinosa constituyen una unidad dinámica para la transmisión de fuerza desde la contracción muscular al sistema esquelético. [27]

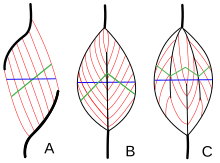
La arquitectura muscular se refiere a la disposición de las fibras musculares con respecto al eje de generación de fuerza , que va desde el origen de un músculo hasta su inserción . Las disposiciones habituales son tipos de músculo paralelo y tipos de músculo penado . En los músculos paralelos, los fascículos corren paralelos al eje de generación de fuerza, pero los fascículos pueden variar en su relación entre sí y con sus tendones. [28] Estas variaciones se observan en los músculos fusiforme , correa y convergente . [4] Un músculo convergente tiene forma triangular o de abanico ya que las fibras convergen en su inserción y se abren en abanico en el origen. [28] Un ejemplo menos común de músculo paralelo es un músculo circular como el orbicular de los ojos , en el que las fibras están dispuestas longitudinalmente, pero crean un círculo desde el origen hasta la inserción. [29] Estas diferentes arquitecturas pueden causar variaciones en la tensión que un músculo puede crear entre sus tendones.
Las fibras de los músculos pennates corren en ángulo con respecto al eje de generación de fuerza. [29] Este ángulo de pennación reduce la fuerza efectiva de cualquier fibra individual, ya que efectivamente tira fuera del eje. Sin embargo, debido a este ángulo, se pueden empaquetar más fibras en el mismo volumen muscular, aumentando el área de sección transversal fisiológica (PCSA). Este efecto se conoce como empaquetamiento de fibra y, en términos de generación de fuerza, supera con creces la pérdida de eficiencia de la orientación fuera del eje. La compensación se produce en la velocidad general de acortamiento muscular y en la excursión total. La velocidad general de acortamiento del músculo se reduce en comparación con la velocidad de acortamiento de las fibras, al igual que la distancia total de acortamiento. [29] Todos estos efectos escalan con el ángulo de pennación; ángulos mayores conducen a una mayor fuerza debido al mayor empaquetamiento de fibra y PCSA, pero con mayores pérdidas en el acortamiento de la velocidad y la excursión. Los tipos de músculo penado son unipenados , bipennados y multipennados . Un músculo unipennate tiene fibras en ángulos similares que se encuentran en un lado de un tendón. Un músculo bipennado tiene fibras en dos lados de un tendón. Los músculos multipennates tienen fibras que están orientadas en múltiples ángulos a lo largo del eje generador de fuerza, y esta es la arquitectura más general y común. [29]
Las fibras musculares crecen cuando se ejercitan y se encogen cuando no están en uso. Esto se debe al hecho de que el ejercicio estimula el aumento de miofibrillas que aumentan el tamaño total de las células musculares. Los músculos bien ejercitados no sólo pueden aumentar su tamaño sino que también pueden desarrollar más mitocondrias , mioglobina , glucógeno y una mayor densidad de capilares . Sin embargo, las células musculares no pueden dividirse para producir nuevas células y, como resultado, hay menos células musculares en un adulto que en un recién nacido. [30]
Hay una serie de términos utilizados para nombrar los músculos, incluidos los relacionados con el tamaño, la forma, la acción, la ubicación, su orientación y el número de cabezas.
A grandes rasgos existen dos tipos de fibras musculares: el tipo I , que es lento, y el tipo II, que son rápidos. El tipo II tiene dos divisiones: el tipo IIA (oxidativo) y el tipo IIX (glicolítico), lo que da tres tipos principales de fibras. [33] Estas fibras tienen propiedades metabólicas, contráctiles y de unidades motoras relativamente distintas . La siguiente tabla diferencia este tipo de propiedades. Este tipo de propiedades, si bien dependen en parte de las propiedades de las fibras individuales, tienden a ser relevantes y medirse a nivel de la unidad motora, más que de la fibra individual. [34]
Las fibras oxidativas lentas (tipo I) se contraen relativamente lentamente y utilizan la respiración aeróbica para producir ATP. Las fibras oxidativas rápidas (tipo IIA) tienen contracciones rápidas y utilizan principalmente respiración aeróbica, pero debido a que pueden cambiar a respiración anaeróbica (glucólisis), pueden fatigarse más rápidamente que las fibras oxidativas lentas. Las fibras glicolíticas rápidas (tipo IIX) tienen contracciones rápidas y utilizan principalmente glucólisis anaeróbica. Las fibras FG se fatigan más rápidamente que las demás. La mayoría de los músculos esqueléticos de un ser humano contienen los tres tipos, aunque en proporciones variables. [35]
Tradicionalmente, las fibras se clasificaban según su color variable, que es un reflejo del contenido de mioglobina . Las fibras tipo I aparecen rojas debido a los altos niveles de mioglobina. Las fibras musculares rojas tienden a tener más mitocondrias y mayor densidad capilar local. Estas fibras son más adecuadas para la resistencia y tardan en fatigarse porque utilizan el metabolismo oxidativo para generar ATP ( trifosfato de adenosina ). Las fibras tipo II, menos oxidativas, son blancas debido a la mioglobina relativamente baja y a la dependencia de las enzimas glicolíticas.
Las fibras también se pueden clasificar según su capacidad de contracción, en contracción rápida y lenta. Estos rasgos se superponen en gran medida, pero no completamente, con las clasificaciones basadas en el color, la ATPasa o el MHC ( cadena pesada de miosina ).
Algunos autores definen una fibra de contracción rápida como aquella en la que la miosina puede dividir el ATP muy rápidamente. Estos incluyen principalmente las fibras ATPasa tipo II y MHC tipo II. Sin embargo, las fibras de contracción rápida también demuestran una mayor capacidad de transmisión electroquímica de potenciales de acción y un nivel rápido de liberación y absorción de calcio por el retículo sarcoplásmico. Las fibras de contracción rápida dependen de un sistema glucolítico anaeróbico , bien desarrollado y de corto plazo para la transferencia de energía y pueden contraerse y desarrollar tensión a una velocidad de 2 a 3 veces mayor que las fibras de contracción lenta. Los músculos de contracción rápida son mucho mejores para generar explosiones cortas de fuerza o velocidad que los músculos lentos, por lo que se fatigan más rápidamente. [36]
Las fibras de contracción lenta generan energía para la resíntesis de ATP mediante un sistema a largo plazo de transferencia de energía aeróbica . Estos incluyen principalmente las fibras ATPasa tipo I y MHC tipo I. Suelen tener un bajo nivel de actividad de ATPasa, una velocidad de contracción más lenta con una capacidad glucolítica menos desarrollada. [36] Las fibras que se vuelven de contracción lenta desarrollan una mayor cantidad de mitocondrias y capilares, lo que las hace mejores para el trabajo prolongado. [37]
Los músculos individuales tienden a ser una mezcla de varios tipos de fibras, pero sus proporciones varían según las acciones de ese músculo. Por ejemplo, en los seres humanos, los músculos cuádriceps contienen ~52% de fibras tipo I, mientras que el sóleo es ~80% de tipo I. [38] El músculo orbicular del ojo es solo ~15% de tipo I. [38] Unidades motoras dentro del músculo, sin embargo, tienen una variación mínima entre las fibras de esa unidad. Es este hecho el que hace viable el tamaño principal del reclutamiento de unidades motoras .
Tradicionalmente se ha pensado que el número total de fibras del músculo esquelético no cambia. Se cree que no existen diferencias de sexo o edad en la distribución de fibras; sin embargo, las proporciones de los tipos de fibras varían considerablemente de un músculo a otro y de una persona a otra. [ cita necesaria ] Entre las diferentes especies hay mucha variación en las proporciones de los tipos de fibras musculares. [39]
Los hombres y mujeres sedentarios (así como los niños pequeños) tienen un 45% de fibras de tipo II y un 55% de tipo I. [ cita necesaria ] Las personas que practican el extremo superior de cualquier deporte tienden a demostrar patrones de distribución de fibras, por ejemplo, los atletas de resistencia muestran un nivel más alto de fibras tipo I. Los atletas de velocidad, por otro lado, necesitan una gran cantidad de fibras de tipo IIX. Los atletas de eventos de media distancia muestran una distribución aproximadamente igual de los dos tipos. Este también suele ser el caso de los atletas de potencia, como los lanzadores y saltadores. Se ha sugerido que varios tipos de ejercicio pueden inducir cambios en las fibras de un músculo esquelético. [40]
Se cree que al realizar eventos de resistencia durante un período de tiempo sostenido, algunas de las fibras de tipo IIX se transforman en fibras de tipo IIA. Sin embargo, no hay consenso sobre el tema. [ cita necesaria ] Es muy posible que las fibras tipo IIX muestren mejoras en la capacidad oxidativa después del entrenamiento de resistencia de alta intensidad, lo que las lleva a un nivel en el que son capaces de realizar el metabolismo oxidativo con tanta eficacia como las fibras de contracción lenta de sujetos no entrenados. Esto se produciría por un aumento en el tamaño y número de mitocondrias y los cambios relacionados asociados, no por un cambio en el tipo de fibra.

Existen numerosos métodos empleados para la tipificación de fibras y la confusión entre los métodos es común entre los no expertos. Dos métodos comúnmente confundidos son la tinción histoquímica para la actividad de la miosina ATPasa y la tinción inmunohistoquímica para el tipo de cadena pesada de miosina (MHC). La actividad de la miosina ATPasa se denomina comúnmente (y correctamente) simplemente "tipo de fibra" y resulta del ensayo directo de la actividad de la ATPasa en diversas condiciones (p. ej., pH ). [34] La tinción de la cadena pesada de miosina se denomina con mayor precisión "tipo de fibra MHC", por ejemplo, "fibras MHC IIa", y resulta de la determinación de diferentes isoformas de MHC . [34] Estos métodos están estrechamente relacionados fisiológicamente, ya que el tipo MHC es el principal determinante de la actividad de la ATPasa. Sin embargo, ninguno de estos métodos de tipificación es de naturaleza directamente metabólica; no abordan directamente la capacidad oxidativa o glicolítica de la fibra.
Cuando se hace referencia genérica a las fibras "tipo I" o "tipo II", esto se refiere con mayor precisión a la suma de los tipos numéricos de fibras (I frente a II) según lo evaluado mediante la tinción de la actividad de miosina ATPasa (por ejemplo, las fibras "tipo II" se refieren al tipo IIA + tipo IIAX + tipo IIXA...etc.).
A continuación se muestra una tabla que muestra la relación entre estos dos métodos, limitada a los tipos de fibra que se encuentran en humanos. Las mayúsculas de subtipo se utilizan en la tipificación de fibras frente a la tipificación de MHC, y algunos tipos de ATPasa en realidad contienen múltiples tipos de MHC. Además, ningún subtipo B o b no se expresa en humanos mediante ninguno de los métodos . [41] Los primeros investigadores creían que los humanos expresaban un MHC IIb, lo que llevó a la clasificación ATPasa de IIB. Sin embargo, investigaciones posteriores demostraron que el MHC IIb humano era en realidad IIx, [41] lo que indica que el IIB se llama mejor IIX. IIb se expresa en otros mamíferos, por lo que todavía se ve con precisión (junto con IIB) en la literatura. Los tipos de fibras no humanas incluyen fibras verdaderas IIb, IIc, IId, etc.
Otros métodos de tipificación de fibras están menos formalmente delineados y existen en un espectro más amplio. Tienden a centrarse más en las capacidades metabólicas y funcionales (es decir, oxidativa frente a glucolítica , tiempo de contracción rápido frente a lento). Como se señaló anteriormente, la tipificación de fibras mediante ATPasa o MHC no mide ni dicta directamente estos parámetros. Sin embargo, muchos de los diversos métodos están vinculados mecánicamente, mientras que otros están correlacionados in vivo . [44] [45] Por ejemplo, el tipo de fibra ATPasa está relacionado con la velocidad de contracción, porque la alta actividad de ATPasa permite un ciclo de puentes cruzados más rápido . [34] Si bien la actividad ATPasa es sólo un componente de la velocidad de contracción, las fibras Tipo I son "lentas", en parte, porque tienen velocidades bajas de actividad ATPasa en comparación con las fibras Tipo II. Sin embargo, medir la velocidad de contracción no es lo mismo que tipificar la fibra ATPasa.
Casi todos los animales multicelulares dependen de los músculos para moverse. [46] Generalmente, los sistemas musculares de la mayoría de los animales multicelulares comprenden fibras musculares de contracción lenta y rápida, aunque las proporciones de cada tipo de fibra pueden variar entre organismos y entornos. La capacidad de cambiar las proporciones fenotípicas de sus tipos de fibras mediante el entrenamiento y la respuesta al medio ambiente ha sido útil para los organismos cuando se los coloca en entornos cambiantes, ya sea que requieren movimientos explosivos cortos (mayor proporción de contracción rápida) o movimientos de larga duración (mayor proporción de contracción lenta) para sobrevivir. [47] El culturismo ha demostrado que los cambios en la masa muscular y la producción de fuerza pueden cambiar en cuestión de meses. [48] A continuación se describen algunos ejemplos de esta variación. [49]
La langosta americana , Homarus americanus , tiene tres tipos de fibras que incluyen fibras de contracción rápida, fibras de contracción lenta y fibras de tónica lenta. [50] El tónico lento es una fibra de contracción lenta que puede sostener contracciones más largas ( tónico ). [51] [52] En las langostas, los músculos de diferentes partes del cuerpo varían en las proporciones del tipo de fibra muscular según el propósito del grupo de músculos. [50]
En el desarrollo temprano de los embriones de vertebrados, el crecimiento y la formación de músculo ocurre en sucesivas ondas o fases de miogénesis . El isotipo de la cadena pesada de miosina es un determinante importante del tipo de fibra específico. En los embriones de pez cebra , las primeras fibras musculares que se forman son las fibras de contracción lenta. Estas células migrarán desde su ubicación original para formar una monocapa de fibras musculares de contracción lenta. Estas fibras musculares se diferencian aún más a medida que el embrión madura. [53]
En animales más grandes, diferentes grupos de músculos requerirán cada vez más diferentes proporciones de tipos de fibras dentro del músculo para diferentes propósitos. Las tortugas , como Trachemys scripta elegans , tienen músculos complementarios dentro del cuello que muestran una posible tendencia inversa de los porcentajes de tipos de fibras (un músculo tiene un alto porcentaje de contracción rápida, mientras que el músculo complementario tendrá un mayor porcentaje de fibras de contracción lenta). Los músculos complementarios de las tortugas tenían porcentajes similares de tipos de fibras. [51]
Los músculos de los chimpancés están compuestos por un 67% de fibras de contracción rápida y tienen una fuerza dinámica máxima y una producción de potencia 1,35 veces mayor que los músculos humanos de tamaño similar. Entre los mamíferos, predominan las fibras de tipo II que utilizan el metabolismo glucolítico. Debido a la discrepancia en las fibras de contracción rápida en comparación con los humanos, los chimpancés superan a los humanos en pruebas relacionadas con la potencia. Los seres humanos, sin embargo, tendrán mejores resultados en el ejercicio en rango aeróbico que requiere grandes costos metabólicos, como caminar (bipedalismo). [54]
En todas las especies, se han conservado ciertas secuencias de genes, pero no siempre tienen el mismo propósito funcional. Dentro del embrión de pez cebra, el gen Prdm1 regula negativamente la formación de nuevas fibras de contracción lenta a través de mecanismos directos e indirectos como Sox6 (indirecto). En ratones, el gen Prdm1 está presente pero no controla los genes del músculo lento en ratones a través de Sox6 . [55]
Además de tener una base genética, la composición de los tipos de fibras musculares es flexible y puede variar según diferentes factores ambientales. Podría decirse que esta plasticidad puede ser la ventaja evolutiva más fuerte entre los organismos con músculo.
En el pescado, se expresan diferentes tipos de fibra a diferentes temperaturas del agua. [53] Las temperaturas frías requieren un metabolismo más eficiente dentro de los músculos y la resistencia a la fatiga es importante. Mientras que en ambientes más tropicales, los movimientos rápidos y poderosos (con proporciones más altas de contracción rápida) pueden resultar más beneficiosos a largo plazo. [56]
En roedores como las ratas, la naturaleza transitoria de su músculo es muy frecuente. Tienen un alto porcentaje de fibras musculares híbridas y tienen hasta un 60% de músculo de transformación rápida a lenta. [48]
Las influencias ambientales, como la dieta, el ejercicio y el estilo de vida, tienen un papel fundamental en las proporciones del tipo de fibra en los seres humanos. El ejercicio aeróbico cambiará las proporciones hacia fibras de contracción lenta, mientras que el levantamiento de pesas explosivo y las carreras de velocidad harán que las fibras pasen a fibras de contracción rápida. [47] En los animales, el "entrenamiento con ejercicio" se parecerá más a la necesidad de movimientos prolongados o movimientos explosivos cortos para escapar de los depredadores o atrapar presas. [57]


El músculo esquelético exhibe un patrón de bandas distintivo cuando se observa bajo el microscopio debido a la disposición de dos proteínas contráctiles , miosina y actina , que son dos de los miofilamentos de las miofibrillas . La miosina forma los filamentos gruesos y la actina forma los filamentos delgados, y están dispuestos en unidades repetitivas llamadas sarcómeros . La interacción de ambas proteínas da como resultado la contracción muscular.
El sarcómero está unido a otros orgánulos como las mitocondrias mediante filamentos intermedios en el citoesqueleto. La costamera une el sarcómero al sarcolema. [5]
Cada orgánulo y macromolécula de una fibra muscular está organizado para garantizar que cumpla las funciones deseadas. La membrana celular se llama sarcolema y el citoplasma se conoce como sarcoplasma . En el sarcoplasma se encuentran las miofibrillas. Las miofibrillas son largos haces de proteínas de aproximadamente un micrómetro de diámetro. Presionados contra el interior del sarcolema se encuentran los inusuales mionúcleos aplanados. Entre las miofibrillas se encuentran las mitocondrias .
Si bien la fibra muscular no tiene cisternas endoplasmáticas lisas, contiene retículo sarcoplásmico . El retículo sarcoplásmico rodea las miofibrillas y contiene una reserva de iones de calcio necesarios para provocar una contracción muscular. Periódicamente, presenta sacos terminales dilatados conocidos como cisternas terminales . Estos atraviesan la fibra muscular de un lado a otro. Entre dos cisternas terminales hay un pliegue tubular llamado túbulo transversal (túbulo T). Los túbulos T son las vías para que los potenciales de acción indiquen al retículo sarcoplásmico que libere calcio, provocando una contracción muscular. Juntos, dos cisternas terminales y un túbulo transversal forman una tríada . [58]

Todos los músculos derivan del mesodermo paraxial . Durante el desarrollo embrionario en el proceso de somitogénesis , el mesodermo paraxial se divide a lo largo del embrión para formar somitas , correspondientes a la segmentación del cuerpo que se observa más claramente en la columna vertebral . [59] Cada somita tiene tres divisiones, esclerotoma (que forma vértebras ), dermatoma (que forma piel) y miotoma (que forma músculo). El miotoma se divide en dos secciones, la epímera y la hipómera, que forman los músculos epaxial e hipaxial , respectivamente. Los únicos músculos epaxiales en los humanos son los erectores de la columna y los pequeños músculos vertebrales, y están inervados por las ramas dorsales de los nervios espinales . Todos los demás músculos, incluidos los de las extremidades, son hipaxiales y están inervados por las ramas ventrales de los nervios espinales. [59]
Durante el desarrollo, los mioblastos (células progenitoras de los músculos) permanecen en el somita para formar músculos asociados con la columna vertebral o migran hacia el cuerpo para formar todos los demás músculos. La migración de mioblastos está precedida por la formación de estructuras de tejido conectivo , generalmente formadas a partir del mesodermo de la placa lateral somática . Los mioblastos siguen señales químicas hasta los lugares apropiados, donde se fusionan en células musculares esqueléticas multinucleadas alargadas. [59]
Entre la décima y la decimoctava semana de gestación, todas las células musculares tienen cadenas pesadas rápidas de miosina; En el feto en desarrollo se distinguen dos tipos de miotubos : ambos expresan cadenas rápidas pero uno expresa cadenas rápidas y lentas. Entre el 10 y el 40 por ciento de las fibras expresan la cadena lenta de miosina. [60]
Los tipos de fibras se establecen durante el desarrollo embrionario y se remodelan más tarde en el adulto por influencias neuronales y hormonales. [39] La población de células satélite presentes debajo de la lámina basal es necesaria para el desarrollo posnatal de las células musculares. [61]
La función principal del músculo es la contracción . [3] Después de la contracción, el músculo esquelético funciona como un órgano endocrino al secretar miocinas , una amplia gama de citocinas y otros péptidos que actúan como moléculas de señalización. [62] A su vez, se cree que las miocinas median los beneficios del ejercicio para la salud . [63] Las miocinas se secretan en el torrente sanguíneo después de la contracción muscular. La interleucina 6 (IL-6) es la miocina más estudiada; otras miocinas inducidas por la contracción muscular incluyen BDNF , FGF21 y SPARC . [64]
El músculo también funciona para producir calor corporal. La contracción muscular es responsable de producir el 85% del calor corporal. [65] Este calor producido es un subproducto de la actividad muscular y en su mayor parte se desperdicia. Como respuesta homeostática al frío extremo, se indica a los músculos que activen contracciones de escalofríos para generar calor. [66]



La contracción se logra por la unidad estructural del músculo, la fibra muscular, y por su unidad funcional, la unidad motora . [4] Las fibras musculares son células excitables estimuladas por neuronas motoras . La unidad motora consta de una neurona motora y las numerosas fibras con las que entra en contacto. Un solo músculo es estimulado por muchas unidades motoras. Las fibras musculares están sujetas a la despolarización por el neurotransmisor acetilcolina , liberado por las neuronas motoras en las uniones neuromusculares . [67]
Además de los miofilamentos de actina y miosina en las miofibrillas que forman los sarcómeros contráctiles , existen otras dos proteínas reguladoras importantes: la troponina y la tropomiosina , que hacen posible la contracción muscular. Estas proteínas están asociadas con la actina y cooperan para prevenir su interacción con la miosina. Una vez que una célula está suficientemente estimulada, el retículo sarcoplásmico de la célula libera calcio iónico (Ca 2+ ), que luego interactúa con la proteína reguladora troponina. La troponina unida a calcio sufre un cambio conformacional que conduce al movimiento de la tropomiosina, exponiendo posteriormente los sitios de unión de miosina en la actina. Esto permite el ciclo de puentes cruzados dependiente de ATP de miosina y actina y el acortamiento del músculo.
El acoplamiento excitación-contracción es el proceso mediante el cual un potencial de acción muscular en la fibra muscular hace que las miofibrillas se contraigan. Este proceso se basa en un acoplamiento directo entre el canal de liberación de calcio del retículo sarcoplásmico RYR1 (receptor de rianodina 1) y los canales de calcio de tipo L dependientes de voltaje (identificados como receptores de dihidropiridina, DHPR). Los DHPR se encuentran en el sarcolema (que incluye el sarcolema superficial y los túbulos transversales ), mientras que los RyR residen a través de la membrana SR. La estrecha aposición de un túbulo transversal y dos regiones SR que contienen RyR se describe como una tríada y es predominantemente donde tiene lugar el acoplamiento excitación-contracción. El acoplamiento excitación-contracción ocurre cuando la despolarización de las células del músculo esquelético da como resultado un potencial de acción muscular, que se extiende a través de la superficie celular y dentro de la red de túbulos T de la fibra muscular , despolarizando así la porción interna de la fibra muscular. La despolarización de las porciones internas activa los receptores de dihidropiridina en las cisternas terminales, que están cerca de los receptores de rianodina en el retículo sarcoplásmico adyacente . Los receptores de dihidropiridina activados interactúan físicamente con los receptores de rianodina para activarlos a través de procesos en los pies (lo que implica cambios conformacionales que activan alostéricamente los receptores de rianodina). A medida que se abren los receptores de rianodina, Ca2+
se libera desde el retículo sarcoplásmico hacia el espacio de unión local y se difunde hacia el citoplasma en masa para provocar una chispa de calcio . El retículo sarcoplásmico tiene una gran capacidad amortiguadora de calcio, en parte debido a una proteína fijadora de calcio llamada calsecuestrina . La activación casi sincrónica de miles de chispas de calcio por el potencial de acción provoca un aumento de calcio en toda la célula, dando lugar al ascenso del transitorio de calcio. La CA2+
liberado en el citosol se une a la troponina C mediante los filamentos de actina , para permitir el ciclo de puentes cruzados, produciendo fuerza y, en algunas situaciones, movimiento. La calcio-ATPasa del retículo endoplásmico/sarco (SERCA) bombea activamente Ca2+
regresa al retículo sarcoplásmico. Como Ca2+
vuelve a los niveles de reposo, la fuerza disminuye y se produce la relajación. [68]
La rama eferente del sistema nervioso periférico es responsable de transmitir órdenes a los músculos y glándulas y, en última instancia, es responsable del movimiento voluntario. Los nervios mueven los músculos en respuesta a señales voluntarias y autónomas (involuntarias) del cerebro . Los músculos profundos, los músculos superficiales, los músculos de la cara y los músculos internos se corresponden con regiones dedicadas en la corteza motora primaria del cerebro , directamente anterior al surco central que divide los lóbulos frontal y parietal.
Además, los músculos reaccionan a estímulos nerviosos reflejos que no siempre envían señales hasta el cerebro. En este caso, la señal de la fibra aferente no llega al cerebro, sino que produce el movimiento reflejo mediante conexiones directas con los nervios eferentes de la columna . Sin embargo, la mayor parte de la actividad muscular es voluntaria y es el resultado de interacciones complejas entre varias áreas del cerebro.
Los nervios que controlan los músculos esqueléticos en los mamíferos se corresponden con grupos de neuronas a lo largo de la corteza motora primaria de la corteza cerebral del cerebro . Las órdenes se envían a través de los ganglios basales y se modifican mediante la entrada del cerebelo antes de transmitirse a través del tracto piramidal hasta la médula espinal y desde allí hasta la placa motora terminal de los músculos. En el camino, la retroalimentación, como la del sistema extrapiramidal, aporta señales para influir en el tono y la respuesta muscular .
Los músculos más profundos, como los que participan en la postura , a menudo están controlados desde núcleos en el tronco del encéfalo y los ganglios basales.
En los músculos esqueléticos, los husos musculares transmiten información sobre el grado de longitud del músculo y se estiran al sistema nervioso central para ayudar a mantener la postura y la posición de las articulaciones. La sensación de dónde están nuestros cuerpos en el espacio se llama propiocepción , la percepción de la conciencia corporal, la conciencia "inconsciente" de dónde se encuentran las distintas regiones del cuerpo en un momento dado. Varias áreas del cerebro coordinan el movimiento y la posición con la información de retroalimentación obtenida de la propiocepción. El cerebelo y el núcleo rojo , en particular, toman muestras continuamente de la posición frente al movimiento y realizan correcciones menores para asegurar un movimiento suave. [ cita necesaria ]

La actividad muscular representa gran parte del consumo de energía del cuerpo . Todas las células musculares producen moléculas de trifosfato de adenosina (ATP) que se utilizan para impulsar el movimiento de las cabezas de miosina . Los músculos tienen una reserva de energía a corto plazo en forma de fosfato de creatina que se genera a partir de ATP y pueden regenerar ATP cuando sea necesario con la creatina quinasa . Los músculos también mantienen una forma de almacenamiento de glucosa en forma de glucógeno . El glucógeno se puede convertir rápidamente en glucosa cuando se requiere energía para contracciones poderosas y sostenidas. Dentro de los músculos esqueléticos voluntarios, la molécula de glucosa se puede metabolizar anaeróbicamente en un proceso llamado glucólisis que produce dos moléculas de ATP y dos de ácido láctico en el proceso (en condiciones aeróbicas, no se forma lactato; en cambio, se forma piruvato y se transmite a través del ácido cítrico). ciclo ). Las células musculares también contienen glóbulos de grasa, que se utilizan como energía durante el ejercicio aeróbico . Los sistemas de energía aeróbicos tardan más en producir ATP y alcanzar la máxima eficiencia, y requieren muchos más pasos bioquímicos, pero producen significativamente más ATP que la glucólisis anaeróbica. El músculo cardíaco, por otro lado, puede consumir fácilmente cualquiera de los tres macronutrientes (proteínas, glucosa y grasas) de forma aeróbica sin un período de "calentamiento" y siempre extrae el máximo rendimiento de ATP de cualquier molécula involucrada. El corazón, el hígado y los glóbulos rojos también consumirán ácido láctico producido y excretado por los músculos esqueléticos durante el ejercicio.
El músculo esquelético utiliza más calorías que otros órganos. [69] En reposo consume 54,4 kJ/kg (13,0 kcal/kg) por día. Esto es mayor que el tejido adiposo (grasa), con 18,8 kJ/kg (4,5 kcal/kg), y el hueso, con 9,6 kJ/kg (2,3 kcal/kg). [70]
La eficiencia del músculo humano se ha medido (en el contexto del remo y el ciclismo ) entre un 18% y un 26%. La eficiencia se define como la relación entre la producción de trabajo mecánico y el costo metabólico total , como se puede calcular a partir del consumo de oxígeno. Esta baja eficiencia es el resultado de aproximadamente un 40% de eficiencia en la generación de ATP a partir de la energía de los alimentos , pérdidas en la conversión de energía del ATP en trabajo mecánico dentro del músculo y pérdidas mecánicas dentro del cuerpo. Las dos últimas pérdidas dependen del tipo de ejercicio y del tipo de fibras musculares que se utilizan (de contracción rápida o de contracción lenta). Para una eficiencia global del 20 por ciento, un vatio de potencia mecánica equivale a 4,3 kcal por hora. Por ejemplo, un fabricante de equipos de remo calibra su remo ergómetro para contar las calorías quemadas como equivalentes a cuatro veces el trabajo mecánico real, más 300 kcal por hora, lo que equivale aproximadamente a un 20 por ciento de eficiencia con 250 vatios de potencia mecánica. La producción de energía mecánica de una contracción cíclica puede depender de muchos factores, incluido el momento de activación, la trayectoria de la tensión muscular y las tasas de aumento y disminución de la fuerza. Estos pueden sintetizarse experimentalmente mediante el análisis de bucles de trabajo .
La fuerza muscular es el resultado de tres factores superpuestos: fuerza fisiológica (tamaño del músculo, área de sección transversal, puentes transversales disponibles, respuestas al entrenamiento), fuerza neurológica (qué tan fuerte o débil es la señal que le indica al músculo que se contraiga) y fuerza mecánica ( ángulo de fuerza del músculo sobre la palanca, longitud del brazo de momento, capacidades articulares). [ cita necesaria ]
El músculo de los vertebrados normalmente produce aproximadamente 25 a 33 N (5,6 a 7,4 lb f ) de fuerza por centímetro cuadrado de área de sección transversal del músculo cuando es isométrico y tiene una longitud óptima. [71] Algunos músculos de invertebrados , como los de las garras de cangrejo, tienen sarcómeros mucho más largos que los de los vertebrados, lo que da como resultado muchos más sitios para que se unan la actina y la miosina y, por lo tanto, una fuerza mucho mayor por centímetro cuadrado a costa de una velocidad mucho más lenta. La fuerza generada por una contracción se puede medir de forma no invasiva mediante mecanomiografía o fonomiografía , medirse in vivo utilizando la tensión del tendón (si hay un tendón prominente) o medirse directamente utilizando métodos más invasivos.
La fuerza de cualquier músculo determinado, en términos de fuerza ejercida sobre el esqueleto, depende de la longitud, la velocidad de acortamiento , el área de la sección transversal, la pennación , la longitud del sarcómero , las isoformas de miosina y la activación neural de las unidades motoras . Reducciones significativas en la fuerza muscular pueden indicar una patología subyacente; el cuadro de la derecha se utiliza como guía.
El tiempo máximo de retención de un músculo contraído depende de su suministro de energía y, según la ley de Rohmert, decae exponencialmente desde el comienzo del esfuerzo.
Dado que tres factores afectan la fuerza muscular simultáneamente y los músculos nunca trabajan individualmente, es engañoso comparar la fuerza en músculos individuales y afirmar que uno es el "más fuerte". Pero a continuación se muestran varios músculos cuya fuerza es destacable por diferentes motivos.
La fuerza muscular es proporcional al área de sección transversal fisiológica (PCSA) y la velocidad muscular es proporcional a la longitud de las fibras musculares. [72] Sin embargo, el torque alrededor de una articulación está determinado por una serie de parámetros biomecánicos, incluida la distancia entre las inserciones musculares y los puntos de pivote, el tamaño del músculo y la relación de transmisión arquitectónica . Los músculos normalmente están dispuestos en oposición de modo que cuando un grupo de músculos se contrae, otro grupo se relaja o se alarga. [73] El antagonismo en la transmisión de impulsos nerviosos a los músculos significa que es imposible estimular completamente la contracción de dos músculos antagonistas al mismo tiempo. Durante los movimientos balísticos como el lanzamiento, los músculos antagonistas actúan para "frenar" los músculos agonistas durante toda la contracción, especialmente al final del movimiento. En el ejemplo del lanzamiento, el pecho y la parte delantera del hombro (deltoides anterior) se contraen para tirar del brazo hacia adelante, mientras que los músculos de la parte posterior y posterior del hombro (deltoides posterior) también se contraen y sufren una contracción excéntrica para ralentizar el movimiento. para evitar lesiones. Parte del proceso de entrenamiento es aprender a relajar los músculos antagonistas para aumentar la entrada de fuerza en el pecho y la parte anterior del hombro.
Los músculos que se contraen producen vibraciones y sonidos. [74] Las fibras de contracción lenta producen de 10 a 30 contracciones por segundo (10 a 30 Hz). Las fibras de contracción rápida producen de 30 a 70 contracciones por segundo (30 a 70 Hz). [75] La vibración se puede presenciar y sentir tensando mucho los músculos, como cuando se cierra el puño con firmeza. El sonido se puede escuchar presionando un músculo muy tenso contra la oreja; nuevamente, un puño firme es un buen ejemplo. El sonido suele describirse como un ruido sordo. Algunas personas pueden producir voluntariamente este sonido retumbante contrayendo el músculo tensor del tímpano del oído medio. El ruido sordo también se puede escuchar cuando los músculos del cuello o de la mandíbula están muy tensos. [ cita necesaria ]
El fenotipo del tipo de fibra del músculo esquelético en animales adultos está regulado por varias vías de señalización independientes. Estas incluyen vías involucradas con la vía Ras /proteína quinasa activada por mitógenos ( MAPK ), calcineurina, proteína quinasa IV dependiente de calcio/calmodulina y el coactivador γ del proliferador de peroxisomas 1 (PGC-1). La vía de señalización Ras/MAPK vincula las neuronas motoras y los sistemas de señalización, acoplando la excitación y la regulación de la transcripción para promover la inducción dependiente de los nervios del programa lento en el músculo en regeneración. La calcineurina , una fosfatasa activada por Ca 2+ / calmodulina implicada en la especificación del tipo de fibra dependiente de la actividad nerviosa en el músculo esquelético, controla directamente el estado de fosforilación del factor de transcripción NFAT , permitiendo su translocación al núcleo y conduciendo a la activación de procesos lentos. -proteínas musculares de tipo en cooperación con proteínas del factor potenciador de miocitos 2 ( MEF2 ) y otras proteínas reguladoras. La actividad de la proteína quinasa dependiente de Ca2+/calmodulina también está regulada positivamente por la actividad lenta de las neuronas motoras, posiblemente porque amplifica las respuestas de tipo lento generadas por la calcineurina al promover las funciones transactivadoras de MEF2 y mejorar la capacidad oxidativa a través de la estimulación de la biogénesis mitocondrial .
Los cambios inducidos por la contracción en el calcio intracelular o en las especies reactivas de oxígeno proporcionan señales a diversas vías que incluyen las MAPK, la calcineurina y la proteína quinasa IV dependiente de calcio/calmodulina para activar factores de transcripción que regulan la expresión génica y la actividad enzimática en el músculo esquelético.

PGC1-α ( PPARGC1A ), un coactivador transcripcional de receptores nucleares importantes para la regulación de varios genes mitocondriales implicados en el metabolismo oxidativo, interactúa directamente con MEF2 para activar sinérgicamente genes musculares selectivos de contracción lenta (ST) y también sirve como objetivo para señalización de calcineurina. Una vía transcripcional mediada por el receptor δ activado por proliferador de peroxisomas ( PPARδ ) está implicada en la regulación del fenotipo de la fibra del músculo esquelético. Los ratones que albergan una forma activada de PPARδ muestran un fenotipo de "resistencia", con un aumento coordinado de las enzimas oxidativas y la biogénesis mitocondrial y una mayor proporción de fibras ST. Así, a través de la genómica funcional, la calcineurina, la quinasa dependiente de calmodulina, la PGC-1α y el PPARδ activado forman la base de una red de señalización que controla la transformación del tipo de fibra del músculo esquelético y los perfiles metabólicos que protegen contra la resistencia a la insulina y la obesidad.
La transición del metabolismo aeróbico al anaeróbico durante el trabajo intenso requiere que varios sistemas se activen rápidamente para asegurar un suministro constante de ATP para los músculos que trabajan. Estos incluyen un cambio de combustibles basados en grasas a combustibles basados en carbohidratos, una redistribución del flujo sanguíneo de los músculos que no trabajan a los que se ejercitan y la eliminación de varios de los subproductos del metabolismo anaeróbico, como el dióxido de carbono y el ácido láctico. Algunas de estas respuestas se rigen por el control transcripcional del fenotipo glucolítico de contracción rápida (FT). Por ejemplo, la reprogramación del músculo esquelético desde un fenotipo glucolítico ST a un fenotipo glucolítico FT implica el complejo Six1/Eya1, compuesto por miembros de la familia de proteínas Six. Además, el factor 1-α inducible por hipoxia ( HIF1A ) ha sido identificado como un regulador maestro de la expresión de genes implicados en respuestas hipóxicas esenciales que mantienen los niveles de ATP en las células. La ablación de HIF-1α en el músculo esquelético se asoció con un aumento en la actividad de las enzimas limitantes de la velocidad de las mitocondrias, lo que indica que el ciclo del ácido cítrico y el aumento de la oxidación de los ácidos grasos pueden estar compensando la disminución del flujo a través de la vía glucolítica en estos animales. Sin embargo, las respuestas de HIF-1α mediadas por hipoxia también están relacionadas con la regulación de la disfunción mitocondrial mediante la formación de especies reactivas de oxígeno excesivas en las mitocondrias.
Otras vías también influyen en el carácter de los músculos adultos. Por ejemplo, la fuerza física dentro de una fibra muscular puede liberar el factor de transcripción de respuesta sérica de la proteína estructural titina, lo que provoca una alteración del crecimiento muscular.

El ejercicio físico a menudo se recomienda como medio para mejorar las habilidades motoras , la condición física , la fuerza de los músculos y huesos y la función de las articulaciones. El ejercicio tiene varios efectos sobre los músculos, el tejido conectivo , los huesos y los nervios que estimulan los músculos. Uno de esos efectos es la hipertrofia muscular , un aumento del tamaño del músculo debido a un aumento del número de fibras musculares o del área transversal de las miofibrillas. [76] Los cambios musculares dependen del tipo de ejercicio utilizado.
Generalmente, existen dos tipos de regímenes de ejercicio, aeróbico y anaeróbico. El ejercicio aeróbico (por ejemplo, maratones) implica actividades de baja intensidad pero de larga duración, durante las cuales los músculos utilizados están por debajo de su fuerza de contracción máxima. Las actividades aeróbicas dependen de la respiración aeróbica (es decir, el ciclo del ácido cítrico y la cadena de transporte de electrones) para obtener energía metabólica mediante el consumo de grasas, proteínas, carbohidratos y oxígeno. Los músculos involucrados en ejercicios aeróbicos contienen un mayor porcentaje de fibras musculares de tipo I (o de contracción lenta), que contienen principalmente enzimas mitocondriales y de oxidación asociadas con la respiración aeróbica. [77] [78] Por el contrario, el ejercicio anaeróbico se asocia con actividades de alta intensidad pero de corta duración, como carreras de velocidad o levantamiento de pesas . Las actividades anaeróbicas utilizan predominantemente fibras musculares de tipo II, de contracción rápida. [79] Las fibras musculares tipo II dependen de la glucogénesis para obtener energía durante el ejercicio anaeróbico. [80] Durante el ejercicio anaeróbico, las fibras tipo II consumen poco oxígeno, proteínas y grasas, producen grandes cantidades de ácido láctico y son fatigables. Muchos ejercicios son parcialmente aeróbicos y anaeróbicos; por ejemplo, fútbol y escalada en roca .
La presencia de ácido láctico tiene un efecto inhibidor sobre la generación de ATP dentro del músculo. Incluso puede detener la producción de ATP si la concentración intracelular aumenta demasiado. Sin embargo, el entrenamiento de resistencia mitiga la acumulación de ácido láctico mediante una mayor capilarización y mioglobina. [81] Esto aumenta la capacidad de eliminar productos de desecho, como el ácido láctico, de los músculos para no afectar la función muscular. Una vez que sale de los músculos, el ácido láctico puede ser utilizado por otros músculos o tejidos corporales como fuente de energía, o transportado al hígado, donde se convierte nuevamente en piruvato . Además de aumentar el nivel de ácido láctico, el ejercicio extenuante provoca la pérdida de iones de potasio en el músculo. Esto puede facilitar la recuperación de la función muscular protegiendo contra la fatiga. [82]
El dolor muscular de aparición tardía es un dolor o malestar que se puede sentir de uno a tres días después de hacer ejercicio y generalmente desaparece dos o tres días después. Alguna vez se pensó que era causado por la acumulación de ácido láctico, pero una teoría más reciente es que es causado por pequeños desgarros en las fibras musculares causados por una contracción excéntrica o niveles de entrenamiento no acostumbrados. Dado que el ácido láctico se dispersa con bastante rapidez, no podría explicar el dolor experimentado días después del ejercicio. [83]
Las enfermedades del músculo esquelético se denominan miopatías , mientras que las enfermedades de los nervios se denominan neuropatías . Ambos pueden afectar la función muscular o causar dolor muscular y caer bajo el paraguas de enfermedad neuromuscular . La causa de muchas miopatías se atribuye a mutaciones en las distintas proteínas musculares asociadas. [5] [84] Algunas miopatías inflamatorias incluyen polimiositis y miositis por cuerpos de inclusión.

Las enfermedades neuromusculares afectan los músculos y su control nervioso. En general, los problemas con el control nervioso pueden provocar espasticidad o parálisis , según la ubicación y la naturaleza del problema. Varios trastornos del movimiento son causados por trastornos neurológicos como la enfermedad de Parkinson y la enfermedad de Huntington, donde existe una disfunción del sistema nervioso central. [85]
Los síntomas de las enfermedades musculares pueden incluir debilidad , espasticidad, mioclono y mialgia . Los procedimientos de diagnóstico que pueden revelar trastornos musculares incluyen pruebas de los niveles de creatina quinasa en la sangre y electromiografía (que mide la actividad eléctrica en los músculos). En algunos casos, se puede realizar una biopsia muscular para identificar una miopatía , así como pruebas genéticas para identificar anomalías del ADN asociadas con miopatías y distrofias específicas .
Se está experimentando con una técnica de elastografía no invasiva que mide el ruido muscular para proporcionar una forma de monitorear la enfermedad neuromuscular. El sonido producido por un músculo proviene del acortamiento de los filamentos de actomiosina a lo largo del eje del músculo. Durante la contracción , el músculo se acorta a lo largo y se expande a lo ancho, produciendo vibraciones en la superficie. [86]
Independientemente de las medidas de fuerza y rendimiento, se puede inducir a los músculos a crecer mediante una serie de factores, incluida la señalización hormonal, factores de desarrollo, entrenamiento de fuerza y enfermedades. Contrariamente a la creencia popular, el número de fibras musculares no se puede aumentar mediante el ejercicio . En cambio, los músculos crecen a través de una combinación de crecimiento de células musculares a medida que se agregan nuevos filamentos de proteínas junto con masa adicional proporcionada por células satélite indiferenciadas junto con las células musculares existentes. [87]
Los factores biológicos como la edad y los niveles hormonales pueden afectar la hipertrofia muscular. Durante la pubertad en los hombres, la hipertrofia se produce a un ritmo acelerado a medida que aumentan los niveles de hormonas estimulantes del crecimiento producidas por el cuerpo. La hipertrofia natural normalmente se detiene en el crecimiento completo al final de la adolescencia. Como la testosterona es una de las principales hormonas de crecimiento del cuerpo, en promedio, a los hombres les resulta mucho más fácil lograr la hipertrofia que a las mujeres. Tomar testosterona adicional u otros esteroides anabólicos aumentará la hipertrofia muscular.
Todos los factores musculares, espinales y neurales afectan la construcción muscular. A veces, una persona puede notar un aumento en la fuerza de un músculo determinado, aunque solo se haya ejercitado su opuesto, como cuando un culturista encuentra que su bíceps izquierdo es más fuerte después de completar un régimen centrado solo en el bíceps derecho. Este fenómeno se llama educación cruzada . [ cita necesaria ]

Cada día, entre el uno y el dos por ciento del músculo se descompone y se reconstruye. La inactividad , la desnutrición , las enfermedades y el envejecimiento pueden aumentar la degradación y provocar atrofia muscular o sarcopenia . La sarcopenia es comúnmente un proceso relacionado con la edad que puede provocar fragilidad y sus consecuencias. [88] Una disminución de la masa muscular puede ir acompañada de un menor número y tamaño de células musculares, así como de un menor contenido de proteínas. [89]
Se sabe que los vuelos espaciales tripulados , que implican períodos prolongados de inmovilización e ingravidez, provocan debilitamiento y atrofia muscular, lo que provoca una pérdida de hasta el 30% de la masa en algunos músculos. [90] [91] Estas consecuencias también se observan en algunos mamíferos después de la hibernación . [92]
Muchas enfermedades y afecciones, incluidos el cáncer , el SIDA y la insuficiencia cardíaca, pueden provocar una pérdida muscular conocida como caquexia . [93]
Las miopatías se han modelado con sistemas de cultivo celular de músculo a partir de biopsias de tejido sano o enfermo . Otra fuente de músculo esquelético y progenitores la proporciona la diferenciación dirigida de células madre pluripotentes . [94]
La investigación sobre las propiedades del músculo esquelético utiliza muchas técnicas. La estimulación muscular eléctrica se utiliza para determinar la fuerza y la velocidad de contracción en diferentes frecuencias relacionadas con la composición y la mezcla del tipo de fibra dentro de un grupo de músculos individual. Las pruebas musculares in vitro se utilizan para una caracterización más completa de las propiedades musculares.
La actividad eléctrica asociada con la contracción muscular se mide mediante electromiografía (EMG). El músculo esquelético tiene dos respuestas fisiológicas: relajación y contracción. Los mecanismos por los cuales ocurren estas respuestas generan actividad eléctrica medida por EMG. Específicamente, la EMG puede medir el potencial de acción de un músculo esquelético, que se produce por la hiperpolarización de los axones motores a partir de los impulsos nerviosos enviados al músculo. La EMG se utiliza en investigaciones para determinar si el músculo esquelético de interés se está activando, la cantidad de fuerza generada y un indicador de fatiga muscular . [95] Los dos tipos de EMG son la EMG intramuscular y la EMG de superficie, la más común. Las señales EMG son mucho mayores cuando un músculo esquelético se contrae en lugar de relajarse. Sin embargo, para los músculos esqueléticos más pequeños y profundos, las señales EMG se reducen y, por lo tanto, se consideran una técnica menos valorada para medir la activación. [96] En la investigación que utiliza EMG, comúnmente se realiza una contracción voluntaria máxima (MVC) en el músculo esquelético de interés, para tener datos de referencia para el resto de las grabaciones de EMG durante las principales pruebas experimentales para ese mismo músculo esquelético. [97]
La investigación sobre el desarrollo de músculos artificiales incluye el uso de polímeros electroactivos .

Los núcleos presentes en el músculo esquelético son aproximadamente un 50% de núcleos de miocitos y un 50% de núcleos de células mononucleares. [13] Las células mononucleares que se encuentran en muestras de tejido del músculo esquelético de ratones y humanos [15] [99] [98] pueden identificarse mediante la transcripción del ARN mensajero de marcadores de tipo celular. Cameron y cols. [98] identificaron nueve tipos de células. Incluyen células endoteliales que recubren los capilares (45% de las células), progenitores fibroadipogénicos (FAP) (20%), [100] pericitos (14%) y pericitos de tipo endotelial (4%). Otro 9% de las células mononucleares son células madre musculares , adyacentes a las células de fibras musculares. Los tipos de células linfoides (como las células B y las células T) (3%) y las células mieloides como los macrófagos (2%) constituyeron la mayoría de las células mononucleares restantes del músculo esquelético. [98] Además, Cameron et al. [98] también identificaron dos tipos de células miocíticas, tipo I y tipo II. Se descubrió que cada uno de los diferentes tipos de células del músculo esquelético expresa diferentes conjuntos de genes. La mediana del número de genes expresados en cada uno de los nueve tipos de células diferentes fue de 1.331 genes. Sin embargo, cuando se toma una biopsia del músculo del muslo, la biopsia contiene todos los diferentes tipos de células. Mezclados, en una biopsia del músculo esquelético del muslo humano, hay entre 13.026 y 13.108 genes con expresión detectada. [101] [102]
Como se señaló en la introducción de este artículo, en diferentes condiciones fisiológicas, en el secretoma de los músculos esqueléticos se producen subconjuntos de 654 proteínas diferentes, así como lípidos, aminoácidos, metabolitos y pequeños ARN . [12] Como se describe en el artículo de Wikipedia " Lista de órganos y acciones endocrinos humanos ", el músculo esquelético se identifica como un órgano endocrino debido a su secreción de citoquinas y otros péptidos producidos por el músculo esquelético como moléculas de señalización. Iizuka et al., [9] indicaron que el músculo esquelético es un órgano endocrino porque "sintetiza y secreta múltiples factores, y estos factores derivados del músculo ejercen efectos beneficiosos sobre órganos periféricos y remotos". Los secretomas alterados después del entrenamiento de resistencia o de resistencia , así como el secretoma del músculo sedentario, parecen tener muchos efectos sobre los tejidos distantes.
Un estudio realizado en Canadá probó el efecto de la masa muscular sobre las funciones mentales durante el envejecimiento. Una expectativa del estudio era que los componentes endocrinos del secretoma específicos del músculo esquelético pudieran proteger las funciones cognitivas. Se midió la masa muscular esquelética de brazos y piernas de 8.279 canadienses mayores de 65 años y con un estado de salud promedio al inicio del estudio y después de tres años. [103] De estos individuos, se consideró que 1.605 participantes (19,4%) tenían una masa de músculo esquelético baja al inicio del estudio, con menos de 7,30 kg/m 2 para los hombres y menos de 5,42 kg/m 2 para las mujeres (niveles definidos como sarcopenia en Canadá).
La función mental ejecutiva , la memoria y la velocidad psicomotora se midieron al inicio y después de tres años. La función mental ejecutiva se midió con pruebas estándar, incluida la capacidad de decir la secuencia 1-A, 2-B, 3-C…, de nombrar varios animales en un minuto, y con el test de Stroop . [103] El estudio encontró que aquellos individuos con menor masa de músculo esquelético al inicio del estudio disminuyeron en su función mental ejecutiva considerablemente más marcadamente que aquellos con mayor masa muscular. La memoria, así como la velocidad psicomotora, por otro lado, no se correlacionaron con la masa del músculo esquelético. [103] Por lo tanto, una masa muscular más grande, con un secretoma concomitantemente más grande, parecía tener la función endocrina de proteger la función mental ejecutiva de individuos mayores de 65 años.
Paluch et al. [104] compararon el número promedio de pasos caminados por día con el riesgo de mortalidad , tanto para adultos mayores de 60 años como para adultos menores de 60 años. El estudio fue un metanálisis de 15 estudios que, combinados, evaluaron a 47.471 adultos durante un período de 7 años. Los individuos se dividieron en cuartiles aproximadamente iguales. El cuartil más bajo promedió 3.553 pasos/día, el segundo cuartil 5.801 pasos/día, el tercer cuartil 7.842 pasos/día y el cuarto cuartil 10.901 pasos/día. La rapidez de la caminata, ajustada al volumen de la caminata, no afectó la mortalidad. Sin embargo, el número de pasos/día estaba claramente relacionado con la mortalidad. Cuando el riesgo de mortalidad para los mayores de 60 años se fijó en 1,0 para el cuartil más bajo de pasos/día, el riesgo relativo de mortalidad para el segundo, tercer y cuarto cuartil fue de 0,56, 0,45 y 0,35, respectivamente. Para los menores de 60 años, los resultados fueron menos pronunciados. Para los menores de 60 años, con el riesgo de mortalidad del primer cuartil fijado en 1,0, los riesgos relativos de mortalidad del segundo, tercer y cuarto cuartil fueron de 0,57, 0,42 y 0,53, respectivamente. Por tanto, el uso de los músculos esqueléticos al caminar tiene un gran efecto, especialmente entre las personas mayores, sobre la mortalidad.
Williams y cols. [102] obtuvieron biopsias de un músculo esquelético del muslo (músculo vasto lateral) de ocho varones caucásicos de 23 años, originalmente sedentarios. Se tomaron biopsias antes y después de un programa de entrenamiento de ejercicios de resistencia de seis semanas de duración. El ejercicio consistió en andar en bicicleta estática durante una hora, cinco días a la semana durante seis semanas.
De los 13.108 genes con expresión detectada en las biopsias musculares, 641 genes estaban regulados positivamente después del entrenamiento de resistencia y 176 genes estaban regulados negativamente. Del total de 817 genes alterados, 531 fueron identificados como en el secretoma por Uniprot o Exocarta o por estudios que investigaron el secretoma de las células musculares. Debido a que muchos de los genes regulados por el ejercicio se identifican como secretados, esto indica que gran parte del efecto del ejercicio tiene una función endocrina más que metabólica. [102] Las principales vías que se encontraron afectadas por las proteínas secretadas reguladas por el ejercicio estaban relacionadas con las funciones cardíaca , cognitiva , renal y plaquetaria .
Entre 2012 y 2019, al menos 25 informes indicaron un papel importante de los mecanismos epigenéticos en las respuestas del músculo esquelético al ejercicio. [105] Las alteraciones epigenéticas a menudo ocurren al agregar grupos metilo a las citosinas en el ADN o al eliminar grupos metilo de las citosinas del ADN , especialmente en los sitios CpG . Las metilaciones de citosinas pueden hacer que el ADN se compacte en heterocromatina , inhibiendo así el acceso de otras moléculas al ADN. [106] Las alteraciones epigenéticas también ocurren a menudo a través de acetilaciones o desacetilaciones de las colas de histonas dentro de la cromatina . El ADN en el núcleo generalmente consta de segmentos de 146 pares de bases de ADN envueltos alrededor de ocho histonas estrechamente conectadas (y cada histona también tiene una cola suelta) en una estructura llamada nucleosoma y un segmento de ADN está conectado a un segmento de ADN adyacente en una nucleosoma por ADN conector . Cuando las colas de histonas se acetilan , generalmente provocan un aflojamiento del ADN alrededor del nucleosoma, lo que aumenta la accesibilidad del ADN.

La expresión génica en el músculo está regulada en gran medida, como en los tejidos en general, por secuencias reguladoras de ADN , especialmente potenciadoras . Los potenciadores son secuencias no codificantes en el genoma que activan la expresión de genes diana distantes, [107] al recorrer e interactuar con los promotores de sus genes diana [108] (consulte la Figura "Regulación de la transcripción en mamíferos"). Según lo informado por Williams et al., [102] la distancia promedio en el bucle entre los potenciadores y promotores de genes conectados es de 239.000 bases de nucleótidos.
El entrenamiento muscular de resistencia altera la expresión de genes musculares mediante la metilación epigenética del ADN o la desmetilación de los sitios CpG dentro de los potenciadores. [109]
En un estudio realizado por Lindholm et al., [109] veintitrés individuos de aproximadamente 27 años y sedentarios se ofrecieron como voluntarios para realizar un entrenamiento de resistencia con una sola pierna durante 3 meses. La otra pierna se utilizó como pierna de control no entrenada. El entrenamiento consistió en extensión de rodilla con una sola pierna durante 3 meses (45 min, 4 sesiones por semana). Se tomaron biopsias del músculo esquelético del vasto lateral (un músculo del muslo) antes de que comenzara el entrenamiento y 24 horas después de la última sesión de entrenamiento de cada una de las piernas. La pierna entrenada en resistencia, en comparación con la pierna no entrenada, tuvo cambios significativos en la metilación del ADN en 4.919 sitios en todo el genoma. Los sitios de metilación del ADN alterados se encontraban predominantemente en potenciadores . El análisis transcripcional, mediante secuenciación de ARN , identificó 4.076 genes expresados diferencialmente.
Los genes transcripcionalmente regulados positivamente se asociaron con potenciadores que tenían una disminución significativa en la metilación del ADN , mientras que los genes transcripcionalmente regulados negativamente se asociaron con potenciadores que tenían una mayor metilación del ADN. El aumento de la metilación se asoció principalmente con genes implicados en la remodelación estructural del músculo y el metabolismo de la glucosa. Los potenciadores con disminución de la metilación se asociaron con genes que funcionan en procesos inflamatorios o inmunológicos y en la regulación transcripcional.

Como se indicó anteriormente, después del ejercicio, las alteraciones epigenéticas de los potenciadores alteran la expresión a largo plazo de cientos de genes musculares. [102] Esto incluye genes que producen proteínas secretadas a la circulación sistémica, muchas de las cuales pueden actuar como mensajeros endocrinos. [102] Seis hombres caucásicos sedentarios, de aproximadamente 23 años, realizaron biopsias del vasto lateral (un músculo del muslo) antes de ingresar a un programa de ejercicio (seis semanas de sesiones de 60 minutos de andar en bicicleta estacionaria, cinco días por semana). Cuatro días después de completar este programa de ejercicios, la expresión de muchos genes fue alterada epigenéticamente de manera persistente . Las alteraciones alteraron las acetilaciones y desacetilaciones de las colas de histonas ubicadas en los potenciadores que controlan los genes con expresión alterada. [102]
Los genes regulados positivamente se asociaron con acetilaciones epigenéticas agregadas en la histona 3 lisina 27 (H3K27ac) de los nucleosomas ubicados en sus potenciadores . Los genes regulados negativamente se asociaron con la eliminación de acetilaciones epigenéticas en H3K27 en nucleosomas ubicados en sus potenciadores (ver Figura "Un nucleosoma con colas de histonas preparadas para la activación transcripcional"). Las biopsias del músculo vasto lateral mostraron la expresión de 13.108 genes al inicio del programa de entrenamiento. Cuatro días después de completar el programa de ejercicio, las biopsias de los mismos músculos mostraron una expresión genética alterada, con 641 genes regulados positivamente y 176 genes regulados negativamente. [102] Williams y otros. identificaron 599 interacciones gen potenciador, que cubren 491 potenciadores y 268 genes (se encontraron múltiples potenciadores conectados a algunos genes), donde tanto el potenciador como el gen diana conectado estaban coordinadamente regulados hacia arriba o hacia abajo después del entrenamiento físico. [102]
{{cite web}}: CS1 maint: multiple names: authors list (link)