El ácido butírico ( / ˈbj uːt ɪr ɪk / ; del griego antiguo : βούτῡρον , que significa "mantequilla"), también conocido bajo el nombre sistemático de ácido butanoico , es un ácido alquilcarboxílico de cadena lineal con la fórmula química CH 3 CH 2 CH 2 CO 2 H . Es un líquido aceitoso, incoloro y con un olor desagradable . El ácido isobutírico (ácido 2-metilpropanoico) es un isómero . Las sales y ésteres del ácido butírico se conocen como butiratos o butanoatos . El ácido no se encuentra ampliamente en la naturaleza, pero sus ésteres están muy extendidos. Es una sustancia química industrial común [7] y un componente importante en el intestino de los mamíferos.
El ácido butírico fue observado por primera vez en una forma impura en 1814 por el químico francés Michel Eugène Chevreul . En 1818, lo había purificado lo suficiente como para caracterizarlo. Sin embargo, Chevreul no publicó sus primeras investigaciones sobre el ácido butírico; en cambio, depositó sus hallazgos en forma de manuscrito con el secretario de la Academia de Ciencias en París, Francia. Henri Braconnot , un químico francés, también estaba investigando la composición de la mantequilla y estaba publicando sus hallazgos y esto dio lugar a disputas sobre la prioridad. Ya en 1815, Chevreul afirmó que había encontrado la sustancia responsable del olor de la mantequilla. [8] En 1817, publicó algunos de sus hallazgos sobre las propiedades del ácido butírico y lo nombró. [9] Sin embargo, no fue hasta 1823 que presentó las propiedades del ácido butírico en detalle. [10] El nombre ácido butírico proviene de βούτῡρον , que significa "mantequilla", la sustancia en la que se encontró por primera vez. El nombre latino butyrum (o buturum ) es similar.
Los triglicéridos del ácido butírico componen el 3-4% de la mantequilla . Cuando la mantequilla se vuelve rancia, el ácido butírico se libera del glicérido por hidrólisis . [11] Es uno del subgrupo de ácidos grasos llamados ácidos grasos de cadena corta . El ácido butírico es un ácido carboxílico típico que reacciona con bases y afecta a muchos metales. [12] Se encuentra en la grasa animal y los aceites vegetales , la leche bovina , la leche materna , la mantequilla , el queso parmesano , el olor corporal , el vómito y como producto de la fermentación anaeróbica (incluso en el colon ). [13] [14] Tiene un sabor parecido a la mantequilla y un olor desagradable . Los mamíferos con buenas habilidades de detección de olores, como los perros , pueden detectarlo en 10 partes por mil millones , mientras que los humanos pueden detectarlo solo en concentraciones superiores a 10 partes por millón . En la fabricación de alimentos , se utiliza como agente aromatizante . [15]
En los seres humanos, el ácido butírico es uno de los dos agonistas endógenos primarios del receptor 2 del ácido hidroxicarboxílico humano ( HCA 2 ), un receptor acoplado a la proteína G acoplado a G i/o . [16] [17]
El ácido butírico está presente en forma de éster octílico en la chirivía ( Pastinaca sativa ) [18] y en la semilla del árbol de ginkgo . [19]
En la industria, el ácido butírico se produce por hidroformilación a partir de propeno y gas de síntesis , formando butiraldehído , que se oxida hasta el producto final. [7]
Se puede separar de soluciones acuosas por saturación con sales como el cloruro de calcio . La sal de calcio, Ca(C 4 H 7 O 2 ) 2 · H 2 O , es menos soluble en agua caliente que en fría.
El butirato se produce mediante varios procesos de fermentación realizados por bacterias anaeróbicas obligadas . [20] Esta vía de fermentación fue descubierta por Louis Pasteur en 1861. Ejemplos de especies de bacterias productoras de butirato :
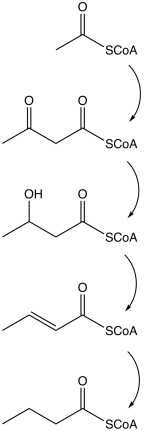
La vía comienza con la escisión glucolítica de la glucosa en dos moléculas de piruvato , como sucede en la mayoría de los organismos. El piruvato se oxida a acetil coenzima A catalizada por la piruvato:ferredoxina oxidorreductasa . Se forman dos moléculas de dióxido de carbono ( CO2 ) y dos moléculas de hidrógeno ( H2 ) como productos de desecho. Posteriormente, se produce ATP en el último paso de la fermentación. Se producen tres moléculas de ATP por cada molécula de glucosa, un rendimiento relativamente alto. La ecuación balanceada para esta fermentación es
Otras vías para el butirato incluyen la reducción de succinato y la desproporción de crotonato.
Varias especies forman acetona y n -butanol en una vía alternativa, que comienza como fermentación del butirato. Algunas de estas especies son:
Estas bacterias comienzan con la fermentación del butirato, como se ha descrito anteriormente, pero, cuando el pH desciende por debajo de 5, pasan a producir butanol y acetona para evitar que el pH siga bajando. Se forman dos moléculas de butanol por cada molécula de acetona.
El cambio de vía ocurre después de la formación de acetoacetil CoA. Este intermediario toma entonces dos posibles vías:
Para fines comerciales, las especies de Clostridium se utilizan preferentemente para la producción de ácido butírico o butanol. La especie más común utilizada para probióticos es Clostridium butyricum . [21]
Los residuos de fibra altamente fermentables, como los del almidón resistente , el salvado de avena , la pectina y el guar, son transformados por las bacterias colónicas en ácidos grasos de cadena corta (AGCC), incluido el butirato, lo que produce más AGCC que las fibras menos fermentables, como las celulosas . [14] [22] Un estudio encontró que el almidón resistente produce consistentemente más butirato que otros tipos de fibra dietética . [23] La producción de AGCC a partir de fibras en animales rumiantes , como el ganado, es responsable del contenido de butirato de la leche y la mantequilla. [13] [24]
Los fructanos son otra fuente de fibras dietéticas solubles prebióticas que se pueden digerir para producir butirato. [25] A menudo se encuentran en las fibras solubles de alimentos con alto contenido de azufre , como el allium y las verduras crucíferas . Las fuentes de fructanos incluyen trigo (aunque algunas cepas de trigo como la espelta contienen cantidades menores), [26] centeno , cebada , cebolla , ajo , alcachofa de Jerusalén y alcachofa , espárragos , remolacha , achicoria , hojas de diente de león , puerro , radicchio , la parte blanca de la cebolla de verdeo , brócoli , coles de Bruselas , repollo , hinojo y prebióticos , como fructooligosacáridos ( FOS ), oligofructosa e inulina . [27] [28]
El ácido butírico reacciona como un ácido carboxílico típico: puede formar derivados de amida , éster , anhídrido y cloruro . [29] Este último, el cloruro de butirilo , se utiliza comúnmente como intermedio para obtener los demás.
El ácido butírico se utiliza en la preparación de diversos ésteres de butirato. Se utiliza para producir acetato butirato de celulosa (CAB), que se utiliza en una amplia variedad de herramientas, pinturas y revestimientos, y es más resistente a la degradación que el acetato de celulosa . [30] El CAB puede degradarse con la exposición al calor y la humedad, liberando ácido butírico. [31]
Los ésteres de ácido butírico de bajo peso molecular, como el butirato de metilo , tienen en su mayoría aromas o sabores agradables. [7] Por ello, se utilizan como aditivos alimentarios y de perfumes. Es un aromatizante alimentario aprobado en la base de datos FLAVIS de la UE (número 08.005).
Debido a su potente olor, también se ha utilizado como aditivo para cebos de pesca. [32] Muchos de los sabores disponibles comercialmente que se utilizan en cebos para carpas ( Cyprinus carpio ) utilizan ácido butírico como base de éster. No está claro si los peces se sienten atraídos por el ácido butírico en sí o por las sustancias que se le añaden. El ácido butírico fue uno de los pocos ácidos orgánicos que demostró ser agradable tanto para la tenca como para el bitterling . [33] La sustancia ha sido utilizada como bomba fétida por la Sea Shepherd Conservation Society para perturbar a las tripulaciones balleneras japonesas . [34]
El ácido butírico (pKa 4,82 ) está completamente ionizado a pH fisiológico , por lo que su anión es el material que tiene mayor relevancia en los sistemas biológicos. Es uno de los dos agonistas endógenos primarios del receptor 2 del ácido hidroxicarboxílico humano ( HCA 2 , también conocido como GPR109A), un receptor acoplado a proteína G (GPCR) acoplado a G i/o , [16] [17]
Al igual que otros ácidos grasos de cadena corta (SCFA), el butirato es un agonista de los receptores de ácidos grasos libres FFAR2 y FFAR3 , que funcionan como sensores de nutrientes que facilitan el control homeostático del equilibrio energético ; sin embargo, entre el grupo de SCFA, solo el butirato es un agonista de HCA 2. [37] [38] [39] También es un inhibidor de HDAC (específicamente, HDAC1, HDAC2, HDAC3 y HDAC8), [35] [ 36] un fármaco que inhibe la función de las enzimas histonas desacetilasas , favoreciendo así un estado acetilado de las histonas en las células. [39] La acetilación de histonas afloja la estructura de la cromatina al reducir la atracción electrostática entre las histonas y el ADN . [39] En general, se cree que los factores de transcripción no podrán acceder a las regiones donde las histonas están estrechamente asociadas con el ADN (es decir, no acetiladas, por ejemplo, heterocromatina). [ cita médica necesaria ] Por lo tanto, se cree que el ácido butírico mejora la actividad transcripcional en los promotores, [39] que normalmente están silenciados o regulados negativamente debido a la actividad de la histona desacetilasa.
El butirato que se produce en el colon a través de la fermentación microbiana de la fibra dietética es absorbido y metabolizado principalmente por los colonocitos y el hígado [nota 1] para la generación de ATP durante el metabolismo energético; sin embargo, algo de butirato se absorbe en el colon distal, que no está conectado a la vena porta, lo que permite la distribución sistémica del butirato a múltiples sistemas orgánicos a través del sistema circulatorio. [39] [40] El butirato que ha alcanzado la circulación sistémica puede cruzar fácilmente la barrera hematoencefálica a través de transportadores monocarboxilato (es decir, ciertos miembros del grupo de transportadores SLC16A ). [41] [42] Otros transportadores que median el paso del butirato a través de las membranas lipídicas incluyen SLC5A8 (SMCT1), SLC27A1 (FATP1) y SLC27A4 (FATP4). [35] [42]
El ácido butírico es metabolizado por varias ligasas XM humanas (ACSM1, ACSM2B, ASCM3, ACSM4, ACSM5 y ACSM6), también conocidas como ligasa butirato-CoA. [43] [44] El metabolito producido por esta reacción es butiril-CoA y se produce de la siguiente manera: [43]
Como ácido graso de cadena corta , el butirato es metabolizado por las mitocondrias como fuente de energía (es decir, trifosfato de adenosina o ATP) a través del metabolismo de los ácidos grasos . [39] En particular, es una fuente de energía importante para las células que recubren el colon de los mamíferos (colonocitos). [25] Sin butiratos, las células del colon experimentan autofagia (es decir, autodigestión) y mueren. [45]
En los seres humanos, el precursor del butirato tributirina , que está presente de forma natural en la mantequilla, es metabolizado por la lipasa de triacilglicerol en dibutirina y butirato a través de la reacción: [46]
El butirato tiene numerosos efectos sobre la homeostasis energética y enfermedades relacionadas ( diabetes y obesidad ), la inflamación y la función inmune (por ejemplo, tiene efectos antimicrobianos y anticancerígenos pronunciados ) en humanos. Estos efectos ocurren a través de su metabolismo por las mitocondrias para generar ATP durante el metabolismo de los ácidos grasos o a través de uno o más de sus objetivos enzimáticos modificadores de histonas (es decir, las histonas desacetilasas de clase I ) y objetivos de receptores acoplados a proteína G (es decir, FFAR2 , FFAR3 y HCA 2 ). [37] [47]
El butirato es esencial para la homeostasis inmunitaria del huésped. [37] Aunque el papel y la importancia del butirato en el intestino no se entienden completamente, muchos investigadores sostienen que un agotamiento de las bacterias productoras de butirato en pacientes con varias afecciones vasculíticas es esencial para la patogénesis de estos trastornos. Un agotamiento de butirato en el intestino generalmente es causado por una ausencia o agotamiento de bacterias productoras de butirato (BPB). Este agotamiento en BPB conduce a una disbiosis microbiana . Esto se caracteriza por una baja biodiversidad general y un agotamiento de los miembros clave productores de butirato. El butirato es un metabolito microbiano esencial con un papel vital como modulador de la función inmune adecuada en el huésped. Se ha demostrado que los niños que carecen de BPB son más susceptibles a la enfermedad alérgica [48] y la diabetes tipo 1. [49] El butirato también se reduce en una dieta baja en fibra dietética , que puede inducir inflamación y tener otros efectos adversos en la medida en que estos ácidos grasos de cadena corta activan PPAR-γ . [50]
El butirato desempeña un papel clave para el mantenimiento de la homeostasis inmune tanto localmente (en el intestino) como sistémicamente (a través del butirato circulante). Se ha demostrado que promueve la diferenciación de las células T reguladoras . En particular, el butirato circulante estimula la generación de células T reguladoras extratímicas. Los bajos niveles de butirato en sujetos humanos podrían favorecer un control reducido mediado por células T reguladoras, promoviendo así una potente respuesta inmunopatológica de las células T. [51] Por otro lado, se ha informado que el butirato intestinal inhibe las citocinas proinflamatorias locales. Por lo tanto, la ausencia o el agotamiento de estas BPB en el intestino podría ser una posible ayuda en la respuesta inflamatoria hiperactiva. El butirato en el intestino también protege la integridad de la barrera epitelial intestinal. Por lo tanto, la disminución de los niveles de butirato conduce a una barrera epitelial intestinal dañada o disfuncional. [52] La reducción de butirato también se ha asociado con la proliferación de Clostridioides difficile . Por el contrario, una dieta rica en fibra produce una mayor concentración de ácido butírico y una inhibición del crecimiento de C. difficile . [53]
En un estudio de investigación de 2013 realizado por Furusawa et al., se descubrió que el butirato derivado de microbios era esencial para inducir la diferenciación de células T reguladoras colónicas en ratones. Esto es de gran importancia y posiblemente relevante para la patogénesis y la vasculitis asociadas con muchas enfermedades inflamatorias porque las células T reguladoras tienen un papel central en la supresión de las respuestas inflamatorias y alérgicas. [54] En varios estudios de investigación, se ha demostrado que el butirato indujo la diferenciación de células T reguladoras in vitro e in vivo. [55] La capacidad antiinflamatoria del butirato ha sido ampliamente analizada y respaldada por muchos estudios. Se ha descubierto que el butirato producido por microorganismos acelera la producción de células T reguladoras, aunque el mecanismo específico por el cual lo hace no está claro. [56] Más recientemente, se ha demostrado que el butirato juega un papel esencial y directo en la modulación de la expresión génica de las células T citotóxicas. [57] El butirato también tiene un efecto antiinflamatorio sobre los neutrófilos, reduciendo su migración a las heridas. Este efecto está mediado por el receptor HCA 1. [58 ]
En los microbiomas intestinales que se encuentran en la clase Mammalia, los omnívoros y herbívoros tienen comunidades bacterianas productoras de butirato dominadas por la vía butiril-CoA:acetato CoA-transferasa, mientras que los carnívoros tienen comunidades bacterianas productoras de butirato dominadas por la vía butirato quinasa. [59]
El olor del ácido butírico, que emana de los folículos sebáceos de todos los mamíferos, actúa sobre la garrapata como una señal.
Los efectos del butirato sobre el sistema inmunológico están mediados por la inhibición de las histonas desacetilasas de clase I y la activación de sus receptores acoplados a proteína G : HCA 2 (GPR109A), FFAR2 (GPR43) y FFAR3 (GPR41). [38] [60] Entre los ácidos grasos de cadena corta , el butirato es el promotor más potente de las células T reguladoras intestinales in vitro y el único entre el grupo que es un ligando HCA 2. [38] Se ha demostrado que es un mediador crítico de la respuesta inflamatoria colónica. Posee potencial tanto preventivo como terapéutico para contrarrestar la colitis ulcerosa y el cáncer colorrectal mediados por inflamación .
El butirato ha establecido propiedades antimicrobianas en humanos que están mediadas a través del péptido antimicrobiano LL-37 , que induce a través de la inhibición de HDAC en la histona H3. [60] [61] [62] In vitro, el butirato aumenta la expresión génica de FOXP3 (el regulador de la transcripción de Tregs ) y promueve las células T reguladoras colónicas (Tregs) a través de la inhibición de las histonas desacetilasas de clase I ; [38] [60] a través de estas acciones, aumenta la expresión de interleucina 10 , una citocina antiinflamatoria . [60] [38] El butirato también suprime la inflamación colónica al inhibir las vías de señalización de IFN-γ - STAT1 , que está mediada parcialmente a través de la inhibición de la histona desacetilasa . Mientras que la señalización transitoria de IFN-γ generalmente se asocia con la respuesta inmune normal del huésped , la señalización crónica de IFN-γ a menudo se asocia con la inflamación crónica. Se ha demostrado que el butirato inhibe la actividad de HDAC1 que está unido al promotor del gen Fas en las células T, lo que da como resultado la hiperacetilación del promotor Fas y la regulación positiva del receptor Fas en la superficie de las células T. [63]
Al igual que otros agonistas de HCA 2 estudiados, el butirato también produce marcados efectos antiinflamatorios en una variedad de tejidos, incluidos el cerebro, el tracto gastrointestinal, la piel y el tejido vascular . [64] [65] [66] La unión del butirato en FFAR3 induce la liberación del neuropéptido Y y promueve la homeostasis funcional de la mucosa colónica y el sistema inmunológico entérico. [67]
Se ha demostrado que el butirato es un mediador crítico de la respuesta inflamatoria colónica. Es responsable de aproximadamente el 70% de la energía de los colonocitos, siendo un SCFA crítico en la homeostasis del colon . [68] El butirato posee potencial tanto preventivo como terapéutico para contrarrestar la colitis ulcerosa (CU) mediada por inflamación y el cáncer colorrectal . [69] Produce diferentes efectos en células sanas y cancerosas: esto se conoce como la "paradoja del butirato". En particular, el butirato inhibe las células tumorales colónicas y estimula la proliferación de células epiteliales colónicas sanas. [70] [71] La explicación de por qué el butirato es una fuente de energía para los colonocitos normales e induce apoptosis en células de cáncer de colon , es el efecto Warburg en las células cancerosas, que lleva a que el butirato no se metabolice adecuadamente. Este fenómeno lleva a la acumulación de butirato en el núcleo, actuando como un inhibidor de la histona desacetilasa (HDAC). [72] Un mecanismo subyacente a la función del butirato en la supresión de la inflamación colónica es la inhibición de las vías de señalización IFN-γ / STAT1 . Se ha demostrado que el butirato inhibe la actividad de HDAC1 que está unida al promotor del gen Fas en las células T , lo que resulta en la hiperacetilación del promotor Fas y la regulación positiva del receptor Fas en la superficie de las células T. Por lo tanto, se sugiere que el butirato mejora la apoptosis de las células T en el tejido colónico y, por lo tanto, elimina la fuente de inflamación (producción de IFN-γ). [73] El butirato inhibe la angiogénesis al inactivar la actividad del factor de transcripción Sp1 y regular negativamente la expresión del gen del factor de crecimiento endotelial vascular . [74]
En resumen, la producción de ácidos grasos volátiles como el butirato a partir de fibras fermentables puede contribuir al papel de la fibra dietética en el cáncer de colon. Los ácidos grasos de cadena corta , que incluyen el ácido butírico, son producidos por bacterias colónicas beneficiosas ( probióticos ) que se alimentan de, o fermentan, prebióticos, que son productos vegetales que contienen fibra dietética. Estos ácidos grasos de cadena corta benefician a los colonocitos al aumentar la producción de energía y pueden proteger contra el cáncer de colon al inhibir la proliferación celular. [22]
Por el contrario, algunos investigadores han intentado eliminar el butirato y lo consideran un posible factor desencadenante de cáncer. [75] Estudios en ratones indican que impulsa la transformación de células epiteliales del colon deficientes en MSH2 . [76]
Debido a la importancia del butirato como regulador inflamatorio y contribuyente al sistema inmunológico, la disminución de butirato podría ser un factor clave que influye en la patogénesis de muchas enfermedades vasculíticas . Por lo tanto, es esencial mantener niveles saludables de butirato en el intestino. Los trasplantes de microbiota fecal (para restablecer la BPB y la simbiosis en el intestino) podrían ser efectivos al reponer los niveles de butirato. En este tratamiento, un individuo sano dona sus heces para que sean trasplantadas a un individuo con disbiosis. Una opción de tratamiento menos invasiva es la administración de butirato (como suplementos orales o enemas), que ha demostrado ser muy eficaz para terminar con los síntomas de inflamación con efectos secundarios mínimos o nulos. En un estudio en el que se trató a pacientes con colitis ulcerosa con enemas de butirato, la inflamación disminuyó significativamente y el sangrado cesó por completo después de la administración de butirato. [77]
El ácido butírico es un HDACinhibidor que es selectivo para las HDAC de clase I en humanos. [35] Las HDAC son enzimas modificadoras de histonas que pueden causar la desacetilación de histonas y la represión de la expresión génica. Las HDAC son reguladores importantes de la formación sináptica, la plasticidad sináptica y la formación de la memoria a largo plazo . Se sabe que las HDAC de clase I están involucradas en la mediación del desarrollo de una adicción . [78] [79] [80] El ácido butírico y otros inhibidores de HDAC se han utilizado en la investigación preclínica para evaluar los efectos transcripcionales, neuronales y conductuales de la inhibición de HDAC en animales adictos a las drogas. [80] [81] [82]
El ion butirato o butanoato , C 3 H 7 C O O − , es la base conjugada del ácido butírico. Es la forma que se encuentra en los sistemas biológicos a pH fisiológico . Un compuesto butírico (o butanoico) es una sal o éster carboxilato del ácido butírico.
Este artículo incorpora texto de una publicación que ahora es de dominio público : Chisholm, Hugh , ed. (1911). "Ácido butírico". Encyclopædia Britannica (11.ª ed.). Cambridge University Press.
Los ácidos grasos de cadena corta (AGCC) como el acetato, el butirato y el propionato, que se producen por fermentación microbiana intestinal de la fibra dietética, se reconocen como fuentes esenciales de energía para el huésped y actúan como moléculas de transducción de señales a través de receptores acoplados a proteína G (FFAR2, FFAR3, OLFR78, GPR109A) y como reguladores epigenéticos de la expresión génica mediante la inhibición de la histona desacetilasa (HDAC). Evidencias recientes sugieren que la fibra dietética y los AGCC derivados de los microbios intestinales ejercen múltiples efectos beneficiosos sobre el metabolismo energético del huésped, no sólo mejorando el ambiente intestinal, sino también afectando directamente a varios tejidos periféricos del huésped.
Las venas rectales media e inferior drenan la parte inferior del recto y la sangre venosa se devuelve a la vena cava inferior. Por lo tanto, los fármacos absorbidos en este último sistema se entregarán preferentemente a la circulación sistémica, evitando el hígado y el metabolismo de primer paso.
Otros estudios in vivo en nuestros laboratorios indicaron que varios compuestos, incluidos acetato, propionato, butirato, ácido benzoico, ácido salicílico, ácido nicotínico y algunos antibióticos β-lactámicos, pueden ser transportados por el MCT en la BHE.
21
... La captación de ácido valproico se redujo en presencia de ácidos grasos de cadena media como hexanoato, octanoato y decanoato, pero no propionato o butirato, lo que indica que el ácido valproico se absorbe en el cerebro a través de un sistema de transporte para ácidos grasos de cadena media, no ácidos grasos de cadena corta.
Se sabe que los transportadores de monocarboxilato (MCT) median el transporte de monocarboxilatos de cadena corta como el lactato, el piruvato y el butirato. ... MCT1 y MCT4 también se han asociado con el transporte de ácidos grasos de cadena corta como el acetato y el formato que luego se metabolizan en los astrocitos [78]. ... SLC5A8 se expresa en el tejido de colon normal y funciona como un supresor tumoral en el colon humano; el silenciamiento de este gen ocurre en el carcinoma de colon. Este transportador está involucrado en la captación concentrativa de butirato y piruvato producidos como producto de la fermentación por las bacterias colónicas.
{{cite encyclopedia}}: |website=ignorado ( ayuda )