Un tumor benigno es una masa de células ( tumor ) que no invade el tejido vecino ni hace metástasis (se propaga por todo el cuerpo). En comparación con los tumores malignos (cancerosos) , los tumores benignos generalmente tienen una tasa de crecimiento más lenta . Los tumores benignos tienen células relativamente bien diferenciadas . A menudo están rodeados por una superficie externa (vaina fibrosa de tejido conectivo ) o permanecen contenidos dentro del epitelio . Los ejemplos comunes de tumores benignos incluyen lunares y fibromas uterinos .
Algunas formas de tumores benignos pueden ser perjudiciales para la salud. El crecimiento de un tumor benigno causa un efecto de masa que puede comprimir los tejidos vecinos. Esto puede provocar daño a los nervios, reducción del flujo sanguíneo ( isquemia ), muerte tisular ( necrosis ) o daño a los órganos. Los efectos sobre la salud del crecimiento de un tumor benigno pueden ser más prominentes si el tumor está contenido dentro de un espacio cerrado como el cráneo , el tracto respiratorio , los senos nasales o los huesos. Por ejemplo, a diferencia de la mayoría de los tumores benignos en otras partes del cuerpo, los tumores cerebrales benignos pueden poner en peligro la vida. Los tumores pueden exhibir comportamientos característicos de su tipo de célula de origen; por ejemplo, los tumores endocrinos como los adenomas tiroideos y los adenomas adrenocorticales pueden producir en exceso ciertas hormonas .
La palabra "benigno" significa "favorable, amable, afortunado, saludable, propicio". [1] Sin embargo, un tumor benigno no es benigno en el sentido habitual; el nombre simplemente especifica que no es "maligno", es decir, canceroso. Si bien los tumores benignos generalmente no representan un riesgo grave para la salud, pueden ser dañinos o fatales. [2] Muchos tipos de tumores benignos tienen el potencial de volverse cancerosos ( malignos ) a través de un proceso conocido como progresión tumoral . Por esta razón y otros posibles daños, algunos tumores benignos se eliminan mediante cirugía. Una vez extirpados, los tumores benignos generalmente no regresan. Las excepciones a esta regla pueden indicar una transformación maligna.
Los tumores benignos son muy diversos; pueden ser asintomáticos o pueden causar síntomas específicos, dependiendo de su ubicación anatómica y tipo de tejido. Crecen hacia afuera, produciendo grandes masas redondeadas que pueden causar lo que se conoce como un "efecto de masa". Este crecimiento puede causar compresión de tejidos u órganos locales, lo que lleva a muchos efectos, como bloqueo de conductos, reducción del flujo sanguíneo ( isquemia ), muerte tisular ( necrosis ) y dolor o daño nervioso. [3] Algunos tumores también producen hormonas que pueden llevar a situaciones potencialmente mortales. Los insulinomas pueden producir grandes cantidades de insulina, causando hipoglucemia . [4] [5] Los adenomas hipofisarios pueden causar niveles elevados de hormonas como la hormona del crecimiento y el factor de crecimiento similar a la insulina-1 , que causan acromegalia ; prolactina ; ACTH y cortisol , que causan enfermedad de Cushing ; TSH , que causa hipertiroidismo ; y FSH y LH . [6] La intususcepción intestinal puede ocurrir con varios tumores colónicos benignos. [7] Los tumores, especialmente los de la piel, pueden producir efectos cosméticos, pudiendo causar malestar psicológico o social a la persona que los padece. [8] Los tumores del tejido vascular pueden sangrar, lo que en algunos casos puede derivar en anemia . [9]
El síndrome de hamartoma PTEN abarca trastornos hamartomatosos caracterizados por mutaciones genéticas en el gen supresor de tumores PTEN , [10] incluyendo el síndrome de Cowden , el síndrome de Bannayan–Riley–Ruvalcaba , el síndrome de Proteus y el síndrome similar a Proteus . La proteína PTEN ausente o disfuncional permite que las células proliferen en exceso, causando hamartomas. [11] El síndrome de Cowden es un trastorno genético autosómico dominante caracterizado por múltiples hamartomas benignos ( triquilemomas y pápulas papilomatosas mucocutáneas) así como una predisposición a cánceres de múltiples órganos incluyendo la mama y la tiroides. [12] [13] El síndrome de Bannayan–Riley–Ruvalcaba es un trastorno congénito caracterizado por poliposis intestinal hamartomatosa, macrocefalia , lipomatosis , hemangiomatosis y máculas en el glande del pene . [11] [14] El síndrome de Proteus se caracteriza por nevos , crecimiento excesivo asimétrico de varias partes del cuerpo, desregulación del tejido adiposo, cistoadenomas , adenomas y malformación vascular. [15] [16]

La poliposis adenomatosa familiar (PAF) es un síndrome de cáncer familiar causado por mutaciones en el gen APC . En la PAF, los pólipos adenomatosos están presentes en el colon . Los pólipos progresan a cáncer de colon a menos que se extirpen. [17] El gen APC es un supresor de tumores . Su producto proteico está involucrado en muchos procesos celulares. La inactivación del gen APC conduce a la acumulación de una proteína llamada β-catenina . Esta proteína activa dos factores de transcripción : el factor de células T (TCF) y el factor potenciador linfoide (LEF). Estos factores causan la regulación positiva de muchos genes involucrados en la proliferación celular , diferenciación , migración y apoptosis (muerte celular programada), lo que causa el crecimiento de tumores benignos. [18]
El complejo de esclerosis tuberosa (TSC) es un trastorno genético autosómico dominante causado por mutaciones en los genes TSC1 y TSC2 . TSC1 produce la proteína hamartina . TSC2 produce la proteína tuberina . Este trastorno se presenta con muchos tumores hamartomatosos benignos, incluidos angiofibromas , angiomiolipomas renales y linfangiomiomatosis pulmonar . La tuberina y la hamartina inhiben la proteína mTOR en la fisiología celular normal. La inactivación de los supresores tumorales de TSC provoca un aumento en la actividad de mTOR. Esto conduce a la activación de genes y la producción de proteínas que aumentan el crecimiento celular. [19] [20] [21]
La enfermedad de von Hippel-Lindau es un síndrome de cáncer de herencia dominante que aumenta significativamente el riesgo de varios tumores. Esto incluye hemangioblastomas benignos y feocromocitomas malignos , carcinomas de células renales , tumores endocrinos pancreáticos y tumores del saco endolinfático . Es causada por mutaciones genéticas en el gen supresor de tumores de von Hippel-Lindau . La proteína VHL (pVHL) está involucrada en la señalización celular en células hambrientas de oxígeno ( hipóxicas ). Una función de pVHL es causar la degradación celular de otra proteína, HIF1α . La pVHL disfuncional conduce a la acumulación de HIF1α. Esto activa varios genes responsables de la producción de sustancias involucradas en el crecimiento celular y la producción de vasos sanguíneos: VEGF , PDGFβ , TGFα y eritropoyetina . [22]
Los tumores benignos del hueso pueden ser similares macroscópicamente y requieren una combinación de una historia clínica con pruebas citogenéticas , moleculares y radiológicas para el diagnóstico. [23] Tres formas comunes de tumores óseos benignos son el tumor de células gigantes del hueso, el osteocondroma y el encondroma ; existen otras formas de tumores óseos benignos pero pueden ser menos frecuentes.
Los tumores de células gigantes del hueso se presentan con frecuencia en las epífisis de los huesos largos del esqueleto apendicular o en el sacro del esqueleto axial . El crecimiento local puede causar la destrucción del hueso cortical vecino y del tejido blando, lo que provoca dolor y limita el rango de movimiento. El hallazgo radiológico característico de los tumores de células gigantes del hueso es una lesión lítica que no tiene esclerosis marginal del hueso. En la histología, las células gigantes de los osteoclastos fusionados se ven como una respuesta a las células mononucleares neoplásicas. Cabe destacar que las células gigantes no son exclusivas entre los tumores óseos benignos de los tumores de células gigantes del hueso. Las características moleculares de las células neoplásicas que causan los tumores de células gigantes del hueso indican un origen de células madre mesenquimales pluripotentes que adoptan marcadores preosteoblásticos. Las causas citogenéticas de los tumores de células gigantes del hueso involucran a los telómeros . El tratamiento implica curetaje quirúrgico con bifosfonatos adyuvantes .
Los osteocondromas forman proyecciones óseas recubiertas de cartílago. Las estructuras como la cavidad medular y el hueso cortical del osteocondroma son contiguas a las del hueso de origen. Los sitios de origen a menudo involucran metáfisis de huesos largos. Si bien muchos osteocondromas se producen de manera espontánea, existen casos en los que pueden aparecer varios osteocondromas en el mismo individuo; estos pueden estar relacionados con una condición genética conocida como osteocondromas múltiples hereditarios. El osteocondroma aparece en la radiografía como una masa saliente que a menudo apunta lejos de las articulaciones. [23] Estos tumores dejan de crecer con el cierre de las placas de crecimiento del hueso parental. La incapacidad de detener el crecimiento puede ser indicativa de transformación a condrosarcoma maligno. El tratamiento no está indicado a menos que sea sintomático. En ese caso, la escisión quirúrgica suele ser curativa.
Los encondromas son tumores benignos del cartílago hialino. Dentro de un hueso, los encondromas se encuentran a menudo en las metáfisis. Se pueden encontrar en muchos tipos de huesos, incluidos los huesos pequeños, los huesos largos y el esqueleto axial. La radiografía de los encondromas muestra bordes bien definidos y una apariencia punteada. [23] La presentación de encondromas múltiples es consistente con la encondromatosis múltiple ( enfermedad de Ollier ). El tratamiento de los encondromas implica legrado quirúrgico e injerto.
Los lipomas son tumores benignos subcutáneos de células grasas ( adipocitos ). Por lo general, son masas indoloras, de crecimiento lento y móviles que pueden aparecer en cualquier parte del cuerpo donde haya células grasas, pero que se encuentran típicamente en el tronco y las extremidades superiores. [24]
[25] Aunque los lipomas pueden desarrollarse a cualquier edad, aparecen más comúnmente entre los 40 y 60 años. [24] Los lipomas afectan a alrededor del 1% de la población, sin sesgo de sexo documentado, y aproximadamente 1 de cada 1000 personas tendrá un lipoma durante su vida. [25] [26] La causa de los lipomas no está bien definida. Las causas genéticas o hereditarias de los lipomas juegan un papel en alrededor del 2-3% de los pacientes. [25] En individuos con síndromes familiares hereditarios como el síndrome de Proteus o la lipomatosis múltiple familiar , es común ver múltiples lipomas en todo el cuerpo. [25] Estos síndromes también están asociados con síntomas y subpoblaciones específicas. Se han identificado mutaciones en el cromosoma 12 en alrededor del 65% de los casos de lipoma. [25] También se ha demostrado que los lipomas aumentan en aquellos con obesidad , hiperlipidemia y diabetes mellitus . [25]
Los lipomas generalmente se diagnostican clínicamente, aunque se pueden utilizar imágenes ( ultrasonido , tomografía computarizada o resonancia magnética ) para ayudar con el diagnóstico de lipomas en ubicaciones atípicas. [24] El principal tratamiento para los lipomas es la escisión quirúrgica, después de lo cual se examina el tumor con histopatología para confirmar el diagnóstico. [24] El pronóstico para los lipomas benignos es excelente y la recurrencia después de la escisión es rara, pero puede ocurrir si la eliminación fue incompleta. [25]

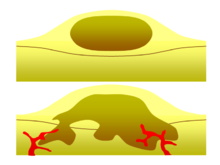
Uno de los factores más importantes para clasificar un tumor como benigno o maligno es su potencial invasivo. Si un tumor carece de la capacidad de invadir tejidos adyacentes o propagarse a sitios distantes mediante metástasis, entonces es benigno, mientras que los tumores invasivos o metastásicos son malignos. [3] Por esta razón, los tumores benignos no se clasifican como cáncer. [27] Los tumores benignos crecerán en un área contenida generalmente encapsulada en una cápsula de tejido conectivo fibroso . Las tasas de crecimiento de los tumores benignos y malignos también difieren; los tumores benignos generalmente crecen más lentamente que los tumores malignos. Aunque los tumores benignos plantean un riesgo de salud menor que los tumores malignos, ambos pueden poner en peligro la vida en ciertas situaciones. Hay muchas características generales que se aplican tanto a los tumores benignos como a los malignos, pero a veces un tipo puede mostrar características del otro. Por ejemplo, los tumores benignos están en su mayoría bien diferenciados y los tumores malignos a menudo son indiferenciados. Sin embargo, pueden ocurrir tumores benignos indiferenciados y tumores malignos diferenciados. [28] [29] Aunque los tumores benignos generalmente crecen lentamente, también se han documentado casos de tumores benignos de crecimiento rápido. [30] Algunos tumores malignos son en su mayoría no metastásicos, como en el caso del carcinoma de células basales . [31] La TC y la radiografía de tórax pueden ser un examen de diagnóstico útil para visualizar un tumor benigno y diferenciarlo de un tumor maligno. Cuanto más pequeño sea el tumor en una radiografía, más probable es que sea benigno, ya que el 80% de los nódulos pulmonares de menos de 2 cm de diámetro son benignos. La mayoría de los nódulos benignos son densidades radiopacas suavizadas con márgenes claros, pero estos no son signos exclusivos de tumores benignos. [32]
Los tumores se forman por carcinogénesis , un proceso en el que las alteraciones celulares conducen a la formación de cáncer. La carcinogénesis en múltiples etapas implica los cambios genéticos o epigenéticos secuenciales en el ADN de una célula , donde cada paso produce un tumor más avanzado. A menudo se divide en tres etapas: iniciación, promoción y progresión, y pueden ocurrir varias mutaciones en cada etapa. La iniciación es donde ocurre la primera mutación genética en una célula. La promoción es la expansión clonal (división repetida) de esta célula transformada en un tumor visible que generalmente es benigno. Después de la promoción, puede tener lugar la progresión donde se adquieren más mutaciones genéticas en una subpoblación de células tumorales. La progresión cambia el tumor benigno en un tumor maligno. [33] [34] Un ejemplo destacado y bien estudiado de este fenómeno es el adenoma tubular, un tipo común de pólipo de colon que es un precursor importante del cáncer de colon. Las células de los adenomas tubulares, como la mayoría de los tumores que con frecuencia progresan al cáncer, muestran ciertas anomalías de maduración y apariencia celular conocidas colectivamente como displasia . Estas anomalías celulares no se observan en tumores benignos que rara vez o nunca se vuelven cancerosos, pero sí se observan en otras anomalías tisulares precancerosas que no forman masas discretas, como las lesiones precancerosas del cuello uterino .
Las neoplasias benignas están típicamente, pero no siempre, compuestas de células que tienen un gran parecido con un tipo de célula normal en su órgano de origen. Estos tumores reciben su nombre por el tipo de célula o tejido del que se originan. El sufijo "-oma" (pero no -carcinoma, -sarcoma o -blastoma, que generalmente son cánceres) se aplica para indicar un tumor benigno. Por ejemplo, un lipoma es un tumor benigno común de células grasas ( lipocitos ), y un condroma es un tumor benigno de células formadoras de cartílago ( condrocitos ). Los adenomas son tumores benignos de células formadoras de glándulas y generalmente se especifican además por su célula u órgano de origen, como en el adenoma hepático (un tumor benigno de hepatocitos o células del hígado ). Los teratomas contienen muchos tipos de células como piel, nervios, cerebro y tiroides, entre otras, porque se derivan de células germinales. [36] Los hamartomas son un grupo de tumores benignos que tienen una diferenciación celular relativamente normal pero exhiben una organización tisular desorganizada. [19]
Existen excepciones a las reglas de nomenclatura por razones históricas; los ejemplos malignos incluyen el melanoma (un cáncer de células cutáneas pigmentadas o melanocitos ) y el seminoma (un cáncer de células reproductivas masculinas). [37]
Los tumores benignos no incluyen todos los crecimientos benignos. Los acrocordones, los pólipos de las cuerdas vocales y los pólipos hiperplásicos del colon suelen denominarse benignos, pero son crecimientos excesivos de tejido normal en lugar de neoplasias. [36]
Los tumores benignos normalmente no necesitan tratamiento a menos que causen problemas como convulsiones, malestar o problemas estéticos. La cirugía suele ser el método más eficaz y se utiliza para tratar la mayoría de los tumores benignos. En algunos casos, se pueden utilizar otros tratamientos. Los adenomas del recto se pueden tratar con escleroterapia , en la que se utilizan productos químicos para encoger los vasos sanguíneos con el fin de cortar el suministro de sangre. [38] La mayoría de los tumores benignos no responden a la quimioterapia o la radioterapia , aunque hay excepciones; los tumores intercraneales benignos a veces se tratan con radioterapia y quimioterapia en determinadas circunstancias. [39] [40] La radiación también se puede utilizar para tratar los hemangiomas en el recto. [38] Los tumores benignos de la piel suelen resecarse quirúrgicamente, pero se utilizan otros tratamientos como la crioterapia , el legrado , la electrodesecación , la terapia con láser , la dermoabrasión , las exfoliaciones químicas y la medicación tópica . [41] [42]
Los niños con este tipo de tumor [inoperable, benigno] suelen morir a causa de un ritmo cardíaco anormal a una edad temprana.