Pirrol
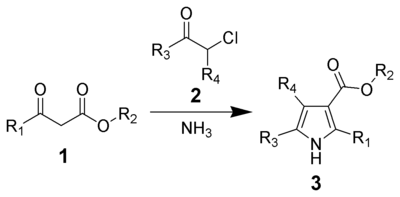
El pirrol es un compuesto químico orgánico heterocíclico aromático, un anillo de cinco miembros con la fórmula C4H5N.
La protonación del pirrol resulta en la pérdida de su aromaticidad y por lo tanto, la misma es termodinámicamente desfavorable.
El pirrol puede entonces ser desprotonado con bases fuertes como el butil-litio o el hidruro de sodio.
Luego al tratar esta base conjugada con un electrófilo como el ioduro de metilo nos da N-metilpirrol.
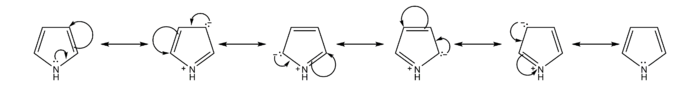
Como el furano y el tiofeno, el pirrol es más reactivo que el benceno frente a la sustitución electrofilica aromática debido a que el mismo es capaz de estabilizar la carga positiva en el carbocatión intermedio.
Luego el pirrol experimenta la sustitución electrofílica aromática(SEAr) predominantemente en las posiciones 2 y 5.
Por lo que se puede usar un agente oxidante como el persulfato de amonio a 0 °C en la oscuridad, para controlar la polimerización.