Una neurona , neurona , [1] o célula nerviosa es una célula excitable que dispara señales eléctricas llamadas potenciales de acción a través de una red neuronal en el sistema nervioso . Las neuronas se comunican con otras células a través de sinapsis , que son conexiones especializadas que comúnmente utilizan cantidades minúsculas de neurotransmisores químicos para pasar la señal eléctrica de la neurona presináptica a la célula objetivo a través del espacio sináptico.
Las neuronas son los componentes principales del tejido nervioso en todos los animales , excepto en las esponjas y los placozoos . Las plantas y los hongos no tienen células nerviosas. La evidencia molecular sugiere que la capacidad de generar señales eléctricas apareció por primera vez en la evolución hace unos 700 a 800 millones de años, durante el período Toniano . Los predecesores de las neuronas fueron las células secretoras peptidérgicas . Con el tiempo, estas adquirieron nuevos módulos genéticos que permitieron a las células crear andamiajes postsinápticos y canales iónicos que generan señales eléctricas rápidas. La capacidad de generar señales eléctricas fue una innovación clave en la evolución del sistema nervioso. [2]
Las neuronas se clasifican típicamente en tres tipos según su función. Las neuronas sensoriales responden a estímulos como el tacto, el sonido o la luz que afectan a las células de los órganos sensoriales y envían señales a la médula espinal o al cerebro . Las neuronas motoras reciben señales del cerebro y la médula espinal para controlar todo, desde las contracciones musculares [3] hasta la salida glandular . Las interneuronas conectan neuronas con otras neuronas dentro de la misma región del cerebro o la médula espinal. Cuando varias neuronas están conectadas funcionalmente entre sí, forman lo que se llama un circuito neuronal .
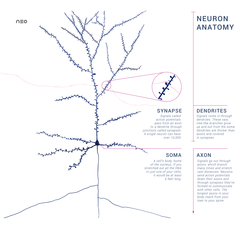
Una neurona contiene todas las estructuras de otras células, como un núcleo , mitocondrias y aparatos de Golgi , pero tiene estructuras únicas adicionales, como un axón y dendritas . [4] El soma es una estructura compacta, y el axón y las dendritas son filamentos que sobresalen del soma. Las dendritas normalmente se ramifican profusamente y se extienden unos cientos de micrómetros desde el soma. El axón sale del soma en una hinchazón llamada montículo axónico y viaja hasta 1 metro en los humanos o más en otras especies. Se ramifica, pero generalmente mantiene un diámetro constante. En la punta más alejada de las ramas del axón se encuentran las terminales axónicas , donde la neurona puede transmitir una señal a través de la sinapsis a otra célula. Las neuronas pueden carecer de dendritas o no tener axón. El término neurita se utiliza para describir una dendrita o un axón, particularmente cuando la célula no está diferenciada .
La mayoría de las neuronas reciben señales a través de las dendritas y el soma y envían señales a través del axón. En la mayoría de las sinapsis, las señales pasan del axón de una neurona a la dendrita de otra. Sin embargo, las sinapsis pueden conectar un axón con otro axón o una dendrita con otra dendrita. El proceso de señalización es en parte eléctrico y en parte químico. Las neuronas son eléctricamente excitables, debido al mantenimiento de gradientes de voltaje a través de sus membranas . Si el voltaje cambia en una cantidad lo suficientemente grande durante un intervalo corto, la neurona genera un pulso electroquímico de todo o nada llamado potencial de acción . Este potencial viaja rápidamente a lo largo del axón y activa las conexiones sinápticas a medida que las alcanza. Las señales sinápticas pueden ser excitatorias o inhibidoras , aumentando o reduciendo el voltaje neto que llega al soma.
En la mayoría de los casos, las neuronas son generadas por células madre neuronales durante el desarrollo cerebral y la infancia. La neurogénesis cesa en gran medida durante la edad adulta en la mayoría de las áreas del cerebro.
Las neuronas son los componentes principales del sistema nervioso , junto con las células gliales que les dan soporte estructural y metabólico. [5] El sistema nervioso está formado por el sistema nervioso central , que incluye el cerebro y la médula espinal , y el sistema nervioso periférico , que incluye los sistemas nerviosos autónomo , entérico y somático . [6] En los vertebrados, la mayoría de las neuronas pertenecen al sistema nervioso central , pero algunas residen en ganglios periféricos , y muchas neuronas sensoriales están situadas en órganos sensoriales como la retina y la cóclea .
Los axones pueden agruparse en fascículos nerviosos que forman los nervios en el sistema nervioso periférico (como los hilos de alambre que forman un cable). En el sistema nervioso central, los haces de axones se denominan tractos nerviosos .
Las neuronas están altamente especializadas en el procesamiento y transmisión de señales celulares. Dada la diversidad de funciones que desempeñan en diferentes partes del sistema nervioso, existe una amplia variedad en cuanto a forma, tamaño y propiedades electroquímicas. Por ejemplo, el soma de una neurona puede variar de 4 a 100 micrómetros de diámetro. [7]
La visión aceptada de la neurona atribuye funciones específicas a sus diversos componentes anatómicos; sin embargo, las dendritas y los axones a menudo actúan de manera contraria a su llamada función principal. [9]
Los axones y las dendritas del sistema nervioso central tienen un grosor de tan solo un micrómetro, mientras que algunos del sistema nervioso periférico son mucho más gruesos. El soma suele tener un diámetro de entre 10 y 25 micrómetros y, a menudo, no es mucho más grande que el núcleo celular que contiene. El axón más largo de una neurona motora humana puede tener más de un metro de longitud y se extiende desde la base de la columna hasta los dedos de los pies.
Las neuronas sensoriales pueden tener axones que van desde los dedos de los pies hasta la columna posterior de la médula espinal, de más de 1,5 metros en los adultos. Las jirafas tienen axones únicos de varios metros de longitud que recorren toda la longitud de sus cuellos. Gran parte de lo que se sabe sobre la función axonal proviene del estudio del axón gigante del calamar , una preparación experimental ideal debido a su tamaño relativamente inmenso (0,5-1 milímetro de grosor, varios centímetros de largo).
Las neuronas completamente diferenciadas son permanentemente postmitóticas [10] , sin embargo, las células madre presentes en el cerebro adulto pueden regenerar neuronas funcionales a lo largo de la vida de un organismo (ver neurogénesis ). Se ha observado que los astrocitos son células gliales con forma de estrella que se convierten en neuronas en virtud de su característica de pluripotencia similar a la de las células madre . [11]
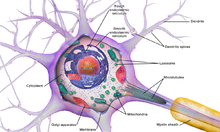
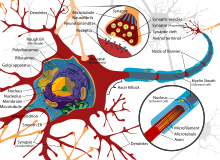
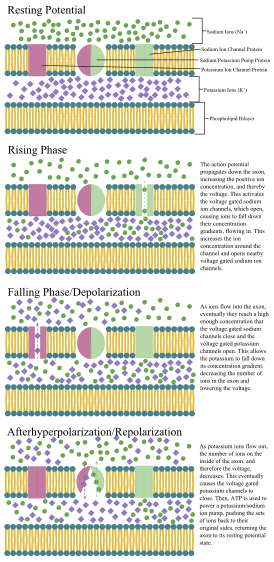
Al igual que todas las células animales, el cuerpo celular de cada neurona está rodeado por una membrana plasmática , una bicapa de moléculas lipídicas con muchos tipos de estructuras proteicas incrustadas en ella. [12] Una bicapa lipídica es un poderoso aislante eléctrico , pero en las neuronas, muchas de las estructuras proteicas incrustadas en la membrana son eléctricamente activas. Estas incluyen canales iónicos que permiten que los iones cargados eléctricamente fluyan a través de la membrana y bombas de iones que transportan químicamente iones de un lado de la membrana al otro. La mayoría de los canales iónicos son permeables solo a tipos específicos de iones. Algunos canales iónicos están regulados por voltaje , lo que significa que pueden cambiarse entre estados abiertos y cerrados alterando la diferencia de voltaje a través de la membrana. Otros están regulados químicamente, lo que significa que pueden cambiarse entre estados abiertos y cerrados mediante interacciones con sustancias químicas que se difunden a través del líquido extracelular. Los materiales iónicos incluyen sodio , potasio , cloruro y calcio . Las interacciones entre los canales iónicos y las bombas iónicas producen una diferencia de voltaje a través de la membrana, normalmente un poco menos de 1/10 de voltio en la línea base. Este voltaje tiene dos funciones: primero, proporciona una fuente de energía para una variedad de maquinaria proteica dependiente del voltaje que está incrustada en la membrana; segundo, proporciona una base para la transmisión de señales eléctricas entre diferentes partes de la membrana.


Cuando los cuerpos de las células nerviosas se tiñen con un colorante basófilo ("amante de las bases"), se observan numerosos grumos microscópicos llamados cuerpos de Nissl (o sustancia de Nissl). Estas estructuras consisten en retículo endoplasmático rugoso y ARN ribosómico asociado . Nombrados en honor al psiquiatra y neuropatólogo alemán Franz Nissl (1860-1919), están involucrados en la síntesis de proteínas y su prominencia se puede explicar por el hecho de que las células nerviosas son muy activas metabólicamente. Los colorantes basófilos como la anilina o (débilmente) la hematoxilina [13] resaltan los componentes con carga negativa y, por lo tanto, se unen a la estructura de fosfato del ARN ribosómico.
El cuerpo celular de una neurona está sostenido por una compleja red de proteínas estructurales llamadas neurofilamentos , que junto con los neurotúbulos (microtúbulos neuronales) se ensamblan en neurofibrillas más grandes. [14] Algunas neuronas también contienen gránulos de pigmento, como la neuromelanina (un pigmento marrón-negro que es un subproducto de la síntesis de catecolaminas ) y la lipofuscina (un pigmento marrón-amarillento), los cuales se acumulan con la edad. [15] [16] [17] Otras proteínas estructurales que son importantes para la función neuronal son la actina y la tubulina de los microtúbulos . La β-tubulina de clase III se encuentra casi exclusivamente en las neuronas. La actina se encuentra predominantemente en las puntas de los axones y las dendritas durante el desarrollo neuronal. Allí, la dinámica de la actina se puede modular a través de una interacción con los microtúbulos. [18]
Existen diferentes características estructurales internas entre los axones y las dendritas. Los axones típicos casi nunca contienen ribosomas , excepto algunos en el segmento inicial. Las dendritas contienen retículo endoplasmático granular o ribosomas, en cantidades decrecientes a medida que aumenta la distancia desde el cuerpo celular.

Las neuronas varían en forma y tamaño y pueden clasificarse por su morfología y función. [20] El anatomista Camillo Golgi agrupó las neuronas en dos tipos: tipo I con axones largos utilizados para mover señales a largas distancias y tipo II con axones cortos, que a menudo pueden confundirse con dendritas. Las células de tipo I pueden clasificarse además por la ubicación del soma. La morfología básica de las neuronas de tipo I, representadas por las neuronas motoras espinales , consiste en un cuerpo celular llamado soma y un axón largo y delgado cubierto por una vaina de mielina . El árbol dendrítico envuelve el cuerpo celular y recibe señales de otras neuronas. El extremo del axón tiene terminales axónicas ramificadas que liberan neurotransmisores en un espacio llamado hendidura sináptica entre las terminales y las dendritas de la siguiente neurona. [ cita requerida ]
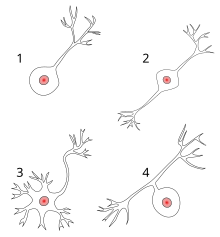
La mayoría de las neuronas se pueden caracterizar anatómicamente como: [4]
Se pueden identificar algunos tipos de neuronas únicos según su ubicación en el sistema nervioso y su forma distintiva. Algunos ejemplos son: [ cita requerida ]
Aferente y eferente también se refieren en general a las neuronas que, respectivamente, llevan información al cerebro o envían información desde el cerebro.
Una neurona afecta a otras neuronas liberando un neurotransmisor que se une a receptores químicos . El efecto sobre la neurona postsináptica está determinado por el tipo de receptor que se activa, no por la neurona presináptica o por el neurotransmisor. Un neurotransmisor puede considerarse como una llave y un receptor como una cerradura: el mismo neurotransmisor puede activar múltiples tipos de receptores. Los receptores pueden clasificarse en general como excitadores (que provocan un aumento en la tasa de activación), inhibidores (que provocan una disminución en la tasa de activación) o moduladores (que provocan efectos duraderos no relacionados directamente con la tasa de activación). [ cita requerida ]
Los dos neurotransmisores más comunes (90%+) en el cerebro, el glutamato y el GABA , tienen acciones en gran medida consistentes. El glutamato actúa sobre varios tipos de receptores y tiene efectos que son excitatorios en los receptores ionotrópicos y un efecto modulador en los receptores metabotrópicos . De manera similar, el GABA actúa sobre varios tipos de receptores, pero todos ellos tienen efectos inhibidores (en animales adultos, al menos). Debido a esta consistencia, es común que los neurocientíficos se refieran a las células que liberan glutamato como "neuronas excitadoras", y a las células que liberan GABA como "neuronas inhibidoras". Algunos otros tipos de neuronas tienen efectos consistentes, por ejemplo, las neuronas motoras "excitadoras" en la médula espinal que liberan acetilcolina , y las neuronas espinales "inhibitorias" que liberan glicina . [ cita requerida ]
La distinción entre neurotransmisores excitadores e inhibidores no es absoluta, sino que depende de la clase de receptores químicos presentes en la neurona postsináptica. En principio, una sola neurona, que libera un solo neurotransmisor, puede tener efectos excitadores en algunos objetivos, efectos inhibidores en otros y efectos moduladores en otros más. Por ejemplo, las células fotorreceptoras de la retina liberan constantemente el neurotransmisor glutamato en ausencia de luz. Las llamadas células bipolares OFF son, como la mayoría de las neuronas, excitadas por el glutamato liberado. Sin embargo, las neuronas diana vecinas, llamadas células bipolares ON, son inhibidas por el glutamato, porque carecen de receptores de glutamato ionotrópicos típicos y en su lugar expresan una clase de receptores de glutamato metabotrópicos inhibidores . [21] Cuando hay luz, los fotorreceptores dejan de liberar glutamato, lo que libera a las células bipolares ON de la inhibición, activándolas; esto simultáneamente elimina la excitación de las células bipolares OFF, silenciándolas. [ cita requerida ]
Es posible identificar el tipo de efecto inhibidor que una neurona presináptica tendrá sobre una neurona postsináptica, basándose en las proteínas que expresa la neurona presináptica. Las neuronas que expresan parvalbúmina típicamente amortiguan la señal de salida de la neurona postsináptica en la corteza visual , mientras que las neuronas que expresan somatostatina típicamente bloquean las entradas dendríticas a la neurona postsináptica. [22]
Las neuronas tienen propiedades electrorresponsivas intrínsecas como patrones oscilatorios de voltaje transmembrana intrínsecos . [23] Por lo tanto, las neuronas se pueden clasificar según sus características electrofisiológicas :

Los neurotransmisores son mensajeros químicos que pasan de una neurona a otra o a una célula muscular o glandular .
Desde 2012, la comunidad de neurociencia celular y computacional ha impulsado la creación de una clasificación universal de las neuronas que se aplique a todas las neuronas del cerebro y a todas las especies. Esto se hace teniendo en cuenta las tres cualidades esenciales de todas las neuronas: electrofisiología, morfología y el transcriptoma individual de las células. Además de ser universal, esta clasificación tiene la ventaja de poder clasificar también a los astrocitos. El Instituto Allen de Ciencias del Cerebro utiliza ampliamente un método llamado secuenciación de parches en el que se pueden medir las tres cualidades a la vez . [27] En 2023, se creó un atlas celular completo del cerebro humano adulto y en desarrollo a nivel transcripcional, epigenético y funcional mediante una colaboración internacional de investigadores que utilizan los enfoques de biología molecular más avanzados. [28]

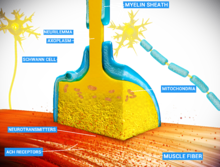
Las neuronas se comunican entre sí a través de sinapsis , donde la terminal axónica de una célula contacta con la dendrita, el soma o, con menos frecuencia, el axón de otra neurona. Las neuronas como las células de Purkinje en el cerebelo pueden tener más de 1000 ramificaciones dendríticas, que establecen conexiones con decenas de miles de otras células; otras neuronas, como las neuronas magnocelulares del núcleo supraóptico , tienen solo una o dos dendritas, cada una de las cuales recibe miles de sinapsis.
Las sinapsis pueden ser excitatorias o inhibidoras, aumentando o disminuyendo la actividad en la neurona diana, respectivamente. Algunas neuronas también se comunican a través de sinapsis eléctricas, que son uniones directas y conductoras de electricidad entre células. [29]
Cuando un potencial de acción alcanza la terminal axónica, abre canales de calcio dependientes del voltaje , lo que permite que los iones de calcio entren en la terminal. El calcio hace que las vesículas sinápticas llenas de moléculas de neurotransmisores se fusionen con la membrana, liberando su contenido en la hendidura sináptica. Los neurotransmisores se difunden a través de la hendidura sináptica y activan los receptores en la neurona postsináptica. El alto nivel de calcio citosólico en la terminal axónica desencadena la captación de calcio mitocondrial, que, a su vez, activa el metabolismo energético mitocondrial para producir ATP para apoyar la neurotransmisión continua. [30]
Una autapsis es una sinapsis en la que el axón de una neurona se conecta a sus propias dendritas.
El cerebro humano tiene unas 8,6 x 10 10 (ochenta y seis mil millones) de neuronas. [31] [32] Cada neurona tiene una media de 7.000 conexiones sinápticas con otras neuronas. Se ha estimado que el cerebro de un niño de tres años tiene unas 10 15 sinapsis (un cuatrillón). Esta cifra disminuye con la edad y se estabiliza en la edad adulta. Las estimaciones varían para un adulto, y van desde 10 14 hasta 5 x 10 14 sinapsis (100 a 500 billones). [33]
Más allá de la señalización eléctrica y química, los estudios sugieren que las neuronas en los cerebros humanos sanos también pueden comunicarse a través de:
También pueden ser moduladas por la información del entorno y las hormonas liberadas desde otras partes del organismo, [37] que podrían ser influenciadas más o menos directamente por las neuronas. Esto también se aplica a las neurotrofinas como el BDNF . El microbioma intestinal también está conectado con el cerebro. [38] Las neuronas también se comunican con la microglia , las principales células inmunes del cerebro a través de sitios de contacto especializados, llamados "uniones somáticas". Estas conexiones permiten que la microglia monitoree y regule constantemente las funciones neuronales y ejerza neuroprotección, cuando sea necesario. [39]
En 1937, John Zachary Young sugirió que el axón gigante del calamar podría utilizarse para estudiar las propiedades eléctricas neuronales. [40] Es más grande que las neuronas humanas, pero similar a ellas, lo que facilita su estudio. Al insertar electrodos en los axones gigantes del calamar, se realizaron mediciones precisas del potencial de membrana .
La membrana celular del axón y del soma contiene canales iónicos dependientes del voltaje que permiten a la neurona generar y propagar una señal eléctrica (un potencial de acción). Algunas neuronas también generan oscilaciones de potencial de membrana subumbral . Estas señales son generadas y propagadas por iones portadores de carga , incluidos el sodio (Na + ), el potasio (K + ), el cloruro (Cl − ) y el calcio (Ca 2+ ) .
Varios estímulos pueden activar una neurona y provocar actividad eléctrica, entre ellos, presión , estiramiento, transmisores químicos y cambios del potencial eléctrico a través de la membrana celular. [41] Los estímulos hacen que se abran canales iónicos específicos dentro de la membrana celular, lo que genera un flujo de iones a través de la membrana celular y cambia el potencial de membrana. Las neuronas deben mantener las propiedades eléctricas específicas que definen su tipo de neurona. [42]
Las neuronas y los axones delgados requieren un menor gasto metabólico para producir y transportar potenciales de acción, pero los axones más gruesos transmiten impulsos más rápidamente. Para minimizar el gasto metabólico manteniendo al mismo tiempo una conducción rápida, muchas neuronas tienen vainas aislantes de mielina alrededor de sus axones. Las vainas están formadas por células gliales : oligodendrocitos en el sistema nervioso central y células de Schwann en el sistema nervioso periférico. La vaina permite que los potenciales de acción viajen más rápido que en axones no mielinizados del mismo diámetro, mientras que utilizan menos energía. La vaina de mielina en los nervios periféricos normalmente corre a lo largo del axón en secciones de aproximadamente 1 mm de largo, puntuadas por nódulos de Ranvier sin vaina , que contienen una alta densidad de canales iónicos dependientes de voltaje. La esclerosis múltiple es un trastorno neurológico que resulta de la desmielinización de los axones en el sistema nervioso central.
Algunas neuronas no generan potenciales de acción, sino una señal eléctrica gradual que, a su vez, provoca una liberación gradual de neurotransmisores. Estas neuronas que no producen picos tienden a ser neuronas sensoriales o interneuronas, porque no pueden transportar señales a largas distancias.
La codificación neuronal se ocupa de la forma en que las neuronas representan la información sensorial y de otro tipo en el cerebro. El objetivo principal del estudio de la codificación neuronal es caracterizar la relación entre el estímulo y las respuestas neuronales individuales o del conjunto , así como las relaciones entre las actividades eléctricas de las neuronas dentro del conjunto. [43] Se cree que las neuronas pueden codificar tanto información digital como analógica . [44]

The conduction of nerve impulses is an example of an all-or-none response. In other words, if a neuron responds at all, then it must respond completely. Greater intensity of stimulation, like brighter image/louder sound, does not produce a stronger signal but can increase firing frequency.[45]: 31 Receptors respond in different ways to stimuli. Slowly adapting or tonic receptors respond to a steady stimulus and produce a steady rate of firing. Tonic receptors most often respond to increased stimulus intensity by increasing their firing frequency, usually as a power function of stimulus plotted against impulses per second. This can be likened to an intrinsic property of light where greater intensity of a specific frequency (color) requires more photons, as the photons can not become "stronger" for a specific frequency.
Other receptor types include quickly adapting or phasic receptors, where firing decreases or stops with a steady stimulus; examples include skin which, when touched causes neurons to fire, but if the object maintains even pressure, the neurons stop firing. The neurons of the skin and muscles that are responsive to pressure and vibration have filtering accessory structures that aid their function.
The pacinian corpuscle is one such structure. It has concentric layers like an onion, which form around the axon terminal. When pressure is applied and the corpuscle is deformed, mechanical stimulus is transferred to the axon, which fires. If the pressure is steady, the stimulus ends; thus, these neurons typically respond with a transient depolarization during the initial deformation and again when the pressure is removed, which causes the corpuscle to change shape again. Other types of adaptation are important in extending the function of a number of other neurons.[46]
The German anatomist Heinrich Wilhelm Waldeyer introduced the term neuron in 1891,[47] based on the ancient Greek νεῦρον neuron 'sinew, cord, nerve'.[48]
The word was adopted in French with the spelling neurone. That spelling was also used by many writers in English,[49] but has now become rare in American usage and uncommon in British usage.[50][48]


The neuron's place as the primary functional unit of the nervous system was first recognized in the late 19th century through the work of the Spanish anatomist Santiago Ramón y Cajal.[51]
To make the structure of individual neurons visible, Ramón y Cajal improved a silver staining process that had been developed by Camillo Golgi.[51] The improved process involves a technique called "double impregnation" and is still in use.
In 1888 Ramón y Cajal published a paper about the bird cerebellum. In this paper, he stated that he could not find evidence for anastomosis between axons and dendrites and called each nervous element "an absolutely autonomous canton."[51][47] This became known as the neuron doctrine, one of the central tenets of modern neuroscience.[51]
In 1891, the German anatomist Heinrich Wilhelm Waldeyer wrote a highly influential review of the neuron doctrine in which he introduced the term neuron to describe the anatomical and physiological unit of the nervous system.[52][53]
The silver impregnation stains are a useful method for neuroanatomical investigations because, for reasons unknown, it stains only a small percentage of cells in a tissue, exposing the complete micro structure of individual neurons without much overlap from other cells.[54]

The neuron doctrine is the now fundamental idea that neurons are the basic structural and functional units of the nervous system. The theory was put forward by Santiago Ramón y Cajal in the late 19th century. It held that neurons are discrete cells (not connected in a meshwork), acting as metabolically distinct units.
Later discoveries yielded refinements to the doctrine. For example, glial cells, which are non-neuronal, play an essential role in information processing.[55] Also, electrical synapses are more common than previously thought,[56] comprising direct, cytoplasmic connections between neurons. In fact, neurons can form even tighter couplings: the squid giant axon arises from the fusion of multiple axons.[57]
Ramón y Cajal also postulated the Law of Dynamic Polarization, which states that a neuron receives signals at its dendrites and cell body and transmits them, as action potentials, along the axon in one direction: away from the cell body.[58] The Law of Dynamic Polarization has important exceptions; dendrites can serve as synaptic output sites of neurons[59] and axons can receive synaptic inputs.[60]
Although neurons are often described of as "fundamental units" of the brain, they perform internal computations. Neurons integrate input within dendrites, and this complexity is lost in models that assume neurons to be a fundamental unit. Dendritic branches can be modeled as spatial compartments, whose activity is related due to passive membrane properties, but may also be different depending on input from synapses. Compartmental modelling of dendrites is especially helpful for understanding the behavior of neurons that are too small to record with electrodes, as is the case for Drosophila melanogaster.[61]
The number of neurons in the brain varies dramatically from species to species.[62] In a human, there are an estimated 10–20 billion neurons in the cerebral cortex and 55–70 billion neurons in the cerebellum.[63] By contrast, the nematode worm Caenorhabditis elegans has just 302 neurons, making it an ideal model organism as scientists have been able to map all of its neurons. The fruit fly Drosophila melanogaster, a common subject in biological experiments, has around 100,000 neurons and exhibits many complex behaviors. Many properties of neurons, from the type of neurotransmitters used to ion channel composition, are maintained across species, allowing scientists to study processes occurring in more complex organisms in much simpler experimental systems.
Charcot–Marie–Tooth disease (CMT) is a heterogeneous inherited disorder of nerves (neuropathy) that is characterized by loss of muscle tissue and touch sensation, predominantly in the feet and legs extending to the hands and arms in advanced stages. Presently incurable, this disease is one of the most common inherited neurological disorders, affecting 36 in 100,000 people.[64]
Alzheimer's disease (AD), also known simply as Alzheimer's, is a neurodegenerative disease characterized by progressive cognitive deterioration, together with declining activities of daily living and neuropsychiatric symptoms or behavioral changes.[65] The most striking early symptom is loss of short-term memory (amnesia), which usually manifests as minor forgetfulness that becomes steadily more pronounced with illness progression, with relative preservation of older memories. As the disorder progresses, cognitive (intellectual) impairment extends to the domains of language (aphasia), skilled movements (apraxia), and recognition (agnosia), and functions such as decision-making and planning become impaired.[66][67]
Parkinson's disease (PD), also known as Parkinsons, is a degenerative disorder of the central nervous system that often impairs motor skills and speech.[68] Parkinson's disease belongs to a group of conditions called movement disorders.[69] It is characterized by muscle rigidity, tremor, a slowing of physical movement (bradykinesia), and in extreme cases, a loss of physical movement (akinesia). The primary symptoms are the results of decreased stimulation of the motor cortex by the basal ganglia, normally caused by the insufficient formation and action of dopamine, which is produced in the dopaminergic neurons of the brain. Secondary symptoms may include high level cognitive dysfunction and subtle language problems. PD is both chronic and progressive.
Myasthenia gravis is a neuromuscular disease leading to fluctuating muscle weakness and fatigability during simple activities. Weakness is typically caused by circulating antibodies that block acetylcholine receptors at the postsynaptic neuromuscular junction, inhibiting the stimulative effect of the neurotransmitter acetylcholine. Myasthenia is treated with immunosuppressants, cholinesterase inhibitors and, in selected cases, thymectomy.

Demyelination is a process characterized by the gradual loss of the myelin sheath enveloping nerve fibers. When myelin deteriorates, signal conduction along nerves can be significantly impaired or lost, and the nerve eventually withers. Demyelination may affect both central and peripheral nervous systems, contributing to various neurological disorders such as multiple sclerosis, Guillain-Barré syndrome, and chronic inflammatory demyelinating polyneuropathy. Although demyelination is often caused by an autoimmune reaction, it may also be caused by viral infections, metabolic disorders, trauma, and some medications.
Although most injury responses include a calcium influx signaling to promote resealing of severed parts, axonal injuries initially lead to acute axonal degeneration, which is the rapid separation of the proximal and distal ends, occurring within 30 minutes of injury.[70] Degeneration follows with swelling of the axolemma, and eventually leads to bead-like formation. Granular disintegration of the axonal cytoskeleton and inner organelles occurs after axolemma degradation. Early changes include accumulation of mitochondria in the paranodal regions at the site of injury. Endoplasmic reticulum degrades and mitochondria swell up and eventually disintegrate. The disintegration is dependent on ubiquitin and calpain proteases (caused by the influx of calcium ion), suggesting that axonal degeneration is an active process that produces complete fragmentation. The process takes about roughly 24 hours in the PNS and longer in the CNS. The signaling pathways leading to axolemma degeneration are unknown.
Neurons develop through the process of neurogenesis, in which neural stem cells divide to produce differentiated neurons. Once fully differentiated they are no longer capable of undergoing mitosis. Neurogenesis primarily occurs during embryonic development.
Neurons initially develop from the neural tube in the embryo. The neural tube has three layers – a ventricular zone, an intermediate zone, and a marginal zone. The ventricular zone surrounds the tube's central canal, and becomes the ependyma. Dividing cells of the ventricular zone form the intermediate zone which stretches to the outermost layer of the neural tube called the pial layer. The gray matter of the brain is derived from the intermediate zone. The extensions of the neurons in the intermediate zone make up the marginal zone that when myelinated become the brain's white matter.[71]
Differentiation of the neurons is ordered by their size. Large motor neurons are first. Smaller sensory neurons together with glial cells differentiate at birth.[71]
Adult neurogenesis can occur and studies of the age of human neurons suggest that this process occurs only for a minority of cells, and that the vast majority of neurons in the neocortex forms before birth and persists without replacement. The extent to which adult neurogenesis exists in humans, and its contribution to cognition are controversial, with conflicting reports published in 2018.[72]
The body contains a variety of stem cell types that have the capacity to differentiate into neurons. Researchers found a way to transform human skin cells into nerve cells using transdifferentiation, in which "cells are forced to adopt new identities".[73]
During neurogenesis in the mammalian brain, progenitor and stem cells progress from proliferative divisions to differentiative divisions. This progression leads to the neurons and glia that populate cortical layers. Epigenetic modifications play a key role in regulating gene expression in differentiating neural stem cells, and are critical for cell fate determination in the developing and adult mammalian brain. Epigenetic modifications include DNA cytosine methylation to form 5-methylcytosine and 5-methylcytosine demethylation.[74] These modifications are critical for cell fate determination in the developing and adult mammalian brain. DNA cytosine methylation is catalyzed by DNA methyltransferases (DNMTs). Methylcytosine demethylation is catalyzed in several stages by TET enzymes that carry out oxidative reactions (e.g. 5-methylcytosine to 5-hydroxymethylcytosine) and enzymes of the DNA base excision repair (BER) pathway.[74]
At different stages of mammalian nervous system development two DNA repair processes are employed in the repair of DNA double-strand breaks. These pathways are homologous recombinational repair used in proliferating neural precursor cells, and non-homologous end joining used mainly at later developmental stages[75]
Intercellular communication between developing neurons and microglia is also indispensable for proper neurogenesis and brain development.[76]
Peripheral axons can regrow if they are severed,[77] but one neuron cannot be functionally replaced by one of another type (Llinás' law).[23]
A bundle of nerve fibers (axons) connecting neighboring or distant nuclei of the CNS is a tract.
{{cite book}}: CS1 maint: multiple names: authors list (link)Ramon y Cajal's first paper on the Golgi stain was on the bird cerebellum, and it appeared in the Revista in 1888. He acknowledged that he found the nerve fibers to be very intricate, but stated that he could find no evidence for either axons or dendrites undergoing anastomosis and forming nets. He called each nervous element 'an absolutely autonomous canton.'
... a man who would write a highly influential review of the evidence in favor of the neuron doctrine two years later. In his paper, Waldeyer (1891), ... , wrote that nerve cells terminate freely with end arborizations and that the 'neuron' is the anatomical and physiological unit of the nervous system. The word 'neuron' was born this way.
Today, Wilhelm von Waldeyer-Hartz is remembered as the founder of the neurone theory, coining the term "neurone" to describe the cellular function unit of the nervous system and enunciating and clarifying that concept in 1891.
By transforming cells from human skin into working nerve cells, researchers may have come up with a model for nervous-system diseases and perhaps even regenerative therapies based on cell transplants. The achievement, reported online today in Nature, is the latest in a fast-moving field called transdifferentiation, in which cells are forced to adopt new identities. In the past year, researchers have converted connective tissue cells found in skin into heart cells, blood cells, and liver cells.