El melanoma es el tipo de cáncer de piel más peligroso ; se desarrolla a partir de células productoras de melanina conocidas como melanocitos . [1] Por lo general, ocurre en la piel, pero rara vez ocurre en la boca, los intestinos o los ojos ( melanoma uveal ). [1] [2] En las mujeres, los melanomas ocurren con mayor frecuencia en las piernas; mientras que en los hombres, en la espalda. [2] El melanoma se conoce frecuentemente como melanoma maligno . Sin embargo, la comunidad médica destaca que no existe un "melanoma benigno" y recomienda evitar el término "melanoma maligno" por considerarlo redundante . [7] [8] [9]
Alrededor del 25% de los melanomas se desarrollan a partir de lunares . [2] Los cambios en un lunar que pueden indicar melanoma incluyen aumento (especialmente un aumento rápido) de tamaño, bordes irregulares, cambio de color, picazón o deterioro de la piel . [1]
La causa principal del melanoma es la exposición a la luz ultravioleta (UV) en personas con niveles bajos del pigmento de la piel melanina . [2] [10] La luz ultravioleta puede provenir del sol u otras fuentes, como dispositivos de bronceado . [2] Aquellos con muchos lunares, antecedentes de familiares afectados y función inmune deficiente corren un mayor riesgo. [1] Varias afecciones genéticas raras , como el xeroderma pigmentoso , también aumentan el riesgo. [11] El diagnóstico se realiza mediante biopsia y análisis de cualquier lesión cutánea que tenga signos de ser potencialmente cancerosa. [1]
Evitar la luz ultravioleta y usar protector solar en condiciones de sol con mucha radiación ultravioleta puede prevenir el melanoma. [2] El tratamiento generalmente consiste en la extirpación mediante cirugía del melanoma y del tejido adyacente potencialmente afectado que bordea el melanoma. [1] En aquellos con cánceres un poco más grandes, se pueden examinar los ganglios linfáticos cercanos para detectar diseminación ( metástasis ). [1] La mayoría de las personas se curan si no se ha producido metástasis. [1] Para aquellos en quienes el melanoma se ha diseminado, la inmunoterapia , la terapia biológica , la radioterapia o la quimioterapia pueden mejorar la supervivencia. [1] [12] Con tratamiento, las tasas de supervivencia a cinco años en los Estados Unidos son del 99 % entre aquellos con enfermedad localizada, del 65 % cuando la enfermedad se ha diseminado a los ganglios linfáticos y del 25 % entre aquellos con diseminación a distancia. [4] La probabilidad de que el melanoma vuelva a ocurrir o se propague depende de su grosor , de la rapidez con la que se dividen las células y de si la piel que lo recubre se ha roto o no. [2]
El melanoma es el tipo de cáncer de piel más peligroso. [2] A nivel mundial, en 2012, se produjo por primera vez en 232.000 personas. [2] En 2015, 3,1 millones de personas tenían la enfermedad activa, lo que provocó 59.800 muertes. [5] [6] Australia y Nueva Zelanda tienen las tasas más altas de melanoma en el mundo. [2] También se producen tasas altas en el norte de Europa y América del Norte, mientras que es menos común en Asia, África y América Latina. [2] En los Estados Unidos, el melanoma ocurre aproximadamente 1,6 veces más a menudo en hombres que en mujeres. [13] El melanoma se ha vuelto más común desde la década de 1960 en áreas mayoritariamente pobladas por personas de ascendencia europea . [2] [11]
Los primeros signos de melanoma son cambios en la forma o el color de los lunares existentes o, en el caso del melanoma nodular , la aparición de un nuevo bulto en cualquier parte de la piel. En etapas posteriores, el lunar puede picar , ulcerarse o sangrar. Los primeros signos de melanoma se resumen en el mnemotécnico "ABCDEEFG": [14] [15]
Esta clasificación no se aplica al melanoma nodular, que tiene sus propias clasificaciones: [16]
El melanoma metastásico puede causar síntomas paraneoplásicos inespecíficos , que incluyen pérdida de apetito, náuseas , vómitos y fatiga. La metástasis (propagación) del melanoma temprano es posible, pero relativamente rara; menos de una quinta parte de los melanomas diagnosticados tempranamente se vuelven metastásicos. Las metástasis cerebrales son particularmente comunes en pacientes con melanoma metastásico. [17] También puede propagarse al hígado, los huesos, el abdomen o los ganglios linfáticos distantes. [ cita necesaria ]
Los melanomas suelen ser causados por daños en el ADN resultantes de la exposición a la luz ultravioleta del sol. La genética también juega un papel. [18] [19] El melanoma también puede ocurrir en áreas de la piel con poca exposición al sol (es decir, boca, plantas de los pies, palmas de las manos, áreas genitales). [20] Las personas con síndrome de nevo displásico , también conocido como melanoma familiar atípico de múltiples lunares, tienen un mayor riesgo de desarrollar melanoma. [21]
Tener más de 50 lunares indica que podría surgir un mayor riesgo de melanoma. Un sistema inmunológico debilitado facilita el desarrollo del cáncer debido a la capacidad debilitada del cuerpo para combatir las células cancerosas. [18]
La exposición a la radiación ultravioleta de las camas de bronceado aumenta el riesgo de melanoma. [22] La Agencia Internacional para la Investigación del Cáncer considera que las camas de bronceado son "cancerígenas para los humanos" y que las personas que comienzan a utilizar dispositivos de bronceado antes de los treinta años tienen un 75% más de probabilidades de desarrollar melanoma. [23]
Quienes trabajan en aviones también parecen tener un mayor riesgo, lo que se cree que se debe a una mayor exposición a los rayos UV. [24]
La luz UVB , que emana del sol en longitudes de onda entre 315 y 280 nm, es absorbida directamente por el ADN de las células de la piel. lo que resulta en un tipo de daño directo al ADN llamado dímeros de ciclobutano-pirimidina . Los dímeros de timina , citosina o citosina-timina se forman mediante la unión de dos bases pirimidínicas adyacentes dentro de una hebra de ADN. La luz UVA se presenta en longitudes de onda más largas que la UVB (entre 400 y 315 nm); y también puede ser absorbido directamente por el ADN de las células de la piel, pero con eficiencias más bajas: alrededor de 1/100 a 1/1000 de los rayos UVB. [25]
La exposición a la radiación (UVA y UVB) contribuye de manera importante al desarrollo del melanoma. [26] La exposición extrema ocasional al sol que produce " quemaduras solares " en áreas del cuerpo humano está causalmente relacionada con el melanoma; [27] y estas áreas de exposición sólo intermitente aparentemente explican por qué el melanoma es más común en la espalda de los hombres y en las piernas de las mujeres. El riesgo parece estar fuertemente influenciado por las condiciones socioeconómicas más que por las ocupaciones interiores versus exteriores; es más común en trabajadores profesionales y administrativos que en trabajadores no calificados. [28] [29] Otros factores son las mutaciones (o la pérdida total) de los genes supresores de tumores . El uso de tumbonas con sus rayos UVA profundamente penetrantes se ha relacionado con el desarrollo de cánceres de piel, incluido el melanoma. [30]
Los posibles elementos importantes para determinar el riesgo incluyen la intensidad y duración de la exposición al sol, la edad a la que se produce la exposición al sol y el grado de pigmentación de la piel . Las tasas de melanoma tienden a ser más altas en los países poblados por inmigrantes del norte de Europa que tienen una gran cantidad de luz solar directa e intensa a la que la piel de los colonos no está adaptada, sobre todo en Australia. La exposición durante la niñez es un factor de riesgo más importante que la exposición en la edad adulta. Esto se ve en los estudios sobre migración en Australia. [31]
Sufrir múltiples quemaduras solares graves aumenta la probabilidad de que futuras quemaduras se conviertan en melanoma debido al daño acumulativo. [18] La luz solar con alto contenido de rayos ultravioleta y las camas de bronceado son las principales fuentes de radiación ultravioleta que aumentan el riesgo de melanoma [32] y vivir cerca del ecuador aumenta la exposición a la radiación ultravioleta. [18]
Varias mutaciones raras, que a menudo son hereditarias, aumentan en gran medida la susceptibilidad al melanoma. [33] Varios genes aumentan los riesgos. Algunos genes raros tienen un riesgo relativamente alto de causar melanoma; Algunos genes más comunes, como un gen llamado MC1R que causa el cabello rojo, tienen un riesgo elevado relativamente menor. Se pueden utilizar pruebas genéticas para buscar mutaciones. [ cita necesaria ]
Una clase de mutaciones afecta al gen CDKN2A . Una mutación del marco de lectura alternativo en este gen conduce a la desestabilización de p53 , un factor de transcripción implicado en la apoptosis y en el 50% de los cánceres humanos. Otra mutación en el mismo gen da como resultado un inhibidor no funcional de CDK4 , una quinasa dependiente de ciclina que promueve la división celular . Las mutaciones que causan la afección de la piel xeroderma pigmentoso (XP) también aumentan la susceptibilidad al melanoma. Distribuidas por todo el genoma, estas mutaciones reducen la capacidad de una célula para reparar el ADN. Tanto las mutaciones CDKN2A como XP son altamente penetrantes (las posibilidades de que un portador exprese el fenotipo son altas). [ cita necesaria ]
El melanoma familiar es genéticamente heterogéneo [19] y los loci del melanoma familiar aparecen en los brazos cromosómicos 1p, 9p y 12q. Se han relacionado múltiples eventos genéticos con la patogénesis (desarrollo de la enfermedad) del melanoma. [34] El gen supresor de tumores múltiples 1 (CDKN2A/MTS1) codifica p16INK4a, una proteína de bajo peso molecular inhibidor de las proteínas quinasas dependientes de ciclina (CDK), que se ha localizado en la región p21 del cromosoma 9 humano . [35] FAMMM generalmente se caracteriza por tener 50 o más lunares combinados además de antecedentes familiares de melanoma. [20] Se transmite de forma autosómica dominante y se asocia principalmente con las mutaciones CDKN2A . [20] Las personas que tienen FAMMM asociada a la mutación CDKN2A tienen un riesgo 38 veces mayor de cáncer de páncreas. [36]
Otras mutaciones confieren un riesgo menor, pero son más comunes en la población. Las personas con mutaciones en el gen MC1R tienen de dos a cuatro veces más probabilidades de desarrollar melanoma que aquellas con dos copias de tipo salvaje (el tipo típico no afectado). Las mutaciones de MC1R son muy comunes y todas las personas pelirrojas tienen una copia mutada. [ cita necesaria ] La mutación del gen MDM2 SNP309 se asocia con mayores riesgos para las mujeres más jóvenes. [37]
Las personas de cabello rubio y pelirrojo, las personas con múltiples nevos atípicos o displásicos y las personas nacidas con nevos melanocíticos congénitos gigantes tienen un mayor riesgo. [38]
Los antecedentes familiares de melanoma aumentan en gran medida el riesgo de una persona, porque se han encontrado mutaciones en varios genes en familias propensas al melanoma. [39] [18] Las personas con antecedentes de un melanoma tienen un mayor riesgo de desarrollar un segundo tumor primario. [40]
La piel clara es el resultado de tener menos melanina en la piel, lo que significa que existe menos protección contra la radiación ultravioleta. [18]


La etapa más temprana del melanoma comienza cuando los melanocitos comienzan a crecer descontroladamente. Los melanocitos se encuentran entre la capa externa de la piel (la epidermis ) y la siguiente capa (la dermis ). Esta etapa temprana de la enfermedad se llama fase de crecimiento radial, cuando el tumor tiene menos de 1 mm de espesor y se disemina al nivel de la epidermis basal. [41] Debido a que las células cancerosas aún no han llegado a los vasos sanguíneos más profundos de la piel, es muy poco probable que este melanoma en etapa temprana se propague a otras partes del cuerpo. Si el melanoma se detecta en esta etapa, generalmente se puede extirpar por completo mediante cirugía. [ cita necesaria ]
Cuando las células tumorales comienzan a moverse en una dirección diferente (verticalmente hacia la epidermis y hacia la dermis papilar ), el comportamiento celular cambia drásticamente. [42]
El siguiente paso en la evolución es la fase de crecimiento radial invasivo, en la que las células individuales comienzan a adquirir potencial invasivo. A partir de este momento, el melanoma es capaz de propagarse. [ cita necesaria ] La profundidad de la lesión de Breslow suele ser inferior a 1 mm (0,04 pulgadas ), mientras que el nivel de Clark suele ser 2.
La siguiente fase de crecimiento vertical (VGP) es el melanoma invasivo. El tumor puede crecer hacia el tejido circundante y diseminarse por todo el cuerpo a través de los vasos sanguíneos o linfáticos . El grosor del tumor suele ser de más de 1 mm (0,04 pulgadas ) y el tumor afecta las partes más profundas de la dermis.
El huésped provoca una reacción inmunológica contra el tumor durante el VGP, [43] que se juzga por la presencia y actividad de los linfocitos infiltrantes del tumor (TIL). En ocasiones, estas células destruyen por completo el tumor primario; esto se llama regresión, que es la última etapa del desarrollo. En determinados casos, el tumor primario se destruye por completo y sólo se descubre el tumor metastásico. Aproximadamente el 40% de los melanomas humanos contienen mutaciones activadoras que afectan la estructura de la proteína B-Raf , lo que da como resultado una señalización constitutiva a través de la vía Raf a MAP quinasa . [44]
Una causa común a la mayoría de los cánceres es el daño al ADN. [45] La luz UVA provoca principalmente dímeros de timina . [46] Los rayos UVA también producen especies reactivas de oxígeno y éstas causan otros daños al ADN, principalmente roturas de una sola hebra, pirimidinas oxidadas y la purina oxidada 8-oxoguanina (un cambio mutagénico del ADN) en 1/10, 1/10 y 1/3. las frecuencias de los dímeros de timina inducidos por UVA, respectivamente.
Si no se reparan, los fotoproductos del dímero de ciclobutano-pirimidina (CPD) pueden provocar mutaciones mediante una síntesis de translesión inexacta durante la replicación o reparación del ADN. Las mutaciones más frecuentes debidas a una síntesis inexacta de las CPD pasadas son las mutaciones de transición de citosina a timina (C>T) o CC>TT . Estas se conocen comúnmente como mutaciones de huellas dactilares UV, ya que son la mutación más específica causada por los rayos UV y se encuentran con frecuencia en la piel expuesta al sol, pero rara vez en los órganos internos. [47] Los errores en la reparación del ADN de los fotoproductos UV, o la síntesis inexacta de estos fotoproductos, también pueden provocar deleciones, inserciones y translocaciones cromosómicas .
Se secuenciaron los genomas completos de 25 melanomas. [48] En promedio, se encontraron alrededor de 80 000 bases mutadas (principalmente transiciones C>T) y alrededor de 100 reordenamientos estructurales por genoma de melanoma. Esto es mucho más alto que las aproximadamente 70 mutaciones entre generaciones (de padres a hijos). [49] [50] Entre los 25 melanomas, alrededor de 6000 genes codificadores de proteínas tenían mutaciones sin sentido , sin sentido o en el sitio de empalme . También se han secuenciado y analizado los transcriptomas de más de 100 melanomas. Casi el 70% de todos los genes codificadores de proteínas humanas se expresan en el melanoma. La mayoría de estos genes también se expresan en otros tejidos normales y cancerosos, y unos 200 genes muestran un patrón de expresión más específico en el melanoma en comparación con otras formas de cáncer. Ejemplos de genes específicos del melanoma son la tirosinasa , MLANA y PMEL . [51] [52]
La radiación ultravioleta causa daños al ADN de las células, típicamente dimerización de timina, que cuando no se repara puede crear mutaciones en los genes de las células. Este fuerte factor mutagénico convierte al melanoma cutáneo en el tipo de tumor con mayor número de mutaciones. [53] Cuando la célula se divide , estas mutaciones se propagan a nuevas generaciones de células. Si las mutaciones ocurren en protooncogenes o genes supresores de tumores , la tasa de mitosis en las células portadoras de mutaciones puede descontrolarse, lo que lleva a la formación de un tumor . Los datos de pacientes sugieren que los niveles aberrantes del factor de transcripción activador en el núcleo de las células de melanoma se asocian con una mayor actividad metastásica de las células de melanoma; [54] [55] [56] Los estudios realizados en ratones sobre el cáncer de piel tienden a confirmar la función de la activación del factor de transcripción 2 en la progresión del cáncer. [57] [58]
Las células madre cancerosas también pueden estar involucradas. [59]
Estudios a gran escala, como The Cancer Genome Atlas , han caracterizado alteraciones somáticas recurrentes que probablemente impulsan el inicio y el desarrollo del melanoma cutáneo. El estudio Cancer Genome Atlas ha establecido cuatro subtipos: mutante BRAF , mutante RAS , mutante NF1 y triple de tipo salvaje. [60]
La mutación más frecuente se produce en el codón 600 de BRAF (50% de los casos). BRAF normalmente participa en el crecimiento celular y esta mutación específica hace que la proteína sea constitutivamente activa e independiente de la regulación fisiológica normal, fomentando así el crecimiento tumoral. [61] Los genes RAS ( NRAS , HRAS y KRAS ) también sufren mutaciones recurrentes (30 % de los casos de TCGA) y las mutaciones en los codones 61 o 12 desencadenan actividad oncogénica. Las mutaciones de pérdida de función a menudo afectan a genes supresores de tumores como NF1 , TP53 y CDKN2A . Otras alteraciones oncogénicas incluyen fusiones que involucran varias quinasas como BRAF, [62] RAF1, [63] ALK, RET, ROS1, NTRK1., [64] NTRK3 [65] y MET [66] BRAF, RAS y NF1 , y mutaciones de quinasa. Las fusiones son notablemente excluyentes entre sí, ya que ocurren en diferentes subconjuntos de pacientes. Por lo tanto, la evaluación del estado de la mutación puede mejorar la estratificación de los pacientes e informar la terapia dirigida con inhibidores específicos. [ cita necesaria ]
En algunos casos (3 a 7%), las versiones mutadas de BRAF y NRAS se someten a una amplificación del número de copias . [60]
La investigación realizada por el equipo de Sarna demostró que las células de melanoma muy pigmentadas tienen un módulo de Young de aproximadamente 4,93, mientras que en las no pigmentadas es sólo de 0,98. [67] En otro experimento descubrieron que la elasticidad de las células del melanoma es importante para su metástasis y crecimiento: los tumores no pigmentados eran más grandes que los pigmentados y les resultaba mucho más fácil propagarse. Demostraron que en los tumores de melanoma hay células pigmentadas y no pigmentadas , por lo que pueden ser tanto resistentes a los medicamentos como metastásicos. [67]


Mirar o inspeccionar visualmente el área en cuestión es el método más común para sospechar un melanoma. [68] Los lunares que son irregulares en color o forma generalmente se tratan como candidatos. Para detectar melanomas (y aumentar las tasas de supervivencia), se recomienda aprender a reconocerlos (ver mnemotécnico "ABCDE"), examinar periódicamente los lunares en busca de cambios (forma, tamaño, color, picazón o sangrado) y consultar a un médico calificado cuando Aparece un candidato. [69] [70] La inspección en persona de lesiones cutáneas sospechosas es más precisa que la inspección visual de imágenes de lesiones cutáneas sospechosas. [71] Cuando la utilizan especialistas capacitados, la dermatoscopia es más útil para identificar lesiones malignas que el uso solo a simple vista. [72] La microscopía confocal de reflectancia puede tener mejor sensibilidad y especificidad que la dermatoscopia en el diagnóstico del melanoma cutáneo, pero se necesitan más estudios para confirmar este resultado. [73]
Sin embargo, muchos melanomas se presentan como lesiones de menos de 6 mm de diámetro y todos los melanomas son malignos cuando aparecen por primera vez como un pequeño punto. Los médicos suelen examinar todos los lunares, incluidos los de menos de 6 mm de diámetro. La queratosis seborreica puede cumplir algunos o todos los criterios ABCD y puede dar lugar a falsas alarmas . Los médicos generalmente pueden distinguir la queratosis seborreica del melanoma mediante un examen o con dermatoscopia . [ cita necesaria ]
Algunos abogan por sustituir "agrandar" por "evolucionar": los lunares que cambian y evolucionan son motivo de preocupación. Alternativamente, algunos profesionales prefieren la "elevación". La elevación puede ayudar a identificar un melanoma, pero la falta de elevación no significa que la lesión no sea un melanoma. La mayoría de los melanomas en los EE. UU. se detectan antes de que se eleven. Cuando la elevación es visible, es posible que hayan progresado a la etapa invasiva más peligrosa. [ cita necesaria ]
Un método es el " signo del patito feo ". [74] Se realiza una correlación de las características comunes de las lesiones. Las lesiones que se desvían de las características comunes se denominan "patito feo" y se requiere un examen profesional adicional. El signo de " Caperucita Roja " [74] sugiere que las personas con piel clara y cabello de color claro pueden tener melanomas amelanóticos difíciles de diagnosticar . Se requiere especial cuidado al examinar a estas personas, ya que pueden tener múltiples melanomas y nevos gravemente displásicos. Se debe utilizar un dermatoscopio para detectar "patitos feos", ya que muchos melanomas en estos individuos se parecen a los no melanomas o se consideran " lobos con piel de oveja ". [75] Estas personas de piel clara a menudo tienen melanomas ligeramente pigmentados o amelanóticos que no presentan cambios ni variaciones de color fáciles de observar. Sus bordes suelen ser confusos, lo que complica la identificación visual sin un dermatoscopio.
Los melanomas amelanóticos y los melanomas que surgen en personas de piel clara son muy difíciles de detectar, ya que no muestran muchas de las características de la regla ABCD, rompen el signo del "patito feo" y son difíciles de distinguir de las cicatrices del acné, las picaduras de insectos, dermatofibromas o lentigos .
Después de un examen visual y un examen dermatoscópico, [75] o herramientas de diagnóstico in vivo como un microscopio confocal, el médico puede realizar una biopsia del lunar sospechoso. A menudo se requiere una biopsia de piel realizada bajo anestesia local para ayudar a realizar o confirmar el diagnóstico y definir la gravedad. Las biopsias por escisión elíptica pueden extirpar el tumor, seguidas de un análisis histológico y una puntuación de Breslow. Las biopsias incisionales, como las biopsias por punción, suelen estar contraindicadas en casos sospechosos de melanoma, debido a la posibilidad de un error de muestreo [76] o de una implantación local que provoque una estimación errónea del espesor del tumor. [77] [78] Sin embargo, los temores de que tales biopsias puedan aumentar el riesgo de enfermedad metastásica parecen infundados. [79] [80]
La fotografía de cuerpo total, que implica documentación fotográfica de la mayor superficie corporal posible, se utiliza a menudo durante el seguimiento de pacientes de alto riesgo. Se ha informado que la técnica permite la detección temprana y proporciona un enfoque rentable (con cualquier cámara digital), pero se ha cuestionado su eficacia debido a su incapacidad para detectar cambios macroscópicos. [68] El método de diagnóstico debe usarse junto con (y no como reemplazo) las imágenes dermatoscópicas, ya que una combinación de ambos métodos parece brindar tasas de detección extremadamente altas.
El melanoma es un tipo de neoplasia neuroectodérmica . [81] Hay cuatro tipos principales de melanoma: [82]
Otros tipos histopatológicos son:

Un melanoma in situ no ha invadido más allá de la membrana basal , mientras que un melanoma invasivo se ha extendido más allá de ella.
Algunos tipos histopatológicos de melanoma son inherentemente invasivos, incluido el melanoma nodular y el melanoma lentigo maligno , donde la contraparte in situ del melanoma lentigo maligno es el lentigo maligno . [85] El lentigo maligno a veces se clasifica como un melanoma muy temprano, [86] y a veces como un precursor del melanoma. [87]
Los melanomas de extensión superficial y los melanomas lentiginosos acros pueden ser in situ o invasivos, [88] pero los melanomas lentiginosos acros casi siempre son invasivos. [89]
Más contexto sobre la estadificación del cáncer está disponible en TNM .

Los melanomas metastásicos se pueden detectar mediante radiografías, tomografías computarizadas, resonancias magnéticas, PET y PET/CT, ultrasonido, pruebas de LDH y detección fotoacústica. [90] Sin embargo, falta evidencia sobre la precisión de la estadificación de las personas con melanoma con diversos métodos de imagen. [91]
Estadios del melanoma según AJCC , 8.ª edición: [92]
Las etapas 1 y 2 requieren una clase N (ganglio linfático) de:
Las etapas 1, 2 y 3 requieren una M (estado de metástasis) de:
Los sistemas más antiguos incluyen el " nivel de Clark " y la " profundidad de Breslow ", que cuantifican la profundidad microscópica de la invasión tumoral.

Las pruebas de lactato deshidrogenasa (LDH) se utilizan a menudo para detectar metástasis , aunque muchos pacientes con metástasis (incluso en etapa terminal) tienen una LDH normal; Una LDH extraordinariamente alta a menudo indica la diseminación metastásica de la enfermedad al hígado.
Es común que a los pacientes diagnosticados con melanoma se les realicen radiografías de tórax y una prueba de LDH y, en algunos casos, tomografías computarizadas , resonancias magnéticas y/o PET . Aunque es controvertido, las biopsias del ganglio linfático centinela y el examen de los ganglios linfáticos también se realizan en pacientes para evaluar la diseminación a los ganglios linfáticos. El diagnóstico de melanoma está respaldado por la presencia del marcador de proteína S-100 .
HMB-45 es un anticuerpo monoclonal que reacciona contra un antígeno presente en tumores melanocíticos como los melanomas. Se utiliza en patología anatómica como marcador de este tipo de tumores. El anticuerpo se generó contra un extracto de melanoma. Reacciona positivamente contra los tumores melanocíticos pero no contra otros tumores, demostrando así especificidad y sensibilidad. El anticuerpo también reacciona positivamente contra las células del nevo de unión, pero no contra los nevos intradérmicos, y contra los melanocitos fetales, pero no contra los melanocitos adultos normales.
El HMB-45 no reacciona con casi todas las neoplasias malignas humanas no melanomas, con la excepción de tumores raros que muestran evidencia de melanogénesis (p. ej., schwannoma pigmentado, sarcoma de células claras) o tumores asociados con el complejo de esclerosis tuberosa (angiomiolipoma y linfangiomioma).
No hay evidencia que apoye o rechace la detección de melanoma en la población adulta. [93]
Minimizar la exposición a fuentes de radiación ultravioleta (el sol y las tumbonas), [94] seguir medidas de protección solar y usar ropa protectora (camisas de manga larga, pantalones largos y sombreros de ala ancha) puede ofrecer protección.
Alguna vez se creyó que el uso de luz artificial para broncearse ayudaba a prevenir el cáncer de piel, pero en realidad puede provocar una mayor incidencia de melanomas. [95]
Las lámparas de uñas UV, que se utilizan en los salones de uñas para secar el esmalte de uñas, son otra fuente común y generalizada de radiación UV que podría evitarse. [96] [97] Aunque el riesgo de desarrollar cáncer de piel mediante el uso de lámparas de uñas UV es bajo, todavía se recomienda usar guantes sin dedos y/o aplicar protector solar SPF 30 o mayor en las manos antes de usar una lámpara de uñas UV. [96] [97]
El cuerpo utiliza la luz ultravioleta para generar vitamina D, por lo que es necesario equilibrar la cantidad de luz solar necesaria para mantener niveles saludables de vitamina D y reducir el riesgo de melanoma; El cuerpo necesita alrededor de media hora de luz solar para generar la vitamina D del día y esto es aproximadamente el mismo tiempo que les toma a las personas de piel clara sufrir una quemadura solar. La exposición a la luz solar puede ser intermitente en lugar de toda al mismo tiempo. [98]
El protector solar parece ser eficaz para prevenir el melanoma. [2] [10] En el pasado, se recomendaba el uso de protectores solares con un factor de protección solar (SPF) de 50 o más en las áreas expuestas; ya que los protectores solares más antiguos bloqueaban más eficazmente los rayos UVA con un SPF más alto. [99] Actualmente, los ingredientes de protección solar más nuevos ( avobenzona , óxido de zinc y dióxido de titanio ) bloquean eficazmente tanto los rayos UVA como los UVB incluso con SPF más bajos. El protector solar también protege contra el carcinoma de células escamosas , otro cáncer de piel. [100]
Han surgido preocupaciones de que el protector solar pueda crear una falsa sensación de seguridad contra el daño solar. [101]
Una revisión de 2005 encontró evidencia provisional de que las estatinas y los fibratos pueden disminuir el riesgo de melanoma. [102] Sin embargo, una revisión de 2006 no respaldó ningún beneficio. [103]

La confirmación del diagnóstico clínico se realiza con una biopsia de piel . Por lo general, a esto le sigue una escisión más amplia de la cicatriz o el tumor. Dependiendo del estadio, se puede realizar una biopsia del ganglio linfático centinela . Existe controversia en torno a la evidencia de los ensayos sobre la biopsia del ganglio linfático centinela; [104] con evidencia poco clara de beneficio a partir de 2015. [105] El tratamiento del melanoma avanzado se realiza desde un enfoque multidisciplinario.
Las biopsias por escisión pueden extirpar el tumor, pero a menudo es necesaria una cirugía adicional para reducir el riesgo de recurrencia. La escisión quirúrgica completa con márgenes quirúrgicos adecuados y la evaluación de la presencia de enfermedad metastásica detectable junto con el seguimiento a corto y largo plazo es el estándar. A menudo, esto se realiza mediante una escisión local amplia (WLE) con márgenes de 1 a 2 cm (0,4 a 0,8 pulgadas). El melanoma in situ y el lentigo maligno se tratan con márgenes quirúrgicos más estrechos, generalmente de 0,2 a 0,5 cm (0,1 a 0,2 pulgadas). Muchos cirujanos consideran que 0,5 cm (0,2 pulgadas) es el estándar de atención para la escisión estándar de melanoma in situ, [106] pero un margen de 0,2 cm (0,1 pulgadas) podría ser aceptable para la cirugía de margen controlado ( cirugía de Mohs o cirugía de doble hoja). técnica con control de márgenes). La escisión amplia tiene como objetivo reducir la tasa de recurrencia del tumor en el sitio de la lesión original. Este es un patrón común de fracaso del tratamiento en el melanoma. Se han realizado considerables investigaciones para dilucidar los márgenes apropiados para la escisión con una tendencia general hacia un tratamiento menos agresivo durante las últimas décadas. [107] Un metanálisis de ensayos controlados aleatorios realizado en 2009 encontró una pequeña diferencia en las tasas de supervivencia a favor de la escisión amplia de melanomas cutáneos primarios, pero estos resultados no fueron estadísticamente significativos. [108]
Se ha informado que la cirugía de Mohs tiene una tasa de curación de tan solo el 77% [109] y de hasta el 98,0% para el melanoma in situ. [110] CCPDMA y la cirugía controlada de márgenes periféricos con "doble bisturí" son equivalentes a la cirugía de Mohs en efectividad en este tipo "intraepitelial" de melanoma.
Los melanomas que se diseminan generalmente lo hacen a los ganglios linfáticos en el área del tumor antes de diseminarse a otros lugares. Los intentos de mejorar la supervivencia mediante la extirpación quirúrgica de los ganglios linfáticos ( linfadenectomía ) se asociaron con muchas complicaciones, pero ningún beneficio en la supervivencia general. Recientemente, se ha desarrollado la técnica de biopsia del ganglio linfático centinela para reducir las complicaciones de la cirugía de ganglio linfático y al mismo tiempo permitir evaluar la afectación de los ganglios con tumor. [111]
La biopsia del ganglio centinela es un procedimiento muy utilizado en el tratamiento del melanoma cutáneo. [112] [113]
No se deben realizar biopsias del ganglio linfático centinela ni otras pruebas de diagnóstico para evaluar el melanoma delgado y temprano, incluido el melanoma in situ, el melanoma T1a o el melanoma T1b ≤ 0,5 mm. [114] Es poco probable que las personas con estas afecciones tengan el cáncer diseminado a los ganglios linfáticos o a cualquier otro lugar y tienen una tasa de supervivencia a 5 años del 97 %. [114] Debido a estas consideraciones, la biopsia del ganglio linfático centinela se considera un cuidado de salud innecesario para ellos. [114] Además, los análisis de sangre basales y los estudios radiográficos no deben realizarse únicamente en función de la identificación de este tipo de melanoma, ya que existen pruebas más precisas para detectar el cáncer y estas pruebas tienen altas tasas de falsos positivos. [114] Para corregir potencialmente los falsos positivos, se pueden utilizar perfiles de expresión génica como prueba auxiliar para lesiones pequeñas y ambiguas. [115] [116]
A menudo se realiza una biopsia del ganglio linfático centinela, especialmente en tumores T1b/T2+, tumores de mucosas, melanoma ocular y tumores de las extremidades. [ cita necesaria ] Se realiza un proceso llamado linfogammagrafía en el que se inyecta un marcador radiactivo en el sitio del tumor para localizar los ganglios centinela. Se proporciona mayor precisión utilizando un tinte trazador azul y se realiza una cirugía para realizar una biopsia de los ganglios. La tinción de rutina con hematoxilina y eosina (H&E) y con inmunoperoxidasa será adecuada para descartar la afectación ganglionar. Las pruebas de reacción en cadena de la polimerasa (PCR) en los ganglios, generalmente realizadas para probar el ingreso a ensayos clínicos, ahora demuestran que muchos pacientes con un ganglio linfático centinela negativo en realidad tenían una pequeña cantidad de células positivas en sus ganglios. Como alternativa, se puede realizar una biopsia por aspiración con aguja fina , que a menudo se utiliza para analizar masas.
Si un ganglio linfático es positivo, dependiendo del grado de diseminación de los ganglios linfáticos, a menudo se realizará una disección radical de los ganglios linfáticos. Si la enfermedad se reseca completamente, se considerará al paciente para terapia adyuvante. La biopsia de piel por escisión es el tratamiento de elección. Aquí, la lesión sospechosa se elimina por completo con una elipse adecuada (pero mínima, generalmente de 1 o 2 mm) de la piel y el tejido circundantes. [117] Para evitar la interrupción del drenaje linfático local, el margen quirúrgico preferido para la biopsia inicial debe ser estrecho (1 mm). La biopsia debe incluir las capas epidérmica, dérmica y subcutánea de la piel. Esto permite al histopatólogo determinar el grosor del melanoma mediante examen microscópico. Esto se describe mediante el espesor de Breslow (medido en milímetros). Sin embargo, para lesiones grandes, como la sospecha de lentigo maligno, o para lesiones en áreas quirúrgicamente difíciles (cara, dedos de los pies, manos, párpados), una pequeña biopsia por punción en áreas representativas brindará información adecuada y no alterará la estadificación final ni la determinación de la profundidad. . En ninguna circunstancia la biopsia inicial debe incluir el margen quirúrgico final (0,5 cm, 1,0 cm o 2 cm), ya que un diagnóstico erróneo puede provocar cicatrices excesivas y morbilidad por el procedimiento. Una escisión inicial grande interrumpirá el drenaje linfático local y puede afectar una mayor disección de los ganglios linfáticos dirigida por linfangiografía. Se puede utilizar una biopsia por punción pequeña en cualquier momento en el que, por motivos logísticos y personales, un paciente rechace una biopsia por escisión más invasiva. Las biopsias con punción pequeña son mínimamente invasivas y sanan rápidamente, generalmente sin dejar cicatrices perceptibles.
El tratamiento adyuvante después de la cirugía puede reducir el riesgo de recurrencia después de la cirugía, especialmente en melanomas de alto riesgo. Las rutinas varían en diferentes países, pero hoy (2024) el tratamiento adyuvante más común es el tratamiento con inhibidores de puntos de control inmunológico durante hasta un año después de la cirugía. [118]
A principios de la década de 2000, una estrategia relativamente común era tratar a los pacientes con alto riesgo de recurrencia con hasta un año de tratamiento con altas dosis de interferón , que tiene efectos secundarios graves, pero puede mejorar ligeramente el pronóstico del paciente. [119] Un metanálisis realizado en 2013 sugirió que la adición de interferón alfa aumentaba la supervivencia general y libre de enfermedad en personas con melanoma cutáneo en estadio II-III TNM del AJCC. [120] Un metanálisis realizado en 2011 demostró que el interferón podría alargar el tiempo antes de que reaparezca un melanoma, pero aumentó la supervivencia en solo un 3 % a los 5 años. Los efectos secundarios desagradables también disminuyen considerablemente la calidad de vida. [121] En la Unión Europea, el interferón generalmente no se utiliza fuera del alcance de los ensayos clínicos. [122] [123]
Los fármacos de quimioterapia como la dacarbazina han sido la columna vertebral del tratamiento del melanoma metastásico desde la aprobación de la FDA en 1975; sin embargo, su eficacia en términos de supervivencia nunca ha sido demostrada en un ECA . [124] Desde la aprobación de los inhibidores de puntos de control inmunológico, la dacarbazina y su contraparte oral, la temozolomida, constituyen posibles opciones de tratamiento en líneas de terapia posteriores. [125]
Hay múltiples medicamentos disponibles para los pacientes para disminuir el tamaño del tumor. Al disminuir el tamaño del tumor, se pueden aliviar algunos síntomas; sin embargo, esto no conduce necesariamente a la remisión. Algunos de estos medicamentos son dacarbazina , temozolomida y fotemustina . También se utilizan combinaciones de fármacos y, en algunos casos, presentan tasas de remisión más altas. Estas combinaciones de medicamentos pueden tener efectos secundarios dañinos. Para mantener la calidad de vida, los pacientes requieren tratamientos de asistencia y observación. Aunque las combinaciones de fármacos aumentan las tasas de remisión, la tasa de supervivencia no muestra un aumento. [126]
En personas con sarcomas y neoplasias malignas cutáneas localmente avanzadas, se ha descubierto que la infusión aislada de extremidades (ILI) es un procedimiento mínimamente invasivo y bien tolerado para administrar quimioterapia regional. [127] [128]
Las células de melanoma tienen mutaciones que les permiten sobrevivir y crecer indefinidamente en el cuerpo. [124] Las terapias dirigidas a moléculas pequeñas funcionan bloqueando los genes implicados en las vías de proliferación y supervivencia de tumores. [124] Los principales tratamientos son los inhibidores de BRAF, C-Kit y NRAS . [129] Estos inhibidores actúan para inhibir las vías posteriores implicadas en la proliferación celular y el desarrollo de tumores debido a mutaciones genéticas específicas. [130] Las personas pueden ser tratadas con inhibidores dirigidos a moléculas pequeñas si dan positivo para la mutación específica. [124] Los inhibidores de BRAF , como vemurafenib y dabrafenib , y un inhibidor de MEK, trametinib, son los tratamientos aprobados más eficaces para el melanoma BRAF positivo. [131] [124] Los tumores de melanoma pueden desarrollar resistencia durante la terapia, lo que puede hacer que la terapia ya no sea efectiva, pero la combinación del uso de inhibidores de BRAF y MEK puede crear una respuesta rápida y duradera a la terapia del melanoma. [132]
Varios tratamientos mejoran la supervivencia con respecto a la quimioterapia tradicional. [124] La bioquimioterapia (quimioterapia con citocinas IL-2 e IFN-α) combinada con inhibidores de BRAF mejoró la supervivencia de las personas con melanoma positivo para BRAF. [124] La bioquimioterapia por sí sola no mejoró la supervivencia general y tuvo una mayor toxicidad que la quimioterapia. [124] La combinación de múltiples agentes de quimioterapia (poliquimioterapia) no mejoró la supervivencia en comparación con la monoquimioterapia. [124] Las terapias dirigidas dan como resultado tiempos de supervivencia libre de progresión (SSP) relativamente cortos. La combinación terapéutica de dabrafenib y trametinib tiene una SSP a 3 años del 23 % y una SSP a 5 años del 13 %. [133]
Lifileucel (Amtagvi) es una inmunoterapia de células T autólogas derivada de tumores que fue aprobada para uso médico en los Estados Unidos en febrero de 2024. [134] [135]
La inmunoterapia tiene como objetivo estimular el sistema inmunológico de la persona contra el tumor, mejorando la capacidad del propio cuerpo para reconocer y destruir las células cancerosas. [136] El enfoque actual para el tratamiento del melanoma con inmunoterapia incluye tres categorías amplias de tratamientos que incluyen citoquinas , inhibidores de puntos de control inmunológico y transferencia de células adoptivas . [136] Estas opciones de tratamiento se utilizan con mayor frecuencia en personas con melanoma metastásico y mejoran significativamente la supervivencia general. [124] Sin embargo, estos tratamientos suelen ser costosos. Por ejemplo, un tratamiento con inhibidores de puntos de control inmunológico, pembrolizumab , cuesta entre 10.000 y 12.000 dólares por una dosis única administrada cada 3 semanas. [137]
Las terapias con citocinas utilizadas para el melanoma incluyen IFN-a e IL-2 . [138] IL-2 ( Proleukin ) fue la primera terapia nueva aprobada (1990 UE, 1992 EE. UU.) para el tratamiento del melanoma metastásico en 20 años. [139] La IL-2 puede ofrecer la posibilidad de una remisión completa y duradera de esta enfermedad en un pequeño porcentaje de personas con melanoma. [140] La IL-2 intralesional para metástasis en tránsito tiene una alta tasa de respuesta completa que oscila entre 40 y 100 %. [131] De manera similar, el IFN-a ha mostrado solo beneficios de supervivencia modestos y alta toxicidad, lo que limita su uso como terapia independiente. [124] [138]
Los inhibidores de los puntos de control inmunológico incluyen anticuerpos monoclonales anti- CTLA-4 ( ipilimumab y tremelimumab ), agonistas del receptor tipo peaje (TLR), agonistas de CD40 , anticuerpos anti- PD-1 ( pembrolizumab , pidilizumab y nivolumab ) y anticuerpos PD-L1 . [136] [138] La evidencia sugiere que los anticuerpos anti- PD-1 son más efectivos que los anticuerpos anti-CTLA4 con menos toxicidad sistémica. [124] La supervivencia libre de progresión a cinco años para la inmunoterapia con pembrolizumab es del 21 %. [133] Un enfoque terapéutico que incluye la combinación de diferentes terapias mejora la supervivencia general y la supervivencia libre de progresión en comparación con el tratamiento con medicamentos de inmunoterapia separados solos. [124]
Las investigaciones en curso analizan el tratamiento mediante transferencia adoptiva de células . [141] La transferencia de células adoptivas se refiere a la aplicación de células T o células dendríticas modificadas y preestimuladas y actualmente se utiliza para minimizar las complicaciones de la enfermedad de injerto contra huésped . [138] [142]
La combinación nivolumab/relatlimab (Opdualag) fue aprobada para uso médico en los Estados Unidos en marzo de 2022. [143]
La mayoría de los cirujanos todavía realizan la escisión estándar. Desafortunadamente, la tasa de recurrencia es extremadamente alta (hasta el 50%). Esto se debe al margen quirúrgico visible mal definido y a la ubicación facial de las lesiones (que a menudo obligan al cirujano a utilizar un margen quirúrgico estrecho). El estrecho margen quirúrgico utilizado, combinado con la limitación de la técnica estándar de histología de tejido fijo de "holgazanía", da como resultado una alta tasa de error de "falsos negativos" y recurrencias frecuentes. El control de márgenes (márgenes periféricos) es necesario para eliminar los errores de falsos negativos. Si se utiliza pan en barra , las distancias desde las secciones deben acercarse a 0,1 mm para asegurar que el método se aproxime al control total de los márgenes. Un metanálisis de la literatura realizado en 2014 no encontró ensayos controlados aleatorios de intervenciones quirúrgicas para tratar el lentigo maligno o el melanoma in situ, a pesar de que la cirugía es el tratamiento más utilizado. [144]
La cirugía de Mohs se ha realizado con una tasa de curación de tan solo el 77% [109] y de hasta el 95% según otro autor. [110] El método de escisión controlada del margen periférico con "doble bisturí" se aproxima al método de Mohs en el control de márgenes, pero requiere un patólogo íntimamente familiarizado con la complejidad del manejo del margen vertical en las secciones periféricas delgadas y los métodos de tinción. [145]
Algunos nevos melanocíticos y melanoma in situ ( lentigo maligno ) se han resuelto con un tratamiento experimental, la crema tópica de imiquimod (Aldara), un agente que mejora el sistema inmunológico. Algunos dermatólogos combinan los dos métodos: extirpar quirúrgicamente el cáncer y luego tratar la zona con crema Aldara después de la operación durante tres meses. Si bien algunos estudios han sugerido el uso adyuvante de tazaroteno tópico, la evidencia actual es insuficiente para recomendarlo y sugiere que aumenta la inflamación tópica, lo que lleva a un menor cumplimiento por parte del paciente. [144]
La radioterapia se utiliza a menudo después de la resección quirúrgica en pacientes con melanoma local o regionalmente avanzado o en pacientes con metástasis a distancia irresecables. Para estos tratamientos se utilizan a menudo haces de rayos X de kilovoltaje que tienen la propiedad de que la dosis máxima de radiación se produce cerca de la superficie de la piel. [146] Puede reducir la tasa de recurrencia local, pero no prolonga la supervivencia. [147] Actualmente se está investigando la radioinmunoterapia del melanoma metastásico. La radioterapia tiene un papel en la paliación del melanoma metastásico. [148]


Los factores que afectan el pronóstico incluyen:
Ciertos tipos de melanoma tienen peor pronóstico pero esto se explica por su grosor . Los melanomas menos invasivos, incluso con metástasis en los ganglios linfáticos, tienen un mejor pronóstico que los melanomas profundos sin metástasis regionales en el momento de la estadificación. Las recurrencias locales tienden a comportarse de manera similar a una primaria a menos que estén en el sitio de una escisión local amplia (a diferencia de una escisión por etapas o una escisión con punzón/afeitado), ya que estas recurrencias tienden a indicar invasión linfática.
Cuando los melanomas se han extendido a los ganglios linfáticos , uno de los factores más importantes es la cantidad de ganglios con malignidad. También es importante el grado de malignidad dentro de un ganglio; Las micrometástasis en las que la malignidad es sólo microscópica tienen un pronóstico más favorable que las macrometástasis. En algunos casos, las micrometástasis sólo pueden detectarse mediante tinciones especiales, y si la malignidad sólo es detectable mediante una prueba rara vez utilizada conocida como reacción en cadena de la polimerasa (PCR), el pronóstico es mejor. Las macrometástasis en las que la malignidad es clínicamente evidente (en algunos casos el cáncer reemplaza completamente un ganglio) tienen un pronóstico mucho peor, y si los ganglios están enmarañados o si hay extensión extracapsular, el pronóstico es aún peor. Además de estas variables, se pueden utilizar los niveles de expresión y las variaciones del número de copias de varios genes relevantes para respaldar la evaluación del pronóstico del melanoma. [115] [116]
El melanoma en estadio IV, en el que ha hecho metástasis, es la neoplasia maligna cutánea más mortal: la supervivencia a cinco años es del 22,5%. [133] Cuando hay metástasis a distancia, el cáncer generalmente se considera incurable. La tasa de supervivencia a cinco años es inferior al 10%. [150] La mediana de supervivencia es de 6 a 12 meses. El tratamiento es paliativo y se centra en la prolongación y la calidad de vida . En algunos casos, los pacientes pueden vivir muchos meses o incluso años con melanoma metastásico (dependiendo de la agresividad del tratamiento). Las metástasis en piel y pulmones tienen mejor pronóstico. Las metástasis en el cerebro, los huesos y el hígado se asocian con un peor pronóstico. La supervivencia es mejor con metástasis en las que se desconoce la ubicación del tumor primario. [151]
No hay suficiente evidencia definitiva para estadificar adecuadamente y, por lo tanto, dar un pronóstico para el melanoma ocular y el melanoma de partes blandas, o el melanoma mucoso (p. ej., melanoma rectal), aunque estos tienden a metastatizarse más fácilmente. Aunque la regresión puede aumentar la supervivencia, cuando un melanoma ha retrocedido, es imposible saber su tamaño original y, por lo tanto, el tumor original suele ser peor de lo que podría indicar un informe patológico .
Alrededor de 200 genes son pronósticos en el melanoma, tanto genes desfavorables donde la alta expresión se correlaciona con una mala supervivencia como genes favorables donde la alta expresión se asocia con tiempos de supervivencia más largos. Ejemplos de genes desfavorables son MCM6 y TIMELESS ; un ejemplo de un gen favorable es WIPI1 . [51] [52]
Una mayor proporción de neutrófilos a linfocitos se asocia con peores resultados. [152] [153] [154]

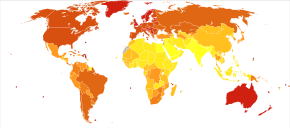
A nivel mundial, en 2012, el melanoma afectó a 232.000 personas y provocó 55.000 muertes. [2] Australia y Nueva Zelanda tienen las tasas más altas de melanoma en el mundo. [2] Se ha vuelto más común en los últimos 20 años en áreas mayoritariamente caucásicas . [2]
La tasa de melanoma ha aumentado en los últimos años, pero no está claro hasta qué punto están implicados cambios en el comportamiento, en el medio ambiente o en la detección temprana. [156]
Australia tiene una tasa muy alta (y creciente) de melanoma. En 2012, las muertes por melanoma se produjeron entre 7,3 y 9,8 por 100.000 habitantes. En Australia, el melanoma es el tercer cáncer más común en ambos sexos; de hecho, su incidencia es mayor que la del cáncer de pulmón , aunque este último causa más muertes. Se estima que en 2012, más de 12.000 australianos fueron diagnosticados con melanoma: dada la modesta población de Australia, esto se expresa mejor como 59,6 nuevos casos por 100.000 habitantes por año; >1 de cada 10 de todos los nuevos casos de cáncer fueron melanomas. [157] La incidencia del melanoma en Australia es un asunto importante por las siguientes razones:
En Estados Unidos, alrededor de 9.000 personas mueren de melanoma al año. [159] En 2011, afectó a 19,7 por 100.000 y provocó la muerte a 2,7 por 100.000. [159]
En 2013:
Las estimaciones de la Sociedad Estadounidense del Cáncer sobre la incidencia del melanoma en los Estados Unidos para 2017 son:
El melanoma es más de 20 veces más común en blancos que en afroamericanos. En general, el riesgo de contraer melanoma a lo largo de la vida es aproximadamente del 2,5 % (1 de cada 40) para los blancos, del 0,1 % (1 de cada 1.000) para los afroamericanos y del 0,5 % (1 de cada 200) para los mexicanos.
El riesgo de melanoma aumenta a medida que las personas envejecen. La edad promedio de las personas cuando se diagnostica la enfermedad es 63 años. [161]
Aunque el melanoma no es una enfermedad nueva, la evidencia de su aparición en la antigüedad es bastante escasa. Sin embargo, un ejemplo se encuentra en un examen realizado en la década de 1960 de nueve momias peruanas , fechadas por radiocarbono en aproximadamente 2400 años, que mostraron signos aparentes de melanoma: masas melanóticas en la piel y metástasis difusas en los huesos. [162]
Se informa que John Hunter fue el primero en operar un melanoma metastásico en 1787. Aunque no sabía exactamente qué era, lo describió como una "excrecencia fúngica cancerosa". El tumor extirpado se conservó en el Museo Hunteriano del Real Colegio de Cirujanos de Inglaterra . No fue hasta 1968 que el examen microscópico de la muestra reveló que se trataba de un ejemplo de melanoma metastásico. [163]
El médico francés René Laennec fue el primero en describir el melanoma como una entidad patológica. Su informe se presentó inicialmente durante una conferencia en la Facultad de Medicina de París en 1804 y luego se publicó como boletín en 1806. [164]
El primer informe en inglés sobre melanoma fue presentado por un médico general inglés de Stourbridge, William Norris, en 1820. [165] En su trabajo posterior de 1857, comentó que existe una predisposición familiar al desarrollo de melanoma ( Ocho casos de melanosis con Observaciones patológicas y terapéuticas sobre esa enfermedad ). Norris también fue pionero al sugerir un vínculo entre los nevos y el melanoma y la posibilidad de una relación entre el melanoma y las exposiciones ambientales, al observar que la mayoría de sus pacientes tenían tez pálida. [166] También describió que los melanomas podrían ser amelanóticos y luego mostró la naturaleza metastásica del melanoma al observar que pueden diseminarse a otros órganos viscerales.
El primer reconocimiento formal del melanoma avanzado como intratable provino de Samuel Cooper en 1840. Afirmó que la única posibilidad de curación depende de la eliminación temprana de la enfermedad (es decir, la extirpación temprana del lunar maligno)...' [167]
Más de un siglo y medio después, esta situación sigue prácticamente sin cambios.
La palabra melanoma llegó al inglés del neolatín del siglo XIX [168] y utiliza formas combinadas derivadas de raíces griegas antiguas : melano- (que denota melanina ) + -oma (que denota una masa de tejido y especialmente una neoplasia ), a su vez del griego. μέλας melas , "oscuro", [169] y -ωμα oma , "proceso". La palabra melanoma tiene una larga historia de uso en un sentido más amplio para referirse a cualquier tumor melanocítico , típicamente, pero no siempre, maligno, [170] [171] pero hoy en día el sentido más estricto que se refiere sólo a tipos malignos se ha vuelto tan dominante que el benigno Por lo general, los tumores ya no se llaman melanomas y ahora la palabra melanoma generalmente se entiende como melanoma maligno, a menos que se especifique lo contrario. Términos como " tumor melanocítico benigno " etiquetan inequívocamente los tipos benignos, y las clasificaciones histopatológicas modernas de tumores utilizadas en medicina no utilizan la palabra para tumores benignos.
Se están realizando investigaciones farmacoterapéuticas para el melanoma irresecable o metastásico. [172]
En la investigación clínica se están probando la terapia celular adoptiva y la terapia génica . [173]
Se han utilizado dos tipos de tratamientos experimentales desarrollados en el Instituto Nacional del Cáncer (NCI) en el melanoma metastásico con éxito provisional. [42]
El primer tratamiento implica la terapia celular adoptiva (ACT) utilizando células inmunes TIL (linfocitos infiltrantes de tumores) aisladas del propio tumor de melanoma de una persona. [131] Estas células se cultivan en grandes cantidades en un laboratorio y se devuelven al paciente después de un tratamiento que reduce temporalmente las células T normales en el cuerpo del paciente. La terapia TIL después de la linfodepleción puede dar como resultado una respuesta completa duradera en una variedad de configuraciones. [174] [175]
El segundo tratamiento, la transferencia adoptiva de linfocitos autólogos genéticamente alterados, depende de la introducción de genes que codifican los llamados receptores de células T (TCR) en los linfocitos del paciente. [131] Después de esa manipulación, los linfocitos reconocen y se unen a ciertas moléculas que se encuentran en la superficie de las células del melanoma y las matan. [176]
Una vacuna contra el cáncer mostró un beneficio modesto en las pruebas de última fase realizadas en 2009 contra el melanoma. [177] [178]
Alrededor del 60% de los melanomas contienen una mutación en el gen B-Raf . Los primeros ensayos clínicos sugirieron que los inhibidores de B-Raf, incluido el vemurafenib de Plexxicon , podrían provocar una regresión sustancial del tumor en la mayoría de los pacientes si su tumor contiene la mutación B-Raf. [179] En junio de 2011, un gran ensayo clínico confirmó los hallazgos positivos de esos ensayos anteriores. [180] [181]
En agosto de 2011, Vemurafenib recibió la aprobación de la FDA para el tratamiento del melanoma en etapa avanzada. En mayo de 2013, la FDA de EE. UU. aprobó dabrafenib como tratamiento de agente único para pacientes con melanoma avanzado con mutación BRAF V600E positiva. [182]
Algunos investigadores creen que las terapias combinadas que bloquean simultáneamente múltiples vías pueden mejorar la eficacia al dificultar que las células tumorales muten antes de ser destruidas. En octubre de 2012, un estudio informó que la combinación de Dabrafenib con un inhibidor de MEK, trametinib, produjo resultados aún mejores. En comparación con dabrafenib solo, la supervivencia libre de progresión aumentó del 9% al 41%, y la mediana de supervivencia libre de progresión aumentó a 9,4 meses frente a 5,8 meses. Sin embargo, algunos efectos secundarios aumentaron en el estudio combinado. [183] [184]
En enero de 2014, la FDA aprobó la combinación de dabrafenib y trametinib para el tratamiento de personas con melanoma metastásico con mutación BRAF V600E/K. [185] En junio de 2018, la FDA aprobó la combinación de un inhibidor de BRAF, encorafenib , y un inhibidor de MEK, binimetinib, para el tratamiento del melanoma irresecable o metastásico con una mutación BRAF V600E o V600K. [186]
La eventual resistencia a los inhibidores de BRAF y MEK puede deberse a una proteína de la superficie celular conocida como EphA2 que ahora se está investigando. [187]
En la Conferencia de la Sociedad Estadounidense de Oncología Clínica en junio de 2010, la compañía farmacéutica Bristol Myers Squibb informó los hallazgos clínicos de su fármaco ipilimumab . El estudio encontró un aumento en la mediana de supervivencia de 6,4 a 10 meses en pacientes con melanomas avanzados tratados con ipilimumab monoclonal, frente a una vacuna experimental. También encontró una tasa de supervivencia a un año del 25% en el grupo de control que usó la vacuna, del 44% en el grupo de vacuna e ipilimumab, y del 46% en el grupo tratado con ipilimumab solo. [188] Sin embargo, algunos han expresado su preocupación acerca de este estudio por su uso del brazo de control no convencional, en lugar de comparar el fármaco con un placebo o un tratamiento estándar. [189] [190] La crítica fue que aunque Ipilimumab funcionó mejor que la vacuna, la vacuna no se ha probado antes y puede estar causando toxicidad, lo que hace que el fármaco parezca mejor en comparación.
La FDA aprobó el ipilimumab en marzo de 2011 para tratar pacientes con melanoma en etapa avanzada que se ha diseminado o que no se puede extirpar mediante cirugía. [191] [192] [193]
En junio de 2011, un ensayo clínico de ipilimumab más dacarbazina combinó este refuerzo del sistema inmunológico con el fármaco de quimioterapia estándar que se dirige a la división celular. Mostró un aumento en la supervivencia media para estos pacientes en etapa avanzada a 11 meses en lugar de los 9 meses que se observan normalmente. Los investigadores también tenían la esperanza de mejorar la tasa de supervivencia a cinco años, aunque en algunos pacientes se observaron efectos secundarios adversos graves. Un tratamiento cuesta 120.000 dólares. La marca del medicamento es Yervoy. [180] [194]
Los avances en la ecografía de alta resolución han permitido la vigilancia de la carga metastásica en los ganglios linfáticos centinela. [195] El ensayo Screening and Surveillance of Ultrasound in Melanoma (SUNMEL) está evaluando el ultrasonido como una alternativa a los métodos quirúrgicos invasivos. [196]
En algunos países se estudian y utilizan métodos de viroterapia oncolítica para tratar el melanoma. La viroterapia oncolítica es una rama prometedora de la viroterapia , donde se utilizan virus oncolíticos para tratar enfermedades; Los virus pueden aumentar el metabolismo, reducir la inmunidad antitumoral y desorganizar la vasculatura. [197] Talimogene laherparepvec (T-VEC) (que es una inmunoterapia oncolítica derivada del virus del herpes simple tipo 1) demostró ser útil contra el melanoma metastásico en 2015 con una mayor supervivencia de 4,4 meses. [198] [12]
Se han probado antirretrovirales in vitro contra el melanoma. La razón detrás de esto radica en su potencial para inhibir los retrovirus endógenos humanos, cuya actividad se ha asociado con el desarrollo del melanoma. [199] [200] Los resultados en células malignas han mostrado una eficacia moderada y se esperan nuevos avances mediante pruebas en modelos animales.
El término "melanoma" en medicina humana indica un crecimiento maligno; el prefijo 'maligno' es redundante.
El término melanoma maligno se está volviendo obsoleto porque la palabra "maligno" es redundante ya que no existen melanomas benignos.
Evite la frase redundante melanoma maligno.
Necesidad de seleccionar "melanoma"
Se ha informado una tasa de curación de hasta el 98% para el melanoma in situ pequeño y de hasta el 95% para la variante del lentigo maligno de la melanona in situ con
la cirugía de Mohs
.