El monóxido de carbono ( fórmula química CO ) es un gas venenoso e inflamable que es incoloro, inodoro, insípido y ligeramente menos denso que el aire. El monóxido de carbono está formado por un átomo de carbono y un átomo de oxígeno conectados por un triple enlace . Es el óxido de carbono más simple . En los complejos de coordinación , el ligando de monóxido de carbono se llama carbonilo . Es un ingrediente clave en muchos procesos de la química industrial. [5]
La fuente más común de monóxido de carbono es la combustión parcial de compuestos que contienen carbono. Numerosas fuentes ambientales y biológicas generan monóxido de carbono. En la industria, el monóxido de carbono es importante en la producción de muchos compuestos, incluidos medicamentos, fragancias y combustibles. [6] Al emitirse a la atmósfera, el monóxido de carbono afecta varios procesos que contribuyen al cambio climático . [7]
El CO en interiores es uno de los contaminantes tóxicos más agudos que afectan la calidad del aire interior . El CO puede ser emitido por el humo del tabaco y generado por estufas que queman combustible (leña, queroseno, gas natural, propano) y sistemas de calefacción que queman combustible (leña, petróleo, gas natural) que funcionan mal y por conductos de humos bloqueados conectados a estos aparatos. [8] El envenenamiento por monóxido de carbono es el tipo más común de envenenamiento mortal del aire en muchos países. [9] [8] [10]
El monóxido de carbono tiene funciones biológicas importantes en todos los reinos filogenéticos. Es producido por muchos organismos, incluidos los humanos. En la fisiología de los mamíferos, el monóxido de carbono es un ejemplo clásico de hormesis donde las concentraciones bajas sirven como un neurotransmisor endógeno ( gasotransmisor ) y las concentraciones altas son tóxicas y provocan intoxicación por monóxido de carbono . Es isoelectrónico tanto con el anión cianuro CN − como con el nitrógeno molecular N 2 .
El monóxido de carbono es el oxocarbono más simple y es isoelectrónico con otras especies diatómicas con triple enlace que poseen 10 electrones de valencia, incluido el anión cianuro , el catión nitrosonio , el monofluoruro de boro y el nitrógeno molecular . Tiene una masa molar de 28,0, lo que, según la ley de los gases ideales , lo hace ligeramente menos denso que el aire, cuya masa molar media es 28,8.
El carbono y el oxígeno están conectados por un triple enlace que consta de dos enlaces pi netos y un enlace sigma . La longitud del enlace entre el átomo de carbono y el átomo de oxígeno es 112,8 pm . [11] [12] La longitud de este enlace es consistente con un triple enlace, como en el nitrógeno molecular (N 2 ), que tiene una longitud de enlace similar (109,76 pm) y casi la misma masa molecular . Los dobles enlaces carbono-oxígeno son significativamente más largos, 120,8 pm en el formaldehído , por ejemplo. [13] El punto de ebullición (82 K) y el punto de fusión (68 K) son muy similares a los del N 2 (77 K y 63 K, respectivamente). La energía de disociación del enlace de 1072 kJ/mol es más fuerte que la del N 2 (942 kJ/mol) y representa el enlace químico más fuerte conocido. [14]
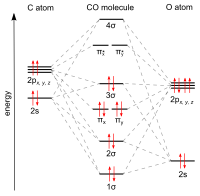
El estado electrónico fundamental del monóxido de carbono es un estado singlete [15] ya que no hay electrones desapareados.
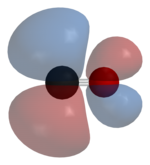
El carbono y el oxígeno juntos tienen un total de 10 electrones en la capa de valencia . Siguiendo la regla del octeto tanto para el carbono como para el oxígeno, los dos átomos forman un triple enlace , con seis electrones compartidos en tres orbitales moleculares de enlace, en lugar del doble enlace habitual que se encuentra en los compuestos carbonílicos orgánicos. Dado que cuatro de los electrones compartidos provienen del átomo de oxígeno y sólo dos del carbono, un orbital de enlace está ocupado por dos electrones del oxígeno, formando un enlace dativo o dipolar . Esto provoca una polarización C←O de la molécula, con una pequeña carga negativa en el carbono y una pequeña carga positiva en el oxígeno. Los otros dos orbitales de enlace están ocupados cada uno por un electrón del carbono y uno del oxígeno, formando enlaces covalentes (polares) con una polarización inversa C→O ya que el oxígeno es más electronegativo que el carbono. En la molécula de monóxido de carbono libre, una carga neta negativa δ – permanece en el extremo del carbono y la molécula tiene un pequeño momento dipolar de 0,122 D. [18]
Por lo tanto, la molécula es asimétrica: el oxígeno tiene más densidad electrónica que el carbono y también tiene una carga ligeramente positiva en comparación con el carbono, que es negativo. Por el contrario, la molécula isoelectrónica de dinitrógeno no tiene momento dipolar.

El monóxido de carbono tiene un orden de enlace fraccionario calculado de 2,6, lo que indica que el "tercer" enlace es importante pero constituye algo menos que un enlace completo. [19] Por lo tanto, en términos de enlace de valencia, – C≡O + es la estructura más importante, mientras que :C=O no es un octeto, pero tiene una carga formal neutra en cada átomo y representa el segundo contribuyente de resonancia más importante. Debido al par solitario y la divalencia del carbono en esta estructura de resonancia, a menudo se considera que el monóxido de carbono es un carbeno extraordinariamente estabilizado . [20] Los isocianuros son compuestos en los que el O se reemplaza por un grupo NR (R = alquilo o arilo) y tienen un esquema de enlace similar.
Si el monóxido de carbono actúa como ligando , la polaridad del dipolo puede invertirse con una carga neta negativa en el extremo del oxígeno, dependiendo de la estructura del complejo de coordinación . [21] Véase también la sección "Química de coordinación" a continuación.
Estudios teóricos y experimentales muestran que, a pesar de la mayor electronegatividad del oxígeno, el momento dipolar apunta desde el extremo del carbono más negativo al extremo del oxígeno más positivo. [22] [23] Los tres enlaces son, de hecho, enlaces covalentes polares que están fuertemente polarizados. La polarización calculada hacia el átomo de oxígeno es del 71% para el enlace σ y del 77% para ambos enlaces π . [24]
El estado de oxidación del carbono en monóxido de carbono es +2 en cada una de estas estructuras. Se calcula contando todos los electrones de enlace como pertenecientes al oxígeno más electronegativo. Sólo los dos electrones no enlazantes del carbono están asignados al carbono. En este recuento, el carbono tiene sólo dos electrones de valencia en la molécula en comparación con cuatro en el átomo libre.
El monóxido de carbono se produce en diversos entornos naturales y artificiales. La degradación fotoquímica de la materia vegetal, por ejemplo, genera aproximadamente 60 millones de toneladas al año. [26] Las concentraciones típicas en partes por millón son las siguientes:

El monóxido de carbono (CO) está presente en pequeñas cantidades (alrededor de 80 ppb) en la atmósfera terrestre . La mayor parte del resto proviene de reacciones químicas con compuestos orgánicos emitidos por actividades humanas y de origen natural debido a reacciones fotoquímicas en la troposfera que generan alrededor de 5 × 10 12 kilogramos por año. [34] Otras fuentes naturales de CO incluyen volcanes, incendios forestales y forestales , y otras formas diversas de combustión, como los combustibles fósiles . [35] También se emiten pequeñas cantidades desde el océano y desde la actividad geológica porque el monóxido de carbono se produce disuelto en roca volcánica fundida a altas presiones en el manto de la Tierra . [36] Debido a que las fuentes naturales de monóxido de carbono varían de un año a otro, es difícil medir con precisión las emisiones naturales del gas.
El monóxido de carbono tiene un efecto indirecto sobre el forzamiento radiativo al elevar las concentraciones de gases de efecto invernadero directos , incluidos el metano y el ozono troposférico . El CO puede reaccionar químicamente con otros componentes atmosféricos (principalmente el radical hidroxilo , • OH) que de otro modo destruiría el metano. [37] A través de procesos naturales en la atmósfera, se oxida a dióxido de carbono y ozono. El monóxido de carbono tiene una vida corta en la atmósfera (con una vida media de entre uno y dos meses) y su concentración es espacialmente variable. [38]
Debido a su larga vida en la troposfera media, el monóxido de carbono también se utiliza como marcador de columnas de contaminantes. [39]
Más allá de la Tierra, el monóxido de carbono es la segunda molécula diatómica más común en el medio interestelar , después del hidrógeno molecular . Debido a su asimetría, esta molécula polar produce líneas espectrales mucho más brillantes que la molécula de hidrógeno, lo que hace que el CO sea mucho más fácil de detectar. El CO interestelar se detectó por primera vez con radiotelescopios en 1970. Actualmente es el marcador de gas molecular más utilizado en general en el medio interestelar de las galaxias, ya que el hidrógeno molecular sólo puede detectarse mediante luz ultravioleta, lo que requiere telescopios espaciales . Las observaciones de monóxido de carbono proporcionan gran parte de la información sobre las nubes moleculares en las que se forman la mayoría de las estrellas . [40] [41]
Beta Pictoris , la segunda estrella más brillante de la constelación de Pictor , muestra un exceso de emisión infrarroja en comparación con las estrellas normales de su tipo, causado por grandes cantidades de polvo y gas (incluido monóxido de carbono) [42] [43] cerca de la estrella .
En la atmósfera de Venus el monóxido de carbono se produce como resultado de la fotodisociación del dióxido de carbono por radiación electromagnética de longitudes de onda inferiores a 169 nm . También ha sido identificado espectroscópicamente en la superficie de la luna Tritón de Neptuno . [44]
El monóxido de carbono sólido es un componente de los cometas . [45] El componente volátil o "hielo" del cometa Halley tiene aproximadamente un 15 % de CO. [46] A temperatura ambiente y a presión atmosférica, el monóxido de carbono en realidad sólo es metaestable (ver reacción de Boudouard ) y lo mismo ocurre a bajas temperaturas donde CO y CO
2son sólidos, pero sin embargo pueden existir durante miles de millones de años en los cometas. Hay muy poco CO en la atmósfera de Plutón , que parece haberse formado a partir de cometas. Esto puede deberse a que hay (o había) agua líquida dentro de Plutón.
El monóxido de carbono puede reaccionar con el agua para formar dióxido de carbono e hidrógeno:
Esto se denomina reacción de cambio agua-gas cuando ocurre en fase gaseosa, pero también puede tener lugar (muy lentamente) en una solución acuosa. Si la presión parcial del hidrógeno es suficientemente alta (por ejemplo, en un mar subterráneo), se formará ácido fórmico :
Estas reacciones pueden tener lugar en unos pocos millones de años incluso a temperaturas como las de Plutón. [47]
El monóxido de carbono es un contaminante atmosférico temporal en algunas zonas urbanas, procedente principalmente de los gases de escape de los motores de combustión interna (incluidos vehículos, generadores portátiles y de reserva, cortadoras de césped, hidrolavadoras, etc.), pero también de la combustión incompleta de varios otros combustibles ( incluyendo madera, carbón vegetal, petróleo, parafina, propano, gas natural y basura).
Se pueden observar grandes episodios de contaminación por CO desde el espacio sobre las ciudades. [48]
El monóxido de carbono forma, junto con los aldehídos , parte de la serie de ciclos de reacciones químicas que forman el smog fotoquímico . Reacciona con el radical hidroxilo ( • OH) para producir un radical intermedio • HOCO, que transfiere rápidamente su radical hidrógeno a O 2 para formar radical peroxi (HO 2 • ) y dióxido de carbono (CO 2 ). [49] El radical peroxi reacciona posteriormente con el óxido de nitrógeno (NO) para formar dióxido de nitrógeno (NO 2 ) y radical hidroxilo. El NO 2 da O ( 3 P) mediante fotólisis, formando así O 3 después de la reacción con O 2 . Dado que el radical hidroxilo se forma durante la formación de NO 2 , el equilibrio de la secuencia de reacciones químicas que comienzan con el monóxido de carbono y conducen a la formación de ozono es:
(donde hν se refiere al fotón de luz absorbido por la molécula de NO 2 en la secuencia)
Aunque la creación de NO 2 es el paso crítico que conduce a la formación de niveles bajos de ozono , también aumenta este ozono de otra manera, algo mutuamente excluyente, al reducir la cantidad de NO que está disponible para reaccionar con el ozono. [50]
El monóxido de carbono es uno de los contaminantes del aire interior más tóxicos . El monóxido de carbono puede ser emitido por el humo del tabaco y generado por estufas que queman combustible (leña, queroseno, gas natural, propano) y sistemas de calefacción que queman combustible (leña, petróleo, gas natural) que funcionan mal y por conductos de humos bloqueados conectados a estos aparatos. [8] En los países desarrollados, las principales fuentes de emisión de CO en interiores provienen de dispositivos de cocina y calefacción que queman combustibles fósiles y están defectuosos, mal instalados o mal mantenidos. [51] El mal funcionamiento del aparato puede deberse a una mala instalación o a la falta de mantenimiento y uso adecuado. [8] En los países de ingresos bajos y medios, las fuentes más comunes de CO en los hogares son la quema de combustibles de biomasa y el humo de los cigarrillos. [51]
Los mineros se refieren al monóxido de carbono como " la humedad blanca " o el "asesino silencioso". Se puede encontrar en áreas confinadas y con poca ventilación, tanto en minas a cielo abierto como en minas subterráneas. Las fuentes más comunes de monóxido de carbono en las operaciones mineras son el motor de combustión interna y los explosivos; sin embargo, en las minas de carbón también se puede encontrar monóxido de carbono debido a la oxidación del carbón a baja temperatura. [52] El modismo " Canario en la mina de carbón " se refería a una alerta temprana de presencia de monóxido de carbono. [53]
La intoxicación por monóxido de carbono es el tipo más común de intoxicación por aire mortal en muchos países. La exposición aguda también puede provocar efectos neurológicos a largo plazo, como cambios cognitivos y de comportamiento. Una intoxicación grave por CO puede provocar pérdida del conocimiento, coma y muerte. La exposición crónica a bajas concentraciones de monóxido de carbono puede provocar letargo, dolores de cabeza, náuseas, síntomas parecidos a los de la gripe y problemas neuropsicológicos y cardiovasculares. [9] [8] [10]
El monóxido de carbono tiene una amplia gama de funciones en todas las disciplinas de la química. Las cuatro categorías principales de reactividad involucran catálisis de metal-carbonilo , química de radicales , química de cationes y aniones . [54]

La mayoría de los metales forman complejos de coordinación que contienen monóxido de carbono unido covalentemente. Sólo los metales en estados de oxidación más bajos formarán complejos con ligandos de monóxido de carbono . Esto se debe a que debe haber suficiente densidad electrónica para facilitar la retrodonación desde el orbital d xz del metal al orbital molecular π* del CO. El par solitario del átomo de carbono en el CO también dona densidad electrónica al d x 2 − y 2 sobre el metal para formar un enlace sigma . Esta donación de electrones también se manifiesta con el efecto cis , o la labilización de ligandos de CO en la posición cis. El níquel carbonilo , por ejemplo, se forma por combinación directa de monóxido de carbono y níquel metálico:
Por este motivo, el níquel de cualquier tubo o pieza no debe entrar en contacto prolongado con el monóxido de carbono. El níquel carbonilo se descompone fácilmente en Ni y CO al entrar en contacto con superficies calientes, y este método se utiliza para la purificación industrial de níquel en el proceso Mond . [55]
En el níquel carbonilo y otros carbonilos, el par de electrones del carbono interactúa con el metal; el monóxido de carbono dona el par de electrones al metal. En estas situaciones, el monóxido de carbono se denomina ligando carbonilo . Uno de los carbonilos metálicos más importantes es el pentacarbonilo de hierro , Fe(CO) 5 :
Muchos complejos de metal-CO se preparan mediante descarbonilación de disolventes orgánicos, no de CO. Por ejemplo, el tricloruro de iridio y la trifenilfosfina reaccionan en 2-metoxietanol o DMF hirviendo para producir IrCl(CO)(PPh 3 ) 2 .
Los carbonilos metálicos en la química de coordinación generalmente se estudian mediante espectroscopia infrarroja .
En presencia de ácidos fuertes y agua, el monóxido de carbono reacciona con los alquenos para formar ácidos carboxílicos en un proceso conocido como reacción de Koch-Haaf . [56] En la reacción de Gattermann-Koch , los arenos se convierten en derivados de benzaldehído en presencia de CO, AlCl 3 y HCl . [57] Los compuestos organolitio (por ejemplo, butil litio ) reaccionan con el monóxido de carbono, pero estas reacciones tienen poco uso científico.
Aunque el CO reacciona con carbocationes y carbaniones , es relativamente no reactivo con compuestos orgánicos sin la intervención de catalizadores metálicos. [58]
Con los reactivos del grupo principal, el CO sufre varias reacciones notables. La cloración de CO es la ruta industrial hacia el importante compuesto fosgeno . Con borano CO forma el aducto H 3 BCO , que es isoelectrónico con el catión acetilio [H 3 CCO] + . El CO reacciona con el sodio para dar productos resultantes del acoplamiento C-C, como el acetilendiolato de sodio 2 Na.+
· C
2oh2-2
. Reacciona con potasio fundido para dar una mezcla de un compuesto organometálico, acetilendiolato de potasio 2 K.+
· C
2oh2-2
, bencenohexolato de potasio 6 K+
C
6oh6-6
, [59] y rodizonato de potasio 2 K+
· C
6oh2-6
. [60]
Como polímeros de monóxido de carbono se pueden considerar los compuestos ciclohexanohexona o triquinoílo (C 6 O 6 ) y ciclopentanopentona o ácido leucónico (C 5 O 5 ), que hasta ahora sólo se han obtenido en pequeñas cantidades. A presiones superiores a 5 GPa , el monóxido de carbono se convierte en policarbonilo , un polímero sólido que es metaestable a presión atmosférica pero que es explosivo. [61] [62]
El monóxido de carbono se produce convenientemente en el laboratorio mediante la deshidratación del ácido fórmico o del ácido oxálico , por ejemplo con ácido sulfúrico concentrado . [56] [57] [63] Otro método es calentar una mezcla íntima de metal de zinc en polvo y carbonato de calcio , que libera CO y deja óxido de zinc y óxido de calcio :
El nitrato de plata y el yodoformo también producen monóxido de carbono:
Finalmente, las sales de oxalato metálico liberan CO al calentarse, dejando un carbonato como subproducto:
La combustión térmica es la fuente más común de monóxido de carbono. El monóxido de carbono se produce por la oxidación parcial de compuestos que contienen carbono ; se forma cuando no hay suficiente oxígeno para producir dióxido de carbono (CO 2 ), como cuando se hace funcionar una estufa o un motor de combustión interna en un espacio cerrado.
Durante los procesos oxidativos para la producción de sustancias químicas se forma una gran cantidad de CO como subproducto. Por este motivo es necesario purificar los gases de proceso.
Se han desarrollado muchos métodos para la producción de monóxido de carbono. [64]
Una importante fuente industrial de CO es el gas productor , una mezcla que contiene principalmente monóxido de carbono y nitrógeno, formada por la combustión de carbono en el aire a alta temperatura cuando hay un exceso de carbono. En un horno, el aire pasa a través de un lecho de coque . El CO 2 producido inicialmente se equilibra con el carbono caliente restante para dar CO. [65] La reacción del CO 2 con el carbono para dar CO se describe como reacción de Boudouard . [66] Por encima de 800 °C, el CO es el producto predominante:
Otra fuente es el " gas de agua ", una mezcla de hidrógeno y monóxido de carbono producida mediante la reacción endotérmica de vapor y carbono:
Otros " gases de síntesis " similares se pueden obtener a partir del gas natural y otros combustibles.
El monóxido de carbono también se puede producir mediante electrólisis a alta temperatura de dióxido de carbono con celdas electrolizadoras de óxido sólido . [67] Un método desarrollado en DTU Energy utiliza un catalizador de óxido de cerio y no tiene ningún problema de contaminación del catalizador. [68] [69]
El monóxido de carbono también es un subproducto de la reducción de minerales de óxidos metálicos con carbono, como se muestra de forma simplificada a continuación:
El monóxido de carbono también se produce por oxidación directa del carbono en un suministro limitado de oxígeno o aire.
Dado que el CO es un gas, el proceso de reducción puede impulsarse mediante calentamiento, aprovechando la entropía positiva (favorable) de la reacción. El diagrama de Ellingham muestra que la formación de CO se ve favorecida sobre la de CO 2 a altas temperaturas.
El monóxido de carbono es un gas industrial que tiene muchas aplicaciones en la fabricación de productos químicos a granel. [70] Se producen grandes cantidades de aldehídos mediante la reacción de hidroformilación de alquenos , monóxido de carbono y H2 . La hidroformilación se acopla al proceso de olefinas superiores de Shell para dar precursores a los detergentes .
El fosgeno , útil para preparar isocianatos, policarbonatos y poliuretanos, se produce haciendo pasar monóxido de carbono purificado y cloro gaseoso a través de un lecho de carbón activado poroso , que sirve como catalizador . La producción mundial de este compuesto se estimó en 2,74 millones de toneladas en 1989. [71]
El metanol se produce por la hidrogenación del monóxido de carbono. En una reacción relacionada, la hidrogenación del monóxido de carbono se acopla a la formación de enlaces C-C, como en el proceso de Fischer-Tropsch, donde el monóxido de carbono se hidrogena hasta obtener combustibles de hidrocarburos líquidos. Esta tecnología permite convertir carbón o biomasa en diésel.
En el proceso Cativa , el monóxido de carbono y el metanol reaccionan en presencia de un catalizador de iridio homogéneo y ácido yodhídrico para dar ácido acético . Este proceso es responsable de la mayor parte de la producción industrial de ácido acético.
El monóxido de carbono es un fuerte agente reductor y se ha utilizado en pirometalurgia para reducir metales de minerales desde la antigüedad. El monóxido de carbono quita el oxígeno de los óxidos metálicos, reduciéndolos a metal puro a altas temperaturas, formando dióxido de carbono en el proceso. El monóxido de carbono normalmente no se suministra tal cual, en fase gaseosa, al reactor, sino que se forma a alta temperatura en presencia de un mineral que transporta oxígeno o un agente carbonífero como el coque, y a alta temperatura. El proceso de alto horno es un ejemplo típico de proceso de reducción de metal a partir de mineral con monóxido de carbono.
Del mismo modo, el gas de alto horno recogido en la parte superior del alto horno todavía contiene entre un 10% y un 30% de monóxido de carbono y se utiliza como combustible en las estufas Cowper y en los hornos Siemens-Martin en la fabricación de acero de hogar abierto .
El monóxido de carbono también se ha utilizado como medio láser en láseres infrarrojos de alta potencia . [72]
El investigador de la NASA Geoffrey Landis ha propuesto el uso del monóxido de carbono como combustible en Marte . Se han sugerido motores de monóxido de carbono/oxígeno para su uso temprano en el transporte por superficie, ya que tanto el monóxido de carbono como el oxígeno pueden producirse directamente a partir de la atmósfera de dióxido de carbono de Marte mediante electrólisis de circonio , sin utilizar ningún recurso hídrico marciano para obtener hidrógeno, que sería necesario para fabricar metano o cualquier combustible a base de hidrógeno. [73]
Landis también propuso fabricar el combustible a partir de la atmósfera similar de dióxido de carbono de Venus para una misión de retorno de muestras, en combinación con vehículos aéreos no tripulados de energía solar y ascensos en globos cohete. [74]
El monóxido de carbono es una molécula bioactiva que actúa como molécula de señalización gaseosa . Se produce naturalmente por muchas vías enzimáticas y no enzimáticas, [75] la mejor comprendida de las cuales es la acción catabólica de la hemo oxigenasa sobre el hemo derivado de hemoproteínas como la hemoglobina . [76] Tras el primer informe de que el monóxido de carbono es un neurotransmisor normal en 1993, [53] el monóxido de carbono ha recibido importante atención clínica como regulador biológico.
Debido al papel del monóxido de carbono en el cuerpo, las anomalías en su metabolismo se han relacionado con una variedad de enfermedades, incluidas neurodegeneraciones, hipertensión, insuficiencia cardíaca e inflamación patológica. [77] En muchos tejidos, el monóxido de carbono actúa como antiinflamatorio , vasodilatador y estimulador del crecimiento neovascular . [78] En estudios de modelos animales, el monóxido de carbono redujo la gravedad de la sepsis bacteriana inducida experimentalmente , la pancreatitis, la lesión por isquemia/reperfusión hepática, la colitis, la osteoartritis, la lesión pulmonar, el rechazo de trasplantes de pulmón y el dolor neuropático, al tiempo que promovía la cicatrización de las heridas de la piel. Por lo tanto, existe un gran interés en el potencial terapéutico del monóxido de carbono como agente farmacéutico y estándar de atención clínica. [79]
En muchos laboratorios de todo el mundo se han realizado estudios con monóxido de carbono por sus propiedades antiinflamatorias y citoprotectoras. [80] Estas propiedades tienen el potencial de usarse para prevenir el desarrollo de una serie de condiciones patológicas que incluyen lesión por isquemia-reperfusión, rechazo de trasplantes, aterosclerosis, sepsis grave, malaria grave o autoinmunidad. [79] Muchas iniciativas de administración de fármacos han desarrollado métodos para administrar de forma segura monóxido de carbono, y ensayos clínicos controlados posteriores han evaluado el efecto terapéutico del monóxido de carbono. [81]
La microbiota también puede utilizar monóxido de carbono como gasotransmisor . [82] La detección de monóxido de carbono es una vía de señalización facilitada por proteínas como CooA . [83] [84] [85] Aún se desconoce el alcance de las funciones biológicas de la detección de monóxido de carbono.
El microbioma humano produce, consume y responde al monóxido de carbono. [75] Por ejemplo, en ciertas bacterias, el monóxido de carbono se produce mediante la reducción del dióxido de carbono mediante la enzima monóxido de carbono deshidrogenasa con bioenergética favorable para impulsar las operaciones celulares posteriores. [86] [75] En otro ejemplo, el monóxido de carbono es un nutriente para las arqueas metanogénicas que lo reducen a metano utilizando hidrógeno. [87]
El monóxido de carbono tiene ciertas propiedades antimicrobianas que se han estudiado para tratar enfermedades infecciosas. [75]
El monóxido de carbono se utiliza en sistemas de envasado en atmósfera modificada en EE. UU., principalmente con productos cárnicos frescos como carne de res, cerdo y pescado para mantenerlos con un aspecto fresco. El beneficio es doble: el monóxido de carbono protege contra el deterioro microbiano y realza el color de la carne para que sea más atractiva para el consumidor. [88] El monóxido de carbono se combina con la mioglobina para formar carboximioglobina, un pigmento rojo cereza brillante. La carboximioglobina es más estable que la forma oxigenada de la mioglobina, la oximioglobina, que puede oxidarse hasta convertirse en el pigmento marrón metmioglobina . Este color rojo estable puede persistir mucho más tiempo que en la carne envasada normalmente. Los niveles típicos de monóxido de carbono utilizados en las instalaciones que utilizan este proceso están entre 0,4% y 0,5%. [88]
La tecnología recibió por primera vez el estatus de " generalmente reconocido como seguro " (GRAS) por la Administración de Alimentos y Medicamentos de los EE. UU. (FDA) en 2002 para su uso como sistema de envasado secundario y no requiere etiquetado. En 2004, la FDA aprobó el CO como método de envasado primario, declarando que el CO no enmascara el olor a deterioro. [89] El proceso actualmente no está autorizado en muchos otros países, incluidos Japón, Singapur y la Unión Europea . [90] [91] [92]
En la historia antigua, Aníbal ejecutó a prisioneros romanos con vapores de carbón durante la Segunda Guerra Púnica . [53]
El monóxido de carbono se había utilizado para genocidio durante el Holocausto en algunos campos de exterminio , el más notable en los camiones de gas en Chelmno , y en el programa de " eutanasia " Acción T4 . [93]
Los seres humanos han mantenido una relación compleja con el monóxido de carbono desde que aprendieron a controlar el fuego alrededor del año 800.000 a.C. Los primeros humanos probablemente descubrieron la toxicidad del envenenamiento por monóxido de carbono al introducir fuego en sus viviendas. El desarrollo temprano de la metalurgia y las tecnologías de fundición que surgieron alrededor del 6.000 a. C. hasta la Edad del Bronce también afectó a la humanidad por la exposición al monóxido de carbono. Además de la toxicidad del monóxido de carbono, los indígenas americanos pueden haber experimentado las propiedades neuroactivas del monóxido de carbono a través de rituales chamánicos junto al fuego. [53]
Las primeras civilizaciones desarrollaron cuentos mitológicos para explicar el origen del fuego, como Prometeo de la mitología griega , que compartía el fuego con los humanos. Aristóteles (384-322 a. C.) registró por primera vez que la quema de carbones producía humos tóxicos. El médico griego Galeno (129-199 d. C.) especuló que había un cambio en la composición del aire que causaba daño al inhalarlo, y muchos otros de la época desarrollaron una base de conocimiento sobre el monóxido de carbono en el contexto de la toxicidad del humo del carbón . Cleopatra pudo haber muerto por intoxicación por monóxido de carbono . [53]
Georg Ernst Stahl mencionó carbonarii halitus en 1697 en referencia a vapores tóxicos que se pensaba que eran monóxido de carbono. Friedrich Hoffmann llevó a cabo la primera investigación científica moderna sobre el envenenamiento por monóxido de carbono procedente del carbón en 1716. Herman Boerhaave realizó los primeros experimentos científicos sobre el efecto del monóxido de carbono (vapores de carbón) en animales en la década de 1730. [53]
Se considera que Joseph Priestley sintetizó por primera vez monóxido de carbono en 1772. Carl Wilhelm Scheele aisló de manera similar el monóxido de carbono del carbón vegetal en 1773 y pensó que podría ser la entidad carbónica que hacía tóxicos los vapores. Torbern Bergman aisló monóxido de carbono a partir de ácido oxálico en 1775. Posteriormente, en 1776, el químico francés de Lassone produjo CO calentando óxido de zinc con coque , pero concluyó erróneamente que el producto gaseoso era hidrógeno , ya que ardía con una llama azul. En presencia de oxígeno, incluidas las concentraciones atmosféricas, el monóxido de carbono arde con una llama azul y produce dióxido de carbono. Antoine Lavoisier realizó experimentos no concluyentes similares a los de Lassone en 1777. William Cruickshank identificó el gas como un compuesto que contiene carbono y oxígeno en 1800. [53] [94]
Thomas Beddoes y James Watt descubrieron que el monóxido de carbono (como hidrocarbonato ) ilumina la sangre venosa en 1793. Watt sugirió que los vapores de carbón podrían actuar como un antídoto contra el oxígeno en la sangre, y Beddoes y Watt también sugirieron que el hidrocarbonato tiene una mayor afinidad por la fibra animal que el oxígeno. en 1796. En 1854, Adrien Chenot sugirió de manera similar el monóxido de carbono para eliminar el oxígeno de la sangre y luego el cuerpo lo oxida a dióxido de carbono. [53] El mecanismo del envenenamiento por monóxido de carbono se atribuye ampliamente a Claude Bernard , cuyas memorias que comenzaron en 1846 y se publicaron en 1857 dicen: "evita que la sangre arterial se vuelva venosa". Felix Hoppe-Seyler publicó de forma independiente conclusiones similares al año siguiente. [53]
El monóxido de carbono ganó reconocimiento como reactivo esencial en el siglo XX. [5] Tres procesos industriales ilustran su evolución en la industria. En el proceso Fischer-Tropsch , el carbón y las materias primas ricas en carbono relacionadas se convierten en combustibles líquidos mediante la intermediación de CO. Desarrollada originalmente como parte del esfuerzo de guerra alemán para compensar su falta de petróleo nacional, esta tecnología continúa en la actualidad. También en Alemania se descubrió que una mezcla de CO e hidrógeno se combinaba con olefinas para dar aldehídos . Este proceso, llamado hidroformilación , se utiliza para producir muchos productos químicos a gran escala, como tensioactivos , así como compuestos especiales que son fragancias y medicamentos populares. Por ejemplo, el CO se utiliza en la producción de vitamina A. [95] En un tercer proceso importante, atribuido a investigadores de Monsanto , el CO se combina con metanol para dar ácido acético . La mayor parte del ácido acético se produce mediante el proceso Cativa . La hidroformilación y la síntesis de ácido acético son dos de los innumerables procesos de carbonilación .
{{cite book}}: Mantenimiento CS1: nombres numéricos: lista de autores ( enlace )Alrededor del 80 por ciento del hielo es hielo de agua y el monóxido de carbono congelado constituye otro 15 por ciento.
"Descripción de la fisiología del monóxido de carbono de la Royal Society of Chemistry" .