
El cultivo celular o cultivo de tejidos es el proceso mediante el cual las células se cultivan en condiciones controladas, generalmente fuera de su entorno natural. Una vez aisladas las células de interés del tejido vivo , se pueden mantener posteriormente en condiciones cuidadosamente controladas. Es necesario mantenerlos a temperatura corporal (37 °C) en una incubadora. [1] Estas condiciones varían para cada tipo de célula, pero generalmente consisten en un recipiente adecuado con un sustrato o medio rico que suministra los nutrientes esenciales ( aminoácidos , carbohidratos , vitaminas , minerales ), factores de crecimiento , hormonas y gases ( CO 2 , O 2 ), y regula el ambiente físico-químico ( tampón de pH , presión osmótica , temperatura ). La mayoría de las células requieren una superficie o un sustrato artificial para formar un cultivo adherente como una monocapa (de una sola célula de espesor), mientras que otras pueden crecer flotando libremente en un medio como un cultivo en suspensión . [2] Esto generalmente se facilita mediante el uso de un medio de crecimiento líquido, semisólido o sólido , como caldo o agar . El cultivo de tejidos comúnmente se refiere al cultivo de células y tejidos animales, mientras que el término más específico cultivo de tejidos vegetales se utiliza para las plantas. La duración de la vida de la mayoría de las células está determinada genéticamente, pero algunas células cultivadas se han "transformado" en células inmortales que se reproducirán indefinidamente si se proporcionan las condiciones óptimas.
En la práctica, el término "cultivo celular" ahora se refiere al cultivo de células derivadas de eucariotas multicelulares , especialmente células animales , en contraste con otros tipos de cultivos que también cultivan células, como el cultivo de tejidos vegetales , el cultivo de hongos y el cultivo microbiológico ( de microbios ). El desarrollo histórico y los métodos del cultivo celular están estrechamente relacionados con los del cultivo de tejidos y el cultivo de órganos . También se relaciona el cultivo viral , con las células como huéspedes de los virus.
La técnica de laboratorio de mantener líneas celulares vivas (una población de células descendientes de una sola célula y que contienen la misma composición genética) separadas de su tejido original se volvió más sólida a mediados del siglo XX. [3] [4]
El fisiólogo inglés del siglo XIX, Sydney Ringer, desarrolló soluciones salinas que contenían cloruros de sodio, potasio, calcio y magnesio, adecuadas para mantener el latido del corazón de un animal aislado fuera del cuerpo. [5] En 1885, Wilhelm Roux extrajo una sección de la placa medular de un embrión de pollo y la mantuvo en una solución salina tibia durante varios días, estableciendo el principio básico del cultivo de tejidos. En 1907 el zoólogo Ross Granville Harrison demostró el crecimiento de células embrionarias de rana que darían lugar a células nerviosas en un medio de linfa coagulada . En 1913, E. Steinhardt, C. Israelí y RA Lambert cultivaron el virus vaccinia en fragmentos de tejido corneal de cobaya . [6] En 1996, el primer uso de tejido regenerativo se utilizó para reemplazar una pequeña longitud de uretra, lo que llevó a comprender que la técnica de obtener muestras de tejido, cultivarlas fuera del cuerpo sin un soporte y volver a aplicarlas, puede utilizarse sólo para distancias pequeñas de menos de 1 cm. [7] [8] [9] Ross Granville Harrison , trabajando en la Facultad de Medicina Johns Hopkins y luego en la Universidad de Yale , publicó los resultados de sus experimentos de 1907 a 1910, estableciendo la metodología del cultivo de tejidos . [10]
Gottlieb Haberlandt fue el primero en señalar las posibilidades del cultivo de tejidos aislados, el cultivo de tejidos vegetales . [11] Sugirió que mediante este método se podrían determinar las potencialidades de las células individuales a través del cultivo de tejidos, así como las influencias recíprocas de los tejidos entre sí. Desde las afirmaciones originales de Haberlandt, se han desarrollado métodos para el cultivo de tejidos y células, lo que ha dado lugar a importantes descubrimientos en biología y medicina. Presentó su idea original de totipotencialidad en 1902, afirmando que "Teóricamente, todas las células vegetales son capaces de dar origen a una planta completa". [12] [13] [14] El término cultivo de tejidos fue acuñado por el patólogo estadounidense Montrose Thomas Burrows . [15]
Las técnicas de cultivo celular avanzaron significativamente en las décadas de 1940 y 1950 para apoyar la investigación en virología . El cultivo de virus en cultivos celulares permitió la preparación de virus purificados para la fabricación de vacunas . La vacuna inyectable contra la polio desarrollada por Jonas Salk fue uno de los primeros productos producidos en masa utilizando técnicas de cultivo celular. Esta vacuna fue posible gracias a la investigación en cultivos celulares de John Franklin Enders , Thomas Huckle Weller y Frederick Chapman Robbins , quienes recibieron el Premio Nobel por su descubrimiento de un método para cultivar el virus en cultivos de células de riñón de mono . El cultivo celular ha contribuido al desarrollo de vacunas para muchas enfermedades. [1]

En el uso moderno, "cultivo de tejidos" generalmente se refiere al crecimiento de células a partir de un tejido de un organismo multicelular in vitro . Estas células pueden ser células aisladas de un organismo donante ( células primarias ) o una línea celular inmortalizada . Las células se bañan en un medio de cultivo que contiene nutrientes esenciales y fuentes de energía necesarias para la supervivencia de las células. [16] Así, en su sentido más amplio, "cultivo de tejidos" se utiliza a menudo indistintamente con "cultivo celular". Por otro lado, el significado estricto de "cultivo de tejidos" se refiere al cultivo de trozos de tejido, es decir, cultivo de explante .
El cultivo de tejidos es una herramienta importante para el estudio de la biología de células de organismos multicelulares. Proporciona un modelo in vitro del tejido en un entorno bien definido que puede manipularse y analizarse fácilmente. En el cultivo de tejidos animales, las células se pueden cultivar como monocapas bidimensionales (cultivo convencional) o dentro de estructuras fibrosas o geles para lograr estructuras tridimensionales similares a tejidos más naturalistas (cultivo 3D). Eric Simon, en un informe de subvención del NIH SBIR de 1988, demostró que el electrohilado podría usarse para producir andamios fibrosos poliméricos a escala nano y submicrónica específicamente destinados a ser utilizados como sustratos de células y tejidos in vitro . Este uso temprano de redes fibrosas electrohiladas para cultivo celular e ingeniería de tejidos demostró que varios tipos de células se adherirían y proliferarían sobre las fibras de policarbonato. Se observó que, a diferencia de la morfología aplanada que normalmente se observa en el cultivo 2D, las células cultivadas en fibras electrohiladas exhibieron una morfología tridimensional más redondeada que generalmente se observa en los tejidos in vivo . [17]
El cultivo de tejidos vegetales en particular se ocupa del crecimiento de plantas enteras a partir de pequeños trozos de tejido vegetal cultivados en un medio. [18]
Las células se pueden aislar de tejidos para cultivo ex vivo de varias maneras. Las células se pueden purificar fácilmente de la sangre; sin embargo, sólo los glóbulos blancos son capaces de crecer en cultivo. Las células se pueden aislar de tejidos sólidos digiriendo la matriz extracelular utilizando enzimas como colagenasa , tripsina o pronasa , antes de agitar el tejido para liberar las células en suspensión. [19] [20] Alternativamente, se pueden colocar trozos de tejido en medios de crecimiento y las células que crecen están disponibles para cultivo. Este método se conoce como cultivo de explante .
Las células que se cultivan directamente de un sujeto se conocen como células primarias. Con la excepción de algunos derivados de tumores, la mayoría de los cultivos de células primarias tienen una vida útil limitada.
Una línea celular establecida o inmortalizada ha adquirido la capacidad de proliferar indefinidamente ya sea mediante mutación aleatoria o modificación deliberada, como la expresión artificial del gen de la telomerasa . Numerosas líneas celulares están bien establecidas como representativas de tipos celulares particulares .
Para la mayoría de las células primarias aisladas, sufren el proceso de senescencia y dejan de dividirse después de un cierto número de duplicaciones de la población, aunque generalmente conservan su viabilidad (descrito como el límite de Hayflick ).

Aparte de la temperatura y la mezcla de gases, el factor que más comúnmente varía en los sistemas de cultivo es el medio de crecimiento celular . Las recetas de medios de crecimiento pueden variar en cuanto a pH , concentración de glucosa, factores de crecimiento y presencia de otros nutrientes. Los factores de crecimiento utilizados para complementar los medios a menudo se derivan del suero de sangre animal, como el suero fetal bovino (SFB), el suero bovino de ternera, el suero equino y el suero porcino. Una complicación de estos ingredientes derivados de la sangre es la posibilidad de contaminación del cultivo con virus o priones , particularmente en aplicaciones de biotecnología médica. La práctica actual es minimizar o eliminar el uso de estos ingredientes siempre que sea posible y utilizar lisado de plaquetas humanas (hPL). [21] Esto elimina la preocupación de la contaminación entre especies cuando se utiliza FBS con células humanas. hPL ha surgido como una alternativa segura y confiable como reemplazo directo del FBS u otro suero animal. Además, se pueden utilizar medios químicamente definidos para eliminar cualquier rastro de suero (humano o animal), pero esto no siempre se puede lograr con diferentes tipos de células. Las estrategias alternativas implican obtener sangre animal de países con un riesgo mínimo de EEB / EET , como Estados Unidos, Australia y Nueva Zelanda, [22] y utilizar concentrados de nutrientes purificados derivados del suero en lugar de suero animal completo para el cultivo celular. [23]
La densidad del revestimiento (número de células por volumen de medio de cultivo) desempeña un papel fundamental para algunos tipos de células. Por ejemplo, una densidad de placas más baja hace que las células de la granulosa exhiban producción de estrógeno, mientras que una densidad de placas más alta las hace aparecer como células luteínas de la teca productoras de progesterona . [24]
Las células pueden cultivarse en suspensión o en cultivos adherentes . [25] Algunas células viven naturalmente en suspensión, sin estar adheridas a una superficie, como las células que existen en el torrente sanguíneo. También hay líneas celulares que se han modificado para poder sobrevivir en cultivos en suspensión, de modo que puedan crecer a una densidad mayor que la que permitirían las condiciones adherentes. Las células adherentes requieren una superficie, como plástico de cultivo de tejidos o microportador , que puede estar recubierta con componentes de matriz extracelular (como colágeno y laminina) para aumentar las propiedades de adhesión y proporcionar otras señales necesarias para el crecimiento y la diferenciación. La mayoría de las células derivadas de tejidos sólidos son adherentes. Otro tipo de cultivo adherente es el cultivo organotípico , que implica el cultivo de células en un entorno tridimensional (3-D) en lugar de placas de cultivo bidimensionales. Este sistema de cultivo 3D es bioquímica y fisiológicamente más similar al tejido in vivo , pero es técnicamente difícil de mantener debido a muchos factores (por ejemplo, difusión). [26]
Existen diferentes tipos de medios de cultivo celular que se utilizan habitualmente en las ciencias biológicas, incluidos los siguientes:
La contaminación cruzada de líneas celulares puede ser un problema para los científicos que trabajan con células cultivadas. [27] Los estudios sugieren que entre el 15 y el 20% de las veces, las células utilizadas en los experimentos han sido identificadas erróneamente o contaminadas con otra línea celular. [28] [29] [30] Incluso se han detectado problemas con la contaminación cruzada de líneas celulares en líneas del panel NCI-60 , que se utilizan de forma rutinaria para estudios de detección de fármacos. [31] [32] Los principales repositorios de líneas celulares, incluida la Colección Americana de Cultivos Tipo (ATCC), la Colección Europea de Cultivos Celulares (ECACC) y la Colección Alemana de Microorganismos y Cultivos Celulares (DSMZ), han recibido presentaciones de líneas celulares de investigadores. que fueron mal identificados por ellos. [31] [33] Dicha contaminación plantea un problema para la calidad de la investigación producida utilizando líneas de cultivo celular, y los principales repositorios ahora están autenticando todas las presentaciones de líneas celulares. [34] ATCC utiliza huellas dactilares de ADN de repetición corta en tándem (STR) para autenticar sus líneas celulares. [35]
Para abordar este problema de contaminación cruzada de líneas celulares, se anima a los investigadores a autenticar sus líneas celulares en una fase temprana para establecer la identidad de la línea celular. La autenticación debe repetirse antes de congelar las líneas celulares, cada dos meses durante el cultivo activo y antes de cualquier publicación de los datos de investigación generados con las líneas celulares. Se utilizan muchos métodos para identificar líneas celulares, incluido el análisis de isoenzimas , la tipificación del antígeno de linfocitos humanos (HLA), el análisis cromosómico, el cariotipo, la morfología y el análisis STR . [35]
Un importante contaminante cruzado de líneas celulares es la línea celular inmortal HeLa . La contaminación con HeLa se observó por primera vez a principios de la década de 1960 en cultivos no humanos en Estados Unidos. En los años setenta se descubrió contaminación intraespecífica en diecinueve líneas celulares. En 1974, se descubrió que cinco líneas celulares humanas de la Unión Soviética eran HeLa. Un estudio de seguimiento que analizó unas 50 líneas celulares indicó que la mitad tenía marcadores HeLa, pero el contaminante HeLa se había hibridado con las líneas celulares originales. Se ha informado de contaminación de células HeLa por gotitas de aire . Jonas Salk incluso inyectó HeLa, sin saberlo, en seres humanos en un ensayo de vacuna en 1978. [36]
Como las células generalmente continúan dividiéndose en cultivo, generalmente crecen para llenar el área o volumen disponible. Esto puede generar varios problemas:
La elección del medio de cultivo podría afectar la relevancia fisiológica de los hallazgos de los experimentos de cultivo celular debido a las diferencias en la composición y concentraciones de nutrientes. [38] Recientemente se demostró un sesgo sistemático en los conjuntos de datos generados para las pruebas de silenciamiento de genes CRISPR y RNAi , [39] y para el perfil metabólico de líneas celulares cancerosas . [38] El uso de un medio de crecimiento que represente mejor los niveles fisiológicos de nutrientes puede mejorar la relevancia fisiológica de los estudios in vitro y recientemente se desarrollaron tipos de medios como Plasmax [40] y Human Plasma Like Medium (HPLM), [41] .
Entre las manipulaciones comunes realizadas en células de cultivo se encuentran los cambios de medio, el paso de células y la transfección de células. Generalmente se realizan mediante métodos de cultivo de tejidos que se basan en técnicas asépticas . La técnica aséptica tiene como objetivo evitar la contaminación con bacterias, levaduras u otras líneas celulares. Las manipulaciones suelen realizarse en una cabina de bioseguridad o en una cabina de flujo laminar para excluir microorganismos contaminantes. También se pueden añadir al medio de crecimiento antibióticos (p. ej., penicilina y estreptomicina ) y antifúngicos (p. ej., anfotericina B y solución antibiótica-antimicótica ).
A medida que las células experimentan procesos metabólicos, se produce ácido y el pH disminuye. A menudo, se añade un indicador de pH al medio para medir el agotamiento de nutrientes.
En el caso de cultivos adherentes, el medio se puede eliminar directamente por aspiración y luego se reemplaza. Los cambios de medios en cultivos no adherentes implican centrifugar el cultivo y resuspender las células en medios nuevos.
El pase (también conocido como subcultivo o división de células) implica transferir una pequeña cantidad de células a un nuevo vaso. Las células se pueden cultivar durante más tiempo si se dividen con regularidad, ya que se evita la senescencia asociada con una alta densidad celular prolongada. Los cultivos en suspensión se pasan fácilmente con una pequeña cantidad de cultivo que contiene unas pocas células diluidas en un volumen mayor de medio nuevo. Para cultivos adherentes, primero es necesario separar las células; esto se hace comúnmente con una mezcla de tripsina - EDTA ; sin embargo, ahora se encuentran disponibles otras mezclas de enzimas para este propósito. Luego se puede utilizar una pequeña cantidad de células desprendidas para sembrar un nuevo cultivo. Algunos cultivos celulares, como las células RAW, se raspan mecánicamente de la superficie de su recipiente con raspadores de goma.
Otro método común para manipular células implica la introducción de ADN extraño mediante transfección . Esto a menudo se realiza para hacer que las células expresen un gen de interés. Más recientemente, la transfección de construcciones de ARNi se ha descubierto como un mecanismo conveniente para suprimir la expresión de un gen/proteína particular. El ADN también se puede insertar en las células utilizando virus, en métodos denominados transducción , infección o transformación . Los virus, como agentes parásitos, son muy adecuados para introducir ADN en las células, ya que esto forma parte de su curso normal de reproducción.
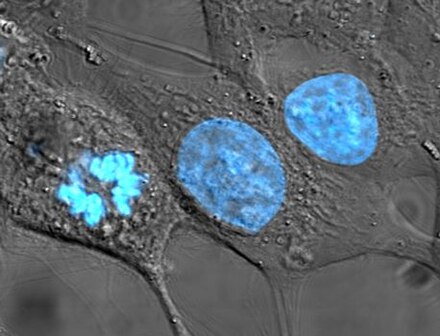
Las líneas celulares que se originan en humanos han sido algo controvertidas en bioética , ya que pueden sobrevivir a su organismo original y luego usarse en el descubrimiento de tratamientos médicos lucrativos. En la decisión pionera en esta área, la Corte Suprema de California sostuvo en Moore v. Regents of the University of California que los pacientes humanos no tienen derechos de propiedad sobre líneas celulares derivadas de órganos extraídos con su consentimiento. [42]
Es posible fusionar células normales con una línea celular inmortalizada . Este método se utiliza para producir anticuerpos monoclonales . En resumen, los linfocitos aislados del bazo (o posiblemente de la sangre) de un animal inmunizado se combinan con una línea celular de mieloma inmortal (linaje de células B) para producir un hibridoma que tiene la especificidad de anticuerpos del linfocito primario y la inmortalidad del mieloma. Se utiliza medio de crecimiento selectivo (HA o HAT) para seleccionar contra células de mieloma no fusionadas; Los linfocitos primarios mueren rápidamente en cultivo y sólo sobreviven las células fusionadas. Estos se analizan para determinar la producción del anticuerpo requerido, generalmente en grupos al principio y luego después de una clonación única.
Una cepa celular se deriva de un cultivo primario o de una línea celular mediante la selección o clonación de células que tienen propiedades o características específicas que deben definirse. Las cepas celulares son células que se han adaptado al cultivo pero, a diferencia de las líneas celulares, tienen un potencial de división finito. Las células no inmortalizadas dejan de dividirse después de 40 a 60 duplicaciones de población [43] y, después de esto, pierden su capacidad de proliferar (un evento determinado genéticamente conocido como senescencia). [44]
El cultivo masivo de líneas celulares animales es fundamental para la fabricación de vacunas virales y otros productos de la biotecnología. El cultivo de células madre humanas se utiliza para ampliar la cantidad de células y diferenciarlas en varios tipos de células somáticas para su trasplante. [45] El cultivo de células madre también se utiliza para recolectar las moléculas y exosomas que las células madre liberan con fines de desarrollo terapéutico. [46]
Los productos biológicos producidos mediante tecnología de ADN recombinante (ADNr) en cultivos de células animales incluyen enzimas , hormonas sintéticas , inmunobiológicos ( anticuerpos monoclonales , interleucinas , linfocinas ) y agentes anticancerígenos . Aunque se pueden producir muchas proteínas más simples utilizando ADNr en cultivos bacterianos, actualmente se deben producir proteínas más complejas glicosiladas ( modificadas con carbohidratos) en células animales. Un ejemplo importante de una proteína tan compleja es la hormona eritropoyetina . El costo de cultivar cultivos de células de mamíferos es alto, por lo que se están realizando investigaciones para producir proteínas tan complejas en células de insectos o en plantas superiores, el uso de células embrionarias individuales y embriones somáticos como fuente para la transferencia directa de genes mediante bombardeo de partículas, expresión de genes de tránsito y La observación por microscopía confocal es una de sus aplicaciones. También ofrece confirmar el origen unicelular de los embriones somáticos y la asimetría de la primera división celular, que inicia el proceso.
El cultivo celular también es una técnica clave para la agricultura celular , cuyo objetivo es proporcionar nuevos productos y nuevas formas de producir productos agrícolas existentes como leche, carne (cultivada) , fragancias y cuerno de rinoceronte a partir de células y microorganismos. Por tanto, se considera un medio para lograr una agricultura libre de animales . También es una herramienta central para la enseñanza de la biología celular. [47]
La investigación en ingeniería de tejidos , células madre y biología molecular implica principalmente cultivos de células en platos planos de plástico. Esta técnica se conoce como cultivo celular bidimensional (2D) y fue desarrollada por primera vez por Wilhelm Roux quien, en 1885, extrajo una porción de la placa medular de un embrión de pollo y la mantuvo en solución salina tibia durante varios días sobre un vidrio plano. lámina. A partir del avance de la tecnología de polímeros surgió la placa de plástico estándar actual para cultivo celular 2D, comúnmente conocida como placa de Petri . A Julius Richard Petri , un bacteriólogo alemán , se le atribuye generalmente este invento mientras trabajaba como asistente de Robert Koch . Hoy en día, varios investigadores también utilizan matraces de laboratorio de cultivo , cónicos e incluso bolsas desechables como las que se utilizan en los biorreactores de un solo uso .
Aparte de las placas de Petri, los científicos llevan mucho tiempo cultivando células dentro de matrices derivadas biológicamente, como el colágeno o la fibrina, y, más recientemente, en hidrogeles sintéticos como la poliacrilamida o el PEG. Lo hacen para provocar fenotipos que no se expresan en sustratos convencionalmente rígidos. Existe un interés creciente en controlar la rigidez de la matriz, [48] un concepto que ha llevado a descubrimientos en campos como:
El cultivo celular en tres dimensiones ha sido promocionado como "la nueva dimensión de la biología". [63] En la actualidad, la práctica del cultivo celular sigue basándose en diversas combinaciones de estructuras celulares únicas o múltiples en 2D. [64] Actualmente, hay un aumento en el uso de cultivos celulares 3D en áreas de investigación que incluyen el descubrimiento de fármacos , la biología del cáncer, la medicina regenerativa , la evaluación de nanomateriales y la investigación básica en ciencias biológicas . [65] [66] [67] Los cultivos de células 3D se pueden cultivar usando un andamio o una matriz, o sin andamio. Los cultivos basados en andamios utilizan una matriz 3D acelular o una matriz líquida. Los métodos sin andamios normalmente se generan en suspensiones. [68] Existe una variedad de plataformas utilizadas para facilitar el crecimiento de estructuras celulares tridimensionales, incluidos sistemas de andamios como matrices de hidrogel [69] y andamios sólidos, y sistemas sin andamios, como placas de baja adherencia, levitación magnética facilitada por nanopartículas. , [70] placas colgantes colgantes, [71] [72] y cultivo celular rotatorio. El cultivo de células en 3D conduce a una amplia variación en las firmas de expresión genética e imita en parte los tejidos en los estados fisiológicos. [73] Un modelo de cultivo celular en 3D mostró un crecimiento celular similar al in vivo que un cultivo en monocapa, y los tres cultivos fueron capaces de sostener el crecimiento celular. [74] A medida que se ha desarrollado el cultivo en 3D, resulta que tiene un gran potencial para diseñar modelos de tumores e investigar la transformación maligna y la metástasis; los cultivos en 3D pueden proporcionar una herramienta completa para comprender los cambios, las interacciones y la señalización celular. [75]
Eric Simon, en un informe de subvención del NIH SBIR de 1988, demostró que el electrohilado podría usarse para producir andamios fibrosos de poliestireno y policarbonato a escala nano y submicrónica específicamente destinados a ser utilizados como sustratos celulares in vitro . Este uso temprano de redes fibrosas electrohiladas para cultivo celular e ingeniería de tejidos demostró que varios tipos de células, incluidos los fibroblastos de prepucio humano (HFF), el carcinoma humano transformado (HEp-2) y el epitelio de pulmón de visón (MLE), se adherirían y proliferarían sobre fibras de policarbonato. . Se observó que, a diferencia de la morfología aplanada que normalmente se observa en el cultivo 2D, las células cultivadas en las fibras electrohiladas exhibieron una morfología tridimensional redondeada más histotípica generalmente observada in vivo . [17]
Como la matriz extracelular natural (ECM) es importante en la supervivencia, proliferación, diferenciación y migración de las células, diferentes matrices de cultivo de hidrogel que imitan la estructura natural de la ECM se consideran enfoques potenciales para el cultivo celular similar al in vivo. [76] Los hidrogeles están compuestos de poros interconectados con alta retención de agua, lo que permite el transporte eficiente de sustancias como nutrientes y gases. Hay varios tipos diferentes de hidrogeles de materiales naturales y sintéticos disponibles para el cultivo celular en 3D, incluidos hidrogeles de extracto de ECM animal, hidrogeles de proteínas, hidrogeles de péptidos, hidrogeles de polímeros e hidrogeles de nanocelulosa a base de madera .
El método de cultivo de células 3D mediante levitación magnética (MLM) es la aplicación del crecimiento de tejido 3D mediante la inducción de células tratadas con conjuntos de nanopartículas magnéticas en campos magnéticos que varían espacialmente utilizando controladores magnéticos de neodimio y promoviendo interacciones entre células levitando las células en el aire. Interfaz líquida de una placa de Petri estándar. Los conjuntos de nanopartículas magnéticas constan de nanopartículas magnéticas de óxido de hierro, nanopartículas de oro y el polímero polilisina. El cultivo de células 3D es escalable, con capacidad para cultivar de 500 células a millones de células o desde un solo plato hasta sistemas de alto rendimiento y bajo volumen.
El cultivo celular es un componente fundamental del cultivo y la ingeniería de tejidos , ya que establece los conceptos básicos del crecimiento y mantenimiento de las células in vitro . La principal aplicación del cultivo de células humanas es en la industria de células madre, donde las células madre mesenquimales pueden cultivarse y criopreservarse para uso futuro. La ingeniería de tejidos ofrece potencialmente mejoras espectaculares en la atención médica de bajo coste para cientos de miles de pacientes al año.
Actualmente, las vacunas contra la polio , el sarampión , las paperas , la rubéola y la varicela se elaboran en cultivos celulares. Debido a la amenaza de la pandemia H5N1 , el gobierno de los Estados Unidos está financiando investigaciones sobre el uso de cultivos celulares para vacunas contra la influenza . Las ideas novedosas en este campo incluyen vacunas basadas en ADN recombinante , como una elaborada utilizando adenovirus humano (un virus del resfriado común) como vector, [77] [78] y nuevos adyuvantes. [79]
La técnica de cocultivo se utiliza para estudiar la diafonía celular entre dos o más tipos de células en una placa o en una matriz 3D. El cultivo de diferentes células madre y la interacción de las células inmunitarias se pueden investigar en un modelo in vitro similar al tejido biológico. Dado que la mayoría de los tejidos contienen más de un tipo de célula, es importante evaluar su interacción en un entorno de cultivo 3D para comprender mejor su interacción e introducir tejidos miméticos. Hay dos tipos de cocultivo: directo e indirecto. Mientras que la interacción directa implica que las células estén en contacto directo entre sí en el mismo medio o matriz de cultivo, la interacción indirecta implica diferentes entornos, lo que permite que participen factores de señalización y solubles. [15] [80]
La diferenciación celular en modelos de tejido durante la interacción entre células se puede estudiar utilizando el sistema de cocultivo para simular tumores cancerosos, evaluar el efecto de los fármacos en ensayos terapéuticos y estudiar el efecto de los fármacos en ensayos terapéuticos. El sistema de cocultivo en modelos 3D puede predecir la respuesta a la quimioterapia y la terapia endocrina si el microambiente define el tejido biológico de las células.
En la ingeniería de tejidos se utiliza un método de cocultivo para generar la formación de tejido con múltiples células que interactúan directamente. [81]

La técnica de microfluídica consiste en sistemas desarrollados que pueden realizar un proceso en un flujo que suele ser en una escala de micras. Los chips de microfluidos también se conocen como Lab-on-a-chip y pueden tener procedimientos y pasos de reacción continuos con una cantidad adicional de reactivos y espacio. Dichos sistemas permiten la identificación y el aislamiento de células y moléculas individuales cuando se combinan con ensayos biológicos apropiados y técnicas de detección de alta sensibilidad. [82] [83]
Los sistemas OoC imitan y controlan el microambiente de las células mediante el crecimiento de tejidos en microfluidos. Combinando ingeniería de tejidos, fabricación de biomateriales y biología celular, ofrece la posibilidad de establecer un modelo biomimético para estudiar enfermedades humanas en el laboratorio. En los últimos años, la ciencia del cultivo celular en 3D ha logrado avances significativos, lo que ha llevado al desarrollo de OoC. La OoC se considera un paso preclínico que beneficia los estudios farmacéuticos, el desarrollo de fármacos y el modelado de enfermedades. [84] [85] OoC es una tecnología importante que puede cerrar la brecha entre las pruebas con animales y los estudios clínicos y también por los avances que la ciencia ha logrado podría ser un reemplazo para los estudios in vivo para la administración de fármacos y los estudios fisiopatológicos. [86]
Además del cultivo de líneas celulares inmortalizadas bien establecidas, las células de explantes primarios de una gran cantidad de organismos se pueden cultivar durante un período de tiempo limitado antes de que se produzca la senescencia (consulte el límite de Hayflick). Las células primarias cultivadas se han utilizado ampliamente en la investigación, como es el caso de los queratocitos de peces en estudios de migración celular. [87] [47] [88]
Los cultivos de células vegetales normalmente se cultivan como cultivos en suspensión celular en un medio líquido o como cultivos de callos en un medio sólido. El cultivo de callos y células vegetales indiferenciadas requiere el equilibrio adecuado de las hormonas de crecimiento vegetal auxina y citoquinina . [ cita necesaria ]
Las células derivadas de Drosophila melanogaster (sobre todo, las células Schneider 2 ) se pueden utilizar para experimentos que pueden ser difíciles de realizar con moscas o larvas vivas, como estudios bioquímicos o estudios que utilizan ARNip . Las líneas celulares derivadas del gusano militar Spodoptera frugiperda , incluidos Sf9 y Sf21 , y de las células High Five del gusano de la col Trichoplusia ni , se usan comúnmente para la expresión de proteínas recombinantes usando baculovirus . [89]
Para las bacterias y levaduras, generalmente se cultivan pequeñas cantidades de células sobre un soporte sólido que contiene nutrientes incrustados, generalmente un gel como el agar, mientras que los cultivos a gran escala se cultivan con las células suspendidas en un caldo nutritivo. [ cita necesaria ]
El cultivo de virus requiere el cultivo de células de origen mamífero, vegetal, fúngico o bacteriano como huéspedes para el crecimiento y replicación del virus. Se pueden generar virus completos de tipo salvaje , virus recombinantes o productos virales en tipos de células distintos de sus huéspedes naturales en las condiciones adecuadas. Dependiendo de la especie del virus, la infección y la replicación viral pueden provocar la lisis de la célula huésped y la formación de una placa viral . [ cita necesaria ]
{{cite magazine}}: Parámetro desconocido |agency=ignorado ( ayuda )