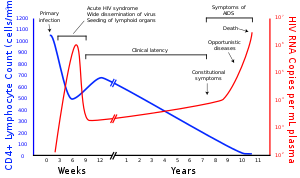
Los virus de la inmunodeficiencia humana ( VIH ) son dos especies de lentivirus (un subgrupo de retrovirus ) que infectan a los humanos. Con el tiempo, causan el síndrome de inmunodeficiencia adquirida (SIDA), [1] [2] una condición en la que la falla progresiva del sistema inmunológico permite que prosperen infecciones oportunistas y cánceres potencialmente mortales. [3] Sin tratamiento, se estima que el tiempo promedio de supervivencia después de la infección por VIH es de 9 a 11 años, dependiendo del subtipo de VIH . [4]
En la mayoría de los casos, el VIH es una infección de transmisión sexual y se produce por contacto o transferencia de sangre , preeyaculación , semen y fluidos vaginales . [5] [6] La transmisión no sexual puede ocurrir de una madre infectada a su bebé durante el embarazo , durante el parto por exposición a su sangre o fluido vaginal y a través de la leche materna . [7] [8] [9] [10] Dentro de estos fluidos corporales, el VIH está presente como partículas de virus libres y como virus dentro de las células inmunes infectadas . Las investigaciones han demostrado (tanto para parejas del mismo sexo como para parejas del sexo opuesto) que el VIH no es transmisible a través de relaciones sexuales sin condón si la pareja VIH positiva tiene una carga viral consistentemente indetectable . [5] [6]
El VIH infecta células vitales del sistema inmunológico humano, como las células T colaboradoras (específicamente las células T CD4 + ), los macrófagos y las células dendríticas . [11] La infección por VIH conduce a niveles bajos de células T CD4 + a través de una serie de mecanismos, incluida la piroptosis de células T infectadas abortivamente, [12] apoptosis de células espectadoras no infectadas, [13] destrucción viral directa de células infectadas y destrucción de células T CD4 + infectadas por linfocitos citotóxicos CD8 + que reconocen las células infectadas. [14] Cuando el número de células T CD4 + disminuye por debajo de un nivel crítico, se pierde la inmunidad mediada por células y el cuerpo se vuelve progresivamente más susceptible a infecciones oportunistas, lo que lleva al desarrollo del SIDA.
El VIH es un miembro del género Lentivirus , [15] parte de la familia Retroviridae . [16] Los lentivirus tienen muchas morfologías y propiedades biológicas en común. Muchas especies están infectadas por lentivirus, que se caracterizan por ser responsables de enfermedades de larga duración con un largo período de incubación . [17] Los lentivirus se transmiten como virus de ARN monocatenario , de sentido positivo y con envoltura . Al ingresar a la célula diana, el genoma de ARN viral se convierte (transcribe de manera inversa) en ADN de doble hebra mediante una enzima codificada por el virus, la transcriptasa inversa , que se transporta junto con el genoma viral en la partícula del virus. El ADN viral resultante luego se importa al núcleo celular y se integra en el ADN celular mediante una enzima codificada por el virus, la integrasa y cofactores del huésped . [18] Una vez integrado, el virus puede volverse latente , lo que permite que el virus y su célula huésped eviten la detección por parte del sistema inmunológico, durante un período de tiempo indeterminado. [19] El virus puede permanecer latente en el cuerpo humano hasta diez años después de la infección primaria; durante este período el virus no causa síntomas. Alternativamente, el ADN viral integrado puede transcribirse , produciendo nuevos genomas de ARN y proteínas virales, utilizando recursos de la célula huésped, que se empaquetan y liberan de la célula como nuevas partículas virales que comenzarán de nuevo el ciclo de replicación.
Se han caracterizado dos tipos de VIH: VIH-1 y VIH-2. El VIH-1 es el virus que se descubrió inicialmente y se denominó virus asociado a linfadenopatía (LAV) y virus linfotrópico T humano 3 (HTLV-III). El VIH-1 es más virulento e infeccioso que el VIH-2 [20] y es la causa de la mayoría de las infecciones por VIH en todo el mundo. La menor infectividad del VIH-2, en comparación con el VIH-1, implica que menos personas expuestas al VIH-2 se infectarán por exposición. Debido a su capacidad de transmisión relativamente pobre, el VIH-2 se limita en gran medida a África occidental . [21]

El VIH tiene una estructura similar a otros retrovirus. Es aproximadamente esférico [22] con un diámetro de aproximadamente 120 nm , alrededor de 100.000 veces más pequeño en volumen que un glóbulo rojo . [23] Está compuesto por dos copias de ARN monocatenario de sentido positivo que codifica los nueve genes del virus encerrados por una cápside cónica compuesta por 2000 copias de la proteína viral p24 . [24] El ARN monocatenario está estrechamente unido a las proteínas de la nucleocápside, p7, y a las enzimas necesarias para el desarrollo del virión, como la transcriptasa inversa , las proteasas , la ribonucleasa y la integrasa . Una matriz compuesta por la proteína viral p17 rodea la cápside asegurando la integridad de la partícula del virión. [24]
Éste, a su vez, está rodeado por la envoltura viral , que está compuesta por la bicapa lipídica extraída de la membrana de una célula huésped humana cuando la partícula viral recién formada brota de la célula. La envoltura viral contiene proteínas de la célula huésped y relativamente pocas copias de la proteína de la envoltura del VIH, [24] que consiste en una cubierta compuesta por tres moléculas conocidas como glicoproteína (gp) 120 , y un tallo que consta de tres moléculas gp41 que anclan la célula huésped. estructura en la envoltura viral. [25] [26] La proteína de la envoltura, codificada por el gen env del VIH , permite que el virus se adhiera a las células objetivo y fusione la envoltura viral con la membrana de la célula objetivo , liberando el contenido viral en la célula e iniciando el ciclo infeccioso. [25]
.jpg/440px-Protein_Structure_Diagram_of_Fusion_Peptide_Epitope_on_HIV_Spike_(41863579304).jpg)
Como única proteína viral en la superficie del virus, la proteína de la envoltura es un objetivo importante para los esfuerzos de la vacuna contra el VIH . [27] Más de la mitad de la masa de la espiga de la envoltura trimérica son glicanos unidos a N. La densidad es alta ya que los glicanos protegen la proteína viral subyacente de la neutralización por parte de los anticuerpos. Esta es una de las moléculas más densamente glicosiladas conocidas y la densidad es suficientemente alta como para impedir el proceso de maduración normal de los glicanos durante la biogénesis en el aparato endoplásmico y de Golgi. [28] [29] Por lo tanto, la mayoría de los glicanos se consideran glicanos inmaduros con "alto contenido de manosa" que normalmente no están presentes en las glicoproteínas humanas que se secretan o están presentes en la superficie celular. [30] El procesamiento inusual y la alta densidad significan que casi todos los anticuerpos ampliamente neutralizantes que se han identificado hasta ahora (de un subconjunto de pacientes que han estado infectados durante muchos meses o años) se unen a estas envolturas o están adaptados para hacerles frente. glicanos. [31]
La estructura molecular del pico viral ahora se ha determinado mediante cristalografía de rayos X [32] y microscopía electrónica criogénica . [33] Estos avances en biología estructural fueron posibles gracias al desarrollo de formas recombinantes estables de la espiga viral mediante la introducción de un enlace disulfuro entre subunidades y una mutación de isoleucina a prolina ( reemplazo radical de un aminoácido) en gp41. [34] Los llamados trímeros SOSIP no solo reproducen las propiedades antigénicas del pico viral nativo, sino que también muestran el mismo grado de glucanos inmaduros que se presentan en el virus nativo. [35] Los picos virales triméricos recombinantes son candidatos a vacunas prometedores, ya que muestran menos epítopos no neutralizantes que la gp120 monomérica recombinante, que actúa para suprimir la respuesta inmune a los epítopos diana. [36]

El genoma de ARN consta de al menos siete puntos de referencia estructurales ( LTR , TAR , RRE , PE, SLIP, CRS e INS) y nueve genes ( gag , pol y env , tat , rev , nef , vif , vpr , vpu , y en ocasiones un décimo tev , que es una fusión de tat , env y rev ), que codifica 19 proteínas. Tres de estos genes, gag , pol y env , contienen información necesaria para producir las proteínas estructurales de las nuevas partículas virales. [24] Por ejemplo, env codifica una proteína llamada gp160 que es cortada en dos por una proteasa celular para formar gp120 y gp41. Los seis genes restantes, tat , rev , nef , vif , vpr y vpu (o vpx en el caso del VIH-2), son genes reguladores de proteínas que controlan la capacidad del VIH para infectar células y producir nuevas copias del virus ( replicarse) o causar enfermedades. [24]
Las dos proteínas tat (p16 y p14) son transactivadores transcripcionales del promotor LTR que actúa uniendo el elemento TAR RNA. El TAR también puede procesarse en microARN que regulan los genes de apoptosis ERCC1 e IER3 . [37] [38] La proteína rev (p19) participa en el transporte de ARN desde el núcleo y el citoplasma uniéndose al elemento de ARN RRE . La proteína vif (p23) previene la acción de APOBEC3G (una proteína celular que desamina la citidina a uridina en el ADN viral monocatenario y/o interfiere con la transcripción inversa [39] ). La proteína vpr (p14) detiene la división celular en G2/M . La proteína nef (p27) regula negativamente el CD4 (el principal receptor viral), así como las moléculas MHC de clase I y clase II . [40] [41] [42]
Nef también interactúa con dominios SH3 . La proteína vpu (p16) influye en la liberación de nuevas partículas virales de las células infectadas. [24] Los extremos de cada hebra de ARN del VIH contienen una secuencia de ARN llamada repetición terminal larga (LTR). Las regiones de la LTR actúan como interruptores para controlar la producción de nuevos virus y pueden ser activadas por proteínas del VIH o de la célula huésped. El elemento Psi participa en el empaquetado del genoma viral y es reconocido por las proteínas gag y rev . El elemento SLIP (TTTTTT) está implicado en el cambio de marco en el marco de lectura de gag - pol necesario para hacer que pol sea funcional . [24]
El término tropismo viral se refiere a los tipos de células que infecta un virus. El VIH puede infectar una variedad de células inmunitarias, como las células T CD4 + , los macrófagos y las células microgliales . La entrada del VIH-1 a los macrófagos y las células T CD4 + está mediada por la interacción de las glicoproteínas de la envoltura del virión (gp120) con la molécula CD4 en la membrana de las células diana y también con los correceptores de quimiocinas . [25] [43]
Las cepas con trópico de macrófagos (trópico M) del VIH-1, o cepas no inductoras de sincitios (NSI; ahora denominadas virus R5 [44] ), utilizan el receptor de quimiocina β , CCR5 , para entrar y, por tanto, son capaces de replicarse en tanto macrófagos como células T CD4 + . [45] Este correceptor CCR5 es utilizado por casi todos los aislados primarios de VIH-1 independientemente del subtipo genético viral. De hecho, los macrófagos desempeñan un papel clave en varios aspectos críticos de la infección por VIH. Parecen ser las primeras células infectadas por el VIH y quizás la fuente de producción del VIH cuando las células CD4 + se agotan en el paciente. Los macrófagos y las células microgliales son las células infectadas por el VIH en el sistema nervioso central . En las amígdalas y adenoides de los pacientes infectados por el VIH, los macrófagos se fusionan formando células gigantes multinucleadas que producen enormes cantidades de virus.
Las cepas T-trópicas del VIH-1, o cepas inductoras de sincitios (SI; ahora llamadas virus X4 [44] ) se replican en células T CD4 + primarias , así como en macrófagos y utilizan el receptor de quimiocina α , CXCR4 , para entrar. [45] [46] [47]
Se cree que las cepas de VIH-1 de trópico dual son cepas de transición de VIH-1 y, por lo tanto, pueden utilizar tanto CCR5 como CXCR4 como correceptores para la entrada viral.
La α -quimiocina SDF-1 , un ligando para CXCR4, suprime la replicación de aislados de VIH-1 con tropismo T. Lo hace regulando negativamente la expresión de CXCR4 en la superficie de las células diana del VIH. Los aislados de VIH-1 con trópico M que utilizan sólo el receptor CCR5 se denominan R5; los que utilizan sólo CXCR4 se denominan X4 y los que utilizan ambos, X4R5. Sin embargo, el uso de correceptores por sí solo no explica el tropismo viral, ya que no todos los virus R5 pueden usar CCR5 en macrófagos para una infección productiva [45] y el VIH también puede infectar un subtipo de células dendríticas mieloides , [48] que Probablemente constituyen un reservorio que mantiene la infección cuando el número de células T CD4 + ha disminuido a niveles extremadamente bajos.
Algunas personas son resistentes a ciertas cepas del VIH. [49] Por ejemplo, las personas con la mutación CCR5-Δ32 son resistentes a la infección por el virus R5, ya que la mutación deja al VIH incapaz de unirse a este correceptor, lo que reduce su capacidad para infectar las células diana.
Las relaciones sexuales son el principal modo de transmisión del VIH. Tanto el VIH X4 como el R5 están presentes en el líquido seminal , lo que permite que el virus se transmita del hombre a su pareja sexual . Los viriones pueden entonces infectar numerosos objetivos celulares y diseminarse por todo el organismo. Sin embargo, un proceso de selección [ se necesita más explicación ] conduce a una transmisión predominante del virus R5 a través de esta vía. [50] [51] [52] En pacientes infectados con el subtipo B del VIH-1, a menudo hay un cambio de correceptor en la etapa tardía de la enfermedad y variantes con trópico T que pueden infectar una variedad de células T a través de CXCR4. [53] Estas variantes luego se replican de manera más agresiva con mayor virulencia que causa un rápido agotamiento de las células T, colapso del sistema inmunológico e infecciones oportunistas que marcan la llegada del SIDA. [54] Los pacientes VIH positivos adquieren un espectro enormemente amplio de infecciones oportunistas, lo cual era particularmente problemático antes del inicio de las terapias TARGA ; sin embargo, se reportan las mismas infecciones entre pacientes infectados por el VIH examinados post mortem después del inicio de terapias antirretrovirales. [3] Por lo tanto, durante el curso de la infección, la adaptación viral al uso de CXCR4 en lugar de CCR5 puede ser un paso clave en la progresión hacia el SIDA. Varios estudios con individuos infectados con el subtipo B han determinado que entre el 40 y el 50 por ciento de los pacientes con SIDA pueden albergar virus del fenotipo SI y, se supone, del fenotipo X4. [55] [56]
El VIH-2 es mucho menos patógeno que el VIH-1 y su distribución mundial está restringida a África occidental . La adopción de "genes accesorios" por parte del VIH-2 y su patrón más promiscuo de uso de correceptores (incluida la independencia de CD4) puede ayudar al virus en su adaptación para evitar factores de restricción innatos presentes en las células huésped. La adaptación para utilizar maquinaria celular normal para permitir la transmisión y la infección productiva también ha ayudado al establecimiento de la replicación del VIH-2 en humanos. Una estrategia de supervivencia para cualquier agente infeccioso no es matar a su huésped, sino convertirse en última instancia en un organismo comensal . Una vez alcanzada una patogenicidad baja, con el tiempo se seleccionarán variantes que tengan más éxito en la transmisión. [57]
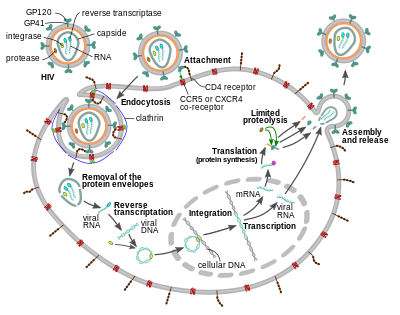

El virión del VIH ingresa a los macrófagos y a las células T CD4 + mediante la adsorción de glicoproteínas en su superficie a los receptores de la célula diana, seguido de la fusión de la envoltura viral con la membrana de la célula diana y la liberación de la cápside del VIH en la célula. [58] [59]
La entrada a la célula comienza mediante la interacción del complejo de envoltura trimérica ( gp160 pico) en la envoltura viral del VIH y tanto CD4 como un correceptor de quimiocina (generalmente CCR5 o CXCR4 , pero se sabe que otros interactúan) en la superficie de la célula objetivo. [58] [59] Gp120 se une a la integrina α 4 β 7 activando LFA-1 , la integrina central involucrada en el establecimiento de sinapsis virológicas , que facilitan la propagación eficiente del VIH-1 de célula a célula. [60] El pico gp160 contiene dominios de unión para los receptores CD4 y de quimiocinas. [58] [59]
El primer paso en la fusión implica la unión de alta afinidad de los dominios de unión a CD4 de gp120 a CD4. Una vez que gp120 se une a la proteína CD4, el complejo de envoltura sufre un cambio estructural, exponiendo los dominios de unión del receptor de quimiocinas de gp120 y permitiéndoles interactuar con el receptor de quimiocina objetivo. [58] [59] Esto permite una unión doble más estable, que permite que el péptido de fusión N-terminal gp41 penetre en la membrana celular. [58] [59] Las secuencias repetidas en gp41, HR1 y HR2 luego interactúan, provocando el colapso de la porción extracelular de gp41 en forma de horquilla. Esta estructura de bucle acerca el virus y las membranas celulares, lo que permite la fusión de las membranas y la posterior entrada de la cápside viral. [58] [59]
Una vez que el VIH se ha unido a la célula diana, se inyectan en la célula el ARN del VIH y varias enzimas, incluidas la transcriptasa inversa, la integrasa, la ribonucleasa y la proteasa. [58] [ verificación fallida ] Durante el transporte basado en microtúbulos al núcleo, el genoma viral de ARN monocatenario se transcribe en ADN bicatenario, que luego se integra en un cromosoma del huésped.
El VIH puede infectar células dendríticas (CD) por esta ruta CD4-CCR5, pero también se puede usar otra ruta que utiliza receptores de lectina tipo C específicos de manosa, como DC-SIGN . [61] Las CD son una de las primeras células que encuentra el virus durante la transmisión sexual. Actualmente se cree que desempeñan un papel importante al transmitir el VIH a las células T cuando las CD capturan el virus en la mucosa . [61] Se cree que la presencia de FEZ-1 , que se produce naturalmente en las neuronas , previene la infección de las células por el VIH. [62]

Durante mucho tiempo se ha creído que la entrada del VIH-1, así como de muchos otros retrovirus, se produce exclusivamente en la membrana plasmática. Más recientemente, sin embargo, también se ha informado de una infección productiva por endocitosis del VIH-1 mediada por clatrina, independiente del pH , y recientemente se ha sugerido que constituye la única vía de entrada productiva. [63] [64] [65] [66] [67]

Poco después de que la cápside viral ingresa a la célula, una enzima llamada transcriptasa inversa libera el genoma de ARN monocatenario de sentido positivo de las proteínas virales unidas y lo copia en una molécula de ADN complementario (ADNc). [68] El proceso de transcripción inversa es extremadamente propenso a errores y las mutaciones resultantes pueden causar resistencia a los medicamentos o permitir que el virus evada el sistema inmunológico del cuerpo. La transcriptasa inversa también tiene actividad ribonucleasa que degrada el ARN viral durante la síntesis de ADNc, así como actividad ADN polimerasa dependiente de ADN que crea un ADN sentido a partir del ADNc antisentido . [69] Juntos, el ADNc y su complemento forman un ADN viral de doble hebra que luego se transporta al núcleo celular . La integración del ADN viral en el genoma de la célula huésped se lleva a cabo mediante otra enzima viral llamada integrasa . [68]
El ADN viral integrado puede entonces permanecer inactivo, en la fase latente de la infección por VIH. [68] Para producir activamente el virus, es necesario que estén presentes ciertos factores de transcripción celular, el más importante de los cuales es el NF- κ B (factor nuclear kappa B), que se regula positivamente cuando las células T se activan. [70] Esto significa que las células con mayor probabilidad de ser atacadas, penetradas y posteriormente destruidas por el VIH son aquellas que luchan activamente contra la infección.
Durante la replicación viral, el provirus de ADN integrado se transcribe en ARN. Los ARN genómicos de longitud completa (ARNg) se pueden empaquetar en nuevas partículas virales en forma pseudodiploide . La selectividad en el empaquetamiento se explica por las propiedades estructurales del confórmero dimérico del ARNg. El dímero de ARNg se caracteriza por una unión en tándem de tres vías dentro del monómero de ARNg, en la que las horquillas SD y AUG , responsables del empalme y la traducción respectivamente, están secuestradas y la horquilla DIS (señal de inicio de dimerización) queda expuesta. La formación del dímero de ARNg está mediada por una interacción de "beso" entre los bucles en horquilla DIS de los monómeros de ARNg. Al mismo tiempo, ciertos residuos de guanosina en el ARNg quedan disponibles para la unión de la proteína de la nucleocápside (NC), lo que conduce al posterior ensamblaje del virión. [71] También se ha informado que el dímero de ARNg lábil logra una conformación más estable después de la unión NC, en la que tanto las regiones DIS como U5:AUG del ARNg participan en un emparejamiento de bases extenso. [72]
El ARN también se puede procesar para producir ARN mensajeros maduros (ARNm). En la mayoría de los casos, este procesamiento implica el empalme del ARN para producir ARNm que son más cortos que el genoma completo. La parte del ARN que se elimina durante el corte y empalme del ARN determina cuál de las secuencias codificantes de proteínas del VIH se traduce. [73]
Los ARNm del VIH maduros se exportan desde el núcleo al citoplasma , donde se traducen para producir proteínas del VIH, incluida Rev. A medida que se produce la proteína Rev recién producida, se mueve hacia el núcleo, donde se une a copias completas y no empalmadas de los ARN del virus y les permite salir del núcleo. [74] Algunos de estos ARN de longitud completa funcionan como ARNm que se traducen para producir las proteínas estructurales Gag y Env. Las proteínas Gag se unen a copias del genoma de ARN del virus para empaquetarlas en nuevas partículas virales. [75] El VIH-1 y el VIH-2 parecen empaquetar su ARN de manera diferente. [76] [77] El VIH-1 se unirá a cualquier ARN apropiado. [78] El VIH-2 se unirá preferentemente al ARNm que se utilizó para crear la propia proteína Gag. [79]
En cada partícula de VIH-1 se encapsidan dos genomas de ARN (ver Estructura y genoma del VIH ). Tras la infección y la replicación catalizada por la transcriptasa inversa, puede ocurrir la recombinación entre los dos genomas. [80] [81] La recombinación se produce cuando los genomas de ARN monocatenario de sentido positivo se transcriben de forma inversa para formar ADN. Durante la transcripción inversa, el ADN naciente puede cambiar varias veces entre las dos copias del ARN viral. Esta forma de recombinación se conoce como elección de copia. Pueden ocurrir eventos de recombinación en todo el genoma. Pueden ocurrir entre dos y 20 eventos de recombinación por genoma en cada ciclo de replicación, y estos eventos pueden mezclar rápidamente la información genética que se transmite desde los genomas de los padres a los de la progenie. [81]
La recombinación viral produce una variación genética que probablemente contribuya a la evolución de la resistencia a la terapia antirretroviral . [82] La recombinación también puede contribuir, en principio, a superar las defensas inmunitarias del huésped. Sin embargo, para que se realicen las ventajas adaptativas de la variación genética, los dos genomas virales empaquetados en partículas de virus infectantes individuales deben haber surgido de virus parentales progenitores separados de constitución genética diferente. Se desconoce con qué frecuencia se producen estos envases mixtos en condiciones naturales. [83]
Bonhoeffer et al. [84] sugirieron que el cambio de plantilla mediante la transcriptasa inversa actúa como un proceso de reparación para abordar las roturas en el genoma del ARN monocatenario. Además, Hu y Temin [80] sugirieron que la recombinación es una adaptación para la reparación de daños en los genomas de ARN. El cambio de cadena (recombinación de elección de copia) mediante la transcriptasa inversa podría generar una copia intacta de ADN genómico a partir de dos copias del genoma de ARN monocatenario dañadas. Esta visión del beneficio adaptativo de la recombinación en el VIH podría explicar por qué cada partícula de VIH contiene dos genomas completos, en lugar de uno. Además, la opinión de que la recombinación es un proceso de reparación implica que el beneficio de la reparación puede ocurrir en cada ciclo de replicación, y que este beneficio puede lograrse independientemente de que los dos genomas difieran genéticamente o no. Desde el punto de vista de que la recombinación en el VIH es un proceso de reparación, la generación de variación recombinacional sería una consecuencia, pero no la causa, de la evolución del cambio de plantilla. [84]
La infección por VIH-1 provoca inflamación crónica y producción de especies reactivas de oxígeno . [85] Por lo tanto, el genoma del VIH puede ser vulnerable al daño oxidativo , incluidas roturas en el ARN monocatenario. Para el VIH, así como para los virus en general, la infección exitosa depende de superar las estrategias de defensa del huésped que a menudo incluyen la producción de especies reactivas de oxígeno que dañan el genoma. Así, Michod et al. [86] sugirieron que la recombinación de los virus es una adaptación para reparar el daño del genoma, y que la variación recombinacional es un subproducto que puede proporcionar un beneficio separado.
El paso final del ciclo viral, el ensamblaje de nuevos viriones del VIH-1, comienza en la membrana plasmática de la célula huésped. La poliproteína Env (gp160) atraviesa el retículo endoplásmico y se transporta al aparato de Golgi , donde la furina la escinde , lo que da como resultado las dos glicoproteínas de la envoltura del VIH, gp41 y gp120 . [87] Estos se transportan a la membrana plasmática de la célula huésped donde gp41 ancla gp120 a la membrana de la célula infectada. Las poliproteínas Gag (p55) y Gag-Pol (p160) también se asocian con la superficie interna de la membrana plasmática junto con el ARN genómico del VIH a medida que el virión en formación comienza a brotar de la célula huésped. El virión en ciernes aún está inmaduro, ya que las poliproteínas gag aún deben escindirse en las proteínas de la matriz, la cápside y la nucleocápside. Esta escisión está mediada por la proteasa viral empaquetada y puede ser inhibida por fármacos antirretrovirales de la clase de inhibidores de proteasa . Luego, los diversos componentes estructurales se ensamblan para producir un virión de VIH maduro. [88] Sólo los viriones maduros pueden infectar otra célula.

El proceso clásico de infección de una célula por un virión puede denominarse "propagación libre de células" para distinguirlo de un proceso reconocido más recientemente llamado "propagación de célula a célula". [89] En la propagación libre de células (ver figura), las partículas de virus brotan de una célula T infectada, ingresan a la sangre o al líquido extracelular y luego infectan otra célula T después de un encuentro casual. [89] El VIH también puede diseminarse mediante transmisión directa de una célula a otra mediante un proceso de diseminación de célula a célula, para el cual se han descrito dos vías. En primer lugar, una célula T infectada puede transmitir el virus directamente a una célula T objetivo a través de una sinapsis virológica . [60] [90] En segundo lugar, una célula presentadora de antígeno (APC), como un macrófago o una célula dendrítica, puede transmitir el VIH a las células T mediante un proceso que implica una infección productiva (en el caso de los macrófagos) o una captura y transferencia. de viriones en trans (en el caso de células dendríticas). [91] Cualquiera que sea la vía que se utilice, se informa que la infección por transferencia de célula a célula es mucho más eficiente que la propagación de virus libres de células. [92] Varios factores contribuyen a esta mayor eficiencia, incluido el virus polarizado que brota hacia el sitio de contacto entre células, la aposición cercana de las células, que minimiza la difusión de los viriones en fase fluida, y la agrupación de los receptores de entrada del VIH en la fase fluida. celda objetivo hacia la zona de contacto. [90] Se cree que la diseminación de célula a célula es particularmente importante en los tejidos linfoides , donde las células T CD4 + están densamente empaquetadas y es probable que interactúen con frecuencia. [89] Los estudios de imágenes intravitales han respaldado el concepto de sinapsis virológica del VIH in vivo . [93] Los numerosos mecanismos de diseminación disponibles para el VIH contribuyen a la replicación continua del virus a pesar de las terapias antirretrovirales. [89] [94]

El VIH se diferencia de muchos virus en que tiene una variabilidad genética muy alta . Esta diversidad es el resultado de su rápido ciclo de replicación, con la generación de aproximadamente 10 10 viriones cada día, junto con una alta tasa de mutación de aproximadamente 3 x 10 −5 por base de nucleótido por ciclo de replicación y propiedades recombinogénicas de la transcriptasa inversa. [95] [96] [97]
Este complejo escenario lleva a la generación de muchas variantes del VIH en un solo paciente infectado en el transcurso de un día. [95] Esta variabilidad se agrava cuando una sola célula es infectada simultáneamente por dos o más cepas diferentes de VIH. Cuando se produce una infección simultánea , el genoma de la progenie de los viriones puede estar compuesto por cadenas de ARN de dos cepas diferentes. Este virión híbrido luego infecta una nueva célula donde se replica. Mientras esto sucede, la transcriptasa inversa, al saltar hacia adelante y hacia atrás entre las dos plantillas de ARN diferentes, generará una secuencia de ADN retroviral recién sintetizada que es recombinante entre los dos genomas parentales. [95] Esta recombinación es más obvia cuando ocurre entre subtipos. [95]
El virus de la inmunodeficiencia simia (VIS), estrechamente relacionado, ha evolucionado en muchas cepas, clasificadas según la especie huésped natural. Se cree que las cepas SIV del mono verde africano (SIVagm) y del mangabey hollín (SIVsmm) tienen una larga historia evolutiva con sus huéspedes. Estos huéspedes se han adaptado a la presencia del virus, [98] que está presente en niveles elevados en la sangre del huésped, pero que sólo provoca una respuesta inmune leve, [99] no causa el desarrollo del SIDA en los simios, [100] y no no sufren la extensa mutación y recombinación típicas de la infección por VIH en humanos. [101]
En cambio, cuando estas cepas infectan especies que no se han adaptado al VIS (huéspedes "heterólogos" o similares como los macacos rhesus o cynomologus ), los animales desarrollan SIDA y el virus genera una diversidad genética similar a la que se observa en la infección humana por VIH. [102] El VIS de chimpancé (SIVcpz), el pariente genético más cercano del VIH-1, se asocia con una mayor mortalidad y síntomas similares al SIDA en su huésped natural. [103] El SIVcpz parece haberse transmitido relativamente recientemente a poblaciones de chimpancés y humanos, por lo que sus huéspedes aún no se han adaptado al virus. [98] Este virus también ha perdido una función del gen nef que está presente en la mayoría de los VIS. Para las variantes de VIS no patógenas, nef suprime la activación de las células T a través del marcador CD3 . La función de Nef en formas no patógenas de VIS es regular negativamente la expresión de citoquinas inflamatorias , MHC-1 , y señales que afectan el tráfico de células T. En VIH-1 y SIVcpz, nef no inhibe la activación de las células T y ha perdido esta función. Sin esta función, es más probable que se agoten las células T, lo que conduce a una inmunodeficiencia. [103] [104]
Se han identificado tres grupos de VIH-1 en función de las diferencias en la región de la envoltura ( env ): M, N y O. [105] El grupo M es el más prevalente y se subdivide en ocho subtipos (o clados ), según en todo el genoma, que son geográficamente distintos. [106] Los más prevalentes son los subtipos B (que se encuentran principalmente en América del Norte y Europa), A y D (que se encuentran principalmente en África) y C (que se encuentran principalmente en África y Asia); estos subtipos forman ramas en el árbol filogenético que representa el linaje del grupo M del VIH-1. La coinfección con distintos subtipos da lugar a formas recombinantes circulantes (CRF). En 2000, último año en el que se realizó un análisis de la prevalencia global de subtipos, el 47,2% de las infecciones en todo el mundo fueron del subtipo C, el 26,7% fueron del subtipo A/CRF02_AG, el 12,3% fueron del subtipo B, el 5,3% fueron del subtipo D, El 3,2% eran de CRF_AE, y el 5,3% restante estaban compuestos por otros subtipos y CRF. [107] La mayor parte de la investigación sobre el VIH-1 se centra en el subtipo B; pocos laboratorios se centran en los otros subtipos. [108] Se ha planteado la hipótesis de la existencia de un cuarto grupo, "P", basándose en un virus aislado en 2009. [109] [110] La cepa aparentemente deriva del gorila SIV (SIVgor), aislado por primera vez de gorilas de tierras bajas occidentales en 2006. [109]
El pariente más cercano del VIH-2 es el SIVsm, una cepa de SIV que se encuentra en los mangabees hollín. Dado que el VIH-1 se deriva de SIVcpz y el VIH-2 de SIVsm, la secuencia genética del VIH-2 es sólo parcialmente homóloga al VIH-1 y se parece más a la de SIVsm. [111] [112]
Muchas personas VIH positivas no saben que están infectadas con el virus. [113] Por ejemplo, en 2001, menos del 1% de la población urbana sexualmente activa de África se había sometido a pruebas, y esta proporción es aún menor en las poblaciones rurales. [113] Además, en 2001 sólo el 0,5% de las mujeres embarazadas que acudían a centros de salud urbanos recibieron asesoramiento, pruebas o recibieron los resultados de las mismas. [113] Nuevamente, esta proporción es aún menor en los establecimientos de salud rurales. [113] Dado que los donantes pueden, por lo tanto, desconocer su infección, la sangre y los productos sanguíneos de los donantes utilizados en medicina e investigación médica se examinan de forma rutinaria para detectar el VIH. [114]
La prueba del VIH-1 se realiza inicialmente mediante un ensayo inmunoabsorbente ligado a enzimas (ELISA) para detectar anticuerpos contra el VIH-1. Las muestras con un resultado no reactivo del ELISA inicial se consideran VIH negativas, a menos que se haya producido una nueva exposición a una pareja infectada o con un estado serológico desconocido. Las muestras con un resultado ELISA reactivo se vuelven a analizar por duplicado. [115] Si el resultado de cualquiera de las pruebas duplicadas es reactivo, la muestra se informa como reactiva repetidamente y se somete a pruebas de confirmación con una prueba complementaria más específica (p. ej., una reacción en cadena de la polimerasa (PCR), Western blot o, menos comúnmente, una prueba de inmunofluorescencia ). ensayo (IFA)). Sólo las muestras que son reactivas repetidamente mediante ELISA y positivas mediante IFA o PCR o reactivas mediante Western blot se consideran VIH positivas e indicativas de infección por VIH. Las muestras que reaccionan repetidamente con ELISA ocasionalmente proporcionan un resultado de Western blot indeterminado, que puede ser una respuesta incompleta de anticuerpos al VIH en una persona infectada o reacciones inespecíficas en una persona no infectada. [116]
Aunque la IFA se puede utilizar para confirmar la infección en estos casos ambiguos, esta prueba no se utiliza ampliamente. En general, se debe recolectar una segunda muestra más de un mes después y volver a analizarla en personas con resultados indeterminados de la prueba Western Blot. Aunque son mucho menos comunes, las pruebas de ácido nucleico (p. ej., método de amplificación de ARN viral o ADN proviral) también pueden ayudar al diagnóstico en determinadas situaciones. [115] Además, algunas muestras analizadas pueden proporcionar resultados no concluyentes debido a una cantidad baja de muestras. En estas situaciones, se recolecta una segunda muestra y se analiza para detectar infección por VIH.
Las pruebas modernas del VIH son extremadamente precisas si se tiene en cuenta el período ventana . Una sola prueba de detección es correcta más del 99% de las veces. [118] Se estima que la probabilidad de un resultado falso positivo en un protocolo de prueba estándar de dos pasos es de aproximadamente 1 en 250.000 en una población de bajo riesgo. [119] Se recomienda realizar pruebas posteriores a la exposición inmediatamente y luego a las seis semanas, tres meses y seis meses. [120]
Las últimas recomendaciones de los Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. muestran que las pruebas del VIH deben comenzar con una prueba combinada de inmunoensayo para detectar anticuerpos contra el VIH-1 y VIH-2 y el antígeno p24 . Un resultado negativo descarta la exposición al VIH, mientras que uno positivo debe ir seguido de un inmunoensayo de diferenciación de anticuerpos VIH-1/2 para detectar qué anticuerpos están presentes. Esto da lugar a cuatro escenarios posibles:
La investigación sobre el VIH/SIDA incluye toda la investigación médica que intenta prevenir, tratar o curar el VIH/SIDA , así como la investigación fundamental sobre la naturaleza del VIH como agente infeccioso y el SIDA como la enfermedad causada por el VIH.
Muchos gobiernos e instituciones de investigación participan en la investigación del VIH/SIDA. Esta investigación incluye intervenciones de salud conductual , como investigaciones sobre educación sexual y desarrollo de medicamentos , como investigaciones sobre microbicidas para enfermedades de transmisión sexual , vacunas contra el VIH y medicamentos antirretrovirales . [122] Otras áreas de investigación médica incluyen los temas de profilaxis previa a la exposición , profilaxis posterior a la exposición , circuncisión y efectos del envejecimiento acelerado .
El tratamiento del VIH/SIDA normalmente incluye el uso de múltiples medicamentos antirretrovirales . En muchas partes del mundo, el VIH se ha convertido en una enfermedad crónica en la que la progresión al SIDA es cada vez más rara.
La latencia del VIH, y el consiguiente reservorio viral en las células T CD4 + , las células dendríticas y los macrófagos, es la principal barrera para la erradicación del virus. [19] [123]
Aunque el VIH es muy virulento, la transmisión no se produce a través del sexo cuando una persona VIH positiva tiene una carga viral constantemente indetectable (<50 copias/ml) debido al tratamiento antirretroviral. Esto fue argumentado por primera vez por la Comisión Federal Suiza para el SIDA/VIH en 2008 en la Declaración Suiza , aunque la declaración fue controvertida en ese momento. [124] [125] Sin embargo, después de múltiples estudios, quedó claro que la posibilidad de transmitir el VIH a través del sexo es efectivamente nula cuando la persona VIH positiva tiene una carga viral consistentemente indetectable; esto se conoce como U=U, "Indetectable=Intransmisible", también expresado como "no se puede transmitir". [126] [127] Los estudios que demuestran que U = U son: Los opuestos se atraen, [128] SOCIO 1, [129] SOCIO 2, [5] [130] (para parejas hombre-hombre) [131] y HPTN052 [132] (para parejas heterosexuales) cuando "la pareja que vive con VIH tenía una carga viral suprimida de forma duradera". [131] En estos estudios, se inscribieron parejas en las que uno de los miembros de la pareja era VIH positivo y el otro VIH negativo y se realizaron pruebas periódicas del VIH. En total, de los cuatro estudios, se inscribieron 4.097 parejas en cuatro continentes y se informaron 151.880 actos sexuales sin condón; No hubo transmisiones de VIH relacionadas filogenéticamente en las que la pareja positiva tuviera una carga viral indetectable. [133] Después de esto, la declaración de consenso U=U que abogaba por el uso del "riesgo cero" fue firmada por cientos de personas y organizaciones, incluidos los CDC de EE. UU ., la Asociación Británica del VIH y la revista médica The Lancet . [134] La importancia de los resultados finales del estudio PARTNER 2 fue descrita por el director médico de Terrence Higgins Trust como "imposible de exagerar", mientras que la autora principal, Alison Rodger, declaró que el mensaje de que "una carga viral indetectable hace que el VIH sea intransmisible". .. puede ayudar a poner fin a la pandemia del VIH al prevenir la transmisión del VIH. [135] Los autores resumieron sus hallazgos en The Lancet de la siguiente manera: [5]
Nuestros resultados proporcionan un nivel de evidencia similar sobre la supresión viral y el riesgo de transmisión del VIH para hombres homosexuales al generado previamente para parejas heterosexuales y sugieren que el riesgo de transmisión del VIH en parejas homosexuales a través de relaciones sexuales sin condón cuando se suprime la carga viral del VIH es efectivamente cero. Nuestros hallazgos respaldan el mensaje de la campaña U=U (indetectable es igual a intransmisible) y los beneficios de las pruebas y el tratamiento tempranos del VIH. [5]
Este resultado es consistente con la conclusión presentada por Anthony S. Fauci , director del Instituto Nacional de Alergias y Enfermedades Infecciosas de los Institutos Nacionales de Salud de EE. UU ., y su equipo en un punto de vista publicado en el Journal of the American Medical Association , de que U=U es un método eficaz de prevención del VIH cuando se mantiene una carga viral indetectable. [6] [131]
La reactivación del herpes genital (HSV-2) en personas infectadas con el virus tiene un aumento asociado en las células T CD4+ enriquecidas con CCR-5, así como en las células dendríticas inflamatorias en la submucosa de la piel genital. El tropismo del VIH por las células positivas para CCR-5 explica el aumento de dos a tres veces en la adquisición del VIH entre personas con herpes genital. La medicación antiviral diaria (p. ej., aciclovir) no reduce la inflamación subclínica posterior a la reactivación y, por lo tanto, no confiere un riesgo reducido de adquisición del VIH. [136] [137]
La primera noticia sobre "una nueva enfermedad exótica" apareció el 18 de mayo de 1981 en el periódico gay New York Native . [138]
El SIDA se observó clínicamente por primera vez en 1981 en los Estados Unidos. [139] Los casos iniciales fueron un grupo de usuarios de drogas inyectables y hombres homosexuales sin causa conocida de deterioro de la inmunidad que mostraban síntomas de neumonía por Pneumocystis (PCP o PJP, este último término reconoce que el agente causante ahora se llama Pneumocystis jirovecii ), un Infección oportunista rara que se sabía que ocurría en personas con sistemas inmunológicos muy comprometidos. [140] Poco después, investigadores de la Facultad de Medicina de la Universidad de Nueva York estudiaron a hombres homosexuales que desarrollaban un cáncer de piel previamente poco común llamado sarcoma de Kaposi (KS). [141] [142] Surgieron muchos más casos de PJP y KS, lo que alertó a los Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. y se formó un grupo de trabajo de los CDC para monitorear el brote. [143] Se cree que el primer caso de SIDA descrito retrospectivamente se produjo en Noruega a partir de 1966. [144]
Al principio, los CDC no tenían un nombre oficial para la enfermedad, a menudo se referían a ella por las enfermedades asociadas con ella, por ejemplo, linfadenopatía , la enfermedad que dio nombre originalmente al virus. [145] [146] También utilizaron Sarcoma de Kaposi e infecciones oportunistas , nombre con el que se había creado un grupo de trabajo en 1981. [147] En la prensa general, el término GRID , que significaba inmunodeficiencia relacionada con los homosexuales , había sido acuñado. [148] El CDC, en busca de un nombre y observando las comunidades infectadas, acuñó "la enfermedad 4H", ya que parecía señalar a los homosexuales, consumidores de heroína, hemofílicos y haitianos . [149] [150] Sin embargo, después de determinar que el SIDA no estaba aislado de la comunidad gay , [147] se dio cuenta de que el término GRID era engañoso y el SIDA se introdujo en una reunión en julio de 1982. [151] En septiembre de 1982, el Los CDC comenzaron a utilizar el nombre SIDA. [152]
En 1983, dos grupos de investigación separados dirigidos por el estadounidense Robert Gallo y los investigadores franceses Françoise Barré-Sinoussi y Luc Montagnier declararon de forma independiente que un nuevo retrovirus podría haber estado infectando a pacientes con SIDA y publicaron sus hallazgos en el mismo número de la revista Science . [153] [146] [154] Gallo afirmó que un virus que su grupo había aislado de una persona con SIDA tenía una forma sorprendentemente similar a otros virus linfotrópicos T humanos (HTLV) que su grupo había sido el primero en aislar. Gallo admitió en 1987 que el virus que afirmaba haber descubierto en 1984 era en realidad un virus que le había enviado desde Francia el año anterior. [155] El grupo de Gallo llamó a su virus recién aislado HTLV-III. El grupo de Montagnier aisló un virus de un paciente que presentaba inflamación de los ganglios linfáticos del cuello y debilidad física , dos síntomas clásicos de la infección primaria por VIH. En contradicción con el informe del grupo de Gallo, Montagnier y sus colegas demostraron que las proteínas centrales de este virus eran inmunológicamente diferentes de las del HTLV-I. El grupo de Montagnier nombró a su virus aislado virus asociado a linfadenopatía (LAV). [143] Como estos dos virus resultaron ser iguales, en 1986 LAV y HTLV-III pasaron a llamarse VIH. [156]
Otro grupo que trabajó simultáneamente con los grupos Montagnier y Gallo fue el de Jay A. Levy en la Universidad de California, San Francisco . Descubrió de forma independiente el virus del SIDA en 1983 y lo llamó retrovirus asociado al SIDA (ARV). [157] Este virus era muy diferente del virus informado por los grupos de Montagnier y Gallo. Las cepas de ARV indicaron, por primera vez, la heterogeneidad de los aislados de VIH y varios de ellos siguen siendo ejemplos clásicos del virus del SIDA encontrado en los Estados Unidos. [158]
Se cree que tanto el VIH-1 como el VIH-2 se originaron en primates no humanos en África central occidental y se cree que se transfirieron a los humanos (un proceso conocido como zoonosis ) a principios del siglo XX. [159] [160]
El VIH-1 parece haberse originado en el sur de Camerún a través de la evolución del SIVcpz, un virus de inmunodeficiencia simio (VIS) que infecta a los chimpancés salvajes (el VIH-1 desciende del SIVcpz endémico en la subespecie de chimpancé Pan troglodytes troglodytes ). [161] [162] El pariente más cercano del VIH-2 es SIVsmm, un virus del mangabey hollín ( Cercocebus atys atys ), un mono del Viejo Mundo que vive en el litoral de África occidental (desde el sur de Senegal hasta el oeste de Costa de Marfil ). [21] Los monos del Nuevo Mundo , como el mono búho, son resistentes a la infección por VIH-1, posiblemente debido a una fusión genómica de dos genes de resistencia viral. [163]
Se cree que el VIH-1 saltó la barrera de las especies al menos en tres ocasiones distintas, dando origen a los tres grupos del virus, M, N y O. [164]

Existe evidencia de que los humanos que participan en actividades de carne de animales silvestres , ya sea como cazadores o vendedores de carne de animales silvestres, comúnmente adquieren el VIS. [165] Sin embargo, el VIS es un virus débil y, por lo general, el sistema inmunológico humano lo suprime a las pocas semanas de la infección. Se cree que son necesarias varias transmisiones del virus de un individuo a otro en rápida sucesión para darle tiempo suficiente para mutar en VIH. [166] Además, debido a su tasa de transmisión de persona a persona relativamente baja, solo puede propagarse entre la población en presencia de uno o más canales de transmisión de alto riesgo, que se cree que estaban ausentes en África antes de la siglo 20.
Los canales de transmisión de alto riesgo específicos propuestos, que permitirán que el virus se adapte a los humanos y se propague por toda la sociedad, dependen del momento propuesto para el cruce de animal a humano. Los estudios genéticos del virus sugieren que el ancestro común más reciente del grupo VIH-1 M se remonta a c. 1910 . [167] Los defensores de esta datación vinculan la epidemia de VIH con el surgimiento del colonialismo y el crecimiento de las grandes ciudades coloniales africanas, lo que lleva a cambios sociales, incluidos diferentes patrones de contacto sexual (especialmente parejas múltiples y concurrentes), la expansión de la prostitución y la Alta frecuencia concomitante de enfermedades ulcerosas genitales (como la sífilis ) en las nacientes ciudades coloniales. [168] Si bien las tasas de transmisión del VIH durante las relaciones sexuales vaginales suelen ser bajas, aumentan muchas veces si una de las personas tiene una infección de transmisión sexual que provoca úlceras genitales. Las ciudades coloniales de principios del siglo XX se destacaban por su alta prevalencia de prostitución y úlceras genitales hasta el punto de que en 1928 se pensaba que hasta el 45% de las residentes del este de Leopoldville (actualmente Kinshasa) habían sido prostitutas y en 1933 alrededor del 15%. de todos los residentes de una misma ciudad fueron infectados por una de las formas de sífilis . [168]
El primer caso bien documentado de VIH en un ser humano se remonta a 1959 en el Congo belga . [169] El virus puede haber estado presente en los Estados Unidos ya a mediados o finales de la década de 1960, cuando un hombre de dieciséis años llamado Robert Rayford presentó síntomas en 1966 y murió en 1969. [170]
Una hipótesis alternativa y probablemente complementaria apunta al uso generalizado de prácticas médicas inseguras en África durante los años posteriores a la Segunda Guerra Mundial, como la reutilización no estéril de jeringas de un solo uso durante campañas de vacunación masiva, antibióticos y tratamiento contra la malaria. [166] [171] [172] La investigación sobre el momento del ancestro común más reciente para los grupos M y O del VIH-1, así como sobre los grupos A y B del VIH-2, indica que el VIS ha dado lugar a linajes transmisibles del VIH a lo largo de todo el mundo. el siglo veinte. [173] El momento disperso de estas transmisiones a humanos implica que no se necesita ningún factor externo para explicar la transmisión del VIH entre especies. Esta observación es consistente con las dos opiniones predominantes sobre el origen de las epidemias de VIH, a saber, la transmisión del VIS a humanos durante el sacrificio o matanza de primates infectados, y la expansión colonial de las ciudades del África subsahariana. [173]
{{cite web}}: Mantenimiento CS1: URL no apta ( enlace ){{cite web}}: Mantenimiento CS1: URL no apta ( enlace )El director del NIAID, Anthony S. Fauci, MD, y sus colegas resumen los resultados de grandes ensayos clínicos y estudios de cohortes que validan U=U. El histórico ensayo clínico HPTN 052, financiado por los NIH, demostró que no se producían transmisiones vinculadas del VIH entre parejas heterosexuales serodiferentes al VIH cuando la pareja que vivía con el VIH tenía una carga viral suprimida de forma duradera. Posteriormente, los estudios PARTNER y Opposites Attract confirmaron estos hallazgos y los ampliaron a las parejas de hombres. ... El éxito de U=U como método de prevención del VIH depende de lograr y mantener una carga viral indetectable tomando TAR diariamente según lo prescrito.
El Dr. Marx cree que el acontecimiento crucial fue la introducción en África de millones de jeringas económicas producidas en masa en los años cincuenta. ... Sospecho que el culpable es el crecimiento de las ciudades coloniales. Antes de 1910, ninguna ciudad centroafricana tenía más de 10.000 habitantes. Pero la migración urbana aumentó, aumentando los contactos sexuales y dando lugar a barrios rojos.