Pila eléctrica
[2] Esta energía resulta accesible mediante dos terminales que tiene la pila, llamados polos, electrodos o bornes.
Lo correcto es utilizar el término pila cuando se menciona al dispositivo que posee una sola celda de energía y baterías cuando posee dos o más celdas de energía, aunque según países y contextos los términos pueden intercambiarse o confundirse.
En el primer caso uno encima de otro, “apilados” (en paralelo), y en el segundo adosados lateralmente (en serie), “en batería”— como se sigue haciendo actualmente, para así aumentar la magnitud de los fenómenos eléctricos y poder estudiarlos sistemáticamente La primera pila eléctrica fue la llamada pila voltaica, que fue dada a conocer por Alessandro Volta en 1800 mediante una carta que envió al presidente de la Royal Society londinense.
Su apilamiento conectados en serie permitía aumentar la tensión a voluntad, otro descubrimiento de Volta.
Fue muy apreciada por su estabilidad y su mayor energía, a pesar del gran inconveniente que representa la emisión de humos corrosivos.
Los tipos hasta ahora descritos eran denominados húmedos, pues contenían líquidos, que no solo hacían inconveniente su transporte, sino que solían emitir gases peligrosos y olores desagradables.
La sequedad es relativa, en primer lugar porque un elemento rigurosamente seco no suministraría electricidad alguna, de modo que lo que se encuentra en el interior de las pilas es una pasta o gel, cuya humedad se procura por todos los medios conservar, pero además porque el uso y el paso del tiempo tienden a corroer el contendedor, de modo que la pila puede verter parte de su electrolito al exterior, donde puede atacar a otros metales.
Estas tensiones se miden en vacío, es decir, sin tener ninguna carga externa conectada, y a una temperatura constante de 20 °C.
Las pilas básicamente consisten en dos electrodos metálicos sumergidos en un líquido, sólido o pasta que se llama electrolito.
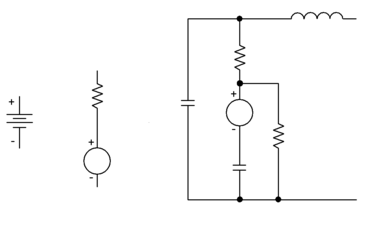
Las propiedades puramente eléctricas de una pila se representan mediante el modelo adjunto.
En circuito abierto, incluso una pila gastada puede indicar 1,4 V, dada la carga insignificante que representa la resistencia de entrada del voltímetro, pero, si la medición se hace con la carga que habitualmente podría soportar, la lectura bajará a 1,0 V o menos, momento en que esa pila ha dejado de tener utilidad.
Cuando se necesita una corriente mayor que la que puede suministrar un elemento único, siendo su tensión en cambio la adecuada, se pueden añadir otros elementos en la conexión llamada en paralelo, es decir, uniendo los polos positivos de todos ellos, por un lado, y los negativos, por otro.
Actualmente, esto no constituye un problema grave pues, dado el enorme consumo que hay de los tipos corrientes, las que se ofrecen en el comercio son de fabricación reciente.
Duran más porque el zinc no está expuesto a un ambiente ácido como el que provocan los iones de amonio en la pila convencional.
Se utilizan para aparatos complejos y de elevado consumo energético.
Esto le confiere mayor duración, más constancia en el tiempo y mejor rendimiento.
Se utiliza en aparatos de mayor consumo como: grabadoras portátiles, juguetes con motor, flashes electrónicos.
El electrolito es una solución de hidróxido potásico (KOH), el cual presenta una resistencia interna bajísima, lo que permite que no se tengan descargas internas y la energía pueda ser acumulada durante mucho tiempo.
Este electrolito, en las pilas comerciales se endurece con gelatinas o derivados de la celulosa.
La pila está sellada con un ojillo o anillo aislante hecho de neopreno.
La envoltura de la pila es químicamente inerte a los ingredientes y forma el electrodo positivo.
Este tipo de baterías presenta algunas desventajas: Juguetes, tocacintas, cámaras fotográficas, grabadoras, linternas, etc.
Con mayor o menor grado, las sustancias son absorbidas por la tierra, pudiéndose filtrar hacia las capas freáticas, y de estas pueden pasar directamente a los seres vivos, entrando con esto en la cadena alimentaria (véase presencia de mercurio en peces).