La noradrenalina ( NE ), también llamada noradrenalina ( NA ) o noradrenalina , es una sustancia química orgánica de la familia de las catecolaminas que funciona en el cerebro y el cuerpo como hormona , neurotransmisor y neuromodulador . El nombre "noradrenalina" (del latín ad , "cerca" y ren , "riñón") se usa más comúnmente en el Reino Unido, mientras que "norepinefrina" (del griego antiguo ἐπῐ́ ( epí ), "sobre" y νεφρός ( nephrós ), "riñón") suele preferirse en los Estados Unidos. [2] "Norepinefrina" es también el nombre común internacional dado al fármaco . [3] Independientemente del nombre que se utilice para la sustancia en sí, las partes del cuerpo que la producen o se ven afectadas por ella se denominan noradrenérgicas .
La función general de la norepinefrina es movilizar el cerebro y el cuerpo para la acción. La liberación de norepinefrina es más baja durante el sueño, aumenta durante la vigilia y alcanza niveles mucho más altos durante situaciones de estrés o peligro, en la llamada respuesta de lucha o huida . En el cerebro, la norepinefrina aumenta la excitación y el estado de alerta, promueve la vigilancia, mejora la formación y recuperación de la memoria y centra la atención; también aumenta la inquietud y la ansiedad. En el resto del cuerpo, la norepinefrina aumenta la frecuencia cardíaca y la presión arterial , desencadena la liberación de glucosa de las reservas de energía, aumenta el flujo sanguíneo al músculo esquelético , reduce el flujo sanguíneo al sistema gastrointestinal e inhibe la evacuación de la vejiga y la motilidad gastrointestinal .
En el cerebro, la noradrenalina se produce en núcleos que son pequeños pero que ejercen efectos poderosos en otras áreas del cerebro. El más importante de estos núcleos es el locus coeruleus , situado en la protuberancia . Fuera del cerebro, la noradrenalina es utilizada como neurotransmisor por los ganglios simpáticos ubicados cerca de la médula espinal o en el abdomen , así como por las células de Merkel ubicadas en la piel. También es liberado directamente al torrente sanguíneo por las glándulas suprarrenales . Independientemente de cómo y dónde se libere, la norepinefrina actúa sobre las células diana uniéndose y activando los receptores adrenérgicos ubicados en la superficie celular.
Una variedad de medicamentos de importancia médica actúan alterando las acciones de los sistemas de noradrenalina. La propia noradrenalina se utiliza ampliamente como fármaco inyectable para el tratamiento de la presión arterial críticamente baja. Los estimulantes a menudo aumentan, mejoran o actúan de otro modo como agonistas de la norepinefrina. Fármacos como la cocaína y el metilfenidato actúan como inhibidores de la recaptación de norepinefrina, al igual que algunos antidepresivos, como los de la clase IRSN . Una de las drogas más notables en la clase de estimulantes es la anfetamina , que actúa como un análogo de la dopamina y la norepinefrina, un inhibidor de la recaptación, así como un agente que aumenta la cantidad de señalización global de catecolaminas en todo el sistema nervioso al invertir los transportadores en las sinapsis. Los betabloqueantes , que contrarrestan algunos de los efectos de la noradrenalina bloqueando sus receptores, se utilizan con frecuencia para tratar el glaucoma , la migraña y una variedad de problemas cardiovasculares. Los alfabloqueantes , que contrarrestan un conjunto diferente de efectos de la noradrenalina, se utilizan para tratar varias afecciones cardiovasculares y psiquiátricas. Los agonistas alfa-2 suelen tener un efecto sedante y se utilizan habitualmente como potenciadores de la anestesia en cirugía, así como en el tratamiento de la dependencia de drogas o alcohol . Por razones que aún no están claras, algunos fármacos alfa-2, como la guanfacina , también han demostrado ser eficaces en el tratamiento de los trastornos de ansiedad y el TDAH . Muchos fármacos psiquiátricos importantes ejercen fuertes efectos sobre los sistemas de noradrenalina del cerebro, lo que produce efectos que pueden ser útiles o perjudiciales.
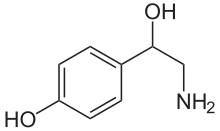
La noradrenalina es una catecolamina y una fenetilamina . [4] Su estructura difiere de la de la epinefrina sólo en que la epinefrina tiene un grupo metilo unido a su nitrógeno, mientras que el grupo metilo es reemplazado por un átomo de hidrógeno en la norepinefrina. [4] El prefijo nor- se deriva como una abreviatura de la palabra "normal", utilizada para indicar un compuesto desmetilado . [5] La noradrenalina consta de un resto catecol (un anillo de benceno con dos grupos hidroxilo contiguos en la posición meta - para ) y una cadena lateral de etilamina que consta de un grupo hidroxilo unido en la posición bencílico. [6] [7]
La noradrenalina se sintetiza a partir del aminoácido tirosina mediante una serie de pasos enzimáticos en la médula suprarrenal y las neuronas posganglionares del sistema nervioso simpático . Mientras que la conversión de tirosina en dopamina ocurre predominantemente en el citoplasma, la conversión de dopamina en norepinefrina por la dopamina β-monooxigenasa ocurre predominantemente dentro de las vesículas de neurotransmisores . [11] La vía metabólica es:
Así, el precursor directo de la noradrenalina es la dopamina , que se sintetiza indirectamente a partir del aminoácido esencial fenilalanina o del aminoácido no esencial tirosina . [11] Estos aminoácidos se encuentran en casi todas las proteínas y, como tales, se obtienen mediante la ingestión de alimentos que contienen proteínas, siendo la tirosina la más común.
La fenilalanina se convierte en tirosina mediante la enzima fenilalanina hidroxilasa , con oxígeno molecular (O 2 ) y tetrahidrobiopterina como cofactores . La tirosina se convierte en L -DOPA mediante la enzima tirosina hidroxilasa , con tetrahidrobiopterina , O 2 y probablemente hierro ferroso (Fe 2+ ) como cofactores. [11] La conversión de tirosina a L -DOPA es inhibida por la metirosina , un análogo de la tirosina. La L -DOPA se convierte en dopamina mediante la enzima L -aminoácido descarboxilasa aromática (también conocida como DOPA descarboxilasa), con piridoxal fosfato como cofactor. [11] Luego, la dopamina se convierte en norepinefrina mediante la enzima dopamina β-monooxigenasa (anteriormente conocida como dopamina β-hidroxilasa ), con O 2 y ácido ascórbico como cofactores. [11]
La propia noradrenalina puede convertirse en epinefrina mediante la enzima feniletanolamina N -metiltransferasa con S -adenosil- L -metionina como cofactor. [11]
En los mamíferos, la norepinefrina se degrada rápidamente a diversos metabolitos . El paso inicial en la descomposición puede ser catalizado por cualquiera de las enzimas monoaminooxidasa (principalmente monoaminooxidasa A ) o COMT . [12] A partir de ahí, el colapso puede proceder por una variedad de vías. Los principales productos finales son el ácido vanililmandélico o una forma conjugada de MHPG , los cuales se cree que son biológicamente inactivos y se excretan en la orina. [13]

Como muchas otras sustancias biológicamente activas, la norepinefrina ejerce sus efectos uniéndose y activando receptores ubicados en la superficie de las células. Se han identificado dos amplias familias de receptores de noradrenalina, conocidos como receptores alfa y beta adrenérgicos. [13] Los receptores alfa se dividen en subtipos α 1 y α 2 ; receptores beta en los subtipos β 1 , β 2 y β 3 . [13] Todos estos funcionan como receptores acoplados a proteína G , lo que significa que ejercen sus efectos a través de un complejo sistema de segundo mensajero . [13] Los receptores alfa-2 generalmente tienen efectos inhibidores, pero muchos están ubicados presinápticamente (es decir, en la superficie de las células que liberan norepinefrina), por lo que el efecto neto de la activación alfa-2 es a menudo una disminución en la cantidad de Se libera norepinefrina. [13] Los receptores alfa-1 y los tres tipos de receptores beta suelen tener efectos excitadores. [13]

Dentro del cerebro la noradrenalina funciona como neurotransmisor y neuromodulador , y está controlada por un conjunto de mecanismos comunes a todos los neurotransmisores monoamino . [14] Después de la síntesis, la norepinefrina es transportada desde el citosol a las vesículas sinápticas mediante el transportador vesicular de monoaminas (VMAT). [15] La reserpina puede inhibir el VMAT, lo que provoca una disminución de las reservas de neurotransmisores. La norepinefrina se almacena en estas vesículas hasta que se expulsa a la hendidura sináptica , normalmente después de que un potencial de acción hace que las vesículas liberen su contenido directamente en la hendidura sináptica mediante un proceso llamado exocitosis . [13]
Una vez en la sinapsis, la noradrenalina se une a los receptores y los activa. Después de un potencial de acción, las moléculas de norepinefrina rápidamente se liberan de sus receptores. Luego se absorben nuevamente en la célula presináptica, mediante recaptación mediada principalmente por el transportador de norepinefrina (NET). [16] Una vez de vuelta en el citosol, la norepinefrina puede ser descompuesta por la monoaminooxidasa o reempaquetada en vesículas por VMAT, dejándola disponible para su futura liberación. [15]

La noradrenalina es el principal neurotransmisor utilizado por el sistema nervioso simpático, que consta de aproximadamente dos docenas de ganglios de la cadena simpática ubicados junto a la médula espinal, además de un conjunto de ganglios prevertebrales ubicados en el pecho y el abdomen. [17] Estos ganglios simpáticos están conectados a numerosos órganos, incluidos los ojos, las glándulas salivales, el corazón, los pulmones, el hígado, la vesícula biliar, el estómago, los intestinos, los riñones, la vejiga urinaria, los órganos reproductivos, los músculos, la piel y las glándulas suprarrenales. [17] La activación simpática de las glándulas suprarrenales hace que la parte llamada médula suprarrenal libere norepinefrina (así como epinefrina) en el torrente sanguíneo, desde el cual, funcionando como una hormona , obtiene mayor acceso a una amplia variedad de tejidos. [17]
En términos generales, el efecto de la norepinefrina en cada órgano objetivo es modificar su estado de manera que lo haga más propicio para el movimiento corporal activo, a menudo a costa de un mayor uso de energía y un mayor desgaste. [18] Esto puede contrastarse con los efectos mediados por la acetilcolina del sistema nervioso parasimpático , que modifica la mayoría de los mismos órganos a un estado más propicio para el descanso, la recuperación y la digestión de los alimentos, y generalmente menos costoso en términos de gasto de energía. . [18]
Los efectos simpáticos de la noradrenalina incluyen:
La noradrenalina y el ATP son cotransmisores simpáticos . Se ha descubierto que el endocannabinoide anandamida y el cannabinoide WIN 55,212-2 pueden modificar la respuesta general a la estimulación del nervio simpático, lo que indica que los receptores CB1 preuncionales median la acción inhibidora del sistema simpático . Por tanto, los cannabinoides pueden inhibir los componentes noradrenérgicos y purinérgicos de la neurotransmisión simpática . [26]

Las neuronas noradrenérgicas del cerebro forman un sistema de neurotransmisores que, cuando se activa, ejerce efectos en grandes áreas del cerebro. Los efectos se manifiestan en estado de alerta, excitación y disposición para la acción.
Las neuronas noradrenérgicas (es decir, neuronas cuyo neurotransmisor principal es la norepinefrina) son comparativamente pocas y sus cuerpos celulares están confinados a unas pocas áreas cerebrales relativamente pequeñas, pero envían proyecciones a muchas otras áreas del cerebro y ejercen efectos poderosos sobre sus objetivos. Estos grupos de células noradrenérgicas fueron mapeados por primera vez en 1964 por Annica Dahlström y Kjell Fuxe, quienes les asignaron etiquetas que comenzaban con la letra "A" (de "aminérgico"). [27] En su esquema, las áreas A1 a A7 contienen el neurotransmisor norepinefrina (A8 a A14 contienen dopamina ). El grupo de células noradrenérgicas A1 se encuentra en la parte ventrolateral caudal de la médula y desempeña un papel en el control del metabolismo de los líquidos corporales. [28] El grupo de células noradrenérgicas A2 está ubicado en un área del tronco del encéfalo llamada núcleo solitario ; Estas células han estado implicadas en una variedad de respuestas, incluido el control de la ingesta de alimentos y las respuestas al estrés. [29] Los grupos celulares A5 y A7 se proyectan principalmente a la médula espinal. [30]
La fuente más importante de norepinefrina en el cerebro es el locus coeruleus , que contiene el grupo de células noradrenérgicas A6 y está junto al grupo de células A4 . El locus coeruleus es bastante pequeño en términos absolutos (en los primates se estima que contiene alrededor de 15.000 neuronas, menos de una millonésima parte de las neuronas del cerebro), pero envía proyecciones a todas las partes principales del cerebro y también a la médula espinal. . [31]
El nivel de actividad en el locus coeruleus se correlaciona ampliamente con la vigilancia y la velocidad de reacción. La actividad de LC es baja durante el sueño y cae prácticamente a nada durante el estado REM (sueño). [32] Se ejecuta en un nivel básico durante la vigilia, pero aumenta temporalmente cuando a una persona se le presenta cualquier tipo de estímulo que llame la atención. Los estímulos desagradables como el dolor, la dificultad para respirar, la distensión de la vejiga, el calor o el frío generan aumentos mayores. Estados extremadamente desagradables, como miedo intenso o dolor intenso, se asocian con niveles muy altos de actividad de LC. [31]
La norepinefrina liberada por el locus coeruleus afecta la función cerebral de varias maneras. Mejora el procesamiento de entradas sensoriales, mejora la atención, mejora la formación y recuperación de la memoria de trabajo y a largo plazo, y mejora la capacidad del cerebro para responder a las entradas cambiando el patrón de actividad en la corteza prefrontal y otras áreas. [33] El control del nivel de excitación es lo suficientemente fuerte como para que la supresión del LC inducida por fármacos tenga un potente efecto sedante. [32]
Existe una gran similitud entre las situaciones que activan el locus coeruleus en el cerebro y las situaciones que activan el sistema nervioso simpático en la periferia: el LC esencialmente moviliza al cerebro para la acción, mientras que el sistema simpático moviliza el cuerpo. Se ha argumentado que esta similitud surge porque ambos están controlados en gran medida por las mismas estructuras cerebrales, particularmente una parte del tronco encefálico llamada núcleo gigantocelular . [31]
La noradrenalina también es producida por las células de Merkel , que forman parte del sistema somatosensorial. Activa la neurona sensorial aferente. [34]
Una gran cantidad de fármacos importantes ejercen sus efectos interactuando con los sistemas de norepinefrina en el cerebro o el cuerpo. Sus usos incluyen el tratamiento de problemas cardiovasculares, shock y una variedad de condiciones psiquiátricas. Estos fármacos se dividen en: fármacos simpaticomiméticos que imitan o potencian al menos algunos de los efectos de la norepinefrina liberada por el sistema nervioso simpático; Los fármacos simpaticolíticos , por el contrario, bloquean al menos algunos de los efectos. [35] Ambos son grandes grupos con diversos usos, dependiendo exactamente de qué efectos se mejoran o bloquean. [35]
La norepinefrina en sí está clasificada como un fármaco simpaticomimético: sus efectos cuando se administra mediante inyección intravenosa aumentan la frecuencia y la fuerza cardíacas y contraen los vasos sanguíneos, lo que la hace muy útil para el tratamiento de emergencias médicas que involucran una presión arterial críticamente baja. [35] La campaña Surviving Sepsis recomendó la norepinefrina como agente de primera línea en el tratamiento del shock séptico que no responde a la reanimación con líquidos , complementada con vasopresina y epinefrina . El uso de dopamina está restringido sólo a pacientes muy seleccionados. [36]
Estos son fármacos simpaticolíticos que bloquean los efectos de los receptores beta adrenérgicos y tienen poco o ningún efecto sobre los receptores alfa. A veces se utilizan para tratar la presión arterial alta , la fibrilación auricular y la insuficiencia cardíaca congestiva , pero revisiones recientes han concluido que otros tipos de fármacos suelen ser superiores para esos fines. [37] [38] Sin embargo, los betabloqueantes pueden ser una opción viable para otras afecciones cardiovasculares, incluidas la angina y el síndrome de Marfan . [39] También se usan ampliamente para tratar el glaucoma , más comúnmente en forma de gotas para los ojos. [40] Debido a sus efectos para reducir los síntomas de ansiedad y los temblores, a veces han sido utilizados por artistas, oradores públicos y atletas para reducir la ansiedad por el desempeño , aunque no están aprobados médicamente para ese propósito y están prohibidos por el Comité Olímpico Internacional . [41] [42]
Sin embargo, la utilidad de los betabloqueantes está limitada por una variedad de efectos secundarios graves, que incluyen disminución de la frecuencia cardíaca, caída de la presión arterial, asma e hipoglucemia reactiva . [40] Los efectos negativos pueden ser particularmente graves en personas con diabetes . [37]
Estos son fármacos simpaticolíticos que bloquean los efectos de los receptores alfa adrenérgicos y tienen poco o ningún efecto sobre los receptores beta. [43] Sin embargo, los medicamentos que pertenecen a este grupo pueden tener efectos muy diferentes, dependiendo de si bloquean principalmente los receptores alfa-1, los receptores alfa-2 o ambos. Los receptores alfa-2, como se describe en otra parte de este artículo, con frecuencia se ubican en las propias neuronas liberadoras de norepinefrina y tienen efectos inhibidores sobre ellas; en consecuencia, el bloqueo de los receptores alfa-2 suele provocar un aumento de la liberación de noradrenalina. [43] Los receptores alfa-1 generalmente se encuentran en las células diana y tienen efectos excitadores sobre ellas; en consecuencia, el bloqueo de los receptores alfa-1 suele provocar el bloqueo de algunos de los efectos de la norepinefrina. [43] Fármacos como la fentolamina que actúan sobre ambos tipos de receptores pueden producir una combinación compleja de ambos efectos. En la mayoría de los casos, cuando el término "alfabloqueante" se utiliza sin calificación, se refiere a un antagonista alfa-1 selectivo.
Los bloqueadores alfa-1 selectivos tienen diversos usos. Dado que uno de sus efectos es inhibir la contracción del músculo liso de la próstata, suelen utilizarse para tratar los síntomas de la hiperplasia prostática benigna . [44] Los alfabloqueantes probablemente también ayuden a las personas a eliminar los cálculos renales. [45] Sus efectos sobre el sistema nervioso central los hacen útiles para tratar el trastorno de ansiedad generalizada , el trastorno de pánico y el trastorno de estrés postraumático . [46] Sin embargo, pueden tener efectos secundarios importantes, incluida una caída de la presión arterial. [43]
Algunos antidepresivos funcionan en parte como bloqueadores alfa-2 selectivos , pero el fármaco más conocido de esa clase es la yohimbina , que se extrae de la corteza del árbol africano yohimbe . [47] La yohimbina actúa como un potenciador de la potencia masculina , pero su utilidad para ese propósito está limitada por efectos secundarios graves que incluyen ansiedad e insomnio. [47] Las sobredosis pueden provocar un aumento peligroso de la presión arterial. [47] La yohimbina está prohibida en muchos países, pero en los Estados Unidos, debido a que se extrae de una planta en lugar de sintetizarse químicamente, se vende sin receta como suplemento nutricional . [48]
Se trata de fármacos simpaticomiméticos que activan los receptores alfa-2 o potencian sus efectos. [49] Debido a que los receptores alfa-2 son inhibidores y muchos están ubicados presinápticamente en las células liberadoras de noradrenalina, el efecto neto de estos fármacos suele ser reducir la cantidad de noradrenalina liberada. [49] Los medicamentos de este grupo que son capaces de ingresar al cerebro a menudo tienen fuertes efectos sedantes, debido a sus efectos inhibidores sobre el locus coeruleus . [49] la clonidina y la guanfacina , por ejemplo, se utilizan para el tratamiento de los trastornos de ansiedad y el insomnio, y también como premedicación sedante para pacientes a punto de someterse a una cirugía. [50] La xilazina , otro fármaco de este grupo, también es un potente sedante y a menudo se utiliza en combinación con ketamina como anestésico general para cirugía veterinaria ; en los Estados Unidos no ha sido aprobado para su uso en humanos. [51]
Se trata de fármacos cuyos efectos primarios se cree que están mediados por diferentes sistemas de neurotransmisores ( dopamina para los estimulantes , serotonina para los antidepresivos ), pero muchos también aumentan los niveles de norepinefrina en el cerebro. [52] La anfetamina , por ejemplo, es un estimulante que aumenta la liberación de noradrenalina y dopamina. [53] Los inhibidores de la monoaminooxidasa A (MAO-A) son antidepresivos que inhiben la degradación metabólica de la norepinefrina, así como de la serotonina y la dopamina. [54] En algunos casos es difícil distinguir los efectos mediados por la noradrenalina de los efectos relacionados con otros neurotransmisores. [ cita necesaria ]
Varios problemas médicos importantes implican una disfunción del sistema de norepinefrina en el cerebro o el cuerpo.
La hiperactivación del sistema nervioso simpático no es una afección reconocida en sí misma, pero es un componente de una serie de afecciones, así como una posible consecuencia de la toma de fármacos simpaticomiméticos . Provoca un conjunto distintivo de síntomas que incluyen dolores y molestias, taquicardia, presión arterial elevada, sudoración, palpitaciones, ansiedad, dolor de cabeza, palidez y caída de la glucosa en sangre. Si la actividad simpática se eleva durante un tiempo prolongado, puede provocar pérdida de peso y otros cambios corporales relacionados con el estrés.
La lista de condiciones que pueden causar hiperactivación simpática incluye lesión cerebral grave, [55] daño de la médula espinal, [56] insuficiencia cardíaca, [57] presión arterial alta, [58] enfermedad renal, [59] y varios tipos de estrés.
Un feocromocitoma es un tumor de la médula suprarrenal que ocurre raramente , causado ya sea por factores genéticos o por ciertos tipos de cáncer. La consecuencia es un aumento masivo en la cantidad de noradrenalina y epinefrina liberadas al torrente sanguíneo. Los síntomas más evidentes son los de hiperactivación simpática, incluido en particular un aumento de la presión arterial que puede alcanzar niveles mortales. El tratamiento más eficaz es la extirpación quirúrgica del tumor.
Estrés , para un fisiólogo, significa cualquier situación que amenace la estabilidad continua del cuerpo y sus funciones. [60] El estrés afecta a una amplia variedad de sistemas corporales: los dos que se activan más consistentemente son el eje hipotalámico-pituitario-suprarrenal y el sistema de noradrenalina, incluidos tanto el sistema nervioso simpático como el sistema centrado en el locus coeruleus en el cerebro. [60] Los factores estresantes de muchos tipos provocan aumentos en la actividad noradrenérgica, que moviliza el cerebro y el cuerpo para enfrentar la amenaza. [60] El estrés crónico, si se continúa durante mucho tiempo, puede dañar muchas partes del cuerpo. Una parte importante del daño se debe a los efectos de la liberación sostenida de noradrenalina, debido a la función general de la noradrenalina de desviar los recursos del mantenimiento, la regeneración y la reproducción, hacia los sistemas necesarios para el movimiento activo. Las consecuencias pueden incluir desaceleración del crecimiento (en niños), insomnio, pérdida de la libido, problemas gastrointestinales, deterioro de la resistencia a las enfermedades, tasas más lentas de curación de lesiones, depresión y mayor vulnerabilidad a la adicción. [60]
El trastorno por déficit de atención con hiperactividad es una afección del desarrollo neurológico que implica problemas de atención, hiperactividad e impulsividad. [61] Se trata más comúnmente con medicamentos estimulantes como el metilfenidato (Ritalin), cuyo efecto principal es aumentar los niveles de dopamina en el cerebro, pero los medicamentos de este grupo generalmente también aumentan los niveles cerebrales de norepinefrina, y ha sido difícil determinarlo. si estas acciones están implicadas en su valor clínico. También existe evidencia sustancial de que muchas personas con TDAH muestran biomarcadores que implican un procesamiento alterado de la norepinefrina. [62] Varios fármacos cuyos efectos principales son sobre la norepinefrina, incluida la guanfacina , la clonidina y la atomoxetina , se han probado como tratamientos para el TDAH y se ha descubierto que tienen efectos comparables a los de los estimulantes. [63] [64]
Varias afecciones, incluida la enfermedad de Parkinson , la diabetes y la llamada insuficiencia autónoma pura , pueden provocar una pérdida de neuronas secretoras de noradrenalina en el sistema nervioso simpático. Los síntomas están muy extendidos, siendo el más grave una reducción de la frecuencia cardíaca y una caída extrema de la presión arterial en reposo, lo que hace imposible que las personas gravemente afectadas permanezcan de pie durante más de unos pocos segundos sin desmayarse. El tratamiento puede implicar cambios en la dieta o medicamentos. [sesenta y cinco]
La norepiprefina previene el sueño REM , y la falta de sueño REM aumenta la secreción de noradrenalina [66] como resultado de que el locus coeruleus no deja de producirla. Provoca neurodegeneración si su pérdida se mantiene durante varios días. [67]
Se ha informado que la noradrenalina existe en una amplia variedad de especies animales, incluidos protozoos , [68] placozoos y cnidarios (medusas y especies relacionadas), [69] pero no en ctenóforos (medusas peine), cuyos sistemas nerviosos difieren mucho de los de otros animales. [70] Generalmente está presente en los deuteróstomos (vertebrados, etc.), pero en los protóstomos (artrópodos, moluscos, platelmintos, nematodos, anélidos, etc.) es reemplazado por octopamina , una sustancia química estrechamente relacionada con una vía de síntesis estrechamente relacionada. [68] En los insectos, la octopamina tiene funciones de alerta y activación que se corresponden (al menos aproximadamente) con las funciones de la noradrenalina en los vertebrados. [71] Se ha argumentado que la octopamina evolucionó para reemplazar la norepinefrina y no al revés ; sin embargo, se ha informado que el sistema nervioso del anfioxo (un cordado primitivo) contiene octopamina pero no noradrenalina, lo que presenta dificultades para esa hipótesis. [68]
A principios del siglo XX, Walter Cannon , que había popularizado la idea de un sistema simpaticoadrenal que preparaba el cuerpo para luchar y huir , y su colega Arturo Rosenblueth desarrollaron una teoría de dos simpatinas , la simpatina E (excitatoria) y la simpatina I (inhibitoria), responsables. para estas acciones. [72] El farmacólogo belga Zénon Bacq , así como farmacólogos canadienses y estadounidenses entre 1934 y 1938 sugirieron que la noradrenalina podría ser un transmisor simpático. [72] En 1939, Hermann Blaschko y Peter Holtz identificaron de forma independiente el mecanismo biosintético de la noradrenalina en el cuerpo de los vertebrados. [73] [74] En 1945, Ulf von Euler publicó el primero de una serie de artículos que establecían el papel de la norepinefrina como neurotransmisor. [75] Demostró la presencia de norepinefrina en los tejidos y el cerebro inervados simpáticamente, y aportó pruebas de que es la simpatina de Cannon y Rosenblueth.
Stanley Peart fue el primero en demostrar la liberación de noradrenalina tras la estimulación de los nervios simpáticos.
Recomendamos la norepinefrina como vasopresor de primera elección (recomendación fuerte, calidad de evidencia moderada).
La inhibición selectiva de MAO-A conduce a niveles aumentados de neurotransmisor dentro de las neuronas noradrenérgicas (NA-érgicas) y 5-HT-érgicas del SNC, y a una acción antidepresiva clínica, mientras que la inhibición de MAO-B conduce a mayores niveles de DA. en el cerebro parkinsoniano...