El subtipo H5N1 del virus de la influenza A (A/H5N1) es un subtipo del virus de la influenza A que puede causar enfermedades en humanos y muchas otras especies. [1] Una cepa de H5N1 adaptada a las aves, llamada HPAI A(H5N1) para el virus de la influenza aviar altamente patógeno de tipo A del subtipo H5N1 , es el agente causante altamente patógeno de la gripe H5N1 , comúnmente conocida como influenza aviar ("gripe aviar" ). Es enzoótico (se mantiene en la población) en muchas poblaciones de aves, especialmente en el sudeste asiático . Una cepa de HPAI A(H5N1) se está propagando globalmente después de haber aparecido por primera vez en Asia. Es epizoótica (una epidemia en no humanos) y panzoótica (que afecta a animales de muchas especies, especialmente en un área amplia), mata a decenas de millones de aves y estimula el sacrificio de cientos de millones de otras para detener su propagación. Muchas referencias a la "gripe aviar" y al H5N1 en los medios populares se refieren a esta cepa. [2]
Según la Organización Mundial de la Salud (OMS) y la Organización de las Naciones Unidas para la Alimentación y la Agricultura , la patogenicidad del H5N1 sigue aumentando gradualmente en las zonas endémicas, pero la situación de la gripe aviar en las aves de granja se está controlando gracias a la vacunación, y hay " "No hay evidencia de transmisión sostenida de persona a persona" del virus. [3] En junio de 2008 se notificaron once brotes de H5N1 en todo el mundo, en cinco países (China, Egipto, Indonesia, Pakistán y Vietnam), en comparación con 65 brotes en junio de 2006 y 55 en junio de 2007. La situación mundial de la IAAP mejoró significativamente en el primer semestre de 2008, pero la FAO informa que los sistemas imperfectos de vigilancia de enfermedades significan que la aparición del virus sigue estando subestimada y subnotificada. [4] En mayo de 2020, la OMS informó un total de 861 casos humanos confirmados que resultaron en la muerte de 455 personas desde 2003. [5]
Varias vacunas contra el H5N1 han sido desarrolladas, aprobadas y almacenadas por varios países, incluidos Estados Unidos (en su Reserva Nacional ), [6] [7] Gran Bretaña, Francia, Canadá y Australia, para su uso en caso de emergencia. [8]
La IAAP A (H5N1) se considera una enfermedad aviar, aunque existe cierta evidencia de transmisión limitada del virus de persona a persona. [9] Un factor de riesgo para contraer el virus es la manipulación de aves de corral infectadas, pero la transmisión del virus de las aves infectadas a los humanos se ha caracterizado como ineficiente. [10] Aún así, alrededor del 60% de los seres humanos que se sabe que han sido infectados con la cepa asiática de HPAI A(H5N1) han muerto a causa de ella, y el H5N1 puede mutar o reagruparse en una cepa capaz de transmitirse eficientemente de persona a persona. En 2003, el virólogo Robert G. Webster publicó un artículo titulado "El mundo se tambalea al borde de una pandemia que podría matar a una gran fracción de la población humana" en American Scientist . Pidió recursos adecuados para luchar contra lo que considera una gran amenaza mundial para posiblemente miles de millones de vidas. [11] El 29 de septiembre de 2005, David Nabarro , el recién nombrado Coordinador Superior del Sistema de las Naciones Unidas para la Influenza Aviar y Humana, advirtió al mundo que un brote de influenza aviar podría matar entre 5 y 150 millones de personas. [12]
Debido a la alta letalidad y virulencia de la IAAP A(H5N1), su presencia endémica, su reservorio huésped cada vez más grande y sus importantes mutaciones en curso, en 2006, el virus H5N1 fue considerado la mayor amenaza pandémica del mundo, y miles de millones de personas Se están gastando dólares en la investigación del H5N1 y en la preparación para una posible pandemia de gripe . [13] Al menos 12 empresas y 17 gobiernos están desarrollando vacunas contra la influenza prepandémica en 28 ensayos clínicos diferentes que, de tener éxito, podrían convertir una infección pandémica mortal en una no mortal. La producción a gran escala de una vacuna que pudiera prevenir cualquier enfermedad causada por esta cepa requeriría al menos tres meses después de la aparición del virus, pero se espera que la producción de vacunas pueda aumentar hasta que se hayan producido mil millones de dosis un año después de la aparición del virus. identificación inicial del virus. [14]
El H5N1 puede causar más de una pandemia de influenza , ya que se espera que continúe mutando en las aves independientemente de si los humanos desarrollan inmunidad colectiva ante una futura cepa pandémica. [15] Las pandemias de influenza a partir de su descendencia genética pueden incluir subtipos del virus de la influenza A distintos del H5N1. [16] Si bien el análisis genético del virus H5N1 muestra que las pandemias de influenza causadas por su descendencia genética pueden ser fácilmente mucho más letales que la pandemia de gripe española , [17] la planificación para una futura pandemia de influenza se basa en lo que se puede hacer y no hay un nivel de índice de gravedad de la pandemia más alto que una pandemia de categoría 5 que, en términos generales, es cualquier pandemia tan mala como la gripe española o peor; y para el cual se deben utilizar todas las medidas de intervención. [18]
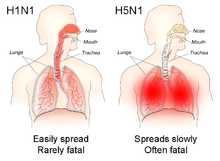
En general, los seres humanos que contraen un virus de la gripe A humanizado (un virus de la gripe humana de tipo A) suelen tener síntomas que incluyen fiebre , tos , dolor de garganta , dolores musculares , conjuntivitis y, en casos graves, problemas respiratorios y neumonía que pueden ser fatal. [20] La gravedad de la infección depende en gran parte del estado del sistema inmunológico de las personas infectadas y de si habían estado expuestas a la cepa antes (en cuyo caso serían parcialmente inmunes). Nadie sabe si estos u otros síntomas serán los síntomas de una gripe H5N1 humanizada.
La hemaglutinina de la influenza aviar se une a los receptores de ácido siálico alfa 2-3 , mientras que las hemaglutininas de la influenza humana se unen a los receptores de ácido siálico alfa 2-6. [21] Esto significa que cuando la cepa H5N1 infecta a los humanos, se replicará en el tracto respiratorio inferior y, en consecuencia, causará neumonía viral . [22] Todavía no existe una forma humana de H5N1, por lo que todos los humanos que lo han contraído hasta ahora han contraído el H5N1 aviar .
La tasa de mortalidad reportada por la influenza aviar H5N1 altamente patógena en humanos es alta; Los datos de la OMS indican que el 60% de los casos clasificados como H5N1 resultaron en muerte. Sin embargo, existe cierta evidencia de que la tasa de mortalidad real de la gripe aviar podría ser mucho menor, ya que puede haber muchas personas con síntomas más leves que no buscan tratamiento y no son contabilizadas. [23] [24]
En un caso, un niño con H5N1 experimentó diarrea seguida rápidamente de un coma sin desarrollar síntomas respiratorios o similares a los de la gripe. [25] Se han realizado estudios sobre los niveles de citoquinas en humanos infectados por el virus de la gripe H5N1. De particular preocupación son los niveles elevados de factor de necrosis tumoral alfa , una proteína asociada con la destrucción de tejido en los sitios de infección y una mayor producción de otras citoquinas. Los aumentos en el nivel de citocinas inducidos por el virus de la gripe también se asocian con síntomas de la gripe, como fiebre, escalofríos, vómitos y dolor de cabeza. El daño tisular asociado con la infección por el virus patógeno de la gripe puede, en última instancia, provocar la muerte. [11] Algunos han llamado a la cascada inflamatoria desencadenada por el H5N1 una ' tormenta de citoquinas ', debido a lo que parece ser un proceso de retroalimentación positiva de daño al cuerpo resultante de la estimulación del sistema inmunológico . El H5N1 induce niveles más altos de citocinas que los tipos de virus de la gripe más comunes. [26]
Los signos clínicos del H5N1 en aves varían desde leves (disminución de la producción de huevos, secreción nasal, tos y estornudos) hasta graves, que incluyen pérdida de coordinación, energía y apetito; huevos con cáscara blanda o deformes; decoloración púrpura de las barbas, la cabeza, los párpados, las crestas y los corvejones; y diarrea. A veces, el primer signo perceptible es la muerte súbita. [20]
La primera cepa conocida de HPAI A(H5N1) (llamada A/chicken/Scotland/59) mató a dos bandadas de pollos en Escocia en 1959, pero esa cepa era muy diferente de la cepa altamente patógena de H5N1. La cepa dominante de HPAI A(H5N1) en 2004 evolucionó de 1999 a 2002 creando el genotipo Z. [27] También se le ha denominado "HPAI A(H5N1) de linaje asiático".
El linaje asiático HPAI A(H5N1) se divide en dos clados antigénicos . "El clado 1 incluye aislados humanos y de aves de Vietnam , Tailandia y Camboya , y aislados de aves de Laos y Malasia . Los virus del clado 2 se identificaron por primera vez en aislados de aves de China , Indonesia , Japón y Corea del Sur antes de extenderse hacia el oeste, hasta el Medio Oriente . Europa y África . Según la OMS, los virus del clado 2 han sido los principales responsables de las infecciones humanas por H5N1 que se produjeron a finales de 2005 y 2006. El análisis genético ha identificado seis subclados del clado 2, tres de los cuales tienen una distribución geográfica distinta y tienen implicado en infecciones humanas: Mapa
Un estudio de 2007 centrado en el subclado de EMA arrojó más luz sobre las mutaciones de EMA. "Los 36 nuevos aislamientos reportados aquí amplían en gran medida la cantidad de datos de secuencia del genoma completo disponibles de aislamientos recientes de influenza aviar (H5N1). Antes de nuestro proyecto, GenBank contenía sólo otros cinco genomas completos de Europa para el período 2004-2006, y contenía "No hay genomas completos del Medio Oriente o el norte de África. Nuestro análisis mostró varios hallazgos nuevos. En primer lugar, todas las muestras europeas, del Medio Oriente y africanas caen en un clado que es distinto de otros clados asiáticos contemporáneos, todos los cuales comparten un ancestro común con el cepa original de Hong Kong de 1997. Los árboles filogenéticos construidos en cada uno de los 8 segmentos muestran una imagen consistente de 3 linajes, como lo ilustra el árbol HA que se muestra en la Figura 1. Dos de los clados contienen aislamientos exclusivamente vietnamitas; el más pequeño de ellos, con 5 A los aislados los denominamos V1; el clado más grande, con 9 aislados, es V2. Los 22 aislamientos restantes pertenecen a un tercer clado claramente distinto, denominado EMA, que comprende muestras de Europa, Oriente Medio y África. Los árboles de los otros 7 segmentos muestran una topología similar, con los clados V1, V2 y EMA claramente separados en cada caso. Los análisis de todos los genomas completos de influenza (H5N1) disponibles y de 589 secuencias de HA ubicaron al clado EMA como distinto de los principales clados que circulan en la República Popular China, Indonesia y el Sudeste Asiático". [30]
Los aislados H5N1 se identifican como este ejemplo real de HPAI A(H5N1), A/chicken/Nakorn-Patom/Thailand/CU-K2/04(H5N1) :
Otros ejemplos incluyen: A/duck/Hong Kong/308/78(H5N3), A/avian/NY/01(H5N2), A/chicken/Mexico/31381-3/94(H5N2) y A/ shoveler / Egypt /03(H5N2). [31]
Al igual que otros virus de la gripe aviar, el H5N1 tiene cepas denominadas "altamente patógenas" (HP) y "poco patógenas" (LP). Los virus de la influenza aviar que causan IAAP son muy virulentos y las tasas de mortalidad en bandadas infectadas a menudo se acercan al 100%. Los virus LPAI tienen una virulencia insignificante, pero estos virus pueden servir como progenitores de los virus HPAI. La cepa de H5N1 responsable de la muerte de aves en todo el mundo es una cepa de IAAP; todas las demás cepas de H5N1, incluida una cepa norteamericana que no causa ninguna enfermedad en ninguna especie, son cepas de LPAI. Todas las cepas de IAAP identificadas hasta la fecha involucran los subtipos H5 y H7. La distinción se refiere a la patogenicidad en aves de corral, no en humanos. Normalmente, un virus aviar altamente patógeno no lo es ni para los humanos ni para las aves que no sean aves de corral. Esta cepa mortal de H5N1 es inusual porque es mortal para tantas especies, incluidas algunas, como los gatos domésticos, que nunca antes habían sido susceptibles a ningún virus de influenza . [32]

H5N1 es un subtipo de la especie Virus de la influenza A del género Alphainfluenzavirus de la familia Orthomyxoviridae . Como todos los demás subtipos de influenza A, el subtipo H5N1 es un virus de ARN . Tiene un genoma segmentado de ocho cadenas simples de ARN de sentido negativo , abreviadas como PB2, PB1, PA, HA, NP, NA, MP y NS. [ cita necesaria ]
HA codifica hemaglutinina , una glicoproteína antigénica que se encuentra en la superficie de los virus de la influenza y es responsable de unir el virus a la célula que está siendo infectada. NA codifica la neuraminidasa , una enzima glicosilada antigénica que se encuentra en la superficie de los virus de la influenza. Facilita la liberación de virus descendientes de las células infectadas. [33] Las hebras de ARN de hemaglutinina (HA) y neuraminidasa (NA) especifican la estructura de las proteínas que son más relevantes desde el punto de vista médico como objetivos para fármacos antivirales y anticuerpos . HA y NA también se utilizan como base para nombrar los diferentes subtipos de virus de la influenza A. De aquí provienen el H y el N en el H5N1 .
Los virus de la influenza A son importantes por su potencial de causar enfermedad y muerte en humanos y otros animales. Los subtipos del virus de la influenza A que se han confirmado en humanos, en orden de número de muertes humanas pandémicas conocidas que han causado, incluyen:
La influenza aviar de baja patogenicidad H5N1 (LPAI H5N1), también llamada H5N1 "norteamericana", ocurre comúnmente en aves silvestres. En la mayoría de los casos, causa enfermedades leves o ningún signo perceptible de enfermedad en las aves. No se sabe que afecte a los humanos en absoluto. La única preocupación al respecto es que es posible que se transmita a las aves de corral y que éstas muten en una cepa altamente patógena.
"En el pasado, no había ningún requisito para informar o rastrear las detecciones de LPAI H5 o H7 en aves silvestres, por lo que los estados y universidades analizaron muestras de aves silvestres independientemente del USDA. Debido a esto, la lista anterior de detecciones anteriores podría no incluir todas las detecciones pasadas. Detecciones de LPAI H5N1. Sin embargo, la Organización Mundial de Sanidad Animal ( OIE ) cambió recientemente su requisito de informar las detecciones de influenza aviar. A partir de 2006, todos los subtipos de LPAI H5 y H7 confirmados deben ser reportados a la OIE debido a su potencial para mutar. "En cepas altamente patógenas. Por lo tanto, el USDA ahora rastrea estas detecciones en aves silvestres, bandadas de traspatio, bandadas comerciales y mercados de aves vivas". [37]
Los virus de la influenza tienen una tasa de mutación relativamente alta que es característica de los virus de ARN . La segmentación de su genoma facilita la recombinación genética mediante reordenamiento de segmentos en huéspedes infectados con dos cepas diferentes de virus de la influenza al mismo tiempo. [38] [39] Una cepa que antes no era contagiosa podría entonces transmitirse entre humanos, uno de varios caminos posibles hacia una pandemia. [ cita necesaria ]
La capacidad de varias cepas de influenza para mostrar selectividad de especie se debe en gran medida a la variación en los genes de hemaglutinina . Las mutaciones genéticas en el gen de la hemaglutinina que causan sustituciones de aminoácidos únicos pueden alterar significativamente la capacidad de las proteínas hemaglutininas virales para unirse a los receptores en la superficie de las células huésped. Tales mutaciones en los virus aviares H5N1 pueden hacer que las cepas de virus pasen de ser ineficientes para infectar células humanas a ser tan eficientes para causar infecciones humanas como los tipos más comunes de virus de la influenza humana. [40] Esto no significa que una sustitución de aminoácidos pueda causar una pandemia, pero sí significa que una sustitución de aminoácidos puede causar que un virus de la gripe aviar que no es patógeno en humanos se vuelva patógeno en humanos. [ cita necesaria ]
El subtipo H3N2 del virus de la influenza A es endémico en cerdos en China y se ha detectado en cerdos en Vietnam, lo que aumenta los temores sobre la aparición de nuevas cepas variantes. La cepa dominante del virus de la gripe anual en enero de 2006 fue la H3N2 , que ahora es resistente a los medicamentos antivirales estándar amantadina y rimantadina . La posibilidad de que H5N1 y H3N2 intercambien genes mediante reordenamiento es una preocupación importante. Si se produce una recombinación en el H5N1, podría seguir siendo un subtipo de H5N1, o podría cambiar de subtipo, como lo hizo el H2N2 cuando evolucionó hacia la cepa H3N2 de la gripe de Hong Kong .
Tanto la cepa pandémica H2N2 como la H3N2 contenían segmentos de ARN del virus de la influenza aviar . "Mientras que los virus de la influenza humana pandémica de 1957 (H2N2) y 1968 (H3N2) surgieron claramente a través de una recombinación entre virus humanos y aviares, el virus de la influenza que causó la 'gripe española' en 1918 parece derivar enteramente de una fuente aviar". [41]
Existen varias vacunas contra el H5N1 para varias de las variedades aviares H5N1, pero la continua mutación del H5N1 hace que su uso sea limitado hasta la fecha: si bien las vacunas a veces pueden proporcionar protección cruzada contra cepas de gripe relacionadas, la mejor protección sería una vacuna producida específicamente para cualquier futura cepa del virus de la gripe pandémica. Daniel R. Lucey , codirector del programa de posgrado sobre Amenazas biológicas y enfermedades emergentes de la Universidad de Georgetown , ha señalado lo siguiente: "No existe una pandemia de H5N1 , por lo que no puede haber una vacuna pandémica ". [42] Sin embargo, se han creado "vacunas prepandémicas"; están siendo perfeccionados y probados; y son prometedores tanto para promover la investigación como para la preparación para la próxima pandemia. [43] [44] [45] Se alienta a las empresas fabricantes de vacunas a aumentar la capacidad para que, si se necesita una vacuna pandémica, haya instalaciones disponibles para la producción rápida de grandes cantidades de una vacuna específica para una nueva cepa pandémica.
" Estados Unidos está colaborando estrechamente con ocho organizaciones internacionales, incluida la Organización Mundial de la Salud (OMS), la Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO), la Organización Mundial de Sanidad Animal (OIE) y 88 gobiernos extranjeros para abordar La situación a través de la planificación, un mayor seguimiento y total transparencia en la notificación e investigación de los casos de influenza aviar. Estados Unidos y estos socios internacionales han liderado esfuerzos globales para alentar a los países a aumentar la vigilancia de los brotes en aves de corral y de un número significativo de muertes en aves migratorias y a introducir rápidamente medidas de contención. La Agencia de los Estados Unidos para el Desarrollo Internacional (USAID) y el Departamento de Estado de los Estados Unidos , el Departamento de Salud y Servicios Humanos (HHS) y el Departamento de Agricultura (USDA) de los Estados Unidos están coordinando futuras medidas de respuesta internacional en nombre de la Casa Blanca. con departamentos y agencias de todo el gobierno federal". [46]
Se están tomando medidas conjuntas para "minimizar el riesgo de una mayor propagación en las poblaciones animales", "reducir el riesgo de infecciones humanas" y "apoyar aún más la planificación y preparación para una pandemia". [46]
El Centro Nacional de Salud de la Vida Silvestre del USGS , los Centros para el Control y la Prevención de Enfermedades , la Organización Mundial de la Salud , la Comisión Europea y otros están realizando e informando sobre los brotes de gripe aviar H5N1 en humanos y animales , una vigilancia y análisis in situ detallados y coordinados mutuamente. [47]
No existe un tratamiento muy eficaz para la gripe H5N1, pero el oseltamivir (comercializado por Roche como Tamiflu) a veces puede inhibir la propagación del virus de la gripe dentro del cuerpo del usuario. Este medicamento se ha convertido en el foco de atención de algunos gobiernos y organizaciones que intentan prepararse para una posible pandemia de H5N1. [48] El 20 de abril de 2006, Roche AG anunció que una reserva de tres millones de tratamientos de Tamiflu estaban esperando a disposición de la Organización Mundial de la Salud para ser utilizado en caso de una pandemia de gripe; Por separado, Roche donó dos millones de medicamentos a la OMS para su uso en países en desarrollo que podrían verse afectados por una pandemia de este tipo pero que carecen de la capacidad de comprar grandes cantidades del medicamento. [49]
Sin embargo, el experto de la OMS, Hassan al-Bushra, ha dicho:
Los estudios en animales y de laboratorio sugieren que Relenza ( zanamivir ), que pertenece a la misma clase de medicamentos que Tamiflu, también puede ser eficaz contra el H5N1. En un estudio realizado en ratones en 2000, "zanamivir demostró ser eficaz en el tratamiento de los virus de la influenza aviar H9N2, H6N1 y H5N1 transmisibles a los mamíferos". [51] Además, los estudios en ratones sugieren que la combinación de zanamivir, celecoxib y mesalazina parece prometedora y produce una tasa de supervivencia del 50 % en comparación con ninguna supervivencia en el grupo de placebo. [52] Si bien nadie sabe si zanamivir será útil o no en una cepa pandémica de H5N1 que aún no existe, podría ser útil almacenar zanamivir y oseltamivir en caso de una pandemia de influenza H5N1. Ni oseltamivir ni zanamivir pueden fabricarse en cantidades significativas una vez que comience la transmisión humana eficiente. [53] En septiembre de 2006, un científico de la OMS anunció que los estudios habían confirmado casos de cepas H5N1 resistentes al Tamiflu y la amantadina. [54] También han aparecido en la UE cepas resistentes al Tamiflu , que siguen siendo sensibles a Relenza. [55] [56]
Las primeras infecciones de humanos por H5N1 coincidieron con una epizoótica (una epidemia en no humanos) de influenza H5N1 en la población de aves de corral de Hong Kong en 1997. Este brote panzoótico (una enfermedad que afecta a animales de muchas especies, especialmente en una amplia zona) fue detenido por la matanza de toda la población de aves de corral domésticas dentro del territorio. Sin embargo, la enfermedad ha seguido propagándose; Se informaron brotes nuevamente en Asia en 2003. El 21 de diciembre de 2009, la OMS anunció un total de 447 casos que resultaron en la muerte de 263. [20] [57]

El H5N1 es fácilmente transmisible entre aves, lo que facilita una posible propagación global del H5N1 . Si bien el H5N1 sufre mutaciones y reordenamientos, creando variaciones que pueden infectar a especies que antes no eran portadoras del virus, no todas estas variantes pueden infectar a los humanos. El H5N1, como virus aviar, se une preferentemente a un tipo de receptores de galactosa que pueblan el tracto respiratorio aviar desde la nariz hasta los pulmones y que están prácticamente ausentes en los humanos y se encuentran solo dentro y alrededor de los alvéolos , estructuras profundas de los pulmones a donde pasa el oxígeno. la sangre. Por tanto, el virus no se expulsa fácilmente tosiendo y estornudando, la vía habitual de transmisión. [21] [22] [58]
El H5N1 se transmite principalmente por aves de corral domésticas , tanto a través de los movimientos de aves y productos avícolas infectados como mediante el uso de estiércol de aves infectadas como fertilizante o alimento. Los seres humanos con H5N1 normalmente lo han contraído de pollos, que a su vez fueron infectados por otras aves de corral o acuáticas. Las aves acuáticas migratorias ( patos , gansos y cisnes salvajes ) son portadoras del H5N1, a menudo sin enfermarse. [59] [60] Muchas especies de aves y mamíferos pueden infectarse con HPAI A(H5N1), pero se desconoce el papel de otros animales, además de las aves de corral y las aves acuáticas, como huéspedes transmisores de enfermedades. [61]
Según un informe de la Organización Mundial de la Salud , el H5N1 puede transmitirse indirectamente. El informe afirma que el virus a veces puede adherirse a las superficies o ser absorbido por el polvo de los fertilizantes para infectar a las personas. [62]
El H5N1 ha mutado en una variedad de cepas con diferentes perfiles patógenos, algunas patógenas para una especie pero no para otras, algunas patógenas para múltiples especies. Cada variación genética específica conocida se puede rastrear hasta un aislado de virus de un caso específico de infección. A través de la deriva antigénica , el H5N1 ha mutado en docenas de variedades altamente patógenas divididas en clados genéticos que se conocen a partir de aislados específicos, pero todos pertenecen al genotipo Z del virus de la influenza aviar H5N1, ahora el genotipo dominante. [39] [38] Los aislados de H5N1 encontrados en Hong Kong en 1997 y 2001 no se transmitieron de manera consistente y eficiente entre las aves y no causaron enfermedades significativas en estos animales. En 2002, aparecieron nuevos aislamientos de H5N1 entre la población de aves de Hong Kong. Estos nuevos aislados causaron enfermedades agudas, incluyendo disfunción neurológica grave y muerte en patos . Este fue el primer caso reportado de infección letal por el virus de la influenza en aves acuáticas silvestres desde 1961. [63]
El genotipo Z surgió en 2002 a través de una recombinación de genotipos anteriores altamente patógenos de H5N1 [2] que infectaron por primera vez a aves en China en 1996 y a humanos en Hong Kong en 1997. [38] [39] [64] El genotipo Z es endémico en aves del sudeste asiático, ha creado al menos dos clados que pueden infectar a los humanos y se está extendiendo por todo el mundo en poblaciones de aves. Las mutaciones que ocurren dentro de este genotipo están aumentando su patogenicidad. [65] Las aves también pueden eliminar el virus durante períodos más largos antes de morir, lo que aumenta la transmisibilidad del virus.

Las aves infectadas transmiten el H5N1 a través de la saliva , las secreciones nasales , las heces y la sangre . Otros animales pueden infectarse con el virus por contacto directo con estos fluidos corporales o por contacto con superficies contaminadas con ellos. El H5N1 sigue siendo infeccioso después de más de 30 días a 0 °C (32 °F) (más de un mes a temperatura bajo cero) o 6 días a 37 °C (99 °F) (una semana a temperatura corporal humana); a temperaturas normales dura semanas en el ambiente. En temperaturas árticas no se degrada en absoluto.
Debido a que las aves migratorias se encuentran entre los portadores del virus H5N1 altamente patógeno, éste se está propagando a todas partes del mundo. El H5N1 se diferencia de todos los virus de gripe aviar altamente patógenos conocidos anteriormente por su capacidad de transmitirse a otros animales además de las aves de corral.
En octubre de 2004, los investigadores descubrieron que el H5N1 es mucho más peligroso de lo que se creía anteriormente. Se reveló que las aves acuáticas estaban propagando directamente esta cepa altamente patógena a pollos , cuervos , palomas y otras aves, y el virus también estaba aumentando su capacidad para infectar a los mamíferos. A partir de ese momento, los expertos en gripe aviar se refirieron cada vez más a la contención como una estrategia que puede retrasar, pero no prevenir en última instancia, una futura pandemia de gripe aviar.
"Desde 1997, los estudios sobre la influenza A (H5N1) indican que estos virus continúan evolucionando, con cambios en la antigenicidad y las constelaciones genéticas internas; una gama ampliada de huéspedes en especies de aves y la capacidad de infectar félidos; mayor patogenicidad en ratones y hurones infectados experimentalmente. , en el que causan infecciones sistémicas; y una mayor estabilidad ambiental". [66]
El New York Times , en un artículo sobre la transmisión del H5N1 a través de aves de contrabando, informa que Wade Hagemeijer de Wetlands International afirma: "Creemos que se propaga tanto por la migración de aves como por el comercio, pero ese comercio, particularmente el comercio ilegal, es más importante". [67]
El 29 de septiembre de 2007, investigadores informaron que el virus de la gripe aviar H5N1 también puede atravesar la placenta de una mujer embarazada para infectar al feto. También encontraron evidencia de lo que los médicos habían sospechado durante mucho tiempo: el virus no solo afecta los pulmones, sino que también pasa por todo el cuerpo hasta el tracto gastrointestinal, el cerebro, el hígado y las células sanguíneas. [68]
En mayo de 2013, Corea del Norte confirmó un brote de gripe aviar H5N1 que obligó a las autoridades a matar más de 160.000 patos en Pyongyang . [70]
Durante el invierno de 2021 y 2022, la gripe aviar se propagó entre la población de gansos percebes en Solway Firth, Reino Unido, y se estima que se perdió hasta un tercio de la población de Svalbard; [71] [72] Los gansos de patas rosadas también se vieron afectados allí y parece que llevaron el virus a nuevos sitios en el norte de Escocia. La enfermedad se confirmó en charranes sándwich en Sudáfrica en abril de 2022. [73] A finales de la primavera de 2022, los brotes de gripe aviar afectaron a muchas especies de aves silvestres en el Reino Unido, y se informaron grandes pérdidas entre las aves marinas que regresaban para reproducirse en las colonias de las Islas del Norte. y las Hébridas Exteriores, [74] incluidas las skúas grandes (bonxie) cuyos brotes se habían informado inicialmente en 2021 [75] (Escocia alberga aproximadamente el 60 % de la población reproductora del mundo); el censo de 2022 en St Kilda mostró una disminución del 64 %. en 2019 con 106 aves muertas registradas hasta el momento (hasta el 6 de junio), [76] alcatraces (más de 1000 aves reportadas muertas solo en la colonia Hermaness de las Shetlands, [74] donde hay alrededor de 26 000 parejas reproductoras), y muchos más alcatraces están siendo reportados muertos en otras colonias ( Troup Head , Bass Rock y St Kilda ); [77] la gama de especies también parece estar ampliándose, con informes de muchas especies de aves silvestres, aves marinas (alcas, charranes y gaviotas) y especies carroñeras (córvidos y aves rapaces). [78] [79]
En otras partes de Europa, el virus mató a cientos (574+) de pelícanos dálmatas en Grecia, [80] [81] y en Israel alrededor de 6000 grullas comunes fueron encontradas muertas en Hula en diciembre de 2021. [82] Un informe del Scientific Task Force on Avian Influenza and Wild Birds en: "H5N1 Highly Pathogenic Avian Influenza in pollies and wild birds: Winter of 2021/2022 with focus on Mass Mortality of Wild Birds in UK and Israel" resume la situación hasta el 24 de enero de 2022 y menciona que "H5N8 HPAI sigue siendo responsable de los casos de aves de corral y aves silvestres, principalmente en Asia, el H5N1 ha reemplazado de hecho a este subtipo en África y Eurasia, tanto en aves de corral como en aves silvestres". [83]
De manera similar a los informes de 2021, se observaron brotes en colonias de alcatraces en Canadá, con miles de aves muertas en junio de 2022, [84] así como eiders comunes y grandes gaviotas de lomo negro . [85] Antes de eso, hubo informes de propagación en aves silvestres en más de 30 estados de los EE. UU., incluidas mortalidades importantes en una colonia de cormoranes de doble cresta en Barrington, Illinois , [86] [87] el virus también se propagó a carroñeros, incluidos Tres águilas calvas en Georgia. [88] Se observaron mortandades masivas tanto de aves como de mamíferos en Perú durante la temporada 2022-2023. [89] En particular, el gobierno peruano informó la muerte de aproximadamente 63.000 aves, así como 716 leones marinos , y la OMS señaló que los derrames en mamíferos debían ser "monitoreados de cerca". [90] [91] En los Estados Unidos, el brote aviar de 2022-2023 fue el peor desde que se detectó por primera vez el H5N1. [90]
Ecuador entró en una "emergencia sanitaria animal" de tres meses el 29 de noviembre de 2022, pocos días después de que se reportara su primer caso, mientras que Argentina y Uruguay declararon "emergencia sanitaria nacional" el 15 de febrero de 2023, luego de que se descubrieran sus respectivos primeros casos. . [92] El 22 de mayo de 2023, Brasil, como mayor exportador mundial de carne de pollo, declaró una emergencia de 180 días luego de varios casos detectados en aves silvestres y creó un centro de operaciones de emergencia para planificar y mitigar una posible propagación adicional del H5N1. [93]
La temporada 2022-2023 también fue el peor brote registrado en el Reino Unido, y el gobierno británico exigió el llamado "bloqueo avícola", que exigía que los granjeros mantuvieran a sus aves en el interior. [90] Mientras tanto, un brote de H5N1 en una granja de visones española llevó a los investigadores a creer que habían observado el primer caso de transmisión de H5N1 de mamífero a mamífero. [94]
Ron Fouchier , del Centro Médico Erasmus de Rotterdam (Países Bajos ), creó nuevas cepas contagiosas de H5N1, quien presentó su trabajo al público por primera vez en una conferencia sobre influenza en Malta en septiembre de 2011. Se introdujeron tres mutaciones en el genoma del virus H5N1. y luego el virus pasó de la nariz de los hurones infectados a la nariz de los no infectados, lo que se repitió 10 veces. [95] Después de estos 10 pases, el virus H5N1 había adquirido la capacidad de transmisión entre hurones a través de aerosoles o gotitas respiratorias.
Después de que Fouchier ofreciera un artículo que describía este trabajo a la importante revista académica Science , el Consejo Asesor Científico Nacional para la Bioseguridad (NSABB) de EE. UU. recomendó no publicar todos los detalles del estudio, y el presentado a Nature por Yoshihiro Kawaoka de la Universidad de Wisconsin que describe trabajos relacionados. Sin embargo, después de consultas adicionales en la Organización Mundial de la Salud y por parte de la NSABB, la NSABB revirtió su posición y recomendó la publicación de versiones revisadas de los dos artículos. [96] Sin embargo, luego el gobierno holandés declaró que este tipo de manuscritos requerían que Fouchier solicitara un permiso de exportación a la luz de la directiva de la UE 428/2009 sobre bienes de doble uso. [nota 1] Después de mucha controversia en torno a la publicación de su investigación, Fouchier cumplió (bajo protesta formal) con las demandas del gobierno holandés de obtener un permiso especial [97] para presentar su manuscrito, y su investigación apareció en un número especial de la revista Science. dedicado al H5N1. [98] [99] [100] Los artículos de Fouchier y Kawaoka concluyen que es completamente posible que una cadena natural de mutaciones pueda llevar a que un virus H5N1 adquiera la capacidad de transmisión aérea entre mamíferos, y que una pandemia de influenza H5N1 no lo haría. ser imposible. [101]
En mayo de 2013, se informó que los científicos del Instituto de Investigación Veterinaria de Harbin , China, habían creado cepas H5N1 que se transmitían entre conejillos de indias . [102]
En respuesta al trabajo de Fouchier y Kawaoka, varios científicos expresaron su preocupación por los riesgos de crear nuevos patógenos pandémicos potenciales, lo que culminó con la formación del Grupo de Trabajo de Cambridge , una declaración de consenso que pedía una evaluación de los riesgos y beneficios de dicha investigación. [103] [104]
Aunque los mamíferos, incluidos los humanos, se habían infectado con cepas de gripe aviar H5N1 en el pasado, estos casos aparentemente habían sido causados por la exposición directa a aves infectadas, como por ejemplo mediante el consumo de aves por parte de la vida silvestre o la exposición a aves de corral infectadas por parte de los granjeros. Por el contrario, el brote de H5N1 en mamíferos en octubre de 2022 en una granja de visones española mostró evidencia de ser el primer caso registrado de transmisión de mamífero a mamífero, con el 4 por ciento de la población de visones de la granja muriendo de neumonía hemorrágica relacionada con el H5N1. [94] [105] El tracto respiratorio del visón es particularmente adecuado para actuar como una vía de transmisión viral a los humanos, lo que ha preocupado a los profesionales de la salud pública debido a la producción de todas las vacunas humanas aprobadas, excepto una, que requieren huevos de gallina, que H5N1 mata a una tasa de mortalidad del 90 al 100 por ciento. [106] También se descubrió que los visones infectados en España habían exhibido la mutación viral "PB2" encontrada cuando el H5N1 saltó a los cerdos más de una década antes, lo que aumentó los temores de que las granjas pudieran estar actuando como incubadoras y/o reservorios del virus, similar a el papel de los visones en el SARS-CoV-2 . [94]
En enero de 2023, quince especies de mamíferos salvajes y cautivos se habían infectado con H5N1 en todo Estados Unidos. [107] Una muerte masiva de focas del Caspio en diciembre de 2022, con 700 focas infectadas encontradas muertas a lo largo de la costa del Mar Caspio en la república rusa de Daguestán , preocupó a los investigadores con respecto a la posibilidad de que hubiera comenzado la propagación de mamíferos salvajes a mamíferos. [108] Una muerte masiva similar del 95% de las crías de elefante marino del sur en 2023 también generó preocupaciones sobre la propagación de mamífero a mamífero, ya que las crías lactantes habrían estado menos expuestas a las aves. [109]
En mayo de 2020, la OMS informó un total de 861 casos humanos confirmados que provocaron la muerte de 455 personas desde 2003. [5]
Tras la muerte por H5N1 en febrero de 2023 de una niña de 11 años de la provincia de Prey Veng de Camboya , se confirmó que su padre daba positivo al virus y varios contactos cercanos también comenzaron a mostrar signos de infección. El 24 de febrero de 2023, la OMS expresó su preocupación por la posibilidad de que el virus hubiera comenzado a propagarse entre los humanos y ordenó la producción de una nueva vacuna humana contra el H5N1. [110] Después de las infecciones confirmadas, la OMS comenzó a trabajar con el gobierno camboyano para determinar si ambos individuos habían contraído el virus directamente de aves de corral infectadas o si de hecho había sido un caso de transmisión de persona a persona. [111] Una secuenciación adicional determinó que al menos uno de los dos casos pertenecía a un clado H5N1 más antiguo, 2.3.2.1c, que había circulado como una cepa H5N1 común en Camboya durante muchos años, en lugar del clado más reciente 2.3.4.4b. , que había causado muertes masivas de aves de corral desde 2020. Este clado más antiguo había saltado a los humanos en el pasado pero no había dado lugar a ninguna transmisión conocida de persona a persona. [112]
El 1 de marzo de 2023, cuando Taiwán elevó su alerta de viaje a Camboya, la OMS y los CDC de EE. UU., en colaboración con las autoridades camboyanas, determinaron que ambos individuos habían sido infectados por contacto directo con aves de corral. [113] [114]
El H5N1 ha tenido un efecto significativo en la sociedad humana , especialmente en las respuestas financieras , políticas , sociales y personales a las muertes reales y previstas de aves , humanos y otros animales . Se están recaudando y gastando miles de millones de dólares para investigar el H5N1 y prepararse para una posible pandemia de influenza aviar . Se han gastado más de 10 mil millones de dólares y se han matado más de 200 millones de aves para tratar de contener el H5N1. [13] [115] [116] [117] [118] [119] [120] [121] [122]
La gente ha reaccionado comprando menos pollo, lo que ha provocado que las ventas y los precios de las aves caigan. [123] Muchas personas han almacenado suministros para una posible pandemia de gripe. Funcionarios de salud internacionales y otros expertos han señalado que aún quedan muchas preguntas desconocidas en torno a la enfermedad. [124]
El Dr. David Nabarro , Coordinador Jefe de la Gripe Aviar de las Naciones Unidas y ex Jefe de Respuesta a Crisis de la Organización Mundial de la Salud, se ha descrito a sí mismo como "bastante asustado" por el impacto potencial del H5N1 en los seres humanos. Nabarro ha sido acusado anteriormente de alarmista y en su primer día en su cargo en las Naciones Unidas proclamó que la gripe aviar podría matar a 150 millones de personas. En una entrevista con el International Herald Tribune , Nabarro compara la gripe aviar con el SIDA en África y advierte que las subestimaciones condujeron a un enfoque inadecuado para la investigación y la intervención. [125]
En febrero de 2020 se produjo un brote de gripe aviar H5N1 en el distrito de Shuangqing de la ciudad de Shaoyang , en la provincia de Hunan . Después de que las aves de corral enfermaran a causa del virus, la ciudad mató cerca de 18.000 pollos para evitar la propagación de la enfermedad. Hunan limita con la provincia de Hubei donde se encuentra Wuhan , epicentro de la pandemia de coronavirus . [126]
{{cite journal}}: CS1 maint: unfit URL (link){{cite journal}}: CS1 maint: multiple names: authors list (link) CS1 maint: numeric names: authors list (link)Instituto de Investigación sobre Problemas de Seguridad Biológica (RIBSP), Región de Zhambyl, República de Kazajstán