El óxido de zinc es un compuesto inorgánico con la fórmula ZnO . Es un polvo blanco insoluble en agua. El ZnO se utiliza como aditivo en numerosos materiales y productos, incluidos cosméticos, complementos alimenticios , cauchos, plásticos, cerámicas, vidrio, cemento, lubricantes, [12] pinturas, protectores solares, ungüentos, adhesivos, selladores, pigmentos, alimentos, baterías, ferritas, retardadores de fuego, semiconductores, [13] y cintas de primeros auxilios. Aunque se produce naturalmente como mineral zincita , la mayor parte del óxido de zinc se produce sintéticamente. [14]
Los compuestos de zinc probablemente fueron utilizados por los primeros humanos, en formas procesadas [14] y sin procesar, como pintura o ungüento medicinal, pero su composición es incierta. El uso de pushpanjan , probablemente óxido de zinc, como ungüento para los ojos y las heridas abiertas, se menciona en el texto médico indio Charaka Samhita , que se cree que data del año 500 a.C. o antes. [15] El ungüento de óxido de zinc también es mencionado por el médico griego Dioscórides (siglo I d.C.). [16] Galeno sugirió tratar los cánceres ulcerosos con óxido de zinc, [17] al igual que Avicena en su El canon de la medicina . Se utiliza como ingrediente en productos como talcos para bebés y cremas contra la dermatitis del pañal , crema de calamina , champús anticaspa y ungüentos antisépticos . [18]
Los romanos produjeron cantidades considerables de latón (una aleación de zinc y cobre ) ya en el año 200 a. C. mediante un proceso de cementación en el que el cobre se hacía reaccionar con óxido de zinc. [19] Se cree que el óxido de zinc se produjo calentando mineral de zinc en un horno de cuba. Esto liberó zinc metálico en forma de vapor, que luego ascendió por la chimenea y se condensó como óxido. Este proceso fue descrito por Dioscórides en el siglo I d.C. [20] También se ha recuperado óxido de zinc de las minas de zinc de Zawar, en la India , que datan de la segunda mitad del primer milenio antes de Cristo. [dieciséis]
Desde el siglo XII al XVI, el zinc y el óxido de zinc fueron reconocidos y producidos en la India mediante una forma primitiva de proceso de síntesis directa. Desde la India, la fabricación de zinc pasó a China en el siglo XVII. En 1743, se estableció la primera fundición europea de zinc en Bristol , Reino Unido. [21] Alrededor de 1782, Louis-Bernard Guyton de Morveau propuso sustituir el pigmento blanco de plomo por óxido de zinc. [22]
El uso principal del óxido de zinc (blanco de zinc) era en pinturas y como aditivo para ungüentos. El blanco de zinc fue aceptado como pigmento en pinturas al óleo en 1834, pero no se mezclaba bien con el óleo. Este problema se resolvió optimizando la síntesis de ZnO. En 1845, Edmé-Jean Leclaire en París producía pintura al óleo a gran escala y, en 1850, el blanco de zinc se fabricaba en toda Europa. El éxito de la pintura blanca de zinc se debió a sus ventajas sobre la tradicional pintura blanca de plomo: la pintura blanca de zinc es esencialmente permanente a la luz solar, no se ennegrece con el aire que contiene azufre, no es tóxica y es más económica. Debido a que el blanco de zinc es tan "limpio", es valioso para hacer tintes con otros colores, pero forma una película seca bastante quebradiza cuando no se mezcla con otros colores. Por ejemplo, a finales de la década de 1890 y principios de 1900, algunos artistas utilizaron blanco zinc como base para sus pinturas al óleo. Todas esas pinturas desarrollaron grietas con el paso de los años. [23]
En los últimos tiempos, la mayor parte del óxido de zinc se utilizaba en la industria del caucho para resistir la corrosión . En la década de 1970, la segunda aplicación más importante del ZnO fue el fotocopiado . Se añadió ZnO de alta calidad producido mediante el "proceso francés" como relleno al papel de fotocopia. Esta aplicación pronto fue desplazada por el titanio . [24]
El ZnO puro es un polvo blanco, pero en la naturaleza se presenta como el raro mineral zincita , que generalmente contiene manganeso y otras impurezas que le confieren un color de amarillo a rojo. [25]
El óxido de zinc cristalino es termocrómico , cambia de blanco a amarillo cuando se calienta en el aire y vuelve a blanco al enfriarse. [26] Este cambio de color es causado por una pequeña pérdida de oxígeno al medio ambiente a altas temperaturas para formar el Zn 1+x O no estequiométrico , donde a 800 °C, x = 0,00007. [26]
El óxido de zinc es un óxido anfótero . Es casi insoluble en agua, pero se disolverá en la mayoría de los ácidos , como el ácido clorhídrico : [27]
El óxido de zinc sólido también se disolverá en álcalis para dar zincatos solubles:
El ZnO reacciona lentamente con los ácidos grasos de los aceites para producir los carboxilatos correspondientes , como el oleato o el estearato . Cuando se mezcla con una solución acuosa fuerte de cloruro de zinc , el ZnO forma productos similares al cemento que se describen mejor como hidroxicloruros de zinc. [28] Este cemento se utilizó en odontología. [29]

El ZnO también forma un material similar al cemento cuando se trata con ácido fosfórico ; Los materiales relacionados se utilizan en odontología. [29] Un componente importante del cemento de fosfato de zinc producido por esta reacción es la esperanza , Zn 3 (PO 4 ) 2 ·4H 2 O. [30]
El ZnO se descompone en vapor de zinc y oxígeno a unos 1975 °C con una presión de oxígeno estándar. En una reacción carbotérmica , el calentamiento con carbono convierte el óxido en vapor de zinc a una temperatura mucho más baja (alrededor de 950 °C). [27]


El óxido de zinc cristaliza en dos formas principales , wurtzita hexagonal [31] y zincblenda cúbica . La estructura de wurtzita es más estable en condiciones ambientales y, por tanto, más común. La forma de zincblenda se puede estabilizar cultivando ZnO en sustratos con estructura reticular cúbica. En ambos casos, los centros de zinc y óxido son tetraédricos , la geometría más característica del Zn(II). El ZnO se convierte en motivo de sal gema a presiones relativamente altas, alrededor de 10 GPa. [13]
Los polimorfos hexagonales y de zincblenda no tienen simetría de inversión (la reflexión de un cristal con respecto a un punto dado no lo transforma en sí mismo). Esta y otras propiedades de simetría reticular dan como resultado la piezoelectricidad del ZnO hexagonal y de zincblenda, y la piroelectricidad del ZnO hexagonal.
La estructura hexagonal tiene un grupo de puntos de 6 mm ( notación de Hermann-Mauguin ) o C 6v ( notación de Schoenflies ), y el grupo espacial es P6 3 mc o C 6v 4 . Las constantes de red son a = 3,25 Å yc = 5,2 Å; su relación c/a ~ 1,60 está cerca del valor ideal para una celda hexagonal c/a = 1,633. [32] Como en la mayoría de los materiales del grupo II-VI , el enlace en ZnO es en gran medida iónico (Zn 2+ O 2− ) con los radios correspondientes de 0,074 nm para Zn 2+ y 0,140 nm para O 2− . Esta propiedad explica la formación preferencial de estructura de wurtzita en lugar de blenda de zinc, [33] así como la fuerte piezoelectricidad del ZnO. Debido a los enlaces polares Zn-O, los planos de zinc y oxígeno están cargados eléctricamente. Para mantener la neutralidad eléctrica, esos planos se reconstruyen a nivel atómico en la mayoría de los materiales relativos, pero no en el ZnO: sus superficies son atómicamente planas, estables y no muestran reconstrucción. [34] Sin embargo, los estudios que utilizan estructuras wurtzoides explicaron el origen de la planitud de la superficie y la ausencia de reconstrucción en las superficies de ZnO wurtzita [35] además del origen de las cargas en los planos de ZnO.
ZnO es un semiconductor de banda prohibida ancha del grupo de semiconductores II-VI . El dopaje nativo del semiconductor debido a vacantes de oxígeno o intersticiales de zinc es de tipo n. [13]
El ZnO es un material relativamente blando con una dureza aproximada de 4,5 en la escala de Mohs . [12] Sus constantes elásticas son más pequeñas que las de los semiconductores III-V relevantes, como el GaN . La alta capacidad calorífica y la conductividad térmica, la baja expansión térmica y la alta temperatura de fusión del ZnO son beneficiosas para la cerámica. [24] El fonón óptico E2 en ZnO exhibe una vida útil inusualmente larga de 133 ps a 10 K. [36]
Entre los semiconductores con enlaces tetraédricos, se ha afirmado que el ZnO tiene el tensor piezoeléctrico más alto, o al menos uno comparable al del GaN y el AlN . [37] Esta propiedad lo convierte en un material tecnológicamente importante para muchas aplicaciones piezoeléctricas , que requieren un gran acoplamiento electromecánico. Por lo tanto, el ZnO en forma de película delgada ha sido uno de los materiales resonadores más estudiados para resonadores acústicos masivos de película delgada .
Las propiedades favorables del óxido de zinc incluyen buena transparencia, alta movilidad de electrones , banda prohibida ancha y fuerte luminiscencia a temperatura ambiente . Esas propiedades hacen que el ZnO sea valioso para una variedad de aplicaciones emergentes: electrodos transparentes en pantallas de cristal líquido , ventanas que ahorran energía o protegen del calor, y electrónica como transistores de película delgada y diodos emisores de luz .
El ZnO tiene una banda prohibida directa relativamente amplia de ~3,3 eV a temperatura ambiente. Las ventajas asociadas con una banda prohibida amplia incluyen voltajes de ruptura más altos , capacidad para sostener grandes campos eléctricos, menor ruido electrónico y funcionamiento a alta temperatura y alta potencia. La banda prohibida del ZnO se puede ajustar aún más a ~3–4 eV mediante su aleación con óxido de magnesio u óxido de cadmio . [13] Debido a esta gran banda prohibida, se han realizado esfuerzos para crear células solares visiblemente transparentes utilizando ZnO como capa absorbente de luz. Sin embargo, hasta ahora estas células solares han demostrado ser muy ineficaces. [38]
La mayor parte del ZnO tiene carácter de tipo n , incluso en ausencia de dopaje intencional . La no estequiometría suele ser el origen del carácter tipo n, pero el tema sigue siendo controvertido. [39] Se ha propuesto una explicación alternativa, basada en cálculos teóricos, según la cual las impurezas sustitutivas involuntarias de hidrógeno son las responsables. [40] El dopaje de tipo n controlable se logra fácilmente sustituyendo Zn por elementos del grupo III como Al, Ga, In o sustituyendo oxígeno por elementos del grupo VII, cloro o yodo . [41]
El dopaje fiable de tipo p con ZnO sigue siendo difícil. Este problema se origina por la baja solubilidad de los dopantes tipo p y su compensación por abundantes impurezas tipo n. Este problema se observa con GaN y ZnSe . La medición del tipo p en material "intrínsecamente" de tipo n se complica por la falta de homogeneidad de las muestras. [42]
Las limitaciones actuales al dopaje p limitan las aplicaciones electrónicas y optoelectrónicas de ZnO, que generalmente requieren uniones de material tipo n y tipo p. Los dopantes de tipo p conocidos incluyen elementos del grupo I Li, Na, K; elementos del grupo V N, P y As; así como cobre y plata. Sin embargo, muchos de ellos forman aceptores profundos y no producen una conducción de tipo p significativa a temperatura ambiente. [13]
La movilidad electrónica del ZnO varía fuertemente con la temperatura y tiene un máximo de ~2000 cm 2 /(V·s) a 80 K. [43] Los datos sobre la movilidad de los huecos son escasos con valores en el rango de 5 a 30 cm 2 /(V· s). [44]
Los discos de ZnO, que actúan como varistor , son el material activo en la mayoría de los descargadores de sobretensiones . [45] [46]
El óxido de zinc se caracteriza por sus propiedades ópticas fuertemente no lineales , especialmente a granel. La no linealidad de las nanopartículas de ZnO se puede ajustar según su tamaño. [47]
Para uso industrial, el ZnO se produce a niveles de 10,5 toneladas por año [25] mediante tres procesos principales: [24]
En el proceso indirecto o francés, el zinc metálico se funde en un crisol de grafito y se vaporiza a temperaturas superiores a 907 °C (normalmente alrededor de 1000 °C). El vapor de zinc reacciona con el oxígeno del aire para dar ZnO, lo que va acompañado de una caída de su temperatura y una brillante luminiscencia. Las partículas de óxido de zinc se transportan a un conducto de refrigeración y se recogen en una cámara de bolsas. Este método indirecto fue popularizado por Edmé Jean LeClaire de París en 1844 y, por lo tanto, se lo conoce comúnmente como proceso francés. Su producto normalmente consiste en partículas aglomeradas de óxido de zinc con un tamaño promedio de 0,1 a unos pocos micrómetros. En peso, la mayor parte del óxido de zinc del mundo se fabrica mediante un proceso francés.
El proceso directo o americano comienza con diversos compuestos de zinc contaminados, como minerales de zinc o subproductos de fundición. Los precursores de zinc se reducen ( reducción carbotérmica ) calentando con una fuente de carbono como la antracita para producir vapor de zinc, que luego se oxida como en el proceso indirecto. Debido a la menor pureza del material de origen, el producto final también es de menor calidad en el proceso directo en comparación con el indirecto.
Una pequeña parte de la producción industrial implica procesos químicos húmedos, que comienzan con soluciones acuosas de sales de zinc, a partir de las cuales se precipita carbonato o hidróxido de zinc . A continuación, el precipitado sólido se calcina a temperaturas de alrededor de 800 °C.

Existen numerosos métodos especializados para producir ZnO para estudios científicos y aplicaciones específicas. Estos métodos se pueden clasificar según la forma de ZnO resultante (a granel, película delgada, nanocables ), temperatura ("baja", es decir, cercana a la temperatura ambiente o "alta", es decir T ~ 1000 °C), tipo de proceso (deposición de vapor o crecimiento a partir de la solución) y otros parámetros.
Los monocristales grandes (muchos centímetros cúbicos) pueden crecer mediante transporte de gas (deposición en fase de vapor), síntesis hidrotermal , [34] [48] [49] o crecimiento en fusión. [7] Sin embargo, debido a la alta presión de vapor del ZnO, el crecimiento a partir de la masa fundida es problemático. El crecimiento por transporte de gas es difícil de controlar, por lo que se prefiere el método hidrotermal. [7] Las películas delgadas se pueden producir mediante deposición química de vapor , epitaxia metalorgánica en fase de vapor , electrodeposición , deposición por láser pulsado , pulverización catódica , síntesis sol-gel , deposición de capas atómicas , pirólisis por pulverización, etc.
El óxido de zinc en polvo blanco común se puede producir en el laboratorio electrolizando una solución de bicarbonato de sodio con un ánodo de zinc. Se producen hidróxido de zinc y gas hidrógeno. El hidróxido de zinc al calentarse se descompone en óxido de zinc:
Las nanoestructuras de ZnO se pueden sintetizar en una variedad de morfologías que incluyen nanocables, nanobarras , tetrápodos, nanocinturones, nanoflores, nanopartículas, etc. Las nanoestructuras se pueden obtener con la mayoría de las técnicas mencionadas anteriormente, en determinadas condiciones, y también con el método vapor-líquido-sólido. . [34] [50] [51] La síntesis normalmente se lleva a cabo a temperaturas de aproximadamente 90 °C, en una solución acuosa equimolar de nitrato de zinc y hexamina , proporcionando esta última el entorno básico. Ciertos aditivos, como el polietilenglicol o la polietilenimina, pueden mejorar la relación de aspecto de los nanocables de ZnO. [52] El dopaje de los nanocables de ZnO se ha logrado añadiendo otros nitratos metálicos a la solución de crecimiento. [53] La morfología de las nanoestructuras resultantes se puede ajustar cambiando los parámetros relacionados con la composición del precursor (como la concentración de zinc y el pH) o con el tratamiento térmico (como la temperatura y la velocidad de calentamiento). [54]
Se han cultivado nanocables de ZnO alineados sobre sustratos de silicio , vidrio y nitruro de galio previamente sembrados utilizando sales acuosas de zinc como nitrato de zinc y acetato de zinc en entornos básicos. [55] Los sustratos pre-sembrados con ZnO crean sitios para la nucleación homogénea de cristales de ZnO durante la síntesis. Los métodos comunes de pre-siembra incluyen la descomposición térmica in situ de cristalitos de acetato de zinc , el recubrimiento por rotación de nanopartículas de ZnO y el uso de métodos físicos de deposición de vapor para depositar películas delgadas de ZnO. [56] [57] La siembra previa se puede realizar junto con métodos de modelado de arriba hacia abajo, como la litografía por haz de electrones y la litografía de nanoesferas, para designar los sitios de nucleación antes del crecimiento. Los nanocables de ZnO alineados se pueden utilizar en células solares sensibilizadas con tintes y en dispositivos de emisión de campo. [58] [59]
Las aplicaciones del polvo de óxido de zinc son numerosas y las principales se resumen a continuación. La mayoría de las aplicaciones aprovechan la reactividad del óxido como precursor de otros compuestos de zinc. Para aplicaciones de ciencia de materiales, el óxido de zinc tiene un alto índice de refracción , alta conductividad térmica, propiedades aglutinantes, antibacterianas y de protección UV. En consecuencia, se agrega a materiales y productos que incluyen plásticos, cerámicas, vidrio, cemento, [60] caucho, lubricantes, [12] pinturas, ungüentos, adhesivos, selladores, fabricación de concreto , pigmentos, alimentos, baterías, ferritas, retardantes de fuego, etc. [61]
Entre el 50% y el 60% del uso de ZnO se produce en la industria del caucho. [62] El óxido de zinc junto con el ácido esteárico se utiliza en la vulcanización del caucho con azufre. [24] [63] Los aditivos de ZnO también protegen el caucho de los hongos (ver aplicaciones médicas) y la luz ultravioleta.
La industria cerámica consume una cantidad significativa de óxido de zinc, en particular en composiciones de fritas y esmaltes cerámicos. La capacidad calorífica relativamente alta, la conductividad térmica y la estabilidad a altas temperaturas del ZnO, junto con un coeficiente de expansión comparativamente bajo, son propiedades deseables en la producción de cerámica. El ZnO afecta el punto de fusión y las propiedades ópticas de los vidriados, esmaltes y formulaciones cerámicas. El óxido de zinc como fundente secundario de baja expansión mejora la elasticidad de los esmaltes al reducir el cambio de viscosidad en función de la temperatura y ayuda a prevenir el agrietamiento y el temblor. Al sustituir BaO y PbO por ZnO, se reduce la capacidad calorífica y se aumenta la conductividad térmica. El zinc en pequeñas cantidades mejora el desarrollo de superficies brillantes y brillantes. Sin embargo, en cantidades moderadas a altas, produce superficies mate y cristalinas. En cuanto al color, el zinc tiene una influencia complicada. [62]
El óxido de zinc en mezcla con aproximadamente un 0,5% de óxido de hierro (III) (Fe 2 O 3 ) se llama calamina y se utiliza en lociones de calamina. Históricamente el mineral calamina es una mezcla de los óxidos zincita y hemimorfita .
El óxido de zinc se usa ampliamente para tratar una variedad de afecciones de la piel, incluida la dermatitis atópica , la dermatitis de contacto , la picazón debida al eccema , la dermatitis del pañal y el acné . [64] Se utiliza en productos como talco para bebés y cremas protectoras para tratar la dermatitis del pañal , crema de calamina , champús anticaspa y ungüentos antisépticos . [18] [65] A menudo se combina con aceite de ricino para formar una crema emoliente y astringente , zinc y aceite de ricino, comúnmente utilizada para tratar a los bebés. [66] [67]
También es un componente de la cinta (llamada "cinta de óxido de zinc") que utilizan los atletas como vendaje para prevenir daños a los tejidos blandos durante los entrenamientos. [68]
El óxido de zinc se utiliza en productos de enjuague bucal y pastas de dientes como un agente antibacteriano propuesto para prevenir la formación de placa y sarro , [69] y para controlar el mal aliento al reducir los gases volátiles y los compuestos volátiles de azufre (VSC) en la boca. [70] Junto con el óxido de zinc o las sales de zinc, estos productos también suelen contener otros ingredientes activos, como cloruro de cetilpiridinio , [71] xilitol , [72] hinokitiol , [73] aceites esenciales y extractos de plantas . [74] [75] El óxido de zinc en polvo tiene propiedades desodorizantes y antibacterianas. [76]
El ZnO se agrega a tejidos de algodón, caucho, productos para el cuidado bucal [77] [78] y envases de alimentos. [79] [80] La acción antibacteriana mejorada de las partículas finas en comparación con el material a granel no es exclusiva del ZnO y se observa en otros materiales, como la plata . [81] Esta propiedad resulta del aumento de la superficie de las partículas finas.
El óxido de zinc se utiliza en protectores solares para absorber la luz ultravioleta . [64] Es el absorbente de UVA y UVB de más amplio espectro [82] [83] aprobado para su uso como protector solar por la Administración de Medicamentos y Alimentos de los EE. UU. (FDA), [84] y es completamente fotoestable. [85] Cuando se utiliza como ingrediente en un protector solar, el óxido de zinc bloquea los rayos de luz ultravioleta tanto UVA (320–400 nm) como UVB (280–320 nm) . El óxido de zinc y el otro protector solar físico más común, el dióxido de titanio , se consideran no irritantes, no alergénicos y no comedogénicos . [86] Sin embargo, el zinc procedente del óxido de zinc se absorbe ligeramente en la piel. [87]
Muchos protectores solares utilizan nanopartículas de óxido de zinc (junto con nanopartículas de dióxido de titanio) porque estas partículas pequeñas no dispersan la luz y, por lo tanto, no parecen blancas. Las nanopartículas no se absorben en la piel más que las partículas de óxido de zinc de tamaño normal [88] y solo se absorben en la capa más externa de la piel, pero no en el cuerpo. [88]
Cuando se mezcla con eugenol , se forma óxido de zinc eugenol , que tiene aplicaciones como restaurador y protésico en odontología . [29] [89]
El óxido de zinc se agrega a muchos productos alimenticios, incluidos los cereales para el desayuno , como fuente de zinc, [90] un nutriente necesario . El sulfato de zinc también se utiliza con el mismo fin. Algunos alimentos preenvasados también incluyen trazas de ZnO, incluso si no está destinado a ser un nutriente.
El óxido de zinc (blanco de zinc) se utiliza como pigmento en pinturas y es más opaco que el litopón , pero menos opaco que el dióxido de titanio . [14] También se utiliza en revestimientos para papel. El blanco chino es un grado especial de blanco de zinc que se utiliza en pigmentos para artistas. [91] El uso del blanco de zinc como pigmento en la pintura al óleo comenzó a mediados del siglo XVIII. [92] Ha sustituido en parte al venenoso blanco de plomo y fue utilizado por pintores como Böcklin , Van Gogh , [93] Manet , Munch y otros. También es un ingrediente principal del maquillaje mineral (CI 77947). [94]
El óxido de zinc micronizado y a nanoescala proporciona una fuerte protección contra la radiación ultravioleta UVA y UVB y, en consecuencia, se utiliza en protectores solares , [95] y también en gafas de sol que bloquean los rayos UV para uso en el espacio y para protección al soldar , según una investigación realizada por científicos de Jet. Laboratorio de Propulsión ( JPL ). [96]
Las pinturas que contienen polvo de óxido de zinc se utilizan desde hace mucho tiempo como revestimientos anticorrosivos para metales. Son especialmente eficaces para el hierro galvanizado. El hierro es difícil de proteger porque su reactividad con los recubrimientos orgánicos provoca fragilidad y falta de adherencia. Las pinturas de óxido de zinc conservan su flexibilidad y adherencia sobre dichas superficies durante muchos años. [61]
El ZnO altamente tipo n dopado con aluminio , galio o indio es transparente y conductor ( transparencia ~90%, resistividad más baja ~10 −4 Ω·cm [97] ). Los revestimientos de ZnO:Al se utilizan para ventanas que ahorran energía o protegen del calor. El revestimiento deja entrar la parte visible del espectro, pero refleja la radiación infrarroja (IR) de vuelta a la habitación (ahorro de energía) o no deja que la radiación IR entre en la habitación (protección contra el calor), dependiendo de qué lado de la ventana esté el revestimiento. [25]
Los plásticos, como el naftalato de polietileno (PEN), se pueden proteger aplicando una capa de óxido de zinc. El recubrimiento reduce la difusión de oxígeno a través del PEN. [98] Las capas de óxido de zinc también se pueden utilizar sobre policarbonato en aplicaciones exteriores. El recubrimiento protege el policarbonato de la radiación solar y disminuye su tasa de oxidación y su fotoamarillamiento. [99]
El óxido de zinc empobrecido en 64 Zn (el isótopo de zinc con masa atómica 64) se utiliza en la prevención de la corrosión en reactores nucleares de agua a presión . El agotamiento es necesario porque el 64 Zn se transforma en 65 Zn radiactivo bajo la irradiación de los neutrones del reactor. [100]
El óxido de zinc (ZnO) se utiliza como paso de pretratamiento para eliminar el sulfuro de hidrógeno (H 2 S) del gas natural después de la hidrogenación de cualquier compuesto de azufre antes de un reformador de metano , que puede envenenar el catalizador. A temperaturas entre aproximadamente 230 y 430 °C (446 y 806 °F), el H 2 S se convierte en agua mediante la siguiente reacción: [101]
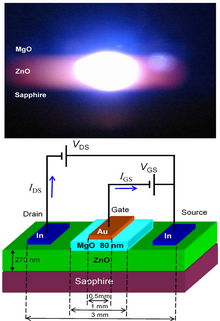

ZnO tiene una amplia banda prohibida directa (3,37 eV o 375 nm a temperatura ambiente). Por tanto, sus posibles aplicaciones más comunes son los diodos láser y los diodos emisores de luz (LED). [104] Además, se han informado no linealidades ultrarrápidas y funciones fotoconductoras en ZnO. [105] Algunas aplicaciones optoelectrónicas de ZnO se superponen con las de GaN , que tiene una banda prohibida similar (~3,4 eV a temperatura ambiente). En comparación con el GaN, el ZnO tiene una energía de unión de excitones mayor (~60 meV, 2,4 veces la energía térmica a temperatura ambiente), lo que da como resultado una emisión brillante a temperatura ambiente del ZnO. ZnO se puede combinar con GaN para aplicaciones LED. Por ejemplo, una capa de óxido conductor transparente y nanoestructuras de ZnO proporcionan un mejor acoplamiento de la luz. [106] Otras propiedades del ZnO favorables para aplicaciones electrónicas incluyen su estabilidad a la radiación de alta energía y su capacidad para modelarse mediante grabado químico húmedo. [107] La resistencia a la radiación [108] convierte al ZnO en un candidato adecuado para aplicaciones espaciales. ZnO es el candidato más prometedor en el campo de los láseres aleatorios para producir una fuente de láser UV bombeada electrónicamente.
Las puntas puntiagudas de las nanobarras de ZnO provocan una fuerte mejora del campo eléctrico. Por tanto, pueden utilizarse como emisores de campo . [109]
Como electrodos transparentes se utilizan capas de ZnO dopadas con aluminio . Los componentes Zn y Al son mucho más baratos y menos tóxicos en comparación con el óxido de indio y estaño (ITO) de uso general. Una aplicación que ha comenzado a estar disponible comercialmente es el uso de ZnO como contacto frontal de células solares o de pantallas de cristal líquido . [110]
Con ZnO se pueden fabricar transistores transparentes de película fina (TTFT). Como transistores de efecto de campo, no necesitan unión ap-n, [111] evitando así el problema de dopaje tipo p del ZnO. Algunos de los transistores de efecto de campo incluso utilizan nanobarras de ZnO como canales conductores. [112]
El óxido de zinc se utiliza en sensores de gas semiconductores para detectar compuestos transportados por el aire, como sulfuro de hidrógeno , dióxido de nitrógeno y compuestos orgánicos volátiles . ZnO es un semiconductor que se dopa con n mediante adsorción de compuestos reductores , lo que reduce la resistencia eléctrica detectada a través del dispositivo, de una manera similar a los sensores de gas semiconductores de óxido de estaño ampliamente utilizados . Se forma en nanoestructuras como películas delgadas, nanopartículas , nanopilares o nanocables para proporcionar una gran superficie para la interacción con los gases. Los sensores se hacen selectivos para gases específicos mediante dopado o materiales de unión a la superficie, como metales nobles catalíticos. [113] [114]
Se ha demostrado que la piezoelectricidad de las fibras textiles recubiertas de ZnO es capaz de fabricar "nanosistemas autoalimentados" con la tensión mecánica cotidiana provocada por el viento o los movimientos corporales. [115] [116]
En 2008, el Centro de Caracterización de Nanoestructuras del Instituto de Tecnología de Georgia informó sobre la producción de un dispositivo generador de electricidad (llamado generador de bomba de carga flexible) que suministra corriente alterna estirando y liberando nanocables de óxido de zinc. Este minigenerador crea un voltaje oscilante de hasta 45 milivoltios, convirtiendo cerca del siete por ciento de la energía mecánica aplicada en electricidad. Los investigadores utilizaron cables con longitudes de 0,2 a 0,3 mm y diámetros de tres a cinco micrómetros, pero el dispositivo se pudo reducir a un tamaño más pequeño. [117]

En forma de película delgada, el ZnO se ha demostrado en resonadores, sensores y filtros de película delgada miniaturizados de alta frecuencia.
El ZnO es un material de ánodo prometedor para baterías de iones de litio porque es barato, biocompatible y respetuoso con el medio ambiente. ZnO tiene una capacidad teórica más alta (978 mAh g −1 ) que muchos otros óxidos de metales de transición como CoO (715 mAh g −1 ), NiO (718 mAh g −1 ) y CuO (674 mAh g −1 ). [118] El ZnO también se utiliza como electrodo en supercondensadores. [119]
Como aditivo alimentario , el óxido de zinc está en la lista de sustancias generalmente reconocidas como seguras o GRAS de la FDA de EE. UU. [120]
El óxido de zinc en sí no es tóxico; Sin embargo, es peligroso inhalar altas concentraciones de vapores de óxido de zinc, como los que se generan cuando el zinc o sus aleaciones se funden y oxidan a altas temperaturas. Este problema ocurre al fundir aleaciones que contienen latón porque el punto de fusión del latón está cerca del punto de ebullición del zinc. [121] La inhalación de óxido de zinc, que puede ocurrir al soldar acero galvanizado (galvanizado) , puede provocar una enfermedad llamada fiebre de vapores metálicos . [121]
En formulaciones de protectores solares que combinaban óxido de zinc con absorbentes de UV de molécula pequeña, la luz ultravioleta provocó la fotodegradación de los absorbentes de molécula pequeña y toxicidad en ensayos de embriones de pez cebra. [122]