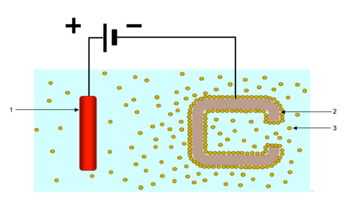
La deposición electroforética ( EPD ) es un término para una amplia gama de procesos industriales que incluyen electrorrecubrimiento , electrodeposición catódica , electrodeposición anódica y recubrimiento electroforético o pintura electroforética . Un rasgo característico de este proceso es que las partículas coloidales suspendidas en un medio líquido migran bajo la influencia de un campo eléctrico ( electroforesis ) y se depositan sobre un electrodo . Todas las partículas coloidales que puedan usarse para formar suspensiones estables y que puedan llevar una carga pueden usarse en deposición electroforética. Esto incluye materiales como polímeros , pigmentos , tintes , cerámicas y metales .
El proceso es útil para aplicar materiales a cualquier superficie eléctricamente conductora . Los materiales que se depositan son el principal factor determinante en las condiciones reales de procesamiento y en el equipo que se puede utilizar.
Debido a la amplia utilización de procesos de pintura electroforética en muchas industrias, la EPD acuosa es el proceso de EPD más comúnmente utilizado comercialmente. Sin embargo, se conocen aplicaciones de deposición electroforética no acuosa. Actualmente se están explorando aplicaciones de EPD no acuosas para su uso en la fabricación de componentes electrónicos y la producción de revestimientos cerámicos . Los procesos no acuosos tienen la ventaja de evitar la electrólisis del agua y el desprendimiento de oxígeno que acompaña a la electrólisis.
Este proceso se utiliza industrialmente para aplicar recubrimientos a productos fabricados con metal. Se ha utilizado ampliamente para recubrir carrocerías y piezas de automóviles, tractores y equipos pesados, interruptores eléctricos, electrodomésticos, muebles metálicos, envases de bebidas, sujetadores y muchos otros productos industriales.
Los procesos de EPD se aplican a menudo para la fabricación de fotocatalizadores de dióxido de titanio (TiO 2 ) soportados para aplicaciones de purificación de agua, utilizando polvos precursores que pueden inmovilizarse mediante métodos de EPD sobre diversos materiales de soporte. Las películas gruesas producidas de esta manera permiten una síntesis más barata y rápida en comparación con las películas delgadas de sol-gel , junto con niveles más altos de superficie del fotocatalizador.
En la fabricación de pilas de combustible de óxido sólido, las técnicas de EPD se emplean ampliamente para la fabricación de ánodos porosos de ZrO 2 a partir de precursores en polvo sobre sustratos conductores.
Los procesos de EPD tienen una serie de ventajas que han hecho que estos métodos se utilicen ampliamente [1]
En varios laboratorios de investigación se han fabricado piezas cerámicas gruesas y complejas. Además, la EPD se ha utilizado para producir microestructuras personalizadas , como gradientes funcionales y laminados, mediante el control de la suspensión durante el procesamiento. [2]
La primera patente para el uso de pintura electroforética fue concedida en 1917 a Davey y General Electric . Desde la década de 1920, el proceso se utiliza para la deposición de látex de caucho . En la década de 1930 se emitieron las primeras patentes que describían resinas dispersables en agua, neutralizadas con base, diseñadas específicamente para EPD.
El recubrimiento electroforético comenzó a tomar su forma actual a fines de la década de 1950, cuando el Dr. George EF Brewer y el equipo de Ford Motor Company comenzaron a trabajar en el desarrollo del proceso para el recubrimiento de automóviles. El primer sistema automotriz anódico comercial comenzó a operar en 1963.
La primera patente para un producto EPD catódico se emitió en 1965 y se asignó a BASF AG . PPG Industries, Inc. fue el primero en introducir EPD catódico comercialmente en 1970. El primer uso de EPD catódico en la industria automotriz fue en 1975. Hoy en día, alrededor del 70 % del volumen de EPD que se utiliza en el mundo es del tipo EPD catódico. , en gran parte debido al alto uso de la tecnología en la industria automotriz. Es probablemente el mejor sistema jamás desarrollado y ha dado como resultado una gran extensión de la vida útil de la carrocería en la industria automotriz.
Se han concedido miles de patentes relacionadas con diversas composiciones de EPD, procesos de EPD y artículos recubiertos con EPD. Aunque las patentes han sido emitidas por varias oficinas de patentes gubernamentales, prácticamente todos los desarrollos importantes se pueden seguir revisando las patentes emitidas por la Oficina de Patentes y Marcas de EE. UU .
El proceso industrial general de deposición electroforética consta de varios subprocesos:
Durante el propio proceso de EPD, se aplica corriente continua a una solución de polímeros con grupos ionizables o una suspensión coloidal de polímeros con grupos ionizables que también pueden incorporar materiales sólidos como pigmentos y cargas. Los grupos ionizables incorporados al polímero se forman mediante la reacción de un ácido y una base para formar una sal . La carga particular, positiva o negativa, que se imparte al polímero depende de la naturaleza química del grupo ionizable. Si los grupos ionizables del polímero son ácidos, el polímero llevará una carga negativa cuando se le agregue sal con una base. Si los grupos ionizables del polímero son bases, el polímero llevará una carga positiva cuando se le agregue sal con un ácido.
Hay dos tipos de procesos EPD, anódicos y catódicos. En el proceso anódico, el material cargado negativamente se deposita sobre el electrodo o ánodo cargado positivamente . En el proceso catódico, el material cargado positivamente se deposita sobre el electrodo o cátodo cargado negativamente . [3]
Cuando se aplica un campo eléctrico, todas las especies cargadas migran mediante el proceso de electroforesis hacia el electrodo con carga opuesta. Existen varios mecanismos mediante los cuales se puede depositar material sobre el electrodo:
El principal proceso electroquímico que se produce durante la electrodeposición acuosa es la electrólisis del agua. Esto se puede demostrar mediante las siguientes dos semirreacciones que ocurren en los dos electrodos:
En la deposición anódica, el material que se deposita tendrá sales de un ácido como grupo portador de carga. Estos aniones cargados negativamente reaccionan con los iones de hidrógeno (protones) cargados positivamente que se producen en el ánodo mediante la electrólisis del agua para reformar el ácido original. El ácido completamente protonado no lleva carga (destrucción de carga) y es menos soluble en agua y puede precipitar del agua al ánodo.
La situación análoga ocurre en la deposición catódica excepto que el material que se deposita tendrá sales de una base como grupo portador de carga. Si la sal de la base se ha formado por protonación de la base, la base protonada reaccionará con los iones hidroxilo que se forman por electrólisis del agua para producir la base cargada neutra (nuevamente destrucción de carga) y agua. El polímero no cargado es menos soluble en agua que cuando estaba cargado y se produce precipitación sobre el cátodo.
Las sales de onio, que se han utilizado en el proceso catódico, no son bases protonadas y no se depositan mediante el mecanismo de destrucción de carga. Este tipo de materiales se pueden depositar en el cátodo mediante coagulación por concentración y sal. A medida que las partículas coloidales alcanzan el objeto sólido que se va a recubrir, se comprimen y el agua de los intersticios sale expulsada. A medida que se comprimen las micelas individuales , colapsan para formar micelas cada vez más grandes. La estabilidad coloidal es inversamente proporcional al tamaño de la micela, de modo que a medida que las micelas crecen, se vuelven cada vez menos estables hasta que precipitan de la solución sobre el objeto a recubrir. A medida que más y más grupos cargados se concentran en un volumen más pequeño, esto aumenta la fuerza iónica del medio, lo que también ayuda a precipitar los materiales fuera de la solución. Ambos procesos ocurren simultáneamente y ambos contribuyen a la deposición de material.
Durante el proceso de deposición acuosa, se forma gas en ambos electrodos. Se forma gas hidrógeno en el cátodo y oxígeno en el ánodo . Para una determinada cantidad de transferencia de carga, se genera exactamente el doble de hidrógeno que oxígeno a nivel molecular.
Esto tiene algunos efectos significativos en el proceso de recubrimiento. El más evidente es el aspecto de la película depositada antes del proceso de horneado. El proceso catódico da como resultado que quede mucho más gas atrapado dentro de la película que el proceso anódico. Dado que el gas tiene una resistencia eléctrica más alta que la película depositada o el baño mismo, la cantidad de gas tiene un efecto significativo sobre la corriente a un voltaje aplicado determinado . Por esta razón, los procesos catódicos a menudo pueden funcionar con tensiones significativamente más altas que los procesos anódicos correspondientes.
El recubrimiento depositado tiene una resistencia significativamente mayor que el objeto que se está recubriendo. A medida que la película depositada precipita, la resistencia aumenta. El aumento de la resistencia es proporcional al espesor de la película depositada y, por tanto, a un voltaje determinado, la corriente eléctrica disminuye a medida que la película se vuelve más gruesa hasta que finalmente llega a un punto en el que la deposición se ha ralentizado o ha dejado de ocurrir (autolimitante). Por tanto, el voltaje aplicado es el control principal de la cantidad de película aplicada.
La capacidad del recubrimiento EPD para cubrir los huecos interiores de una pieza se denomina "potencia de lanzamiento". En muchas aplicaciones, es deseable utilizar materiales de revestimiento con un alto poder de proyección. La potencia de proyección de un recubrimiento depende de una serie de variables, pero en general, se puede afirmar que cuanto mayor sea el voltaje del recubrimiento, más lejos se "arrojará" un recubrimiento determinado hacia los huecos. Las pinturas electroforéticas de alto poder de proyección suelen utilizar voltajes de aplicación superiores a 300 voltios CC.
La temperatura del recubrimiento también es una variable importante que afecta el proceso de EPD. La temperatura del recubrimiento tiene un efecto sobre la conductividad del baño y la conductividad de la película depositada, que aumenta a medida que aumenta la temperatura. La temperatura también tiene un efecto sobre la viscosidad de la película depositada, lo que a su vez afecta la capacidad de la película depositada para liberar las burbujas de gas que se están formando.
La temperatura de coalescencia del sistema de recubrimiento también es una variable importante para el diseñador de recubrimientos. Puede determinarse trazando la estructura de la película de un sistema determinado frente a la temperatura del recubrimiento manteniendo constantes el tiempo de recubrimiento y el perfil de aplicación de voltaje. A temperaturas por debajo de la temperatura de coalescencia, el comportamiento de crecimiento de la película y el comportamiento de ruptura son bastante diferentes de la práctica habitual como resultado de la deposición porosa.
El tiempo de recubrimiento también es una variable importante para determinar el espesor de la película, la calidad de la película depositada y la potencia de proyección. Dependiendo del tipo de objeto a recubrir, pueden ser apropiados tiempos de recubrimiento de varios segundos hasta varios minutos.
El voltaje máximo que se puede utilizar depende del tipo de sistema de recubrimiento y de otros factores. Como ya se indicó, el espesor de la película y la potencia de proyección dependen del voltaje de aplicación. Sin embargo, con tensiones excesivamente altas puede producirse un fenómeno llamado "ruptura". La tensión donde se produce este fenómeno se denomina "tensión de ruptura". El resultado de la rotura es una película que suele ser muy espesa y porosa. Normalmente esta no es una película aceptable desde el punto de vista cosmético o funcional. Las causas y mecanismos de ruptura no se comprenden completamente, sin embargo, se sabe lo siguiente:
Hay dos categorías principales de químicas de EPD: anódica y catódica. Ambos siguen utilizándose comercialmente, aunque el proceso anódico se utiliza industrialmente desde hace más tiempo y, por tanto, se considera el más antiguo de los dos procesos. Existen ventajas y desventajas para ambos tipos de procesos, y diferentes expertos pueden tener diferentes perspectivas sobre algunos de los pros y los contras de cada uno.
Las principales ventajas que normalmente se promocionan para el proceso anódico son:
Las principales ventajas que normalmente se promocionan para los procesos catódicos son:
Una diferencia significativa y real que no se menciona a menudo es el hecho de que las tecnologías de reticulación catalizada por ácido son más apropiadas para el proceso anódico. Estos reticulantes se utilizan ampliamente en todo tipo de aplicaciones de revestimiento. Estos incluyen reticulantes tan populares y relativamente económicos como reticulantes de melamina - formaldehído , fenol -formaldehído, urea-formaldehído y acrilamida -formaldehído.
Los reticulantes del tipo melamina-formaldehído en particular se utilizan ampliamente en electrorrecubrimientos anódicos. Estos tipos de reticulantes son relativamente económicos y proporcionan una amplia gama de características de curado y rendimiento que permiten al diseñador de recubrimientos adaptar el producto al uso final deseado. Los recubrimientos formulados con este tipo de reticulante pueden tener una resistencia a la luz ultravioleta aceptable. Muchos de ellos son materiales de viscosidad relativamente baja y pueden actuar como plastificantes reactivos, reemplazando parte del disolvente orgánico que de otro modo sería necesario. La cantidad de formaldehído libre, así como el formaldehído que puede liberarse durante el proceso de horneado, es motivo de preocupación, ya que se consideran contaminantes atmosféricos peligrosos.
La película depositada en los sistemas catódicos es bastante alcalina y las tecnologías de reticulación catalizada por ácido no han sido preferidas en los productos catódicos en general, aunque ha habido algunas excepciones. El tipo más común de química de reticulación que se utiliza hoy en día con productos catódicos se basa en la química del uretano y la urea.
El reticulador aromático de tipo poliuretano y urea es una de las razones importantes por las que muchos electrorrecubrimientos catódicos muestran altos niveles de protección contra la corrosión. Por supuesto, esta no es la única razón, pero si se comparan las composiciones de electrorrecubrimiento con reticulantes de uretano aromáticos con sistemas análogos que contienen reticulantes de uretano alifáticos, los sistemas con reticulantes de uretano aromáticos funcionan consistentemente significativamente mejor. Sin embargo, los recubrimientos que contienen reticulantes de uretano aromáticos generalmente no funcionan bien en términos de resistencia a la luz UV. Si el recubrimiento resultante contiene reticulaciones de urea aromática, la resistencia a los rayos UV será considerablemente peor que si solo pudieran ocurrir reticulaciones de uretano. Una desventaja de los uretanos aromáticos es que también pueden provocar el amarillamiento del propio revestimiento, así como el amarillamiento de las capas superiores posteriores. Una importante reacción secundaria no deseada que se produce durante el proceso de horneado produce poliaminas aromáticas . Se puede esperar que los reticulantes de uretano basados en diisocianato de tolueno (TDI) produzcan tolueno diamina como reacción secundaria, mientras que los basados en diisocianato de metilendifenilo produzcan diaminodifenilmetano y poliaminas aromáticas de orden superior. Las poliaminas aromáticas no deseadas pueden inhibir el curado de las capas superiores subsiguientes catalizadas por ácido y pueden provocar la deslaminación de las capas superiores posteriores después de la exposición a la luz solar. Aunque la industria nunca ha reconocido este problema, muchas de estas poliaminas aromáticas no deseadas son cancerígenas conocidas o sospechadas.
Además de las dos categorías principales, anódica y catódica, los productos EPD también pueden describirse según la química del polímero base que se utiliza. Hay varios tipos de polímeros que se han utilizado comercialmente. Muchos de los tipos anódicos anteriores se basaban en aceites maleinizados de varios tipos, siendo el tall oil y el aceite de linaza dos de los más comunes. Hoy en día predominan los tipos epoxi y acrílico. La descripción y las ventajas generalmente promocionadas son las siguientes:
La tasa de deposición electroforética (EPD) depende de múltiples procesos cinéticos diferentes que actúan en conjunto. Uno de los principales procesos cinéticos implicados en la EPD es la electroforesis, el movimiento de partículas cargadas en respuesta a un campo eléctrico. Pero a medida que la concentración local de partículas disminuye cerca de los electrodos, la difusión de partículas desde áreas de alta concentración a áreas de baja concentración, impulsada por una diferencia en el potencial químico, también influirá en la velocidad de deposición. Esta sección discutirá las condiciones que determinan las tasas de cada uno de estos procesos y cómo esas variables se incorporan en diferentes modelos utilizados para evaluar la DEP.
Para que ocurra cualquiera de los procesos, las moléculas deben formar una suspensión acuosa estable. Hay cuatro procesos comunes mediante los cuales la partícula puede obtener la carga superficial necesaria para formar una dispersión estable: 1. Disociación o ionización de un grupo superficial 2. Reabsorción de iones 3. Adsorción de tensioactivos ionizados 4. Sustitución isomorfa. La química de la superficie de la molécula y su entorno local determinarán cómo obtiene una carga superficial. Sin suficiente carga superficial para equilibrar las fuerzas de atracción de Van der Waals entre las partículas, estas se agregarán. Una superficie cargada no es el único parámetro que influye en la estabilidad coloidal. El tamaño de las partículas, el potencial zeta y la conductividad, la viscosidad y la constante dieléctrica del disolvente también determinan la estabilidad de la dispersión. [4] Mientras la dispersión sea estable, la velocidad inicial de deposición estará determinada principalmente por la intensidad del campo eléctrico. La resistencia de la solución puede disipar el voltaje aplicado, por lo que la carga superficial real en cada electrodo puede ser menor de lo previsto. Las partículas cargadas se adherirán a un sustrato ubicado en el electrodo con carga opuesta. Como simplificación, bajo voltajes bajos y tiempos de deposición cortos, la ley de Hamaker [3] describe una relación lineal entre la intensidad del campo, el espesor depositado y el tiempo.
Esta ecuación da la masa depositada electroforéticamente m en gramos, como función de la movilidad electroforética μ (en unidades de cm 2 s −1 ), carga de sólidos C s (en g cm −3 ), área de superficie cubierta S (cm 2 ), carga eléctrica intensidad de campo E (V cm −1 ) y tiempo t (s). Esta ecuación es útil para evaluar la eficiencia de los procesos de EPD aplicados en relación con los valores teóricos.
La aproximación lineal simple aplicada por la ley de Hamaker se degrada bajo voltajes más altos y tiempos de deposición más prolongados. Bajo voltajes más altos, las reacciones químicas, como la reducción, impulsadas por la influencia del campo aplicado, pueden oscurecer la cinética. Por lo tanto, se deben utilizar disolventes con altos potenciales de reducción-oxidación para evitar la electrólisis y el desprendimiento de gases. [4] Y si las partículas depositadas son aislantes, a medida que la capa depositada se hace más gruesa, el campo eléctrico efectivo disminuirá. Además, el área que rodea la región electroactiva cerca de los electrodos quedará vacía de partículas. La difusión de partículas desde la masa hasta la región electroactiva puede limitar la tasa de crecimiento. La difusión de partículas de alta a baja concentración puede aproximarse mediante las leyes de Fick y su velocidad estará determinada por la diferencia en la concentración de partículas, así como por la viscosidad del solvente, la masa de las partículas y la estabilidad coloidal. Con el tiempo, a medida que aumenta el espesor de la deposición y disminuye la intensidad del campo, el crecimiento se saturará. El cambio de espesor que se produce al inicio de la saturación se describe mediante la siguiente ecuación. [5]
dónde
w es el peso de las partículas sólidas depositadas sobre el electrodo, k la constante cinética, t el tiempo de deposición, A el área del electrodo, V el volumen de la suspensión, el peso inicial de las partículas sólidas en la suspensión, ε la constante dieléctrica de el líquido, ξ el potencial zeta de la partícula en el disolvente, n la viscosidad del disolvente, E el voltaje de corriente continua aplicado y E la caída de voltaje a través de la capa depositada. [5]
Antes de la saturación existe una relación lineal entre el espesor de deposición y el tiempo. El inicio de la saturación conduce a una disminución en la tasa de deposición que se modela como comportamiento parabólico. El tiempo de transición crítico entre el comportamiento lineal y parabólico se aproxima mediante la siguiente ecuación. [5]
t es el tiempo de transición crítico, es la pendiente del régimen parabólico y es la pendiente de la tasa de crecimiento de la capa de deposición en el régimen lineal.
Al determinar la aplicabilidad de la EPD a un sistema, es necesario garantizar la estabilidad coloidal y la combinación de voltaje aplicado y tiempo de reacción que producirá el espesor depositado deseado.
En determinadas aplicaciones, como la deposición de materiales cerámicos, no se pueden aplicar voltajes superiores a 3-4 V en EPD acuoso si es necesario evitar la electrólisis del agua. Sin embargo, pueden ser deseables voltajes de aplicación más altos para lograr mayores espesores de recubrimiento o aumentar la velocidad de deposición. En tales aplicaciones, se utilizan disolventes orgánicos en lugar de agua como medio líquido. Como disolventes orgánicos se utilizan generalmente disolventes polares como alcoholes y cetonas. El etanol , la acetona y la metiletilcetona son ejemplos de disolventes que se han descrito como candidatos adecuados para su uso en la deposición electroforética.