La enfermedad de Huntington ( EH ), también conocida como corea de Huntington , es una enfermedad neurodegenerativa incurable [7] que se hereda principalmente . [8] Los primeros síntomas suelen ser problemas sutiles con el estado de ánimo o las capacidades mentales/psiquiátricas. [9] [1] A menudo sigue una falta general de coordinación y una marcha inestable. [2] También es una enfermedad de los ganglios basales que causa un trastorno del movimiento hipercinético conocido como corea . [10] [11] A medida que la enfermedad avanza, los movimientos corporales involuntarios y descoordinados de la corea se vuelven más evidentes. [1] Las capacidades físicas empeoran gradualmente hasta que el movimiento coordinado se vuelve difícil y la persona no puede hablar. [1] [2] Las capacidades mentales generalmente disminuyen hasta convertirse en demencia , depresión, apatía e impulsividad en ocasiones. [9] [12] [3] Los síntomas específicos varían un poco entre las personas. [1] Los síntomas generalmente comienzan entre los 30 y los 50 años de edad, y pueden comenzar a cualquier edad, pero generalmente se observan alrededor de los 40 años. [12] [9] [3] [4] La enfermedad puede desarrollarse antes en cada etapa sucesiva. generación . [1] Alrededor del ocho por ciento de los casos comienzan antes de los 20 años y se conocen como EH juvenil , que generalmente se presenta con los síntomas de movimiento lento de la enfermedad de Parkinson en lugar de los de corea. [3]
La EH generalmente se hereda de un padre afectado , que porta una mutación en el gen de la Huntingtina ( HTT ). [4] Sin embargo, hasta el 10% de los casos se deben a una nueva mutación. [1] El gen de la Huntingtina proporciona la información genética para la proteína Huntingtina (Htt). [1] La expansión de las repeticiones CAG de citosina - adenina - guanina (conocida como expansión de repeticiones de trinucleótidos ) en el gen que codifica la proteína Huntingtina da como resultado una proteína mutante anormal (mHtt), que daña gradualmente las células cerebrales a través de varios mecanismos posibles. . [8] [13] La proteína mutante es dominante , por lo que tener un padre que sea portador del rasgo es suficiente para desencadenar la enfermedad en sus hijos. El diagnóstico se realiza mediante pruebas genéticas , que se pueden realizar en cualquier momento, independientemente de si hay síntomas o no. [5] Este hecho plantea varios debates éticos: la edad a la que un individuo se considera lo suficientemente maduro para elegir la prueba; si los padres tienen derecho a que sus hijos sean examinados; y gestionar la confidencialidad y divulgación de los resultados de las pruebas. [2]
No se conoce ninguna cura para la EH y se requiere atención a tiempo completo en las etapas posteriores. [2] Los tratamientos pueden aliviar algunos síntomas y, en algunos casos, mejorar la calidad de vida . [3] La mejor evidencia para el tratamiento de los problemas de movimiento es la tetrabenazina . [3] La EH afecta aproximadamente a entre 4 y 15 de cada 100.000 personas de ascendencia europea. [1] [3] Es raro entre los finlandeses y los japoneses, mientras que se desconoce la tasa de aparición en África. [3] La enfermedad afecta por igual a hombres y mujeres. [3] Complicaciones como neumonía , enfermedades cardíacas y lesiones físicas por caídas reducen la esperanza de vida; aunque la neumonía por aspiración mortal se cita comúnmente como la causa última de muerte de quienes padecen la afección. [14] [12] [3] El suicidio es la causa de muerte en aproximadamente el 9% de los casos. [3] La muerte suele ocurrir entre 15 y 20 años después de que se detectó la enfermedad por primera vez. [4]
La primera descripción conocida de la enfermedad fue realizada en 1841 por el médico estadounidense Charles Oscar Waters. [15] La afección fue descrita con más detalle en 1872 por el médico estadounidense George Huntington . [15] La base genética fue descubierta en 1993 gracias a un esfuerzo de colaboración internacional liderado por la Hereditary Disease Foundation . [16] [17] Las organizaciones de investigación y apoyo comenzaron a formarse a fines de la década de 1960 para aumentar la conciencia pública, brindar apoyo a las personas y sus familias y promover la investigación. [17] [18] Las direcciones de investigación incluyen determinar el mecanismo exacto de la enfermedad, mejorar los modelos animales para ayudar con la investigación, probar medicamentos y su administración para tratar los síntomas o retardar la progresión de la enfermedad, y estudiar procedimientos como el uso de células madre. Terapia con el objetivo de reemplazar neuronas dañadas o perdidas. [dieciséis]
Los signos y síntomas de la enfermedad de Huntington se manifiestan con mayor frecuencia entre los 30 y los 50 años, pero pueden comenzar a cualquier edad [4] y presentarse como una tríada de síntomas motores, cognitivos y psiquiátricos. [19] Cuando se desarrolla en una etapa temprana, se conoce como enfermedad de Huntington juvenil. [20] En el 50% de los casos, los síntomas psiquiátricos aparecen primero. [19] Su progresión se describe a menudo en etapas tempranas, intermedias y tardías con una fase prodrómica anterior . [2] En las primeras etapas, se producen cambios sutiles de personalidad, problemas cognitivos y de habilidades físicas, irritabilidad y cambios de humor, todo lo cual puede pasar desapercibido, [21] [22] y generalmente precede a los síntomas motores. [23] Casi todas las personas con EH eventualmente presentan síntomas físicos similares, pero la aparición, la progresión y el alcance de los síntomas cognitivos y conductuales varían significativamente entre individuos. [24] [25]
Los síntomas físicos iniciales más característicos son los movimientos entrecortados, aleatorios e incontrolables llamados corea . [10] Muchas personas no son conscientes de sus movimientos involuntarios o se ven obstaculizados por ellos. [1] La corea puede manifestarse inicialmente como inquietud general, pequeños movimientos iniciados involuntariamente o incompletos, falta de coordinación o movimientos oculares sacádicos lentos . [26] Estas anomalías motoras menores suelen preceder a signos más evidentes de disfunción motora en al menos tres años. [27] La apariencia clara de síntomas como rigidez, movimientos de contorsión o posturas anormales aparecen a medida que avanza el trastorno. [26] Estos son signos de que el sistema del cerebro responsable del movimiento se ha visto afectado. [28] Las funciones psicomotoras se deterioran cada vez más, de modo que cualquier acción que requiera control muscular se ve afectada. Cuando el control muscular se ve afectado como rigidez o contractura muscular esto se conoce como distonía . La distonía es un trastorno neurológico del movimiento hipercinético que produce movimientos repetitivos o de torsión, que pueden parecerse a un temblor. Las consecuencias comunes son inestabilidad física, expresión facial anormal y dificultades para masticar, tragar y hablar . [26] Los trastornos del sueño y la pérdida de peso también son síntomas asociados. [29] Las dificultades para comer comúnmente causan pérdida de peso y pueden provocar desnutrición. [30] [31] La pérdida de peso es común en personas con enfermedad de Huntington y progresa con la enfermedad. La EH juvenil generalmente progresa a un ritmo más rápido con un mayor deterioro cognitivo, y la corea se presenta brevemente, en todo caso; la variante de Westphal de lentitud de movimientos , rigidez y temblores es más típica en la EH juvenil, al igual que las convulsiones . [26] [29]
Las capacidades cognitivas se deterioran progresivamente y, en general, tienden a declinar hasta llegar a la demencia . [3] Especialmente afectadas son las funciones ejecutivas , que incluyen planificación, flexibilidad cognitiva, pensamiento abstracto , adquisición de reglas, inicio de acciones apropiadas e inhibición de acciones inapropiadas. Los diferentes deterioros cognitivos incluyen dificultad para concentrarse en las tareas, falta de flexibilidad, falta de impulso, falta de conciencia de los propios comportamientos y habilidades y dificultad para aprender o procesar nueva información. A medida que avanza la enfermedad, tienden a aparecer déficits de memoria . Los deterioros reportados van desde déficits de memoria a corto plazo hasta dificultades de memoria a largo plazo , incluidos déficits en la memoria episódica (memoria de la vida), procedimental (memoria del cuerpo sobre cómo realizar una actividad) y de trabajo . [28]
Los signos neuropsiquiátricos informados son ansiedad , depresión , disminución de las emociones , egocentrismo , agresión y conducta compulsiva , alucinaciones y delirios . [32] Otros trastornos psiquiátricos comunes podrían incluir el trastorno obsesivo-compulsivo , la manía , el insomnio y el trastorno bipolar . También se han observado dificultades para reconocer las expresiones negativas de otras personas. [28] La prevalencia de estos síntomas es muy variable entre los estudios, con tasas estimadas de prevalencia de trastornos psiquiátricos a lo largo de la vida entre 33 y 76%. [32] Para muchas personas con la enfermedad y sus familias, estos síntomas se encuentran entre los aspectos más angustiosos de la enfermedad, y a menudo afectan el funcionamiento diario y constituyen un motivo de institucionalización . [32] Los cambios de comportamiento tempranos en la EH resultan en un mayor riesgo de suicidio. [10] A menudo, las personas tienen una conciencia reducida de la corea y de los deterioros cognitivos y emocionales. [33]
La Huntingtina mutante se expresa en todo el cuerpo y se asocia con anomalías en los tejidos periféricos que son causadas directamente por dicha expresión fuera del cerebro. Estas anomalías incluyen atrofia muscular , insuficiencia cardíaca , intolerancia a la glucosa , pérdida de peso , osteoporosis y atrofia testicular . [34]
Todo el mundo tiene dos copias del gen de la Huntingtina ( HTT ), que codifica la proteína Huntingtina (Htt). HTT también se llama gen HD y gen IT15 ( transcripción interesante 15). Parte de este gen es una sección repetida llamada expansión de repetición de trinucleótidos , una repetición corta , que varía en longitud entre individuos y puede cambiar de longitud entre generaciones. Si la repetición está presente en un gen sano, una mutación dinámica puede aumentar el recuento de repeticiones y dar como resultado un gen defectuoso. Cuando la longitud de esta sección repetida alcanza un cierto umbral, produce una forma alterada de la proteína, llamada proteínahuntingtina mutante (mHtt). Las diferentes funciones de estas proteínas son la causa de cambios patológicos, que a su vez provocan los síntomas de la enfermedad. La mutación de la enfermedad de Huntington es genéticamente dominante y casi completamente penetrante ; La mutación de cualquiera de los alelos HTT de una persona causa la enfermedad. No se hereda según el sexo, sino por la longitud de la sección repetida del gen; por lo tanto, su gravedad puede verse influenciada por el sexo del progenitor afectado. [26]
La EH es uno de varios trastornos de repetición de trinucleótidos causados por la longitud de una sección repetida de un gen que excede un rango normal. [26] El gen HTT está ubicado en el brazo corto del cromosoma 4 [26] en 4p16.3. HTT contiene una secuencia de tres bases de ADN , citosina-adenina-guanina (CAG), repetidas varias veces (es decir, CAGCAGCAG...), conocida como repetición de trinucleótidos. [26] CAG es el código genético de tres letras ( codón ) para el aminoácido glutamina , por lo que una serie de ellas da como resultado la producción de una cadena de glutamina conocida como tracto de poliglutamina (o tracto poliQ), y la parte repetida de el gen, la región poliQ . [35]
.jpg/440px-Huntington's_disease_(5880985560).jpg)
Generalmente, las personas tienen menos de 36 glutaminas repetidas en la región poliQ, lo que da como resultado la producción de la proteína citoplasmáticahuntintina . [26] Sin embargo, una secuencia de 36 o más glutaminas da como resultado la producción de una proteína con características diferentes. [26] Esta forma alterada, llamadahuntingtina mutante (mHtt), aumenta la tasa de descomposición de ciertos tipos de neuronas . Las regiones del cerebro tienen diferentes cantidades y dependencia de este tipo de neuronas y se ven afectadas en consecuencia. [26] Generalmente, el número de repeticiones CAG está relacionado con cuánto se ve afectado este proceso y representa aproximadamente el 60% de la variación de la edad de aparición de los síntomas. La variación restante se atribuye al medio ambiente y a otros genes que modifican el mecanismo de la EH. [26] Alrededor de 36 a 39 repeticiones dan como resultado una forma de penetrancia reducida de la enfermedad, con un inicio mucho más tardío y una progresión más lenta de los síntomas. En algunos casos, el inicio puede ser tan tardío que los síntomas nunca se notan. [26] Con recuentos de repeticiones muy grandes (más de 60), el inicio de la EH puede ocurrir antes de los 20 años, lo que se conoce como EH juvenil. La EH juvenil suele ser de la variante de Westphal, que se caracteriza por lentitud de movimiento, rigidez y temblores. Esto representa aproximadamente el 7% de los operadores de HD. [36] [37]
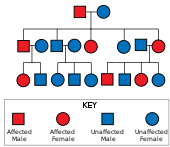
La enfermedad de Huntington tiene una herencia autosómica dominante , lo que significa que un individuo afectado típicamente hereda una copia del gen con una repetición de trinucleótido expandida (el alelo mutante ) de un padre afectado. [26] Dado que la penetrancia de la mutación es muy alta, aquellos que tengan una copia mutada del gen tendrán la enfermedad. En este tipo de patrón de herencia, cada descendiente de un individuo afectado tiene un riesgo del 50% de heredar el alelo mutante, por lo que se ve afectado por el trastorno (ver figura). Esta probabilidad es independiente del sexo. [38] Los genes dependientes del sexo o ligados al sexo son rasgos que se encuentran en los cromosomas X o Y. [39]
Las repeticiones CAG del trinucleótido superiores a 28 son inestables durante la replicación , y esta inestabilidad aumenta con el número de repeticiones presentes. [26] Esto generalmente conduce a nuevas expansiones a medida que pasan las generaciones ( mutaciones dinámicas ) en lugar de reproducir una copia exacta de la repetición del trinucleótido. [26] Esto hace que el número de repeticiones cambie en generaciones sucesivas, de modo que un padre no afectado con un número "intermedio" de repeticiones (28-35), o "penetrancia reducida" (36-40), puede transmitir una copia. del gen con un aumento en el número de repeticiones que produce HD completamente penetrante. [26] La edad más temprana de aparición y la mayor gravedad de la enfermedad en generaciones sucesivas debido al aumento en el número de repeticiones se conoce como anticipación genética . [1] La inestabilidad es mayor en la espermatogénesis que en la ovogénesis ; [26] los alelos heredados por la madre suelen tener una longitud de repetición similar, mientras que los heredados por el padre tienen una mayor probabilidad de aumentar en longitud. [26] [40] Rara vez la enfermedad de Huntington es causada por una nueva mutación , donde ninguno de los padres tiene más de 36 repeticiones CAG. [41]
En las raras situaciones en las que ambos padres tienen un gen de la EH expandido, el riesgo aumenta al 75%, y cuando cualquiera de los padres tiene dos copias expandidas, el riesgo es del 100% (todos los niños se verán afectados). Los individuos con ambos genes afectados son raros. Durante algún tiempo, se pensó que la EH era la única enfermedad en la que la posesión de un segundo gen mutado no afectaba los síntomas ni la progresión, [42] pero desde entonces se ha descubierto que puede afectar el fenotipo y la velocidad de progresión. [26] [43]
La proteína Huntingtina interactúa con más de 100 proteínas más y parece tener múltiples funciones. [44] El comportamiento de la proteína mutada (mHtt) no se comprende completamente, pero es tóxica para ciertos tipos de células, particularmente las células cerebrales . El daño temprano es más evidente en los ganglios basales subcorticales , inicialmente en el cuerpo estriado , pero a medida que avanza la enfermedad, otras áreas del cerebro también se ven afectadas, incluidas regiones de la corteza cerebral . Los primeros síntomas son atribuibles a funciones del cuerpo estriado y sus conexiones corticales, es decir, el control sobre el movimiento, el estado de ánimo y la función cognitiva superior. [26] La metilación del ADN también parece cambiar en la EH. [45]
Htt se expresa en todas las células, encontrándose las concentraciones más altas en el cerebro y los testículos , y cantidades moderadas en el hígado , el corazón y los pulmones . Sus funciones no están claras, pero interactúa con proteínas involucradas en la transcripción , la señalización celular y el transporte intracelular . [46] En animales genéticamente modificados para exhibir HD, se han identificado varias funciones de Htt. [47] En estos animales, Htt es importante para el desarrollo embrionario, ya que su ausencia está relacionada con la muerte embrionaria. Se cree que la caspasa , una enzima que desempeña un papel en la catálisis de la apoptosis , es activada por el gen mutado al dañar el sistema ubiquitina-proteasa. También actúa como agente antiapoptótico previniendo la muerte celular programada y controla la producción del factor neurotrófico derivado del cerebro , una proteína que protege las neuronas y regula su creación durante la neurogénesis . Htt también facilita el transporte vesicular sináptico y la transmisión sináptica , y controla la transcripción de genes neuronales. [47] Si aumenta la expresión de Htt, mejora la supervivencia de las células cerebrales y se reducen los efectos de mHtt, mientras que cuando se reduce la expresión de Htt, las características resultantes son más parecidas a las que se ven en presencia de mHtt. [47] En consecuencia, se cree que la enfermedad no es causada por una producción inadecuada de Htt, sino por una ganancia tóxica de función de mHtt en el cuerpo. [26]

La acción tóxica de mHtt puede manifestarse y producir la patología de la EH a través de múltiples cambios celulares. [48] [49] En su forma mutante (poliglutamina expandida), la proteína es más propensa a la escisión que crea fragmentos más cortos que contienen la expansión de poliglutamina. [48] Estos fragmentos de proteínas tienen propensión a sufrir plegamiento incorrecto y agregación, produciendo agregados fibrilares en los que las cadenas β de poliglutamina no nativa de múltiples proteínas se unen mediante enlaces de hidrógeno. [13] Estos agregados comparten la misma arquitectura fundamental de beta amiloide cruzada que se observa en otras enfermedades por depósito de proteínas . [50] Con el tiempo, los agregados se acumulan para formar cuerpos de inclusión dentro de las células, lo que en última instancia interfiere con la función neuronal. [13] [48] Se han encontrado cuerpos de inclusión tanto en el núcleo celular como en el citoplasma . [48] Los cuerpos de inclusión en las células del cerebro son uno de los primeros cambios patológicos, y algunos experimentos han encontrado que pueden ser tóxicos para la célula, pero otros experimentos han demostrado que pueden formarse como parte del mecanismo de defensa del cuerpo y ayudar. proteger las células. [48]
Se han identificado varias vías por las cuales mHtt puede provocar la muerte celular. Estos incluyen efectos sobre las proteínas chaperonas , que ayudan a plegar las proteínas y eliminar las mal plegadas; interacciones con caspasas , que desempeñan un papel en el proceso de eliminación de células ; los efectos tóxicos de la glutamina sobre las células nerviosas ; deterioro de la producción de energía dentro de las células; y efectos sobre la expresión de genes. [13] [51]
Se ha descubierto que la proteínahuntingtina mutante desempeña un papel clave en la disfunción mitocondrial . [46] El deterioro del transporte de electrones mitocondriales puede resultar en niveles más altos de estrés oxidativo y liberación de especies reactivas de oxígeno . [52]
Se sabe que la glutamina es excitotóxica cuando está presente en grandes cantidades, lo que puede causar daños a numerosas estructuras celulares. El exceso de glutamina no se encuentra en la EH, pero las interacciones de la proteínahuntingtina alterada con numerosas proteínas en las neuronas conducen a una mayor vulnerabilidad a la glutamina. Se cree que el aumento de la vulnerabilidad produce efectos excitotóxicos debido a los niveles normales de glutamina. [13]

Inicialmente, el daño al cerebro es regionalmente específico y el cuerpo estriado dorsal de los ganglios basales subcorticales se ve afectado principalmente, seguido más tarde por la afectación cortical en todas las áreas. [53] [54] Otras áreas de los ganglios basales afectadas incluyen la sustancia negra ; la afectación cortical incluye las capas corticales 3, 5 y 6 ; También es evidente la afectación del hipocampo , las células de Purkinje en el cerebelo , los núcleos tuberales laterales del hipotálamo y partes del tálamo . [26] Estas zonas se ven afectadas según su estructura y los tipos de neuronas que contienen, reduciéndose de tamaño a medida que van perdiendo células. [26] Las neuronas espinosas medias del cuerpo estriado son las más vulnerables, particularmente aquellas con proyecciones hacia el globo pálido externo , siendo menos afectadas las interneuronas y las células espinosas que se proyectan hacia el globo pálido interno . [26] [55] La EH también provoca un aumento anormal de los astrocitos y la activación de las células inmunitarias del cerebro, la microglia . [56]
Los ganglios basales desempeñan un papel clave en el control del movimiento y la conducta. Sus funciones no se comprenden del todo, pero las teorías proponen que forman parte del sistema ejecutivo cognitivo [28] y del circuito motor. [57] Los ganglios basales normalmente inhiben una gran cantidad de circuitos que generan movimientos específicos. Para iniciar un movimiento particular, la corteza cerebral envía una señal a los ganglios basales que hace que se libere la inhibición. El daño a los ganglios basales puede causar que la liberación o restablecimiento de las inhibiciones sea errática e incontrolada, lo que resulta en un comienzo incómodo del movimiento o en movimientos que se inician involuntariamente o en un movimiento que se detiene antes o más allá de su finalización prevista. El daño acumulado en esta área provoca los movimientos erráticos característicos asociados con la EH conocidos como corea, una discinesia . [57] Debido a la incapacidad de los ganglios basales para inhibir los movimientos, las personas afectadas inevitablemente experimentan una capacidad reducida para producir el habla y tragar alimentos y líquidos (disfagia). [58]
La proteína de unión a CREB (CBP), un corregulador transcripcional, es esencial para la función celular porque, como coactivadora de un número significativo de promotores, activa la transcripción de genes para las vías de supervivencia. [51] CBP contiene un dominio de acetiltransferasa al que se une HTT a través de su dominio que contiene poliglutamina. [59] También se ha descubierto que los cerebros sometidos a autopsias de personas que padecían la enfermedad de Huntington tenían cantidades increíblemente reducidas de CBP. [60] Además, cuando se sobreexpresa CBP, la muerte inducida por poliglutamina disminuye, lo que demuestra aún más que CBP desempeña un papel importante en la enfermedad de Huntington y en las neuronas en general. [51]
El diagnóstico de la aparición de la EH se puede realizar tras la aparición de síntomas físicos específicos de la enfermedad. [26] Las pruebas genéticas se pueden utilizar para confirmar un diagnóstico físico si no existen antecedentes familiares de EH. Incluso antes de la aparición de los síntomas, las pruebas genéticas pueden confirmar si un individuo o un embrión porta una copia ampliada de la repetición de trinucleótidos (CAG) en el gen HTT que causa la enfermedad. El asesoramiento genético está disponible para brindar asesoramiento y orientación durante todo el procedimiento de prueba y sobre las implicaciones de un diagnóstico confirmado. Estas implicaciones incluyen el impacto en la psicología, la carrera, las decisiones de planificación familiar, los parientes y las relaciones de un individuo. A pesar de la disponibilidad de pruebas presintomáticas, sólo el 5% de las personas con riesgo de heredar la EH eligen hacerlo. [26]

Un examen físico , a veces combinado con un examen psicológico , puede determinar si ha comenzado la aparición de la enfermedad. [26] Los movimientos excesivos e involuntarios de cualquier parte del cuerpo suelen ser el motivo de consulta médica. Si son abruptos y tienen un momento y una distribución aleatorios, sugieren un diagnóstico de EH. Los síntomas cognitivos o conductuales rara vez son los primeros síntomas diagnosticados; Por lo general, sólo se reconocen en retrospectiva o cuando se desarrollan más. Hasta qué punto ha progresado la enfermedad se puede medir utilizando la escala de calificación unificada de la enfermedad de Huntington, que proporciona un sistema de calificación general basado en evaluaciones motoras, conductuales, cognitivas y funcionales. [62] [63] Las imágenes médicas , como una tomografía computarizada o una resonancia magnética , pueden mostrar atrofia de los núcleos caudados en las primeras etapas de la enfermedad, como se ve en la ilustración de la derecha, pero estos cambios no son, por sí mismos, un diagnóstico de HD. La atrofia cerebral se puede observar en las etapas avanzadas de la enfermedad. Las técnicas de neuroimagen funcional , como la resonancia magnética funcional (fMRI) y la tomografía por emisión de positrones (PET), pueden mostrar cambios en la actividad cerebral antes de la aparición de los síntomas físicos, pero son herramientas experimentales y no se utilizan clínicamente. [26]
Debido a que la EH sigue un patrón de herencia autosómico dominante, existe una fuerte motivación para que las personas con riesgo de heredarla busquen un diagnóstico. La prueba genética para la EH consiste en un análisis de sangre, que cuenta el número de repeticiones CAG en cada uno de los alelos HTT . [64] Los límites se dan de la siguiente manera:
Hacerse la prueba antes de la aparición de los síntomas es un acontecimiento que cambia la vida y una decisión muy personal. [26] La principal razón dada para elegir la prueba de EH es ayudar en las decisiones profesionales y familiares. [26] Las pruebas predictivas para la enfermedad de Huntington han estado disponibles mediante análisis de vinculación (que requiere realizar pruebas a varios miembros de la familia) desde 1986 y mediante análisis de mutación directa desde 1993. [66] En ese momento, las encuestas indicaban que entre el 50% y el 70% de las personas en riesgo Las personas habrían estado interesadas en hacerse las pruebas, pero desde que se ofrecen pruebas predictivas, son muchas menos las que eligen hacérselas. [67] Más del 95% de las personas con riesgo de heredar la EH no se hacen la prueba, principalmente porque no tiene tratamiento. [26] Una cuestión clave es la ansiedad que experimenta un individuo al no saber si eventualmente desarrollará la EH, en comparación con el impacto de un resultado positivo. [26] Independientemente del resultado, los niveles de estrés son más bajos dos años después de la prueba, pero el riesgo de suicidio aumenta después de un resultado positivo. [26] Las personas que no han heredado el trastorno pueden sentir culpa de sobreviviente por los miembros de la familia afectados. [26] Otros factores que se tienen en cuenta al considerar las pruebas incluyen la posibilidad de discriminación y las implicaciones de un resultado positivo, lo que generalmente significa que un padre tiene un gen afectado y que los hermanos del individuo correrán el riesgo de heredarlo. [26] En un estudio, se encontró discriminación genética en el 46% de las personas en riesgo de padecer la enfermedad de Huntington. Ocurrió en tasas más altas dentro de las relaciones personales que en el seguro médico o las relaciones laborales. [68] El asesoramiento genético en la EH puede proporcionar información, asesoramiento y apoyo para la toma de decisiones inicial y luego, si se elige, durante todas las etapas del proceso de prueba. [69] Debido a las implicaciones de esta prueba, los pacientes que deseen someterse a la prueba deben completar tres sesiones de asesoramiento que proporcionen información sobre la enfermedad de Huntington. [70]
El asesoramiento y las directrices sobre el uso de pruebas genéticas para la EH se han convertido en modelos para otros trastornos genéticos, como la ataxia cerebelosa autosómica dominante . [26] [71] [72] Las pruebas presintomáticas para la EH también han influido en las pruebas para otras enfermedades con variantes genéticas, como la poliquistosis renal , la enfermedad de Alzheimer familiar y el cáncer de mama . [71] La Red Europea de Calidad de Genética Molecular ha publicado un plan anual de evaluación externa de la calidad de las pruebas genéticas moleculares para esta enfermedad y ha desarrollado directrices de mejores prácticas para las pruebas genéticas de la EH para ayudar en las pruebas y la notificación de los resultados. [73]
Los embriones producidos mediante fertilización in vitro pueden someterse a pruebas genéticas para detectar la EH mediante un diagnóstico genético previo a la implantación . Esta técnica, en la que se extraen una o dos células de un embrión de 4 a 8 células y luego se analiza para detectar la anomalía genética, se puede utilizar para garantizar que los embriones afectados con genes de la EH no se implanten, de modo que ninguna descendencia herede los genes. enfermedad. Algunas formas de diagnóstico genético preimplantacional (pruebas de no divulgación o de exclusión) permiten que las personas en riesgo tengan descendencia libre de EH sin revelar su propio genotipo parental, sin brindar información sobre si ellos mismos están destinados a desarrollar EH. En las pruebas de exclusión, el ADN del embrión se compara con el de los padres y abuelos para evitar la herencia de la región cromosómica que contiene el gen de la EH del abuelo afectado. En las pruebas de confidencialidad, sólo se reemplazan en el útero embriones libres de enfermedades, mientras que el genotipo de los padres y, por tanto, el riesgo de los padres de padecer EH nunca se revelan. [74] [75]
También es posible obtener un diagnóstico prenatal de un embrión o feto en el útero, utilizando material genético fetal adquirido mediante muestreo de vellosidades coriónicas . Se puede realizar una amniocentesis si el embarazo está más avanzado, entre 14 y 18 semanas. Este procedimiento analiza el líquido amniótico que rodea al bebé en busca de indicadores de la mutación de la EH. [76] Esto también puede combinarse con pruebas de exclusión para evitar la divulgación del genotipo parental. Las pruebas prenatales se pueden realizar cuando a los padres se les ha diagnosticado EH, cuando se les han realizado pruebas genéticas que muestran la expansión del gen HTT o cuando tienen un 50% de posibilidades de heredar la enfermedad. Se puede asesorar a los padres sobre sus opciones, que incluyen la interrupción del embarazo , y sobre las dificultades de un niño con el gen identificado. [77] [78]
Además, en embarazos de riesgo debidos a una pareja masculina afectada, se puede realizar un diagnóstico prenatal no invasivo analizando el ADN fetal libre de células en una muestra de sangre extraída de la madre (mediante venopunción ) entre las seis y 12 semanas de embarazo. [65] No tiene ningún riesgo de aborto espontáneo relacionado con el procedimiento. [sesenta y cinco]
Alrededor del 99% de los diagnósticos de EH basados en los síntomas típicos y los antecedentes familiares de la enfermedad se confirman mediante pruebas genéticas que tienen la repetición expandida de trinucleótidos que causa la EH. La mayoría de los restantes se denominan síndromes similares a HD (HDL) . [26] [79] Se desconoce la causa de la mayoría de las enfermedades HDL, pero aquellas con causas conocidas se deben a mutaciones en el gen de la proteína priónica (HDL1), el gen de la junctofilina 3 (HDL2), un gen desconocido de herencia recesiva (solo HDL3). encontrado en dos familias y poco comprendido), y el gen que codifica la proteína de unión a la caja TATA ( SCA17, a veces llamada HDL4 ). Otras enfermedades autosómicas dominantes que pueden diagnosticarse erróneamente como EH son la atrofia dentorubral-palidoluysiana y la neuroferritinopatía . Además, algunos trastornos autosómicos recesivos se parecen a los casos esporádicos de EH. Estos incluyen corea, acantocitosis y neurodegeneración asociada a pantotenato quinasa . Un trastorno ligado al cromosoma X de este tipo es el síndrome de McLeod . [79]
.pdf/page1-440px-Report_(IA_report00comm_6).pdf.jpg)
Hay tratamientos disponibles para reducir la gravedad de algunos síntomas de la EH. [80] Para muchos de estos tratamientos, la evidencia que confirma su efectividad en el tratamiento específico de los síntomas de la EH es incompleta. [26] [81] A medida que la enfermedad progresa, la capacidad de cuidar de uno mismo disminuye y el cuidado multidisciplinario cuidadosamente administrado se vuelve cada vez más necesario. [26] Aunque relativamente pocos estudios sobre ejercicios y terapias han demostrado ser útiles para rehabilitar los síntomas cognitivos de la EH, alguna evidencia muestra la utilidad de la fisioterapia , la terapia ocupacional y la terapia del habla . [26]
La pérdida de peso y los problemas para comer debido a la disfagia y otras descoordinaciones musculares son comunes, lo que hace que el manejo de la nutrición sea cada vez más importante a medida que avanza la enfermedad. [26] Se pueden agregar agentes espesantes a los líquidos, ya que los líquidos más espesos son más fáciles y seguros de tragar. [26] Recordarle a la persona afectada que coma lentamente y que se lleve trozos más pequeños de comida a la boca también puede ser útil para prevenir la asfixia. [26] Si comer se vuelve demasiado peligroso o incómodo, está disponible la opción de utilizar una gastrostomía endoscópica percutánea . Esta sonda de alimentación, conectada permanentemente a través del abdomen hasta el estómago , reduce el riesgo de aspirar alimentos y proporciona un mejor manejo nutricional. [82] Se recomienda la evaluación y el tratamiento por parte de logopedas con experiencia en la enfermedad de Huntington. [26]
Las personas con enfermedad de Huntington pueden consultar a un fisioterapeuta para buscar formas no invasivas y sin medicamentos de controlar los síntomas físicos. Los fisioterapeutas pueden implementar la evaluación y prevención del riesgo de caídas, así como ejercicios de fortalecimiento, estiramiento y cardiovasculares. Se pueden prescribir ayudas para caminar según corresponda. Los fisioterapeutas también prescriben ejercicios de respiración y técnicas de limpieza de las vías respiratorias cuando se desarrollan problemas respiratorios. [83] La Red Europea de EH ha elaborado directrices de consenso sobre fisioterapia en la enfermedad de Huntington. [83] Los objetivos de las intervenciones de rehabilitación temprana son la prevención de la pérdida de función. La participación en programas de rehabilitación durante la etapa temprana a media de la enfermedad puede ser beneficiosa ya que se traduce en el mantenimiento a largo plazo del rendimiento motor y funcional. La rehabilitación durante la etapa tardía tiene como objetivo compensar las pérdidas motoras y funcionales. [84] Para un manejo independiente a largo plazo, el terapeuta puede desarrollar programas de ejercicios en el hogar para las personas adecuadas. [85]
Además, un número cada vez mayor de personas con EH recurren a los cuidados paliativos , cuyo objetivo es mejorar la calidad de vida mediante el tratamiento de los síntomas y el estrés de una enfermedad grave, además de sus otros tratamientos. [86]
La tetrabenazina fue aprobada en 2000 para el tratamiento de la corea en la enfermedad de Huntington en la UE y en 2008 en Estados Unidos. [87] Aunque se habían utilizado otros medicamentos " fuera de etiqueta ", la tetrabenazina fue el primer tratamiento aprobado para la enfermedad de Huntington en los EE. UU. El compuesto se conoce desde la década de 1950. Una alternativa a la tetrabenazina es la amantadina , pero existe evidencia limitada de su seguridad y eficacia. [88]
Otros medicamentos que ayudan a reducir la corea incluyen los antipsicóticos y las benzodiazepinas . [22] La hipocinesia y la rigidez, especialmente en casos juveniles, se pueden tratar con fármacos antiparkinsonianos , y la hipercinesia mioclónica se puede tratar con ácido valproico . [22] La evidencia provisional ha encontrado que el ácido etil eicosapentaenoico mejora los síntomas motores al año. [89] En 2017, la FDA aprobó la deutetrabenazina , una forma más potente de medicamento de tetrabenazina para el tratamiento de la corea en la EH. [90] Esto se comercializa como Austedo.
Los síntomas psiquiátricos se pueden tratar con medicamentos similares a los utilizados en la población general. [26] [81] Los inhibidores selectivos de la recaptación de serotonina y la mirtazapina se han recomendado para la depresión, mientras que los antipsicóticos atípicos se recomiendan para la psicosis y los problemas de conducta. [81] Se recomienda la participación de un especialista neuropsiquiátrico, ya que las personas pueden requerir un tratamiento a largo plazo con múltiples medicamentos en combinación. [26]
Se han experimentado varias terapias alternativas en la medicina ayurvédica con productos de origen vegetal, aunque ninguna ha proporcionado buena evidencia de eficacia. Un estudio reciente demostró que la peptidasa de procesamiento del estroma (SPP), una enzima sintética que se encuentra en los cloroplastos de las plantas , impedía la agregación de proteínas asociadas con la enfermedad de Huntington. [91] Sin embargo, se necesitan estudios repetidos y validación clínica para confirmar su verdadero potencial terapéutico.
Las familias de las personas, y la sociedad en general, que han heredado o están en riesgo de heredar la EH tienen generaciones de experiencia con la EH, pero pueden desconocer los avances recientes en la comprensión de la enfermedad y la disponibilidad de pruebas genéticas. El asesoramiento genético beneficia a estas personas actualizando sus conocimientos, buscando disipar cualquier creencia infundada que puedan tener y ayudándoles a considerar sus opciones y planes futuros. El Programa de educación para pacientes con enfermedad de Huntington se creó para ayudar a educar a los familiares, cuidadores y personas diagnosticadas con la enfermedad de Huntington. [92] También se cubre información sobre opciones de planificación familiar, gestión de la atención y otras consideraciones. [26] [93]
La longitud de la repetición del trinucleótido representa el 60% de la variación de la edad de aparición de los síntomas y su tasa de progresión. Una repetición más prolongada da como resultado una edad de aparición más temprana y una progresión más rápida de los síntomas. [26] [94] Las personas con más de sesenta repeticiones a menudo desarrollan la enfermedad antes de los 20 años, mientras que aquellos con menos de 40 repeticiones pueden permanecer asintomáticos. [95] La variación restante se debe a factores ambientales y otros genes que influyen en el mecanismo de la enfermedad. [26]
La esperanza de vida en la EH es generalmente de 10 a 30 años después de la aparición de los síntomas visibles. [26] La enfermedad de Huntington juvenil tiene una esperanza de vida de 10 años después de la aparición de los síntomas visibles. La mayoría de las complicaciones potencialmente mortales se deben a la coordinación muscular y, en menor medida, a cambios de comportamiento inducidos por el deterioro de la función cognitiva. El mayor riesgo es la neumonía , que causa la muerte en un tercio de las personas con EH. A medida que se deteriora la capacidad de sincronizar movimientos, la dificultad para limpiar los pulmones y un mayor riesgo de aspirar alimentos o bebidas aumentan el riesgo de contraer neumonía . El segundo mayor riesgo es la enfermedad cardíaca , que causa casi una cuarta parte de las muertes de las personas con EH. [96] El suicidio es la tercera causa de muerte: el 7,3% de las personas con EH se quitan la vida y hasta el 27% intentan hacerlo. No está claro hasta qué punto los pensamientos suicidas están influenciados por síntomas conductuales, ya que significan un deseo de evitar las últimas etapas de la enfermedad. [97] [98] [99] El suicidio es el mayor riesgo de esta enfermedad antes de que se realice el diagnóstico y en las etapas intermedias de desarrollo durante toda la enfermedad. Otros riesgos asociados incluyen asfixia; debido a la incapacidad para tragar, lesiones físicas por caídas y desnutrición. [96] [20]
La aparición tardía de la enfermedad de Huntington significa que no suele afectar a la reproducción. [26] La prevalencia mundial de la EH es de 5 a 10 casos por cada 100.000 personas, [100] [101] pero varía mucho geográficamente como resultado del origen étnico, la migración local y los patrones de inmigración anteriores. [26] La prevalencia es similar para hombres y mujeres. La tasa de aparición es más alta en los pueblos de ascendencia europea occidental, con un promedio de alrededor de siete por cada 100.000 personas, y es más baja en el resto del mundo; por ejemplo, uno por cada millón de personas de ascendencia asiática y africana. Un estudio epidemiológico de 2013 sobre la prevalencia de la enfermedad de Huntington en el Reino Unido entre 1990 y 2010 encontró que la prevalencia promedio para el Reino Unido era de 12,3 por 100.000. [26] [102] Además, algunas áreas localizadas tienen una prevalencia mucho mayor que el promedio regional. [26] Una de las incidencias más altas se da en las poblaciones aisladas de la región del Lago de Maracaibo en Venezuela , donde la EH afecta hasta 700 por 100.000 personas. [26] [103] Otras áreas de alta localización se han encontrado en Tasmania y regiones específicas de Escocia , Gales y Suecia . [99] En algunos casos, el aumento de la prevalencia se debe a un efecto fundador local , una migración histórica de portadores a un área de aislamiento geográfico . [99] [104] Algunos de estos portadores se han rastreado cientos de años atrás mediante estudios genealógicos . [99] Los haplotipos genéticos también pueden dar pistas sobre las variaciones geográficas de la prevalencia. [99] [105] Islandia , por el contrario, tiene una prevalencia bastante baja de 1 por 100.000, a pesar de que los islandeses como pueblo descienden de las primeras tribus germánicas de Escandinavia que también dieron origen a los suecos ; todos los casos, a excepción de uno que se remonta a casi dos siglos atrás, derivaron de la descendencia de una pareja que vivió a principios del siglo XIX. [106] Finlandia también tiene una baja incidencia de sólo 2,2 por 100.000 personas. [107]
Hasta el descubrimiento de una prueba genética, las estadísticas sólo podían incluir el diagnóstico clínico basado en síntomas físicos y antecedentes familiares de EH, excluyendo a aquellos que murieron por otras causas antes del diagnóstico. Estos casos ahora pueden incluirse en las estadísticas; y, a medida que la prueba esté más disponible, es probable que aumenten las estimaciones de la prevalencia e incidencia del trastorno. [99] [108]

En siglos pasados, varios tipos de corea fueron denominados en ocasiones con nombres como danza de San Vito , sin entenderse bien su causa o tipo en cada caso.
La primera mención definitiva de la EH fue en una carta de Charles Oscar Waters (1816–1892), publicada en la primera edición de Practice of Medicine de Robley Dunglison en 1842. [110] Waters describió "una forma de corea, vulgarmente llamada magrums". ", incluidas descripciones precisas de la corea, su progresión y la fuerte herencia de la enfermedad. [111] En 1846, Charles Rollin Gorman (1817–1879) observó cómo parecía producirse una mayor prevalencia en regiones localizadas. [112] [111] Independientemente de Gorman y Waters, ambos estudiantes de Dunglison en el Jefferson Medical College de Filadelfia, [113] Johan Christian Lund (1830-1906) también produjo una descripción temprana en 1860. [111] Él específicamente observaron que en Setesdalen , un aislado valle montañoso de Noruega , la alta prevalencia de demencia se asociaba con un patrón de trastornos de movimientos espasmódicos hereditarios. [114]
La primera descripción detallada de la enfermedad fue realizada por George Huntington en 1872. Al examinar el historial médico combinado de varias generaciones de una familia que presentaban síntomas similares, se dio cuenta de que sus condiciones debían estar relacionadas; Presentó su definición detallada y precisa de la enfermedad en su primer artículo. Huntington describió el patrón exacto de herencia de la enfermedad autosómica dominante años antes del redescubrimiento por parte de los científicos de la herencia mendeliana .
De su carácter hereditario. Cuando uno o ambos padres han mostrado manifestaciones de la enfermedad... uno o más de los descendientes casi invariablemente padecen la enfermedad... Pero si por casualidad estos hijos pasan por la vida sin ella, el hilo se rompe y los nietos y los bisnietos de los agitadores originales pueden estar seguros de que están libres de la enfermedad. [109] [115]
Sir William Osler estaba interesado en el trastorno y la corea en general, y quedó impresionado con el artículo de Huntington, afirmando: "En la historia de la medicina, hay pocos casos en los que una enfermedad haya sido descrita con mayor precisión, gráfica o brevemente". [116] [111] [117] El continuo interés de Osler en la EH, combinado con su influencia en el campo de la medicina, ayudó a difundir rápidamente la conciencia y el conocimiento sobre el trastorno en toda la comunidad médica. [111] Científicos de Europa, entre ellos Louis Théophile Joseph Landouzy , Désiré-Magloire Bourneville , Camillo Golgi y Joseph Jules Dejerine , mostraron un gran interés, y hasta finales de siglo, gran parte de la investigación sobre la EH era de origen europeo. [111] A finales del siglo XIX, se habían publicado investigaciones e informes sobre la EH en muchos países y la enfermedad fue reconocida como una afección mundial. [111]
Durante el redescubrimiento de la herencia mendeliana a principios del siglo XX, la EH se utilizó tentativamente como ejemplo de herencia autosómica dominante. [111] El biólogo inglés William Bateson utilizó los pedigríes de las familias afectadas para establecer que la EH tenía un patrón de herencia autosómico dominante. [118] [113] El fuerte patrón de herencia llevó a varios investigadores, incluido Smith Ely Jelliffe , a intentar rastrear y conectar a miembros de la familia de estudios anteriores. [111] Jelliffe recopiló información de toda Nueva York y publicó varios artículos sobre la genealogía de la EH en Nueva Inglaterra . [119] La investigación de Jelliffe despertó el interés de su amigo de la universidad, Charles Davenport , quien encargó a Elizabeth Muncey que produjera el primer estudio de campo en la costa este de los Estados Unidos sobre familias con EH y construyera sus pedigríes. [120] Davenport utilizó esta información para documentar la edad variable de aparición y el rango de síntomas de la EH; Afirmó que la mayoría de los casos de EH en los EE. UU. se remontan a un puñado de personas. [120] Esta investigación fue embellecida aún más en 1932 por PR Vessie, quien popularizó la idea de que tres hermanos que abandonaron Inglaterra en 1630 con destino a Boston fueron los progenitores de la EH en los EE. UU. [121] La afirmación de que se habían establecido los primeros progenitores y el sesgo eugenésico del trabajo de Muncey, Davenport y Vessie contribuyeron a malentendidos y prejuicios sobre la EH. [113] Muncey y Davenport también popularizaron la idea de que en el pasado, se podía pensar que algunas personas con EH estaban poseídas por espíritus o víctimas de brujería , y en ocasiones eran rechazadas o exiliadas por la sociedad. [122] [123] Esta idea no ha sido probada. Los investigadores han encontrado evidencia contraria; por ejemplo, la comunidad de la familia estudiada por George Huntington acogió abiertamente a quienes presentaban síntomas de EH. [113] [122]
La búsqueda de la causa de esta afección se intensificó considerablemente en 1968, cuando la Fundación de Enfermedades Hereditarias (HDF) fue creada por Milton Wexler , un psicoanalista radicado en Los Ángeles , California , cuya esposa Leonore Sabin había sido diagnosticada a principios de ese año con la enfermedad de Huntington. . [124] Los tres hermanos de la esposa de Wexler también padecían esta enfermedad.
La fundación participó en el reclutamiento de más de 100 científicos en el Proyecto Colaborativo Estados Unidos-Venezuela sobre la Enfermedad de Huntington, que durante un período de 10 años desde 1979, trabajó para localizar la causa genética. [125] Esto se logró en 1983 cuando se ubicó aproximadamente un gen causal, [104] y en 1993, el gen se ubicó precisamente en el cromosoma 4 (4p16.3). [126] El estudio se había centrado en las poblaciones de dos aldeas venezolanas aisladas , Barranquitas y Lagunetas, donde había una prevalencia inusualmente alta de la EH, e involucró a más de 18.000 personas, en su mayoría de una sola familia extendida, y dio como resultado que la EH fuera la primera "Locus de enfermedad autosómica encontrado mediante análisis de ligamiento genético" . [126] [127] Entre otras innovaciones, el proyecto desarrolló métodos de marcado de ADN que fueron un paso importante para hacer posible el Proyecto Genoma Humano . [125]
Al mismo tiempo, se hicieron descubrimientos clave sobre los mecanismos del trastorno, incluidos los hallazgos del grupo de investigación de Anita Harding sobre los efectos de la longitud del gen. [128]
La modelización de la enfermedad en varios tipos de animales, como el ratón transgénico desarrollado en 1996, permitió realizar experimentos a mayor escala. Como estos animales tienen metabolismos más rápidos y una esperanza de vida mucho más corta que los humanos, los resultados de los experimentos se reciben antes, lo que acelera la investigación. El descubrimiento en 1997 de que los fragmentos de mHtt estaban mal plegados condujo al descubrimiento de las inclusiones nucleares que provocan. Estos avances han llevado a una investigación cada vez más extensa sobre las proteínas involucradas en la enfermedad, posibles tratamientos farmacológicos, métodos de atención y el gen mismo. [111] [129]
Las redes de atención y apoyo que se habían desarrollado en Venezuela y Colombia durante los proyectos de investigación allí entre los años 1970 y 2000 fueron finalmente erosionadas por diversas fuerzas, como la crisis actual en Venezuela y la muerte de un investigador principal en Colombia (Jorge Daza Barriga). ). [130] Los médicos están trabajando para reavivar estas redes porque las personas que han contribuido a la ciencia de la enfermedad de Huntington al participar en estos estudios merecen una atención de seguimiento adecuada; Las sociedades de otras partes del mundo que se benefician de los avances científicos así logrados deben al menos esa misma cantidad a quienes participaron en la investigación. [130]
La afección se llamaba antiguamente corea de Huntington, pero este término ha sido sustituido por enfermedad de Huntington porque no todos los pacientes desarrollan corea y debido a la importancia de los problemas cognitivos y de conducta. [131]
Las pruebas genéticas para la enfermedad de Huntington han planteado varias cuestiones éticas. Las cuestiones relativas a las pruebas genéticas incluyen definir qué tan maduro debe ser un individuo antes de ser considerado elegible para las pruebas, garantizar la confidencialidad de los resultados y si se debe permitir a las empresas utilizar los resultados de las pruebas para tomar decisiones sobre empleo, seguros de vida u otros asuntos financieros. Hubo controversia cuando Charles Davenport propuso en 1910 que se utilizara la esterilización obligatoria y el control de la inmigración para personas con ciertas enfermedades, incluida la EH, como parte del movimiento eugenésico . [132] La fertilización in vitro tiene algunos problemas con respecto al uso de embriones. Algunas investigaciones sobre la EH tienen problemas éticos debido al uso de pruebas con animales y células madre embrionarias . [133] [134]
El desarrollo de una prueba de diagnóstico precisa para la enfermedad de Huntington ha generado preocupaciones sociales, legales y éticas sobre el acceso y el uso de los resultados de una persona. [135] [136] Muchas pautas y procedimientos de prueba tienen procedimientos estrictos de divulgación y confidencialidad para permitir que las personas decidan cuándo y cómo recibir sus resultados y también a quién se ponen a disposición los resultados. [26] Las compañías de seguros y las empresas se enfrentan a la cuestión de si deben utilizar los resultados de las pruebas genéticas al evaluar a un individuo, por ejemplo para un seguro de vida o un empleo. Las compañías de seguros del Reino Unido acordaron con el Departamento de Salud y Asistencia Social que hasta 2017 los clientes no necesitarían revelarles pruebas genéticas predictivas, pero este acuerdo excluía explícitamente la prueba aprobada por el gobierno para la enfermedad de Huntington al redactar pólizas con un valor superior a £ 500 000. . [137] [138] Al igual que con otras afecciones genéticas intratables y de aparición tardía, es éticamente cuestionable realizar pruebas presintomáticas en un niño o adolescente, ya que no habría ningún beneficio médico para ese individuo. Existe consenso en evaluar sólo a personas que se consideran cognitivamente maduras, aunque existe un contraargumento de que los padres tienen derecho a tomar la decisión en nombre de sus hijos. Ante la falta de un tratamiento eficaz, en la mayoría de los casos se considera poco ético realizar pruebas a una persona menor de edad que no se considera competente . [49] [139] [140]
Existen preocupaciones éticas relacionadas con las pruebas genéticas prenatales o el diagnóstico genético previo a la implantación para garantizar que un niño no nazca con una enfermedad determinada. [141] Por ejemplo, las pruebas prenatales plantean la cuestión del aborto selectivo, una opción considerada inaceptable por algunos. [141] Como es una enfermedad dominante, existen dificultades en situaciones en las que un padre no quiere conocer su propio diagnóstico. Esto requeriría que partes del proceso se mantuvieran en secreto para los padres. [141]

En 1968, después de experimentar la EH en la familia de su esposa, el Dr. Milton Wexler se inspiró para iniciar la Fundación de Enfermedades Hereditarias (HDF), con el objetivo de curar enfermedades genéticas coordinando y apoyando la investigación. [17] La fundación y la hija de Wexler, Nancy Wexler , fueron partes clave del equipo de investigación en Venezuela que descubrió el gen de la EH. [17]
Aproximadamente al mismo tiempo que se formó la HDF, Marjorie Guthrie ayudó a fundar el comité para combatir la enfermedad de Huntington (ahora Sociedad Estadounidense de la Enfermedad de Huntington ), después de que su esposo, el cantautor folk Woody Guthrie muriera por complicaciones de la EH. [18]
Desde entonces, se han formado organizaciones de apoyo e investigación en muchos países del mundo y han ayudado a aumentar la conciencia pública sobre la EH. Varios de ellos colaboran en organizaciones coordinadoras, como la Asociación Internacional Huntington y la red europea HD. [142] Muchas organizaciones de apoyo celebran un evento anual de concientización sobre la EH, algunos de los cuales han sido respaldados por sus respectivos gobiernos. Por ejemplo, el Senado de los Estados Unidos designa el 6 de junio como "Día Nacional de Concientización sobre la Enfermedad de Huntington" . [143] Existen muchas organizaciones para apoyar e informar a los afectados por la EH, incluida la Asociación de Enfermedad de Huntington en el Reino Unido. El mayor financiador de la investigación lo proporciona la Fundación Iniciativa para la Enfermedad de Cure Huntington (CHDI). [144]
La investigación sobre el mecanismo de la EH se centra en identificar el funcionamiento de Htt, en qué se diferencia o interfiere mHtt con él y la patología cerebral que produce la enfermedad. [145] La investigación se lleva a cabo utilizando métodos in vitro , animales genéticamente modificados (también llamados modelos animales transgénicos ) y voluntarios humanos. Los modelos animales son fundamentales para comprender los mecanismos fundamentales que causan la enfermedad y para respaldar las primeras etapas del desarrollo de fármacos . [129] La identificación del gen causante ha permitido el desarrollo de muchos organismos genéticamente modificados, incluidos nematodos (gusanos redondos), moscas de la fruta Drosophila y mamíferos genéticamente modificados , incluidos ratones, ratas, ovejas, cerdos y monos, que expresan Huntingtina mutante y desarrollan neurodegeneración progresiva. y síntomas similares a los de la EH. [129]
Se están realizando investigaciones utilizando muchos enfoques para prevenir la enfermedad de Huntington o retardar su progresión. [145] Las estrategias de modificación de la enfermedad se pueden agrupar ampliamente en tres categorías: reducir el nivel de la proteínahuntingtina mutante (incluido el empalme y el silenciamiento de genes ); enfoques destinados a mejorar la supervivencia neuronal reduciendo el daño causado por la proteína a vías y mecanismos celulares específicos (incluida la homeostasis de las proteínas y la inhibición de la histona desacetilasa ); y estrategias para reemplazar las neuronas perdidas. Además, se están desarrollando nuevas terapias para mejorar el funcionamiento del cerebro; estos buscan producir terapias sintomáticas en lugar de terapias modificadoras de la enfermedad e incluyen inhibidores de la fosfodiesterasa . [146] [147]
La Fundación CHDI financia muchas iniciativas de investigación y proporciona numerosas publicaciones. [148] La fundación CHDI es el mayor financiador de la investigación de la enfermedad de Huntington a nivel mundial y tiene como objetivo encontrar y desarrollar medicamentos que desaceleren la progresión de la EH. [144] [149] CHDI se conocía anteriormente como High Q Foundation. En 2006, gastó 50 millones de dólares en la investigación de la enfermedad de Huntington. [144] CHDI colabora con muchos laboratorios académicos y comerciales a nivel mundial y participa en la supervisión y gestión de proyectos de investigación, así como en la financiación. [150]
El silenciamiento genético tiene como objetivo reducir la producción de la proteína mutante, ya que la EH es causada por un único gen dominante que codifica una proteína tóxica. Los experimentos de silenciamiento genético en modelos de ratón han demostrado que cuando se reduce la expresión de mHtt, los síntomas mejoran. [151] La seguridad de la interferencia de ARN y los métodos de silenciamiento génico con oligonucleótidos específicos de alelo (ASO) se ha demostrado en ratones y en el cerebro de macaco de primate más grande. [152] [153] El silenciamiento específico de alelo intenta silenciar el htt mutante mientras deja intacto el Htt de tipo salvaje. Una forma de lograr esto es identificar polimorfismos presentes en un solo alelo y producir fármacos silenciadores de genes que se dirijan a los polimorfismos solo en el alelo mutante. [154] El primer ensayo de silenciamiento genético en humanos con EH comenzó en 2015, probando la seguridad de IONIS-HTTRx, producido por Ionis Pharmaceuticals y dirigido por el Instituto de Neurología de la UCL . [155] [156] La Huntingtina mutante se detectó y cuantificó por primera vez en el líquido cefalorraquídeo de portadores de mutaciones de la enfermedad de Huntington en 2015 mediante un novedoso inmunoensayo de "recuento de una sola molécula" , [157] que proporciona una forma directa de evaluar si la Huntingtina- Los tratamientos reductores están consiguiendo el efecto deseado. [158] [159] Un ensayo de fase 3 de este compuesto, rebautizado como tominersen y patrocinado por Roche Pharmaceuticals , comenzó en 2019, pero se detuvo en 2021 después de que la junta de monitoreo de seguridad concluyó que el equilibrio riesgo-beneficio era desfavorable. [160] En 2019 comenzó un ensayo de terapia génica reductora de la Huntingtina realizado por Uniqure, y se han anunciado varios ensayos de compuestos moduladores del empalme reductores de la Huntingtina administrados por vía oral. [161] Se están estudiando técnicas de empalme de genes para intentar reparar un genoma con el gen erróneo que causa la EH, utilizando herramientas como CRISPR/Cas9 . [147]
Otra estrategia para reducir el nivel de Huntingtina mutante es aumentar la velocidad a la que las células pueden eliminarla. [162] Como mHtt (y muchos otros agregados de proteínas ) se degradan mediante la autofagia , aumentar la tasa de autofagia tiene el potencial de reducir los niveles de mHtt y, por lo tanto, mejorar la enfermedad. [163] Se han probado inductores farmacológicos y genéticos de la autofagia en una variedad de modelos de la enfermedad de Huntington; Se ha demostrado que muchos reducen los niveles de mHtt y disminuyen la toxicidad. [162]
Entre los enfoques destinados a mejorar la supervivencia celular en presencia de Huntingtina mutante se encuentran la corrección de la regulación transcripcional utilizando inhibidores de la histona desacetilasa , la modulación de la agregación de Huntingtina, la mejora del metabolismo y la función mitocondrial y la restauración de la función de las sinapsis . [151]
La terapia con células madre se utiliza para reemplazar neuronas dañadas mediante el trasplante de células madre en regiones afectadas del cerebro. Los experimentos en modelos animales (sólo ratas y ratones) han dado resultados positivos. [164]
Cualquiera que sea su potencial terapéutico futuro, las células madre son ya una herramienta valiosa para estudiar la enfermedad de Huntington en el laboratorio. [165]
La ferroptosis es una forma de muerte celular regulada caracterizada por la acumulación de hidroperóxidos lipídicos dependiente del hierro hasta niveles letales. La ferroptosis mediada por ALOX5 actúa como una vía de muerte celular ante el estrés oxidativo en la enfermedad de Huntington. [166] Los inhibidores de la ferroptosis tienen un efecto protector en modelos de trastornos cerebrales degenerativos, incluidas las enfermedades de Parkinson, Huntington y Alzheimer. [166]
En 2020, había 197 ensayos clínicos relacionados con diversas terapias y biomarcadores para la enfermedad de Huntington listados como en curso, en proceso de reclutamiento o recién completados. [167] Los compuestos probados que no han logrado prevenir o retardar la progresión de la enfermedad de Huntington incluyen remacemida , coenzima Q10 , riluzol , creatina , minociclina , etil-EPA , fenilbutirato y dimebon . [168]