
En química , un alcohol (de la palabra árabe al-kuḥl , الكحل ) es un tipo de compuesto orgánico que lleva al menos un grupo funcional hidroxilo ( −OH ) unido a un átomo de carbono saturado . [2] [3] Los alcoholes varían desde los simples, como el metanol y el etanol , hasta los complejos, como los azúcares y el colesterol . La presencia de un grupo OH modifica fuertemente las propiedades de los hidrocarburos, confiriendo propiedades hidrófilas (amantes del agua). El grupo OH proporciona un sitio en el que pueden ocurrir muchas reacciones.
La naturaleza inflamable de las exhalaciones del vino ya era conocida por antiguos filósofos naturales como Aristóteles (384-322 a. C.), Teofrasto ( c. 371-287 a. C.) y Plinio el Viejo (23/24-79 d. C.). [4] Sin embargo, esto no condujo inmediatamente al aislamiento del alcohol, incluso a pesar del desarrollo de técnicas de destilación más avanzadas en el Egipto romano de los siglos II y III . [5] Un reconocimiento importante, encontrado por primera vez en uno de los escritos atribuidos a Jābir ibn Ḥayyān (siglo IX d. C.), fue que al agregar sal al vino hirviendo, lo que aumenta la volatilidad relativa del vino , se puede mejorar la inflamabilidad de los vapores resultantes. [6] La destilación del vino está atestiguada en obras árabes atribuidas a al-Kindī ( c. 801-873 d. C.) y a al-Fārābī ( c. 872-950 ), y en el libro 28 del Kitāb al-Taṣrīf de al-Zahrāwī (latín: Abulcasis, 936-1013) (posteriormente traducido al latín como Liber servatoris ). [7] En el siglo XII, las recetas para la producción de aqua ardens ("agua ardiente", es decir, alcohol) mediante la destilación del vino con sal comenzaron a aparecer en varias obras latinas y, a fines del siglo XIII, se había convertido en una sustancia ampliamente conocida entre los químicos de Europa occidental. [8]
Las obras de Taddeo Alderotti (1223-1296) describen un método para concentrar alcohol que implicaba una destilación fraccionada repetida a través de un alambique enfriado por agua, con el que se podía obtener una pureza de alcohol del 90%. [9] Las propiedades medicinales del etanol fueron estudiadas por Arnaldo de Villanova (1240-1311 d. C.) y Juan de Rupescissa ( c. 1310-1366 ), el último de los cuales lo consideraba una sustancia que preservaba la vida y podía prevenir todas las enfermedades (el aqua vitae o "agua de vida", también llamada por Juan la quintaesencia del vino). [10]
La palabra "alcohol" deriva del árabe kohl ( árabe : الكحل , romanizado : al-kuḥl ), un polvo utilizado como delineador de ojos. [11] La primera parte de la palabra ( al- ) es el artículo definido árabe , equivalente a the en español. La segunda parte de la palabra ( kuḥl ) tiene varios antecedentes en lenguas semíticas , derivando en última instancia del acadio 𒎎𒋆𒁉𒍣𒁕 ( guḫlum ), que significa estibina o antimonio . [12]
Al igual que sus antecesores en árabe y en lenguas más antiguas, el término alcohol se utilizó originalmente para el polvo muy fino producido por la sublimación del mineral natural estibina para formar trisulfuro de antimonio Sb2S3 . Se consideraba que era la esencia o "espíritu" de este mineral. Se utilizaba como antiséptico , delineador de ojos y cosmético . Más tarde, el significado de alcohol se extendió a las sustancias destiladas en general, y luego se redujo nuevamente a etanol, cuando "bebidas espirituosas" era sinónimo de licor fuerte . [13]
Tanto Paracelso como Libavio utilizaron el término alcohol para designar un polvo fino; el último se refería a un alcohol derivado del antimonio. Al mismo tiempo, Paracelso utiliza la palabra para designar un líquido volátil; alcool o alcool vini aparece a menudo en sus escritos. [14]
Bartholomew Traheron , en su traducción de 1543 de Juan de Vigo , introduce la palabra como un término usado por autores "bárbaros" para referirse a "polvo fino". Vigo escribió: "los autores bárbaros usan alcohol, o (como lo encuentro escrito a veces) alcofoll, para referirse a la pólvora más fina". [15]
El Lexicon Chymicum de 1657 , de William Johnson, glosa la palabra como "antimonium sive stibium". [16] Por extensión, la palabra llegó a referirse a cualquier fluido obtenido por destilación, incluyendo "alcohol de vino", la esencia destilada del vino. Libavius en Alchymia (1594) se refiere a " vini alcohol vel vinum alcalisatum ". Johnson (1657) glosa alcohol vini como " quando omnis superfluitas vini a vino separatur, ita ut accensum ardeat donec totum consumatur, nihilque fæcum aut phlegmatis in fundo remaneat ". El significado de la palabra se restringió a "espíritu de vino" (la sustancia química conocida hoy como etanol ) en el siglo XVIII y se extendió a la clase de sustancias denominadas "alcoholes" en la química moderna después de 1850. [15]
El término etanol fue inventado en 1892, mezclando " etano " con la terminación "-ol" de "alcohol", que se generalizó como una libfija . [17]
El término alcohol se refería originalmente al alcohol primario etanol (alcohol etílico), que se utiliza como droga y es el principal alcohol presente en las bebidas alcohólicas .

El sufijo -ol aparece en el nombre químico de la Unión Internacional de Química Pura y Aplicada (IUPAC) de todas las sustancias en las que el grupo hidroxilo es el grupo funcional con mayor prioridad. Cuando en el compuesto hay un grupo con mayor prioridad, se utiliza el prefijo hidroxi- en su nombre IUPAC. El sufijo -ol en nombres que no son IUPAC (como paracetamol o colesterol ) también suele indicar que la sustancia es un alcohol. Sin embargo, algunos compuestos que contienen grupos funcionales hidroxilo tienen nombres triviales que no incluyen el sufijo -ol o el prefijo hidroxi- , por ejemplo, los azúcares glucosa y sacarosa .
La nomenclatura IUPAC se utiliza en publicaciones científicas y en escritos donde la identificación precisa de la sustancia es importante. Al nombrar alcoholes simples, el nombre de la cadena de alcano pierde la e terminal y agrega el sufijo -ol , p. ej ., como en "etanol" del nombre de la cadena de alcano " etano ". [18] Cuando es necesario, la posición del grupo hidroxilo se indica mediante un número entre el nombre del alcano y el -ol : propan-1-ol para CH 3 CH 2 CH 2 OH , propan-2-ol para CH 3 CH(OH)CH 3 . Si está presente un grupo de mayor prioridad (como un aldehído , una cetona o un ácido carboxílico ), entonces se utiliza el prefijo hidroxi- , [18] p. ej., como en 1-hidroxi-2-propanona ( CH 3 C(O)CH 2 OH ). [19] Los compuestos que tienen más de un grupo hidroxi se denominan polioles . Se nombran utilizando los sufijos -diol, -triol, etc., siguiendo una lista de los números de posición de los grupos hidroxilo, como en propano-1,2-diol para CH 3 CH(OH)CH 2 OH (propilenglicol).
En los casos en que el grupo hidroxi está unido a un carbono sp 2 en un anillo aromático , la molécula se clasifica por separado como fenol y se nombra utilizando las reglas de la IUPAC para nombrar fenoles. [20] Los fenoles tienen propiedades distintas y no se clasifican como alcoholes.
En otros contextos menos formales, a menudo se hace referencia a un alcohol con el nombre del grupo alquilo correspondiente seguido de la palabra "alcohol", por ejemplo, alcohol metílico , alcohol etílico . El alcohol propílico puede ser alcohol n -propílico o alcohol isopropílico , dependiendo de si el grupo hidroxilo está unido al carbono final o medio de la cadena de propano lineal . Como se describe en la denominación sistemática, si otro grupo en la molécula tiene prioridad, la fracción de alcohol a menudo se indica utilizando el prefijo "hidroxi-". [21]
En la nomenclatura arcaica, los alcoholes pueden denominarse derivados del metanol utilizando "-carbinol" como terminación. Por ejemplo, (CH 3 ) 3 COH puede denominarse trimetilcarbinol .
Los alcoholes se clasifican en primarios, secundarios ( sec- , s- ) y terciarios ( tert- , t- ), según el número de átomos de carbono conectados al átomo de carbono que lleva el grupo funcional hidroxilo . Las abreviaturas numéricas respectivas 1°, 2° y 3° se utilizan a veces en entornos informales. [22] Los alcoholes primarios tienen fórmulas generales RCH 2 OH . El alcohol primario más simple es el metanol ( CH 3 OH ), para el cual R = H, y el siguiente es el etanol, para el cual R = CH 3 , el grupo metilo . Los alcoholes secundarios son aquellos de la forma RR'CHOH, el más simple de los cuales es el 2-propanol ( R = R' = CH 3 ). Para los alcoholes terciarios, la forma general es RR'R"COH. El ejemplo más simple es el terc -butanol (2-metilpropan-2-ol), para el cual cada uno de R, R' y R" es CH3 . En estas abreviaturas, R, R' y R" representan sustituyentes , grupos alquilo u otros grupos unidos, generalmente orgánicos.
Los alcoholes tienen una larga historia de usos múltiples. En el caso de los monoalcoholes simples, que son el tema central de este artículo, los alcoholes industriales más importantes son los siguientes: [24]
El metanol es el alcohol industrial más común, con una producción de alrededor de 12 millones de toneladas al año en 1980. La capacidad combinada de los demás alcoholes es aproximadamente la misma y se distribuye de manera más o menos equitativa. [24]
En cuanto a la toxicidad aguda, los alcoholes simples tienen una toxicidad aguda baja . Se toleran dosis de varios mililitros. En el caso de los pentanoles , hexanoles , octanoles y alcoholes más largos, la DL50 oscila entre 2 y 5 g/kg (ratas, vía oral). El etanol es menos tóxico en estado agudo. [25] Todos los alcoholes son irritantes leves de la piel. [24]
El metanol y el etilenglicol son más tóxicos que otros alcoholes simples. Su metabolismo se ve afectado por la presencia de etanol, que tiene una mayor afinidad por la alcohol deshidrogenasa hepática . De esta manera, el metanol se excretará intacto en la orina. [26] [27] [28]
En general, el grupo hidroxilo hace que los alcoholes sean polares . Estos grupos pueden formar enlaces de hidrógeno entre sí y con la mayoría de los demás compuestos. Debido a la presencia del OH polar, los alcoholes son más solubles en agua que los hidrocarburos simples. El metanol, el etanol y el propanol son miscibles en agua. El 1-butanol , con una cadena de cuatro carbonos, es moderadamente soluble.
Debido a los enlaces de hidrógeno , los alcoholes tienden a tener puntos de ebullición más altos que los hidrocarburos y éteres comparables . El punto de ebullición del alcohol etanol es de 78,29 °C, en comparación con los 69 °C del hidrocarburo hexano y los 34,6 °C del éter dietílico .
Los alcoholes se encuentran ampliamente presentes en la naturaleza, como derivados de la glucosa , como la celulosa y la hemicelulosa , y en los fenoles y sus derivados, como la lignina . [29] A partir de la biomasa , se producen comercialmente 180 mil millones de toneladas/año de carbohidratos complejos (polímeros de azúcar) (a partir de 2014). [30] Muchos otros alcoholes son omnipresentes en los organismos, como se manifiesta en otros azúcares como la fructosa y la sacarosa , en polioles como el glicerol y en algunos aminoácidos como la serina . Los alcoholes simples como el metanol, el etanol y el propanol se encuentran en cantidades modestas en la naturaleza y se sintetizan industrialmente en grandes cantidades para su uso como precursores químicos, combustibles y disolventes.
Muchos alcoholes se producen por hidroxilación , es decir, la instalación de un grupo hidroxi mediante oxígeno o un oxidante relacionado. La hidroxilación es el medio por el cual el cuerpo procesa muchos venenos , convirtiendo compuestos lipofílicos en derivados hidrofílicos que se excretan más fácilmente. Las enzimas llamadas hidroxilasas y oxidasas facilitan estas conversiones.
Muchos alcoholes industriales, como el ciclohexanol para la producción de nailon , se producen por hidroxilación.
En el proceso Ziegler , se producen alcoholes lineales a partir de etileno y trietilaluminio, seguido de oxidación e hidrólisis. [24] Se muestra una síntesis idealizada de 1-octanol :
El proceso genera una gama de alcoholes que se separan por destilación .
Muchos alcoholes superiores se producen por hidroformilación de alquenos seguida de hidrogenación. Cuando se aplica a un alqueno terminal , como es habitual, se obtiene típicamente un alcohol lineal: [24]
Estos procesos producen alcoholes grasos , que son útiles para detergentes.
Algunos alcoholes de bajo peso molecular de importancia industrial se producen mediante la adición de agua a los alquenos. El etanol, el isopropanol, el 2-butanol y el terc -butanol se producen mediante este método general. Se emplean dos implementaciones, los métodos directo e indirecto. El método directo evita la formación de intermediarios estables, típicamente utilizando catalizadores ácidos. En el método indirecto, el alqueno se convierte en el éster de sulfato , que posteriormente se hidroliza. La hidratación directa utiliza etileno ( hidratación de etileno ) [31] u otros alquenos del craqueo de fracciones de petróleo crudo destilado .
La hidratación también se utiliza industrialmente para producir el diol etilenglicol a partir de óxido de etileno .
El etanol se obtiene por fermentación de la glucosa (que a menudo se obtiene del almidón ) en presencia de levadura. El dióxido de carbono se cogenera. Al igual que el etanol, el butanol se puede producir mediante procesos de fermentación. Se sabe que la levadura Saccharomyces produce estos alcoholes superiores a temperaturas superiores a 75 °F (24 °C). La bacteria Clostridium acetobutylicum puede alimentarse de celulosa (también un alcohol) para producir butanol a escala industrial. [32]
Los haluros de alquilo primarios reaccionan con NaOH o KOH acuosos para dar alcoholes en sustitución alifática nucleófila . Los haluros de alquilo secundarios y especialmente terciarios darán en cambio el producto de eliminación (alqueno). Los reactivos de Grignard reaccionan con grupos carbonilo para dar alcoholes secundarios y terciarios. Reacciones relacionadas son la reacción de Barbier y la reacción de Nozaki-Hiyama .
Los aldehídos o cetonas se reducen con borohidruro de sodio o hidruro de litio y aluminio (después de un tratamiento ácido). Otra reducción que utiliza isopropóxido de aluminio es la reducción de Meerwein-Ponndorf-Verley . La hidrogenación asimétrica de Noyori es la reducción asimétrica de β-cetoésteres.
Los alquenos participan en una reacción de hidratación catalizada por ácido utilizando ácido sulfúrico concentrado como catalizador que da lugar, por lo general, a alcoholes secundarios o terciarios. La formación de un alcohol secundario mediante la reducción e hidratación de un alqueno se muestra a continuación:
La hidroboración-oxidación y la oximercuración-reducción de alquenos son más fiables en la síntesis orgánica. Los alquenos reaccionan con N -bromosuccinimida y agua en la reacción de formación de halohidrina . Las aminas se pueden convertir en sales de diazonio , que luego se hidrolizan.
Con valores de p K a acuoso de alrededor de 16-19, los alcoholes son, en general, ácidos ligeramente más débiles que el agua . Con bases fuertes como el hidruro de sodio o el sodio forman sales [a] llamadas alcóxidos , con la fórmula general RO − M + (donde R es un alquilo y M es un metal ).
La acidez de los alcoholes se ve fuertemente afectada por la solvatación . En la fase gaseosa, los alcoholes son más ácidos que en agua. [33] En DMSO , los alcoholes (y el agua) tienen un p K a de alrededor de 29-32. Como consecuencia, los alcóxidos (y el hidróxido) son bases poderosas y nucleófilos (por ejemplo, para la síntesis del éter de Williamson ) en este solvente. En particular, RO − o HO − en DMSO se pueden utilizar para generar concentraciones de equilibrio significativas de iones acetiluro a través de la desprotonación de alquinos (ver reacción de Favorskii ). [34] [35]
Los alcoholes terciarios reaccionan con ácido clorhídrico para producir cloruro de alquilo terciario . Los alcoholes primarios y secundarios se convierten en los cloruros correspondientes utilizando cloruro de tionilo y varios reactivos de cloruro de fósforo. [36]
Los alcoholes primarios y secundarios también se convierten en bromuros de alquilo utilizando tribromuro de fósforo , por ejemplo:
En la desoxigenación de Barton-McCombie, un alcohol se desoxigena a un alcano con hidruro de tributilestaño o un complejo de trimetilborano -agua en una reacción de sustitución radical .
Mientras tanto, el átomo de oxígeno tiene pares solitarios de electrones no enlazados que lo vuelven débilmente básico en presencia de ácidos fuertes como el ácido sulfúrico . Por ejemplo, con el metanol:
Al ser tratados con ácidos fuertes, los alcoholes experimentan la reacción de eliminación E1 para producir alquenos . La reacción, en general, obedece a la regla de Zaitsev , que establece que se forma el alqueno más estable (normalmente el más sustituido). Los alcoholes terciarios se eliminan fácilmente a una temperatura ligeramente superior a la ambiente, pero los alcoholes primarios requieren una temperatura más alta.
Este es un diagrama de deshidratación catalizada por ácido del etanol para producir etileno :
Una reacción de eliminación más controlada requiere la formación del éster xantato.
Los alcoholes terciarios reaccionan con ácidos fuertes para generar carbocationes. La reacción está relacionada con su deshidratación, por ejemplo, el isobutileno a partir del alcohol terc -butílico. Un tipo especial de reacción de deshidratación involucra al trifenilmetanol y especialmente a sus derivados sustituidos con amina. Cuando se tratan con ácido, estos alcoholes pierden agua para dar carbocationes estables, que son colorantes comerciales. [37]

El alcohol y los ácidos carboxílicos reaccionan en la denominada esterificación de Fischer . La reacción suele requerir un catalizador , como ácido sulfúrico concentrado:
Otros tipos de ésteres se preparan de manera similar; por ejemplo, los ésteres de tosilo (tosilato) se obtienen mediante la reacción del alcohol con cloruro de 4-toluenosulfonilo en piridina .
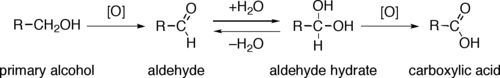
Los alcoholes primarios ( R−CH 2 OH ) pueden oxidarse a aldehídos ( R−CHO ) o a ácidos carboxílicos ( R−CO 2 H ). La oxidación de los alcoholes secundarios ( R 1 R 2 CH−OH ) normalmente termina en la etapa de cetona ( R 1 R 2 C=O ). Los alcoholes terciarios ( R 1 R 2 R 3 C−OH ) son resistentes a la oxidación.
La oxidación directa de alcoholes primarios a ácidos carboxílicos normalmente se produce a través del aldehído correspondiente, que se transforma mediante un hidrato de aldehído ( R−CH(OH) 2 ) por reacción con agua antes de que pueda oxidarse aún más al ácido carboxílico.
Los reactivos útiles para la transformación de alcoholes primarios en aldehídos normalmente también son adecuados para la oxidación de alcoholes secundarios en cetonas. Entre ellos se encuentran el reactivo de Collins y el peryodinano de Dess-Martin . La oxidación directa de alcoholes primarios en ácidos carboxílicos se puede llevar a cabo utilizando permanganato de potasio o el reactivo de Jones .
Como ol es indicativo de un derivado de OH, no parece haber ninguna razón por la que la simple palabra ácido no deba connotar carboxilo, y por qué al no deba connotar COH; los nombres etanol etanal y ácido etanoico o simplemente ácido etanoico representarían entonces los derivados OH, COH y COOH del etano.