La enfermedad de células falciformes ( ECF ), también llamada simplemente anemia falciforme , es un grupo de trastornos sanguíneos relacionados con la hemoglobina que generalmente se heredan . [2] El tipo más común se conoce como anemia de células falciformes . [2] Resulta en una anomalía en la hemoglobina, la proteína transportadora de oxígeno que se encuentra en los glóbulos rojos . [2] Esto lleva a que los glóbulos rojos adopten una forma anormal similar a una hoz en determinadas circunstancias; con esta forma, no pueden deformarse al pasar por los capilares , lo que causa bloqueos. [2] Los problemas de la enfermedad de células falciformes suelen comenzar alrededor de los 5 a 6 meses de edad. [1] Pueden desarrollarse varios problemas de salud, como ataques de dolor (conocidos como crisis de células falciformes ) en las articulaciones, anemia , hinchazón en las manos y los pies, infecciones bacterianas , mareos [8] y accidente cerebrovascular . [1] La probabilidad de síntomas graves, incluido el dolor a largo plazo, aumenta con la edad. [2] Sin tratamiento, las personas con anemia falciforme rara vez llegan a la edad adulta, pero con una buena atención médica, la expectativa de vida media es de entre 58 y 66 años. [9] [10] Todos los órganos principales se ven afectados por la enfermedad de células falciformes. El hígado, el corazón, los riñones, la vesícula biliar, los ojos, los huesos y las articulaciones también pueden sufrir daños debido a las funciones anormales de las células falciformes y su incapacidad para fluir correctamente a través de los vasos sanguíneos pequeños. [11]
La enfermedad de células falciformes se produce cuando una persona hereda dos copias anormales del gen de la β-globina que produce la hemoglobina, una de cada progenitor. [3] Existen varios subtipos, dependiendo de la mutación exacta en cada gen de la hemoglobina. [2] Un ataque puede ser desencadenado por cambios de temperatura, estrés, deshidratación y gran altitud. [1] Una persona con una sola copia anormal no suele tener síntomas y se dice que tiene el rasgo de células falciformes . [3] A estas personas también se las conoce como portadoras . [5] El diagnóstico se realiza mediante un análisis de sangre , y algunos países realizan pruebas a todos los bebés al nacer para detectar la enfermedad. [4] El diagnóstico también es posible durante el embarazo. [4]
El cuidado de las personas con anemia de células falciformes puede incluir la prevención de infecciones con vacunas y antibióticos , una ingesta elevada de líquidos, suplementos de ácido fólico y analgésicos . [5] [6] Otras medidas pueden incluir la transfusión de sangre y el medicamento hidroxicarbamida (hidroxiurea). [6] En 2023, se aprobaron nuevas terapias genéticas que implican la modificación genética y el reemplazo de células madre formadoras de sangre en la médula ósea. [12] [13]
A partir de 2021 [actualizar], se estima que la SCD afecta a alrededor de 7,7 millones de personas en todo el mundo, causando directamente 34.000 muertes anuales y un factor contribuyente a otras 376.000 muertes. [7] Se cree que alrededor del 80% de los casos de enfermedad de células falciformes ocurren en África subsahariana . [14] También ocurre en menor grado en partes de la India , el sur de Europa , Asia occidental , el norte de África y entre personas de origen africano (subsaharianos) que viven en otras partes del mundo. [15] La condición fue descrita por primera vez en la literatura médica por el médico estadounidense James B. Herrick en 1910. [16] [17] En 1949, su transmisión genética fue determinada por EA Beet y JV Neel. [17] En 1954, se estableció que los portadores del gen anormal están protegidos en cierto grado contra la malaria . [17]
_(14768428942).jpg/440px-The_diseases_of_infancy_and_childhood_(1920)_(14768428942).jpg)


Los síntomas de la enfermedad de células falciformes suelen aparecer en la primera infancia. La gravedad de los síntomas puede variar de una persona a otra, al igual que la frecuencia de los episodios de crisis. [18] [14] La enfermedad de células falciformes puede provocar diversas complicaciones agudas y crónicas , varias de las cuales tienen una alta tasa de mortalidad. [19]
Cuando la anemia falciforme se presenta durante el primer año de vida, el problema más común es un episodio de dolor e hinchazón en las manos y los pies del niño, conocido como dactilitis o "síndrome mano-pie". La palidez, la ictericia y la fatiga también pueden ser signos tempranos debido a la anemia resultante de la enfermedad de células falciformes. [20]
Entre los niños mayores de 2 años, la presentación inicial más frecuente es un evento doloroso de tipo generalizado o variable, y una versión ligeramente menos común aparece como un evento de dolor torácico agudo. La dactilitis rara vez o nunca ocurre en niños mayores de 2 años. [20] [21]
También denominada "crisis de células falciformes" o "crisis drepanocítica", la crisis vasooclusiva (VOC) se manifiesta principalmente como dolor extremo, que afecta con mayor frecuencia al pecho, la espalda, las piernas y/o los brazos. [22] La causa subyacente son los glóbulos rojos en forma de hoz que obstruyen los capilares y restringen el flujo sanguíneo a un órgano, lo que resulta en isquemia , dolor , necrosis y, a menudo, daño orgánico. La frecuencia, gravedad y duración de estas crisis varían considerablemente. Las crisis dolorosas se tratan con hidratación, analgésicos y transfusión de sangre ; el manejo del dolor requiere la administración de fármacos opioides a intervalos regulares hasta que la crisis se haya resuelto. Para las crisis más leves, un subgrupo de pacientes se maneja con medicamentos antiinflamatorios no esteroides como diclofenaco o naproxeno . Para las crisis más graves, la mayoría de los pacientes requieren tratamiento hospitalario para opioides intravenosos; los dispositivos de analgesia controlados por el paciente se utilizan comúnmente en este entorno. Las crisis vasooclusivas que afectan órganos como el pene [23] o los pulmones se consideran una emergencia y se tratan con transfusiones de glóbulos rojos. Se recomienda la espirometría incentivada , una técnica para estimular la respiración profunda y minimizar el desarrollo de atelectasias . [24]
Aunque no siempre está claro qué desencadena una VOC, cualquier cosa que provoque la constricción de los vasos sanguíneos es un desencadenante potencial. Esto incluye el estrés físico o mental , el frío y la deshidratación . [25] " Después de que la HbS se desoxigena en los capilares, lleva algún tiempo (segundos) para la polimerización de la HbS y la posterior transformación de flexible a rígida. Si el tiempo de tránsito de los glóbulos rojos a través de la microvasculatura es más largo que el tiempo de polimerización, los glóbulos rojos falciformes se alojarán en la microvasculatura " . [26]
El bazo es especialmente propenso a sufrir daños en la SCD debido a su papel como filtro de sangre. Una crisis de secuestro esplénico, también conocida como crisis del bazo, es una emergencia médica que ocurre cuando los glóbulos rojos falciformes bloquean el mecanismo de filtrado del bazo , lo que hace que el bazo se hinche y se llene de sangre. La acumulación de glóbulos rojos en el bazo da como resultado una caída repentina de la hemoglobina circulante y una anemia potencialmente mortal. Los síntomas incluyen dolor en el lado izquierdo, bazo hinchado (que se puede detectar mediante palpación ), fatiga, mareos, irritabilidad, ritmo cardíaco rápido o piel pálida. Afecta más comúnmente a niños pequeños, la edad media de la primera aparición es de 1,4 años. A la edad de 5 años, los casos repetidos de secuestro causan cicatrices y, finalmente, atrofia del bazo . [27] [28] [29]
El tratamiento es de apoyo, con transfusión de sangre si los niveles de hemoglobina bajan demasiado. Puede ser necesaria una esplenectomía total o parcial . [30] Las consecuencias a largo plazo de la pérdida de la función del bazo son una mayor susceptibilidad a las infecciones bacterianas . [29]
El síndrome torácico agudo es causado por una VOC que afecta los pulmones, posiblemente desencadenada por una infección o por émbolos que han circulado desde otros órganos. Los síntomas incluyen sibilancia, dolor torácico, fiebre, infiltrado pulmonar (visible en la radiografía) e hipoxemia . Después de la crisis drepanocítica (ver arriba), es la segunda causa más común de hospitalización y representa aproximadamente el 25% de las muertes en pacientes con drepanocitosis. La mayoría de los casos se presentan con crisis vasooclusivas y luego desarrollan un síndrome torácico agudo. [31] [32]
Las crisis aplásicas son casos de un empeoramiento agudo de la anemia de base del paciente, que produce palidez , frecuencia cardíaca rápida y fatiga. Esta crisis normalmente es desencadenada por el parvovirus B19 , que afecta directamente la producción de glóbulos rojos al invadir los precursores de los glóbulos rojos y multiplicarse en ellos y destruirlos. [33] La infección por parvovirus [34] impide casi por completo la producción de glóbulos rojos durante dos o tres días (aplasia de glóbulos rojos). En individuos normales, esto tiene pocas consecuencias, pero la vida acortada de los glóbulos rojos de los pacientes con SCD da lugar a una situación abrupta y potencialmente mortal. El recuento de reticulocitos cae drásticamente durante la enfermedad (lo que provoca reticulocitopenia ), la producción de glóbulos rojos disminuye y la rápida destrucción de los glóbulos rojos existentes conduce a una anemia aguda y grave. Esta crisis tarda entre cuatro y siete días en resolverse. La mayoría de los pacientes pueden tratarse con medidas de apoyo; algunos necesitan una transfusión de sangre. [35]


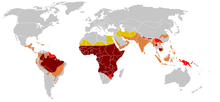
La anemia falciforme es más frecuente en áreas que históricamente han estado asociadas con malaria endémica . El rasgo drepanocítico proporciona a un portador una ventaja de supervivencia contra la mortalidad por malaria en comparación con las personas con hemoglobina normal en regiones donde la malaria es endémica. [36] [37]
La infección por el parásito de la malaria afecta a los portadores asintomáticos del gen de la hemoglobina anormal de forma diferente a los pacientes con anemia falciforme completa. Los portadores (heterocigotos para el gen) que contraen malaria tienen menos probabilidades de sufrir síntomas graves que las personas con hemoglobina normal. Los pacientes con anemia falciforme (homocigotos para el gen) tienen, de manera similar, menos probabilidades de infectarse con malaria; sin embargo, una vez infectados, tienen más probabilidades de desarrollar anemia grave y potencialmente mortal. [38] [39]
El impacto del rasgo de la anemia falciforme en la inmunidad contra la malaria ilustra algunas compensaciones evolutivas que se han producido debido a la malaria endémica. Aunque la menor esperanza de vida de quienes tienen la condición homocigótica tendería a desfavorecer la supervivencia del rasgo, este se conserva en las regiones propensas a la malaria debido a los beneficios que proporciona la forma heterocigótica; un ejemplo de selección natural. [40]
La anemia de células falciformes puede provocar diversas complicaciones, [41] entre ellas:

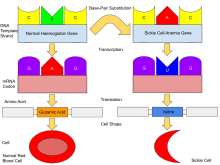
Normalmente, los seres humanos tienen hemoglobina A , que consta de dos cadenas alfa y dos cadenas beta, hemoglobina A2 , que consta de dos cadenas alfa y dos delta, y hemoglobina F (HbF), que consta de dos cadenas alfa y dos gamma en sus cuerpos. De estos tres tipos, la hemoglobina F domina hasta aproximadamente las 6 semanas de edad. Posteriormente, la hemoglobina A domina durante toda la vida. [58] En las personas diagnosticadas con anemia falciforme, al menos una de las subunidades de β-globina en la hemoglobina A se reemplaza con lo que se conoce como hemoglobina S. En la anemia falciforme, una forma común de anemia falciforme, la hemoglobina S reemplaza ambas subunidades de β-globina en la hemoglobina. [18]
La anemia falciforme tiene un patrón autosómico recesivo de herencia de los padres. [59] Los tipos de hemoglobina que una persona produce en los glóbulos rojos dependen de los genes de hemoglobina que hereda de sus padres. Si uno de los padres tiene anemia falciforme y el otro tiene el rasgo falciforme, entonces cualquier niño tiene un 50% de probabilidades de tener anemia falciforme y un 50% de probabilidades de tener el rasgo falciforme. Cuando ambos padres tienen el rasgo falciforme, cualquier niño tiene un 25% de probabilidades de tener anemia falciforme; un 25% de probabilidades de no tener alelos falciformes y un 50% de probabilidades de tener la condición heterocigótica. [60] [61] [ ¿ Fuente médica poco confiable? ]
La mutación del gen de la anemia falciforme probablemente surgió espontáneamente en diferentes áreas geográficas, [62] como lo sugiere el análisis de endonucleasas de restricción. Estas variantes se conocen como Camerún, Senegal, Benín, Bantú y Arabia Saudita-Asiática. Su importancia clínica se debe a que algunas están asociadas con niveles más altos de HbF, por ejemplo, las variantes de Senegal y Arabia Saudita-Asiática, y tienden a causar una enfermedad más leve. [63]
El defecto genético es una mutación de un solo nucleótido (ver polimorfismo de un solo nucleótido – SNP) ( el codón GAG cambia a GTG) del gen de la β-globina, que da como resultado que el glutamato (E/Glu) sea sustituido por valina (V/Val) en la posición 6 (sustitución E6V). [64] [nota 1] La hemoglobina S con esta mutación se conoce como HbS, a diferencia de la HbA adulta normal. Esta es normalmente una mutación benigna, que no causa efectos aparentes en las estructuras secundaria , terciaria o cuaternaria de la hemoglobina en condiciones de concentración normal de oxígeno . Sin embargo, bajo baja concentración de oxígeno , la HbS se polimeriza y forma precipitados fibrosos porque la forma desoxi de la hemoglobina expone un parche hidrofóbico en la proteína entre las hélices E y F (Phe 85, Leu 88). [65]
En las personas heterocigotas para la HbS ( portadoras de hemoglobina falciforme), los problemas de polimerización son menores porque el alelo normal puede producir la mitad de la hemoglobina. En las personas homocigotas para la HbS, la presencia de polímeros de cadena larga de HbS distorsiona la forma del glóbulo rojo, que pasa de ser liso, como una rosquilla , a ser irregular y lleno de púas, lo que lo hace frágil y susceptible de romperse dentro de los capilares . Los portadores tienen síntomas solo si se les priva de oxígeno (por ejemplo, al escalar una montaña) o cuando están gravemente deshidratados . [ cita requerida ]
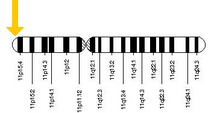
El alelo responsable de la anemia de células falciformes se encuentra en el brazo corto del cromosoma 11 , más específicamente en el 11p15.5. Una persona que recibe el gen defectuoso tanto del padre como de la madre desarrolla la enfermedad; una persona que recibe un alelo defectuoso y uno sano permanece sana, pero puede transmitir la enfermedad y se la conoce como portadora o heterocigota. Los heterocigotos aún pueden contraer malaria, pero sus síntomas son generalmente menos graves. [66]
Debido a la ventaja adaptativa del heterocigoto, la enfermedad aún prevalece, especialmente entre personas con ascendencia reciente en áreas afectadas por la malaria, como África , el Mediterráneo , India y Medio Oriente . [67] La malaria fue históricamente endémica del sur de Europa, pero fue declarada erradicada a mediados del siglo XX, con la excepción de raros casos esporádicos. [68]
El parásito de la malaria tiene un ciclo de vida complejo y pasa parte de él en los glóbulos rojos. En un portador, la presencia del parásito de la malaria hace que los glóbulos rojos con hemoglobina defectuosa se rompan prematuramente, lo que hace que el parásito Plasmodium sea incapaz de reproducirse. Además, la polimerización de la Hb afecta la capacidad del parásito para digerir la Hb en primer lugar. Por lo tanto, en las zonas donde la malaria es un problema, las posibilidades de supervivencia de las personas en realidad aumentan si son portadoras de rasgos de anemia falciforme (selección para el heterocigoto). [ cita requerida ]
En los Estados Unidos, donde no hay malaria endémica, la prevalencia de la anemia de células falciformes entre las personas de ascendencia africana es menor (alrededor del 0,25%) que entre las personas de África occidental (alrededor del 4,0%) y está disminuyendo. Sin malaria endémica, la mutación de la anemia de células falciformes es puramente desventajosa y tiende a disminuir en la población afectada por selección natural , y ahora artificialmente a través del cribado genético prenatal . Sin embargo, la comunidad afroamericana desciende de varios grupos étnicos africanos y no africanos, incluidos los esclavos estadounidenses. Por lo tanto, un grado de dilución genética a través del mestizaje con personas no africanas y una alta presión selectiva de la salud a través de la esclavitud (especialmente la trata de esclavos y el frecuentemente mortal Paso Medio ) pueden ser las explicaciones más plausibles para la menor prevalencia de la anemia de células falciformes (y, posiblemente, otras enfermedades genéticas) entre los afroamericanos en comparación con los africanos occidentales. Otro factor que limita la propagación de los genes de la anemia de células falciformes en América del Norte es la relativa ausencia de poligamia . En las sociedades polígamas, los varones afectados pueden ser padres de muchos hijos con múltiples parejas. [69]
La pérdida de elasticidad de los glóbulos rojos es fundamental para la fisiopatología de la enfermedad de células falciformes. Los glóbulos rojos normales son bastante elásticos y tienen una forma de disco bicóncavo, lo que permite que las células se deformen para pasar a través de los capilares. [70] En la enfermedad de células falciformes, la baja tensión de oxígeno promueve la drepanocitosis de los glóbulos rojos y los episodios repetidos de drepanocitosis dañan la membrana celular y disminuyen la elasticidad de la célula. Estas células no vuelven a su forma normal cuando se restablece la tensión de oxígeno normal. Como consecuencia, estas células sanguíneas rígidas no pueden deformarse al pasar a través de capilares estrechos, lo que conduce a la oclusión de los vasos y a la isquemia . [ cita requerida ]
La anemia propiamente dicha de la enfermedad se debe a la hemólisis , la destrucción de los glóbulos rojos, debido a su forma. Aunque la médula ósea intenta compensar esto creando nuevos glóbulos rojos, no alcanza el ritmo de destrucción. [71] Los glóbulos rojos sanos suelen funcionar durante 90 a 120 días, pero las células falciformes sólo duran entre 10 y 20 días. [72]
En la HbS, el hemograma completo revela niveles de hemoglobina en el rango de 6-8 g/dl con un alto recuento de reticulocitos (ya que la médula ósea compensa la destrucción de las células falciformes produciendo más glóbulos rojos). En otras formas de enfermedad de células falciformes, los niveles de Hb tienden a ser más altos. Un frotis de sangre puede mostrar características de hipoesplenismo ( células diana y cuerpos de Howell-Jolly ). [73]
La drepanocitosis de los glóbulos rojos en un frotis de sangre se puede inducir mediante la adición de metabisulfito de sodio . La presencia de hemoglobina drepanocítica también se puede demostrar con la "prueba de solubilidad drepanocítica" (también llamada "sickledex"). [74] Una mezcla de hemoglobina S (HbS) en una solución reductora (como el ditionito de sodio ) da un aspecto turbio, mientras que la Hb normal da una solución clara. [75]
Las formas anormales de hemoglobina se pueden detectar mediante electroforesis de hemoglobina , una forma de electroforesis en gel en la que los distintos tipos de hemoglobina se mueven a distintas velocidades. La hemoglobina falciforme (HgbS) y la hemoglobina C con drepanocitosis (HgbSC), las dos formas más comunes, se pueden identificar a partir de ahí. El diagnóstico se puede confirmar con cromatografía líquida de alto rendimiento . Rara vez se realizan pruebas genéticas , ya que otras investigaciones son altamente específicas para HbS y HbC. [76]
Una crisis aguda de anemia falciforme suele ser desencadenada por una infección. Por lo tanto, se debe realizar de forma rutinaria un análisis de orina para detectar una infección oculta del tracto urinario y una radiografía de tórax para buscar una neumonía oculta. [77]
Las personas que son portadoras conocidas de la enfermedad o que corren el riesgo de tener un hijo con anemia de células falciformes pueden someterse a asesoramiento genético . Los asesores genéticos trabajan con las familias para discutir los beneficios, las limitaciones y la logística de las opciones de pruebas genéticas, así como el posible impacto de las pruebas y los resultados de las pruebas en el individuo. [78] [79] Durante el embarazo, las pruebas genéticas se pueden realizar en una muestra de sangre del feto o en una muestra de líquido amniótico . Durante el primer trimestre del embarazo, la muestra de vellosidades coriónicas (CVS) también es una técnica utilizada para el diagnóstico prenatal de SCD. [80] Dado que tomar una muestra de sangre de un feto tiene mayores riesgos, generalmente se utiliza esta última prueba. El cribado neonatal, a veces denominado cribado del recién nacido , no solo proporciona un método de detección temprana para las personas con enfermedad de células falciformes, sino que también permite la identificación de los grupos de personas que son portadoras del rasgo de células falciformes. [81] Los asesores genéticos pueden ayudar a las personas de color y a sus familias a abordar las disparidades raciales y étnicas que existen en la atención médica. [82]
En 2010, en los EE. UU. se debatió y se consideró de manera significativa la necesidad de realizar pruebas exhaustivas para detectar la anemia falciforme en los atletas. [83] [84] [85] [86] En 2012, la Sociedad Estadounidense de Hematología concluyó que no respaldaba la realización de pruebas o la divulgación del estado de anemia falciforme como requisito previo para participar en actividades deportivas debido a la falta de evidencia científica, la inconsistencia con las buenas prácticas médicas y la inconsistencia con la ética de la salud pública. Recomendó intervenciones universales para reducir las lesiones y muertes relacionadas con el esfuerzo que fueran efectivas para todos los atletas independientemente de su estado de anemia falciforme. [87]
El tratamiento implica una serie de medidas. Si bien históricamente se ha recomendado que las personas con anemia falciforme eviten el ejercicio, el ejercicio regular puede ser beneficioso para las personas. [88] Se debe evitar la deshidratación. [89] Se recomienda una dieta rica en calcio [90], pero la eficacia de los suplementos de vitamina D sigue siendo incierta. [91] La FDA respaldó el uso de L-glutamina a partir de los cinco años, ya que disminuye las complicaciones. [92]
Desde el nacimiento hasta los cinco años de edad, se recomienda administrar penicilina diariamente, debido al sistema inmunológico inmaduro que los hace más propensos a las enfermedades de la primera infancia. [93] La OMS había recomendado anteriormente la suplementación dietética de ácido fólico . [5] Una revisión Cochrane de 2016 sobre su uso encontró que "el efecto de la suplementación sobre la anemia y cualquier síntoma de anemia sigue sin estar claro" debido a la falta de evidencia médica. [94]

El efecto protector del rasgo drepanocítico no se aplica a las personas con enfermedad de células falciformes; de hecho, son más vulnerables a la malaria, ya que la causa más común de crisis dolorosas en los países palúdicos es la infección por malaria. Las personas con enfermedad de células falciformes que viven en países palúdicos deben recibir medicación de por vida para la prevención . [95]
La mayoría de las personas con enfermedad de células falciformes tienen episodios intensamente dolorosos llamados crisis vasooclusivas. Sin embargo, la frecuencia, gravedad y duración de estas crisis varían enormemente. Las crisis dolorosas se tratan sintomáticamente con analgésicos ; el manejo del dolor requiere la administración de fármacos opioides a intervalos regulares hasta que la crisis se haya resuelto. Para las crisis más leves, un subgrupo de pacientes se maneja con AINE (como diclofenaco o naproxeno ). Para las crisis más graves, la mayoría de los pacientes requieren tratamiento hospitalario para opioides intravenosos. [96]
Los líquidos adicionales, administrados por vía oral o intravenosa, son una parte rutinaria del tratamiento de las crisis vasooclusivas, pero la evidencia sobre la vía, la cantidad y el tipo de reemplazo de líquidos más efectivos sigue siendo incierta. [97]
En 2019, Crizanlizumab , un anticuerpo monoclonal dirigido contra la p-selectina, fue aprobado en los Estados Unidos para reducir la frecuencia de crisis vasooclusivas en personas de 16 años o más. [98]
La ecografía Doppler transcraneal (TCD) puede detectar a niños con anemia falciforme que tienen un alto riesgo de sufrir un accidente cerebrovascular. La prueba de ultrasonido detecta los vasos sanguíneos parcialmente obstruidos por la anemia falciforme midiendo la velocidad de la sangre que ingresa al cerebro, ya que la velocidad del flujo sanguíneo está inversamente relacionada con el diámetro arterial y, en consecuencia, la alta velocidad del flujo sanguíneo se correlaciona con el estrechamiento de las arterias. [99] En 2002, el Instituto Nacional de Salud (NIH) emitió una declaración recomendando que los niños con anemia falciforme se sometan a la ecografía Doppler transcraneal anualmente, y en 2014, un panel de expertos convocado por el NIH emitió pautas que reiteraban la misma recomendación. Una revisión de los registros médicos, realizada por la hematóloga Dra. Julie Kanter en la Universidad de Alabama en Birmingham, mostró que, en promedio, solo el 48,4 por ciento de los niños con anemia falciforme se someten a la prueba de ultrasonido recomendada. [100]
Un estudio de los NIH de 1994 mostró que los niños con riesgo de sufrir accidentes cerebrovasculares que recibieron transfusiones de sangre tuvieron una tasa anual de accidentes cerebrovasculares de menos del 1 por ciento, mientras que aquellos niños que no recibieron transfusiones de sangre tuvieron una tasa de accidentes cerebrovasculares del 10 por ciento por año. (Véase también el estudio de 1998 en el New England Journal of Medicine . [99] ) Además de las ecografías y las transfusiones de sangre, el fármaco genérico económico hidroxiurea puede reducir el riesgo de daño irreversible a los órganos y al cerebro. Las directrices de los NIH publicadas en 2014 establecen que todos los niños y adolescentes deben tomar hidroxiurea, al igual que los adultos con complicaciones graves o tres o más crisis de dolor en un año. [100]
El tratamiento es similar al de una crisis vasooclusiva, con la adición de antibióticos (generalmente una quinolona o un macrólido, ya que se cree que las bacterias deficientes en la pared celular ["atípicas"] contribuyen al síndrome), [101] suplementos de oxígeno para la hipoxia y observación estrecha. En ausencia de evidencia de alta calidad con respecto a la efectividad de los antibióticos para el síndrome torácico agudo en personas con enfermedad de células falciformes, no existe un tratamiento antibiótico estándar a partir de 2019. [102] Se recomienda que las personas con sospecha de síndrome torácico agudo sean ingresadas en el hospital con empeoramiento del gradiente Aa como indicación de ingreso en la UCI. [24]
Si el infiltrado pulmonar empeora o aumentan los requerimientos de oxígeno, está indicada una transfusión sanguínea simple o una exanguinotransfusión . Esta última implica el intercambio de una porción significativa de la masa de glóbulos rojos de la persona por glóbulos rojos normales, lo que disminuye el nivel de hemoglobina S en la sangre del paciente. Sin embargo, actualmente hay evidencia incierta sobre los posibles beneficios o daños de la transfusión sanguínea para el síndrome torácico agudo en personas con enfermedad de células falciformes. [103]
La hidroxiurea , también conocida como hidroxicarbamida , probablemente reduce la frecuencia de episodios dolorosos y el riesgo de enfermedad potencialmente mortal o muerte, pero actualmente no hay evidencia suficiente con respecto al riesgo de efectos adversos. [104] La hidroxiurea y la flebotomía combinadas pueden ser más efectivas que la transfusión y la quelación combinadas en términos de dolor, enfermedad potencialmente mortal y riesgo de muerte. [104]
Fue el primer fármaco aprobado para el tratamiento de la anemia de células falciformes, y se demostró que reducía el número y la gravedad de los ataques en 1995 [105] y que posiblemente aumentaba el tiempo de supervivencia en un estudio de 2003. [106] Esto se logra, en parte, reactivando la producción de hemoglobina fetal en lugar de la hemoglobina S que causa la anemia de células falciformes. La hidroxiurea se había utilizado anteriormente como agente de quimioterapia , y existe cierta preocupación de que su uso a largo plazo pueda ser perjudicial, pero este riesgo es inexistente o muy pequeño y los beneficios probablemente superen los riesgos. [19] [107]
El voxelotor fue aprobado en los Estados Unidos en 2019 para aumentar la hemoglobina en personas con enfermedad SS. [108] Sin embargo, tras un mayor riesgo de convulsiones vasooclusivas y muerte observado en registros y ensayos clínicos, la Agencia Europea de Medicamentos suspendió la autorización de comercialización del voxelotor en septiembre de 2024, tras lo cual el fabricante, Pfizer , lo retiró del mercado en todo el mundo. [109] [110]
Las terapias psicológicas como la educación del paciente , la terapia cognitiva , la terapia conductual y la psicoterapia psicodinámica , que tienen como objetivo complementar los tratamientos médicos actuales, requieren más investigaciones para determinar su eficacia. [111]
Las transfusiones de sangre se utilizan a menudo en el tratamiento de la enfermedad de células falciformes en casos agudos y para prevenir complicaciones al disminuir la cantidad de glóbulos rojos (RBC) que pueden formar células falciformes al agregar glóbulos rojos normales. [112] En los niños, se ha demostrado que la terapia de transfusión de glóbulos rojos preventiva reduce el riesgo de un primer accidente cerebrovascular o un accidente cerebrovascular silencioso cuando la ecografía Doppler transcraneal muestra un flujo sanguíneo cerebral anormal. [6] En aquellos que han sufrido un accidente cerebrovascular previo, también reduce el riesgo de accidente cerebrovascular recurrente y accidentes cerebrovasculares silenciosos adicionales. [113] [114]
Los trasplantes de médula ósea han demostrado ser eficaces en niños; son la única cura conocida para la anemia drepanocítica. [115] Sin embargo, los trasplantes de médula ósea son difíciles de obtener debido a la tipificación específica de HLA necesaria. Lo ideal sería que un pariente cercano (alogénico) donara la médula ósea necesaria para el trasplante. El pariente cercano debe tener el mismo tipo de sangre que el paciente. Se están desarrollando algunas terapias genéticas que alterarían las células madre de la médula ósea del propio paciente ex vivo, que luego se pueden trasplantar nuevamente al paciente después de que la quimioterapia elimine las células originales no modificadas. [116]
Trasplante de células madre hematopoyéticas
El trasplante de células madre hematopoyéticas (TCMH) implica reemplazar las células madre disfuncionales de una persona con enfermedad de células falciformes con células sanas de un donante compatible. [117] Encontrar al donante ideal, por lo general un donante de reserva o alguien casi compatible, es esencial para el éxito del proceso. Diferentes tipos de donantes pueden ser adecuados e incluyen sangre del cordón umbilical , parientes compatibles con antígeno leucocitario humano (HLA), donantes compatibles con HLA que no están relacionados con la persona que está siendo tratada, haploidénticos pero que se sometieron a un procedimiento mieloblativo (quimioterapia para matar las células de la médula ósea) u otras combinaciones. [117]
El TPH se utiliza para tratar a personas con enfermedad de células falciformes grave en grandes centros, sin embargo, la evidencia que sustenta la eficacia de este procedimiento considerando los riesgos no es clara. [118] No hay evidencia médica sólida para determinar los riesgos y los beneficios potenciales relacionados con el tratamiento de personas con enfermedad de células falciformes con trasplantes de células madre hematopoyéticas. [118] [119] Los riesgos asociados con el TPH pueden incluir enfermedad de injerto contra huésped, muerte, falla del injerto y otra toxicidad relacionada con el trasplante. [117]
En 2023, tanto el exagamglogene autotemcel como el lovotibeglogene autotemcel fueron aprobados para el tratamiento de la anemia de células falciformes. [12] [120] El 24 de octubre de 2024, después de 44 días de tratamiento, Kendric Cromer, el primer caso comercial en recibir terapia génica, fue dado de alta del Children's National Hospital . Se sometió a esta última terapia y, según las empresas involucradas, decenas de otros pacientes están recibiendo actualmente estos tratamientos. [121]
En el tratamiento de la necrosis avascular del hueso en personas con enfermedad de células falciformes, el objetivo del tratamiento es reducir o detener el dolor y mantener la movilidad de las articulaciones . [46] Las opciones de tratamiento actuales incluyen el reposo de la articulación, la fisioterapia , los analgésicos , la cirugía de reemplazo articular o el injerto óseo . [46] Se necesitan ensayos controlados, aleatorizados y de alta calidad para evaluar la opción de tratamiento más eficaz y determinar si una combinación de fisioterapia y cirugía es más eficaz que la fisioterapia sola. [122] [123]
Alrededor del 90% de las personas sobreviven hasta los 20 años, y cerca del 50% sobreviven más allá de los 50 años . [124] En 2001, según un estudio realizado en Jamaica, la supervivencia media estimada para las personas con anemia drepanocítica homocigótica era de 53 años para los hombres y de 58 años para las mujeres. [125] Se desconoce la esperanza de vida en gran parte del mundo en desarrollo. [126] En 1975, alrededor del 7,3% de las personas con anemia drepanocítica morían antes de cumplir 23 años; mientras que en 1989, el 2,6% de las personas con anemia drepanocítica morían antes de cumplir 20 años. [127] : 348
El gen HbS se puede encontrar en todos los grupos étnicos. [128] La frecuencia más alta de la enfermedad de células falciformes se encuentra en las regiones tropicales, particularmente en África subsahariana, las regiones tribales de la India y Oriente Medio. [129] Se cree que alrededor del 80% de los casos de enfermedad de células falciformes ocurren en África subsahariana . [14] La migración de poblaciones sustanciales de estas áreas de alta prevalencia a países de baja prevalencia en Europa ha aumentado drásticamente en las últimas décadas y en algunos países europeos, la enfermedad de células falciformes ahora ha superado condiciones genéticas más familiares como la hemofilia y la fibrosis quística . [130] En 2015, resultó en alrededor de 114.800 muertes. [131]
La enfermedad de células falciformes se presenta con mayor frecuencia entre personas cuyos antepasados vivieron en regiones subsaharianas tropicales y subtropicales donde la malaria es o fue común. En los lugares donde la malaria es común, ser portador de un solo alelo (rasgo) de la enfermedad de células falciformes confiere una ventaja heterocigótica ; los seres humanos con uno de los dos alelos de la enfermedad de células falciformes muestran síntomas menos graves cuando se infectan con malaria. [132]
Esta afección se hereda con un patrón autosómico recesivo, lo que significa que ambas copias del gen en cada célula tienen mutaciones. Cada uno de los padres es portador de una copia del gen mutado, pero por lo general no presentan signos ni síntomas de la afección. [133]
Tres cuartas partes de los casos de anemia falciforme se producen en África. Un informe reciente de la OMS estimó que alrededor del 2% de los recién nacidos en Nigeria estaban afectados por anemia falciforme, lo que da un total de 150.000 niños afectados nacidos cada año solo en Nigeria. La frecuencia de portadores varía entre el 10 y el 40% en África ecuatorial, disminuyendo al 1-2% en la costa norteafricana y a menos del 1% en Sudáfrica. [134] Los estudios en África muestran una disminución significativa en la tasa de mortalidad infantil, de 2 a 16 meses de edad, debido al rasgo falciforme. Esto sucedió en áreas de casos predominantes de malaria. [135]
Uganda tiene la quinta mayor carga de enfermedad de células falciformes en África. [136] Un estudio indica que 20 000 bebés por año nacen con enfermedad de células falciformes, con el rasgo de células falciformes en el 13,3% y con la enfermedad en el 0,7%. [137]
El número de personas con la enfermedad en los Estados Unidos es de aproximadamente 100.000 (una de cada 3.300), y afecta principalmente a estadounidenses de ascendencia africana subsahariana. [138] En los Estados Unidos, aproximadamente uno de cada 365 niños afroamericanos y uno de cada 16.300 niños hispanoamericanos tienen anemia de células falciformes. [139] La esperanza de vida de los hombres con anemia falciforme es de aproximadamente 42 años, mientras que las mujeres viven aproximadamente seis años más. [140] Otros 2 millones son portadores del rasgo de células falciformes. [141] La mayoría de los bebés con anemia falciforme nacidos en los Estados Unidos se identifican mediante pruebas de detección neonatal de rutina. A partir de 2016, los 50 estados incluyen la detección de la enfermedad de células falciformes como parte de su detección neonatal. [142] Se toma una muestra de sangre del recién nacido a través de un pinchazo en el talón y se envía a un laboratorio para su análisis. El bebé debe haber estado comiendo durante un mínimo de 24 horas antes de que se pueda realizar la prueba del talón. Algunos estados también exigen que se realice un segundo análisis de sangre cuando el bebé tenga dos semanas de vida para garantizar los resultados. [143]
La anemia de células falciformes es el trastorno genético más común entre los afroamericanos. Aproximadamente el 8% son portadores y 1 de cada 375 nace con la enfermedad. [144] Los defensores de los pacientes de la enfermedad de células falciformes se han quejado de que recibe menos fondos gubernamentales y privados para la investigación que enfermedades raras similares, como la fibrosis quística , y el investigador Elliott Vichinsky dice que esto muestra discriminación racial o el papel de la riqueza en la defensa de la atención médica. [145] En general, sin considerar la raza, aproximadamente el 1,5% de los bebés nacidos en los Estados Unidos son portadores de al menos una copia del gen mutante (causante de la enfermedad). [146]

Como resultado del crecimiento de la población en las regiones africanas y caribeñas de ultramar de Francia y la inmigración desde el norte de África y África subsahariana a Francia continental, la enfermedad de células falciformes se ha convertido en un importante problema de salud en Francia. [147] La SCD se ha convertido en la enfermedad genética más común en el país, con una prevalencia general al nacer de uno en 2415 en Francia metropolitana , por delante de la fenilcetonuria (uno en 10 862), el hipotiroidismo congénito (uno en 3132), la hiperplasia suprarrenal congénita (uno en 19 008) y la fibrosis quística (uno en 5014) para el mismo período de referencia. [148]

Desde el año 2000, se ha realizado un cribado neonatal de la anemia drepanocítica a nivel nacional para todos los recién nacidos definidos como "en riesgo" de padecerla según su origen étnico (definidos como aquellos nacidos de padres originarios de África subsahariana, África del Norte, la zona mediterránea (sur de Italia, Grecia y Turquía ), la península Arábiga, las islas francesas de ultramar y el subcontinente indio). [149]
En el Reino Unido, se cree que entre 12.000 y 15.000 personas padecen la enfermedad de células falciformes [150] y se calcula que hay 250.000 portadores de la enfermedad solo en Inglaterra. Como el número de portadores es solo una estimación, a todos los recién nacidos en el Reino Unido se les realiza un análisis de sangre de rutina para detectar la enfermedad. [151] Debido a que muchos adultos en grupos de alto riesgo no saben si son portadores, a las mujeres embarazadas y a ambos miembros de la pareja se les ofrece la posibilidad de hacerse una prueba de detección para que puedan recibir asesoramiento si tienen el rasgo de células falciformes. [152] Además, a los donantes de sangre de aquellos en grupos de alto riesgo también se les realiza una prueba de detección para confirmar si son portadores y si su sangre se filtra correctamente. [153] A los donantes que se descubre que son portadores se les informa y su sangre, aunque a menudo se utiliza para aquellos del mismo grupo étnico, no se utiliza para aquellos con enfermedad de células falciformes que requieren una transfusión de sangre. [154]
En Arabia Saudita , aproximadamente el 4,2% de la población es portadora del gen de la anemia falciforme y el 0,26% tiene la enfermedad de células falciformes. La prevalencia más alta se encuentra en la provincia oriental, donde aproximadamente el 17% de la población es portadora del gen y el 1,2% tiene la enfermedad de células falciformes. [155] En 2005, Arabia Saudita introdujo una prueba prematrimonial obligatoria que incluía la electroforesis de HB, cuyo objetivo era reducir la incidencia de la anemia falciforme y la talasemia . [156]
En Bahréin , un estudio publicado en 1998 que abarcó a unas 56.000 personas en hospitales de Bahréin encontró que el 2% de los recién nacidos tienen anemia falciforme, el 18% de las personas encuestadas tienen el rasgo de anemia falciforme y el 24% eran portadores de la mutación genética que causa la enfermedad. [157] El país comenzó a realizar pruebas de detección a todas las mujeres embarazadas en 1992, y se empezó a realizar pruebas a los recién nacidos si la madre era portadora. En 2004, se aprobó una ley que exigía que las parejas que planeaban casarse se sometieran a asesoramiento prematrimonial gratuito . Estos programas fueron acompañados de campañas de educación pública. [158]
La enfermedad de células falciformes es común en algunos grupos étnicos de la India central, [159] donde la prevalencia ha oscilado entre el 9,4 y el 22,2% en las zonas endémicas de Madhya Pradesh , Rajasthan y Chhattisgarh . [160] También es endémica entre los tharu de Nepal y la India; sin embargo, tienen una tasa siete veces menor de malaria a pesar de vivir en una zona infestada de malaria. [161]
En Jamaica , el 10% de la población es portadora del gen de la anemia falciforme, lo que lo convierte en el trastorno genético más prevalente en el país. [162]
El primer informe moderno sobre la enfermedad de células falciformes puede haber sido en 1846, donde se discutió la autopsia de un esclavo fugitivo ejecutado; el hallazgo clave fue la ausencia del bazo. [163] [164] Según se informa, los esclavos africanos en los Estados Unidos mostraron resistencia a la malaria, pero eran propensos a las úlceras en las piernas. [164] Las características anormales de los glóbulos rojos, que más tarde prestaron su nombre a la enfermedad, fueron descritas por primera vez por Ernest E. Irons (1877-1959), interno del cardiólogo de Chicago y profesor de medicina James B. Herrick (1861-1954), en 1910. Irons vio células "peculiares alargadas y en forma de hoz" en la sangre de un hombre llamado Walter Clement Noel, un estudiante de odontología de primer año de 20 años de Granada. Noel había sido ingresado en el Hospital Presbiteriano de Chicago en diciembre de 1904 con anemia. [16] [165] Noel fue readmitido varias veces durante los siguientes tres años por " reumatismo muscular " y "ataques biliosos", pero completó sus estudios y regresó a la capital de Granada (St. George's) para ejercer la odontología . Murió de neumonía en 1916 y está enterrado en el cementerio católico de Sauteurs , en el norte de Granada. [16] [17] Poco después del informe de Herrick, apareció otro caso en el Virginia Medical Semi-Monthly con el mismo título, "Peculiar Elongated and Falke-Shaped Red Blood Corpuscles in a Case of Severe Anemia". [166] Este artículo se basa en un paciente ingresado en el Hospital de la Universidad de Virginia el 15 de noviembre de 1910. [167] En la descripción posterior de Verne Mason en 1922, se utiliza por primera vez el nombre "anemia de células falciformes". [17] [168] Los problemas infantiles relacionados con la enfermedad de células falciformes no se informaron hasta la década de 1930, a pesar del hecho de que esto no puede haber sido poco común en las poblaciones afroamericanas. [164]
El médico de Memphis Lemuel Diggs , un prolífico investigador de la enfermedad de células falciformes, introdujo por primera vez la distinción entre la enfermedad de células falciformes y el rasgo en 1933, aunque hasta 1949, las características genéticas no habían sido dilucidadas por James V. Neel y EA Beet. [17] 1949 fue el año en que Linus Pauling describió el comportamiento químico inusual de la hemoglobina S y lo atribuyó a una anomalía en la propia molécula. [17] [169] El cambio molecular en HbS fue descrito en 1956 por Vernon Ingram . [170] A finales de la década de 1940 y principios de la de 1950 se comprendió mejor el vínculo entre la malaria y la enfermedad de células falciformes. En 1954, la introducción de la electroforesis de hemoglobina permitió el descubrimiento de subtipos particulares, como la enfermedad HbSC. [17]
En los años 1970 y 1980 se introdujeron estudios de historia natural a gran escala y otros estudios de intervención, lo que condujo al uso generalizado de la profilaxis contra las infecciones neumocócicas, entre otras intervenciones. La película para televisión de Bill Cosby ganadora de un Emmy en 1972, To All My Friends on Shore , describía la historia de los padres de un niño con anemia de células falciformes. [171] En los años 1990 se desarrolló la hidroxicarbamida y en 2007 aparecieron informes de curación mediante trasplante de médula ósea. [17]
Algunos textos antiguos se refieren a ella como drepanocitosis. [172]
La enfermedad de células falciformes se considera con frecuencia una discapacidad. [173] A partir del 15 de septiembre de 2017, la Administración del Seguro Social de los EE. UU. emitió una Resolución de Interpretación de Políticas que proporciona información de fondo sobre la enfermedad de células falciformes y una descripción de cómo el Seguro Social evalúa la enfermedad durante su proceso de adjudicación de reclamos por discapacidad. [174] [175]
En los EE. UU., existen estigmas en torno a la anemia drepanocítica que desalientan a las personas con anemia drepanocítica a recibir la atención necesaria. Estos estigmas afectan principalmente a las personas de ascendencia afroamericana y latinoamericana, según el Instituto Nacional del Corazón, los Pulmones y la Sangre. [2] Las personas con anemia drepanocítica experimentan el impacto de los estigmas de la enfermedad en múltiples aspectos de la vida, incluido el bienestar social y psicológico. Los estudios han demostrado que las personas con anemia drepanocítica con frecuencia sienten que deben mantener su diagnóstico en secreto para evitar la discriminación en el lugar de trabajo y también entre pares en las relaciones. [176] En la década de 1960, el gobierno de los EE. UU. apoyó iniciativas para la detección de enfermedades genéticas en el lugar de trabajo en un intento de proteger a las personas con anemia drepanocítica. Al realizar esta detección, se pretendía que los empleados no se encontraran en entornos que pudieran ser potencialmente dañinos y desencadenar la anemia drepanocítica. [177]
Uganda tiene la quinta carga más alta de enfermedad de células falciformes (ECF) en el mundo. [178] En Uganda , existe un estigma social para aquellos con enfermedad de células falciformes debido a la falta de conocimiento general de la enfermedad. La brecha general en el conocimiento sobre la enfermedad de células falciformes se nota entre los adolescentes y adultos jóvenes debido al secreto culturalmente sancionado sobre la enfermedad. [178] Si bien la mayoría de las personas han oído hablar en general de la enfermedad, una gran parte de la población está relativamente mal informada sobre cómo se diagnostica o se hereda la ECF. Aquellos que están informados sobre la enfermedad se enteraron de ella por familiares o amigos y no por profesionales de la salud . El hecho de no proporcionar al público información sobre la enfermedad de células falciformes da como resultado una población con una comprensión deficiente de las causas de la enfermedad, los síntomas y las técnicas de prevención. [179] Las diferencias, físicas y sociales, que surgen en las personas con enfermedad de células falciformes, como ictericia, retraso del crecimiento físico y retraso de la madurez sexual, también pueden llevarlos a convertirse en blancos de acoso, rechazo y estigma. [178]
Los datos recopilados sobre la enfermedad de células falciformes en Uganda no se han actualizado desde principios de la década de 1970. La deficiencia de datos se debe a la falta de fondos gubernamentales para la investigación, a pesar de que los ugandeses mueren diariamente por anemia de células falciformes. [180] Los datos muestran que la frecuencia del rasgo de la enfermedad de células falciformes es del 20% de la población de Uganda. [180] Esto significa que 66 millones de personas corren el riesgo de tener un hijo con enfermedad de células falciformes. [180] También se estima que alrededor de 25.000 ugandeses nacen cada año con anemia de células falciformes y el 80% de esas personas no viven más allá de los cinco años. [180] La anemia de células falciformes también contribuye en un 25% a la tasa de mortalidad infantil en Uganda. [180] El pueblo bamba de Uganda, ubicado en el suroeste del país, es portador del 45% del gen, que es la frecuencia de rasgo más alta registrada en el mundo. [180] La Clínica de Anemia Falciforme en Mulago es la única clínica de esta enfermedad en el país y atiende en promedio a 200 pacientes por día. [180]
El estigma en torno a la enfermedad es particularmente grave en las regiones del país que no están tan afectadas. Por ejemplo, los ugandeses del este tienden a tener más conocimientos sobre la enfermedad que los ugandeses del oeste, que son más propensos a creer que la anemia falciforme es el resultado de un castigo de Dios o de la brujería . [181] Otros conceptos erróneos sobre la anemia falciforme incluyen la creencia de que es causada por factores ambientales, pero, en realidad, la anemia falciforme es una enfermedad genética. [182] Se han realizado esfuerzos en toda Uganda para abordar los conceptos erróneos sociales sobre la enfermedad. En 2013, se creó la Uganda Sickle Cell Rescue Foundation para difundir la conciencia sobre la anemia falciforme y combatir el estigma social asociado a la enfermedad. [183] Además de los esfuerzos de esta organización, es necesario incluir la educación sobre la anemia falciforme en los programas de educación sanitaria comunitaria preexistentes con el fin de reducir la estigmatización de la anemia falciforme en Uganda. [179]
El estigma profundamente arraigado de la anemia de células falciformes en la sociedad hace que las familias a menudo oculten el estado de enfermedad de sus familiares por miedo a ser etiquetados, maldecidos o excluidos de los eventos sociales. [184] A veces en Uganda, cuando se confirma que un miembro de la familia tiene anemia de células falciformes, se evitan las relaciones íntimas con todos los miembros de la familia. [184] La estigmatización y el aislamiento social que tienden a experimentar las personas con anemia de células falciformes es a menudo la consecuencia de conceptos erróneos populares de que las personas con anemia de células falciformes no deben socializar con personas libres de la enfermedad. Esta mentalidad priva a las personas con anemia de células falciformes del derecho a participar libremente en actividades comunitarias como todos los demás. [178] El estigma relacionado con la anemia de células falciformes y el aislamiento social en las escuelas, especialmente, pueden hacer que la vida de los jóvenes que viven con anemia de células falciformes sea extremadamente difícil. [178] Para los niños en edad escolar que viven con anemia de células falciformes, el estigma al que se enfrentan puede conducir al rechazo de los compañeros. [178] El rechazo de los compañeros implica la exclusión de grupos o reuniones sociales. Esto a menudo lleva a que el individuo excluido experimente angustia emocional y puede dar como resultado un bajo rendimiento académico, el rechazo a la escuela y un fracaso laboral más adelante en la vida. [178] Este aislamiento social también es probable que afecte negativamente la autoestima y la calidad de vida general de las personas con ECF . [178]
Las madres de niños con anemia falciforme tienden a recibir cantidades desproporcionadas de estigma por parte de sus pares y miembros de la familia. A menudo se culpa a estas mujeres por el diagnóstico de anemia falciforme de su hijo, especialmente si la anemia falciforme no está presente en generaciones anteriores, debido a la sospecha de que la mala salud del niño puede haber sido causada por el fracaso de la madre para implementar medidas de salud preventivas o promover un entorno saludable para que su hijo prospere. [182] La dependencia de teorías relacionadas con factores ambientales para culpar a la madre refleja el escaso conocimiento de muchos ugandeses sobre cómo se adquiere la enfermedad, ya que está determinada por la genética, no por el medio ambiente. [182] Las madres de niños con anemia falciforme también suelen quedarse con recursos muy limitados para salvaguardar su futuro contra el estigma de tener anemia falciforme. [182] Esta falta de acceso a los recursos es resultado de sus roles subordinados dentro de las estructuras familiares, así como de las disparidades de clase que obstaculizan la capacidad de muchas madres para satisfacer los costos y responsabilidades adicionales del cuidado infantil. [182]
Las mujeres que viven con anemia falciforme y quedan embarazadas a menudo enfrentan una discriminación extrema y desánimo en Uganda. Estas mujeres son frecuentemente tildadas por sus pares de irresponsables por tener un bebé mientras viven con enfermedad de células falciformes o incluso tener relaciones sexuales mientras viven con anemia de células falciformes. Carga del rasgo y la enfermedad de células falciformes en el Estudio de Vigilancia de la Anemia de Células Falciformes de Uganda (US3): un estudio transversal Las críticas y los juicios que reciben estas mujeres, no solo de los profesionales de la salud sino también de sus familias, a menudo las dejan sintiéndose solas, deprimidas, ansiosas, avergonzadas y con muy poco apoyo social . Carga del rasgo y la enfermedad de células falciformes en el Estudio de Vigilancia de la Anemia de Células Falciformes de Uganda (US3): un estudio transversal - The Lancet Global Health La mayoría de las mujeres embarazadas con anemia de células falciformes también se convierten en madres solteras, ya que es común que sus parejas masculinas las abandonen y aleguen que no sabían que su pareja tenía anemia de células falciformes. Padres de niños con anemia de células falciformes mal preparados y mal informados: es hora de repensar las campañas de concienciación El abandono que experimentan estas mujeres no solo les causa angustia emocional, sino que este bajo nivel de apoyo parental puede estar relacionado con síntomas depresivos y, en general, menor calidad de vida para el niño una vez nacido. [185]
En 2021, se descubrió que muchos pacientes tenían miedo de visitar los hospitales, tal era el nivel de ignorancia entre el personal, por lo que compraron analgésicos para tratarse fuera del NHS. A menudo esperaban mucho tiempo para recibir el alivio del dolor y, a veces, se sospechaba que tenían un comportamiento de "búsqueda de medicamentos". Los retrasos en el tratamiento, la falta de información al equipo de hematología del hospital y el mal manejo del dolor habían causado muertes. El personal de hematología especializado prefería trabajar en hospitales docentes más grandes, lo que provocó una escasez de experiencia en otros lugares. [186] En 2021, el NHS inició su primer tratamiento nuevo en 20 años para la anemia falciforme. Esto implicó el uso de Crizanlizumab , un medicamento que se administra mediante goteo transfusional, lo que reduce el número de visitas a urgencias de los pacientes. Se puede acceder al tratamiento, a través de consultores, en cualquiera de los diez nuevos centros establecidos en todo el país. [187] Sin embargo, ese mismo año, un grupo parlamentario de todos los partidos elaboró un informe sobre la anemia falciforme y la talasemia titulado "Nadie está escuchando". [188] En parte como respuesta a esto, el 19 de junio de 2022, Día Mundial de la Anemia Falciforme, el NHS lanzó una campaña llamada "¿Puedes decir que es anemia falciforme?". La campaña tenía un doble objetivo. Uno era aumentar la conciencia de los signos y síntomas clave de este trastorno sanguíneo para que las personas estuvieran tan alertas a los signos de una crisis de anemia falciforme como a un ataque cardíaco o un derrame cerebral inminente. El segundo objetivo era establecer un nuevo programa de capacitación para ayudar a los paramédicos, el personal de accidentes y emergencias, los cuidadores y el público en general a atender de manera efectiva a los pacientes en crisis. [189]
Las enfermedades como la anemia falciforme, en las que el fenotipo o la función celular normal de una persona pueden restaurarse en las células que padecen la enfermedad mediante una copia normal del gen que está mutado, pueden ser buenas candidatas para el tratamiento con terapia génica. No se conocen los riesgos y beneficios relacionados con la terapia génica para la anemia falciforme. [190]
En 2001, se informó que la enfermedad de células falciformes había sido tratada con éxito en ratones mediante terapia génica . [191] [192] Los investigadores utilizaron un vector viral para hacer que los ratones, que tienen esencialmente el mismo defecto que causa la enfermedad de células falciformes humana, expresaran la producción de hemoglobina fetal (HbF), que un individuo normalmente deja de producir poco después del nacimiento. En humanos, se sabe que el uso de hidroxiurea para estimular la producción de HbF alivia temporalmente los síntomas de la enfermedad de células falciformes. Los investigadores demostraron que este método de terapia génica es una forma más permanente de aumentar la producción terapéutica de HbF. [193]
En 2014 se iniciaron los ensayos clínicos de fase 1 de terapia génica para la anemia falciforme en humanos. Los ensayos clínicos evaluaron la seguridad de la médula ósea modificada con vectores lentivirales para adultos con anemia falciforme grave. [194] [195] En marzo de 2017 se publicó un informe de caso de la primera persona tratada, y desde entonces se ha tratado a algunas personas más. [196] [197]
Las plataformas de edición genética como CRISPR/Cas9 se han utilizado para corregir la mutación causante de la enfermedad en células madre hematopoyéticas extraídas de una persona con la afección. [198] En julio de 2019, la herramienta de edición genética CRISPR se utilizó para editar células de la médula ósea de una persona con SCD para aumentar la hemoglobina fetal inhibiendo el gen BCL11A . [199] [200] Varios investigadores han considerado las implicaciones éticas de que la SCD sea una de las primeras aplicaciones potenciales de la tecnología CRISPR, dados los abusos históricos y el abandono de la comunidad afroamericana por parte del campo médico. [201]
En 2017, doce ensayos clínicos se centraron en la terapia génica para tratar la anemia de células falciformes. De esos 12 ensayos, cuatro de ellos reemplazaron el gen HBB mutado por uno sano. Tres ensayos utilizaron Mozobil, un medicamento utilizado para tratar tipos de cáncer, para determinar si el aumento de células madre se puede utilizar para la terapia génica. Un ensayo se centró en analizar muestras de médula ósea de pacientes con anemia de células falciformes. Otro ensayo experimentó con el uso de sangre del cordón umbilical de bebés con y sin anemia de células falciformes para desarrollar una terapia génica. [202]
En noviembre de 2023, los reguladores del Reino Unido aprobaron un tratamiento genético que utiliza la herramienta de edición genética CRISPR para el tratamiento de la anemia de células falciformes y también para el trastorno sanguíneo beta talasemia dependiente de transfusiones . [13] [120]
Si bien el trasplante de sangre del cordón umbilical puede curar potencialmente la enfermedad, solo el 10% de las personas tienen un donante adecuado disponible. [203] Un trasplante de sangre del cordón umbilical no está exento de riesgos graves y se estima que el 7% de las personas mueren como resultado del procedimiento de trasplante de sangre del cordón umbilical y existe el riesgo de enfermedad de injerto contra huésped . [203]
{{cite journal}}: |last=tiene nombre genérico ( ayuda )Mantenimiento de CS1: nombres numéricos: lista de autores ( enlace )Penicilina profiláctica dos veces al día comenzando en la primera infancia y continuando hasta al menos los 5 años.
... equipos informan que dos estrategias para reparar directamente células sanguíneas defectuosas han mejorado drásticamente la salud de un puñado de personas con estas enfermedades genéticas.
{{cite news}}: CS1 maint: estado de la URL ( enlace ){{cite journal}}: CS1 maint: DOI inactivo a partir de junio de 2024 ( enlace )