La hemodiálisis , también escrita como hemodiálisis , o simplemente diálisis , es un proceso de filtración de la sangre de una persona cuyos riñones no funcionan con normalidad. Este tipo de diálisis consigue la eliminación extracorpórea de productos de desecho como la creatinina y la urea y el agua libre de la sangre cuando los riñones se encuentran en estado de insuficiencia renal . La hemodiálisis es una de las tres terapias de reemplazo renal (las otras dos son el trasplante de riñón y la diálisis peritoneal ). Un método alternativo para la separación extracorpórea de componentes sanguíneos como plasma o células es la aféresis .
La hemodiálisis puede ser una terapia ambulatoria o hospitalaria . La hemodiálisis de rutina se lleva a cabo en un centro de diálisis ambulatorio, ya sea en una sala especialmente diseñada en un hospital o en una clínica independiente y dedicada. Con menos frecuencia la hemodiálisis se realiza en casa . Los tratamientos de diálisis en una clínica son iniciados y gestionados por personal especializado formado por enfermeras y técnicos; Los tratamientos de diálisis en el hogar pueden ser iniciados y administrados por uno mismo o realizarse conjuntamente con la asistencia de un ayudante capacitado que generalmente es un miembro de la familia. [1]

La hemodiálisis es la opción de terapia de reemplazo renal para pacientes que necesitan diálisis de forma aguda y, para muchos pacientes, como terapia de mantenimiento. Proporciona una excelente y rápida eliminación de solutos. [2]
Un nefrólogo (un médico especialista en riñones) decide cuándo se necesita hemodiálisis y los diversos parámetros para un tratamiento de diálisis. Estos incluyen la frecuencia (cuántos tratamientos por semana), la duración de cada tratamiento y los caudales de sangre y solución de diálisis, así como el tamaño del dializador. En ocasiones, la composición de la solución de diálisis también se ajusta en cuanto a sus niveles de sodio, potasio y bicarbonato. En general, cuanto mayor sea el tamaño corporal de un individuo, más diálisis necesitará. En América del Norte y el Reino Unido , son típicos tratamientos de 3 a 4 horas (a veces hasta 5 horas para pacientes más grandes) administrados 3 veces por semana. Las sesiones de dos veces por semana se limitan a pacientes que tienen una función renal residual sustancial. A menudo se prescriben cuatro sesiones por semana para pacientes más grandes, así como para pacientes que tienen problemas con la sobrecarga de líquidos . Por último, existe un interés creciente por la hemodiálisis domiciliaria diaria de corta duración , que consiste en sesiones de 1,5 a 4 horas administradas de 5 a 7 veces por semana, generalmente en casa. También hay interés en la diálisis nocturna , que implica dializar a un paciente, generalmente en casa, durante 8 a 10 horas por noche, 3 a 6 noches por semana. También se ofrece diálisis nocturna en centros, 3 a 4 veces por semana, en un puñado de unidades de diálisis en los Estados Unidos .
La hemodiálisis a menudo implica la eliminación de líquidos (mediante ultrafiltración ), porque la mayoría de los pacientes con insuficiencia renal orinan poco o nada. Los efectos secundarios causados por eliminar demasiado líquido o eliminarlo demasiado rápido incluyen presión arterial baja , fatiga , dolores en el pecho, calambres en las piernas, náuseas y dolores de cabeza . Estos síntomas pueden ocurrir durante el tratamiento y pueden persistir después del tratamiento; A veces se les conoce colectivamente como resaca de diálisis o lavado de diálisis. La gravedad de estos síntomas suele ser proporcional a la cantidad y velocidad de eliminación del líquido. Sin embargo, el impacto de una determinada cantidad o velocidad de eliminación de líquido puede variar mucho de persona a persona y de un día a otro. Estos efectos secundarios se pueden evitar y/o disminuir su gravedad limitando la ingesta de líquidos entre tratamientos o aumentando la dosis de diálisis, por ejemplo, dializando con más frecuencia o más tiempo por tratamiento que el estándar tres veces por semana, de 3 a 4 horas por programa de tratamiento.
Dado que la hemodiálisis requiere acceso al sistema circulatorio, los pacientes sometidos a hemodiálisis pueden exponer su sistema circulatorio a microbios , lo que puede provocar bacteriemia , una infección que afecta las válvulas cardíacas ( endocarditis ) o una infección que afecta los huesos ( osteomielitis ). El riesgo de infección varía según el tipo de acceso utilizado (ver más abajo). También puede producirse sangrado; nuevamente, el riesgo varía según el tipo de acceso utilizado. Las infecciones se pueden minimizar siguiendo estrictamente las mejores prácticas de control de infecciones .
El desprendimiento de la aguja venosa (VND) es una complicación fatal de la hemodiálisis en la que el paciente experimenta una rápida pérdida de sangre debido a una conexión fallida de la aguja al punto de acceso venoso. [3]
La heparina no fraccionada (UHF) es el anticoagulante más utilizado en hemodiálisis, ya que generalmente se tolera bien y puede revertirse rápidamente con sulfato de protamina . Sin embargo, la heparina de bajo peso molecular (HBPM) se está volviendo cada vez más popular y actualmente es la norma en Europa occidental. [4] En comparación con la UHF, la HBPM tiene la ventaja de un modo de administración más fácil y un sangrado reducido, pero el efecto no se puede revertir fácilmente. [5] En raras ocasiones, la heparina puede causar un recuento bajo de plaquetas debido a una reacción llamada trombocitopenia inducida por heparina (TIH) . El riesgo de TIH es menor con HBPM que con UHF. En tales pacientes, se pueden utilizar anticoagulantes alternativos. Aunque la TIH causa un recuento bajo de plaquetas, paradójicamente puede predisponer a la trombosis. [6] Al comparar la UHF con la HBPM en cuanto al riesgo de efectos adversos, la evidencia no está clara en cuanto a qué enfoque de tratamiento para la sangre diluida tiene menos efectos secundarios y cuál es la estrategia de tratamiento ideal para prevenir los coágulos sanguíneos durante la hemodiálisis. [7] En pacientes con alto riesgo de hemorragia, la diálisis se puede realizar sin anticoagulación. [8]
El síndrome del primer uso es una reacción anafiláctica rara pero grave al riñón artificial . Sus síntomas incluyen estornudos, sibilancias, dificultad para respirar, dolor de espalda, dolor de pecho o muerte súbita. Puede ser causada por esterilizante residual en el riñón artificial o por el material de la propia membrana. En los últimos años, la incidencia del síndrome del primer uso ha disminuido debido a un mayor uso de irradiación gamma , esterilización con vapor o radiación por haz de electrones en lugar de esterilizantes químicos, y al desarrollo de nuevas membranas semipermeables de mayor biocompatibilidad . Siempre se deben considerar nuevos métodos de procesamiento de componentes de diálisis que antes eran aceptables. Por ejemplo, en 2008, se produjeron una serie de reacciones del tipo de primer uso, incluidas muertes, debido a la heparina contaminada durante el proceso de fabricación con sulfato de condroitina sobresulfatado . [9]
Las complicaciones a largo plazo de la hemodiálisis incluyen amiloidosis asociada a la hemodiálisis , neuropatía y diversas formas de enfermedades cardíacas . Se ha demostrado que aumentar la frecuencia y la duración de los tratamientos mejora la sobrecarga de líquidos y el agrandamiento del corazón que se observa comúnmente en estos pacientes. [10] [11]
La deficiencia de folato puede ocurrir en algunos pacientes sometidos a hemodiálisis. [12]
Aunque para la filtración de sangre se utiliza un líquido dializado, que es una solución que contiene electrolitos diluidos, la hemodiálisis puede provocar un desequilibrio electrolítico. Estos desequilibrios pueden derivar de concentraciones anormales de potasio ( hipopotasemia , hiperpotasemia ) y de sodio ( hiponatremia , hipernatremia ). Estos desequilibrios electrolíticos se asocian con una mayor mortalidad cardiovascular. [13]
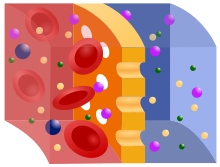
El principio de la hemodiálisis es el mismo que el de otros métodos de diálisis ; Implica la difusión de solutos a través de una membrana semipermeable. La hemodiálisis utiliza un flujo a contracorriente , donde el dializado fluye en la dirección opuesta al flujo sanguíneo en el circuito extracorpóreo . El flujo a contracorriente mantiene el gradiente de concentración a través de la membrana al máximo y aumenta la eficiencia de la diálisis.
La eliminación de líquido ( ultrafiltración ) se logra alterando la presión hidrostática del compartimento del dializado, lo que hace que el agua libre y algunos solutos disueltos se muevan a través de la membrana a lo largo de un gradiente de presión creado.
La solución de diálisis que se utiliza puede ser una solución esterilizada de iones minerales y se denomina dializado. La urea y otros productos de desecho, incluidos el potasio y el fosfato , se difunden en la solución de diálisis. Sin embargo, las concentraciones de sodio y cloruro son similares a las del plasma normal para evitar pérdidas. Se añade bicarbonato de sodio en una concentración más alta que el plasma para corregir la acidez de la sangre. También se suele utilizar una pequeña cantidad de glucosa. La concentración de electrolitos en el líquido de diálisis se ajusta según el estado del paciente antes de la diálisis. Si se añade una alta concentración de sodio al dializado, el paciente puede tener sed y acabar acumulando líquidos corporales, lo que puede provocar daños cardíacos. Por el contrario, las bajas concentraciones de sodio en la solución de diálisis se han asociado con una presión arterial baja y un aumento de peso intradiálisis, que son marcadores de mejores resultados. Sin embargo, los beneficios del uso de una baja concentración de sodio aún no han sido demostrados, ya que estos pacientes también pueden desarrollar calambres, hipotensión intradiálisis y niveles bajos de sodio en suero, síntomas asociados con un alto riesgo de mortalidad. [14]
Tenga en cuenta que este es un proceso diferente a la técnica relacionada de hemofiltración .

Se utilizan tres métodos principales para acceder a la sangre para hemodiálisis: un catéter intravenoso, una fístula arteriovenosa (AV) y un injerto sintético. El tipo de acceso está influenciado por factores como el curso temporal esperado de la insuficiencia renal de un paciente y el estado de su vasculatura. Los pacientes pueden tener múltiples procedimientos de acceso, generalmente porque una fístula o injerto AV está madurando y todavía se usa un catéter. La colocación de un catéter suele realizarse bajo sedación ligera, mientras que las fístulas y los injertos requieren operación.
Existen tres tipos de hemodiálisis: hemodiálisis convencional, hemodiálisis diaria y hemodiálisis nocturna. A continuación se muestra una adaptación y un resumen de un folleto del Hospital de Ottawa.

La hemodiálisis convencional generalmente se realiza tres veces por semana, durante aproximadamente tres a cuatro horas por cada tratamiento (a veces cinco horas para pacientes más grandes), durante el cual se extrae la sangre del paciente a través de un tubo a una velocidad de 200 a 400 ml/min. El tubo está conectado a una aguja de calibre 15, 16 o 17 insertada en la fístula o injerto de diálisis, o conectado a un puerto de un catéter de diálisis . Luego, la sangre se bombea a través del dializador y luego la sangre procesada se bombea de regreso al torrente sanguíneo del paciente a través de otro tubo (conectado a una segunda aguja o puerto). Durante el procedimiento, la presión arterial del paciente se controla de cerca y, si baja o el paciente desarrolla cualquier otro signo de bajo volumen sanguíneo, como náuseas, el asistente de diálisis puede administrar líquido adicional a través de la máquina. Durante el tratamiento, todo el volumen de sangre del paciente (aproximadamente 5000 cc) circula por la máquina cada 15 minutos. Durante este proceso, el paciente de diálisis está expuesto al agua equivalente a una semana para una persona promedio.
La hemodiálisis diaria suele ser utilizada por aquellos pacientes que realizan su propia diálisis en casa. Es menos estresante (más suave) pero requiere un acceso más frecuente. Esto es sencillo con catéteres, pero más problemático con fístulas o injertos. La "técnica del ojal" se puede utilizar para fístulas que requieren acceso frecuente. La hemodiálisis diaria generalmente se realiza durante 2 horas, seis días a la semana.
El procedimiento de hemodiálisis nocturna es similar a la hemodiálisis convencional excepto que se realiza de tres a seis noches a la semana y entre seis y diez horas por sesión mientras el paciente duerme. [15]

La máquina de hemodiálisis bombea la sangre del paciente y el dializado a través del dializador. [16] Las máquinas de diálisis más nuevas del mercado están altamente informatizadas y monitorean continuamente una serie de parámetros críticos para la seguridad, incluidos los caudales de sangre (QB) y dializado QD); [17] conductividad, temperatura y pH de la solución de diálisis; y análisis del dializado en busca de evidencia de fuga de sangre o presencia de aire. Cualquier lectura que esté fuera del rango normal activa una alarma audible para alertar al técnico de atención al paciente que está monitoreando al paciente. [18] Los fabricantes de máquinas de diálisis incluyen empresas como Nipro , Fresenius , Gambro , Baxter, B. Braun , NxStage y Bellco. [ cita necesaria ] Los caudales de QB a QD deben alcanzar una proporción de 1: 2, donde QB se establece en alrededor de 250 ml/min y QD se establece en alrededor de 500 ml/min para garantizar una buena eficiencia de la diálisis. [17]
Un amplio sistema de purificación de agua es fundamental para la hemodiálisis. Dado que los pacientes en diálisis están expuestos a grandes cantidades de agua, que se mezcla con concentrado de dializado para formar el dializado, incluso trazas de contaminantes minerales o endotoxinas bacterianas pueden filtrarse en la sangre del paciente. Debido a que los riñones dañados no pueden realizar su función prevista de eliminar impurezas, las moléculas introducidas en el torrente sanguíneo a partir del agua purificada incorrectamente pueden acumularse hasta niveles peligrosos, causando numerosos síntomas o la muerte. El aluminio , el cloro y/o las cloraminas , el fluoruro , el cobre y el zinc , así como los fragmentos bacterianos y las endotoxinas , han causado problemas a este respecto.
Por este motivo, el agua utilizada en hemodiálisis se purifica cuidadosamente antes de su uso. Un sistema de purificación de agua común incluye un sistema de múltiples etapas.
Primero se ablanda el agua. Luego, el agua pasa por un tanque que contiene carbón activado para adsorber contaminantes orgánicos, cloro y cloraminas. Luego se puede ajustar la temperatura del agua si es necesario. Luego, la purificación primaria se realiza forzando el agua a través de una membrana con poros muy pequeños, la llamada membrana de ósmosis inversa . Esto deja pasar el agua, pero retiene incluso los solutos muy pequeños, como los electrolitos. La eliminación final de los electrolitos sobrantes se realiza en algunos sistemas de agua haciendo pasar el agua a través de un dispositivo de electrodosionización (EDI), que elimina los aniones o cationes sobrantes y los reemplaza con iones de hidroxilo e hidrógeno, respectivamente, dejando agua ultrapura.
Incluso este grado de purificación del agua puede resultar insuficiente. La tendencia últimamente es hacer pasar esta agua purificada final (tras mezclarla con concentrado de dializado) a través de una membrana de ultrafiltración o filtro absoluto. Esto proporciona otra capa de protección al eliminar las impurezas, especialmente aquellas de origen bacteriano, que pueden haberse acumulado en el agua después de su paso por el sistema de purificación de agua original.

Una vez purificada el agua se mezcla con el dializado (también llamado líquido de diálisis) concentrado compuesto por: sodio , potasio , calcio , magnesio y dextrosa mezclados en una solución ácida; esta solución se mezcla con agua purificada y un tampón químico . Esto forma la solución de dializado, que contiene los electrolitos básicos que se encuentran en la sangre humana. Esta solución de dializado contiene iones cargados que conducen la electricidad. Durante la diálisis, la conductividad de la solución de diálisis se controla continuamente para garantizar que el agua y el concentrado de dializado se mezclen en las proporciones adecuadas. Tanto la solución de diálisis excesivamente concentrada como la solución excesivamente diluida pueden causar problemas clínicos graves. Alternativamente, se pueden agregar tampones químicos como bicarbonato o lactato para regular el pH del dializado. Ambos tampones pueden estabilizar el pH de la solución a un nivel fisiológico sin impactos negativos para el paciente. Existe cierta evidencia de una reducción en la incidencia de problemas cardíacos y sanguíneos y eventos de presión arterial alta cuando se usa bicarbonato como amortiguador de pH en comparación con el lactato. Sin embargo, las tasas de mortalidad después de utilizar ambos amortiguadores no muestran una diferencia significativa. [19]
El dializador es el equipo que filtra la sangre. Casi todos los dializadores que se utilizan hoy en día son del tipo de fibra hueca. Un haz cilíndrico de fibras huecas, cuyas paredes están compuestas por una membrana semipermeable, está anclado en cada extremo a un compuesto para macetas (una especie de pegamento). Luego, este conjunto se coloca en una carcasa cilíndrica de plástico transparente con cuatro aberturas. Una abertura o puerto de sangre en cada extremo del cilindro se comunica con cada extremo del haz de fibras huecas. Éste forma el "compartimento de sangre" del dializador. Otros dos puertos están cortados en el costado del cilindro. Estos se comunican con el espacio alrededor de las fibras huecas, el "compartimento de dializado". La sangre se bombea a través de los puertos sanguíneos a través de este haz de tubos capilares muy delgados , y el dializado se bombea a través del espacio que rodea las fibras. Se aplican gradientes de presión cuando es necesario para mover el líquido desde la sangre al compartimento del dializado.
Las membranas del dializador vienen con diferentes tamaños de poro. Aquellos con un tamaño de poro más pequeño se denominan "de bajo flujo" y aquellos con tamaños de poro más grandes se denominan "de alto flujo". Algunas moléculas más grandes, como la beta-2-microglobulina, no se eliminan en absoluto con los dializadores de bajo flujo; Últimamente la tendencia ha sido utilizar dializadores de alto flujo. Sin embargo, dichos dializadores requieren máquinas de diálisis más nuevas y una solución de diálisis de alta calidad para controlar adecuadamente la velocidad de eliminación de líquido y evitar el reflujo de impurezas de la solución de diálisis hacia el paciente a través de la membrana.
Las membranas de los dializadores solían estar hechas principalmente de celulosa (derivada de la fibra de algodón). La superficie de tales membranas no era muy biocompatible, porque los grupos hidroxilo expuestos activarían el complemento en la sangre que pasaba a través de la membrana. Por lo tanto, se modificó la membrana de celulosa básica "no sustituida". Un cambio fue cubrir estos grupos hidroxilo con grupos acetato (acetato de celulosa); otra fue mezclar algunos compuestos que inhibirían la activación del complemento en la superficie de la membrana (celulosa modificada). Las membranas originales de "celulosa no sustituida" ya no se utilizan ampliamente, mientras que todavía se utilizan acetato de celulosa y dializadores de celulosa modificados. Las membranas celulósicas se pueden fabricar en configuración de flujo bajo o alto, dependiendo del tamaño de sus poros.
Otro grupo de membranas está fabricado a partir de materiales sintéticos, utilizando polímeros como poliariletersulfona , poliamida , polivinilpirrolidona , policarbonato y poliacrilonitrilo . Estas membranas sintéticas activan el complemento en menor grado que las membranas de celulosa no sustituidas. Sin embargo, en general son más hidrofóbicos, lo que conduce a una mayor adsorción de proteínas en la superficie de la membrana, lo que a su vez puede conducir a la activación del sistema del complemento. [20] [21] Las membranas sintéticas se pueden fabricar en configuración de flujo alto o bajo, pero la mayoría son de alto flujo.
La nanotecnología se utiliza en algunas de las membranas de alto flujo más recientes para crear un tamaño de poro uniforme. El objetivo de las membranas de alto flujo es dejar pasar moléculas relativamente grandes como la beta-2-microglobulina (PM 11.600 daltons), pero no pasar albúmina (PM ~66.400 daltons). Cada membrana tiene poros en una variedad de tamaños. A medida que aumenta el tamaño de los poros, algunos dializadores de alto flujo comienzan a dejar pasar la albúmina de la sangre al dializado. Se cree que esto es indeseable, aunque una escuela de pensamiento sostiene que eliminar algo de albúmina puede ser beneficioso en términos de eliminación de toxinas urémicas unidas a proteínas.
Es algo controvertido si el uso de un dializador de alto flujo mejora los resultados de los pacientes, pero varios estudios importantes han sugerido que tiene beneficios clínicos. El ensayo HEMO, financiado por los NIH, comparó la supervivencia y las hospitalizaciones en pacientes asignados al azar a diálisis con membranas de bajo o alto flujo. Aunque el resultado primario (mortalidad por todas las causas) no alcanzó significación estadística en el grupo asignado al azar para usar membranas de alto flujo, varios resultados secundarios fueron mejores en el grupo de alto flujo. [22] [23] Un análisis Cochrane reciente concluyó que aún no se ha demostrado el beneficio de la elección de la membrana en los resultados. [24] Un ensayo colaborativo aleatorizado realizado en Europa, el estudio MPO (Membrane Permeabilities Outcomes), [25] que comparó la mortalidad en pacientes que recién iniciaban diálisis usando membranas de alto flujo o de bajo flujo, encontró una tendencia no significativa a una mejor supervivencia en aquellos que usaban membranas de alto flujo o de bajo flujo. membranas de alto flujo y un beneficio de supervivencia en pacientes con niveles de albúmina sérica más bajos o en diabéticos.
Las membranas de diálisis de alto flujo y/o la hemodiafiltración interna intermitente en línea (iHDF) también pueden ser beneficiosas para reducir las complicaciones de la acumulación de beta-2-microglobulina. Debido a que la beta-2-microglobulina es una molécula grande, con un peso molecular de aproximadamente 11.600 daltons, no pasa en absoluto a través de las membranas de diálisis de bajo flujo. Beta-2-M se elimina con diálisis de alto flujo, pero se elimina aún más eficientemente con IHDF. Después de varios años (por lo general, al menos 5 a 7), los pacientes en hemodiálisis comienzan a desarrollar complicaciones por la acumulación de beta-2-M, incluido el síndrome del túnel carpiano, quistes óseos y depósitos de este amiloide en las articulaciones y otros tejidos. La amiloidosis beta-2-M puede causar complicaciones muy graves, incluida la espondiloartropatía , y a menudo se asocia con problemas en las articulaciones del hombro. Estudios observacionales de Europa y Japón han sugerido que el uso de membranas de alto flujo en modo de diálisis, o IHDF, reduce las complicaciones beta-2-M en comparación con la diálisis regular que utiliza una membrana de bajo flujo. [26] [27] [28] [29] [30]
Los dializadores vienen en muchos tamaños diferentes. Un dializador más grande con un área de membrana más grande (A) generalmente eliminará más solutos que un dializador más pequeño, especialmente a velocidades de flujo sanguíneo altas. Esto también depende del coeficiente de permeabilidad de la membrana K 0 para el soluto en cuestión. Por lo tanto, la eficiencia del dializador generalmente se expresa como K 0 A , el producto del coeficiente de permeabilidad y el área. La mayoría de los dializadores tienen áreas superficiales de membrana de 0,8 a 2,2 metros cuadrados y valores de K 0 A que oscilan entre aproximadamente 500 y 1500 ml/min. K 0 A , expresada en ml/min, puede considerarse como el aclaramiento máximo de un dializador a velocidades de flujo de sangre y de dializado muy altas.
El dializador puede desecharse después de cada tratamiento o reutilizarse. La reutilización requiere un extenso procedimiento de desinfección de alto nivel. Los dializadores reutilizados no se comparten entre pacientes. Hubo una controversia inicial sobre si la reutilización de dializadores empeoraba los resultados de los pacientes. El consenso actual es que la reutilización de dializadores, si se hace cuidadosa y adecuadamente, produce resultados similares a los de un solo uso. [31]
La reutilización del dializador es una práctica que existe desde la invención del producto. Esta práctica incluye la limpieza de un dializador usado para reutilizarlo varias veces para el mismo paciente. Las clínicas de diálisis reutilizan los dializadores para ser más económicos y reducir los altos costos de la diálisis de "un solo uso", que puede ser extremadamente costosa y derrochadora. Los dializadores de un solo uso se inician una sola vez y luego se desechan, generando una gran cantidad de desechos biomédicos sin piedad por el ahorro de costos. Si se hace correctamente, la reutilización del dializador puede ser muy segura para los pacientes en diálisis.
Existen dos formas de reutilizar los dializadores, manual y automatizada. La reutilización manual implica la limpieza manual de un dializador. El dializador se desmonta parcialmente y luego se lava repetidamente antes de enjuagarlo con agua. Luego se almacena con un desinfectante líquido (PAA) durante más de 18 horas hasta su próximo uso. Aunque muchas clínicas fuera de EE. UU. utilizan este método, algunas clínicas están cambiando hacia un proceso más automatizado/simplificado a medida que avanza la práctica de diálisis. El método más nuevo de reutilización automatizada se logra mediante un dispositivo médico que comenzó a principios de los años 1980. Estos dispositivos son beneficiosos para las clínicas de diálisis que practican la reutilización, especialmente para entidades clínicas de diálisis grandes, porque permiten varios ciclos consecutivos por día. Primero, un técnico realiza una limpieza previa del dializador y luego una máquina lo limpia automáticamente mediante un proceso de ciclos por pasos hasta que finalmente se llena con desinfectante líquido para su almacenamiento. Aunque la reutilización automatizada es más efectiva que la reutilización manual, la tecnología más nueva ha provocado aún más avances en el proceso de reutilización. Cuando se reutiliza más de 15 veces con la metodología actual, el dializador puede perder B2m, el aclaramiento de la molécula media y la integridad de la estructura de los poros de las fibras, lo que tiene el potencial de reducir la efectividad de la sesión de diálisis del paciente. Actualmente, a partir de 2010, una tecnología de reprocesamiento más nueva y avanzada ha demostrado la capacidad de eliminar por completo el proceso de limpieza previa manual y también ha demostrado el potencial de regenerar (restaurar completamente) todas las funciones de un dializador a niveles que son aproximadamente equivalentes a un solo dializador. -uso durante más de 40 ciclos. [32] A medida que las tasas de reembolso médico comienzan a caer aún más, muchas clínicas de diálisis continúan operando eficazmente con programas de reutilización, especialmente porque el proceso es más fácil y simplificado que antes.
La hemodiálisis fue uno de los procedimientos más comunes realizados en los hospitales de EE. UU. en 2011, con 909.000 estancias (una tasa de 29 estancias por 10.000 habitantes). Esto supuso un aumento del 68 por ciento con respecto a 1997, cuando hubo 473.000 estancias. Fue el quinto procedimiento más común en pacientes de 45 a 64 años. [33]
Muchos han desempeñado un papel en el desarrollo de la diálisis como tratamiento práctico para la insuficiencia renal, empezando por Thomas Graham de Glasgow , quien presentó por primera vez los principios del transporte de solutos a través de una membrana semipermeable en 1854. [34] El riñón artificial fue desarrollado por primera vez por Abel , Rountree y Turner en 1913, [35] la primera hemodiálisis en un ser humano fue realizada por Haas (28 de febrero de 1924) [36] y Kolff desarrolló el riñón artificial hasta convertirlo en un aparato clínicamente útil entre 1943 y 1945. [37] Esta investigación demostró que la vida podría prolongarse en pacientes que mueren por insuficiencia renal .
Willem Kolff fue el primero en construir un dializador funcional en 1943. La primera paciente tratada con éxito fue una mujer de 67 años en coma urémico que recuperó la conciencia después de 11 horas de hemodiálisis con el dializador de Kolff en 1945. En el momento de su creación, El objetivo de Kolff era brindar soporte vital durante la recuperación de una insuficiencia renal aguda. Después de que terminó la Segunda Guerra Mundial , Kolff donó los cinco dializadores que había fabricado a hospitales de todo el mundo, incluido el Hospital Mount Sinai de Nueva York . Kolff entregó un conjunto de planos para su máquina de hemodiálisis a George Thorn en el Hospital Peter Bent Brigham de Boston . Esto llevó a la fabricación de la próxima generación del dializador Kolff, una máquina de diálisis Kolff-Brigham de acero inoxidable .
Según McKellar (1999), el cirujano canadiense Gordon Murray hizo una contribución significativa a las terapias renales con la ayuda de dos médicos, un estudiante universitario de química y personal de investigación. El trabajo de Murray se llevó a cabo simultánea e independientemente del de Kolff. El trabajo de Murray condujo al primer riñón artificial construido con éxito en América del Norte en 1945-1946, que se utilizó con éxito para tratar a una mujer de 26 años que salía de un coma urémico en Toronto. El dializador "Murray-Roschlau" de segunda generación, menos tosco y más compacto, se inventó en 1952-53, cuyos diseños fueron robados por el inmigrante alemán Erwin Halstrup y hecho pasar como propio (el "riñón artificial Halstrup-Baumann") . [38]
En la década de 1950, la invención del dializador de Willem Kolff se utilizó para la insuficiencia renal aguda, pero no se consideró un tratamiento viable para pacientes con enfermedad renal crónica (ERC) en etapa 5. En ese momento, los médicos creían que era imposible que los pacientes recibieran diálisis de forma indefinida por dos razones. En primer lugar, pensaban que ningún dispositivo fabricado por el hombre podría sustituir la función de los riñones a largo plazo. Además, un paciente sometido a diálisis desarrolló venas y arterias dañadas, por lo que después de varios tratamientos, resultó difícil encontrar un vaso para acceder a la sangre del paciente.
El riñón de Kolff original no fue muy útil clínicamente porque no permitía la eliminación del exceso de líquido. El profesor sueco Nils Alwall [39] encerró una versión modificada de este riñón dentro de un recipiente de acero inoxidable, al que se podía aplicar una presión negativa, efectuando de esta manera la primera aplicación verdaderamente práctica de la hemodiálisis, que se realizó en 1946 en la Universidad de Lund . Podría decirse que Alwall también fue el inventor de la derivación arteriovenosa para diálisis. Informó esto por primera vez en 1948, cuando utilizó una derivación arteriovenosa en conejos. Posteriormente, utilizó tales derivaciones, hechas de vidrio, así como su dializador encerrado en un recipiente, para tratar a 1.500 pacientes con insuficiencia renal entre 1946 y 1960, como informó en el Primer Congreso Internacional de Nefrología celebrado en Evian en septiembre de 1960. Alwall fue designado para una recién creada Cátedra de Nefrología en la Universidad de Lund en 1957. Posteriormente, colaboró con el empresario sueco Holger Crafoord para fundar una de las empresas clave que fabricarían equipos de diálisis en los últimos 50 años, Gambro . Stanley Shaldon ha revisado la historia temprana de la diálisis . [40]
Belding H. Scribner , en colaboración con el ingeniero biomecánico Wayne Quinton , modificó las derivaciones de vidrio utilizadas por Alwall haciéndolas de teflón . Otra mejora clave fue conectarlos a un trozo corto de tubo de elastómero de silicona. Esto formó la base de la llamada derivación de Scribner, quizás más propiamente llamada derivación de Quinton-Scribner. Después del tratamiento, el acceso circulatorio se mantendría abierto conectando los dos tubos fuera del cuerpo usando un pequeño tubo de teflón en forma de U, que desviaría la sangre del tubo en la arteria de regreso al tubo en la vena. [41]
En 1962, Scribner puso en marcha el primer centro de diálisis para pacientes ambulatorios del mundo, el Seattle Artificial Kidney Center, que más tarde pasó a llamarse Northwest Kidney Centers . Inmediatamente surgió el problema de quién debía recibir diálisis, ya que la demanda excedía con creces la capacidad de las seis máquinas de diálisis del centro. Scribner decidió que él no tomaría la decisión sobre quién recibiría diálisis y quién no. En cambio, las decisiones las tomaría un comité anónimo, que podría considerarse como uno de los primeros comités de bioética .
Para conocer una historia detallada de los intentos exitosos y fallidos de diálisis, incluidos pioneros como Abel y Roundtree, Haas y Necheles, consulte esta reseña de Kjellstrand. [42]