Un axón (del griego ἄξων áxōn , eje) o fibra nerviosa (o fibra nerviosa : véanse las diferencias ortográficas ) es una proyección larga y delgada de una célula nerviosa, o neurona , en los vertebrados , que normalmente conduce impulsos eléctricos conocidos como potenciales de acción lejos de el cuerpo de las células nerviosas . La función del axón es transmitir información a diferentes neuronas, músculos y glándulas. En determinadas neuronas sensoriales ( neuronas pseudounipolares ), como las del tacto y el calor, los axones se denominan fibras nerviosas aferentes y el impulso eléctrico viaja a lo largo de ellas desde la periferia hasta el cuerpo celular y desde el cuerpo celular hasta la médula espinal a lo largo de otra rama. del mismo axón. La disfunción axónica puede ser la causa de muchos trastornos neurológicos hereditarios y adquiridos que afectan tanto a las neuronas periféricas como a las centrales . Las fibras nerviosas se clasifican en tres tipos: fibras nerviosas del grupo A , fibras nerviosas del grupo B y fibras nerviosas del grupo C. Los grupos A y B están mielinizados y el grupo C no está mielinizado. Estos grupos incluyen tanto fibras sensoriales como fibras motoras. Otra clasificación agrupa únicamente las fibras sensoriales como Tipo I, Tipo II, Tipo III y Tipo IV.
Un axón es uno de los dos tipos de protuberancias citoplasmáticas del cuerpo celular de una neurona; el otro tipo es una dendrita . Los axones se distinguen de las dendritas por varias características, incluida la forma (las dendritas a menudo se estrechan mientras que los axones generalmente mantienen un radio constante), la longitud (las dendritas están restringidas a una pequeña región alrededor del cuerpo celular, mientras que los axones pueden ser mucho más largos) y la función (las dendritas reciben señales mientras que los axones las transmiten). Algunos tipos de neuronas no tienen axón y transmiten señales desde sus dendritas. En algunas especies, los axones pueden emanar de dendritas conocidas como dendritas portadoras de axones. [1] Ninguna neurona tiene nunca más de un axón; sin embargo, en invertebrados como insectos o sanguijuelas, el axón a veces consta de varias regiones que funcionan más o menos independientemente unas de otras. [2]
Los axones están cubiertos por una membrana conocida como axolema ; el citoplasma de un axón se llama axoplasma . La mayoría de los axones se ramifican, en algunos casos de forma muy abundante. Las ramas terminales de un axón se llaman telodendrias . El extremo hinchado de un telodendro se conoce como terminal del axón y se une a la dendrita o cuerpo celular de otra neurona formando una conexión sináptica . Los axones hacen contacto con otras células (generalmente otras neuronas, pero a veces células musculares o glandulares) en uniones llamadas sinapsis . En algunas circunstancias, el axón de una neurona puede formar una sinapsis con las dendritas de la misma neurona, lo que resulta en una autapsis . En una sinapsis, la membrana del axón está muy unida a la membrana de la célula diana y estructuras moleculares especiales sirven para transmitir señales eléctricas o electroquímicas a través de la brecha. Algunas uniones sinápticas aparecen a lo largo de un axón a medida que se extiende; éstas se denominan sinapsis de paso ("de paso") y pueden ser cientos o incluso miles a lo largo de un axón. [3] Otras sinapsis aparecen como terminales en los extremos de las ramas axonales.
Un solo axón, con todas sus ramas juntas, puede apuntar a múltiples partes del cerebro y generar miles de terminales sinápticas. Un haz de axones forma un tracto nervioso en el sistema nervioso central [4] y un fascículo en el sistema nervioso periférico . En los mamíferos placentarios , el tracto de materia blanca más grande del cerebro es el cuerpo calloso , formado por unos 200 millones de axones en el cerebro humano . [4]
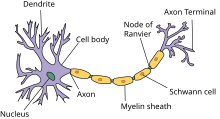

Los axones son las principales líneas de transmisión del sistema nervioso y, como haces, forman los nervios . Algunos axones pueden extenderse hasta un metro o más, mientras que otros se extienden tan solo un milímetro. Los axones más largos del cuerpo humano son los del nervio ciático , que van desde la base de la médula espinal hasta el dedo gordo de cada pie. El diámetro de los axones también es variable. La mayoría de los axones individuales tienen un diámetro microscópico (normalmente alrededor de un micrómetro (μm) de ancho). Los axones de los mamíferos más grandes pueden alcanzar un diámetro de hasta 20 µm. El axón gigante del calamar , que está especializado en conducir señales muy rápidamente, tiene cerca de 1 milímetro de diámetro, el tamaño de una pequeña mina de lápiz. El número de telodendrios axonales (las estructuras ramificadas al final del axón) también puede diferir de una fibra nerviosa a otra. Los axones del sistema nervioso central (SNC) suelen mostrar múltiples telodendros, con muchos puntos finales sinápticos. En comparación, el axón de las células granulares del cerebelo se caracteriza por un único nódulo ramificado en forma de T desde el cual se extienden dos fibras paralelas . La ramificación elaborada permite la transmisión simultánea de mensajes a una gran cantidad de neuronas objetivo dentro de una sola región del cerebro.
Hay dos tipos de axones en el sistema nervioso: axones mielinizados y axones amielinizados . [5] La mielina es una capa de una sustancia grasa aislante, que está formada por dos tipos de células gliales : células de Schwann y oligodendrocitos . En el sistema nervioso periférico, las células de Schwann forman la vaina de mielina de un axón mielinizado. Los oligodendrocitos forman la mielina aislante en el SNC. A lo largo de las fibras nerviosas mielinizadas, se producen espacios en la vaina de mielina conocidos como nódulos de Ranvier a intervalos uniformemente espaciados. La mielinización permite un modo especialmente rápido de propagación del impulso eléctrico llamado conducción saltatoria .
Los axones mielinizados de las neuronas corticales forman la mayor parte del tejido neural llamado materia blanca en el cerebro. La mielina da el aspecto blanco al tejido en contraste con la materia gris de la corteza cerebral que contiene los cuerpos celulares neuronales. Una disposición similar se ve en el cerebelo . Los haces de axones mielinizados forman los tractos nerviosos del SNC. Cuando estos tractos cruzan la línea media del cerebro para conectar regiones opuestas, se denominan comisuras . El mayor de ellos es el cuerpo calloso que conecta los dos hemisferios cerebrales , y tiene alrededor de 20 millones de axones. [4]
Se considera que la estructura de una neurona consta de dos regiones funcionales o compartimentos separados: el cuerpo celular junto con las dendritas como una región y la región axonal como la otra.
La región o compartimento axonal incluye el montículo del axón, el segmento inicial, el resto del axón, los telodendros del axón y las terminales del axón. También incluye la vaina de mielina. Los cuerpos de Nissl que producen las proteínas neuronales están ausentes en la región axonal. [3] Las proteínas necesarias para el crecimiento del axón y la eliminación de materiales de desecho necesitan una estructura para el transporte. Este transporte axonal se realiza en el axoplasma mediante disposiciones de microtúbulos y filamentos intermedios conocidos como neurofilamentos .

El montículo del axón es el área formada a partir del cuerpo celular de la neurona a medida que se extiende para convertirse en el axón. Precede al segmento inicial. Los potenciales de acción recibidos que se suman en la neurona se transmiten al montículo del axón para generar un potencial de acción a partir del segmento inicial.
El segmento inicial axonal (AIS) es un microdominio estructural y funcionalmente separado del axón. [6] [7] Una función del segmento inicial es separar la parte principal de un axón del resto de la neurona; otra función es ayudar a iniciar potenciales de acción. [8] Ambas funciones respaldan la polaridad de las células neuronales , en la que las dendritas (y, en algunos casos, el soma ) de una neurona reciben señales de entrada en la región basal, y en la región apical el axón de la neurona proporciona señales de salida. [9]
El segmento inicial del axón no está mielinizado y contiene un complejo especializado de proteínas. Tiene aproximadamente entre 20 y 60 µm de longitud y funciona como el sitio de iniciación del potencial de acción. [10] [11] Tanto la posición en el axón como la longitud del AIS pueden cambiar mostrando un grado de plasticidad que puede afinar la producción neuronal. [10] [12] Un AIS más largo se asocia con una mayor excitabilidad. [12] La plasticidad también se ve en la capacidad del AIS para cambiar su distribución y mantener la actividad de los circuitos neuronales en un nivel constante. [13]
El AIS está altamente especializado en la conducción rápida de impulsos nerviosos . Esto se logra mediante una alta concentración de canales de sodio dependientes de voltaje en el segmento inicial donde se inicia el potencial de acción. [13] Los canales iónicos van acompañados de una gran cantidad de moléculas de adhesión celular y proteínas de andamio que los anclan al citoesqueleto. [10] Las interacciones con ankyrin-G son importantes ya que es el principal organizador en el AIS. [10]
El axoplasma es el equivalente al citoplasma de la célula. Los microtúbulos se forman en el axoplasma en el montículo del axón. Están dispuestos a lo largo del axón, en secciones superpuestas, y todos apuntan en la misma dirección: hacia las terminales del axón. [14] Esto se nota por las terminaciones positivas de los microtúbulos. Esta disposición superpuesta proporciona las rutas para el transporte de diferentes materiales desde el cuerpo celular. [14] Los estudios sobre el axoplasma han demostrado que se observa el movimiento de numerosas vesículas de todos los tamaños a lo largo de los filamentos del citoesqueleto (los microtúbulos y los neurofilamentos ) en ambas direcciones entre el axón y sus terminales y el cuerpo celular.
El transporte anterógrado saliente desde el cuerpo celular a lo largo del axón transporta mitocondrias y proteínas de membrana necesarias para el crecimiento hasta la terminal del axón. El transporte retrógrado entrante transporta materiales de desecho celular desde el terminal del axón hasta el cuerpo celular. [15] Las vías salientes y entrantes utilizan diferentes conjuntos de proteínas motoras . [14] El transporte de salida lo proporciona la kinesina y el tráfico de regreso de entrada lo proporciona la dineína . La dineína está dirigida hacia el extremo negativo. [15] Hay muchas formas de proteínas motoras cinesina y dineína, y se cree que cada una lleva una carga diferente. [14] Los estudios sobre el transporte en el axón llevaron a la denominación de la cinesina. [14]


En el sistema nervioso, los axones pueden estar mielinizados o amielinizados. Se trata de la provisión de una capa aislante, llamada vaina de mielina. La membrana de mielina es única por su proporción relativamente alta de lípidos y proteínas. [dieciséis]
En el sistema nervioso periférico los axones están mielinizados por células gliales conocidas como células de Schwann . En el sistema nervioso central la vaina de mielina la proporciona otro tipo de célula glial, el oligodendrocito . Las células de Schwann mielinizan un solo axón. Un oligodendrocito puede mielinizar hasta 50 axones. [17]
La composición de la mielina es diferente en los dos tipos. En el SNC, la principal proteína de mielina es la proteína proteolípida , y en el SNP, es la proteína básica de mielina .
Los nodos de Ranvier (también conocidos como espacios de la vaina de mielina ) son segmentos cortos amielínicos de un axón mielinizado , que se encuentran periódicamente intercalados entre segmentos de la vaina de mielina. Por tanto, en el punto del nódulo de Ranvier, el axón tiene un diámetro reducido. [18] Estos nodos son áreas donde se pueden generar potenciales de acción. En la conducción saltatoria , las corrientes eléctricas producidas en cada nodo de Ranvier se conducen con poca atenuación al siguiente nodo de la línea, donde permanecen lo suficientemente fuertes como para generar otro potencial de acción. Así, en un axón mielinizado, los potenciales de acción "saltan" efectivamente de un nódulo a otro, evitando los tramos mielinizados intermedios, lo que da como resultado una velocidad de propagación mucho más rápida de la que puede sostener incluso el axón amielínico más rápido.
Un axón puede dividirse en muchas ramas llamadas telodendria (en griego, "final del árbol"). Al final de cada telodendro hay una terminal de axón (también llamada botón sináptico o botón terminal). Las terminales de los axones contienen vesículas sinápticas que almacenan el neurotransmisor para su liberación en la sinapsis . Esto hace posibles múltiples conexiones sinápticas con otras neuronas. A veces, el axón de una neurona puede hacer sinapsis con las dendritas de la misma neurona, lo que se conoce como autapsis .
En el cerebro normalmente desarrollado, a lo largo del eje de algunos axones se encuentran botones presinápticos, también conocidos como varicosidades axonales , y se han encontrado en regiones del hipocampo que funcionan en la liberación de neurotransmisores. [19] Sin embargo, las varicosidades axonales también están presentes en enfermedades neurodegenerativas donde interfieren con la conducción de un potencial de acción. Las varicosidades axonales también son el sello distintivo de las lesiones cerebrales traumáticas . [19] [20] El daño axonal suele afectar al citoesqueleto del axón y altera el transporte. Como consecuencia, las acumulaciones de proteínas, como la proteína precursora beta-amiloide, pueden acumularse en una inflamación que resulta en una serie de varicosidades a lo largo del axón. [19] [20]
La mayoría de los axones transportan señales en forma de potenciales de acción, que son impulsos electroquímicos discretos que viajan rápidamente a lo largo de un axón, comenzando en el cuerpo celular y terminando en los puntos donde el axón hace contacto sináptico con las células diana. La característica definitoria de un potencial de acción es que es "todo o nada": cada potencial de acción que genera un axón tiene esencialmente el mismo tamaño y forma. Esta característica de todo o nada permite que los potenciales de acción se transmitan de un extremo de un axón largo al otro sin ninguna reducción de tamaño. Sin embargo, existen algunos tipos de neuronas con axones cortos que transportan señales electroquímicas graduadas y de amplitud variable.
Cuando un potencial de acción llega a una terminal presináptica, activa el proceso de transmisión sináptica. El primer paso es la rápida apertura de los canales de iones de calcio en la membrana del axón, lo que permite que los iones de calcio fluyan hacia adentro a través de la membrana. El aumento resultante en la concentración de calcio intracelular hace que las vesículas sinápticas (pequeños recipientes encerrados por una membrana lipídica) llenos de un neurotransmisor químico se fusionen con la membrana del axón y vacíen su contenido en el espacio extracelular. El neurotransmisor se libera del nervio presináptico mediante exocitosis . La sustancia química del neurotransmisor luego se difunde a los receptores ubicados en la membrana de la célula diana. El neurotransmisor se une a estos receptores y los activa. Dependiendo del tipo de receptores que se activen, el efecto sobre la célula diana puede ser excitar la célula diana, inhibirla o alterar su metabolismo de alguna manera. Toda esta secuencia de acontecimientos suele tener lugar en menos de una milésima de segundo. Luego, dentro de la terminal presináptica, un nuevo conjunto de vesículas se coloca junto a la membrana, listo para ser liberado cuando llegue el siguiente potencial de acción. El potencial de acción es el paso eléctrico final en la integración de mensajes sinápticos a escala de la neurona. [5]

Se han demostrado registros extracelulares de la propagación del potencial de acción en los axones en animales que se mueven libremente. Si bien los potenciales de acción somáticos extracelulares se han utilizado para estudiar la actividad celular en animales que se mueven libremente, como las células de lugar , también se puede registrar la actividad axonal tanto en la materia blanca como en la gris. Los registros extracelulares de la propagación del potencial de acción del axón se distinguen de los potenciales de acción somáticos en tres formas: 1. La señal tiene una duración pico-valle más corta (~150 μs) que la de las células piramidales (~500 μs) o las interneuronas (~250 μs). 2. El cambio de voltaje es trifásico. 3. La actividad registrada en un tetrodo se ve sólo en uno de los cuatro cables de grabación. En grabaciones de ratas que se mueven libremente, se han aislado señales axonales en tractos de materia blanca, incluidos el alveo y el cuerpo calloso, así como en la materia gris del hipocampo. [21]
De hecho, la generación de potenciales de acción in vivo es de naturaleza secuencial, y estos picos secuenciales constituyen los códigos digitales en las neuronas. Aunque estudios previos indican un origen axonal de un solo pico provocado por pulsos de corta duración, las señales fisiológicas in vivo desencadenan el inicio de picos secuenciales en los cuerpos celulares de las neuronas. [22] [23]
Además de propagar los potenciales de acción a las terminales axonales, el axón es capaz de amplificar los potenciales de acción, lo que garantiza una propagación segura de los potenciales de acción secuenciales hacia la terminal axonal. En términos de mecanismos moleculares, los canales de sodio dependientes de voltaje en los axones poseen un umbral más bajo y un período refractario más corto en respuesta a pulsos de corta duración. [24]
El desarrollo del axón hasta su objetivo es una de las seis etapas principales del desarrollo general del sistema nervioso . [25] Los estudios realizados en neuronas cultivadas del hipocampo sugieren que las neuronas inicialmente producen múltiples neuritas que son equivalentes, pero solo una de estas neuritas está destinada a convertirse en el axón. [26] No está claro si la especificación del axón precede a la elongación del axón o viceversa, [27] aunque evidencia reciente apunta a lo último. Si se corta un axón que no está completamente desarrollado, la polaridad puede cambiar y otras neuritas pueden potencialmente convertirse en el axón. Esta alteración de polaridad sólo ocurre cuando el axón se corta al menos 10 μm más corto que las otras neuritas. Una vez realizada la incisión, la neurita más larga se convertirá en el futuro axón y todas las demás neuritas, incluido el axón original, se convertirán en dendritas. [28] Imponer una fuerza externa sobre una neurita, haciendo que se alargue, hará que se convierta en un axón. [29] No obstante, el desarrollo axonal se logra a través de una interacción compleja entre la señalización extracelular, la señalización intracelular y la dinámica citoesquelética .
Las señales extracelulares que se propagan a través de la matriz extracelular que rodea a las neuronas desempeñan un papel destacado en el desarrollo axonal. [30] Estas moléculas de señalización incluyen proteínas, factores neurotróficos y moléculas de adhesión y matriz extracelular.La netrina (también conocida como UNC-6), una proteína secretada, funciona en la formación de axones. Cuando se muta el receptor de netrina UNC-5 , varias neuritas se proyectan irregularmente fuera de las neuronas y, finalmente, un solo axón se extiende anteriormente. [31] [32] [33] [34] Los factores neurotróficos: el factor de crecimiento nervioso (NGF), el factor neurotrófico derivado del cerebro (BDNF) y la neurotrofina-3 (NTF3) también participan en el desarrollo de los axones y se unen a los receptores Trk . [35]
La enzima convertidora de gangliósidos gangliósido sialidasa de membrana plasmática (PMGS), que participa en la activación de TrkA en la punta de los neutritos, es necesaria para el alargamiento de los axones. PMGS se distribuye asimétricamente hasta la punta de la neurita que está destinada a convertirse en el futuro axón. [36]
Durante el desarrollo axonal, la actividad de PI3K aumenta en la punta del axón destinado. La interrupción de la actividad de PI3K inhibe el desarrollo axonal. La activación de PI3K da como resultado la producción de fosfatidilinositol (3,4,5)-trifosfato (PtdIns) que puede causar un alargamiento significativo de una neurita, convirtiéndola en un axón. Como tal, la sobreexpresión de fosfatasas que desfosforilan las PtdIns conduce al fallo de la polarización. [30]
La neurita con menor contenido de filamentos de actina se convertirá en el axón. La concentración de PGMS y el contenido de actina f están inversamente correlacionados; cuando PGMS se enriquece en la punta de una neurita, su contenido de actina f disminuye sustancialmente. [36] Además, la exposición a fármacos despolimerizantes de actina y a la toxina B (que inactiva la señalización Rho ) provoca la formación de múltiples axones. En consecuencia, la interrupción de la red de actina en un cono de crecimiento promoverá que su neurita se convierta en axón. [37]

Los axones en crecimiento se mueven a través de su entorno a través del cono de crecimiento , que se encuentra en la punta del axón. El cono de crecimiento tiene una extensión ancha en forma de lámina llamada lamellipodium que contiene protuberancias llamadas filopodios . Los filopodios son el mecanismo por el cual todo el proceso se adhiere a las superficies y explora el entorno circundante. La actina juega un papel importante en la movilidad de este sistema. Los entornos con altos niveles de moléculas de adhesión celular (CAM) crean un entorno ideal para el crecimiento axonal. Esto parece proporcionar una superficie "pegajosa" para que crezcan los axones. Ejemplos de CAM específicas de los sistemas neuronales incluyen N-CAM , TAG-1 (una glicoproteína axonal [38] ) y MAG , todas las cuales forman parte de la superfamilia de inmunoglobulinas . Otro conjunto de moléculas llamado matriz extracelular : las moléculas de adhesión también proporcionan un sustrato pegajoso para que crezcan los axones. Ejemplos de estas moléculas incluyen laminina , fibronectina , tenascina y perlecano . Algunos de ellos están unidos a la superficie de las células y, por tanto, actúan como atrayentes o repelentes de corto alcance. Otros son ligandos difusibles y, por tanto, pueden tener efectos de largo alcance.
Las células llamadas células guía ayudan a guiar el crecimiento de los axones neuronales. Estas células que ayudan a la guía de los axones suelen ser otras neuronas que a veces son inmaduras. Cuando el axón ha completado su crecimiento en su conexión con el objetivo, el diámetro del axón puede aumentar hasta cinco veces, dependiendo de la velocidad de conducción requerida. [39]
También se ha descubierto a través de investigaciones que si los axones de una neurona estuvieran dañados, siempre y cuando el soma (el cuerpo celular de una neurona) no esté dañado, los axones se regenerarían y reharían las conexiones sinápticas con las neuronas con la ayuda de una guía. células . Esto también se conoce como neuroregeneración . [40]
Nogo-A es un tipo de componente inhibidor del crecimiento de neuritas que está presente en las membranas de mielina del sistema nervioso central (que se encuentran en un axón). Tiene un papel crucial en la restricción de la regeneración axonal en el sistema nervioso central de mamíferos adultos. En estudios recientes, si Nogo-A se bloquea y neutraliza, es posible inducir la regeneración axonal a larga distancia, lo que conduce a una mejora de la recuperación funcional en la médula espinal de ratas y ratones. Esto aún no se ha hecho en humanos. [41] Un estudio reciente también ha descubierto que los macrófagos activados a través de una vía inflamatoria específica activada por el receptor Dectin-1 son capaces de promover la recuperación del axón, aunque también causan neurotoxicidad en la neurona. [42]
Los axones varían mucho en longitud, desde unos pocos micrómetros hasta metros en algunos animales. Esto enfatiza que debe haber un mecanismo de regulación de la longitud celular que permita a las neuronas detectar la longitud de sus axones y controlar su crecimiento en consecuencia. Se descubrió que las proteínas motoras desempeñan un papel importante en la regulación de la longitud de los axones. [43] Basándose en esta observación, los investigadores desarrollaron un modelo explícito para el crecimiento axonal que describe cómo las proteínas motoras podrían afectar la longitud del axón a nivel molecular. [44] [45] [46] [47] Estos estudios sugieren que las proteínas motoras transportan moléculas de señalización desde el soma al cono de crecimiento y viceversa, cuya concentración oscila en el tiempo con una frecuencia dependiente de la longitud.
Los axones de las neuronas del sistema nervioso periférico humano se pueden clasificar según sus características físicas y propiedades de conducción de señales. Se sabía que los axones tenían diferentes espesores (de 0,1 a 20 µm) [3] y se pensaba que estas diferencias estaban relacionadas con la velocidad a la que un potencial de acción podía viajar a lo largo del axón: su velocidad de conductancia . Erlanger y Gasser comprobaron esta hipótesis e identificaron varios tipos de fibras nerviosas, estableciendo una relación entre el diámetro de un axón y su velocidad de conducción nerviosa. Publicaron sus hallazgos en 1941 dando la primera clasificación de axones.
Los axones se clasifican en dos sistemas. El primero introducido por Erlanger y Gasser, agrupaba las fibras en tres grupos principales utilizando las letras A, B y C. Estos grupos, grupo A , grupo B y grupo C incluyen tanto las fibras sensoriales ( aferentes ) como las fibras motoras. ( eferentes ). El primer grupo A se subdividió en fibras alfa, beta, gamma y delta: Aα, Aβ, Aγ y Aδ. Las neuronas motoras de las diferentes fibras motoras eran las neuronas motoras inferiores : la neurona motora alfa , la neurona motora beta y la neurona motora gamma que tenían las fibras nerviosas Aα, Aβ y Aγ, respectivamente.
Hallazgos posteriores de otros investigadores identificaron dos grupos de fibras Aa que eran fibras sensoriales. Luego se introdujeron en un sistema (clasificación de Lloyd) que solo incluía fibras sensoriales (aunque algunas de ellas eran nervios mixtos y también eran fibras motoras). Este sistema se refiere a los grupos sensoriales como Tipos y utiliza números romanos: Tipo Ia, Tipo Ib, Tipo II, Tipo III y Tipo IV.
Las neuronas motoras inferiores tienen dos tipos de fibras:
Diferentes receptores sensoriales inervan diferentes tipos de fibras nerviosas. Los propioceptores están inervados por fibras sensoriales de tipo Ia, Ib y II, los mecanorreceptores por fibras sensoriales de tipo II y III y los nociceptores y termorreceptores por fibras sensoriales de tipo III y IV.
El sistema nervioso autónomo tiene dos tipos de fibras periféricas:
En orden de gravedad, la lesión de un nervio del sistema nervioso periférico puede describirse como neuropraxia , axonotmesis o neurotmesis .La conmoción cerebral se considera una forma leve de lesión axonal difusa . [51] La lesión axonal también puede causar cromatólisis central . La disfunción de los axones en el sistema nervioso es una de las principales causas de muchos trastornos neurológicos heredados y adquiridos que afectan tanto a las neuronas periféricas como a las centrales. [5]
Cuando se aplasta un axón, tiene lugar un proceso activo de degeneración axonal en la parte del axón más alejada del cuerpo celular. Esta degeneración tiene lugar rápidamente después de la lesión, con la parte del axón sellada en las membranas y descompuesta por los macrófagos. Esto se conoce como degeneración walleriana . [52] La muerte de un axón también puede ocurrir en muchas enfermedades neurodegenerativas , particularmente cuando el transporte axonal está alterado, esto se conoce como degeneración de tipo walleriano. [53] Los estudios sugieren que la degeneración ocurre como resultado de que a la proteína axonal NMNAT2 se le impide llegar a todo el axón. [54]
La desmielinización de los axones provoca multitud de síntomas neurológicos que se encuentran en la enfermedad de la esclerosis múltiple .
La dismielinización es la formación anormal de la vaina de mielina. Esto está implicado en varias leucodistrofias y también en la esquizofrenia . [55] [56] [57]
Una lesión cerebral traumática grave puede provocar lesiones generalizadas en los tractos nerviosos que dañan los axones en una afección conocida como lesión axonal difusa . Esto puede conducir a un estado vegetativo persistente . [58] Se ha demostrado en estudios en ratas que el daño axonal de una sola lesión cerebral traumática leve puede dejar una susceptibilidad a daños mayores, después de repetidas lesiones cerebrales traumáticas leves. [59]
Un conducto de guía nerviosa es un medio artificial para guiar el crecimiento de los axones para permitir la neuroregeneración y es uno de los muchos tratamientos utilizados para diferentes tipos de lesiones nerviosas .
Algunos diccionarios generales definen "fibra nerviosa" como cualquier proceso neuronal , incluidos tanto los axones como las dendritas . [60] [61] Sin embargo, las fuentes médicas generalmente utilizan "fibra nerviosa" para referirse únicamente al axón. [62] [63]
Al anatomista alemán Otto Friedrich Karl Deiters generalmente se le atribuye el descubrimiento del axón al distinguirlo de las dendritas. [5] El suizo Rüdolf Albert von Kölliker y el alemán Robert Remak fueron los primeros en identificar y caracterizar el segmento inicial del axón. Kölliker nombró el axón en 1896. [64] Louis-Antoine Ranvier fue el primero en describir los espacios o nodos que se encuentran en los axones y, por esta contribución, estas características axonales ahora se conocen comúnmente como nodos de Ranvier . Santiago Ramón y Cajal , anatomista español, propuso que los axones eran los componentes de salida de las neuronas, describiendo su funcionalidad. [5] Joseph Erlanger y Herbert Gasser desarrollaron anteriormente el sistema de clasificación de las fibras nerviosas periféricas, [65] basado en la velocidad de conducción axonal, la mielinización , el tamaño de las fibras, etc. Alan Hodgkin y Andrew Huxley también emplearon el axón gigante del calamar (1939) y en 1952 Habían obtenido una descripción cuantitativa completa de la base iónica del potencial de acción, lo que condujo a la formulación del modelo de Hodgkin-Huxley . Hodgkin y Huxley recibieron conjuntamente el Premio Nobel por este trabajo en 1963. Las fórmulas que detallan la conductancia axonal se extendieron a los vertebrados en las ecuaciones de Frankenhaeuser-Huxley. La comprensión de las bases bioquímicas para la propagación del potencial de acción ha avanzado aún más e incluye muchos detalles sobre los canales iónicos individuales .
Los axones de los invertebrados han sido ampliamente estudiados. El calamar costero de aleta larga , utilizado a menudo como organismo modelo, tiene el axón más largo conocido. [66] El calamar gigante tiene el axón más grande conocido. Su tamaño oscila entre 0,5 (normalmente) y 1 mm de diámetro y se utiliza en el control de su sistema de propulsión a chorro . La velocidad de conducción más rápida registrada, 210 m/s, se encuentra en los axones envainados de algunos camarones Peneidos pelágicos [67] y el rango habitual es entre 90 y 200 metros/s [68] ( cf. 100-120 m/s para el axón de vertebrados mielinizado más rápido).
En otros casos, como se ha visto en estudios con ratas, un axón se origina a partir de una dendrita; Se dice que estos axones tienen "origen dendrítico". Algunos axones con origen dendrítico tienen de manera similar un segmento inicial "proximal" que comienza directamente en el origen del axón, mientras que otros tienen un segmento inicial "distal", claramente separado del origen del axón. [69] En muchas especies, algunas de las neuronas tienen axones que emanan de la dendrita y no del cuerpo celular, y estos se conocen como dendritas portadoras de axones. [1] En muchos casos, un axón se origina en un montículo axónico en el soma; Se dice que tales axones tienen "origen somático". Algunos axones con origen somático tienen un segmento inicial "proximal" adyacente al cono axónico, mientras que otros tienen un segmento inicial "distal", separado del soma por un cono axónico extendido. [69]
Kölliker le daría su nombre al "axón" en 1896.